Состав
В составе раствора для инфузий Акласта содержится активный ингредиент моногидрат золедроновой кислоты и дополнительные составляющие: цитрат натрия, маннитол, вода для инъекций.
Форма выпуска
Лекарство производится в форме раствора для инфузий. Это прозрачная жидкость без цвета, которая содержится во флаконах из полиэтилена по 100 мл. Флаконы упакованы в картонные коробки.
Фармакологическое действие
Препарат производит ингибирующее костную резорбцию действие. Активное вещество — золедроновая кислота относится к амино бисфосфонатам и в основном воздействует на костную ткань, подавляя резорбцию ткани кости и активность остеокластов.
Селективное влияние бисфосфонатов на костную ткань основывается на сродстве к минерализованной костной ткани. После того, как средство Акласта вводится внутривенно, золедроновая кислота активно перераспределяется в костную ткань и в основном локализуется в местах ремоделирования, как и другие бисфосфонаты. В основном на молекулярном уровне золедроновая кислота в остеокласте действует на фермент фарнезилпирофосфатсинтетаза. Также не исключены другие механизмы действия этого средства.
Золедроновая кислота ингибирует костную резорбцию, при этом, не оказывая нежелательного влияния на формирование костной ткани, ее механические свойства и минерализацию. Действующий компонент дозозависимо снижает активность остеокластов и частоту новых очагов ремоделирования в кортикальной и трабекулярной частях кости, не провоцируя при этом образования волокнистой ткани кости и аберрантной аккумуляции остеоида.
Если исключить антирезорбтивное воздействие, золедроновая кислота воздействует на костную ткань так же, как и другие бисфосфонаты.
При лечении препаратом Акласта пациенток с постменопаузным остеопорозом к окончанию третьего года лечения было отмечено понижение вероятности вертебральных переломов на 70% (статистически достоверное). Также на 60–70%. снижался риск проявления повторных и новых переломов позвонков. У женщин в возрасте 75 лет и более, страдающих остеопорозом, риск вертебральных переломов уменьшался на 61%.
У людей, которые применяли препарат Акласта, на 33% понижался относительный риск невертебральных переломов разной локализации. Применение средства на протяжении трех лет пациентками с постменопаузным остеопорозом вело к увеличению минеральной плотности кости (МПК) поясничных позвонков, бедренной кости.
Лечение на протяжении 3 лет способствовало уменьшению периода иммобилизации у пациенток с остеопорозом в постменопаузе и снижению выраженности боли.
Если препарат Акласта был введен больным с переломами проксимального отдела бедренной кости, было отмечено уменьшение на 35% частоты остеопоротических переломов в будущем.
Применение Акласты пациентами с переломами бедренной кости на протяжении двух лет вело к росту МПК бедренной кости.
Выраженное увеличение МПК поясничных позвонков отмечалось у мужчин с первичным либо вторичным остеопорозом, при условии, что препарат применялся один раз в год.
Также МПК увеличивалась после терапии Акластой у людей, страдающих остеопорозом, вызванным применением ГКС. При этом не отмечалось негативного влияния на структуру ткани кости и минерализацию.
Отмечено положительное воздействие лечения на пациентов, которые страдали костной болезнью Педжета, а также у тех, кто раньше проходил терапию пероральными бисфосфонатами.
Есть данные о том, что у большинства пациентов, которым вводится золедроновая кислота, сохраняется терапевтический ответ в течение всего периода лечения. На шестом месяце лечения выраженное понижение болевого синдрома после введения Акласты однократно в дозе 5 мг такое же, как при введении 30 мг/сут. ризедроновой кислоты.
Фармакокинетика и фармакодинамика
Фармакокинетика не зависит от дозы лекарства. По мере того, как лекарство Акласта постепенно вводится пациенту, в плазме происходит быстрое увеличение концентрации золедроновой кислоты. Максимальная концентрация достигается в конце введения. После того, как инфузия завершается, уровень активного вещества в крови начинает снижаться. Далее, на протяжении продолжительного периода, в плазме отмечается низкая концентрация активного составляющего. Если время инфузии увеличивается с 5 до 15 минут, концентрация золедроновой кислоты в конце введения снижается на 30%, однако биодоступность препарата остается неизменной. С белками крови связывается на 43–55%, эти показатели не зависят от концентрации. В организме связывается с костной тканью.
Выведение лекарства происходит через почки. Сначала происходит быстрое двухфазное выведение с периодом полувыведения 0,24 ч и 1,87 ч. Далее отмечается длительная фаза, где окончательное время полувыведения составляет 146 ч. Выводится в неизмененном виде, не метаболизируясь.
Не отмечается кумуляция при повторном применении каждые 28 дней.
Показания к применению
Средство Акласта (Aclasta) назначают больным, страдающим постменопаузным остеопорозом, с целью уменьшения вероятности переломов позвонков, бедренной кости, а также вневертебральных переломов. Также лекарство назначают в следующих случаях:
- с целью улучшения минеральной плотности кости;
- в случае остеопороза у мужчин;
- для предотвращения переломов у пациентов, у которых уже случались переломы проксимального отдела бедренной кости;
- с целью профилактики постменопаузного остеопороза у женщин с остеопенией;
- для лечения и профилактики остеопороза, спровоцированного приемом ГКС;
- при костной болезни Педжета.
Противопоказания
Средство не следует принимать в таких случаях:
- при высоком уровне чувствительности к составляющим этого средства, а также к другим бисфосфонатам;
- во время беременности и кормления грудью;
- при тяжелых формах нарушения минерального обмена, при гипокальциемии;
- пациентам в возрасте до 18 лет, так как не была изучена безопасность приема этого средства;
- при тяжелых заболеваниях почек.
Побочные действия Акласты
В случае введения внутривенно Акласты в дозе 5 мг один раз в год большинство побочных реакций у пациентов были выражены слабо либо умеренно. Чаще всего отмечаются следующие побочные эффекты, длящиеся не больше трех дней:
- лихорадка;
- гриппоподобный синдром;
- миалгии, артралгии;
- головная боль.
При введении препарата повторно выраженность указанных побочных эффектов существенно снижалась.
В процессе лечения также проявлялись другие побочные действия Акласты, которые, по мнению специалистов, связаны с применением лекарства:
- нервная система: головокружение и головная боль, парестезия, тремор, заторможенность, сонливость;
- дыхательная система: кашель и одышка;
- органы чувств: боль в глазах, конъюнктивит, вертиго;
- пищеварение: рвота, тошнота, диарея, ухудшение аппетита, анорексия, диспепсия, ощущение сухости во рту, боль в животе, эзофагит, запор;
- кожные покровы, подкожная клетчатка: гипергидроз, сыпь, эритема, зуд;
- скелетно-мышечная система, соединительная ткань: миалгии, артралгии, боль в спине, конечностях и костях, мышечные спазмы, боль в плечевом поясе и грудной клетке, чувство скованности и слабости в мышцах, артриты;
- кроветворение: анемия;
- мочевыделительная система: поллакиурия, увеличение показателей креатинина крови, протеинурия;
- сердце и сосуды: увеличение артериального давления, покраснение лица;
- инвазии, инфекции: грипп, назофарингит;
- другие проявления: гриппоподобный синдром, увеличение температуры, озноб, сильная утомляемость, астения, общее недомогание, отеки периферические, ощущение жажды, сильная возбудимость.
В редких случаях отмечаются местные реакции в местах введения Акласты в виде отечности, покраснения и болезненности.
Акласта, инструкция по применению (Способ и дозировка)
При назначении препарата Акласта инструкция по применению должна тщательно соблюдаться пациентом. Раствор вводится пациенту внутривенно, при этом применяется клапанная инфузионная система, обеспечивающая постоянную скорость введения не менее 15 минут. Перед тем, как вводить лекарство, следует провести гидратацию организма. Особенно важен этот момент при лечении людей, которым уже исполнилось 65 лет, а также при введении раствора пациентам, которые проходят лечение диуретиками.
С целью лечения остеопороза у мужчин и постменопаузного остеопороза у женщин рекомендуется вводить один раз в год 5 мг в/в. Если пациент получает при этом мало витамина D и кальция с пищей, ему дополнительно назначают препараты, содержащие эти составляющие.
С целью профилактики переломов у людей с переломами проксимального отдела бедренной кости следует вводить внутривенно аналогичную дозу лекарства один раз в год. Тем, у кого такой перелом произошел недавно, рекомендовано за две недели перед введением Акласты принять однократно высокую дозу витамина D (до 125000 ME), а также каждый день на протяжении двух недель принимать перорально витамин D и кальций. После проведения инфузии на протяжении года необходимо продолжать прием этих препаратов. Рекомендуется вводить Акласту в период от 6 до 12 недель после операции, связанной с переломом бедренной кости.
С целью терапии остеопороза, который связан с лечением ГКС, рекомендуется вводить один раз в год 5 мг препарата внутривенно. Дополнительно возможно назначение препаратов кальция, витамина D.
Чтобы обеспечить профилактику постменопаузного остеопороза, рекомендовано водить внутривенно 5 мг лекарства один раз в два года.
Пациентам с костной болезнью Педжета однократно вводят внутривенно 5 мг раствора Акласта. На протяжении десяти дней после инфузии людям с таким диагнозом рекомендовано принимать кальций и витамин D в суточной дозе.
Повторное введение раствора при болезни Педжета возможно только после обследований и назначения врача.
Людям с заболеваниями печени и почек, а также пожилым пациентам корректировать дозировку не нужно.
При введении раствора нужно тщательно соблюдать все правила асептики. Нельзя использовать лекарство, если изменился его цвет, или присутствуют нерастворенные частицы. Раствор перед введением должен иметь комнатную температуру.
Акласту нельзя вводить с другими лекарствами, для введения ЛС нужно применять отдельную систему для в/в введения. Нельзя использовать раствор, который остался во флаконе после инфузии.
Передозировка
Существует ограниченная информация о передозировке средства. Важно, чтобы после получения дозы, которая превышает допустимую, пациент пребывал под наблюдением специалиста.
В случае передозировки золедроновой кислоты могут развиваться серьезные нарушения функции почек, в том числе почечная недостаточность, гипомагниемия, гипофосфатемия, гипокальциемия. При таких проявлениях пациенту нужно вводить внутривенно растворы, которые содержат фосфаты, ионы магния, кальция.
Взаимодействие
Не проводилось исследований, в процессе которых было бы изучено взаимодействие золедроновой кислоты с другими препаратами.
Отмечается несовместимость раствора с препаратами, в которых содержится кальций, поэтому эти лекарства нельзя использовать в одной системе для инфузий.
Следует осторожно применять ЛС со средствами, которые оказывают выраженное воздействие на функцию почек.
Условия продажи
Приобрести можно по рецепту.
Условия хранения
Хранить раствор Акласта следует при температуре до 25 °C. После того, как флакон был вскрыт, его хранят 24 часа, при этом температура должна составлять 2–8 °C. Беречь средство от детей.
Срок годности
Акласту можно хранить 3 года. После истечения этого срока не использовать.
Особые указания
Терапию Акластой людей, которые страдают костной болезнью Педжета, должны практиковать исключительно специалисты, у которых уже есть опыт лечения этого недуга.
Чтобы уменьшить выраженность и частоту негативных проявлений, которые отмечаются в процессе приема лекарства в первые три дня, сразу после в/в лекарства пациентам может быть назначен Ибупрофен или Парацетамол.
В составе лекарства Зомета, которое применяется для лечения онкологических больных, также содержится активное вещество золедроновая кислота. Но два этих ЛС не могут заменять друг друга. Одновременно применять их также не следует.
Людям, страдающим гипокальциемией, перед началом терапии нужно принимать витамин D и препараты кальция. Важно также обеспечить лечение других нарушений минерального обмена.
Не рекомендовано применять Акласту людям, страдающим тяжелыми нарушениями функции почек.
Перед тем, как проводить инфузию, важно определить уровень креатинина в плазме крови. У пациентов с болезнями почек содержание креатинина следует определять регулярно.
При однократной инфузии доза лекарства не должна быть выше 5 мг, период введения должен длиться не меньше, чем 15 минут.
На сегодняшний день не подтверждена связь остеонекроза челюсти с приемом бисфосфонатов, но все же при лечении Акластой рекомендуется не проводить стоматологических хирургических вмешательств, так как после проведения таких операций может увеличиться период восстановления. Полное стоматологическое исследование и профилактические процедуры нужно провести перед началом терапии бисфосфонатами.
Нет данных о том, что применение Акласты оказывает влияние на реакцию пациента, но ввиду вероятности проявления негативных эффектов рекомендуется осторожно водить транспорт и выполнять все действия, требующие быстрой реакции.
Аналоги Акласты
Совпадения по коду АТХ 4-го уровня:
Аналоги лекарства Акласта – препараты: Золедронат-Тева, Блазтера, Золедрэкс, Золерикс, Зомета, Резокластин ФС и др.
Однако, применять любой из аналогов без назначения доктора, нельзя.
Детям
Пациентам до 18 лет средство не назначают.
При беременности и лактации
Нельзя назначать средство беременным женщинам и кормящим матерям. Есть данные о тератогенном влиянии активного вещества на один из видов грызунов.
Отзывы об Акласте
Встречаются очень разные отзывы об Акласте на форумах, где обсуждают проблемы, связанные с остеопорозом. Часто пациенты, перенесшие переломы и практиковавшие лечение этим препаратом, пишут, что после его приема состояние улучшалось. Об этом свидетельствовали и результаты обследований, и общее состояние пациентов. При этом многие отмечают, что введение лекарства переносится тяжело: повышается температура тела, развивается озноб, рвота.
Есть также мнения о том, что Акласта не является эффективным средством, так как пациенты после лечения не почувствовали улучшения состояния.
Цена Акласты, где купить
Купить Акласту в Москве можно в аптеках или по заказу в Интернете. Цена Акласты в руб. — около 18000 рублей за флакон 50 мкг/мл, 100 мл. Цена Акласты в Украине – от 7000 грн.
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Акласта р-р для инфузий 5мг 100мл
ЗдравСити
-
Акласта р-р д/инф. 5мг/100млФрезениус Каби Австрия ГмбХ/Новартис Фарма Штейн АГ
Аптека Диалог
-
Акласта 5мг/100млNovartis
показать еще
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.Боль в суставахБоль в суставах и мышцахВоспаление суставовДля суставов и связокТаблетки
Содержание статьи
- Акласта: РЛС
- Акласта: противопоказания
- Акласта: побочные действия
- Акласта или Остеостатикс: что лучше?
- Резокластин или Акласта: что лучше?
- Краткое содержание
- Задайте вопрос эксперту по теме статьи
В Российской Федерации остеопороз регистрируется у каждой третьей женщины и каждого четвертого мужчины в возрасте старше 50 лет. Что это за болезнь? Остеопороз относится к хроническим заболеваниям костей скелета, при котором из-за изменения обмена веществ снижается плотность костей и нарушается структура костной ткани. Это приводит к переломам даже при минимальной травме.
В нашем обществе много факторов риска этого заболевания: дефицит витамина D, курение, употребление спиртных напитков, низкое потребление кальция с продуктами питания, отсутствие физической активности. Также нарушение метаболизма веществ, необходимых для обновления костной ткани (кальций, фосфор и витамин D) часто связано с пожилым возрастом, а у женщин — с менопаузой.
Мы попросили провизора Наталью Асанову рассказать о препарате Акласта, который применяют для лечения остеопороза. Рассказываем как применяется это лекарство, его противопоказаниях и побочных действиях. Сравниваем с аналогами.
Акласта: РЛС
Регистр лекарственных средств России содержит информацию, что Акласта — препарат класса бисфосфонатов. В ее составе мощный ингибитор костной резорбции золедроновая кислота. Федеральные клинические рекомендации по диагностике, лечению и профилактике остеопороза предусматривают антирезорбтивную терапию именно бифосфонатами.
Провизор : «Чтобы разобраться, как действует Акласта в организме, объясним, что такое резорбция. Это разрушение (рассасывание) костной ткани клетками остеокластами, которые выделяют ферменты и уничтожают старые и поврежденные костные клетки».
Препарат Акласта — капельница с готовым инфузионным раствором. Содержит 5 мг золедроновой кислоты в 100 мл. После внутривенного введения активное вещество локализуется в местах ремоделирования костной ткани. Она подавляет активность остеокластов и резорбцию костной ткани. При этом не оказывает негативного действия на формирование, минерализацию и механические свойства ткани костей. Капельницу с Акластой ставят один раз в год или два, в зависимости от заболевания.
Золедроновая кислота (Акласта) показана при:
- остеопорозе в постменопаузе для снижения рисков переломов и увеличения плотности костей
- переломах бедренной кости при остеопорозе у мужчин и женщин для профилактики новых переломов
- остеопорозе у мужчин
- остеопорозе, вызванном приемом гормонов-глюкокортикостероидов
- костной болезни Педжета
После введения Акласты необходим постоянный контроль за концентрацией кальция, фосфора, магния и креатинина в сыворотке крови. Терапия остеопороза должна сопровождаться достаточным поступлением в организм кальция (500-1000 мг/сутки) и витамина D (800-1000 МЕ/сутки).
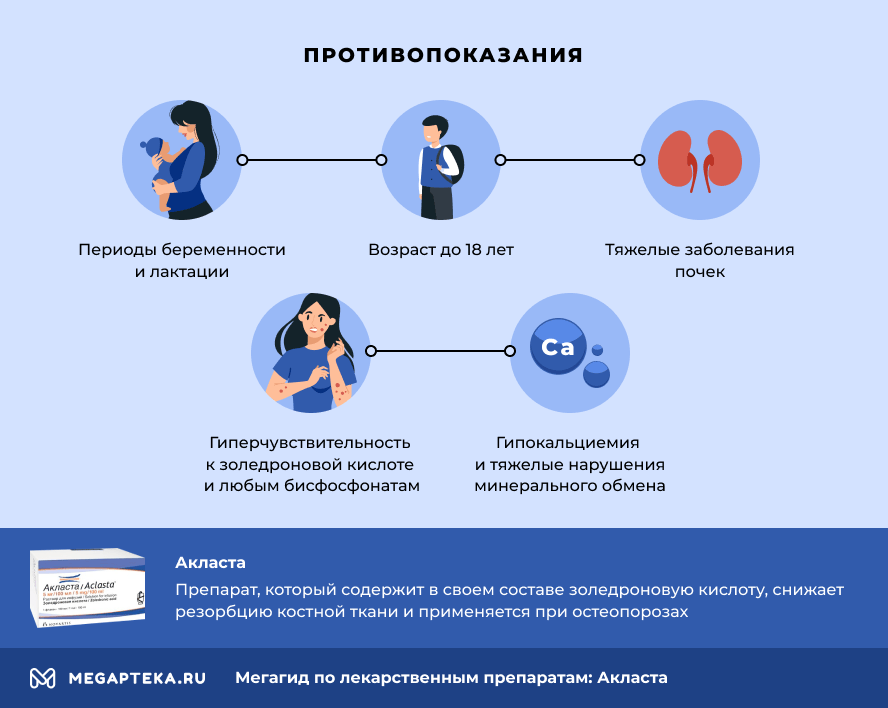
Акласта: противопоказания
Препарат нельзя применять в следующих случаях:
- гиперчувствительность к золедроновой кислоте и любым бисфосфонатам
- гипокальциемия и тяжелые нарушения минерального обмена
- периоды беременности и лактации
- возраст до 18 лет
- тяжелые заболевания почек
Акласта: побочные действия
Пациенты переносят препарат, как правило, хорошо. Нежелательные реакции бывают слабыми или умеренно выраженными. Наиболее часто проявляются:
- лихорадка
- боли в мышцах и суставах, спине и конечностях
- гриппоподобное состояние
- головная боль, головокружение
- покраснение склеры глаза
- тошнота, рвота, диарея
- фибрилляция предсердий
При повторных введениях частота побочных эффектов уменьшается. При введении Акласты важно исключить обезвоживание у пациента. При необходимости вводят физиологический раствор.
Акласта или Остеостатикс: что лучше?
Остеостатикс — российский дженерик Акласты, содержащий золедроновую кислоту. Производит его компания Фарм-Синтез из отечественной субстанции. Субстанция золедроновой кислоты для Акласты синтезируется в Швейцарии. Показания к применению, противопоказания и побочные действия у препаратов идентичные.
Преимуществом Остеостатикса может быть более доступная для пациентов цена. Но при этом качество «копийных» препаратов и их клиническая эффективность по сравнению с оригиналом могут существенно отличаться.
Резокластин или Акласта: что лучше?
Резокластин — первый дженерический препарат золедроновой кислоты в дозе 5 мг, зарегистрированный в России. От Акласты он отличается лекарственной формой, дозировкой и показаниями.
Резокластин представлен как
- концентрат для приготовления раствора для инфузий 4 мг/5 мл
- концентрат для приготовления раствора для инфузий 5 мг/6.25 мл
и показан для применения при :
- гиперкальциемии, которая спровоцирована злокачественными опухолями
- поражении костей метастазами злокачественных опухолей
- миеломной болезни
- первичного остеопороза в постменопаузе и у пожилых пациентов
- вторичного остеопороза
- при костной болезни Педжета
Резокластин в дозе 4 мг назначают при опухолях, в дозе 5 мг — при остеопорозах.
Анализ российского клинического опыта применения Резокластина 5 мг у пациентов с первичным и вторичным остеопорозом показал, что профиль переносимости сходен с оригинальным препаратом. Врачи и пациенты в целом высоко оценивают эффективность, переносимость и удобство назначения исследуемого дженерика.
Краткое содержание
- Акласта содержит активное вещество золедроновая кислота из класса бисфосфонатов. Препарат эффективно снижает резорбцию костной ткани и применяется при остеопорозах.
- Противопоказания к терапии Акластой: гиперчувствительность к любым бисфосфонатам, гипокальциемия, беременность, лактация, возраст до 18 лет и тяжелая почечная недостаточность.
- Пациенты хорошо переносят лечение препаратом, нежелательные реакции обычно слабо или умеренно выражены.
- Остеостатикс — дженерик Акласты, они взаимозаменяемы.
- Резокластин имеет 2 дозировки с разными показаниями к применению. В дозировке 5 мг может заменять Акласту
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
Выпускающий редактор
Эксперт-провизор
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда
Лечение различных видов остеопороза, костной болезни Педжета и профилактика новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости. При в/в введении 5 мг препарата Акласта 1 раз в год для лечения постменопаузного остеопороза у женщин, остеопороза у мужчин, для профилактики новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости, для профилактики и лечения остеопороза, вызванного применением ГКС и для лечения костной болезни Педжета большинство нежелательных явлений (НЯ) были слабо или умеренно выраженными. После в/в введения препарата Акласта у данных больных наиболее часто наблюдались следующие НЯ: длительностью обычно не более 3 дней («постдозные» симптомы) — лихорадка (18,1%), миалгии (9,4%), гриппоподобный синдром (7,8%), артралгии (6,8%), головная боль (6,5%). Большинство вышеназванных НЯ, отмечавшихся в течение 3 дней после введения препарата, были слабо или умеренно выраженными. При повторном введении препарата выраженность данных НЯ значительно уменьшалась. Ниже представлены НЯ, возможно связанные (по мнению лечащих врачей) с применением препарата для лечении различных видов остеопороза, костной болезни Педжета и для профилактики новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости.
Частота развития данных НЯ, оценивалась следующим образом: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000), очень редко (<1/10000), включая отдельные сообщения.
Со стороны нервной системы: часто — головная боль, головокружение; иногда — заторможенность*, парестезия, сонливость, тремор, обморок.
Со стороны органов чувств: иногда — конъюнктивит, боль в глазах, вертиго; редко — увеит*, эписклерит, ирит.
Со стороны дыхательной системы: иногда — одышка*, кашель.
Со стороны пищеварительной системы: часто — тошнота, рвота, диарея; иногда — анорексия*, снижение аппетита, диспепсия*, боль в животе*, сухость во рту, эзофагит*, гастроэзофагеальный рефлюкс, боль в верхних отделах живота, запоры.
Со стороны кожи и подкожной клетчатки: иногда — сыпь, гипергидроз*, зуд, эритема.
Со стороны скелетно-мышечной системы и соединительной ткани: часто — артралгии*, миалгии*; боли в костях, боли в спине и конечностях; иногда — боль в области шеи, отек в области суставов*, мышечные спазмы, боль в области плечевого пояса, боль в области грудной клетки* мышечно-скелетного происхождения, слабость в мышцах, скованность в мышцах* и суставах*, артриты, мышечно-скелетные боли.
Со стороны мочевыделительной системы: иногда — повышение уровня креатинина крови, поллакиурия, протеинурия.
Со стороны системы кроветворения: иногда — анемия.
Со стороны сердечно-сосудистой системы: иногда — повышение АД, внезапное покраснение лица.
Инфекции и инвазии: иногда — грипп, назофарингит.
Со стороны организма в целом: очень часто — повышение температуры; часто — гриппоподобный синдром, озноб, повышенная утомляемость*, астения, боль*, общее недомогание; нечасто — периферические отеки, чувство жажды*, повышенная возбудимость*, боль в груди (не связанная с заболеваниями сердца).
*Примечание: в отдельных исследованиях частота данных НЯ увеличивалась следующим образом: очень часто — миалгии, артралгии, повышенная утомляемость, боль; часто — заторможенность, одышка, диспепсия, эзофагит, боль в животе, гипергидроз, скованность в мышцах, отек в области суставов, боль в области грудной клетки мышечно-скелетного происхождения, скованность в суставах, анорексия, чувство жажды, повышенная возбудимость; нечасто — увеит.
В ходе отдельных исследований были зарегистрированы следующие НЯ, частота развития которых в группе препарата Акласта была ниже, чем у больных, не получавших препарат: покраснение глаз, повышение содержания С-реактивного белка, гипокальциемия, вкусовые нарушения, зубная боль, гастрит, ощущение сильного сердцебиения, реакции в месте введения препарата.
При применении препарата Акласта у пациенток с постменопаузным остеопорозом общая частота развития фибрилляции предсердий на фоне терапии препаратом Акласта составляла 2,5% (96 человек из 3862) по сравнению с 1,9% (75 из 3852 больных) у больных, не получавших лечение препаратом (группа плацебо). У 1,3% больных (51 пациентка из 3862), получавших препарат Акласта, и у 0,6% (22 человека из 3852) в группе плацебо данное нежелательное явление было расценено как серьезное. Причина повышения частоты фибрилляции предсердий на фоне терапии препаратом Акласта в данном исследовании не установлена. Повышение частоты фибрилляции предсердий в сравнении с плацебо, отмеченное в данном исследовании, не было обнаружено в других клинических исследованиях золедроновой кислоты.
Профилактика постменопаузного остеопороза
При применении препарата Акласта для профилактики постменопаузного остеопороза (ПМО) общий профиль безопасности препарата был сравним с таковым при лечении ПМО, за исключением НЯ, возникавших в течение 3 дней после инфузии: боль, лихорадка, озноб, миалгия, тошнота, головная боль, повышенная утомляемость, артралгия, частота которых была выше у женщин, получавших препарат для профилактики ПМО. Большинство этих НЯ были легкой или средней степени выраженности и проходили в течение 3 дней после проявления. При повторном введении препарата выраженность данных НЯ значительно уменьшалась.
Ниже представлены НЯ, возможно связанные с применением препарата для профилактика ПМО (по мнению лечащих врачей):
1) НЯ, отмечавшиеся более чем 1 раз при введении препарата Акласта для профилактики ПМО и не зарегистрированные при применении препарата для лечении различных видов остеопороза, костной болезни Педжета и для профилактика новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости;
2) НЯ, частота которых была выше у женщин, получавших препарат для профилактики ПМО (по сравнению с другими категориями больных).
Частота развития данных НЯ оценивалась следующим образом: очень часто (≥1/10); часто (≥1/100,<1/10); нечасто (≥1/1000, <1/100).
Психические нарушения: иногда — тревога.
Со стороны нервной системы: очень часто — головная боль; часто — тремор, заторможенность; нечасто — пониженная чувствительность, нарушения вкуса.
Со стороны органа зрения: часто — конъюнктивит, боль в глазах, ирит; нечасто — нечеткое зрение.
Со стороны пищеварительной системы: очень часто — тошнота; часто — анорексия, боль в животе, боль в верхних отделах живота, запор.
Со стороны кожи и подкожной клетчатки: часто — повышенное потоотделение в ночное время.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто — миалгии; часто — костно-мышечные боли, спазм мышц, боль в области грудной клетки мышечно-скелетного происхождения, боль в области челюсти, боль в области шеи; нечасто — боль в боку.
Со стороны организма в целом и реакции в месте введения препарата: очень часто — боль, озноб; часто — периферические отеки, реакции в месте введения препарата, некардиальная боль в области грудной клетки.
Изменение результатов лабораторных исследований
У пациенток с постменопаузным остеопорозом на фоне применения препарата Акласта в 0,2% случаев отмечалось снижение концентрации кальция (<1,87 ммоль/л) в сыворотке крови, клинических признаков гипокальциемии при этом не наблюдалось.
При применении препарата у больных с переломами бедренной кости, при остеопорозе у мужчин и остеопорозе, вызванном приемом ГКС, не отмечалось снижение концентрации кальция в плазме крови <1,87 ммоль/л.
При применении препарата у больных для профилактики постменопаузного остеопороза не отмечалось снижение концентрации кальция в плазме крови <1,87 ммоль/л. У пациентов с болезнью Педжета приблизительно в 1% случаев обнаруживалась преходящая гипокальциемия, сопровождавшаяся клиническими проявлениями.
Нарушения функций почек. При в/в введении бисфосфонатов, включая золедроновую кислоту, отмечались случаи нарушения функции почек, проявлявшиеся повышением концентрации креатинина крови и в редких случаях — острой почечной недостаточностью. Нарушение функции почек на фоне применения золедроновой кислоты наблюдалось у больных с наличием либо почечной патологии в анамнезе, либо дополнительных факторов риска (например онкологических заболеваний, требующих проведения химиотерапии, применения нефротоксических препаратов, диуретиков или тяжелой дегидратации). Большинство таких пациентов получали терапию золедроновой кислотой в дозе 4 мг каждые 3–4 нед, однако в ряде случаев нарушение функции почек отмечалось после однократного применения золедроновой кислоты. При терапии препаратом Акласта в течение 3 лет у больных постменопаузным остеопорозом частота повышения содержания креатинина в плазме крови и развития почечной недостаточности не отличалась от таковой при применении плацебо. У пациенток, получавших препарат Акласта, несколько чаще наблюдалось преходящее повышение концентрации креатинина крови в течение 10 дней после инфузии по сравнению с плацебо (1,8 и 0,8% соответственно).
При применении препарата Акласта в течение 2 лет у мужчин с остеопорозом частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе алендроновой кислоты.
У больных с остеопорозом, вызванным применением ГКС, на фоне терапии препаратом Акласта частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе ризедроновой кислоты.
Реакции в месте введения препарата. При применении препарата Акласта у пациенток с постменопаузным остеопорозом в 0,7% случаев отмечались покраснение, отечность и /или болезненность в месте введения.
У больных с переломами бедренной кости частота развития реакций в месте введения препарата была сравнимой с таковой в группе плацебо. При лечении остеопороза у мужчин частота развития реакций в месте введения препарата Акласта составляла 2,6% (по сравнению с 1,4% в группе алендроновой кислоты). У больных с остеопорозом, вызванным применением ГКС, не отмечалось реакций в месте введения препарата. При применении препарата для профилактики постменопаузного остеопороза частота развития реакций в месте введения препарата Акласта составляла 1,1% (по сравнению с 2,0% в группе плацебо).
Остеонекроз челюсти. Случаи развития остеонекроза (наиболее часто – челюсти) имели место в основном у онкологических пациентов, получающих лечение бисфосфонатами, после экстракции зуба или иных стоматологических манипуляций. У большинства больных были симптомы местного инфекционно-воспалительного процесса, включая остеомиелит. В клинических исследованиях у больных с остеопорозом случай остеонекроза челюсти имел место у 1 пациентки, принимавшей препарат Акласта, и у 2 больных, принимавших плацебо. Во всех трех случаях отмечалось разрешение процесса. При применении препарата Акласта у больных с переломами бедренной кости, при остеопорозе у мужчин и остеопорозе, вызванном приемом ГКС, а также при применении препарата для профилактики постменопаузного остеопороза не отмечалось случаев развития остеонекроза челюсти.
Отдельные сообщения о нежелательных явлениях
На фоне терапии препаратом Акласта в клинической практике отмечались следующие НЯ без указаний на причинно-следственную связь с применением препарата (частота НЯ не установлена): реакции гиперчувствительности, включая в редких случаях бронхообструкцию, крапивницу, ангионевротический отек и отдельные сообщения о развитии анафилактических реакций, в т.ч. анафилактического шока. В редких случаях при применении препарата Акласта в клинической практике у пациентов отмечались нарушения функции почек, включая почечную недостаточность, требующую проведения гемодиализа, особенно у больных с наличием либо почечной патологии в анамнезе, либо дополнительных факторов риска (например при сопутствующей терапии нефротоксическими препаратами, диуретиками или при тяжелой дегидратации).
В очень редких случаях сообщалось о развитии следующих НЯ: дегидратация вследствие лихорадки, рвоты и диареи, возникающих после введения препарата; выраженное снижение АД у пациентов с факторами риска, остеонекроз челюсти, склерит и воспаление в области глазницы.
Функция почек
Применение Акласты противопоказано пациентам с тяжелыми нарушениями функции почек (клиренс креатинина < 35 мл/мин), в связи с повышенным риском развития почечной недостаточности в этой популяции. При применении Акласты наблюдались случаи нарушения функции почек, особенно среди пациентов с наличием либо почечной патологии в анамнезе, либо других факторов риска, включая пожилой возраст, сопутствующий прием нефротоксических препаратов, сопутствующую терапию диуретиками или дегидратацию. Нарушение функции почек наблюдалось у пациентов после однократного применения препарата. В редких случаях у пациентов с другими заболеваниями почек или с любым из перечисленных выше факторов риска наблюдалась почечная недостаточность, требующая проведения диализа, или повлекшая летальный исход.
Для минимизации риска развития нежелательных реакций со стороны почек следует соблюдать следующие меры предосторожности:
Контроль клиренса креатинина должен проводиться перед каждой очередной дозой Акласты. Клиренс креатинина должен рассчитываться с учетом массы тела пациента по формуле Кокрофта-Гаулта.
Кратковременное повышение сывороточного креатинина может быть больше у пациентов с изначально нарушенной функцией почек. Промежуточный мониторинг клиренса креатинина рекомендуется пациентам, у которых выявлены факторы риска развития нарушений функции почек.
При сопутствующем применении других лекарственных препаратов, способных влиять на функцию почек, Акласту следует применять с осторожностью.
Перед применением Акласты, особенно у пожилых и получающих терапию диуретическими препаратами пациентов, необходимо обеспечить достаточную степень гидратации.
Однократная доза Акласты не должна превышать 5 мг, а длительность инфузии должна составлять не менее 15 минут.
Гипокальциемия
Ранее существующую гипокальциемию необходимо лечить адекватным приемом кальция и витамина D до начала терапии Акластой. Другие нарушения минерального обмена необходимо также эффективно лечить (например, уменьшение паращитовидной железы, нарушение абсорбции кальция в кишечнике). Врач должен тщательным образом контролировать этих пациентов.
Костная болезнь Педжета характеризуется высоким уровнем костного обмена. Вследствие быстрого наступления эффекта золедроновой кислоты в отношении костного обмена в течение первых 10 дней после инфузии препарата Акласта возможно развитие преходящей гипокальциемии, иногда симптоматической. На фоне назначения препарата Акласта рекомендуется прием достаточной дозы кальция и витамина D. Как дополнение, пациентам с болезнью Педжета настоятельно рекомендуется принимать адекватную дозу препарата кальция, соответствующую не менее чем по 500 мг элементарного кальция 2 раза в день, как минимум в течение первых 10 дней после введения препарата Акласта.
Следует проинформировать пациентов о симптомах гипокальциемии и обеспечить адекватный клинический мониторинг в период риска. Рекомендуется определять у пациентов с болезнью Педжета уровень кальция в сыворотке до инфузии препарата Акласта.
Сообщалось о нечастых случаях тяжелых и приводящих к временной нетрудоспособности болей в костях, суставах и/или мышцах у пациентов, принимающих бисфосфонаты, включая золедроновую кислоту.
Остеонекроз челюсти
Об остеонекрозе челюсти сообщалось в постмаркетинговых отчетах у пациентов, которые проходили курс лечения препаратом Акласта (золедроновой кислотой) по поводу остеопороза.
Начало лечения или проведение очередного курса лечения должно быть отложено у пациентов с неизлеченными открытыми повреждениями мягких тканей ротовой полости. Пациентам с сопутствующими факторами риска до начала лечения препаратом Акласта рекомендуется проходить стоматологическое обследование с проведением надлежащей стоматологической профилактики.
При оценке индивидуального риска развития остеонекроза челюсти следует рассматривать следующие факторы риска:
Потенцирование эффектов лекарственного средства, которое ингибирует костную резорбцию (повышенный риск для сильнодействующих веществ), способ введения (повышенный риск для парентерального введения) и суммарная доза препаратов, влияющих на костную резорбцию.
Диагностированный рак, сопутствующие заболевания (например, анемия, коагулопатии, инфекции), курение.
Сопутствующая терапия: химиотерапия, лучевая терапия шеи и головы, использование ингибиторов ангиогенеза, кортикостероидов.
Стоматологические заболевания в анамнезе, недостаточная гигиена полости рта, заболевания пародонта, плохо подогнанные зубные протезы, инвазивные стоматологические процедуры (например, удаление зуба).
Все пациенты должны быть проинформированы о необходимости поддержания хорошей гигиены полости рта и прохождения регулярных осмотров у стоматолога. Они должны немедленно сообщать о появлении во время лечения препаратом Акласта любых симптомов со стороны ротовой полости, таких как подвижность зубов, боль, припухлость, незаживающие язвочки или выделения. Во время лечения необходимые инвазивные стоматологические процедуры следует выполнять с осторожностью, и избегать их проведения в непосредственной близости по времени от инфузии золедроновой кислоты. План лечения пациентов, у которых развивается остеонекроз челюсти, должен быть разработан совместно лечащим врачом и хирургом-стоматологом с опытом лечения остеонекроза челюсти. Следует рассматривать временное прерывание лечения золедроновой кислоты до улучшения состояния и уменьшения факторов риска, если это возможно.
Остеонекроз наружного слухового прохода
Сообщалось об остеонекрозе наружного слухового прохода при долгосрочной терапии бисфосфонатами. Возможные факторы риска развития остеонекроза наружного слухового прохода включают использование стероидов и химиотерапию и/или местные факторы риска, такие как инфекция или травма. Возможность остеонекроза наружного слухового прохода следует рассматривать у пациентов, получающих бисфосфонаты, у которых есть симптомы, связанные с ухом, включая хронические инфекции уха.
Атипичный передом бедра
При терапии бисфосфонатами сообщалось о случаях возникновения атипичных подвертельных переломов и переломов диафиза бедренной кости, что наблюдалось главным образом среди пациентов, получавших длительную терапию при остеопорозе. Эти поперечные или короткие косые переломы могут возникнуть в любом участке бедренной кости, начиная с точки непосредственно ниже малого вертела и заканчивая точкой непосредственно выше надмыщелкового расширения. Эти переломы могут возникать в результате минимального травматического воздействия или даже без него, и у некоторых пациентов еще за несколько недель или месяцев до развития полного перелома бедренной кости может возникать чувство боли в области тазобедренного сустава или в паховой области. Переломы часто являются двусторонними; поэтому у пациентов, получающих терапию бисфосфонатами и у которых возник перелом диафиза бедренной кости, необходимо проводить оценку также и противоположной бедренной кости. Также сообщалось, что такие переломы плохо срастаются. У пациентов с подозрением на атипичный перелом бедренной кости, ориентируясь на индивидуальную оценку риска и пользы, следует рассмотреть возможность прекращения терапии бисфосфонатами, пока не будет выполнено достаточное уточняющее обследование данного пациента.
Во время лечения бисфосфонатами, включая Акласту, пациентов следует информировать о необходимости сообщать врачу, если у них возникает боль в области тазобедренного сустава, бедра или паха. При этом каждого пациента, у которого возникают такие симптомы, необходимо обследовать на предмет возможного возникновения перелома бедренной кости.
Общие
Симптомы недомогания, возникающие в течение первых трех дней после введения препарата Акласта, могут быть уменьшены приемом парацетамола или ибупрофена вскоре введения препарата.
Другие препараты, содержащие в качестве активного вещества золедроновую кислоту, применяются по онкологическим показаниям. Такие препараты или любой другой бисфосфонат нельзя назначать пациентам, уже получающим лечение препаратом Акласта, одновременно.
Этот лекарственный препарат содержит в 100 мл флаконе 23 мг (менее 1 ммоль) натрия, то есть может быть отнесен к препаратам, не содержащим натрия.
Способность влиять на скорость реакции при управлении автотранспортом или работе с другими механизмами
Акласта не оказывает или оказывает крайне слабое влияние на способность управлять автомобилем и сложными механизмами. Такие побочные реакции, как головокружение, могут отрицательно повлиять на способность управлять транспортными средствами или работать со сложными механизмами, несмотря на то, что прямых исследований подобных влияний препарата Акласта не проводилось.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Специальные исследования взаимодействия лекарственных средств с золедроновой кислотой не проводились. Золедроновая кислота систематически не метаболизируется и не влияет на энзимы цитохрома Р450 человека in vitro. Золедроновая кислота связывается с белками плазмы в незначительном количестве (связывание составляет приблизительно 4355 %), поэтому взаимодействия, происходящие в результате замещения лекарственных препаратов с высокой степенью связывания с белком, маловероятны.
Золедроновая кислота выводится из организма путем почечной экскреции. Следует соблюдать осторожность при применении Акласты в сочетании с препаратами, которые могут в значительной степени влиять на функцию почек (например, с аминогликозидами или диуретиками, которые могут вызвать дегидратацию). У пациентов с нарушением функции почек может увеличиваться системная экспозиция сопутствующих лекарственных препаратов, которые выводятся из организма главным образом почками.
Фармакологические свойства
Фармакодинамика
Механизм действия
Золедроновая кислота принадлежит к классу азотсодержащих бисфосфонатов и действует в первую очередь на кости. Она является ингибитором опосредованной остеокластами резорбции костной ткани.
Селективное действие бисфосфонатов предопределено их высоким сродством к минерализованной костной ткани. Золедроновая кислота, которая применяется внутривенно, быстро распределяется в костной ткани и, подобно другим бисфосфонатам, локализуется преимущественно в местах интенсивного обмена в костях. Главной молекулярной мишенью золедроновой кислоты в остеокласте является фермент фарнезилпирофосфатсинтаза, но это не исключает и другие механизмы. Относительно большая длительность действия золедроновой кислоты предопределена высоким сродством ее связывания с активным центром фарнезилпирофосфатсинтазы и сродством к связыванию с костными минералами.
Фармакодинамические эффекты
Лечение Акластой быстро уменьшает интенсивность метаболизма в костной ткани: от повышенных в постклимактерический период уровней с самой низкой точкой для маркеров резорбции на 7 сутки и до маркеров формирования костной ткани на 12 неделе. После этого уровень маркеров состояния костной ткани стабилизировался в пределах диапазона, наблюдаемого в пременопаузе. Не наблюдалось прогрессирующего снижения уровня маркеров метаболизма в костной ткани при введении повторных ежегодных доз.
Клиническая эффективность в лечении постменопаузального остеопороза (ПКО)
Эффективность и безопасность препарата Акласта в дозе 5 мг один раз в год в течение 3 лет была продемонстрирована в выборке женщин в постменопаузе (7736 женщин в возрасте 6589 лет) с: Т-баллом минеральной плотности кости (МПК) в области шейки бедренной кости ≤ -1,5 и как минимум двумя легкими или одним средним существующим переломом позвонков; или Т-баллом для МПК в области шейки бедренной кости ≤ -2,5 в сочетании или без сочетания с вертебральными переломами. 85 % ранее не получали терапии бисфосфонатами. Женщины, у которых оценивали частоту вертебральных переломов, не получали сопутствующей терапии по поводу остеопороза, такая терапия допускалась у женщин, у которых оценивалась частота переломов бедренной кости и всех клинических переломов. Сопутствующая терапия остеопороза также включала: кальцитонин, ралоксифен, тамоксифен, гормонзаместительную терапию, тиболон; но не включались другие бисфосфонаты. Все женщины получали 10001500 мг элементарного кальция и 4001200 ME витамина D в сутки.
Влияние на морфометрические вертебралъные переломы
Акласта значительно снижает частоту развития одного и более новых вертебральных переломов в течение трех лет уже по истечении одного года терапии (см. таблицу 2).
Таблица 2. Резюме эффективности профилактики вертебральных переломов через 12, 24 и 36 месяцев
| Исход | Акласта(%) | Плацебо(%) | Абсолютное снижение частоты переломов %(ДИ) | Относительное снижение частоты переломов % (ДИ) |
| Не менее одного вертебрального перелома (01 год) | 1,5 | 3,7 | 2,2 (1,4, 3,1) | 60 (43, 72)** |
| Не менее одного вертебрального перелома (02 год) | 2,2 | 7,7 | 5,5 (4,4, 6,6) | 71 (62, 78)** |
| Не менее одного вертебрального перелома (03 год) | 3,3 | 10,9 | 7,6 (6,3, 9,0) 1 | 70 (62, 76)** |
| ** p < 0,0001 |
У пациентов в возрасте 75 лет и старше, получавших Акласту, наблюдалось 60 % снижение риска вертебральных переломов по сравнению с пациентами, получавшими плацебо (p < 0,0001).
Влияние на переломы костей тазобедренного сустава
Акласта оказывала стойкий эффект в течение 3 лет, обеспечивая 41 % снижение риска переломов костей тазобедренного сустава (95 % ДИ, 17 % 58 %). Частота таких переломов среди пациентов из группы Акласта составляла 1,44 %, а в группе плацебо 2,49 %. Среди пациентов, не получавших ранее бисфосфонатов, снижение риска составляло 51 %, а среди пациентов, у которых допускалась сопутствующая терапия остеопороза, 42 %.
Влияние на все клинические переломы
Все клинические переломы верифицировали на основании рентгенологических и/или клинических данных. Сводка всех полученных результатов представлена в таблице 3.
Таблица 3. Сравнение частоты ключевых клинических переломов в течение 3 лет при различных режимах терапии
| Исход | Акласта(N = 3875)частота явлений(%) | Плацебо(N = 3861)частота явлений(%) | Абсолютное снижение частоты явлений в виде переломов %(ДИ) | Относительное снижение риска частоты переломов %(ДИ) |
| Любой клинический перелом (1) | 8,4 | 12,8 | 4,4 (3,0, 5,8) | 33 (23, 42)** |
| Клинический вертебральный перелом (2) | 0,5 | 2,6 | 2,1 (1,5, 2,7) | 77 (63, 86)** |
| Невертебральный перелом (1) | 8,0 | 10,7 | 2,7 (1,4, 4,0) | 25 (13, 36)* |
| * р-значение < 0,001, ** р-значение < 0,0001(1)Исключая пальцы рук, пальцы ног и костей лица(2)Включая клинические переломы позвонков грудного и поясничного отделов |
Влияние на минеральную плотность кости (МПК)
Акласта значительно повышала МПК в области поясничного отдела позвоночника, бедренной кости и дистального отдела лучевой кости в сравнении с плацебо во все временные точки (6, 12, 24 и 36 месяцев). Лечение Акластой привело к повышению МПК поясничных позвонков на 6,7 %, проксимального отдела бедра на 6,0 % , шейки бедра на 5,1 % и дистальной части лучевой кости на 3,2 % в течение 3 лет по сравнению с плацебо.
Гистология костей
Биопсию костей получали из области гребня подвздошной кости через 1 год после третьей ежегодной дозы в выборке 152 женщин в постменопаузе с остеопорозом, получавших Акласту (N = 82) или плацебо (N = 70). Гистоморфометрический анализ выявил снижение ремоделирования кости на 63 %. У пациентов, получавших Акласту, не выявили остеомаляции, фиброза костного мозга или образования костной ткани. Тетрациклиновая метка выявлялась во всех кроме одного из 82 биоптатов у пациентов, получавших Акласту. Результаты микрокомпьютерной томографии (МКТ) выявили увеличение трабекулярного объема кости и сохранение трабекулярной архитектуры кости у пациентов, получавших Акласту по сравнению с пациентами, получавшими плацебо.
Маркеры ремоделирования кости
В подвыборках, включающих от 517 до 1246 пациентов, с определенной периодичностью на протяжении всего исследования оценивали уровни костной щелочной фосфатазы (КЩФ), сывороточного N-терминального пропептида коллагена I типа (P1NP) и сывороточных бета-С-телопептидов (b-СТх). Лечение с ежегодным введением дозы 5 мг препарата Акласта значительно снижало уровни КЩФ на 30 % на 12 месяце в сравнении с исходным этапом, при этом на 36 месяце это снижение составляло 28 % в сравнении с исходным этапом. Уровни P1NP значительно снижались на 61 % ниже исходного уровня на 12 месяце, а на 36 месяце были на 52 % ниже исходного уровня. Уровни В-СТх значительно снижались на 61 % ниже исходного уровня на 12 месяце, а на 36 месяце были на 55 % ниже исходного уровня. В течение всего периода времени в конце каждого года маркеры костного ремоделирования находились в пределах пременопаузного диапазона. Многократное применение препарата не вызывало дальнейшего снижения маркеров костного ремоделирования.
Влияние на рост
В трехлетнем исследовании остеопороза ежегодно измеряли рост в положении стоя с помощью ростомера. В группе препарата Акласта наблюдалось снижение потери роста примерно на 2,5 мм в сравнении с группой плацебо (95 % ДИ: 1,6 мм, 3,5 мм) [p < 0,0001].
Продолжительность нетрудоспособности
Акласта значительно снижал среднюю продолжительность (на 17,9 дней) ограничения активности и продолжительность постельного режима по причине боли в спине (на 11,3 дней) по сравнению с плацебо, а также по сравнению с плацебо значительно снижал среднюю продолжительность ограничения активности (на 2,9 дней) и продолжительность постельного режима (на 0,5 дней) по причине переломов (все p < 0,01).
Клиническая эффективность в лечении остеопороза у пациентов с повышенным риском переломов после недавнего перелома тазобедренных костей (НПТК)
Частота возникновения клинических переломов, включая позвоночные, непозвоночные переломы и переломы бедра, оценивалась среди у 2127 мужчин и женщин в возрасте от 50 до 95 лет (средний возраст 74,5 лет) с недавним (в течение 90 суток) переломом бедренных костей при минимальной травме; пациенты находились в среднем в течение 2 лет наблюдения на фоне терапии исследуемым препаратом. Примерно у 42 % пациентов Т-балл МПК в области шейки бедра был ниже -2,5 и примерно у 45 % пациентов Т-балл МПК в области шейки бедра был выше -2,5. Акласта назначался один раз в год до тех пор, пока как минимум у 211 пациентов в исследуемой выборке не были подтверждены клинические переломы. Рутинного измерения уровней витамина D в организме не проводили, однако за 2 недели до инфузии большинство пациентов получало нагрузочную дозу витамина D (50 000125 000 ME внутрь или внутривенно). Все участники получали 10001500 мг элементарного кальция и 8001200 ME витамина D в сутки. Девяносто пять процентов пациентов получили инфузию препарата через 2 и более недель после восстановительного вмешательства по поводу перелома тазобедренных костей, при этом медиана периода времени от реперативного вмешательства по поводу перелома до проведения инфузии составляла шесть недель. Основной конечный показатель эффективности был ??? частотой клинических переломов в течение периода исследования.
Влияние на все клинические переломы
Показатели частоты ключевых клинических переломов представлены в таблице 4.
Таблица 4. Сравнение частоты ключевых клинических переломов при различных режимах терапии
| Исход | Акласта(N = 1065)частота явлений(%) | Плацебо(N = 1062)частота явлений(%) | Абсолютное снижение частоты явлений в виде переломов %(ДИ) | Относительное снижение риска частоты переломов%(ДИ) |
| Любой клинический перелом (1) | 8,6 | 13,9 | 5,3 (2,3, 8,3) | 35 (16, 50)** |
| Клинический вертебральный перелом (2) | 1,7 | 3,8 | 2,1 (0,5, 3,7) | 46 (8, 68)* |
| Невертебральный перелом (1) | 7,6 | 10,7 | 3,1 (0,3, 5,9) | 27 (2, 45)* |
| * р-значение < 0,05, ** р-значение < 0,01(1)Исключая пальцы рук, пальцы ног и костей лица(2)Включая клинические переломы позвонков грудного и поясничного отделов |
Дизайн исследования не предусматривал возможность измерения достоверной разницы между показателями частоты переломов костей тазобедренного сустава, тем не менее, наблюдалась тенденция к снижению частоты новых переломов костей тазобедренного сустава.
В группе, получавшей препарат Акласта, общая смертность составляла 10 % (101 пациент), а в группе плацебо 13 % (141 пациент). Это соответствует 28 % снижению риска общей смертности (p = 0,01).
Частота замедленного сращения переломов костей тазобедренной области в группе Акласта (34 [3,2 %]) и группе плацебо (29 [2,7 %]) были сравнимы.
Влияние на минеральную плотность кости (МПК)
В исследовании HORIZON-RFT терапия препаратом Акласта во всех оцениваемых моментах времени значительно увеличивала МПК во всех костях тазобедренного сустава и в области шейки бедренной кости по сравнению с плацебо. Лечение препаратом Акласта по сравнению с плацебо в течение 24 месяцев обеспечивало увеличение МПК на 5,4 % во всех костях тазобедренного сустава и на 4,3 % в области шейки бедренной кости.
Клиническая эффективность у мужчин
В исследовании HORIZON-RFT рандомизировали 508 мужчин, а на 24 месяце оценку МПК удалось выполнить у 185 пациентов. В исследовании HORIZON-PFT на 24 месяце у пациентов, получавших Акласту, наблюдалось схожее значительное повышение на 3,6 % МПК всех костей тазобедренного сустава, по сравнению с женщинами в постменопаузе. Исследование не обладало достаточной силой для выявления снижения частоты клинических переломов у мужчин; частота клинических переломов составляла 7,5 % у мужчин, получавших Акласту, и 8,7 %, получавших плацебо.
В другом исследовании у мужчин (исследование CZOL446M2308) ежегодная инфузия препарата Акласта не уступала по эффективности еженедельному применение алендроната в рамках процентного изменения МПК поясничных позвонков на 24 месяцев в сравнении с исходным уровнем.
Клиническая эффективность в лечении остеопороза, ассоциированного с длительной системной терапией кортикостероидами
Эффективность и безопасность препарата Акласта в лечении и профилактике остеопороза, ассоциированного с длительной системной терапией глюкокортикостероидами оценивали в рамках рандомизированного, многоцентрового, двойного слепого, стратифицированного, исследования с активным контрольным препаратом, среди 833 мужчин и женщин в возрасте 1885 лет (средний возраст мужчин 56,4 лет; женщин 53,5 года), получавших > 7,5 мг/сутки преднизолона внутрь (или его эквивалент). Пациентов стратифицировали в зависимости от длительности глюкокортикоидной терапии до рандомизации (≤ 3 месяца или > 3 месяцев). Длительность исследования составляла один год. Пациентов рандомизировали либо на получение однократной инфузии Акласта 5 мг, либо на пероральный прием ризедроната 5 мг в сутки на протяжении одного года. Все участники получали 1000 мг элементарного кальция и 4001000 ME витамина D в сутки. Эффективность констатировали, если последовательно наблюдалась не меньшая эффективность по сравнению с ризедронатом в рамках процентного изменения МПК поясничных позвонков на 12 месяце по сравнению с исходным этапом в подвыборках участников, которым проводили лечение и профилактику. Большинство пациентов продолжали получать глюкокортикоиды в течение всего однолетнего периода исследования.
Влияние на минеральную плотность кости (МПК)
На 12 месяце в группе препарата Акласта по сравнению с группой ризедроната наблюдалось значительно большее повышение МПК поясничного отдела позвоночника и костей тазобедренной области (во всех случаях p < 0,03). В подвыборке пациентов, получавших глюкокортикоиды в течение более 3 месяцев до рандомизации, препарат Акласта повышал МПК поясничных позвонков на 4,06 %, тогда как в группе ризедроната данный показатель повышался на 2,71 % (средняя разница: 1,36 %; p < 0,001). В подвыборке пациентов, получавших глюкокортикоиды в течение 3 месяцев и менее до рандомизации, препарат Акласта повышал МПК поясничных позвонков на 2,60 %, тогда как в группе ризедроната данный показатель повышался на 0,64 % (средняя разница: 1,96 %; p < 0,001). Данное исследование не обладало достаточной силой для выявления снижения частоты клинических переломов по сравнению с ризедронатом. Частота переломов среди пациентов из группы Акласта составляла 8, а среди пациентов из группы ризедроната 7 (p = 0,8055).
Клиническая эффективность в лечении костной болезни Педжета
Препарат Акласта исследовали среди пациентов мужского и женского пола в возрасте старше 30 лет, страдающих болезнью Педжета преимущественно легкой и умеренной степени тяжести (на момент включения в исследование медиана уровня сывороточной щелочной фосфатазы в 2,63,0 раза выше верхней границы диапазона нормальных значений при коррекции на возраст) согласно рентгенологическим данным.
Эффективность одной инфузии 5 мг золедроновой кислоты в сравнении с ежедневными дозами 30 мг ризедроната на протяжении 2 месяцев была продемонстрирована в двух 6-месячных исследованиях. По истечении 6 месяцев Акласта обеспечивал в 96 % (169/176) случаев ответную реакцию и в 89 % (156/176) нормализацию уровней сывороточной щелочной фосфатазы (СЩФ), в группе ризедроната эти показатели составляли соответственно 74 % (127/171) и 58 % (99/171) (все значения p < 0,001).
При рассмотрении сгруппированных результатов для Акласты и для ризедроната в течение 6 месяцев наблюдались схожие снижения баллов тяжести боли и влияния боли в сравнении с исходными этапами.
Пациенты, классифицированные к концу 6 месяца основного этапа исследования как отреагировавшие, были пригодны к участию в продленном наблюдательном периоде исследования. Из 153 пациентов, получавших Акласту, и из 115 пациентов, получавших ризедронат, которые были включены в продленное обсервационное исследование, после периода наблюдения в среднем 3,8 лет с момента получения препарата доля пациентов, выходящих из продленного периода наблюдения по причине необходимости повторного приема препарата (по клиническому суждению) была выше в группе ризедроната (48 пациентов, или 41,7 %), чем в группе золедроновой кислоты (11 пациентов, или 7,2 %). Среднее время выхода из продленного периода наблюдения из-за необходимости повторного приема препарата для лечения болезни Педжета от момента приема первой дозы была большей в группе золедроновой кислоты (7,7 лет) по сравнению с группой ризедроната (5,1 год).
Шесть пациентов, достигших терапевтического ответа на 6 месяце после терапии препаратом Акласта, и у которых позднее развивался рецидив заболевания в течение Продленного Наблюдательного Периода, получили повторно препарат Акласта, при этом медиана времени от предыдущего получения препарата по повторного получения препарата составляла 6,5 лет. У пяти из шести пациентов на 6-ом месяце уровни СЩФ находились в пределах нормальных значений (Последнее наблюдение, перенесенное вперед, LOCF).
У 7 пациентов с болезнью Педжета через 6 месяцев после получения 5 мг золедроновой кислоты оценивали гистологию костной ткани. Результаты биопсии костной ткани выявили нормальное качество костной ткани без признаков нарушения ремоделирования кости и без признаков нарушения минерализации. Эти результаты соответствовали данным исследования биохимических маркеров, свидетельствовавшим о нормализации костного обмена.
Европейское агентство по лекарственным препаратам устранило необходимость предоставления результатов исследований с применением Акласты во всех категориях пациентов педиатрического профиля по показаниям костная болезнь Педжета, остеопороз у женщин в постменопаузе с повышенным риском переломов, остеопороз у мужчин с повышенным риском переломов и профилактика клинических переломов после переломов после уже перенесенных переломов костей тазобедренного сустава у мужчин и женщин (информация о применении у детей представлена в разделе «Дозы и способ применения»).
Фармакокинетика
В результате проведения однократных и многократных 5- и 15-минутных инфузий в дозах 2, 4, 8 и 16 мг золедроновой кислоты 64 пациентам были получены нижеследующие данные фармакокинетики, не зависящих от дозы.
После начала инфузии золедроновой кислоты плазменные концентрации активного вещества быстро увеличивались, достигая пика в конце инфузии, потом быстро снижались до < 10 % пика через 4 часа и до < 1 % пика через 24 часа, с дальнейшим длительным периодом очень низких концентраций, которые не превышают 0,1 % пиковых уровней.
Внутривенно введенная золедроновая кислота выделяется почками в три этапа: быстрое двухфазное выведение препарата из системной циркуляции с периодами полувыведения t½α 0,24 и t½β 1,87 часов, потом продолжительная фаза элиминации с конечным периодом полувыведения t½γ 146 часов. Накопления активного вещества в плазме после многократных доз, которые вводились каждые 28 дней, не наблюдалось. На ранних фазах диспозиций (α и β, с указанными выше значениями t½) возможно быстрое распределение в костях и выведение через почки. Золедроновая кислота не метаболизируется и выделяется в неизмененном виде почками. В течение первых 24 часов 39 ± 16 % введенной дозы экскретируется с мочой, тогда как другое количество препарата в основном связывается с костной тканью. Впоследствии происходит медленное обратное высвобождение золедроновой кислоты из костной ткани в системную циркуляцию и ее выделение почками. Общий клиренс препарата составляет 5,04 ± 2,5 л/час. Он не зависит от дозы, пола, возраста, расовой принадлежности и массы тела пациента. Увеличение длительности инфузии с 5 до 15 минут приводит к снижению концентрации золедроновой кислоты в конце инфузии, но не влияет на площадь под кривой зависимости концентрации от времени.
Поскольку золедроновая кислота не метаболизируется в организме человека, и обнаруженное вещество имеет лишь незначительную активность или не имеет совсем как непосредственно действующий и/или необратимый ингибитор ферментов цитохрома Р450, золедроновая кислота вряд ли будет уменьшать метаболический клиренс вещества, которое метаболизируется системой ферментов цитохрома Р450. Золедроновая кислота не имеет высокой степени связывания с белками плазмы (связывание составляет приблизительно 4355 %), и это связывание не зависит от концентрации.
Отдельные популяции. Почечный клиренс золедроновой кислоты коррелировал с клиренсом креатинина, почечный клиренс составлял 75 ± 33 % от клиренса креатинина, который продемонстрировал среднее значение 84 ± 29 мл/мин (диапазон от 22 до 143 мл/мин) у 64 исследуемых пациентов. Незначительное увеличение AUC(024ч), приблизительно на 3040 % при почечной недостаточности от легкой до умеренной степени тяжести в сравнении с таковым у пациентов с нормальной почечной функцией и отсутствие накопления лекарственного средства при многократных введениях доз независимо от почечной функции свидетельствуют о том, что в коррекции дозы золедроновой кислоты при почечной недостаточности легкой (Clcr = 5080 мл/мин) и умеренной (Clcr = 3550 мл/мин) степени тяжести нет необходимости. Применение Акласты противопоказано пациентам с тяжелыми нарушениями функции почек (клиренс креатинина < 35 мл/мин), в связи с повышенным??? риском развития почечной недостаточности в этой популяции.
Фармацевтические характеристики
Основные физико-химические свойства
Стерильный, прозрачный и бесцветный раствор.
Несовместимость
Раствор Акласты для инфузии нельзя смешивать с растворами, которые содержат ионы кальция и другие бивалентные катионы.
Препарат Акласта совместим с типичными материалами инфузионной линии такими как, поливинилхлорид, полиуретан и полиэтилен.