Боль. Практическое руководство. 2-е издание
Под редакцией Н.Н. Яхно
МЕДпресс-информ, 2023 г.
Твердый переплет, 416 стр., илл.
ISBN 978-5-907632-12-7
Описание:
Боль – одна из актуальных проблем медицины. В руководстве изложены современные сведения о физиологии, патофизиологии острой и хронической боли, методах обследования пациентов с болевыми синдромами, включая специализированные опросники и шкалы, их лечение. В отдельных главах рассматриваются основные формы болевых синдромов: невропатическая боль, головные и лицевые боли, боль в спине и тазовая боль, боль при ревматических и онкологических заболеваниях, а также психологические аспекты боли. Руководство подготовлено ведущими российскими специалистами и предназначено для врачей разных специальностей и студентов медицинских вузов.
Дополнительно:
См. содержание и примеры страниц
Гипермаркет для медиков

Время работы (по Москве)
пн • вт • ср • чт • пт • сб • вс
9-20
Звонок по России бесплатный

Боль. Практическое руководство
| Артикул | NF0022217 |
|---|
| ISBN |
978-5-907504-41-7 |
|---|---|
| Издательство |
МЕДпресс-информ |
| Автор |
Под ред. Н.Н. Яхно |
| Год |
2022 |
| Страниц |
416 |
| Переплет |
твердый |
1430 руб.
В наличии
-
Описание
-
Комментарии
Боль – одна из актуальных проблем медицины. В руководстве изложены современные сведения о физиологии, патофизиологии острой и хронической боли, методах обследования пациентов с болевыми синдромами, включая специализированные опросники и шкалы, их лечение. В отдельных главах рассматриваются основные формы болевых синдромов: невропатическая боль, головные и лицевые боли, боль в спине и тазовая боль, боль при ревматических и онкологических заболеваниях, а также психологические аспекты боли. Руководство подготовлено ведущими российскими специалистами и предназначено для врачей разных специальностей и студентов медицинских вузов.
Книга «Боль. Практическое руководство»
Автор: Н. Н. Яхно
ISBN 978-5-907504-41-7
Боль – одна из актуальных проблем медицины. В руководстве изложены современные сведения о физиологии, патофизиологии острой и хронической боли, методах обследования пациентов с болевыми синдромами, включая специализированные опросники и шкалы, их лечение. В отдельных главах рассматриваются основные формы болевых синдромов: невропатическая боль, головные и лицевые боли, боль в спине и тазовая боль, боль при ревматических и онкологических заболеваниях, а также психологические аспекты боли. Руководство подготовлено ведущими российскими специалистами и предназначено для врачей разных специальностей и студентов медицинских вузов.
Содержание книги «Боль. Практическое руководство» — Н. Н. Яхно
Глава 1. НЕЙРОФИЗИОЛОГИЯ, НЕЙРОХИМИЯ, ПАТОФИЗИОЛОГИЯ И ПРИНЦИПЫ ТЕРАПИИ БОЛИ
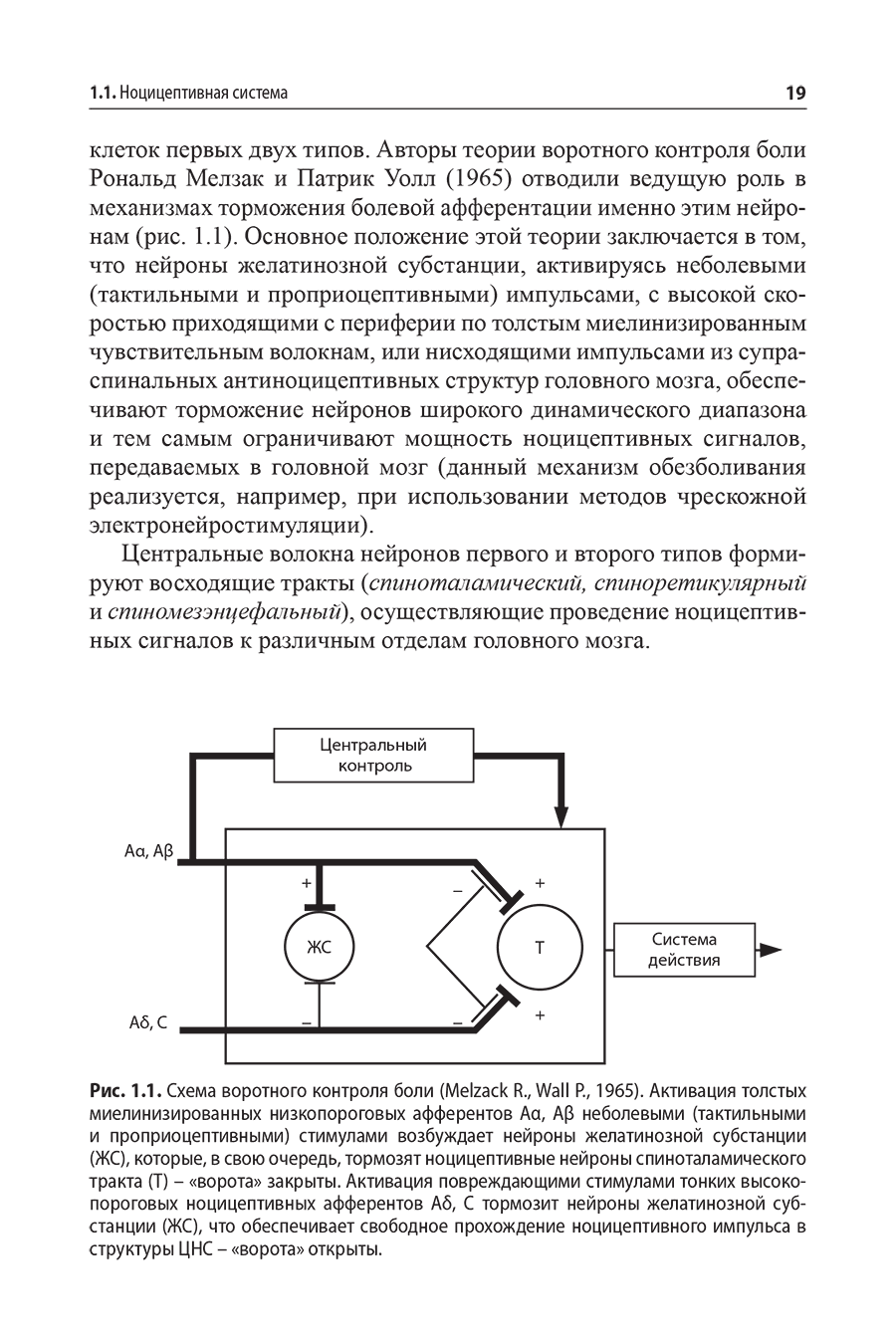
1.1. Ноцицептивная система
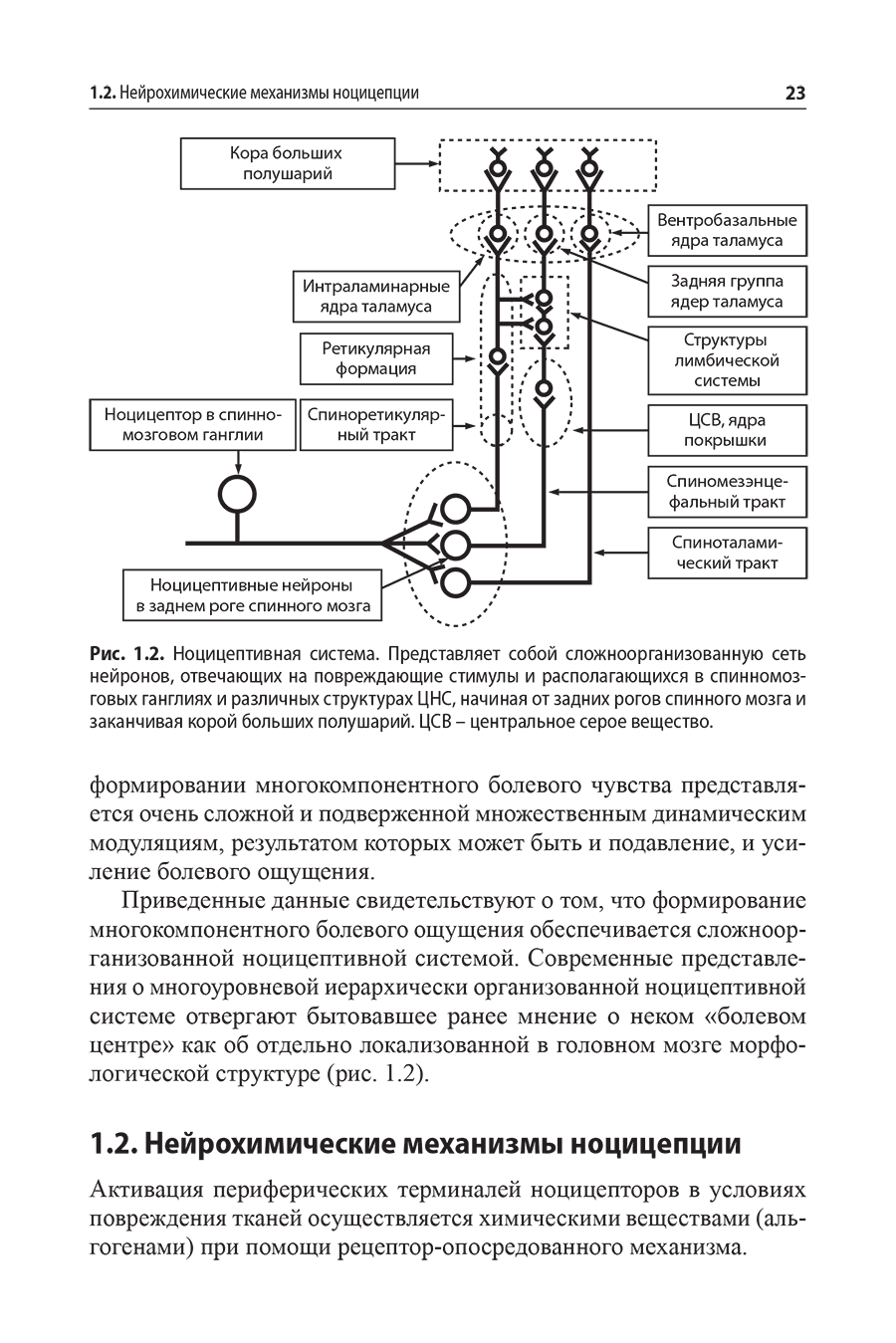
1.2. Нейрохимические механизмы ноцицепции
1.3. Антиноцицептивная система мозга
1.4. Патофизиология боли
1.4.1. Патофизиология ноцицептивной боли
1.4.2. Патофизиология невропатической боли
1.4.3. Патофизиология дисфункциональной боли
1.4.4. Патофизиология хронической боли
1.5. Принципы терапии боли
1.5.1. Медикаментозная терапия боли
1.5.2. Немедикаментозная терапия боли
Тесты для самоконтроля
Глава 2. ОБСЛЕДОВАНИЕ ПАЦИЕНТА С БОЛЕВЫМ СИНДРОМОМ
2.1. Опрос
2.2. Клиническое обследование
2.2.1. Оценка чувствительных и двигательных нарушений
2.2.2. Шкалы и опросники для оценки боли
2.2.3. Оценка поведенческих составляющих болевого ощущения
2.3. Инструментальные методы исследования
2.3.1. Ноцицептивный флексорный рефлекс
2.3.2. Количественное сенсорное тестирование
2.3.3. Электронейромиография
2.3.4. Исследование вызванных кожных симпатических потенциалов
2.3.5. Термография
2.3.6. Морфологические исследования
Тесты для самоконтроля
Глава 3. НЕВРОПАТИЧЕСКАЯ БОЛЬ
3.1. Определение и классификация невропатической боли
3.2. Эпидемиология и общая характеристика невропатической боли
3.3. Диагностика невропатической боли
3.4. Периферическая невропатическая боль
3.5. Центральная невропатическая боль
3.6. Комплексный регионарный болевой синдром
3.7. Невропатическая боль при онкологических заболеваниях
3.8. Лечение невропатической боли
3.8.1. Принципы и подходы к терапии
3.8.2. Фармакотерапия невропатической боли
3.8.3. Нелекарственные методы лечения невропатической боли
3.8.4. Интервенционные и хирургические методы лечения невропатической боли
Тесты для самоконтроля
Глава 4. ГОЛОВНАЯ БОЛЬ
4.1. Патофизиология головной и лицевой боли
4.2. Обследование пациентов с головной болью
4.3. Первичные головные боли
4.3.1. Мигрень
4.3.2. Пучковая головная боль
4.3.3. Головная боль напряжения
4.4. Вторичная головная боль
4.4.1. Посттравматическая головная боль
4.4.2. Цервикогенная головная боль
4.4.3. Головная боль при цереброваскулярных заболеваниях
4.4.4. Головная боль, обусловленная артериальной гипертензией
4.4.5. Головная боль, обусловленная изменением давления цереброспинальной жидкости
4.4.6. Лекарственно-индуцированная головная боль
4.5. Хроническая ежедневная головная боль
Тесты для самоконтроля
Глава 5. ЛИЦЕВЫЕ И РОТОВЫЕ БОЛЕВЫЕ СИНДРОМЫ
5.1. Невралгия тройничного нерва
5.2. Постгерпетическая невралгия тройничного нерва (постгерпетическая невропатия тройничного нерва)
5.3. Невралгия языкоглоточного нерва
5.4. Кратковременные односторонние невралгические приступы головной боли с конъюнктивальной инъекцией и слезотечением (синдром КОНКС)
5.5. Синдром Толосы–Ханта
5.6. Офтальмоплегическая мигрень
5.7. Миофасциальный орофациальный болевой синдром
5.8. Синдром «горящего рта» (глоссодиния)
5.9. Атипичная лицевая боль (персистирующая идиопатическая лицевая боль)
Тесты для самоконтроля
Глава 6. БОЛЬ В ШЕЕ И СПИНЕ
6.1. Причины боли в шее и спине
6.1.1. Неспецифические причины боли в шее и спине
6.1.2. Специфические причины боли в шее и спине
6.2. Психологические и социальные факторы боли в шее и спине
6.3. Обследование пациентов
6.3.1. Жалобы, анамнез и физикальное исследование
6.3.2. Инструментальные методы исследования
6.3.3. Оценка психосоциальных факторов боли
6.4. Клиническая картина
6.4.1. Неспецифическая боль в шее и спине
6.5. Вертеброгенная радикулопатия.
6.6. Шейная миелопатия
6.7. Поясничный стеноз
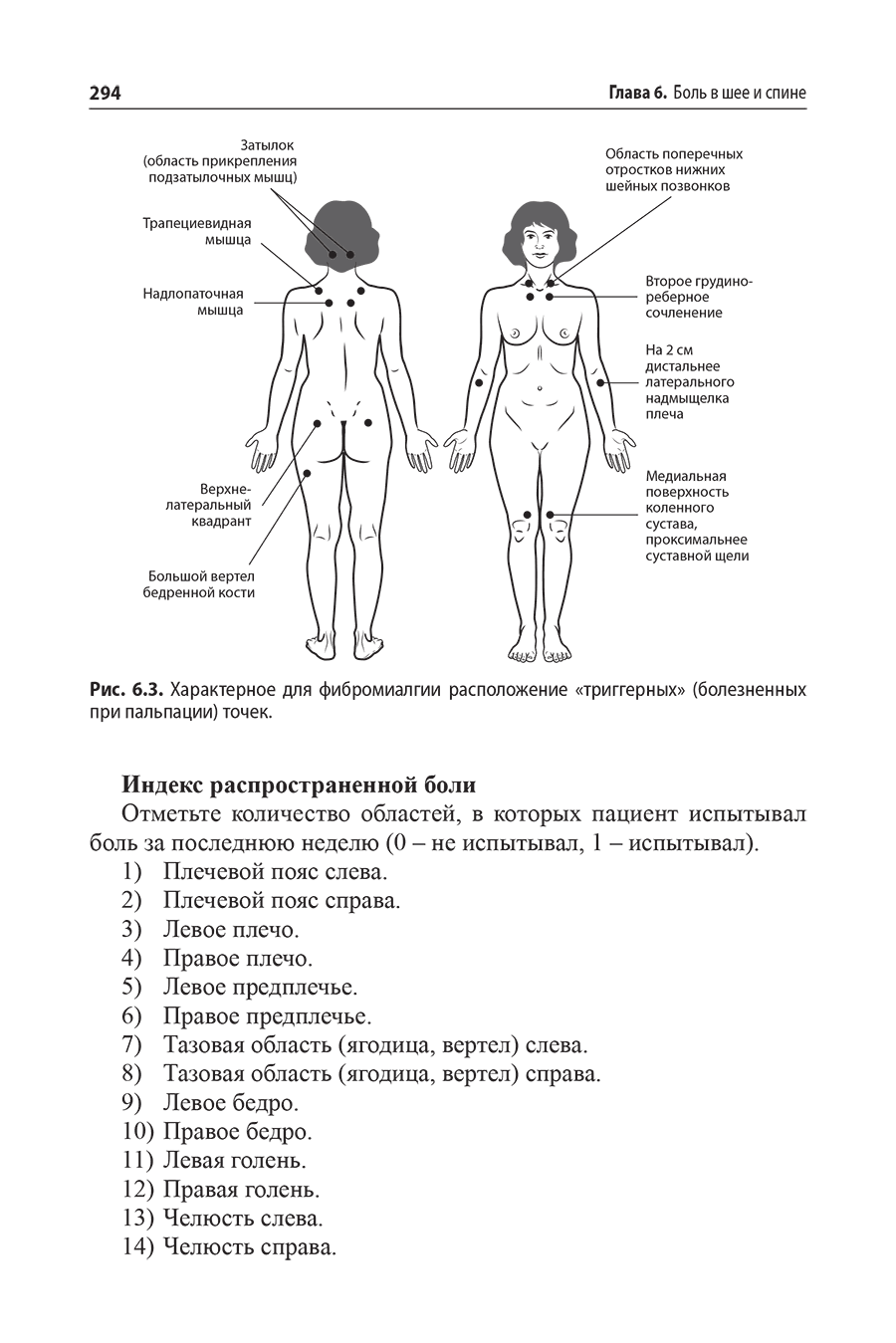
6.8. Фибромиалгия
6.9. Лечение и профилактика.
6.9.1. Лечение острой неспецифической боли
6.9.2. Лечение хронической неспецифической боли
6.9.3. Лечение вертеброгенной радикулопатии
6.9.4. Лечение шейной миелопатии
6.9.5. Лечение центрального поясничного стеноза
6.9.6. Лечение фибромиалгии
Тесты для самоконтроля
Глава 7. СИНДРОМ ХРОНИЧЕСКОЙ ТАЗОВОЙ БОЛИ
7.1. Клинические варианты синдрома хронической тазовой боли
7.2. Лечение
Глава 8. БОЛЬ В СУСТАВАХ ПРИ РЕВМАТИЧЕСКИХ ЗАБОЛЕВАНИЯХ
8.1. Клиническое обследование
8.2. Наиболее частые причины боли в суставах
8.3. Наиболее распространенные ревматические заболевания: общая информация
8.4. Основные направления лечения боли при ревматических заболеваниях
8.5. Патология околосуставных мягких тканей
8.6. Артралгии и артриты при неревматических заболеваниях
Тесты для самоконтроля
Глава 9. ХРОНИЧЕСКИЙ БОЛЕВОЙ СИНДРОМ В ОНКОЛОГИИ
9.1. Эпидемиология и классификация
9.2. Диагностика
9.3. Лечение
9.3.1. Контроль боли у пациентов, возможности противоопухолевой терапии у которых исчерпаны
9.3.2. Основные опиоидные анальгетики
9.3.3. Обезболивание в конце жизни
Тесты для самоконтроля
Глава 10. ПСИХОЛОГИЧЕСКИЕ АСПЕКТЫ ХРОНИЧЕСКОЙ БОЛИ
10.1. Когнитивные, эмоционально-аффективные и поведенческие аспекты хронической боли
10.2. Психологические методы лечения боли
Тесты для самоконтроля
Приложения
Приложение 1. Краткий болевой опросник
Приложение 2. Опросник Роланда–Морриса
Приложение 3. Опросник выраженности психопатологической симптоматики (SCL-90R)
Приложение 4. Шкала Гамильтона для оценки депрессии
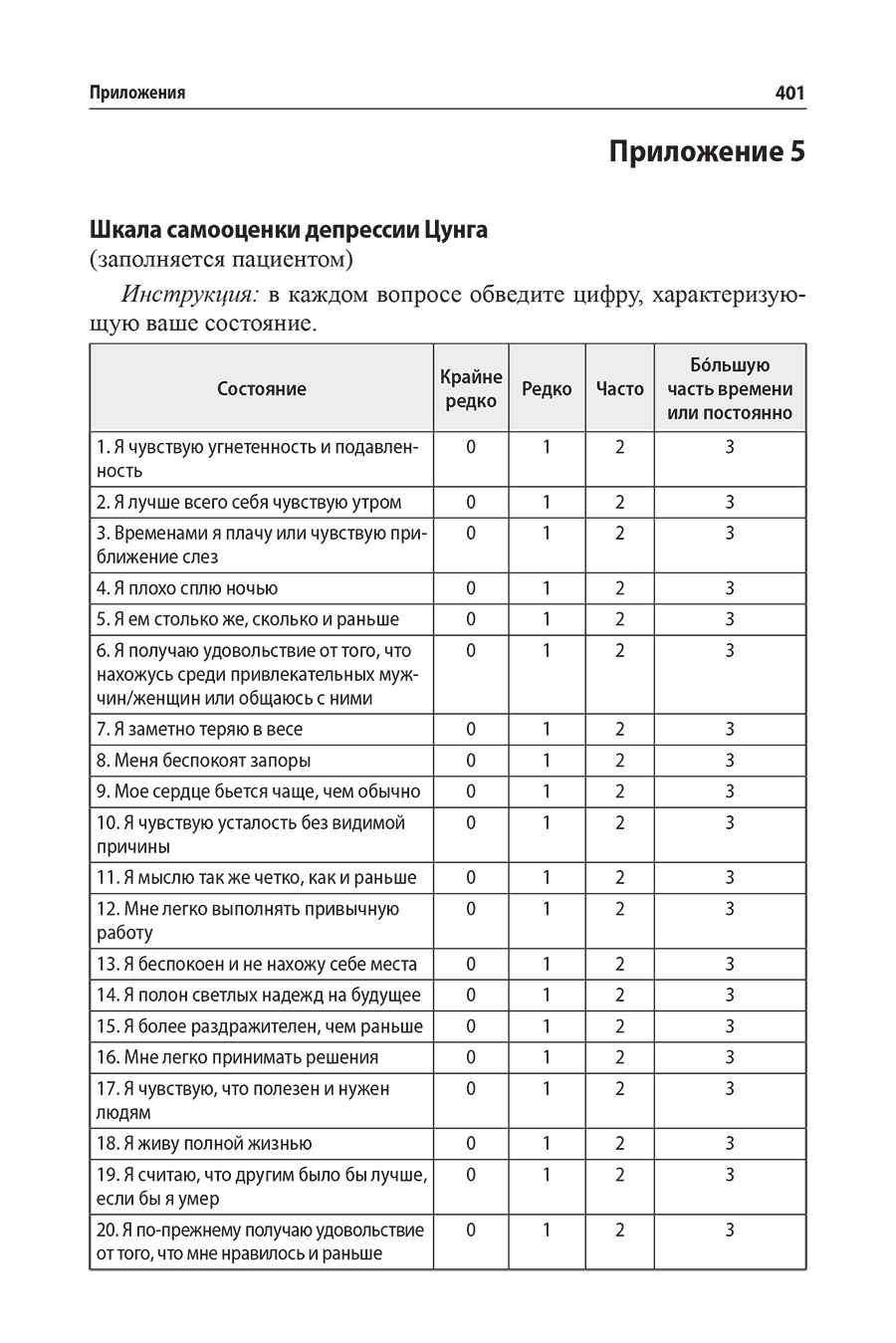
Приложение 5. Шкала самооценки депрессии Цунга
Приложение 6. Опросник стратегий преодоления хронической боли
Приложение 7. Шкала болевого поведения Университета Алабамы
Приложение 8. Опросник Освестри
Приложение 9. Анкета Ван-Корффа для оценки выраженности хронического болевого синдрома
Примеры страниц из книги «Боль. Практическое руководство» — Н. Н. Яхно
Читать онлайн «Боль. Руководство для студентов и врачей»
Деменции: руководство для врачей
СПИСОК СОКРАЩЕНИЙ
БА — болезнь Альцгеймера
БВК — болезнь Вильсона-Коновалова
БГ — болезнь Гентингтона
БТЛД — Батарея тестов для оценки лобной дисфункции
БП — болезнь Паркинсона
БТ — болезнь Туретта
ВИЧ — вирус иммунодефицита человека
ВОЗ — Всемирная организация здравоохранения
ГЭ — герпетический энцефалит
ДТЛ — деменция с тельцами Леви
ЗКА — задняя корковая атрофия
КБД — кортико-базальная дегенерация
KP — когнитивные расстройства
KT — компьютерная томография
КФ — когнитивная функция
КШОПС — Краткая шкала оценки психического статуса
ЛБ — Лайма болезнь
ЛВД — лобно-височная дегенерация
ЛКР — легкие когнитивные расстройства
МРТ — магнитно-резонансная томография
МВС — менинговаскулярный сифилис
МСА — множественная системная атрофия
НТГ — нормотензивная гидроцефалия
OA — общая анестезия
ПНП — прогрессирующий надъядерный паралич
ПОКД — послеоперационная когнитивная дисфункция
ПП — прогрессирующий паралич
ППА — первичная прогрессирующая афазия
ПТА — посттравматическая афазия
PC — рассеянный склероз
СГ — субдуральная гематома
СКН — сосудистые когнитивные нарушения
СмД — смешанная деменция
СоД — сосудистая деменция
СПИД — синдром приобретенного иммунодефицита
ТКР — тяжелые когнитивные расстройства
ТРЧ — тест рисования часов
УКР — умеренные когнитивные расстройства
ХСГ — хроническая субдуральная гематома
ЧМТ — черепно-мозговая травма
ЦАА — церебральная амилоидная ангиопатия
ВВЕДЕНИЕ
Начиная со второй половины XX в. во всем мире наблюдается изменение возрастной структуры населения с постоянным увеличением в популяции доли пожилых и старых людей. Поэтому в современной медицине приобретают все большее значение профилактика и лечение большого числа возраст-зависимых заболеваний. Среди последних одно из ведущих мест занимают неврологические и нервно-психические нарушения, обусловленные как первичными расстройствами нервной системы, так и различными соматическими заболеваниями.
Деменция и недементные когнитивные нарушения по распространенности являются ведущими среди заболеваний головного мозга. По данным европейских эпидемиологических исследований, деменция наблюдается у 6–7% людей старше 65 лет, и одна лишь болезнь Альцгеймера занимает 2-3-е место по величине расходов на медицинскую и социальную помощь среди неврологических и психических расстройств. Еще чаще встречаются недементные когнитивные нарушения. Исходя из этого, очевидна их медицинская и социальная значимость.
До недавнего времени вопросы диагностики и лечения больных с деменцией относились к сфере профессиональных обязанностей психиатров. Между тем, в Международной классификации болезней рубрики, относящиеся к синдрому деменции и ее отдельным нозологическим формам, присутствуют в разделах, касающихся и психиатрических, и неврологических заболеваний. При этом некоторая часть деменций носит соматогенный характер, может быть обусловлена токсическими и ятрогенными воздействиями. Из этого видно, что проблема деменции носит мультидисциплинарный характер и о ней должны быть осведомлены не только неврологи и психиатры, но и врачи других специальностей. Важность этого положения усиливается и тем, что во многих случаях синдром деменции развивается из более легких (недементных) когнитивных нарушений, сопровождающих большое число неврологических и соматических заболеваний. Своевременное выявление когнитивных нарушений на додементных стадиях повышает возможности их лечения и вторичной профилактики деменций.
Головная боль — одна из наиболее частых жалоб на приеме врача общей практики. Диагностика и терапия головной боли нередко представляют большие трудности, особенно на этапе первичной медицинской помощи.
Основным инструментом диагностики любых форм головной боли как для неврологов, так и для других специалистов является Международная классификация головной боли третьего пересмотра (МКГБ-3), которая содержит не только диагностические критерии, но и основные принципы диагностики первичных и вторичных цефалгий [1].
По данным многочисленных эпидемиологических исследований наибольшее распространение в популяции имеют первичные (доброкачественные) формы головной боли, когда не удается выявить органическую причину боли (табл. 1). Частота вторичных (симптоматических) форм, обусловленных органическими поражениями головного мозга или других структур, расположенных в области головы и шеи, а также системными заболеваниями, составляет лишь 2–5% [2].
Наибольшее распространение в популяции, а значит, и в практике терапевта имеют следующие формы головной боли [1]:
- Мигрень (с аурой и без ауры).
- Хроническая мигрень. Хроническая мигрень представляет собой головную боль любого типа (мигренеподобную или подобную головной боли напряжения (ГБН)), возникающую 15 и более дней в месяц, при этом 8 дней в месяц возникает головная боль, соответствующая критериям мигрени.
- Эпизодическая ГБН.
- Другие хронические ежедневные или почти ежедневные головные боли, в том числе хроническая головная боль напряжения и медикаментозно-индуцированная (абузусная) головная боль, обусловленная избыточным приемом обезболивающих препаратов. Абузусная головная боль развивается у пациентов, которые исходно имели первичные формы — мигрень и ГБН при злоупотреблении ими обезболивающими препаратами (более 15 доз в месяц). Наибольшую угрозу для возникновения абузусной головной боли представляют комбинированные анальгетики, содержащие кодеин и барбитураты.
Принципы диагностики головной боли
Анализ жалоб и анамнеза заболевания
Диагностика первичных форм головной боли является исключительно клинической и включает в себя сбор жалоб, анамнеза, общий и неврологический осмотр пациента, а также получение сведений о предшествующей терапии, ее эффективности и количестве принимаемых обезболивающих препаратов.
Первым этапом диагностики головной боли является исключение вторичных ее причин. Симптомы — «красные флажки» могут быть выявлены в ходе расспроса и осмотра пациента (табл. 2) [3].
Также необходимо помнить, что многие лекарственные средства могут провоцировать развитие головной боли [4].
Как правило, во время общего и неврологического осмотра пациентов с первичными головными болями и абузусной головной болью патологии не выявляется. При осмотре пациента во время приступа мигрени можно отметить признаки вегетативной дисфункции: ладонный гипергидроз, изменение окраски пальцев кистей (синдром Рейно), признаки повышенной нервно-мышечной возбудимости (симптом Хвостека). При пальпации у пациентов с мигренью и ГБН часто обнаруживается болезненность и напряжение перикраниальных мышц.
Роль дополнительных исследований
Дополнительные исследования, включая инструментальные, лабораторные (электроэнцефалография, рентгенография черепа, ультразвуковая допплерография, реоэнцефалография, методы нейровизуализации и др.) и консультации специалистов, в большинстве случаев не являются информативными и не имеют диагностической ценности при первичных формах головной боли и абузусной головной боли [5].
Таким образом, диагностический алгоритм при обращении пациента с основной жалобой на головную боль начинается с подробного сбора анамнеза, общего и неврологического осмотра (рис.). При наличии симптомов — «красных флажков» пациент должен быть обследован. Показаниями для нейровизуализации также могут быть атипичное течение первичных форм головных болей (мигрени, головной боли напряжения, кластерной головной боли), а также их резистентность к стандартной терапии. Если у пациента имеются симптомы — «красные флажки», но магнитно-резонансная томография и другая диагностика не выявила патологических изменений, то пациента следует вести как страдающего первичной формой головной боли, однако проводить динамическое наблюдение. При развитии громоподобной или внезапно начавшейся головной боли в первую очередь необходимо исключать внутримозговое или субарахноидальное кровоизлияние, поэтому методом выбора в данной ситуации является компьютерная томография [6, 7].
Лечение первичных форм головной боли
Фармакотерапия пациентов с первичными формами головной боли включает в себя два направления — купирование возникшей головной боли и профилактику и лечение хронических форм. Препараты, рекомендованные международными стандартами, представлены в табл. 5. Следует отметить, что консультация пациента с головной болью должна включать элементы когнитивно-поведенческой психотерапии. Пациенту необходимо сообщить об отсутствии у него серьезного заболевания, а также об оптимальных методах купирования приступов (ранний прием препаратов, когда боль еще слабая или умеренная), методах профилактики. Для контроля количества дней с головной болью рекомендуется ведение дневника головной боли [3].
В настоящее время для пациентов с головной болью, в том числе и с мигренью, стал доступен комбинированный анальгетик Экседрин. Экседрин представляет собой комбинацию ацетилсалициловой кислоты, парацетамола и кофеина. Дозы каждого из составляющих подбирались таким образом, чтобы достичь максимальной эффективности в сочетании с максимальной безопасностью. Экседрин рекомендован Европейской федерацией неврологических обществ (EFNS) как средство для лечения мигрени уровня А. Кроме мигрени Экседрин может быть использован для купирования других типов головной боли. Достоверное уменьшение мигренозной боли возникает уже через 30 мин после приема Экседрина. В отличие от простых анальгетиков и НПВС Экседрин уменьшает и сопутствующие симптомы мигренозной головной боли — тошноту, рвоту, свето- и звукобоязнь. Препарат характеризуется благоприятным профилем переносимости. Серьезные нежелательные явления не были зарегистрированы ни в одном из трех крупных контролируемых исследований [8, 9].
Литература
- Headache Classification Committee of the International Headache Society (IHS). Th International Classification of Headache Disorders, 3 rd edition (beta version) // Cephalalgia. 2013, v. 33, p. 629–808.
- Ayzenberg I., Katsarava Z., Sborowski A. et al. The prevalence of primary headache disorders in Russia: A countrywide survey // Cephalalgia. 2012, 32 (5), 373–381.
- Стайнер Т. Дж. и соавт. Европейские принципы ведения пациентов с наиболее распространенными формами головной боли в общей практике. Практическое руководство для врачей / Пер. с англ. Ю. Э. Азимовой, В. В. Осиповой; науч. ред. В. В. Осиповой, Т. Г. Вознесенской, Г. Р. Табеевой. М.: ООО «ОГГИ. Рекламная продукция», 2010. 56 с.
- Осипова В. В., Азимова Ю. Э., Табеева Г. Р. Международные принципы диагностики головных болей: проблемы диагностики головных болей в России / Вестник семейной медицины. 2010, № 2, с. 8–18.
- Goldstein L. H., Seed P. T., Clark L. V. et al. Predictors of outcome in patients consulting their general practitioners for headache: a prospective study // Psychol Health. 2011, 26 (6) 751–764.
- De Klippel N., Jansen J. P., Carlos J. S. Survey to evaluate diagnosis and management of headache in primary care: Headache Management Pattern programme // Curr Med Res Opin. 2008. 24 (12): 3413–3422.
- Massetto N., Gambini C., Bernardoni P. et al. Underdiagnosis of primary headaches: results of a survey on patients attending headache centres // Neurol Sci. 2009, 30 Suppl 1: S129–131.
- Diener H. C., Pfaffenrath V., Pageler V. et al. The fixed combination of acetylsalicylic acid, paracetamol and caffeine is more effective than single substances and dual combination for the treatment of headache: a multicentre, randomized, double-blind, single-dose, placebo-controlled parallel group study // Cephalalgia. 2005, 25, 776–787.
- Evers S., A´ frab J., Frese A. et al. EFNS guideline on the drug treatment of migraine — revised report of an EFNS task force // European Journal of Neurology. 2009, 16: 968–981.
Статья подготовлена при поддержке ООО «Новартис Консьюмер Хелс»
Ю. Э. Азимова1, кандидат медицинских наук
В. В. Осипова, доктор медицинских наук, профессор
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
1 Контактная информация: azimova.j@mail.ru
Боль: от патогенеза к выбору лекарственного препарата
Статьи
Алексей Данилов
Назад | Оглавление | Читать далее
Глава 2. Боль: от патогенеза к выбору лекарственного препарата
Боль является наиболее частой и сложной по субъективному восприятию жалобой пациентов. В 40% всех первичных обращений к врачу боль является ведущей жалобой. Большая распространенность болевых синдромов оборачивается значительными материальными, социальными и духовными потерями.
Как уже говорилось выше, комитет по классификации Международной ассоциации по изучению боли определяет боль как «неприятное сенсорное и эмоциональное переживание, связанное с существующим или возможным повреждением ткани или описываемое в терминах такого повреждения» [37]. В этом определении подчеркивается, что ощущение боли может возникать не только при повреждении ткани, но даже при отсутствии какого-либо повреждения, что указывает на важную роль психических факторов в формировании и поддержании боли.
Классификация боли
Боль — понятие клинически и патогенетически сложное и неоднородное. Она различается по интенсивности, локализации и по своим субъективным проявлениям. Боль может быть стреляющей, давящей, пульсирующей, режущей, а также постоянной или периодической. Все существующее многообразие характеристик боли во многом связано с самой причиной, вызвавшей ее, анатомической областью, в которой возникает ноцицептивный импульс, и очень важно для определения причины боли и последующего лечения [3].
Одним из наиболее существенных факторов в понимании этого феномена является разделение боли на острую и хроническую (рис. 8).
Рис. 8. Боль: острая и хроническая. Главным отличием хронической боли от острой является не временной фактор, а качественно иные нейрофизиологические, психофизиологические и клинические соотношения.
Острая боль всегда указывает на конкретную проблему или угрозу для человека. В этом ее биологический смысл и «польза». Хроническая боль является во всех случаях патологическим состоянием, приводящим к дезадаптации и снижению качества жизни пациента. А для общества хроническая боль оборачивается огромными экономическими потерями.
Острая боль — это сенсорная реакция с последующим включением эмоционально-мотивационных вегетативных и других факторов при нарушении целостности организма. Развитие острой боли связано, как правило, с вполне определенными болевыми раздражениями поверхностных или глубоких тканей и внутренних органов, нарушением функций гладкой мускулатуры. Острый болевой синдром развивается в 80% случаев, имеет защитное, предупредительное значение, так как свидетельствует о «повреждении» и вынуждает человека предпринять меры для выяснения причины боли и ее устранения. Длительность острой боли определяется временем восстановления поврежденных тканей и/или нарушенной функции гладких мышц и обычно не превышает 3 месяцев. Острая боль обычно хорошо купируется анальгетиками.
В 10–20% случаев острая боль переходит в хроническую, которая длится более 3–6 месяцев. Однако главным отличием хронической боли от острой является не временной фактор, а качественно иные нейрофизиологические, психофизиологические и клинические соотношения. Хроническая боль не носит защитного характера. Хроническая боль в последние годы стала рассматриваться не только как синдром, но и как отдельная нозология. Ее формирование и поддержание зависит в большей степени от комплекса психологических факторов, нежели от характера и интенсивности периферического ноцицептивного воздействия. Хроническая боль может сохраняться после завершения процессов заживления, т.е. существовать вне зависимости от повреждения (наличия ноцицептивного воздействия). Хроническая боль не купируется анальгетиками и часто приводит к психологической и социальной дезадаптации пациентов.
Одной из возможных причин, способствующих хронификации боли, является лечение, неадекватное причине и патогенезу болевого синдрома. Устранение причины острой боли и/или максимально эффективное ее лечение — залог профилактики трансформации острой боли в хроническую.
Важное значение для успешного лечения боли имеет определение ее патогенеза. Наиболее часто встречается ноцицептивная боль, возникающая при раздражении периферических болевых рецепторов — «ноцицепторов», локализованных практически во всех органах и системах (коронарный синдром, плеврит, панкреатит, язва желудка, почечная колика, суставной синдром, повреждения кожи, связок, мышц и т.д). Нейропатическая боль возникает вследствие повреждения различных отделов (периферической и центральной) соматосенсорной нервной системы [9].
Ноцицептивные болевые синдромы чаще всего являются острыми (ожог, порез, ушиб, ссадина, перелом, растяжение), но могут носить и хронический характер (остеоартроз). При этом виде боли фактор, вызвавший ее, как правило, очевиден, боль обычно четко локализована (обычно в зоне повреждения). Описывая ноцицептивную боль, пациенты чаще всего пользуются определениями «сжимающая», «ноющая», «пульсирующая», «режущая». В лечении ноцицептивной боли хороший терапевтический эффект можно получить при назначении простых анальгетиков и НПВП. При ликвидации причины (прекращении раздражения «ноцицепторов») ноцицептивная боль проходит [9].
Причинами нейропатической боли могут быть повреждения афферентной соматосенсорной системы на любом уровне, начиная от периферических чувствительных нервов и заканчивая корой больших полушарий, а также нарушения в нисходящих антиноцицептивных системах. При поражении периферической нервной системы боли называют периферическими, при поражении центральной нервной системы — центральными (рис. 9).
Нейропатическая боль, возникающая при повреждении различных участков нервной системы, характеризуется пациентами как жгучая, стреляющая, холодящая и сопровождается объективными симптомами раздражения нервов (гиперестезия, парестезия, гипералгезия) и/или нарушения их функции (гипестезия, анестезия). Характерным симптомом нейропатической боли является аллодиния — феномен, характеризующийся возникновением боли в ответ на действие безболевого стимула (поглаживание кисточкой, ватой, температурного фактора).
Рис. 9. Периферическая и центральная нейропатическая боль.
Нейропатическая боль характерна для хронических болевых синдромов разной этиологии. При этом их объединяют общие патофизиологические механизмы формирования и поддержания боли.
Нейропатическая боль плохо поддается лечению стандартными анальгетиками и НПВП и часто приводит к выраженной дезадаптации пациентов.
В практике невролога, травматолога, онколога встречаются болевые синдромы, в клинической картине которых наблюдаются симптомы как ноцицептивной, так и нейропатической боли — «смешанная боль» (рис. 10). Такая ситуация может возникать, например, при компрессии опухолью нервного ствола, раздражении межпозвонковой грыжей спинномозгового нерва (радикулопатии) или при компрессии нерва в костном или мышечном канале (туннельные синдромы). В лечении смешанных болевых синдромов необходимо воздействие на оба, ноцицептивный и нейропатический, компоненты боли.
Рис. 10. Представленность различных типов боли.
Ноцицептивная и антиноцицептивная системы
Сегодняшние представления о формировании боли основаны на представлениях о существовании двух систем: ноцицептивной (НС) и антиноцицептивной (АНС) (рис. 11).
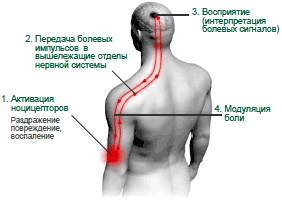
Ноцицептивная система (является восходящей) обеспечивает проведение боли от периферических (ноцицептивных) рецепторов до коры головного мозга. Антиноцицептивная система (является нисходящей) предназначена для контроля над болью [17, 18].
На первом этапе формирования боли происходит активация болевых (ноцицептивных) рецепторов. К активации болевых рецепторов может привести, например, воспалительный процесс. Это вызывает проведение болевых импульсов к задним рогам спинного мозга.
На сегментарном спинальном уровне происходит модуляция ноцицептивной афферентации, которая осуществляется влиянием нисходящих антиноцицептивных систем на различные опиатные, адренергические, глютаматные, пуриновые и другие рецепторы, расположенные на нейронах заднего рога. Этот болевой импульс затем передается в вышележащие отделы центральной нервной системы (таламус, кора головного мозга), где происходит обработка и интерпретация информации о характере и локализации боли.
Рис. 11. Современные представления о боли: ноцицептивная (НС) и антиноцицептивная системы (АНС).
Однако итоговое восприятие боли в значительной степени зависит от активности АНС. АНС головного мозга играют ключевую роль в формировании боли и изменении реакции на боль. Очевидна их широкая представленность в головном мозге и включение в различные нейротрансмиттерные механизмы (норадреналин, серотонин, опиоиды, дофамин). АНС работают не изолированно, а, взаимодействуя между собой и с другими системами, они регулируют не только болевую чувствительность, но и сопряженные с болью вегетативные, моторные, нейроэндокринные, эмоциональные и поведенческие проявления боли. Это обстоятельство позволяет рассматривать их как важнейшую систему, определяющую не только характеристики болевого ощущения, но и его многообразные психофизиологические и поведенческие корреляты [3]. В зависимости от активности АНС боль может усиливаться или уменьшаться.
Препараты для лечения боли
Препараты для лечения боли назначают с учетом предполагаемых механизмов боли. Понимание механизмов формирования болевого синдрома позволяет проводить индивидуальный подбор лечения. При ноцицептивной боли с наилучшей стороны зарекомендовали себя нестероидные противовоспалительные препараты (НПВП) и опиоидные анальгетики. При нейропатической боли обоснованным является применение антидепрессантов, антиконвульсантов, местных анестетиков, а также блокаторов калиевых каналов.
Нестероидные противовоспалительные препараты
Если в патогенезе болевого синдрома ведущую роль играют механизмы воспаления, то наиболее целесообразно в этом случае применение НПВП. Их использование позволяет подавить синтез альгогенов в поврежденных тканях, что предотвращает развитие периферической и центральной сенситизации [26]. Помимо болеутоляющего эффекта препараты из группы НПВП оказывают противовоспалительное и жаропонижающее действие.
Современная классификация НПВП предполагает разделение этих средств на несколько групп, отличающихся селективностью в отношении ферментов циклооксигеназы 1 и 2 типа, которые участвуют в ряде физиологических и патологических процессов (рис. 12).
Рис. 12. Селективные и неселективные НПВП.
Считается, что противоболевой эффект препаратов из группы НПВП связан в основном с их влиянием на ЦОГ2, а желудочно-кишечные осложнения обусловлены их влиянием на ЦОГ1. Однако исследования последних лет обнаруживают и другие механизмы анальгетического действия некоторых препаратов из группы НПВП. Так, было показано, что диклофенак (Вольтарен) может оказывать противоболевое действие не только через ЦОГ-зависимые, но и другие периферические, а также центральные механизмы [15].
Местные анестетики
Ограничения поступления ноцицептивной информации в ЦНС можно достичь при применении различных местных анестетиков, которые могут не только предотвратить сенситизацию ноцицептивных нейронов, но и способствовать нормализации микроциркуляции в зоне повреждения, уменьшению воспаления и улучшению обмена веществ. Наряду с этим местные анестетики расслабляют поперечно-полосатую мускулатуру, устраняют патологическое напряжение мышц, которое является дополнительным источником боли [26].
К местным анестетикам относят вещества, вызывающие временную потерю чувствительности тканей в результате блокады проведения импульсов в нервных волокнах. Наибольшее распространение среди них получили лидокаин, новокаин, артикаин и бупивакаин. Механизм действия местных анестетиков связан с блокированием Na+-каналов на мембране нервных волокон и торможением генерации потенциалов действия.
Антиконвульсанты
Длительно существующее раздражение ноцицепторов или периферических нервов приводит к развитию периферической и центральной сенситизации (гипервозбудимости).
Существующие сегодня антиконвульсанты, применяемые для лечения боли, имеют различные точки приложения. Дифенин, карбамазепин, окскарбазепин, ламотриджин, вальпроаты, топиромат действуют главным образом, подавляя активность потенциал-зависимых натриевых каналов, предотвращая спонтанную генерацию эктопических разрядов в поврежденном нерве. Эффективность этих препаратов доказана у пациентов с тригеминальной невралгией, диабетической невропатией, фантомно-болевым синдромом.
Габапентин и прегабалин тормозят вход ионов кальция в пресинаптическую терминаль ноцицепторов, тем самым уменьшая выброс глутамата, что приводит к уменьшению возбудимости ноцицептивных нейронов спинного мозга (уменьшает центральную сенситизацию). Эти препараты также модулируют активность NMDA-рецепторов и снижают активность Na+-каналов.
Антидепрессанты
Антидепрессанты и препараты из группы опиоидов назначают с целью усиления антиноцицептивных влияний. При лечении болевых синдромов в основном используют препараты, механизм действия которых связан с блокадой обратного захвата моноаминов (серотонина и норадреналина) в ЦНС. Обезболивающий эффект антидепрессантов может быть частично обусловлен и непрямым анальгетическим действием, так как улучшение настроения благоприятно сказывается на оценке боли и уменьшает болевое восприятие. Кроме того, антидепрессанты потенцируют действие наркотических анальгетиков, повышая их сродство к опиоидным рецепторам [26].
Мышечные релаксанты
Мышечные релаксанты применяют в случаях, когда вклад в формирование боли вносит мышечный спазм. Следует отметить, что мышечные релаксанты оказывают воздействие на уровне спинного мозга, а не на уровне мышц.
В нашей стране для лечения болезненных мышечных спазмов используются тизанидин, баклофен, мидокалм, а также препараты из группы бензодиазепинов (диазепам). В последнее время с целью расслабления мышц в лечении миофасциальных болевых синдромов применяются инъекции ботулинотоксина типа А [22]. У представленных препаратов — разные точки приложения. Баклофен является агонистом ГАМК-рецепторов, ингибирует активность вставочных нейронов на спинальном уровне.
Толперизон блокирует Na+-и Ca2+-каналы интернейронов спинного мозга и уменьшает выброс болевых медиаторов в нейронах спинного мозга. Тизанидин относится к мышечным релаксантам центрального действия. Основная точка приложения его действия находится в спинном мозге. Стимулируя пресинаптические a2-рецепторы, он подавляет высвобождение возбуждающих аминокислот, которые стимулируют рецепторы к N-метил-D-аспартату (NMDA-рецепторы). Вследствие этого на уровне промежуточных нейронов спинного мозга происходит подавление полисинаптической передачи возбуждения. Поскольку именно этот механизм отвечает за избыточный мышечный тонус, то при его подавлении мышечный тонус снижается. В дополнение к миорелаксирующим свойствам, тизанидин оказывает также центральный умеренно выраженный анальгезирующий эффект.
Исходно тизанидин был разработан для лечения мышечного спазма при различных неврологических заболеваниях (при травматических повреждениях головного и спинного мозга, рассеянном склерозе, инсульте). Однако в скором времени после начала его применения были выявлены анальгетические свойства тизанидина. В настоящее время применение тизанидина в монотерапии и в комплексном лечении болевых синдромов получило широкое распространение [11].
Селективные активаторы нейрональных калиевых каналов (SNEPCO)
Принципиально новым классом препаратов для лечения болевых синдромов являются селективные активаторы нейрональных калиевых каналов — SNEPCO (Selective Neuronal Potassium Channel Opener), оказывающие воздействие на процессы сенситизации нейронов заднего рога за счет стабилизации мембранного потенциала покоя.
Первый представитель этого класса лекарственных средств — флупиртин (Катадолон), обладающий широким спектром ценных фармакологических свойств, выгодно отличающих его от других обезболивающих препаратов.
В последующих главах подробно изложены сведения о фармакологических свойствах и механизме действия Катадолона, представлены результаты исследований его эффективности и безопасности, рассказывается об опыте применения препарата в разных странах мира, даны рекомендации по применению Катадолона при различных болевых синдромах.
Назад | Оглавление | Читать далее
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
1. Яхно НН, Кукушкин МЛ, редакторы. Боль (практическое руководство для врачей). Москва: Издательство РАМН; 2012. 512 c. [Yakhno NN, Kukushkin ML, editors. Bol’ (prakticheskoe rukovodstvo dlya vrachei) [Pain (a practical guide for doctors)]. Moscow: Publishing of Russian Academy of Medical Sciences; 2012. 512 p.].
2. Яхно НН, Кукушкин МЛ. Хроническая боль: медико-биологические и социально-экономические аспекты. Вестник РАМН. 2012;(9):54-8 [Yakhno NN, Kukushkin ML. Chronic pain: medical-biological and socio-economic aspects. Vestnik RAMN. 2012;(9):54-8 (In Russ.)].
3. Яхно НН, Баринов АН, Подчуфарова ЕВ. Невропатическая и скелетно-мышечная боль. Современные подходы к диагностике и лечению. Клиническая медицина. 2008;(11):9-15 [Yakhno NN, Barinov AN, Podchufarova EV. Neuropathic and musculoskeletal pain. Current approaches to diagnosis and treatment. Klinicheskaya Meditsina. 2008;(11):9-15 (In Russ.)].
4. Насонов ЕЛ, Насонова ВА. Фармакотерапия боли: взгляд ревматолога. Consilium medicum. 2000;2(12):7-14 [Nasonov EL, Nasonova VA. Pharmacotherapy of pain: a view of the rheumatologist. Consilium medicum. 2000; 2 (12): 7-14 (In Russ.)].
5. Кукушкин МЛ, Хитров НК. Общая патология боли. Москва: Медицина; 2004. 144 с. [Kukushkin ML, Khitrov NK. Obshchaya patologiya boli [General pathology of pain]. Moscow: Medicine; 2004. 144 p.].
6. Голубев ВЛ. Боль – междисциплинарная проблема. Русский медицинский журнал. 2008;16 (Спец. выпуск):3-7 [Golubev VL. The pain – an interdisciplinary problem. Russkii Meditsinskii Zhurnal. 2008;16 (Special Issue):3-7 (In Russ.)].
7. Vos T, Flaxman AD, Naghavi M, et al. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet. 2012 Dec 15;380(9859):2163-96. doi: 10.1016/S0140-6736(12)61729-2
8. Harker J, Reid K, Bekkering G, et al. Epidemiology of chronic pain in Denmark and Sweden. Pain Res Treat. 2012;2012:371248. doi: 10.1155/2012/371248
9. Woolf A, Pfleger B. Burden of major musculoskeletal conditions. Bull WHO. 2003;81:646-56.
10. Breivik H, Collett B, Ventafridda V, et al. Survey of chronic pain in Europe: prevalence, impact on daily life, and treatment. Eur J Pain. 2006;10(4):287-333. doi: 10.1016/j.ejpain.2005.06.009
11. Эрдес ШФ, Дубинина ТВ, Галушко ЕА. Боли в нижней части спины в общеклинической практике. Терапевтический архив. 2008;80(5):59-61 [Erdes ShF, Dubinina TV, Galushko EA. Pain in the lower back in the general clinical practice. Terapevticheskii Arkhiv. 2008;80(5):59-61 (In Russ.)].
12. Friedly J, Standaert C, Chan L. Epidemiology of spine care: the back pain dilemma. Phys Med Rehabil Clin N Am. 2010;21(4):659-77. doi: 10.1016/j.pmr.2010.08.002
13. Juniper M, Le T, Mladsi D. The epidemiology, economic burden, and pharmacological treatment of chronic low back pain in France, Germany, Italy, Spain and the UK: a literature-based review. Expert Opin Pharmacother. 2009;10(16):2581-92. doi: 10.1517/14656560903304063
14. Litwic A, Edwards M, Dennison E, Cooper C. Epidemiology and burden of osteoarthritis. Br Med Bull. 2013;105:185-99. doi: 10.1093/bmb/lds038
15. Zhang Y, Jordan J. Epidemiology of osteoarthritis. Clin Geriatr Med. 2010;26(3):355-69. doi: 10.1016/j.cger.2010.03.001
16. Murphy L, Helmick C. The impact of osteoarthritis in the United States: a population-health perspective. Am J Nurs. 2012;112(3 Suppl 1):13-9. doi: 10.1097/01.NAJ.0000412646.80054.21
17. Millar NL, Murrell GA, McInnes IB. Alarmins in tendinopathy: unravelling new mechanisms in a common disease. Rheumatology (Oxford). 2013 May;52(5):769-79. doi: 10.1093/rheumatology/kes409. Epub 2013 Jan 28.
18. Scott A, Ashe MC. Common tendinopathies in the upper and lower extremities. Curr Sports Med Rep. 2006 Sep;5(5):233-41. doi: 10.1097/01.CSMR.0000306421.85919.9c
19. Van Tulder M, Malmivaara A, Koes B. Repetitive strain injury. Lancet. 2007;369(9575):1815-22. doi: 10.1016/S0140-6736(07)60820-4
20. Кукушкин МЛ, Табеева ГР, Подчуфарова ЕВ. Болевой синдром: патофизиология, клиника, лечение. Москва: ИМА-ПРЕСС; 2011. 72 с. [Kukushkin ML, Tabeeva GR, Podchufarova EV. Bolevoi sindrom: patofiziologiya, klinika, lechenie [Pain syndrome: pathophysiology, clinical features, treatment]. Moscow: IMA-PRESS; 2011. 72 p.].
21. Staud R. Evidence for shared pain mechanisms in osteoarthritis, low back pain, and fibromyalgia. Curr Rheumatol Rep. 2011 Dec;13(6):513-20. doi: 10.1007/s11926-011-0206-6
22. Edmonds S. Therapeutic targets for osteoarthritis. Maturitas. 2009 Jul 20;63(3):191-4. doi: 10.1016/j.maturitas.2009.03.015. Epub 2009 May 6.
23. Felson DT. The sources of pain in knee osteoarthritis. Curr Opin Rheumatol. 2005 Sep;17(5):624-8. doi: 10.1097/01.bor.0000172800.49120.97
24. Blondell RD, Azadfard M, Wisniewski AM. Pharmacologic therapy for acute pain. Am Fam Physician. 2013 Jun 1;87(11):766-72.
25. Kroenke K, Krebs EE, Bair MJ. Pharmacotherapy of chronic pain: a synthesis of recommendations from systematic reviews. Gen Hosp Psychiatry. 2009 May-Jun;31(3):206-19. doi: 10.1016/j.genhosppsych. 2008.12.006. Epub 2009 Mar 4.
26. Насонова ВА, Фоломеева ОМ, Эрдес ШФ. Ревматические заболевания в Российской Федерации в начале XXI века глазами статистики. Терапевтический архив. 2009;(6):5-10 [Nasonova VA, Folomeeva OM, Erdes ShF. Rheumatic diseases in the Russian Federation at the beginning of the XXI century through the eyes of statistics. Terapevticheskii Arkhiv. 2009;(6):5-10 (In Russ.)].
27. Балабанова РМ, Эрдес ШФ. Распространенность ревматических заболеваний в России в 2012-2013 гг. Научно-практическая ревматология. 2015;52(2):120-4 [Balabanova RM, Erdes ShF. The incidence and prevalence of rheumatic diseases in Russia in 2012–2013. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2015;53(2):120-4 (In Russ.)]. doi: 10.14412/1995-4484-2015-120-124
28. Каратеев АЕ. Болезни костно-мышечной системы в практике 2102 врачей разных специальностей: структура патологии и мнение специалистов об эффективности НПВП (предварительные данные эпидемиологического исследования КОРОНА-2). Consilium medicum, 2013;15(9):95-100 [Karateev AE. Diseases of the musculoskeletal system in practice in 2102 doctors of different specialties: pathology structure and experts’ opinion on the effectiveness of non-steroidal anti-inflammatory drugs (preliminary data of CROWN-2 epidemiological studies). Consilium medicum. 2013;15(9):95-100. (In Russ.)].
29. McAlindon TE, Bannuru RR, Sullivan MC, et al. OARSI guidelines for the non-surgical management of knee osteoarthritis. Osteoarthritis Cartilage. 2014 Mar;22(3):363-88. doi: 10.1016/j.joca.2014.01.003. Epub 2014 Jan 24.
30. Bruyere O, Cooper C, Pelletier J-P, et al. An algorithm recommendation for the management of knee Osteoarthritis in Europe and internationally: A report from a task force of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO). Semin Arthritis Rheum. 2014;44:253-63. doi: 10.1016/j.semarthrit.2014.05.014
31. Koes BW, van Tulder M, Lin CW, et al. An updated overview of clinical guidelines for the management of non-specific low back pain in primary care. Eur Spine J. 2010 Dec;19(12):2075-94. doi: 10.1007/s00586-010-1502-y
32. Van Hecke O, Torrance N, Smith B. Chronic pain epidemiology and its clinical relevance. Br J Anaesth. 2013;111(1):13-8. doi: 10.1093/bja/aet123
33. Smith B, Elliott A, Hannaford P, Chambers W. Factors related to the onset and persistence of chronic back pain in the community: results from a general population follow-up study. Spine. 2004;29(9):1032-40. doi: 10.1097/00007632-200405010-00016
34. Bergman S, Herrstrom P, Jacobsson L, Petersson I. Chronic widespread pain: a three year follow-up of pain distribution and risk factors. J Rheumatol. 2002;29:818-25.
35. Andersen JC. Is immediate imaging important in managing low back pain? J Athl Train. 2011 Jan-Feb;46(1):99-102. doi: 10.4085/1062-6050-46.1.99
36. Chou R, Fu R, Carrino JA, Deyo RA. Imaging strategies for lowback pain: systematic review and meta-analysis. Lancet. 2009 Feb 7;373(9662):463-72. doi: 10.1016/S0140-6736(09)60172-0
37. Jarvik J, Gold L, Comstock B, et al. Association of early imaging for back pain with clinical outcomes in older adults. JAMA. 2015;313(11):1143-53. doi: 10.1001/jama.2015.1871
38. Igarashi A, Kikuchi S, Konno S, Olmarker K. Inflammatory cytokines released from the facet joint tissue in degenerative lumbar spinal disorders. Spine (Phila Pa 1976). 2004 Oct 1;29(19):2091-5. doi: 10.1097/01.brs.0000141265.55411.30
39. Genevay S, Finckh A, Payer M, et al. Elevated levels of tumor necrosis factor-alpha in periradicular fat tissue in patients with radiculopathy from herniated disc. Spine (Phila Pa 1976). 2008 Sep 1;33(19):2041-6. doi: 10.1097/BRS.0b013e318183bb86
40. Cuellar JM, Golish SR, Reuter MW, et al. Cytokine evaluation in individuals with low back pain using discographic lavage. Spine J. 2010 Mar;10(3):212-8. doi: 10.1016/j.spinee.2009.12.007
41. Schaible H. Mechanisms of chronic pain in osteoarthritis. Curr Rheumatol Rep. 2012;14(6):549-56. doi: 10.1007/s11926-012-0279-x
42. Walsh D, Bonnet C, Turner E, et al. Angiogenesis in the synovium and at the osteochondral junction in osteoarthritis. Osteoarthritis Cartilage. 2007 Jul;15(7):743-51. Epub 2007 Mar 21. doi: 10.1016/j.joca.2007.01.020
43. Pelletier JP, Martel-Pelletier J, Abramson SB. Osteoarthritis, an inflammatory disease: potential implication for the selection of new therapeutic targets. Arthritis Rheum. 2001 Jun;44(6):1237-47. doi: 10.1002/1529-0131(200106)44:6<1237::AID-ART214>3.0.CO;2-F
44. Alvarez-Soria MA, Largo R, Santillana J, et al. Long term NSAID treatment inhibits COX-2 synthesis in the knee synovial membrane of patients with osteoarthritis: differential proinflammatory cytokine profile between celecoxib and aceclofenac. Ann Rheum Dis. 2006 Aug;65(8):998-1005. Epub 2006 Feb 13. doi: 10.1136/ard.2005.046920
45. McCarberg BH, Ruoff GE, Tenzer-Iglesias P, Weil AJ. Diagnosis and treatment of low-back pain because of paraspinous muscle spasm: a physician roundtable. Pain Med. 2011 Nov;12 Suppl 4:S119-27. doi: 10.1111/j.1526-4637.2011.01253.x
46. Lund JP, Donga R, Widmer CG, Stohler CS. The pain-adaptation model: a discussion of the relationship between chronic musculoskeletal pain and motor activity. Can J Physiol Pharmacol. 1991;69:683-94. doi: 10.1139/y91-102
47. Roland M. A critical review of the evidence for pain-spasm-pain cycle in spinal disorders. Clin Biomech. 1986;1:102-9. doi: 10.1016/0268-0033(86)90085-9
48. Iglesias-Gonzalez JJ, Munoz-Garcia MT, Rodrigues-de-Souza DP, et al. Myofascial trigger points, pain, disability, and sleep quality in patients with chronic nonspecific low back pain. Pain Med. 2013 Dec;14(12):1964-70. doi: 10.1111/pme.12224. Epub 2013 Aug 15.
49. Ramsook RR, Malanga GA. Myofascial low back pain. Curr Pain Headache Rep. 2012 Oct;16(5):423-32. doi: 10.1007/s11916-012-0290-y
50. Fisher NM, Pendergast DR. Reduced muscle function in patients with osteoarthritis. Scand J Rehabil Med. 1997 Dec;29(4):213-21.
51. Arokoski MH, Arokoski JP, Haara M, et al. Hip muscle strength and muscle cross sectional area in men with and without hip osteoarthritis. J Rheumatol. 2002 Oct;29(10):2185-95.
52. Blume C, Wang SS. Comparison of changes in supraspinatus muscle thickness in persons with subacromial impingement syndrome and asymptomatic adults. Physiother Theory Pract. 2014 Nov;30(8):544-51. doi: 10.3109/09593985.2014.902522. Epub 2014 Mar 28.
53. Silldorff MD, Choo AD, Choi AJ, et al. Effect of supraspinatus tendon injury on supraspinatus and infraspinatus muscle passive tension and associated biochemistry. J Bone Joint Surg Am. 2014 Oct 15;96(20):e175. doi: 10.2106/JBJS.M.01315
54. Thomopoulos S, Parks WC, Rifkin DB, Derwin KA. Mechanisms of tendon injury and repair. J Orthop Res. 2015 Jan 29. doi: 10.1002/jor.22806 [Epub ahead of print].
55. Millar NL, Hueber AJ, Reilly JH, et al. Inflammation is present in early human tendinopathy. Am J Sports Med. 2010;38(10):2085-91. doi: 10.1177/0363546510372613. Epub 2010 Jul 1.
56. McGonagle D, Benjamin M. Entheses, entehesitis and enthesopathy. Report of rheumatic diseases, series 6, autumn 2009, №4. Available from: www.arc.org.uk/arthinfo/rdr.asp
57. Gotoh M, Hamada K, Yamakawa H, et al. Interleukin-1-induced glenohumeral synovitis and shoulder pain in rotator cuff diseases. J Orthop Res. 2002 Nov;20(6):1365-71. doi: 10.1016/S0736-0266(02)00063-3
58. Voloshin I, Gelinas J, Maloney MD, et al. Proinflammatory cytokines and metalloproteases are expressed in the subacromial bursa in patients with rotator cuff disease. Arthroscopy. 2005 Sep;21(9):1076.e1-1076.e9. doi: 10.1016/j.arthro.2005.05.017
59. Benjamin M, McGonagle D. Histopathologic changes at «synovio-entheseal complexes» suggesting a novel mechanism for synovitis in osteoarthritis and spondylarthritis. Arthritis Rheum. 2007;56 (11):3601-9. doi: 10.1002/art.23078
60. Haviv B, Bronak S, Thein R. The complexity of pain around the knee in patients with osteoarthritis. Isr Med Assoc J. 2013 Apr;15(4):178-81.
61. Felson DT. Osteoarthritis as a disease of mechanics. Osteoarthritis Cartilage. 2013 Jan;21(1):10-5. doi: 10.1016/j.joca.2012.09.012. Epub 2012 Oct 4.
62. Tsao H, Tucker KJ, Coppieters MW, Hodges PW. Experimentally induced low back pain from hypertonic saline injections into lumbar interspinous ligament and erector spinae muscle. Pain. 2010 Jul;150(1):167-72. doi: 10.1016/j.pain.2010.04.023. Epub 2010 May 26.
63. Panjabi MM. A hypothesis of chronic back pain: ligament subfailure injuries lead to muscle control dysfunction. Eur Spine J. 2006 May;15(5):668-76. doi: 10.1007/s00586-005-0925-3. Epub 2005 Jul 27.
64. Longo UG, Berton A, Khan WS, et al. Histopathology of rotator cuff tears. Sports Med Arthrosc. 2011 Sep;19(3):227-36. doi: 10.1097/JSA.0b013e318213bccb
65. Ko JY, Wang FS. Rotator cuff lesions with shoulder stiffness: updated pathomechanisms and management. Chang Gung Med J. 2011 Jul-Aug;34(4):331-40.
66. Raastad J, Reiman M, Coeytaux R, et al. The association between lumbar spine radiographic features and low back pain: A systematic review and meta-analysis. Semin Arthritis Rheum. 2015 Apr;44(5):571-85. doi: 10.1016/j.semarthrit.2014.10.006. Epub 2014 Dec 8.
67. De Schepper EI, Damen J, van Meurs JB, et al. The association between lumbar disc degeneration and low back pain: the influence of age, gender, and individual radiographic features. Spine (Phila Pa 1976). 2010 Mar 1;35(5):531-6. doi: 10.1097/BRS.0b013e3181aa5b33
68. Scheele J, de Schepper EI, van Meurs JB, et al. Association between spinal morning stiffness and lumbar disc degeneration: the Rotterdam Study. Osteoarthritis Cartilage. 2012 Sep;20(9):982-7. doi: 10.1016/j.joca.2012.05.011. Epub 2012 Jun 12.
69. Beresford ZM, Kendall RW, Willick SE. Lumbar facet syndromes. Curr Sports Med Rep. 2010 Jan-Feb;9(1):50-6. doi: 10.1249/JSR.0b013e3181caba05
70. Cohen SP, Raja SN. Pathogenesis, diagnosis, and treatment of lumbar zygapophysial (facet) joint pain. Anesthesiology. 2007 Mar;106(3):591-614. doi: 10.1097/00000542-200703000-00024
71. Туровская ЕФ, Алексеева ЛИ, Филатова ЕГ. Современные представления о патогенетических механизмах боли при остеоартрозе. Научно-практическая ревматология. 2014;52(4):438-44 [Turovskaya EF, Alekseeva LI, Filatova EG. Current ideas about the pathogenetic mechanisms of pain in osteoarthrosis. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2014;52(4):438-44 (In Russ.)]. doi: 10.14412/1995-4484-2014-438-444
72. Mease P, Hanna S, Frakes E, Altman R. Pain mechanisms in osteoarthritis: understanding the role of central pain and current approaches to its treatment. J Rheumatol. 2011;38(8):1546-51. doi: 10.3899/jrheum.100759
73. Hochman J, French M, Bermingham S, Hawker G. The nerve of osteoarthritis pain. Arthritis Care Res (Hoboken). 2010;62(7):1019-23. doi: 10.1002/acr.20142
74. Fishbain DA, Cole B, Lewis JE, Gao J. What is the evidence that neuropathic pain is present in chronic low back pain and soft tissue syndromes? An evidence-based structured review. Pain Med. 2014 Jan;15(1):4-15. doi: 10.1111/pme.12229. Epub 2013 Oct 4.
75. Coombes BK, Bisset L, Vicenzino B. Thermal hyperalgesia distinguishes those with severe pain and disability in unilateral lateral epicondylalgia. Clin J Pain. 2012;28:595-601. doi: 10.1097/AJP.0b013e31823dd333
76. Данилов АБ, Давыдов ОС. Нейропатическая боль. Москва: Боргес; 2007. С. 11, 37-45 [Danilov AB, Davydov OS. Neiropaticheskaya bol’ [Neuropathic pain]. Moscow: Borges; 2007. P. 11, 37-45].
77. Englbrecht M, Tarner I, van der Heijde D, et al. Measuring pain and efficacy of pain treatment in inflammatory arthritis: A systematic literature review. J Rheumatol Suppl. 2012;90:3-10. doi: 10.3899/jrheum.120335
78. Whittle S, Colebatch A, Buchbinder R, et al. Multinational evidence-based recommendations for pain management by pharmacotherapy in inflammatory arthritis: Integrating systematic literature research and expert opinion of a broad panel of rheumatologists in the 3e Initiative. Rheumatology. 2012;51(8):1416-25. doi: 10.1093/rheumatology/kes032
79. Ostelo R, de Vet H. Clinically important outcomes in low back pain. Best Pract Res Clin Rheumatol. 2005;19(4):593-607. doi: 10.1016/j.berh.2005.03.003
80. Stauffer M, Taylor S, Watson D, et al. Definition of nonresponse to analgesic treatment of arthritic pain: An analytical literature review of the smallest detectable difference, the minimal detectable change, and the minimal clinically important difference on the pain visual analog scale. Int J Inflam. 2011;2011:231926. doi: 10.4061/2011/231926
81. Angst F, Aeschlimann A, Stucki G. Smallest detectable and minimal clinically important differences of rehabilitation intervention with their implications for required sample sizes using WOMAC and SF-36 quality of life measurement instruments in patients with osteoarthritis of the lower extremities. Arthritis Rheum. 2001;45(4):384-91. doi: 10.1002/1529-0131(200108)45:4<384::AID-ART352>3.0.CO;2-0
82. Cepeda M, Africano J, Polo R, et al. What decline in pain intensity is meaningful to patients with acute pain? Pain. 2003;105(1-2):151-7. doi: 10.1016/S0304-3959(03)00176-3
83. Каратеев АЕ. Факторы, влияющие на эффективность обезболивающей терапии. Эффективная фармакотерапия. Неврология и Психиатрия. 2013;47(5):46-53 [Karateev AE. Factors affecting the effectiveness of pain therapy. Effektivnaya farmakoterapiya. Nevrologiya i Psikhiatriya. 2013;47(5):46-53 (In Russ.)].
84. Farrar J, Young J, La Moreaux L, et al. Clinical importance of changes in chronic pain intensity measured on an 11-point numerical pain rating scale. Pain. 2001;94(2):149-58. doi: 10.1016/S0304-3959(01)00349-9
85. Salaffi F, Stancati A, Silvestri C, et al. Minimal clinically important changes in chronic musculoskeletal pain intensity measured on a numerical rating scale. Eur J Pain. 2004;8(4):283-91. doi: 10.1016/j.ejpain.2003.09.004
86. Kovacs F, Abraira V, Royuela A, et al. Minimum detectable and minimal clinically important changes for pain in patients with nonspecific neck pain. BMC Musculoskelet Disord. 2008;9:43. doi: 10.1186/1471-2474-9-43
87. Каратеев АЕ, Насонов ЕЛ, Яхно НН и др. Клинические рекомендации «Рациональное применение нестероидных противовоспалительных препаратов (НПВП) в клинической практике». Современная ревматология. 2015;9(1):4-24 [Karateev AE, Nasonov EL, Yakhno NN, et al. Clinical guidelines «Rational use of nonsteroidal anti-inflammatory drugs (NSAIDs) in clinical practice». Sovremennaya Revmatologiya = Modern Rheumatology Journal. 2015;9(1):4-23. (In Russ.)]. doi: 10.14412/1996-7012-2015-1-4-23
88. Brune K, Patrignani P. New insights into the use of currently available non-steroidal anti-inflammatory drugs. J Pain Res. 2015 Feb 20;8:105-18. doi: 10.2147/JPR.S75160. eCollection 2015.
89. Daniels S, Bandy D, Christensen S, et al. Evaluation of the dose range of etoricoxib in an acute pain setting using the postoperative dental pain model. Clin J Pain. 2011;27(1):1-8. doi: 10.1097/AJP.0b013e3181ed0639
90. Brattwall M, Turan I, Jakobsson J. Pain management after elective hallux valgus surgery: a prospective randomized double-blind study comparing etoricoxib and tramadol. Anesth Analg. 2010;111(2):544-9. doi: 10.1213/ANE.0b013e3181e3d87c
91. O’Donnell J, Ekman E, Spalding W, et al. The effectiveness of a weak opioid medication versus a cyclo-oxygenase-2 (COX-2) selective non-steroidal anti-inflammatory drug in treating flareup of chronic low-back pain: results from two randomized, double-blind, 6-week studies. J Int Med Res. 2009;37(6):1789-802. doi: 10.1177/147323000903700615
92. DeLemos B, Xiang J, Benson C, et al. Tramadol hydrochloride extended-release once-daily in the treatment of osteoarthritis of the knee and/or hip: a double-blind, randomized, dose-ranging trial. Am J Ther. 2011;18(3):216-26. doi: 10.1097/MJT.0b013e3181cec307
93. Innes G, Croskerry P, Worthington J, et al. Ketorolac versus acetaminophen-codeine in the emergency department treatment of acute low back pain. J Emerg Med. 1998 Jul-A Aug;16(4):549-56. doi: 10.1016/S0736-4679(98)00044-4
94. Beaulieu A, Peloso P, Haraoui B, et al. Once-daily, controlledrelease tramadol and sustained-release diclofenac relieve chronic pain due to osteoarthritis: a randomized controlled trial. Pain Res Manag. 2008;13(2):103-10. doi: 10.1155/2008/903784
95. Bjordal J, Klovning A, Ljunggren A, Slordal L. Short-term efficacy of pharmacotherapeutic interventions in osteoarthritic knee pain: A meta-analysis of randomised placebo-controlled trials. Eur J Pain. 2007 Feb;11(2):125-38. Epub 2006 May 8. doi: 10.1016/j.ejpain.2006.02.013
96. Roelofs PD, Deyo RA, Koes BW, et al. Non-steroidal anti-inflammatory drugs for low back pain. Cochrane Database Syst Rev. 2008 Jan 23;(1):CD000396. doi: 10.1002/14651858.CD000396.pub3
97. Boudreault J, Desmeules F, Roy J, et al. The efficacy of oral nonsteroidal anti-inflammatory drugs for rotator cuff tendinopathy: a systematic review and meta-analysis. J Rehabil Med. 2014 Apr;46(4):294-306. doi: 10.2340/16501977-1800
98. Moore R, Derry S, McQuay H. Discontinuation rates in clinical trials in musculoskeletal pain: meta-analysis from etoricoxib clinical trial reports. Arthritis Res Ther. 2008;10(3):R53. doi: 10.1186/ar2422
99. Furst D, Kolba K, Fleischmann R, et al. Dose response and safety study of meloxicam up to 22.5 mg daily in rheumatoid arthritis: a 12 week multicenter, double blind, dose response study versus placebo and diclofenac. J Rheumatol. 2002;29(3):436-46.
100. Derry S, Moore RA. Single dose oral celecoxib for acute postoperative pain in adults. Cochrane Database Syst Rev. 2013 Oct 22;10:CD004233. doi: 10.1002/14651858. CD004233.pub4.
101. Yakhno N, Guekht A, Skoromets A, et al. Analgesic efficacy and safety of lornoxicam quick-release formulation compared with diclofenac potassium. Clin Drug Invest. 2006;26(5):267-77. doi: 10.2165/00044011-200626050-00004
102. Dougados M, Le Henanff A, Logeart I, Ravaud P. Short-term efficacy of rofecoxib and diclofenac in acute shoulder pain: a placebo-controlled randomized trial. PLoS Clin Trials. 2007 Mar 9;2(3):e9. doi: 10.1371/journal.pctr.0020009
103. Chandanwale AS, Sundar S, Latchoumibady K, et al. Efficacy and safety profile of combination of tramadol-diclofenac versus tramadol-paracetamol in patients with acute musculoskeletal conditions, postoperative pain, and acute flare of osteoarthritis and rheumatoid arthritis: a Phase III, 5-day open-label study. J Pain Res. 2014 Aug 12;7:455-63. doi: 10.2147/JPR.S67817. eCollection 2014.
104. Tramer MR, Williams JE, Carroll D, et al. Comparing analgesic efficacy of non-steroidal anti-inflammatory drugs given by different routes in acute and chronic pain: a qualitative systematic review. Acta Anaesthesiol Scand. 1998 Jan;42(1):71-9. doi: 10.1111/j.1399-6576.1998.tb05083.x
105. Altman R, Barthel H. Topical therapies for osteoarthritis. Drugs. 2011;71(10):1259-79. doi: 10.2165/11592550-000000000-00000
106. Derry S, Moore R, Rabbie R. Topical NSAIDs for chronic muscoloskeletal pain in adults. Cochrane Database Sys Rev. 2012 Sep 12;9:CD 007400.
107. Baraf H, Gloth F, Barthel H, et al. Safety and efficacy of topical diclofenac sodium gel for knee osteoarthritis in elderly and younger patients: pooled data from three randomized, doubleblind, parallel-group, placebo-controlled, multicentre trials. Drugs Aging. 2011;28(1):27-40. doi: 10.2165/11584880-000000000-00000
108. Goldstein JL, Cryer B. Gastrointestinal injury associated with NSAID use: a case study and review of risk factors and preventative strategies. Drug Healthc Patient Saf. 2015 Jan 22;7:31-41. doi: 10.2147/DHPS.S71976. eCollection 2015.
109. Harirforoosh S, Asghar W, Jamali F. Adverse effects of nonsteroidal antiinflammatory drugs: an update of gastrointestinal, cardiovascular and renal complications. J Pharm Pharm Sci. 2013;16(5):821-47. doi: 10.18433/J3VW2F
110. Moore A, Makinson G, Li C. Patient-level pooled analysis of adjudicated gastrointestinal outcomes in celecoxib clinical trials: meta-analysis of 51,000 patients enrolled in 52 randomized trials. Arthritis Res Ther. 2013 Jan 8;15(1):R6. doi: 10.1186/ar4134
111. Day R, Graham G, Whelton A. The position of paracetamol in the world of analgesics. Am J Therap. 2000;7:51-5. doi: 10.1097/00045391-200007020-00002
112. Prescott L. Paracetamol: past, present and future. Am J Ther. 2000;7:135-43. doi: 10.1097/00045391-200007020-00011 113. Towheed T, Maxwell L, Judd M, et al. Acetaminophen for osteoarthritis. Cochrane Database Syst Rev. 2006;25(1):CD004257. doi: 10.1002/14651858.cd004257.pub2
113. Machado G, Maher C, Ferreira P, et al. Efficacy and safety of paracetamol for spinal pain and osteoarthritis: systematic review and meta-analysis of randomised placebo controlled trials. Brit Med J. 2015 Mar 31;350:h1225. doi: 10.1136/bmj.h1225
114. Garcia Rodriguez L, Hernandez-Diaz S. Relative risk of upper gastrointestinal complications among users of acetaminophen and nonsteroidal anti-inflammatory drugs. Epidemiology. 2001;12(5):570-6. doi: 10.1097/00001648-200109000-00018
115. Chan A, Manson J, Albert C, et al. Nonsteroidal antiinflammatory drugs, acetaminophen, and the risk of cardiovascular events. Circulation. 2006;113(12):1578-87. doi: 10.1161/CIRCULATIONAHA.105.595793
116. Dedier J, Stampfer M, Hankinson S, et al. Nonnarcotic analgesic use and the risk of hypertension in US women. Hypertension. 2002;40(5):604-8. doi: 10.1161/01.HYP.0000035856.77718.DA
117. Forman J, Rimm E, Curhan G. Frequency of analgesic use and risk of hypertension among men. Arch Intern Med. 2007;167(4):394-9. doi: 10.1001/archinte.167.4.394
118. Ong C, Seymour R, Lirk P, Merry A. Combining paracetamol (acetaminophen) with nonsteroidal antiinflammatory drugs: a qualitative systematic review of analgesic efficacy for acute postoperative pain. Anesth Analg. 2010,110(4):1170-9. doi: 10.1213/ane.0b013e3181cf9281
119. McQuay H, Edwards J. Meta-analysis of single dose oral tramadol plus acetaminophen in acute postoperative pain. Eur J Anaesthesiol Suppl. 2003;28:19-22.
120. Bronstein A, Spyker D, Cantilena L, et al. 2006 Annual Report of the American Association of Poison Control Centers National Poison Data System (NPDS). Clin Toxicol (Phila). 2007;45:815-917. doi: 10.1080/15563650701754763
121. Chaparro LE, Furlan AD, Deshpande A, et al. Opioids compared with placebo or other treatments for chronic low back pain: an update of the Cochrane Review. Spine (Phila Pa 1976). 2014 Apr 1;39(7):556-63. doi: 10.1097/BRS.0000000000000249
122. Cepeda M, Camargo F, Zea C, Valencia L. Tramadol for osteoarthritis: a systematic review and metaanalysis. J Rheumatol. 2007,34(3):543-55.
123. Da Costa BR, Nü esch E, Kasteler R, et al. Oral or transdermal opioids for osteoarthritis of the knee or hip. Cochrane Database Syst Rev. 2014 Sep 17;9:CD003115. doi: 10.1002/14651858.cd003115.pub4
124. Metscher B, Kü bler U, Jahnel-Kracht H. Dexketoprofentrometamol and tramadol in acute lumbago. Fortschr Med Orig. 2001;118(4):147-51.
125. Pavelka K, Peliskova Z, Stehlikova H, et al. Intraindividual differences in pain relief and functional improvement in osteoarthritis with diclofenac or tramadol. Clin Drug Investig. 1998;16(6):421-9. doi: 10.2165/00044011-199816060-00002
126. Adams E, Breiner S, Cicero T, et al. A comparison of the abuse liability of tramadol, NSAIDs, and hydrocodone in patients with chronic pain. J Pain Symptom Manage. 2006;31(5):465-76. doi: 10.1016/j.jpainsymman.2005.10.006
127. Ritvo J, Koonce R, Thurstone C, Causey HL 3rd. Tramadol dependence: treatment with buprenor-phine/naloxone. Am J Addict. 2007;16(1):67-8. doi: 10.1080/10550490601080118
128. Trescot A, Helm S, Hansen H, et al. Opioids in the management of chronic non-cancer pain: An update of American Society of the Interventional Pain Physicians’ (ASIPP) Guidelines. Pain Physician. 2008;Opioids Special Issue 11:5-62.
129. Van Tulder MW, Touray T, Furlan AD, et al. Muscle relaxants for non-specific low back pain. Cochrane Database Syst Rev 2003;(2):CD004252. doi: 10.1002/14651858.cd004252
130. Гурак СВ, Парфенов ВА, Борисов КН. Мидокалм в комплексной терапии острой поясничной боли. Боль. 2006;(3):27-30 [Gurak SV, Parfenov VA, Borisov KN. Mydocalm in the treatment of acute low back pain. Bol’. 2006;(3):27-30 (In Russ.)].
131. Ходинка Л, Меилингер М, Сабо Ж, Залавари И. Лечение острой поясничной боли Мидокалмом. Результаты международного мультицентрового рандомизированного двойного-слепого плацебо-контролируемого клинического исследования. Русский медицинский журнал. 2003;(5):246-9 [Khodinka L, Meilinger M, Sabo Zh, Zalavari I. Treatment of acute low back pain Mydocalm. The results of an international, multicentre, randomized, double-blind, placebo-controlled clinical trial. Russkii Meditsinskii Zhurnal. 2003;(5):246-9 (In Russ.)].
132. Pratzel HG, Alken RG, Ramm S. Efficacy and tolerance of repeated doses of tolperisone hydrochloride in the treatment of painful reflex muscle spasm: results of a prospective placebo-controlled double-blind trial. Pain. 1996 Oct;67(2-3):417-25. doi: 10.1016/0304-3959(96)03187-9
133. Кукушкин МЛ. Современный взгляд на механизм действия Мидокалма. Consilium medicum. 2013;15(2):89-94 [Kukushkin ML. Modern view of the mechanism of action Mydocalm. Consilium medicum. 2013;15(2):89-94. (In Russ.)].
134. Шарапова ЕП, Алексеева ЛИ, Зайцева ЕМ и др. Применение миорелаксантов в комплексной терапии остеоартроза. Consilium medicum. 2008;(2):30-2 [Sharapova EP, Alekseeva LI, Zaitseva EM, et al. The use of muscle relaxants in the treatment of osteoarthritis. Consilium Medicum. 2008;(2):30-2 (In Russ.)].
135. Berry H, Hutchinson D. A multicentre placebo-controlled study in general practice to evaluate the efficacy and safety of tizanidine in acute low-back pain. J Int Med Res. 1988;16(2):75-82.
136. Berry H, Hutchinson D. Tizanidine and ibuprofen in acute lowback pain: results of a double-blind multicentre study in general practice. J Int Med Res. 1988;16(2):83-91.
137. Sirdalud Ternilin Asia-Pacific Study group. Efficacy and gastroprotective effects of tizanidine plus diclofenac versus placebo plus diclofenac in patients with painful muscle spasm. Curr Ther Res. 1998;59:13-22. doi: 10.1016/S0011-393X(98)85019-4
138. Pareek A, Chandurkar N, Chandanwale A, et al. Aceclofenactizanidine in the treatment of acute low back pain: a doubleblind, double-dummy, randomized, multicentric, comparative study against aceclofenac alone. Eur Spine J. 2009;18(12):1836-42. doi: 10.1007/s00586-009-1019-4
139. Karol D, Muzyk A, Preud’homme X. A case of delirium, motor disturbances, and autonomic dysfunction due to baclofen and tizanidine withdrawal: a review of the literature. Gen Hosp Psychiatry. 2011;33(1):84.
140. Del Rosario M, Weachter R, Flaker G. Drug-induced QT prolongation and sudden death. Mol Med. 2010;107(1):53-8.
141. Kaddar N, Vigneault P, Pilote S, et al. Tizanidine (Zanaflex): A muscle relaxant that may prolong the QT interval by blocking IKr. J Cardiovasc Pharmacol Ther. 2012 Mar;17(1):102-9. doi: 10.1177/1074248410395020. Epub 2011 Feb 11.
142. Publow S, Branam D. Hypotension and bradycardia associated with concomitant tizanidine and lisinopril therapy. Am J Health Syst Pharm. 2010;67(19):1606-10. doi: 10.2146/ajhp090657
143. Devulder J. Flupirtine in pain management: pharmacological properties and clinical use. CNS Drugs. 2010;24(10):867-81. doi: 10.2165/11536230-000000000-00000
144. Klawe C, Maschke M. Flupirtine: pharmacology and clinical applications of a nonopioid analgesic and potentially neuroprotective compound. Expert Opin Pharmacother. 2009;10(9):1495-500. doi: 10.1517/14656560902988528
145. Harish S, Bhuvana K, Bengalorkar GM, Kumar TN. Flupirtine: Clinical pharmacology. J Anaesthesiol Clin Pharmacol. 2012;28:172-7. doi: 10.4103/0970-9185.94833
146. Ueberall M, Mueller-Schwefe G, Terhaag B. Efficacy and tolerability of flupirtine in subacute/chronic musculoskeletal pain – results of a patient level, pooled re-analysis of randomized, double-blind, controlled trials. Int J Clin Pharmacol Ther. 2011;49(11):637-47. doi: 10.5414/CP210000
147. Uberall MA, Mueller-Schwefe GH, Terhaag B. Efficacy and safety of flupirtine modified release for the management of moderate to severe chronic low back pain: results of SUPREME, a prospective randomized, double-blind, placebo- and active-controlled parallel-group phase IV study. Curr Med Res Opin. 2012 Oct;28(10):1617-34. doi: 10.1185/03007995.2012.726216
148. Данилов АБ, Николаева НС. Эффективность новой формы флупиртина® (Катадолона форте) в лечении острой боли в спине. Manage pain. 2013;(1):44-8 [Danilov AB, Nikolaeva NS. The effectiveness of a new form of flupirtina® (Katadolona fort) in the treatment of acute pain in the back. Manage Pain. 2013;(1):44-8 (In Russ.)].
149. Richards B, Whittle S, van der Heijde D, Buchbinder R. Efficacy and safety of neuromodulators in inflammatory arthritis: A Cochrane Systematic Review. J Rheumatol Suppl. 2012;90:28-33. doi: 10.3899/jrheum.120339
150. Chappell A, Ossanna M, Liu-Seifert H, et al. Duloxetine, a centrally acting analgesic, in the treatment of patients with osteoarthritis knee pain: A 13-week, randomized, placebo-controlled trial. Pain. 2009;146(3):253-60. doi: 10.1016/j.pain.2009.06.024
151. Williamson O, Schroer M, Ruff D, et al. Onset of response with duloxetine treatment in patients with osteoarthritis knee pain and chronic low back pain: a post hoc analysis of placebo-controlled trials. Clin Ther. 2014 Apr 1;36(4):544-51. doi: 10.1016/j.clinthera.2014.02.009. Epub 2014 Mar 17.
152. Pergolizzi JV Jr, Raffa RB, Taylor R Jr, et al. A review of duloxetine 60 mg once-daily dosing for the management of diabetic peripheral neuropathic pain, fibromyalgia, and chronic musculoskeletal pain due to chronic osteoarthritis pain and low back pain. Pain Pract. 2013 Mar;13(3):239-52. doi: 10.1111/j.1533-2500.2012.00578.x. Epub 2012 Jun 21.
153. Giladi H, Choiniere M, Fitzcharles MA, et al. Pregabalin for chronic pain: does one medication fit all? Curr Med Res Opin. 2015 Jul;31(7):1403-11. doi: 10.1185/03007995.2015.1040750. Epub 2015 May 11.
154. Sakai Y, Ito K, Hida T, et al. Pharmacological management of chronic low back pain in older patients: a randomized controlled trial of the effect of pregabalin and opioid administration. Eur Spine J. 2015 Jun;24(6):1309-17. doi: 10.1007/s00586-015-3812-6. Epub 2015 Feb 15.
155. Romano CL, Romano D, Lacerenza M. Antineuropathic and antinociceptive drugs combination in patients with chronic low back pain: a systematic review. Pain Res Treat. 2012;2012:154781. doi: 10.1155/2012/154781. Epub 2012 Apr 26.
156. Ohtori S, Inoue G, Orita S, et al. Efficacy of combination of meloxicam and pregabalin for pain in knee osteoarthritis. Yonsei Med J. 2013 Sep;54(5):1253-8. doi: 10.3349/ymj.2013.54.5.1253
157. Carmichael N, Katz J, Clarke H, et al. An intensive perioperative regimen of pregabalin and celecoxib reduces pain and improves physical function scores six weeks after total hip arthroplasty: a prospective randomized controlled trial. Pain Res Manag. 2013 May-Jun;18(3):127-32. doi: 10.1155/2013/258714
158. Hameed F, Ihm J. Injectable medications for osteoarthritis. PM&R. 2012;4(5 Suppl):75-81. doi: 10.1016/j.pmrj.2012.02.010
159. Habib G, Saliba W, Nashashibi M. Local effects of intra-articular corticosteroids. Clin Rheumatol. 2010;29(4):347-56. doi: 10.1007/s10067-009-1357-y
160. Dean BJF, Lostis E, Oakley T, et al. Risks and benefits of glucocorticoid treatment for tendinopathy: A systematic review of the effects of local glucocorticoid on tendon. Semin Arthritis Rheum. 2014;43(4):570-6. doi: 10.1016/j.semarthrit.2013.08.006
161. Tallia A, Cardone D. Diagnostic and therapeutic injection of the shoulder region. Am Fam Physician. 2003;67(6):1271-8.
162. Coombes BK, Bisset L, Vicenzino B. Efficacy and safety of corticosteroid injections and other injections for management of tendinopathy: a systematic review of randomised controlled trials. Lancet. 2010 Nov 20;376(9754):1751-67. doi: 10.1016/S0140-6736(10)61160-9. Epub 2010 Oct 21.
163. Bellamy N, Campbell J, Robinson V, et al. Intraarticular corticosteroid for treatment of osteoarthritis of the knee. Cochrane Database Syst Rev. 2006 Apr 19;(2):CD005328. doi: 10.1002/14651858.cd005328.pub2
164. Насонов ЕЛ, редактор. Ревматология. Клинические рекомендации. Москва: ГЭОТАР-Медиа; 2010. 752 с. [Nasonov EL, editor. Revmatologiya. Klinicheskie rekomendatsii [Rheumatology. Clinical recommendations]. Moscow: GEOTAR-Media; 2010. 752 p.].
165. Peloso P, Gross A, Haines T, et al. Medicinal and injection therapies for mechanical neck disorders. Cochrane Database Syst Rev. 2007 Jul 18;(3):CD000319. doi: 10.1002/14651858.cd000319.pub4
166. Staal JB, de Bie RA, de Vet HC, et al. Injection therapy for subacute and chronic low back pain: an updated Cochrane review. Spine (Phila Pa 1976). 2009 Jan 1;34(1):49-59. doi: 10.1097/BRS.0b013e3181909558
167. Chou R, Hashimoto R, Friedly J, et al. Pain Management Injection Therapies for Low Back Pain [Internet]. Rockville (MD): Agency for Healthcare Research and Quality (US); 2015 Mar. AHRQ Technology Assessments.
168. Farooq M, Devitt A. Perceived efficacy and risks of infection following intra-articular injections: a survey of orthopaedic surgeons. Ir J Med Sci. 2005;174(1):26-32. doi: 10.1007/BF03168515
169. Charalambous C, Tryfonidis M, Sadiq S, et al. Septic arthritis following intraarticular glucocorticoid injection of the knee – a survey of current practice regarding antiseptic technique used during intra-articular glucocorticoid injection of the knee. Clin Rheumatol. 2003;22:386-90. doi: 10.1007/s10067-003-0757-7
170. Younes M, Neffati F, Touzi M, et al. Systemic effects of epidural and intra-articular glucocorticoid injections in diabetic and nondiabetic patients. Joint Bone Spine. 2007 Oct;74(5):472-6. Epub 2007 Jul 6. doi: 10.1016/j.jbspin.2006.10.009
171. Moon HJ, Choi KH, Lee SI, et al. Changes in blood glucose and cortisol levels after epidural or shoulder intraarticular glucocorticoid injections in diabetic or nondiabetic patients. Am J Phys Med Rehabil. 2014 May;93(5):372-8. doi: 10.1097/PHM.0000000000000001
172. Strand V, McIntyre LF, Beach WR, et al. Safety and efficacy of US-approved viscosupplements for knee osteoarthritis: a systematic review and meta-analysis of randomized, saline-controlled trials. J Pain Res. 2015 May 7;8:217-28. doi: 10.2147/JPR.S83076. eCollection 2015.
173. Campbell KA, Erickson BJ, Saltzman BM, et al. Is local viscosupplementation injection clinically superior to other therapies in the treatment of osteoarthritis of the knee: A systematic review of overlapping meta-analyses. Arthroscopy. 2015 May 18. pii: S0749-8063(15)00257-1. doi: 10.1016/j.arthro.2015.03.030 [Epub ahead of print].
174. Bannuru RR, Vaysbrot EE, Sullivan MC, McAlindon TE. Relative efficacy of hyaluronic acid in comparison with NSAIDs for knee osteoarthritis: a systematic review and meta-analysis. Semin Arthritis Rheum. 2014 Apr;43(5):593-9. doi: 10.1016/j.semarthrit.2013.10.002. Epub 2013 Oct 14.
175. Colen S, Haverkamp D, Mulier M, van den Bekerom MP. Hyaluronic acid for the treatment of osteoarthritis in all joints except the knee: what is the current evidence? BioDrugs. 2012 Apr 1;26(2):101-12. doi: 10.2165/11630830-000000000-00000
176. Lieberman JR, Engstrom SM, Solovyova O, et al. Is intra-articular hyaluronic acid effective in treating osteoarthritis of the hip joint? J Arthroplasty. 2015 Mar;30(3):507-11. doi: 10.1016/j.arth.2013.10.019. Epub 2013 Nov 8.
177. Van den Bekerom MP, Lamme B, Sermon A, Mulier M. What is the evidence for viscosupplementation in the treatment of patients with hip osteoarthritis? Systematic review of the literature. Arch Orthop Trauma Surg. 2008 Aug;128(8):815-23. Epub 2007 Sep 15. doi: 10.1007/s00402-007-0447-z
178. Blaine T, Moskowitz R, Udell J, et al. Treatment of persistent shoulder pain with sodium hyaluronate: a randomized, controlled trial. A multicenter study. J Bone Joint Surg Am. 2008;90(5):970-9. doi: 10.2106/JBJS.F.01116
179. Chang KV, Hsiao MY, Chen WS, et al. Effectiveness of intra-articular hyaluronic acid for ankle osteoarthritis treatment: a systematic review and meta-analysis. Arch Phys Med Rehabil. 2013 May;94(5):951-60. doi: 10.1016/j.apmr.2012.10.030. Epub 2012 Nov 10.
180. Баринов АН, Пархоменко ЕВ, Махинов КА. Причины отрицательных исходов лечения боли в спине и способы их преодоления. Эффективная фармакотерапия. Неврология. 2014;49(5):40-50 [Barinov AN, Parkhomenko EV, Makhinov KA. The reasons for the negative outcomes of the treatment of back pain and how to overcome them. Effektivnaya farmakoterapiya. Nevrologiya. 2014;49(5):40-50 (In Russ.)].
181. Алексеева ЛИ. Препараты замедленного действия в лечении остеоартроза. Русский медицинский журнал. 2012;(7):389-94 [Alekseeva LI. Slow-acting drugs in the treatment of osteoarthritis. Russkii Meditsinskii Zhurnal. 2012;(7):389-94 (In Russ.)].
182. Imagawa K, de Andres M, Hashimoto K, et al. The epigenetic effect of glucosamine and a nuclear factor-kappa B (NF-kB) inhibitor on primary human chondrocytes – implications for
183. osteoarthritis. Biochem Biophys Res Commun. 2011;405(3):362-7. doi: 10.1016/j.bbrc.2011.01.007
184. Calamia V, Ruiz-Romero C, Rocha B, et al. Pharmacoproteomic study of the effects of chondroitin and glucosamine sulfate on human articular chondrocytes. Arthritis Res Ther. 2010;12(4):R138. doi: 10.1186/ar3077
185. Au R, Au A, Rashmir-Raven A, Frondoza C. Inhibition proinflammatory gene expression in chondrocytes, monocytes, and fibroblasts by combination of avocado soybean unsaponiables, glucosamine and chondroitin sulfate. FASEB. 2007;21(6):702-7.
186. Towheed T, Maxwell L, Anastassiades T, et al. Glucosamine therapy for treating osteoarthritis. Cochrane Database Syst Rev. 2005 Apr 18;(2):CD002946. doi: 10.1002/14651858.cd002946.pub2
187. Reichenbach S, Sterchi R, Scherer M, et al. Meta-analysis: chondroitin for osteoarthritis of the knee or hip. Ann Intern Med. 2007;146(8):580-90. doi: 10.7326/0003-4819-146-8-200704170-00009
188. Fidelix TS, Macedo CR, Maxwell LJ, Fernandes Moca Trevisani V. Diacerein for osteoarthritis. Cochrane Database Syst Rev. 2014 Feb 10;2:CD005117. doi: 10.1002/14651858.cd005117.pub3
189. Christensen R, Bartels E, Astrup A, Bliddal H. Symptomatic efficacy of avocado-soybean unsaponifiables (ASU) in osteoarthritis (OA) patients: a meta-analysis of randomized controlled trials. Osteoarthritis Cartilage. 2008;16(4):399-408. doi: 10.1016/j.joca.2007.10.003
190. Singh G, Alekseeva L, Alexeev V, Triadafilopoulos G. Glucosamin-chondroitin sulfate reduces pain, disability and NSAID consumption in patients with chronic low back pain: a large, community-based, pilot, open prospective observational study. ELAR, 2013, SAT0419
191. Каратеев АЕ, Алексеева ЛИ. Оценка переносимости диацереина в реальной клинической практике. Результаты исследования РОКАДА (Ретроспективная Оценка Клинических Аспектов применения Диафлекса при остеоартрозе). Научно-практическая ревматология. 2015;53(2):169-74 [Karateev AE, Alekseeva LI. Estimation of diacerein tolerability in real clinical practice: Results of the RACADA (Retrospective Assessment of Clinical Aspects of using Diaflex in osteoArthritis). Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2015;53(2):169-74 (In Russ.)]. doi: 10.14412/1995-4484-2015-169-174
192. Atchison J, Vincent HK. Obesity and low back pain: relationships and treatment. Pain Manag. 2012 Jan;2(1):79-86. doi: 10.2217/pmt.11.64
193. Kotowski S, Davis KG. Influence of weight loss on musculoskeletal pain: Potential short-term relevance. Work. 2010;36(3):295-304. doi: 10.3233/WOR-2010-1031
194. Wai EK, Rodriguez S, Dagenais S, Hall H. Evidence-informed management of chronic low back pain with physical activity, smoking cessation, and weight loss. Spine J. 2008 JanFeb;8(1):195-202. doi: 10.1016/j.spinee.2007.10.024
195. Christensen R, Bartels EM, Astrup A, Bliddal H. Effect of weight reduction in obese patients diagnosed with knee osteoarthritis: a systematic review and meta-analysis. Ann Rheum Dis. 2007 Apr;66(4):433-9. doi: 10.1136/ard.2006.065904. Epub 2007 Jan 4.
196. Gudbergsen H, Boesen M, Lohmander LS, et al. Weight loss is effective for symptomatic relief in obese subjects with knee osteoarthritis independently of joint damage severity assessed by high-field MRI and radiography. Osteoarthritis Cartilage. 2012 Jun;20(6):495-502. doi: 10.1016/j.joca.2012.02.639. Epub 2012 Mar 5.
197. Jones A, Silva PG, Silva AC, et al. Impact of cane use on pain, function, general health and energy expenditure during gait in patients with knee osteoarthritis: a randomised controlled trial. Ann Rheum Dis. 2012 Feb;71(2):172-9. doi: 10.1136/ard.2010.140178. Epub 2011 Nov 29.
198. Duivenvoorden T, Brouwer RW, van Raaij TM, et al. Braces and orthoses for treating osteoarthritis of the knee. Cochrane Database Syst Rev. 2015 Mar 16;3:CD004020. doi: 10.1002/14651858.cd004020.pub3
199. Segal NA. Bracing and orthoses: a review of efficacy and mechanical effects for tibiofemoral osteoarthritis. PM&R. 2012 May;4(5 Suppl):S89-96. doi: 10.1016/j.pmrj.2012.01.018
200. Raja K, Dewan N. Efficacy of knee braces and foot orthoses in conservative management of knee osteoarthritis: a systematic review. Am J Phys Med Rehabil. 2011 Mar;90(3):247-62. doi: 10.1097/PHM.0b013e318206386b
201. Bennell KL, Buchbinder R, Hinman RS. Physical therapies in the management of osteoarthritis: current state of the evidence. Curr Opin Rheumatol. 2015 May;27(3):304-11. doi: 10.1097/BOR.0000000000000160
202. Bervoets DC, Luijsterburg PA, Alessie JJ, et al. Massage therapy has short-term benefits for people with common musculoskeletal disorders compared to no treatment: a systematic review. J Physiother. 2015 Jul;61(3):106-16. doi: 10.1016/j.jphys.2015.05.018. Epub 2015 Jun 17.
203. Kadhim-Saleh A, Maganti H, Ghert M, et al. Is low-level laser therapy in relieving neck pain effective? Systematic review and meta-analysis. Rheumatol Int. 2013 Oct;33(10):2493-501. doi: 10.1007/s00296-013-2742-z. Epub 2013 Apr 12.
204. Brosseau L, Robinson V, Wells G, et al. WITHDRAWN: Low level laser therapy (Classes III) for treating osteoarthritis. Cochrane Database Syst Rev. 2007 Jul 18;(1):CD002046.
205. Pittler MH, Brown EM, Ernst E. Static magnets for reducing pain: systematic review and meta-analysis of randomized trials. CMAJ. 2007 Sep 25;177(7):736-42. doi: 10.1503/cmaj.061344
206. Ryang We S, Koog YH, Jeong KI, Wi H. Effects of pulsed electromagnetic field on knee osteoarthritis: a systematic review. Rheumatology (Oxford). 2013 May;52(5):815-24. doi: 10.1093/rheumatology/kes063. Epub 2012 Apr 13.
207. Li S, Yu B, Zhou D, et al. Electromagnetic fields for treating osteoarthritis. Cochrane Database Syst Rev. 2013 Dec 14;12:CD003523. doi: 10.1002/14651858.cd003523.pub2
208. Menke JM. Do manual therapies help low back pain? A comparative effectiveness meta-analysis. Spine (Phila Pa 1976). 2014 Apr 1;39(7):E463-72. doi: 10.1097/BRS.0000000000000230
209. Rubinstein SM, Terwee CB, Assendelft WJ, et al. Spinal manipulative therapy for acute low-back pain. Cochrane Database Syst Rev. 2012 Sep 12;9:CD008880. doi: 10.1002/14651858.cd008880.pub2
210. Franke H, Franke JD, Fryer G. Osteopathic manipulative treatment for nonspecific low back pain: a systematic review and meta-analysis. BMC Musculoskelet Disord. 2014 Aug 30;15:286. doi: 10.1186/1471-2474-15-286
211. Lam M, Galvin R, Curry P. Effectiveness of acupuncture for nonspecific chronic low back pain: a systematic review and metaanalysis. Spine (Phila Pa 1976). 2013 Nov 15;38(24):2124-38. doi: 10.1097/01.brs.0000435025.65564.b7
212. Xu M, Yan S, Yin X, et al. Acupuncture for chronic low back pain in long-term follow-up: a meta-analysis of 13 randomized controlled trials. Am J Chin Med. 2013;41(1):1-19. doi: 10.1142/S0192415X13500018
213. Haake M, Mü ller H, Schade-Brittinger C, et al. German Acupuncture Trials (GERAC) for chronic low back pain: randomized, multicenter, blinded, parallel-group trial with 3 groups. Arch Intern Med. 2007;167(17):1892-8. doi: 10.1001/Archinte.167.17.1892
214. Manheimer E, Cheng K, Linde K, et al. Acupuncture for peripheral joint osteoarthritis. Cochrane Database Syst Rev. 2010 Jan 20;(1):CD001977. doi: 10.1002/14651858.CD001977.pub2
215. Manyanga T, Froese M, Zarychanski R, et al. Pain management with acupuncture in osteoarthritis: a systematic review and metaanalysis. BMC Complement Altern Med. 2014 Aug 23;14:312. doi: 10.1186/1472-6882-14-312
216. So P, Jiang Y, Qin Y. Touch therapies for pain relief in adults. Cochrane Database Syst Rev. 2008 Oct 8;(4):CD006535. doi: 10.1002/14651858.cd006535.pub2
217. Smith K. Against homeopathy – a utilitarian perspective. Bioethics. 2012;26(8):398-409. doi: 10.1111/j.1467-8519.2010.01876.x
218. Brien S, Lachance L, Prescott P, et al. Homeopathy has clinical benefits in rheumatoid arthritis patients that are attributable to the consultation process but not the homeopathic remedy: a randomized controlled clinical trial. Rheumatology (Oxford). 2011;50(6):1070-82. doi: 10.1093/rheumatology/keq234
219. Beer A, Fey S, Zimmer M, et al. Effectiveness and safety of homeopathic drug combination in the treatment of chronic low back pain. A double-blind, randomized, placebo-controlled clinical trial. MMW Fortschr Med. 2012 Jun 28;154 Suppl 2:48-57.
220. Long L, Ernst E. Homeopathic remedies for the treatment of osteoarthritis: a systematic review. Br Homeopath J. 2001 Jan;90(1):37-43. doi: 10.1054/homp.1999.0449
221. Koley M, Saha S, Ghosh S. A double-blind, randomized, placebo-controlled feasibility study evaluating individualized homeopathy in managing pain of knee osteoarthritis. J Evid Based Complement Altern Med. 2015 Jul;20(3):186-91. doi: 10.1177/2156587214568668
222. Lembeck M. Quantum physics, medicine and insurance. Versicherungsmedizin. 2007;59(4):179-85.
223. Jain S, Mills P. Biofield therapies: helpful or full of hype? A best evidence synthesis. Int J Behav Med. 2010;17(1):1-16. doi: 10.1007/s12529-009-9062-4
224. Rosch P. Bioelectromagnetic and subtle energy medicine: the interface between mind and matter. Ann N Y Acad Sci. 2009;1172:297-311. doi: 10.1111/j.1749-6632.2009.04535.x
225. Galle M. Bioresonance, a study of pseudo-scientific language. Forsch Komplementarmed Klass Naturheilkd. 2004;11(5):306.
226. Hammerschlag R, Marx B, Aickin M. Nontouch biofield therapy: a systematic review of human randomized controlled trials reporting use of only nonphysical contact treatment. J Altern Compliment Med. 2014 Dec;20(12):881-92. doi: 10.1089/acm.2014.0017
Боль [Текст] : (практическое руководство для врачей)
Карточка
Боль [Текст] : (практическое руководство для врачей) / [Абузаров Г. Р.. и др.] ; под ред. Н. Н. Яхно, М. Л. Кукушкина ; Российская акад. мед. наук. — Москва : Изд-во РАМН : МОО «О-во по изучению боли», 2011. — 511 с. : ил.; 21 см.; ISBN 978-5-7901-0115-1
Авт. указаны на 3-й с.
Указ.
Здравоохранение. Медицинские науки — Невропатология — Симптоматология нервных болезней — Нарушения чувствительности — Боль — Пособие для специалистов
Боль — Практические пособия
Шифр хранения:
FB 2 12-12/321
FB 2 12-12/322
Описание
| Заглавие | Боль [Текст] : (практическое руководство для врачей) |
|---|---|
| Дата поступления в ЭК | 05.03.2012 |
| Каталоги | Книги (изданные с 1831 г. по настоящее время) |
| Сведения об ответственности | [Абузаров Г. Р.. и др.] ; под ред. Н. Н. Яхно, М. Л. Кукушкина ; Российская акад. мед. наук |
| Выходные данные | Москва : Изд-во РАМН : МОО «О-во по изучению боли», 2011 |
| Физическое описание | 511 с. : ил.; 21 см |
| ISBN | ISBN 978-5-7901-0115-1 |
| Примечание | Авт. указаны на 3-й с. |
| Указ. | |
| Тема | Здравоохранение. Медицинские науки — Невропатология — Симптоматология нервных болезней — Нарушения чувствительности — Боль — Пособие для специалистов |
| Боль — Практические пособия | |
| BBK-код | Р62-324.21,07 |
| Язык | Русский |
| Места хранения | FB 2 12-12/321 |
| FB 2 12-12/322 |