Состав:
Применение:
Применяется при лечении:
Страница осмотрена фармацевтом Милитян Инессой Месроповной Последнее обновление 2020-03-16
Внимание!
Информация на странице предназначена только для медицинских работников!
Информация собрана в открытых источниках и может содержать значимые ошибки!
Будьте внимательны и перепроверяйте всю информацию с этой страницы!
Топ 20 лекарств с такими-же компонентами:
Топ 20 лекарств с таким-же применением:
Предоставленная в разделе Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Bristaflam
Состав
Предоставленная в разделе Состав Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Состав
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Aceclofenac
Терапевтические показания
Предоставленная в разделе Терапевтические показания Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Терапевтические показания
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Крем для наружного применения; Таблетки, покрытые пленочной оболочкой; Порошок для пероральной суспензии; Порошок для приготовления суспензии для приема внутрь
Порошок для суспензии; Таблетка
лечение местной боли вследствие травматических повреждений и воспалительных заболеваний опорно-двигательного аппарата, в т.ч. спортивных травм;
уменьшение воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения или ушибов, а также лечение люмбаго, кривошеи и периартрита.
лечение местной боли вследствие травматических повреждений и воспалительных заболеваний опорно-двигательного аппарата, в т.ч. спортивных травм;
уменьшение воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения или ушибов, а также лечение люмбаго, кривошеи и периартрита.
Способ применения и дозы
Предоставленная в разделе Способ применения и дозы Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Способ применения и дозы
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Крем для наружного применения; Таблетки, покрытые пленочной оболочкой; Порошок для пероральной суспензии; Порошок для приготовления суспензии для приема внутрь
Порошок для суспензии; Таблетка
Местно.
Крем Аэртал® предназначен только для наружного применения и не должен наноситься под окклюзионные повязки.
Крем Аэртал® следует наносить легкими массирующими движениями на пораженный участок 3 раза в день. Применяемая доза зависит от размера пораженного участка: 1,5–2 г крема Аэртал® (приблизительно соответствует полоске крема длиной 5–7 см).
Особые группы пациентов
Дети. Опыт применения крема Аэртал® у детей отсутствует, поэтому крем Аэртал® противопоказан к применению у детей.
Пожилой возраст. Коррекция режима дозирования у лиц пожилого возраста не требуется.
Местно.
Крем Bristaflam® предназначен только для наружного применения и не должен наноситься под окклюзионные повязки.
Крем Bristaflam® следует наносить легкими массирующими движениями на пораженный участок 3 раза в день. Применяемая доза зависит от размера пораженного участка: 1,5–2 г крема Bristaflam® (приблизительно соответствует полоске крема длиной 5–7 см).
Особые группы пациентов
Дети. Опыт применения крема Bristaflam® у детей отсутствует, поэтому крем Bristaflam® противопоказан к применению у детей.
Пожилой возраст. Коррекция режима дозирования у лиц пожилого возраста не требуется.
Противопоказания
Предоставленная в разделе Противопоказания Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Противопоказания
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
повышенная чувствительность к ацеклофенаку или каким-либо из вспомогательных веществ;
наличие в прошлом непереносимости НПВП, в т.ч. диклофенака;
наличие в прошлом приступов бронхиальной астмы, уртикарной сыпи или острого ринита на фоне приема ацетилсалициловой кислоты или других НПВП;
наличие инфекции, вызванной вирусом варицелла-зостер;
нарушение целостности кожных покровов в предполагаемом месте нанесения;
беременность;
детский возраст до 18 лет.
С осторожностью: печеночная порфирия (обострение); эрозивно-язвенные поражения ЖКТ (в фазе обострения); тяжелые нарушения функции печени и почек; хроническая сердечная недостаточность; бронхиальная астма; крапивница или острый ринит, спровоцированные приемом АСК или других НПВП; нарушения свертываемости крови (в т.ч. гемофилия, удлинение времени кровотечения, склонность к кровотечениям); пожилой возраст; период лактации.
Побочные эффекты
Предоставленная в разделе Побочные эффекты Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Побочные эффекты
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
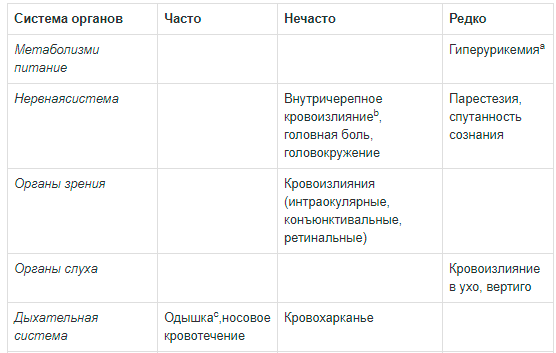
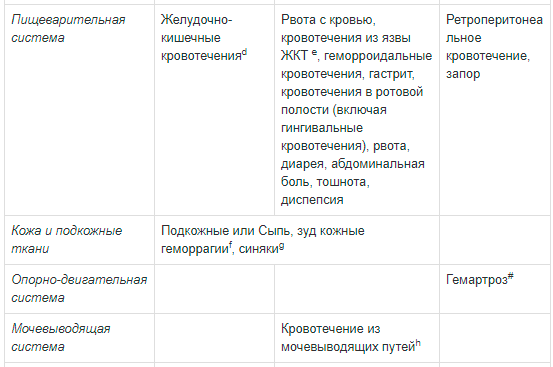
Ниже представлены нежелательные явления, информация о которых была получена в клинических исследованиях и в ходе постмаркетингового наблюдения; нежелательные явления сгруппированы в соответствии с классами систем органов согласно MedDRA и частотой возникновения: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000).
Общие расстройства и нарушения в месте введения: нечасто — реакция фоточувствительности, эритема, кожный зуд; редко — раздражение кожи; очень редко — буллезные реакции (в т.ч. синдром Стивенса-Джонсона и токсический эпидермальный некролиз).
Известны очень редкие сообщения о тяжелых кожных реакциях, иногда приводящих к смерти, включающие эксфолиативный дерматит, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, связанные с применением НПВП.
Передозировка
Предоставленная в разделе Передозировка Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Передозировка
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Случаи передозировки ацеклофенака неизвестны. Точные симптомы передозировки ацеклофенака неизвестны.
Симптомы: в случае неправильного применения или случайного проглатывания могут развиваться артериальная гипотензия, почечная недостаточность, судороги, раздражение слизистой оболочки ЖКТ, а также угнетение дыхания.
Лечение: симптоматическая и поддерживающая терапия. Следует как можно скорее предотвратить всасывание препарата путем промывания желудка и назначения активированного угля. Форсированный диурез или гемоперфузия неэффективны вследствие высокой степени связывания ацеклофенака с белками плазмы крови и его интенсивным метаболизмом.
Фармакодинамика
Предоставленная в разделе Фармакодинамика Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Фармакодинамика
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Крем для наружного применения; Таблетки, покрытые пленочной оболочкой; Порошок для пероральной суспензии; Порошок для приготовления суспензии для приема внутрь
Порошок для суспензии; Таблетка
Ацеклофенак представляет собой НПВП, обладающее противовоспалительным и анальгезирующим действием. Препарат подавляет развитие отека и эритемы независимо от этиологии воспаления. Ацеклофенак подавляет образование ПГ и ЛТ за счет обратимого подавления ЦОГ-1 и ЦОГ-2.
Установленная клиническая эффективность препарата дополняется хорошей переносимостью.
Применение крема Аэртал® целесообразно у пациентов с травматическими повреждениями или воспалительными заболеваниями опорно-двигательного аппарата.
Ацеклофенак представляет собой НПВП, обладающее противовоспалительным и анальгезирующим действием. Препарат подавляет развитие отека и эритемы независимо от этиологии воспаления. Ацеклофенак подавляет образование ПГ и ЛТ за счет обратимого подавления ЦОГ-1 и ЦОГ-2.
Установленная клиническая эффективность препарата дополняется хорошей переносимостью.
Применение крема Bristaflam® целесообразно у пациентов с травматическими повреждениями или воспалительными заболеваниями опорно-двигательного аппарата.
Фармакокинетика
Предоставленная в разделе Фармакокинетика Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Фармакокинетика
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Всасывание. После нанесения ацеклофенак всасывается из зоны нанесения, быстро достигая насыщения. Он накапливается в зоне всасывания, что способствует увеличению противовоспалительной активности, и постепенно поступает в системный кровоток в небольших количествах, в связи с чем риск побочного действия, в т.ч. на ЖКТ, минимизируется.
Распределение. Ацеклофенак распределяется по всему организму.
Выведение. Ацеклофенак метаболизируется в печени и выводится медленно почками и через кишечник, частично в неизмененном виде.
Взаимодействие
Предоставленная в разделе Взаимодействие Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Взаимодействие
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
Несмотря на отсутствие данных о возможных взаимодействиях ацеклофенака с другими препаратами, необходимо соблюдать осторожность при назначении его пациентам, принимающим другие лекарственные препараты, в особенности те, в состав которых входят литий, дигоксин.
Также следует соблюдать осторожность при сопутствующей терапии антикоагулянтами, диуретиками или другими обезболивающими препаратами.
Фармокологическая группа
Предоставленная в разделе Фармокологическая группа Bristaflamинформация составлена на основе данных о другом лекарстве с точно таким же составом как лекарство Bristaflam. Будьте
внимательны и обязательно уточняйте информацию по разделу Фармокологическая группа
в инструкции к лекарству Bristaflam непосредственно из упаковки или у фармацевта в аптеке.
more…
- Нестероидный противовоспалительный препарат (НПВП) [НПВС — Производные уксусной кислоты и родственные соединения]
Bristaflam цена
У нас нет точных данных по стоимости лекарства.
Однако мы предоставим данные по каждому действующему веществу
Средняя стоимость Aceclofenac 100 mg за единицу в онлайн аптеках от 0.3$ до 0.55$, за упаковку от 23$ до 39$.
Источники:
- https://www.drugs.com/search.php?searchterm=bristaflam
- https://pubmed.ncbi.nlm.nih.gov/?term=bristaflam
Доступно в странах
Найти в стране:
А
Б
В
Г
Д
Е
З
И
Й
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ч
Ш
Э
Ю
Я
Торговое название:
- Бристафлам
- Bristaflam
Состав:
Каждый 100 грамм крема содержит:
Ацеклофенак (микронизированный) – 1.5 г
Вспомогательные компоненты:
Воск эмульсионный, парафин жидкий, метилпарагидроксибензоат, пропилпарагидроксибензоат, вода.
Свойства:
Ацеклофенак представляет собой НПВП, обладающий также жаропонижающим и анальгезирующим действием. Препарат подавляет развитие отека и эритемы независимо от этиологии воспаления. Ацеклофенак подавляет образование простагландинов и лейкотриенов за счет обратимого ингибирования ЦОГ.
Клиническая эффективность и безопасность: Установленная клиническая эффективность препарата дополняется хорошей переносимостью.
Показания:
- Лечение местной боли вследствие травматических повреждений и воспалительных заболеваний опорно-двигательного аппарата, в т.ч. спортивных травм;
- Для уменьшения воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения и ушибов;
- Люмбаго;
- Кривошея;
- Периартрит.
Способ применения и дозы:
- Крем Бристафлам предназначен только для наружного применения. Не следует наносить крем под окклюзионные повязки.
- Крем следует наносить легкими массирующими движениями на пораженный участок 3 раза/сут. Применяемая доза зависит от размера пораженного участка: 1.5-2 г крема (приблизительно соответствует полоске крема длиной 5-7 см).
- Необходимо обратить внимание пациента на то, что при применении препарата без назначения лечащим врачом для лечения повреждений мышц и суставов (растяжений, перенапряжения, ушибов) или тендинита, продолжительность применения не должна превышать 2 недель.
- Продолжительность применения препарата без назначения лечащим врачом для лечения артрита не должна превышать 3 недель.
- Если симптомы ухудшаются или не уменьшаются после 7 дней применения, пациент должен обратиться к врачу с целью дальнейшего обследования.
Противопоказания:
- Повышенная чувствительность к компонентам препарата: к ацеклофенаку или каким-либо из вспомогательных веществ;
- Указание в анамнезе на повышенную чувствительность к другим НПВП (несмотря на то, что возможная перекрестная гиперчувствительность с диклофенаком не была подтверждена, препарат не рекомендован пациентам с гиперчувствительностью к диклофенаку в анамнезе);
- Ацеклофенак, по аналогии с другими НПВП, противопоказан пациентам, у которых ацетилсалициловая кислота или другие НПВП вызывают астматические приступы, крапивницу или острый ринит;
- Наличие инфекции, вызванной вирусом Varicella zoster;
- Беременность;
- Детский возраст до 18 лет;
- Нарушение целостности кожных покровов в месте предполагаемого нанесения.
Меры предосторожности:
- При развитии раздражения в месте нанесения крема необходимо прекратить его применение и провести соответствующее лечение.
- Крем Бристафлам нельзя применять для лечения открытых ран, слизистых оболочек, а также раздражения (экзематозного) кожи или в случаях, когда на коже в месте нанесения крема имеется какой-либо другой патологический процесс. Крем следует наносить только на неповрежденную кожу.
- Для предотвращения реакций фоточувствительности следует защищать участок, на который наносится крем, от воздействия солнечного света.
Побочные эффекты:
- Продемонстрирована хорошая переносимость крема.
- В ряде случаев описано легкое или умеренное местное раздражение, сопровождающееся гиперемией кожи и зудом, которые исчезают при прекращении лечения.
- В редких случаях вирус Varicella zoster в сочетании с лечением НПВП может вызывать серьезные осложнения в форме инфекции кожи и мягких тканей.
Способ хранения:
Хранить при температуре не выше 30 градусов.
Упаковка:
Картонная коробка вмещает тубу по 30 грамм, бумажную инструкцию.
Активное вещество: каждая покрытая пленочной оболочкой таблетка содержит 6,355 мг/12,71 мг/25,42 мг вортиоксетина гидробромида, что эквивалентно 5 мг/10 мг/20 мг вортиоксетина.
Вспомогательные вещества:
Ядро таблетки: маннитол, микрокристаллическая целлюлоза, гидроксипропилцеллюлоза, натрия крахмалгликолят, магния стеарат.
Пленочная оболочка (таблетки, покрытые пленочной оболочкой, 5 мг): гипромеллоза, макрогол 400, титана диоксид (Е 171), железа оксид красный (Е 172).
Пленочная оболочка (таблетки, покрытые пленочной оболочкой, 10 мг): гипромеллоза, макрогол 400, титана диоксид (Е 171), железа оксид желтый (Е 172).
Пленочная оболочка (таблетки, покрытые пленочной оболочкой, 20 мг): гипромеллоза, макрогол 400, титана диоксид (Е 171), железа оксид красный (Е 172).
Таблетки, покрытые пленочной оболочкой, 5 мг:
Таблетки, покрытые пленочной оболочкой, розового цвета, миндалевидной формы, с гравировкой «ТL» на одной стороне и «5» на другой стороне.
Таблетки, покрытые пленочной оболочкой, 10 мг:
Таблетки, покрытые пленочной оболочкой, желтого цвета, миндалевидной формы, с гравировкой «ТL» на одной стороне и «10» на другой стороне.
Таблетки, покрытые пленочной оболочкой, 20 мг:
Таблетки, покрытые пленочной оболочкой, красно-коричневого цвета, миндалевидной формы, с гравировкой «ТL» на одной стороне и «20» на другой стороне.
Психоаналептические средства. Прочие антидепрессанты.
Код АТХ: N06AX26.
Фармакологические свойства
Фармакодинамика
Механизм действия
Предполагается, что механизм действия вортиоксетина связан с его прямым модулированием серотонинергической активности и ингибированием переносчика серотонина (5-НТ). Доклинические исследования показали, что вортиоксетин является антагонистом 5-НТз, 5-НТ7 и 5-НТ1D рецепторов, частичным агонистом в отношении 5-HT1B рецепторов, агонистом в отношении 5-НТ1А рецепторов и ингибитором 5-НТ транспортера, модулируя тем самым нейротрансмиссию в нескольких системах, прежде всего, серотонинергическую, и, вероятно, также и норадренергическую, дофаминергическую, нейротрансмиссию, опосредованную гистамином, ацетилхолином, ГАМК и глутаматом. Такая мультимодальная активность лежит в основе антидепрессивных и анксиолитических свойств вортиоксетина, а также определяет улучшение когнитивных функций, обучения и памяти, наблюдаемые в исследованиях на животных. Однако поскольку вклад индивидуальных объектов в наблюдаемый фармакодинамический профиль вортиоксетина остается неясным, экстраполяция приведенных доклинических данных на человека должна осуществляться с осторожностью.
В двух исследованиях с использованием позитронной эмиссионной томографии (ПЭТ) у людей с целью количественного определения степени занятости переносчиков 5-НТ (с использованием лигандов 11C-MADAM или 11C-DASB) при приеме различных доз вортиоксетина получены следующие данные: среднее количество переносчиков 5-НТ в серотонинергических нейронах ядер шва в мозге, связанных с вортиоксетином, составляло 50% при приеме 5 мг/сут., 65% при приеме 10 мг/сут. и повышалось до 80% при увеличении дозы до 20 мг/cyт.
Клиническая эффективность и безопасность
Эффективность и безопасность вортиоксетина изучались в ряде клинических исследований, включавших более 6700 пациентов, из которых более 3700 принимали вортиоксетин в краткосрочных (≤12 недель) исследованиях при тяжелом депрессивном расстройстве. Двенадцать двойных слепых, плацебо- контролируемых, 6/8 недельных исследований с фиксированными дозами были проведены с целью определения краткосрочной эффективности вортиоксетина при тяжелом депрессивном расстройстве у взрослых пациентов (включая пожилых пациентов). Эффективность вортиоксетина была продемонстрирована, по крайней мере, в группе с применением одной дозы, в 9 из 12 испытаний, где было показано изменение минимально на 2 балла в сравнении с плацебо по шкалам оценки депрессии Монтгомери-Асберг (MADRS) и Гамильтона (НАМ-D24). Это клинически подтверждалось количеством пациентов, ответивших на терапию и достигших ремиссии, а также улучшением по шкале общего клинического впечатления (CGI-I). Эффективность вортиоксетина возрастала при повышении дозы.
Эффективность в отдельных испытаниях подтверждена мета-анализом (MMRM) средних изменений общего балла по шкале оценки депрессии Монтгомери-Асберг на 6/8 неделях в краткосрочных плацебо-контролируемых испытаниях у взрослых. По результатам мета-анализа этих исследований отличия от плацебо были статистически значимы: -2,3 балла (р=0,007), -3,6 балла (р <0,001), -4,6 балла (р <0,001) при приеме 5,10 и 20 мг/сут. соответственно, при приеме 15 мг/сут. статистически значимые различия с плацебо не были достигнуты по данным метаанализа, но средние различия по сравнению с плацебо составили -2,6 балла. Эффективность вортиоксетина подтверждается и в сводном анализе, в котором процент пациентов, у которых был достигнут лечебный эффект, составил от 46% до 49% при применении вортиоксетина по сравнению с 34% в группе плацебо (р <0,01; анализ пациентов, у которых не был достигнут лечебный эффект).
Кроме того, вортиоксетин при приеме в дозах 5-20 мг/сут. продемонстрировал эффективность в отношении широкого спектра симптомов депрессии (изменение баллов по всем отдельным подшкалам оценки депрессии Монтгомери-Асберг).
Эффективность вортиоксетина в дозах 10 или 20 мг/сут. была также продемонстрирована в 12-недельном, двойном слепом, плацебо-контролируемом, с фиксированными дозами сравнительном испытании с агомелатином в дозах 25 или 50 мг/сут. у пациентов с тяжелым депрессивным расстройством. Вортиоксетин продемонстрировал статистически значимое превосходство над агомелатином по общему баллу шкалы оценки депрессии Монтгомери-Асберг, что было и клинически значимо по числу пациентов, ответивших на терапию, достигших ремиссии и улучшения по шкале общего клинического впечатления.
Поддерживающее лечение
Сохранение эффективности антидепрессантной терапии было продемонстрировано в испытании по профилактике рецидивов. Пациенты, находившиеся в ремиссии после первоначального 12-недельного открытого периода терапии вортиоксетином, были рандомизированы в группы, принимающие вортиоксетин 5 или 10 мг/сут. или плацебо. Длительность периода двойного-слепого наблюдения ремиссии составила по меньшей мере 24 недели (от 24 до 64 недель). Вортиоксетин превосходил плацебо (р=0,004) по первичному критерию эффективности и времени, прошедшего до рецидива тяжелого депрессивного расстройства, с отношением рисков 2:0, это означает, что риск рецидива был в два раза выше в группе плацебо, чем в группе вортиоксетина.
Пожилые пациенты
В двойном слепом, плацебо-контролируемом, 8-недельном, с фиксированной дозой испытании у пожилых пациентов с депрессией (старше 65 лет, n=452, 156 из них получали вортиоксетин) вортиоксетин в дозе 5 мг/сут. превосходил плацебо при оценке общего балла по шкалам оценки депрессии Монтгомери-Асберг и Гамильтона. Различия между вортиоксетином и плацебо составили 4,7 балла по шкале оценки депрессии Монтгомери-Асберг на 8-й неделе терапии (анализ смешанной модели с повторными измерениями).
Пациенты с тяжелой депрессией или с депрессией и высоким уровнем тревоги Эффективность вортиоксетина также была продемонстрирована у пациентов с тяжелой депрессией (исходный общий балл по шкале оценки депрессии Монтгомери-Асберг ≥30) и у пациентов с депрессией с сопутствующим высоким уровнем тревоги (исходный общий балл по шкале тревоги Гамильтона ≥20) в краткосрочных испытаниях у взрослых (среднее отличие от плацебо по шкале оценки депрессии Монтгомери-Асберг на неделях 6 и 8 варьировалось от 2,8 до 7,3 баллов и от 3,6 до 7,3 баллов соответственно (анализ смешанной модели с повторными измерениями)). В специальном испытании у пожилых пациентов вортиоксетин также показал свою эффективность.
Сохранение антидепрессивной эффективности у данной популяции пациентов было также продемонстрировано и в долгосрочном испытании по профилактике рецидивов.
Эффекты вортиоксетина на тест замены цифровых символов (Digit Symbol Substitution Test (DSST)), шкалу Калифорнийского университета в Сан-Диего по оценке качества основных жизненных навыков (the University of California San Diego Performance—Based Skills Assessment (UPSA)) (объективная оценка) и опросник оценки когнитивного и физического функционирования (Cognitive and Physical Functioning Questionnaire (CPFQ)) (субъективная оценка).
Эффективность вортиоксетина (5-20 мг/сут.) у пациентов с большим депрессивным расстройством было исследовано в краткосрочных плацебо-контролируемых исследованиях, в 2 из которых участвовали взрослые пациенты и в 1 — пожилые.
Вортиоксетин показал статистически значимый эффект в сравнении с плацебо по тесту замены цифровых символов (DSST) в диапазоне от ∆=1,75 (р=0,019) до 4,26 (р <0,0001) в 2 исследованиях у взрослых и от ∆=2,79 (р=0,023) в исследовании у пожилых людей. В мета-анализе (ANCOVA, LOCF) среднего отклонения от базовой линии в DSST количества правильных символов во всех 3 исследованиях, вортиоксетин отличался от плацебо (р <0,05) со стандартизированной величиной эффекта 0,35. При поправке для отклонений в MADRS общий балл в мета-анализе тех же исследований показал, что вортиоксетин отличался от плацебо (р <0,05) со стандартизированной величиной эффекта 0,24.
В одном исследовании оценивали влияние вортиоксетина на функциональные способности с использованием шкалы Калифорнийского университета в Сан-Диего по оценке качества основных жизненных навыков (UPSA). Вортиоксетин отличался от плацебо статистически с результатами 8,0 для вортиоксетина против 5,1 для группы плацебо (р=0,0003).
В одном исследовании вортиоксетин превосходил плацебо по субъективным показателям, оцененным с использованием опросника дефицита восприятия, с результатами -14,6 для группы вортиоксетина и -10,5 для группы плацебо (р=0,002). Вортиоксетин не отличался от плацебо по субъективным показателям при оценке с помощью опросника оценки когнитивного и физического функционирования с результатами -8,1 для группы вортиоксетина против -6,9 для группы плацебо (р=0,086).
Переносимость и безопасность
Безопасность и переносимость вортиоксетина были установлены в ходе краткосрочных и долгосрочных испытаний при приеме от 5 до 20 мг/сут. Информация о побочных реакциях представлена в разделе «Побочное действие».
Вортиоксетин не повышал частоту возникновения бессонницы или сонливости в сравнении с плацебо.
Симптомы отмены после резкого прекращения применения вортиоксетина систематически оценивались в ходе клинических краткосрочных и долгосрочных плацебо-контролируемых испытаний. Не было выявлено клинически значимой разницы с плацебо в частоте возникновения или характере симптомов при отмене лечения, как после краткосрочной (6-12 недель), так и после долгосрочной (24-64 недель) терапии вортиоксетином.
Частота спонтанных сообщений о побочных реакциях со стороны половой системы была низкой и схожей с плацебо, как в ходе краткосрочных, так и в ходе долгосрочных испытаний. В испытаниях с применением Аризонской шкалы сексуальной функции (ASEX) частота возникновения сексуальной дисфункции, вызванной терапией, и общий балл по Аризонской шкале сексуальной функции не отличалась от плацебо при применении вортиоксетина в дозах 5-15 мг/сут. Доза вортиоксетина 20 мг/сут. привела к увеличению частоты возникновения сексуальных дисфункций, которая оставалась сопоставимой с плацебо (среднее различие в частоте 14,2%, ДИ 95% (1,4; 27,0)).
В краткосрочных и долгосрочных клинических испытаниях вортиоксетин в сравнении с плацебо не влиял на массу тела, частоту сердечных сокращений или артериальное давление.
В клинических испытаниях не наблюдалось клинически значимых изменений оценки функции печени и почек.
Вортиоксетин не продемонстрировал какого-либо клинического значимого влияния на параметры ЭКГ, включая интервалы QT, QTc, PR и QRS, у пациентов с тяжелым депрессивным расстройством. При тщательном исследовании интервала QTc у здоровых участников испытания при приеме вортиоксетина в дозах до 40 мг/сут. удлинение интервала QTc не наблюдалось.
Фармакокинетика
Всасывание
Вортиоксетин медленно, но хорошо всасывается после перорального приема. Максимальная плазменная концентрация достигается через 7-11 ч. После многократного применения в дозах 5, 10 или 20 мг/сут. средняя максимальная плазменная концентрация составляет 9-33 нг/мл. Абсолютная биодоступность — 75%. Прием пищи не оказывает влияние на фармакокинетику лекарственного средства (см. раздел «Способ применения и дозы»).
Распределение
Средний объем распределения (Vss) составляет 2600 л, что свидетельствует об экстенсивном внесосудистом распределении лекарственного средства. Степень связывания вортиоксетина с белками плазмы крови — высокая (98-99%) и, вероятно, не зависит от концентрации вортиоксетина в плазме крови.
Биотрансформация
Вортиоксетин экстенсивно метаболизируется в печени, главным образом путем окисления, катализируемого CYP2D6 и в меньшей степени CYP3A4/5 и CYP2C9, и последующей конъюгации с глюкуроновой кислотой.
Не обнаружено ингибирующего или индуцирующего эффекта вортиоксетина на изоферменты CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 или CYP3A4/5 (см. раздел «Взаимодействие с другими лекарственными средствами»). Вортиоксетин является слабым ингибитором и субстратом Р- гликопротеина.
Основной метаболит вортиоксетина фармакологически неактивен.
Выведение
Средний период полувыведения и клиренс при пероральном приеме лекарственного средства составляют 66 ч и 33 л/ч соответственно.
Приблизительно 2/3 неактивных метаболитов вортиоксетина выводятся с мочой и около 1/3 с калом. Лишь незначительное количество вортиоксетина выводится с калом. Равновесная плазменная концентрация достигается приблизительно через 2 недели.
Линейность/нелинейность
Фармакокинетика носит линейный характер и не зависит от времени в изучавшемся диапазоне доз (2,5-60 мг/сут.).
В соответствии с периодом полувыведения, на основании AUC0-24 после многократного приема 5-20 мг/сут. индекс накопления составляет от 5 до 6.
Особые группы пациентов
Пожилые
У пожилых здоровых участников испытания (возраст ≥65 лет; n=20), экспозиция вортиоксетина увеличивалась до 27% (Сmах и AUC) в сравнении с молодыми здоровыми участниками контрольной группы (возраст ≤45 лет) после многократного приема доз 10 мг/сут. Минимальная эффективная доза вортиоксетина 5 мг/сут. должна всегда использоваться в качестве начальной дозы у пациентов в возрасте ≥65 лет (см. раздел «Способ применения и дозы»). Назначать вортиоксетин пожилым пациентам в дозе выше 10 мг/сут. следует с осторожностью (см. раздел «Меры предосторожности»).
Нарушение функции почек
После однократной дозы вортиоксетина 10 мг нарушение функции почек, оцениваемое по формуле Кокрофта-Голта (легкое, умеренное или тяжелое; n=8 в группе), приводило к небольшому увеличению экспозиции (до 30%), в сравнении со здоровыми участниками контрольной группы. У пациентов с терминальной почечной недостаточностью диализ приводил лишь к незначительному снижению экспозиции (AUC и Сmax снижались на 13% и 27% соответственно; n=8) после однократной дозы вортиоксетина 10 мг. Коррекция дозы не требуется (см. раздел «Меры предосторожности»).
Нарушение функции печени
После приема однократной дозы вортиоксетина 10 мг пациентами с легким или умеренным нарушением функции печени (критерии А или В по Чайлд-Пью; n=8 в группе) изменений фармакокинетики вортиоксетина не наблюдалось (изменение AUC менее чем на 10%). Коррекции дозы не требуется (см. раздел «Способ применения и дозы»). Вортиоксетин не изучался у пациентов с тяжелым нарушением функции печени, поэтому назначать лекарственное средство таким пациентам следует с осторожностью (см. раздел «Меры предосторожности»).
Типы генов изофермента CYP2D6
Плазменная концентрация вортиоксетина была приблизительно в два раза выше у пациентов со сниженной метаболической активностью изофермента CYP2D6 по сравнению с экстенсивными метаболизаторами. В присутствии сильных ингибиторов изоферментов CYP3A4/2C9 экспозиция вортиоксетина потенциально может увеличиться (см. раздел «Взаимодействие с другими лекарственными средствами»),
У пациентов с чрезвычайно быстрым метаболизмом CYP2D6 плазменная концентрация вортиоксетина была в пределах значений, полученных у экстенсивных метаболизаторов при приеме 5 мг/сут. и 10 мг/сут. Как и для всех пациентов, в зависимости от индивидуальной реакции следует рассмотреть возможность коррекции дозы лекарственного средства (см. раздел «Способ применения и дозы»).
Лекарственное средство Бринтелликс показано для лечения депрессивных эпизодов у взрослых.
Режим дозирования
Начальная и рекомендуемая доза Бринтелликса составляет 10 мг вортиоксетина однократно в сутки взрослым до 65 лет.
В зависимости от индивидуального ответа пациента суточная доза может быть увеличена до максимальной 20 мг вортиоксетина однократно, либо снижена до минимальной 5 мг вортиоксетина однократно.
После устранения симптомов депрессии лечение рекомендовано продолжать в течение, по крайней мере, 6 месяцев для закрепления антидепрессивного эффекта.
Прекращение лечения
Пациенты, принимающие Бринтелликс, могут прекратить прием этого лекарственного средства без постепенного снижения дозы (см. раздел: «Фармакодинамика»).
Особые группы пациентов
Пожилые пациенты
Пациентам в возрасте 65 лет и старше в качестве начальной дозы всегда следует назначать минимальную эффективную дозу 5 мг вортиоксетина однократно в сутки. Необходимо соблюдать осторожность при лечении пациентов старше 65 лет с применением доз выше 10 мг вортиоксетина однократно в сутки, так как данные о применении лекарственного средства у таких пациентов ограничены (см. раздел «Меры предосторожности»).
Ингибиторы цитохрома Р450
В зависимости от индивидуальной реакции пациента может потребоваться снижение дозы вортиоксетина в случае добавления терапии сильными ингибиторами изофермента CYP2D6 (например, бупропион, хинидин, флуоксетин, пароксетин) к терапии Бринтелликсом (см. раздел «Взаимодействие с другими лекарственными средствами»).
Индукторы цитохрома Р450
В зависимости от индивидуальной реакции пациента может потребоваться коррекция дозы вортиоксетина в случае добавления терапии сильными индукторами цитохрома Р450 (например, рифампицин, карбамазепин, фенитоин) к терапии Бринтелликсом (см. раздел «Взаимодействие с другими лекарственными средствами»).
Дети
Безопасность и эффективность лекарственного средства Бринтелликс у детей и подростков в возрасте до 18 лет не установлена. Данные отсутствуют (см. раздел «Меры предосторожности»).
Способ применения
Бринтелликс предназначен для перорального применения.
Таблетки, покрытые пленочной оболочкой, можно принимать вне зависимости от приема пищи.
Наиболее частой нежелательной реакцией была тошнота. Нежелательные реакции обычно были слабо или умеренно выраженными и отмечались на протяжении первых двух недель лечения. Нежелательные реакции обычно носили временный характер и, в общем, не являлись причиной отмены лекарственного средства. Нежелательные реакции со стороны пищеварительной системы, такие как тошнота, наблюдались чаще у женщин.
Нежелательные реакции, перечисленные ниже, распределены по частоте следующим образом: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000), неизвестно (имеющиеся данные не позволяют провести оценку).
Нарушения психики
Часто: необычные сновидения.
Нарушения со стороны нервной системы
Часто: головокружение.
Неизвестно: серотониновый синдром.
Нарушения со стороны сосудов
Нечасто: приливы.
Нарушения со стороны желудочно-кишечного тракта
Очень часто: тошнота.
Часто: диарея, запор, рвота.
Нарушения со стороны кожи и подкожных тканей
Часто: зуд, включая генерализованный.
Нечасто: ночная потливость.
Описание отдельных побочных реакций
Пожилые пациенты
При приеме ≥10 мг вортиоксетина один раз в сутки уровень выбывания из испытаний был выше у пациентов в возрасте ≥65 лет.
При приеме 20 мг вортиоксетина один раз в сутки случаев возникновения тошноты и запоров было больше у пациентов в возрасте ≥65 лет (42% и 15%, соответственно) по сравнению с пациентами <65 лет (27% и 4%, соответственно) (см. раздел «Меры предосторожности»).
Сексуальная дисфункция
В клинических испытаниях сексуальная дисфункция оценивалась с использованием Аризонской шкалы сексуальной функции. Дозы от 5 до 15 мг не демонстрировали отличия от плацебо. Однако доза 20 мг вортиоксетина ассоциировалась с возникающей во время лечения сексуальной дисфункцией (см. раздел «Фармакодинамика»).
Класс-специфический эффект
Эпидемиологические исследования преимущественно с участием пациентов в возрасте 50 лет и старше показали повышенный риск переломов у пациентов, принимающих лекарственные средства, относящиеся к соответствующим фармакологическим классам антидепрессантов (СИОЗС и ТЦА). Механизм, приводящий к этому риску, неизвестен, также как неизвестно, существует ли данный риск при приеме вортиоксетина.
Гиперчувствительность к действующему веществу или к какому-либо из вспомогательных веществ (см. раздел «Состав»).
Одновременное применение с неселективными ингибиторами моноаминоксидазы (ИМАО) или селективными ингибиторами МАО-А (см. раздел «Взаимодействие с другими лекарственными средствами»).
Опыт передозировок вортиоксетина ограничен.
Прием внутрь вортиоксетина в дозах 40-75 мг приводил к усилению следующих побочных реакций: тошнота, постуральное головокружение, диарея, неприятные ощущения в животе, генерализованный зуд, сонливость и приливы.
В случае возникновения передозировки необходимо проводить симптоматическое лечение и установить наблюдение за пациентом. Также рекомендуется осуществлять последующее медицинское наблюдение в специализированном медицинском учреждении.
Применение у детей
Бринтелликс не рекомендуется применять для терапии депрессий у пациентов, не достигших возраста 18 лет, поскольку безопасность и эффективность лекарственного средства в данной возрастной группе не была установлена (см. раздел «Способ применения и дозы»). В клинических испытаниях у детей и подростков, получавших другие антидепрессанты, чаще наблюдалось суицидальное поведение (суицидальные попытки и суицидальные мысли) и враждебность (главным образом, агрессия, оппозиционное поведение и гнев) в сравнении с получавшими плацебо.
Суицид/суицидальные мысли или клиническое ухудшение
Депрессия связана с повышенным риском возникновения суицидальных мыслей, нанесения себе вреда и совершения суицида (суицидальных действий и проявлений). Этот риск присутствует до возникновения стойкой ремиссии. Поскольку улучшение может не наблюдаться в течение первых нескольких недель лечения и более, за пациентами необходимо тщательно наблюдать до появления улучшения. Согласно общему клиническому опыту риск суицида может повышаться на ранних стадиях выздоровления.
Пациенты с суицидальными действиями и проявлениями в анамнезе или те, у которых наблюдается значительная выраженность суицидального мышления до начала лечения, находятся в группе повышенного риска возникновения суицидальных мыслей и суицидальных попыток, и должны тщательно наблюдаться в период лечения. Мета-анализ плацебо-контролируемых клинических испытаний антидепрессантов у взрослых пациентов с психическими расстройствами выявил повышенный риск суицидального поведения у пациентов, принимающих антидепрессанты, в сравнении с плацебо, среди пациентов в возрасте до 25 лет.
Пациенты должны находиться под строгим наблюдением, в частности пациенты с высоким суицидальным риском, особенно в начале лечения или при изменении дозы лекарственного средства. Пациенты (и лица, осуществляющие уход за ними) должны быть предупреждены о необходимости отслеживать признаки любого клинического ухудшения, возникновения суицидальных мыслей или поведения, необычных изменений в поведении, и в случае возникновения подобных симптомов срочно обращаться за медицинской помощью.
Судороги
Существует возможный риск развития судорог при применении антидепрессантов. Поэтому Бринтелликс необходимо применять с осторожностью у пациентов с судорогами в анамнезе или у пациентов с нестабильной эпилепсией (см. раздел «Взаимодействие с другими лекарственными средствами»). Лечение необходимо прекратить у любого пациента, у которого развиваются судороги или наблюдается увеличение частоты судорожных припадков.
Серотониновый синдром (СС) или злокачественный нейролептический синдром (ЗНС)
Серотониновый синдром (СС) или злокачественный нейролептический синдром (ЗНС) являются потенциально угрожающими жизни состояниями и могут возникать на фоне применения лекарственного средства Бринтелликс. Риск возникновения СС или ЗНС повышается при совместном применении с серотонинергическими препаратами (в том числе триптанами), препаратами, нарушающими катаболизм серотонина (включая ИМАО), антипсихотиками либо другими антагонистами дофамина. Пациентов необходимо наблюдать на предмет возникновения симптомов СС и ЗНС (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными средствами»).
Симптомы серотонинового синдрома включают в себя изменения психического состояния (например, ажитация, галлюцинации, кома), расстройства вегетативной нервной системы (например, тахикардия, лабильность артериального давления, гипертермия), нервно-мышечные расстройства (например, гиперрефлексия, нарушение координации) и/или симптомы со стороны желудочно-кишечного тракта (например, тошнота, рвота, диарея). В случае возникновения таких симптомов следует немедленно прекратить терапию Бринтелликсо и начать симптоматическое лечение.
Мания/гипомания
Бринтелликс следует применять с осторожностью у пациентов с манией/гипоманией в анамнезе. Лекарственное средство следует отменить у любого пациента, у которого развивается маниакальная фаза.
Кровотечение
На фоне применения антидепрессантов с серотонинергическим действием (СИОЗС, СИОЗСН) описаны редкие случаи нарушения гемостаза, такие как экхимозы, пурпура, желудочно-кишечные и гинекологические кровотечения. Лекарственное средство рекомендуется применять с осторожностью у пациентов, принимающих антикоагулянты и/или препараты, влияющие на функцию тромбоцитов (например, атипичные антипсихотики, фенотиазины, большинство трициклических антидепрессантов, нестероидные противовоспалительные средства (НПВС) и ацетилсалициловая кислота) (см. раздел «Взаимодействие с другими лекарственными средствами») и у пациентов, предрасположенных к кровотечениям.
Гипонатриемия
На фоне применения антидепрессантов с серотонинергическим действием (СИОЗС и СИОЗСН) сообщалось о редких случаях гипонатриемии, вероятно, вследствие синдрома неадекватной секреции антидиуретического гормона. Пациентам с факторами риска, т.е. пожилым пациентам, пациентам с циррозом печени или пациентам, одновременно принимающим лекарственные средства, вызывающие гипонатриемию, следует соблюдать осторожность.
Следует рассмотреть прекращение приема Бринтелликса у пациентов с симптоматической гипонатриемией и принять соответствующие меры.
Пожилые пациенты
Данные применения Бринтелликса у пожилых пациентов с тяжелыми депрессивными эпизодами ограничены. Поэтому необходимо соблюдать осторожность при терапии пациентов в возрасте 65 лет и старше с использованием доз выше 10 мг вортиоксетина один раз в сутки (см. разделы «Побочное действие» и «Фармакокинетика»).
Нарушение функции почек
Данные применения лекарственного средства у пациентов с тяжелым нарушением функции почек ограничены, поэтому при назначении таким пациентам следует соблюдать осторожность (см. раздел «Фармакокинетика»).
Нарушение функции печени
Вортиоксетин не изучался у пациентов с тяжелым нарушением функции печени, поэтому при назначении таким пациентам следует соблюдать осторожность (см. раздел «Фармакокинетика»).
Беременность и лактация
Беременность
Данные о применении вортиоксетина беременными женщинами ограничены. Исследования на животных выявили репродуктивную токсичность.
У новорожденных, матери которых получают серотонинергические препараты на поздних сроках беременности, могут наблюдаться следующие симптомы: респираторный дистресс, цианоз, апноэ, судороги, нестабильность температуры, трудности с приемом пищи, рвота, гипогликемия, гипертония, гипотония, гиперрефлексия, тремор, синдром повышенной нервно-рефлекторной возбудимости, раздражительность, летаргия, постоянный плач, сонливость и нарушение сна. Данные симптомы могут быть связаны как с синдромом отмены, так и с избыточной серотонинергической активностью. В большинстве случаев подобные симптомы начинаются немедленно, либо вскоре (<24 часов) после рождения.
Эпидемиологические данные позволяют предположить, что применение СИОЗС во время беременности, особенно на поздних сроках, может повысить риск возникновения персистирующей легочной гипертензии у новорожденных. Хотя на сегодняшний день возможность взаимосвязи данного состояния с применением вортиоксетина не изучалась, принимая во внимание механизм его действия (повышение концентрации серотонина) возможный риск не может быть исключен. Бринтелликс не должен применяться во время беременности, если того не требует клиническое состояние женщины.
Период грудного вскармливания
Доступные данные, полученные в исследованиях на животных, свидетельствуют о том, что вортиоксетин и его метаболиты проникают в грудное молоко. Вероятно, вортиоксетин также выделяется с грудным молоком у человека.
Риск для ребенка при грудном вскармливании не может быть исключен. Решение о прекращении грудного вскармливания или прекращении/перерыве в применении Бринтелликса должно приниматься с учетом оценки относительной пользы грудного вскармливания для ребенка и необходимости терапии для матери.
Фертильность
Исследования фертильности на самцах и самках крыс показали, что вортиоксетин не оказывает влияния на фертильность, качество спермы или способность к спариванию.
Случаи применения у человека лекарственных средств, относящихся к соответствующему фармакологическому классу антидепрессантов (СИОЗС) показали наличие воздействия на качество спермы, которое носит обратимый характер. Влияние на фертильность человека на настоящий момент не наблюдалось.
Влияние на способность управлять транспортными средствами и механизмами
Бринтелликс не оказывает или оказывает очень незначительное влияние на способность управлять автомобилем или механизмами. Тем не менее, пациенты должны соблюдать осторожность при управлении транспортными средствами или опасными механизмами, особенно в начале лечения вортиоксетином или при изменении дозы.
Вортиоксетин подвергается экстенсивному метаболизму в печени главным образом за счет окисления, катализируемого изоферментом CYP2D6, и в меньшей степени — CYP3A4/5 и CYP2C9 (см. раздел «Фармакокинетика»).
Возможное влияние других лекарственных средств на вортиоксетин
Необратимые неселективные ингибиторы МАО
В связи с риском развития серотонинового синдрома вортиоксетин противопоказано применять в комбинации с необратимыми неселективными ингибиторами МАО. Вортиоксетин может быть назначен не ранее, чем через 14 дней после отмены необратимых неселективных ингибиторов МАО. Вортиоксетин необходимо отменить не менее чем за 14 дней до начала применения необратимых неселективных ингибиторов МАО (см. раздел «Противопоказания»).
Обратимый селективный ингибитор МАО-А (моклобемид)
Одновременное применение вортиоксетина с обратимыми селективными ингибиторами МАО-А, например, моклобемидом, противопоказано (см. раздел «Противопоказания»). В случае доказанной необходимости одновременного применения добавляемое лекарственное средство должно применяться в минимальных дозах при тщательном клиническом контроле симптомов развития серотонинового синдрома (см. раздел «Меры предосторожности»).
Обратимый неселективный ингибитор МАО (линезолид)
Комбинация вортиоксетина со слабым обратимым и неселективным ингибитором МАО, например, антибиотиком линезолидом, противопоказана (см. раздел «Противопоказания»). В случае доказанной необходимости одновременного применения добавляемое лекарственное средство должно применяться в минимальных дозах при тщательном клиническом контроле симптомов развития серотонинового синдрома (см. раздел «Меры предосторожности»).
Необратимые селективные ингибиторы МАО-В (селегилин, разагилин)
Хотя риск возникновения серотонинового синдрома при одновременном применении вортиоксетина и селективных ингибиторов МАО-В ниже, чем при одновременном применении вортиоксетина и селективных ингибиторов МАО-А, комбинированное применение вортиоксетина с необратимыми ингибиторами МАО-В такими, как селегилин или разагилин, должно осуществляться с осторожностью. В случае одновременного применения необходим тщательный контроль симптомов развития серотонинового синдрома (см. раздел «Меры предосторожности»).
Серотонинергические препараты
Одновременное применение лекарственных средств с серотонинергическим эффектом (например, трамадол, суматриптан и другие триптаны) может привести к развитию серотонинового синдрома (см. раздел «Меры предосторожности»).
Зверобой продырявленный
Одновременное применение антидепрессантов с серотонинергическим эффектом с растительными препаратами, содержащими зверобой продырявленный (Hypericum perforatum) может привести к увеличению частоты возникновения побочных реакций, включая серотониновый синдром (см. раздел «Меры предосторожности»).
Препараты, снижающие порог судорожной готовности
Антидепрессанты с серотонинергическим эффектом могут снижать порог судорожной готовности. Одновременное применение с лекарственными средствами, снижающими порог судорожной готовности (например, антидепрессантами (ТЦА, СИОЗС, СИОЗСН), нейролептиками (фенотиазины, тиоксантены, бутирофеноны), мефлохином, бупропионом, трамадолом) должно назначаться с осторожностью (см. раздел «Меры предосторожности»).
ЭСТ (электросудорожная терапия)
В настоящее время клинический опыт одновременного применения вортиоксетина и ЭСТ отсутствует, поэтому рекомендуется соблюдать осторожность.
Ингибиторы цитохрома CYP2D6
Экспозиция вортиоксетина возросла в 2,3 раза при определении по показателю площадь под кривой (AUC) при применении в дозе 10 мг/сут. одновременно с бупропионом (сильным ингибитором CYP2D6) в дозе 150 мг два раза в сутки в течение 14 дней у здоровых участников испытания. Побочные реакции чаще наблюдались при добавлении бупропиона к текущей терапии вортиоксетином, чем при добавлении вортиоксетина к текущей терапии бупропионом. В зависимости от индивидуальной реакции пациента при добавлении к текущей терапии вортиоксетином сильного ингибитора CYP2D6 (например, бупропиона, хинидина, флуоксетина, пароксетина) следует рассмотреть возможность снижения дозы вортиоксетина (см. раздел «Способ применения и дозы»).
Ингибиторы цитохрома CYP3A4 и CYP2C9
Добавление вортиоксетина через 6 дней после начала приема кетоконазола в дозе 400 мг/сут. (ингибитор CYP3A4/5 и Р-гликопротеина) или через 6 дней после начала приема флуконазола в дозе 200 мг/сут. (ингибитор CYP2C9, CYP2C19 и CYP3A4/5) у здоровых участников испытания, экспозиция (AUC) вортиоксетина возросла в 1,3 и 1,5 раза соответственно. Коррекция дозы не требуется.
Взаимодействие у медленных метаболизаторов CYP2D6
Применение вортиоксетина одновременно с сильными ингибиторами изофермента CYP3A4 (такими как итраконазол, вориконазол, кларитромицин, телитромицин, нефазодон, кониваптан и многими ингибиторами протеазы ВИЧ) и изофермента CYP2C9 (такими как флуконазол и амиодарон) у медленных метаболизаторов CYP2D6 (см. раздел «Фармакокинетика») специально не исследовалось, однако, в данном случае можно ожидать, что у таких пациентов это приведет к более выраженной экспозиции вортиоксетина по сравнению с описанным выше умеренным действием.
Введение однократной дозы омепразола 40 мг (ингибитор CYP2C19) на фоне многократных доз вортиоксетина не изменяло фармакокинетику последнего у здоровых участников испытания.
Индукторы цитохрома Р450
При введении однократной дозы вортиоксетина 20 мг через 10 дней после начала применения рифампицина в дозе 600 мг/сут. (сильный индуктор изоферментов CYP) у здоровых участников испытания, AUC вортиоксетина снизилась на 72%. В зависимости от индивидуальной реакции пациента при добавлении к терапии вортиоксетином сильного индуктора изоферментов цитохрома Р450 (например, рифампицина, карбамазепина, фенитоина) следует рассмотреть возможность коррекции дозы вортиоксетина (см. раздел «Способ применения и дозы»).
Алкоголь
При одновременном введении однократных доз вортиоксетина (20 мг и 40 мг) и этанола (0,6 г/кг) здоровым участникам испытания не наблюдалось влияния на фармакокинетику вортиоксетина или этанола и значимого нарушения когнитивных функций в сравнении с плацебо. Однако во время терапии антидепрессантами прием алкоголя не рекомендуется.
Ацетилсалициловая кислота
Многократный прием ацетилсалициловой кислоты в дозе 150 мг/сут. не изменял фармакокинетику многократных доз вортиоксетина у здоровых участников испытания.
Возможное влияние вортиоксетина на другие лекарственные средства
Антикоагулянты и антиагреганты
Не наблюдалось значимого влияния вортиоксетина в сравнении с плацебо на МНО, протромбин или соотношение R-/S-варфарина в плазме крови при одновременном применении многократных доз вортиоксетина с фиксированной дозой варфарина у здоровых участников испытания. Также не наблюдалось значимого ингибирующего влияния вортиоксетина на агрегацию тромбоцитов и фармакокинетику ацетилсалициловой и салициловой кислоты в сравнении с плацебо при одновременном применении ацетилсалициловой кислоты в дозе 150 мг/сут. на фоне многократных доз вортиоксетина у здоровых участников испытания. Тем не менее, как и в случае других серотонинергических препаратов следует соблюдать осторожность при одновременном применении вортиоксетина и пероральных антикоагулянтов/антиагрегантов в связи с потенциальным риском развития кровотечений, вызванных фармакодинамическим взаимодействием (см. раздел «Меры предосторожности»).
Субстраты цитохрома Р450
В исследованиях in vitro не было выявлено способности вортиоксетина ингибировать или индуцировать изоферменты системы цитохрома Р450 (см. раздел «Фармакокинетика»).
После приема многократных доз вортиоксетина не было обнаружено ингибирующего действия на активность изоферментов системы цитохрома Р450 CYP2C19 (омепразол, диазепам), CYP3A4/5 (этинилэстрадиол, мидазолам), CYP2B6 (бупропион), CYP2C9 (толбутамид, S-варфарин), CYP1A2 (кофеин) или CYP2D6 (декстрометорфан) у здоровых участников испытания.
Фармакодинамические взаимодействия не наблюдались. Не было обнаружено значимого нарушения когнитивных функций в сравнении с плацебо при введении вортиоксетина в комбинации с однократной дозой диазепама 10 мг. Не было обнаружено значимого влияния вортиоксетина в сравнении с плацебо на уровень половых гормонов после его введения совместно с комбинированным оральным контрацептивом (этинилэстрадиол 30 мкг + левоноргестрел 150 мкг).
Литий, триптофан
У здоровых участников испытания не было выявлено каких-либо клинически значимых изменений при равновесной экспозиции лития после одновременного применения лития и многократных доз вортиоксетина. Тем не менее, в связи с тем, что были описаны случаи усиления эффекта серотонинергических антидепрессантов при одновременном их применении с препаратами лития или триптофана, одновременное применение вортиоксетина с этими препаратами должно осуществляться с осторожностью.
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 5 мг, 10 мг и 20 мг.
По 14 таблеток, покрытых пленочной оболочкой, в блистере из ПВХ/ПВДХ и фольги алюминиевой. 1 или 2 блистера с инструкцией по применению в картонную пачку.
Хранить при температуре не выше 30°С. Хранить в местах, недоступных для детей.
4 года.
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту врача.
Название и адрес производителя
X. Лундбек А/О
Оттилиавай 9
DK-2500 Вальбю
Дания
Агентство в РБ
г. Минск, ул. В. Хоружей, 22-1402.
Тел.: (+375 17) 283 16 33, факс: (+375 17) 283 16 40.
Частое повышение показателей артериального давления (АД) – причина развития серьезных заболеваний (инсульт, инфаркт миокарда и пр.). Гипертоническая болезнь в России диагностируется у каждого третьего человека преклонного возраста. Для борьбы с гипертонией многим пациентам приходится принимать препараты на протяжении всей жизни, чтобы исключить осложнения.
Современные фармакологические компании предлагают большой выбор лекарственных средств, эффективных при гипертонии. Если не знаете, как выбрать таблетки от повышенного давления, ознакомьтесь с рейтингом, представленным ниже. В ТОП вошли лучшие медикаменты с учетом эффективности, стоимости и отзывов.
Классификация препаратов от повышенного давления
В зависимости от достигаемого эффекта, лекарства от АД делятся на следующие группы:
- АПФ (ингибиторы ангиотензин-превращающего фермента). Препятствуют выработке ангиотензина (вещества обладающего сосудосуживающим эффектом). Расширяют артерии, снижая АД.
- БРА (блокаторы рецепторов ангиотензина II). Ингибируют те рецепторы, с которыми связывается ангиотензин, расширяя сосуды и снижая АД.
- Антагонисты кальция/блокаторы кальциевых каналов. Предотвращают проникновение ионов кальция в клетки сосудов и миокарда (сердечной мышцы), предотвращая механизмы сокращения. Артерии расслабляются, что приводит к увеличению их диаметра и снижению АД.
- Мочегонные (диуретики). Нормализуют показатели АД, выводя излишки жидкостей и солей из организма. Петлевые диуретики назначаются преимущественно в стационарных условиях.
- Бета-адреноблокаторы. Уменьшают сердечную нагрузку, нормализуя объем крови, выбрасываемый сердцем. Достигает должных показателей АД и поддерживает их на определенном уровне.
Назначение нескольких таблеток из различных групп дает возможность снизить суточную дозировку, обеспечив синергическое (взаимодополняющее) действие между ними. Существуют схемы, предполагающие однократный прием препаратов в течение дня, что незаменимо для большинства пациентов. Гипертоники нуждаются в пожизненном лечении, поэтому комбинации средств являются более актуальными, т. к. практически полностью исключают побочные реакции и негативное воздействие на внутренние органы и системы.
Причины гипертонии
Развивается на фоне следующих заболеваний:
- болезни почек и надпочечников;
- патологии щитовидной железы;
- атеросклероз и коарктация (стеноз) аорты.
Среди предрасполагающих факторов следует выделить нервные перенапряжения, употребление большого количества соленых продуктов, наследственную предрасположенность. Женщины сталкиваются с гипертонией в климактерическом периоде. Провоцирующими факторами является алкоголизм, курение и возраст (от 60-65 лет и старше).
Когда нужно вызвать врача на дом при повышении давления?
Общепринятые показатели АД – 120/80. Параметры могут незначительно варьировать в зависимости от времени суток, физической активности и возраста человека.
Таблица – Показатели артериального давления и рекомендации
|
Категория АД |
Систолическое, мм рт. ст. |
Диастолическое, мм рт. ст. |
Какие меры нужно принять |
|
Гипотония |
…100 |
…60 |
проконсультироваться с врачом |
|
Оптимальное |
100…120 |
60…80 |
самоконтроль |
|
Допустимое |
120…130 |
80…85 |
самоконтроль |
|
Высокое |
130…140 |
85…90 |
коррекция образа жизни |
|
Умеренная гипертония |
140…160 |
90…100 |
незамедлительная консультация специалиста |
|
Средняя тяжесть гипертонии |
160…180 |
100…110 |
незамедлительная консультация специалиста |
|
Тяжелая гипертония |
180… |
110… |
незамедлительная консультация специалиста |
Необходимость во врачебной помощи возникает, если показатели отклоняются на 15 единиц и более, и при этом присутствуют следующие симптомы:интенсивная и давящая головная боль;
- снижение зрения и появление черных точек перед глазами;
- появление шума в ушах;
- осложнение дыхания и появление хрипов;
- наличие болезненного дискомфорта в области сердца;
- онемение языка и лицевых мышц;
- появление тошноты, сопровождаемой рвотой;
- чрезмерная сухость в ротовой полости;
- нарушение речевой способности;
- ощущение чувства сильного сердцебиения в висках и в конечностях.
Если вовремя не принять мер, то есть риск развития таких осложнений, как инсульт, атеросклероз, ретинопатия, сердечная недостаточность, инфаркт миокарда, микроальбуминурия и почечная недостаточность.
При развитии гипертонического криза необходимо оказать помощь как можно быстрее:
- осложненная форма – в течение часа;
- неосложненная форма – на протяжении суток;
- гипертонический рецидив – незамедлительно.
При отсутствии медицинской помощи гипертонический приступ осложняется необратимыми функциональными нарушениями внутренних органов. Люди, которые страдают гипертонией, должны заранее позаботиться о возможных осложнениях болезни проще принять меры для того, чтобы их предотвратить.
Рейтинг препаратов против гипертонии
Предлагаем ознакомиться с информацией о том, какие таблетки лучше от повышенного давления в том или ином случае. Чтобы выбрать наиболее подходящее средство, следует опираться на имеющиеся показания и свойства медикамента.
ТОП лекарств от повышенного давления
Многие интересуются, существуют ли безопасные препараты для понижения АД. К большому сожалению, подобных лекарств еще разработано не было. Но лучше всего отдавать предпочтение препаратам нового поколения, которые практически не имеют побочных эффектов. Благодаря технологиям нового времени удалось разработать максимально действенные средства, подходящие к проблеме комплексно.
Обратите внимание, что артериальная гипертензия требует комплексного подхода к лечению. Для назначения эффективной и безопасной терапии важно знать не только особенности организма пациента, но и взаимодействие лекарственных средств.
№1 – «Небиволол-Тева» (Teva, Венгрия)
Обладает мягким сосудорасширяющим действием. Снижает частоту сердечных сокращений и нормализует показатели АД при нагрузке и в состоянии покоя. Улучшает диастолическую функцию сердца, увеличивая фракцию выброса.
Назначается при гипертензии и стабильной сердечной недостаточности хронического типа. Беременным женщинам назначается только при наличии жизненных показаний. При лечении необходим контроль пациентов, сначала ежедневный, потом 1 раз в 3-4 месяца.
№2 – «Небилет» (Berlin-Chemie/A. Menarini, Германия)
Бета-адреноблокатор III поколения обладает вазодилатирующими (закономерными физиологическими реакциями сосудов на оказываемое воздействие) свойствами.
Способствует развитию устойчивого гипотензивного действия через 1 или 2 недели от начала приема. Считается лучшим лекарством от повышенного давления благодаря тому, что снижает потребность сердечной мышцы в кислороде и урежению ЧСС. Уменьшает тяжесть и количество приступов стенокардии, а также повышает переносимость физических нагрузок.
№3 – «Эдарби» (Takeda, Япония)
Антагонист рецепторов ангиотензина II является пролекарством (химически модифицированной формой лекарственного средства, которая в биосреде превращается в активную молекулу азилсартана). Преимуществом является отсутствие синдрома отмены.
Является лучшим лекарством от повышенного давления для пожилых. Таблетки показаны для приема при эссенциальной гипертензии. Терапия должна быть ежедневной и непрерывной. При отмене следует уведомить об этом врача.
№4 – «Эдарби» (Takeda, Ирландия)
Специфический антагонист рецепторов ангиотензина II, разработанный на основе азилсартана медоксомила. Эффективность и безопасность препарата не зависит от возраста пациента.
Антигипертензивный результат наблюдается в течение первых 2-х недель применения. Стойкий терапевтический эффект наблюдается уже через месяц от начала приема. Доза корректируется в зависимости от возраста и показаний.
№5 – «Лозартан» (Вертекс, Россия)
Блокирует рецепторы АТ1, предотвращая или устраняя сосудосуживающее действие ангиотензина II, а также его стимулирующее влияние на функции надпочечников. Лозартан быстро абсорбируется в желудочно-кишечном тракте. Его биодоступность находится в пределах 33%.
«Лозартан» лучше принимать от повышенного давления при первичной гипертензии и застойной сердечной недостаточности. Отличается длительным действием – более 24 часов.
№6 – «Лозартан» (Канонфарма продакшн ЗАО, Россия)
Разработан на основе одноименного активного вещества – лозартана. Назначается при первичной гипертензии, в случае сердечной недостаточности застойного типа и при гломерулярном поражении, характерном для сахарного диабета.
Основные фармакологические характеристики:
- связывается с рецепторами, которые находятся в сосудах, сердце, надпочечниках и в почках;
- выполняют такие важные биологические функции, как высвобождение альдостерона и вазоконстрикцию (сужение просвета кровеносных сосудов);
- стимулирует разрастание гладкомышечных клеточных структур.
Антигипертензивное действие достигается уже через 6 часов после однократного приема – снижаются систолические и диастолические показатели. Эффективность снижается постепенно в течение суток.
№7 – «Лозап» (Zentiva, Словацкая Республика)
Действующее вещество – лозартан калия. Ангиотензин II представляет собой мощный вазоконстриктор и основное патофизиологическое звено артериальной гипертензии. Активный компонент не ингибирует АПФ, приводящий к деградации брадикинина (пептида, расширяющего кровеносные сосуды) и развитию отеков.
«Лозап» — это лучшие таблетки от повышенного давления, устраняющие отрицательную обратную связь, которая заключается в подавлении секреции ренина, регулирующего кровяное давление. Назначается для снижения риска развития сердечно-сосудистых нарушений и при хроническом заболевании почек.
№8 – «Лозап» (Zentiva, Чешская Республика)
При прохождении терапии устраняется отрицательная обратная связь , направленная на подавление ренина. Антигипертензивная активность отмечается на 2-6 неделю лечения, что свидетельствует о, эффективной блокаде рецепторов ангиотензина II (гормона, повышающего кровяное давление).
Лекарство нового поколения от повышенного давления практически не имеет данных передозировке. При беременности не используется, т. к. присутствуют риски для развития плода. Побочные действия являются проходящими, поэтому при их возникновении нет необходимости в прекращении лечения.
№9 – «Физиотенз» (Нобел Алматинская Фармацевтическая фабрика АО, Казахстан)
Гипотензивное средство является альфа 2-адреномиметиком центрального действия. Пожилым пациентам рекомендуется принимать с осторожностью, т. к. возможно изменение фармакокинетики, что связано с повышенной биодоступностью и недостаточной метаболической активностью. Клиническая значимость при этом отсутствует.
Препарат воздействует на центральную нервную систему, селективно стимулируя рецепторы головного мозга. Благодаря снижению активности симпатической нервной системы происходит снижение показателей кровяного давления.
№10 – «Норваск» (Pfizer, Германия)
Блокатор кальциевых каналов, который разработан на основе амлодипина. Обладает выраженным антигипертензивным и антиангинальным действием. Снижает переход ионов кальция в гладкомышечные клетки сосудов.
Эффективность таблеток «Новарск»:
- при стенокардии уменьшает ишемию миокарда;
- уменьшает постнагрузку на сердце;
- снижает ОПСС (общее периферическое сопротивление сосудов);
- расширяет периферические артериолы;
- уменьшает потребность сердечной мышцы в кислороде.
Препарат повышает физическую выносливость и минимизирует частоту приступов стенокардии. Это исключает необходимость в использовании нитроглицерина.
№11 – «Моксонидин» (Северная звезда ЗАО, Россия)
Агонист имидазолиновых рецепторов обладает центральным действием. Селективно стимулирует в стволовых структурах мозга рецепторы, которые участвуют в рефлекторной и тонической регуляции симпатической нервной системы.
Самые лучшие таблетки от повышенного давления при артериальной форме гипертензии. Нет необходимости в коррекции начальной дозы для пациентов, страдающих почечной недостаточностью. Передозировка не опасна для жизни. Для восстановления оптимальных показателей в этом случае инъекционно вводится допамин.
Выводы
Список лучших таблеток от повышенного давления рекомендуется использовать в ознакомительных целях. При артериальной гипертензии самолечение недопустимо.
Эффективные лекарства нового поколения от повышенного давления может назначить только врач. Специалист проведет обследование, учтет результаты анализов и индивидуальные особенности организма больного. Предварительная консультация с врачом является обязательной мерой для предотвращения развития серьезных для здоровья и жизни осложнений.
Список литературы:
https://www.eurolab.ua/hypertension-high-blood-pressure/2246/16996
https://www.rlsnet.ru/mkb_index_id_3669.htm
https://www.vidal.ru/encyclopedia/zabolevaniya-serdechno-sosudistoyi-sistemi-kardiologiya/arterialna…
https://cyberleninka.ru/article/n/sovremennye-napravleniya-medikamentoznoy-terapii-arterialnoy-giper…
Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Флурбипрофен
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Флурбипрофен
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Флурбипрофен
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Торговые названия с действующим веществом Флурбипрофен
Структурная формула
Русское название
Флурбипрофен
Английское название
Flurbiprofen
Латинское название
Flurbiprophenum (род. Flurbipropheni)
Химическое название
2-Фтор-альфа-метил[1,1′-бифенил]-4-уксусная кислота
Брутто формула
C15H13FO2
Фармакологическая группа вещества Флурбипрофен
Нозологическая классификация
Код CAS
5104-49-4
Фармакологическое действие
—
анальгезирующее, противовоспалительное.
Характеристика
НПВС. Производное фенилпропионовой кислоты.
Фармакология
Ингибирует обе изоформы циклооксигеназы (ЦОГ-1 и ЦОГ-2), блокирует реакции арахидонового каскада и нарушает синтез простагландинов и тромбоксана A2.
При использовании таблеток для рассасывания, а также лекарственных форм для перорального приема хорошо и полностью всасывается. Cmax в плазме крови достигается через 90 мин (лекарственные формы для приема внутрь) или через 30–40 мин (таблетки для рассасывания). Абсорбировавшаяся часть флурбипрофена связывается с белками плазмы более чем на 90%, метаболизируется в печени путем гидроксилирования и выводится почками в основном в виде метаболитов и в неизмененном виде (около 20%). T1/2 — 3–6 ч. При использовании лекарственной формы флурбипрофена для рассасывания действие наступает через 30 мин после начала рассасывания таблетки в ротовой полости и продолжается 2–3 ч.
Показана эффективность флурбипрофена в различных лекарственных формах при следующих заболеваниях и состояниях: ревматоидный артрит, остеоартрит, анкилозирующий спондилоартрит, острый бурсит, тендинит, суставной синдром при обострении подагры; болевой синдром слабой и средней интенсивности: артралгия, миалгия, невралгия, мигрень, зубная и головная боль, альгодисменорея, травмы, ожоги; лихорадочный синдром.
Применение вещества Флурбипрофен
Для облегчения боли в горле при инфекционно-воспалительных заболеваниях полости рта и глотки (в качестве симптоматического средства).
Противопоказания
Гиперчувствительность, обострение эрозивно-язвенных поражений ЖКТ (язвенная болезнь желудка и двенадцатиперстной кишки, язвенный колит), бронхиальная астма и ринит на фоне приема ацетилсалициловой кислоты или других НПВС, дефицит глюкозо-6-фосфатдегидрогеназы, детский возраст до 12 лет.
Ограничения к применению
Гипербилирубинемия (в т.ч. синдром Жильбера, Дубина-Джонсона и Ротора), хроническая недостаточность кровообращения, отеки, артериальная гипертензия, гемофилия, гипокоагуляция, язвенная болезнь желудка и двенадцатиперстной кишки (в стадии ремиссии, в анамнезе), печеночная и/или почечная недостаточность, угнетение костномозгового кроветворения, снижение слуха, патология вестибулярного аппарата, пожилой возраст.
Применение при беременности и кормлении грудью
Применение возможно только после консультации с врачом.
Побочные действия вещества Флурбипрофен
Местные реакции при применении таблеток для рассасывания: искажение вкусовых восприятий и проявления парестезии (жжение, покалывание или пощипывание), изъязвление слизистой оболочки полости рта.
Нежелательные побочные эффекты, свойственные препаратам группы НПВС, могут наблюдаться при приеме флурбипрофена внутрь в дозе 50–100 мг 2–3 раза в сутки (12–30 табл. в день).
Со стороны нервной системы и органов чувств: головная боль, головокружение, сонливость/бессонница, астения, депрессия, тремор, возбуждение; редко — атаксия, парестезия, нарушение сознания.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): повышение АД, тахикардия, сердечная недостаточность; редко — анемия (железодефицитная, гемолитическая, апластическая), агранулоцитоз, лейкопения, тромбоцитопения.
Со стороны органов ЖКТ: диспептические явления (тошнота, рвота, изжога, диарея), НПВС-гастропатия, абдоминальная боль, нарушение функции печени; при длительном применении в больших дозах — изъязвление слизистой оболочки ЖКТ, кровотечение (желудочно-кишечное, десневое, геморроидальное).
Со стороны мочеполовой системы: тубулоинтерстициальный нефрит, нарушение функции почек, отечный синдром.
Аллергические реакции: кожная сыпь, зуд, крапивница, бронхоспазм, фотосенсибилизация, отек Квинке, анафилактический шок.
Взаимодействие
Индукторы микросомального окисления (фенитоин, этанол, барбитураты, рифампицин, фенилбутазон, трициклические антидепрессанты) увеличивают продукцию активных гидроксилированных метаболитов флурбипрофена. Флурбипрофен понижает эффективность урикозурических, гипотензивных и мочегонных ЛС, усиливает действие антикоагулянтов (повышает риск кровотечений), антиагрегантов, фибринолитиков, гипогликемический эффект производных сульфонилмочевины, побочные эффекты минерало- и глюкокортикоидов, эстрогенов. Увеличивает концентрацию в крови препаратов лития, метотрексата.
Передозировка
Симптомы: сонливость, возбуждение, тошнота, головная боль, головокружение, боль в эпигастрии, диплопия, миоз, гипотонус, угнетение сознания вплоть до комы.
Лечение: прекращение применения препарата, симптоматическая терапия.
Способ применения и дозы
Таблетку необходимо рассасывать в полости рта до полного растворения, равномерно перемещая ее по всей полости рта во избежание повреждения слизистой оболочки в месте рассасывания. Взрослым и детям старше 12 лет — по 8,75 мг (1 табл.) не более 5 раз в течение 24 ч. Таблетки не следует применять более 3 дней.
Меры предосторожности
При необходимости определения 17-кетостероидов препарат следует отменить за 48 ч до исследования. В период применения следует воздерживаться от занятий потенциально опасными видами деятельности, требующими быстрой психической и физической реакции, а также связанными с повышенной концентрацией внимания.
Торговые названия с действующим веществом Флурбипрофен
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Ракстан-Сановель |
от 555.00 до 555.00 |
| Стрепсилс® Интенсив |
от 272.00 до 403.00 |
| Флурбипрофен-Фармстандарт |
195.00 |
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-001059
Торговое название:
Брилинта®
Международное непатентованное название:
тикагрелор
Лекарственная форма:
таблетки, покрытые плёночной оболочкой
Состав на 1 таблетку:
Активное вещество: тикагрелор 90 мг
Вспомогательныевещества: маннитол 126 мг, кальция гидрофосфат 63 мг, карбоксиметилкрахмал натрия 9 мг, гипролоза 9 мг, магния стеарат 3 мг;
всоставеплёночнойоболочкитаблетки: гипромеллоза 2910 5,6 мг, титана диоксид E 171 1,7 мг, тальк 1,0 мг, макрогол 400 0,6 мг, краситель железа оксид жёлтый E 172 0,1 мг.
Описание
Круглые, двояковыпуклые таблетки, покрытые плёночной оболочкой жёлтого цвета, с гравировкой 90 на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА:
антиагрегантное средство
Код АТХ: В01АС24
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Механизм действия
Препарат Брилинта® содержит в своем составе тикагрелор, представитель химического класс циклопентилтриазолопиримидинов, который является пероральным, селективным и обратимым антагонистом P2Y12 рецепторов прямого действия и предотвращает аденозиндифосфат-опосредованную P2Y12-зависимую активацию и агрегацию тромбоцитов. Тикагрелор не предотвращает связывание аденозиндифосфата (АДФ), но его взаимодействие с Р2Y12 рецептором тромбоцитов предотвращает АДФ-индуцированную трансдукцию сигналов. Так как тромбоциты участвуют в инициировании и/или развитии тромботических осложнений атеросклероза, было показано, что ингибирование функции тромбоцитов уменьшает риск развития сердечно-сосудистых явлений, таких как летальный исход, инфаркт миокарда или инсульт.
Тикагрелор имеет дополнительный механизм действия, повышая локальные концентрации эндогенного аденозина путем ингибирования эндогенного равновесного нуклеозидного транспортера (ENT-1).
Аденозин образуется локально в местах гипоксии и повреждения тканей путем высвобождения из аденозинтрифосфата и АДФ. Тикагрелор ингибирует ENT-1 и продлевает период полувыведения аденозина, тем самым увеличивая его локальную внеклеточную концентрацию, усиливая локальный аденозиновый
ответ. Тикагрелор не имеет клинически значимого прямого влияния на аденозиновые рецепторы (A1, A2a, A2b, A3) и не метаболизируется до аденозина.
Аденозин обладает следующими эффектами, которые включают в себя: вазодилатацию, кардиопротекцию, ингибирование агрегации тромбоцитов, модуляцию воспаления и возникновение одышки, которые могут влиять на клинический профиль тикагрелора. Было показано, что у здоровых добровольцев и у пациентов с острым коронарным синдромом (ОКС) тикагрелор усиливал следующие эффекты аденозина: вазодилатацию (оцениваемую как увеличение коронарного кровотока у здоровых добровольцев; головную боль), ингибирование функции тромбоцитов ( in vitro в цельной человеческой крови) и одышку. Тем не менее, связь повышенных локальных концентраций аденозина с клиническими исходами (показатели заболеваемости и смертности) не доказана.
Фармакодинамика
Начало действия
У пациентов со стабильным течением ишемической болезни сердца (ИБС) на фоне применения ацетилсалициловой кислоты тикагрелор начинает быстро действовать, что подтверждается результатами определения среднего значения ингибирования агрегации тромбоцитов (ИАТ): через 0,5 часа после приема нагрузочной дозы 180 мг тикагрелора среднее значение ИАТ составляет примерно 41%, максимальное значение ИАТ 89% достигается через 2-4 часа после приема препарата и поддерживается в течение 2-8 часов. У 90% пациентов окончательное значение ИАТ более 70% достигается через 2 часа после приема препарата.
Конец действия
При планировании АКШ, риск кровотечений возрастает, если тикагрелор прекращают менее, чем за 96 часов до процедуры.
Данные о переходе с одного препарата на другой
Переход с клопидогрела на тикагрелор приводит к увеличению абсолютного значения ИАТ на 26,4%, а изменение терапии с тикагрелора на клопидогрел приводит к снижению абсолютного значения ИАТ на 24,5%. Можно менять терапию с клопидогрела на тикагрелор без прерывания антитромботического эффекта.
Клиническая эффективность
В исследовании PLATO (PLATelet Inhibition and Patient Outcomes – Ингибирование тромбоцитов и исходы у пациентов) участвовало 18 624 пациента, у которых за последние 24 часа развились симптомы нестабильной стенокардии, инфаркта миокарда без подъема сегмента ST или инфаркта миокарда с подъемом сегмента ST и которые лечились консервативно, или посредством чрескожного коронарного вмешательства (ЧКВ), или аортокоронарного шунтирования (АКШ) (см. раздел «Показания к применению»). В этом исследовании на фоне ежедневной терапии ацетилсалициловой кислотой тикагрелор 90 мг дважды в сутки сравнивался с клопидогрелом 75 мг в сутки в отношении эффективности в предупреждении развития комбинированной конечной точки сердечно-сосудистой смерти, инфаркта миокарда или инсульта за счет влияния на частоту сердечнососудистых смертей и инфарктов миокарда. Нагрузочная доза составляла 300 мг клопидогрела (доза 600 мг также допускалась при проведении ЧКВ) или 180 мг тикагрелора.
Эффект тикагрелора проявлялся рано (на 30 день снижение абсолютного риска (САР) на 0,6% и снижение относительного риска (СОР) на 12%), с поддержанием постоянного эффекта терапии в течение 12 месяцев, что приводило к снижению абсолютного риска (САР) на 1,9% и снижению относительного риска (СОР) на 16% в течение года.
Брилинта® снижает относительный риск комбинированной конечной точки (совокупность сердечно-сосудистых смертей, инфаркта и инсульта) у пациентов с нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST и инфарктом миокарда с подъемом сегмента ST на 16% (отношение рисков (ОР) 0,84; 95% доверительный интервал (ДИ) 0,77-0,92; p = 0,0003), сердечно-сосудистой смерти на 21% (ОР 0,79; 95% ДИ 0,69-0,91; р=0,0013), инфаркта миокарда на 16% (ОР 0,84; 95% ДИ 0,75-0,95; р=0,0045).
Эффективность препарата Брилинта® показана у различных подгрупп пациентов, независимо от массы тела, пола, наличия в анамнезе сахарного диабета, транзиторной ишемической атаки или негеморрагического инсульта, реваскуляризации, сопутствующей терапии (включая гепарин, ингибиторы гликопротеиновых llb/llla рецепторов (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»), окончательного диагноза (инфаркт миокарда без подъема сегмента ST, инфаркт миокарда с подъемом сегмента ST и нестабильная стенокардия) и лечения, запланированного при рандомизации (инвазивное или консервативное). Дополнительный анализ позволил предположить наличие возможной связи с дозой ацетилсалициловой кислоты, которая выражалась в том, что пониженная эффективность наблюдалась при приеме препарата Брилинта® в комбинации с повышенными дозами ацетилсалициловой кислоты. Рекомендуемая доза ацетилсалициловой кислоты для постоянного приема в сочетании с препаратом Брилинта® — 75-150 мг (см. разделы «Способ применения и дозы» и «Особые указания»).
Брилинта® продемонстрировала статистически значимое СОР по совокупному критерию: смерть от сердечно-сосудистых причин, инфаркт миокарда и инсульт — у пациентов с острым коронарным синдромом, которым запланировано инвазивное вмешательство (СОР 16%, САР 1,7%, р=0,0025). В поисковом анализе Брилинта® также продемонстрировала СОР по первичной конечной точке у пациентов с острым коронарным синдромом, которым назначалась консервативная терапия (СОР 15%, САР 2,3%, номинальное р=0,0444). У пациентов после стентирования при применении тикагрелора отмечалось снижение частоты тромбоза стентов (СОР 32%, САР 0,6%, номинальное р=0,0123).
Брилинта® вызывала статистически значимое СОР на 16% (САР 2,1%) по такому совокупному критерию как смерть от всех причин, инфаркт миокарда и инсульт. СОР смерти от всех причин на приеме препарата Брилинта® составляло 22% при номинальном уровне значимости р=0,0003 и САР — 1,4%.
Совокупный критерий объединенной эффективности и безопасности
Совокупный критерий объединенной эффективности и безопасности (смерть от сердечно-сосудистых причин, инфаркт миокарда, инсульт или большое кровотечение по определению исследования PLATO) подтверждает, что в течение 12 месяцев после острого коронарного синдрома положительный эффект тикагрелора не нейтрализуется случаями больших кровотечений (СОР 8%, САР 1,4%, OP 0,92; p=0,0257).
Фармакокинетика
Тикагрелор демонстрирует линейную фармакокинетику, и экспозиция тикагрелора и активного метаболита (AR-C124910XX) примерно пропорциональна дозе вплоть до 1260 мг.
Абсорбция
Тикагрелор быстро абсорбируется со средней tmax примерно 1,5 часа. Формирование основного циркулирующего в крови метаболита AR-C124910XX (также активного) из тикагрелора происходит быстро со средней tmax примерно 2,5 часа. После приема натощак тикагрелора в дозе 90 мг Cmax составляет 529 нг/мл и AUC – 3451 нг*ч/мл.
Средняя абсолютная биодоступность тикагрелора составляет 36%. Прием жирной пищи не влияет на Cmax тикагрелора или AUC активного метаболита, но приводит к повышению на 21% AUC тикагрелора и снижению на 22% Cmax активного метаболита. Эти небольшие изменения имеют минимальную клиническую значимость; поэтому тикагрелор можно назначать вне зависимости от приема пищи.
Тикагрелор в виде суспензии измельченных таблеток в питьевой воде, принятой внутрь или введенной в желудок через назогастральный зонд, биоэквивалентен тикагрелору, принятому внутрь в виде таблеток препарата Брилинта ® (AUC и Cmax тикагрелора и активного метаболита в диапазоне 80-125%).
В случае приема суспензии первоначальная экспозиция (через 0,5 ч и 1 ч после приема) была выше, чем при приеме тикагрелора в виде таблеток препарата Брилинта ®, но в дальнейшем (от 2 до 48 часов) профиль концентраций был практически одинаковым.
Распределение
Объем распределения тикагрелора в равновесном состоянии составляет 87,5 л. Тикагрелор и активный метаболит активно связываются с белками плазмы крови (> 99%).
Метаболизм
CYP3A4 является основным изоферментом, отвечающим за метаболизм тикагрелора и формирование активного метаболита, и их взаимодействия с другими субстратами CYP3A варьируют от активации до ингибирования.
Тикагрелор и активный метаболит являются слабыми ингибиторами гликопротеина Р (P-gp).
Основным метаболитом тикагрелора является AR-C124910XX, который также активен, что подтверждается результатами оценки связывания с P2Y12 рецептором АДФ тромбоцитов in vitro. Системная экспозиция активного метаболита составляет примерно 30-40% от экспозиции тикагрелора.
Экскреция
Основной путь выведения тикагрелора – через печеночный метаболизм. При введении меченного изотопом тикагрелора в среднем примерно 57,8% радиоактивности выделяется с фекалиями, 26,5% с мочой. Выведение тикагрелора и активного метаболита с мочой составляет менее 1% дозы. В основном активный метаболит выводится с желчью. Средний период полувыведения тикагрелора и активного метаболита составлял 7 и 8,5 часов, соответственно.
Особые популяции больных
Пожилые пациенты
У пожилых пациентов (в возрасте от 75 лет и старше) отмечена более высокая экспозиция тикагрелора (Cmax и AUC примерно на 25% выше) и активного метаболита по сравнению с молодыми пациентами. Эти различия не считаются клинически значимыми (см. раздел «Способ применения и дозы»).
Дети
Нет данных по применению тикагрелора у детей.
Пол
У женщин отмечена более высокая экспозиция тикагрелора и активного метаболита по сравнению с мужчинами. Эти различия не считаются клинически значимыми.
Этнические группы
Средняя биодоступность препарата у пациентов-азиатов на 39% выше, чем у европеоидов. Биодоступность препарата Брилинта ® на 18% ниже у пациентов негроидной расы по сравнению с больными европеоидной расы.
Почечная недостаточность
Экспозиция тикагрелора примерно на 20% ниже, а его активного метаболита примерно на 17% выше у пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин) по сравнению с пациентами с нормальной функцией почек (см. раздел «Способ применения и дозы»).
Печеночная недостаточность
Сmах и AUC тикагрелора были на 12% и 23% выше у пациентов с печеночной недостаточностью легкой степени по сравнению со здоровыми добровольцами. Не проводились исследования тикагрелора у пациентов с умеренной или тяжелой печеночной недостаточностью, и его использование у этих пациентов противопоказано (см. разделы «Способ применения и дозы» и «Противопоказания»).
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Брилинта®, применяемая одновременно с ацетилсалициловой кислотой, показана для профилактики атеротромботических событий у пациентов с острым коронарным синдромом (нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST или инфарктом миокарда с подъемом сегмента ST [STEMI]), включая больных, получавших лекарственную терапию, и пациентов, подвергнутых чрескожному коронарному вмешательству (ЧКВ) или аортокоронарному шунтированию (АКШ)).
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к тикагрелору или любому из компонентов препарата
- Активное патологическое кровотечение
- Внутричерепное кровоизлияние в анамнезе
- Умеренная или тяжелая печеночная недостаточность
- Совместное применение тикагрелора с мощными ингибиторами CYP3A4 (например, кетоконазолом, кларитромицином, нефазодоном, ритонавиром и атазанавиром)
- Детский возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности применения у данной группы пациентов)
С ОСТОРОЖНОСТЬЮ
Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением) (см. раздел «Особые указания»).
Пациенты с сопутствующей терапией препаратами, повышающими риск кровотечений (т.е. нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики) в течение 24 часов до приема препарата Брилинта ®.
Пациенты с повышенным риском развития брадикардии (например, больные с синдромом слабости синусового узла без кардиостимулятора, с атриовентрикулярной блокадой 2-ой или 3-ей степени; обмороком, связанным с брадикардией) в связи с недостаточным опытом клинического применения препарата Брилинта ® (см. раздел «Особые указания»). При совместном применении с препаратами, вызывающими брадикардию.
Тикагрелор должен использоваться с осторожностью у пациентов с бронхиальной астмой и хронической обструктивной болезнью легких (ХОБЛ). Если пациент сообщает о возникновении нового эпизода одышки, о длительной одышке или ухудшении одышки, необходимо провести обследование, и в случаенепереносимости, лечение тикагрелором должно быть прекращено.
На фоне приема препарата Брилинта® уровень креатинина может повыситься (см. разделы «Побочное действие», «Особые указания»), в связи с чем необходимо производить оценку почечной функции в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью, пациентов, получающих терапию антагонистами рецепторов к ангиотензину.
Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Не рекомендуется совместное применение тикагрелора и высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), в связи с чем их совместное применение должно осуществляться с осторожностью (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
БЕРЕМЕННОСТЬ И ПЕРИОД ЛАКТАЦИИ
Данные о применении препарата Брилинта ® у беременных женщин отсутствуют или ограничены.
В исследованиях на животных тикагрелор вызывал незначительное снижение прибавки массы тела у матери, снижение жизнеспособности новорожденного и его массы тела, замедление роста. Брилинта ® не рекомендована во время беременности.
Доступные фармакодинамические, токсикологические данные у животных показали, что тикагрелор и его активные метаболиты выделяются с молоком. Не может быть исключен риск для новорожденного/младенца. Не рекомендуется применять препарат Брилинта ® в период кормления ребенка грудью.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Для приёма внутрь. Препарат Брилинта ® можно принимать вне зависимости от приёма пищи.
Применение препарата Брилинта® следует начинать с однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем продолжать прием по 90 мг два раза в сутки.
Для пациентов с затруднением глотания таблетку (или 2 таблетки – в случае приема нагрузочной дозы) следует измельчить до состояния мелкого порошка, размешать в половине стакана питьевой воды и сразу же выпить полученную суспензию. Остатки смешать с дополнительной половиной стакана питьевой воды и выпить полученную суспензию. Суспензию можно также вводить через назогастральный зонд (CH8 или большего размера). После введения суспензии необходимо промыть назогастральный зонд водой для того, чтобы доза препарата полностью попала в желудок пациента.
Пациенты, принимающие препарат Брилинта®, должны ежедневно принимать ацетилсалициловую кислоту (от 75 мг до 150 мг при постоянном приеме) (см.раздел «Фармакологические свойства»), если отсутствуют специфические противопоказания.
Следует избегать перерывов в терапии. Пациент, пропустивший прием препарата Брилинта®, должен принять только одну таблетку 90 мг (следующая доза) в намеченное время.
При необходимости пациенты, принимающие клопидогрел, могут быть переведены на прием препарата Брилинта ® (см. раздел «Фармакологические свойства»).
Рекомендуется проводить терапию препаратом Брилинта ® в течение 12 месяцев, кроме случаев клинической необходимости в досрочной отмене препарата (см. раздел «Фармакологические свойства»). Данные о применении тикагрелора более 12 месяцев ограничены. У пациентов с острым коронарным синдромом досрочная отмена любой антиагрегантной терапии, включая препарат Брилинта ®, может повысить риск сердечно-сосудистой смерти или инфаркта миокарда в результате основного заболевания (см. раздел «Особые указания»). Необходимо избегать преждевременного прекращения приема препарата.
Пожилые пациенты
Не требуется коррекции дозы (см. раздел «Фармакологические свойства»).
Пациенты с почечной недостаточностью
Не требуется корректировать дозу препарата у пациентов с почечной недостаточностью (см. раздел «Фармакологические свойства»). Отсутствует информация о применении препарата Брилинта ® у пациентов на гемодиализе, поэтому его применение у этих пациентов не показано.
Пациенты с печеночной недостаточностью
Не требуется корректировать дозу препарата у пациентов с легкой печеночной недостаточностью. Не проводились исследования препарата Брилинта ® у пациентов с умеренной или тяжелой печеночной недостаточностью, поэтому его у этих пациентов противопоказано (см. разделы «Фармакологические свойства» и «Противопоказания»).
Дети
Безопасность и эффективность препарата Брилинта ® у детей младше 18 лет по одобренному у взрослых показанию не установлена.
ПОБОЧНОЕ ДЕЙСТВИЕ
По данным исследования PLATO самыми частыми отмечавшимися нежелательными явлениями у пациентов, принимавших тикагрелор, были одышка, ушибы и носовые кровотечения.
Нежелательные реакции классифицированы по частоте развития и классу системы органов. Частота развития нежелательных реакций определяется с использованием следующих условных обозначений: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000).
Нежелательные лекарственные реакции по частоте развития и классу системы органов
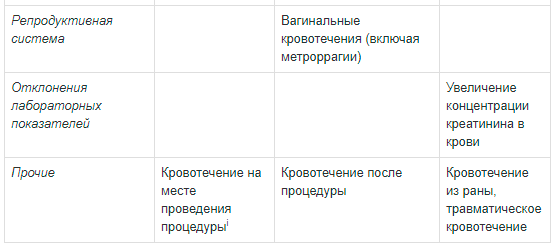
a гиперурикемия, повышение концентрации мочевой кислоты в крови; смотрите раздел «Отклонения в значениях лабораторных показателей» ниже.
b кровоизлияние в мозг, внутричерепное кровоизлияние, геморрагический инсульт.
c одышка, одышка при нагрузке, одышка в покое, ночная одышка
d желудочно-кишечное кровотечение, ректальное кровотечение, кишечное
кровотечение, мелена, положительный анализ на скрытую кровь
е кровотечение из язвы ЖКТ, кровотечение из язвы желудка, кровотечение из язвы двенадцатиперстной кишки, кровотечение из пептической язвы
f подкожная гематома, кожные и подкожные геморрагии, петехии
g ушиб, гематома, экхимоз, повышенная тенденция к синякам, травматическая гематома
h гематурия, кровотечение из мочевыводящих путей
i кровотечение из места пункции сосуда, гематома в месте пункции сосуда, кровотечение из места инъекции, кровотечение из места пункции, кровотечение из места катетеризации
# у пациентов, принимавших тикагрелор в исследовании PLATO (п=9235), случаев гемартроза отмечено не было. Частота гемартроза была рассчитана с использованием верхнего предела 95% ДИ для ожидаемой частоты (по формуле 3/Х, где Х — количество пациентов, получавших тикагрелор, т.е. 9235).
Предполагаемая частота гемартроза составляет 3/9235, что соответствует частоте «редко».
Описание некоторых нежелательных реакций
Кровотечение
В исследовании PLATO использовались следующие определения кровотечения:
• Большое летальное/угрожающее жизни кровотечение: летальное, или внутричерепное кровоизлияние, или кровотечение в полость перикарда с тампонадой сердца; или гиповолемический шок или тяжелая гипотония, вызванные кровотечением и требующие применения вазоконстрикторов или проведения оперативного вмешательства, или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина более, чем на 50 г/л, или требующее трансфузии 4 или более единиц цельной крови или эритроцитов.
• Большое иное кровотечение: вызывающее существенную недееспособность больного (например, внутриглазное кровоизлияние с необратимой потерей зрения), или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина на 30-50 г/л, или требующее трансфузии 2-3 единиц цельной крови или эритроцитов.
• Малое кровотечение: требует медицинского вмешательства для остановки или лечения кровотечения (например, носовое кровотечение, требующее посещения больницы для тампонады носа).
Брилинта® и клопидогрел не различались по частоте больших кровотечений в целом по критериям PLATO (11,6%/год и 11,2%/год, соответственно), летальных/угрожающих жизни кровотечений по критериям PLATO (5,8%/год в обеих группах). Однако частота совокупности больших и малых кровотечений по критериям PLATO была выше в группе тикагрелора (16,1%) по сравнению с клопидогрелом (14,6%, р=0,0084).
Возраст, пол, масса тела, раса, географический регион, сопутствующие заболевания, сопутствующая терапия, анамнез, включая предшествующий инсульт и транзиторную ишемическую атаку, не влияли на частоту больших кровотечений в целом и несвязанных с процедурами по критериям PLATO. Не было выявлено групп с повышенным риском кровотечений.
Кровотечение, связанное с АКШ: В исследовании PLATO у 42% больных из 1584 (12% из когорты), подвергнутых АКШ, развивались большие летальные/ угрожающие жизни больного кровотечения без значимых различий в обеих группах лечения. Летальное кровотечение, связанное с АКШ, отмечалось у 6 пациентов в каждой группе лечения.
Кровотечение, не связанное с АКШ, и кровотечение, не связанное с процедурами:
Брилинта® и клопидогрел не отличались по частоте случаев большого летального/ угрожающего жизни кровотечения, не связанного с АКШ по критериям PLATO, но при применении препарата Брилинта® чаще развивались большие кровотечения в целом по определению исследования PLATO (4,5%/год по сравнению с 3,8%/год; р=0,0264). Если удалить случаи развития кровотечений, связанных с АКШ, в группе тикагрелора отмечалось больше кровотечений (3,1%/год), чем в группе клопидогрела (2,3%/год; р=0,0058). Прекращение лечения вследствие кровотечений, не связанных с процедурой, было более частым на фоне тикагрелора (2,9%) по сравнению с клопидогрелом (1,2%, p<0,001).
Внутричерепное кровоизлияние: В группе тикагрелора развивалось больше внутричерепных кровотечений, не связанных с процедурами (n=27 кровотечений у 26 пациентов, 0,3%), чем в группе клопидогрела (n=14 кровотечений, 0,2%), из которых 11 кровотечений на тикагрелоре и 1 на клопидогреле были фатальными. Однако не было значимых различий по общему числу фатальных кровотечений.
Одышка
Нежелательные явления в виде одышки (одышка, одышка в покое, одышка при физической нагрузке, пароксизмальная ночная одышка и ночная одышка) в комбинации развивались у 13,8% больных, получавших препарат Брилинта ®, и у 7,8% пациентов, принимавших клопидогрел. Исследователи посчитали, что у 2,2% пациентов из группы тикагрелора одышка была связана с терапией. Большинство случаев одышки были слабыми или умеренными по своей интенсивности и представляли собой однократные эпизоды сразу после начала терапии. Примерно 30% от всех случаев одышки разрешились в течение 7 дней. Чаще одышка развивалась у пожилых больных, у пациентов с застойной сердечной недостаточностью, ХОБЛ или бронхиальной астмой в начале исследования. 0,9% пациентов прекращали прием препарата Брилинта ® из-за одышки. Одышка не была связана с развитием нового или ухудшением имеющегося заболевания сердца или легких (см. раздел «Особые указания»). Препарат Брилинта® не влияет на показатели функции внешнего дыхания.
Отклонения в значениях лабораторных показателей
Сывороточная концентрация креатинина повышалась более, чем на 30% у 25,5% пациентов и больше, чем на 50% у 8,3% пациентов, получающих препарат Брилинта®. Повышение креатинина более, чем на 50%, чаще встречалось у пациентов старше 75 лет, у пациентов с тяжелой почечной недостаточностью при включении в исследование и у пациентов, получающих терапию антагонистами рецепторов к ангиотензину. Общее число почечных нежелательных явлений составляло 4,9% у пациентов на тикагрелоре, однако исследователи связывали их с приемом препарата в 0,6% случаев.
Сывороточная концентрация мочевой кислоты увеличивалась выше верхней границы нормы у 22% пациентов, получающих препарат Брилинта®.
Нежелательные явления, связанные с гиперурикемией, отмечались в 0,5% случаев на тикагрелоре, из них исследователи связывали с приемом тикагрелора 0,05% случаев. Подагрический артрит наблюдался у 0,2% пациентов на тикагрелоре, ни один из этих случаев не был расценен исследователем, как связанный с приемом препарата.
Постмаркетинговое применение
Ниже представлены нежелательные реакции, которые были отмечены при постмаркетинговом применении препарата Брилинта ®. Поскольку сообщения получены спонтанно от популяции неустановленного размера, не всегда возможно достоверно оценить частоту развития.
Нарушениясостороныиммуннойсистемы:реакции повышенной чувствительности, включая ангионевротический отек (см. раздел «Противопоказания»).
ПЕРЕДОЗИРОВКА
Тикагрелор хорошо переносится в однократной дозе препарата до 900 мг. В единственном исследовании с увеличением дозы неблагоприятное воздействие на желудочно-кишечный тракт было дозолимитирующим. Другими клинически значимыми нежелательными явлениями, которые могли наблюдаться при передозировке, были одышка и желудочковые паузы. В случае передозировки рекомендуется осуществлять наблюдение на предмет этих нежелательных явлений и проводить мониторирование ЭКГ.
Брилинта® не выводится при гемодиализе (см. раздел «Особые указания»), антидот не известен. При передозировке следует проводить симптоматическую терапию в соответствии с локальными стандартами. В связи с ингибированием тромбоцитов увеличение продолжительности кровотечения является предполагаемым фармакологическим действием передозировки препаратом Брилинта®, поэтому при развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ДРУГИЕ ВИДЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Воздействие других лекарственных препаратов на препарат Брилинта®
Лекарственные препараты, метаболизируемые изоферментом CYP3A4 Ингибиторы CYP3A4
• Мощные ингибиторы CYP3A4: совместное применение кетоконазола с тикагрелором увеличивает Cmax и AUC тикагрелора в 2,4 и 7,3 раза, соответственно. Cmax и AUC активного метаболита понижается на 89% и 56%, соответственно. Другие мощные ингибиторы CYP3A4 (кларитромицин, нефазодон, ритонавир и атазанавир) будут оказывать такие же эффекты, поэтому их совместное применение с препаратом Брилинта® противопоказано (см. разделы «Противопоказания», «Особые указания»).
• Умеренные ингибиторы CYP3A4: совместное применение дилтиазема с тикагрелором увеличивает Сmax тикагрелора на 69%, а AUC в 2,7 раз, и снижает Сmax активного метаболита на 38%, а AUC не меняется. Тикагрелор не влияет на плазменные концентрации дилтиазема. Другие умеренные ингибиторы CYP3A4 (например, ампренавир, апрепитант, эритромицин, флуконазол) можно назначать одновременно с препаратом Брилинта®.
Циклоспорин (ингибитор P-gp и CYP3A4)
Совместное применение циклоспорина (600 мг) с тикагрелором увеличивает C max и AUC тикагрелора в 2,3 и 2,8 раз, соответственно. При этом отмечается увеличение AUC активного метаболита на 32% и снижение Cmax на 15%. Тикагрелор не влияет на плазменную концентрацию циклоспорина.
Индукторы CYP3A4
Совместное применение рифампицина с тикагрелором снижает C max и AUC тикагрелора на 73% и 86%, соответственно. Cmax активного метаболита не меняется, а AUC понижается на 46%. Другие индукторы CYP3A4 (например, фенитоин, карбамазепин и фенобарбитал), по-видимому, будут снижать экспозицию препарата Брилинта®. Мощные индукторы CYP3A4 могут уменьшать экспозицию и эффективность препарата Брилинта®.
Другие
По результатам фармакологических исследований взаимодействия сопутствующее применение тикагрелора с гепарином, эноксапарином и ацетилсалициловой кислотой или десмопрессином не влияет на фармакокинетику тикагрелора, его активного метаболита и АДФ-зависимую агрегацию тромбоцитов. В случае наличия клинических показаний к назначению препаратов, влияющих на гемостаз, они должны использоваться с осторожностью в комбинации с препаратом Брилинта® (см. раздел «С осторожностью»).
Нет данных о совместном применении препарата Брилинта® с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Особые указания»).
Влияние препарата Брилинта® на другие лекарственные средства
Лекарственные препараты, метаболизируемые изоферментом CYP3A4
• Симвастатин: сопутствующее применение тикагрелора и симвастатина повышает C max и AUC симвастатина на 81% и 56%, соответственно, и увеличивает C max и AUC симвастатиновой кислоты на 64% и 52%, соответственно, при этом, в некоторых случаях эти показатели повышаются в 2-3 раза. Совместное применение симвастатина в дозе выше 40 мг/сут. с тикагрелором может приводить к развитию побочных эффектов симвастатина, и необходимо оценить соотношение потенциального риска и пользы. Не рекомендуется совместное применение препарата Брилинта® с симвастатином и ловастатином в дозе свыше 40 мг. Аторвастатин: сопутствующее применение аторвастатина и тикагрелора повышает Сmax и AUC метаболитов аторвастатиновой кислоты на 23% и 36%, соответственно. Подобное увеличение значений Cmax и AUC наблюдается для всех метаболитов аторвастатиновой кислоты. Эти изменения признаны клинически не значимыми.
• Сходные эффекты со статинами, метаболизирующимися CYP3A4, не могут быть исключены. В исследовании PLATO пациенты, получавшие тикагрелор, принимали различные статины при отсутствии каких-либо опасений относительно безопасности у 93% пациентов, принимавших эту группу препаратов.
Тикагрелор — умеренный ингибитор CYP3A4. Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд или алкалоиды спорыньи) не рекомендуется, так как тикагрелор может увеличивать экспозицию этих препаратов.
Лекарственные препараты, метаболизируемые изоферментом CYP2C9
Сопутствующее применение тикагрелора и толбутамида не меняло плазменные концентрации ни одного из этих препаратов, что говорит о том, что тикагрелор не является ингибитором изофермента CYP2C9, и, маловероятно, что он влияет на СУР2С9-опосредованный метаболизм препаратов, подобных варфарину и толбутамиду.
Оральные контрацептивы
Совместное применение тикагрелора, левоноргестрела и этинилэстрадиола увеличивает экспозицию этинилэстрадиола примерно на 20%, но не влияет на фармакокинетику левоноргестрела. Не ожидается клинически значимого воздействия на эффективность контрацепции при одновременном применении левоноргестрела, этинилэстрадиола и препарата Брилинта®.
Субстрат Р—др (включая дигоксин и циклоспорин)
Сопутствующее применение дигоксина с тикагрелором повышает Cmax и AUC дигоксина на 75% и 28%, соответственно. При совместном приеме с тикагрелором среднее значение самой низкой концентрации дигоксина увеличивалось на 30%, в некоторых индивидуальных случаях в два раза. Cmax и AUC тикагрелора при применении дигоксина не менялись. Поэтому рекомендуется проводить соответствующий клинический и/или лабораторный мониторинг при одновременном применении препарата Брилинта® и P-gp-зависимых препаратов с узким терапевтическим индексом, наподобие дигоксина и циклоспорина.
Другая сопутствующая терапия
При совместном применении препарата Брилинта® с препаратами, способными
вызвать брадикардию, должна соблюдаться осторожность. Однако в исследовании PLATO не наблюдалось клинически значимых нежелательных явлений при совместном применении с одним или более препаратами, способными вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% антагонисты кальция, включая дилтиазем и верапамил, и 4% – дигоксин). В исследовании PLATO Брилинта® преимущественно назначалась совместно с ацетилсалициловой кислотой, ингибиторами протонной помпы, статинами, бета-адреноблокаторами, ингибиторами ангиотензинпревращающего фермента и антагонистами рецепторов ангиотензина в рамках длительного приема, а также с гепарином, низкомолекулярными гепаринами, ингибиторами гликопротеиновых IIb/IIIa рецепторов для внутривенного введения в рамках краткосрочной терапии. По результатам этих исследований не выявлено клинически значимых нежелательных взаимодействий.
Совместное применение препарата Брилинта® с гепарином, эноксапарином или десмопрессином не оказывало влияние на активированное частичное тромбопластиновое время (АЧТВ), активированное время свертывания (АВС) и исследование фактора Xa, однако вследствие потенциального фармакодинамического взаимодействия, требуется соблюдать осторожность при совместном применении с препаратами, влияющими на гемостаз.
В связи с сообщениями о подкожных кровоизлияниях на фоне селективных ингибиторов обратного захвата cеротонина, (например, пароксетин, сертралин и циталопрам), рекомендуется соблюдать осторожность при их совместном приеме с препаратом Брилинта ®.
При ежедневном употреблении больших объемов грейпфрутового сока (по 200 мл 3 раза в день) было отмечено 2-кратное увеличение экспозиции тикагрелора. Ожидается, что такое увеличение экспозиции тикагрелора не имеет клинического значения для большинства пациентов.
ОСОБЫЕ УКАЗАНИЯ
Риск развития кровотечения
У пациентов с острым коронарным синдромом, получавших терапию препаратом Брилинта® и ацетилсалициловой кислотой, отмечался повышенный риск несвязанных с АКШ больших кровотечений и кровотечений, требующих повышенного медицинского внимания, таких как большие + малые кровотечения по определению PLATO, но не увеличился риск летальных/угрожающих жизни кровотечений (см. раздел «Побочное действие»). При назначении препарата Брилинта® следует оценить соотношение пользы от профилактики атеротромботических событий и риска у пациентов с повышенным риском развития кровотечений.
При наличии клинических показаний Брилинта® должна использоваться с осторожностью в следующих группах пациентов:
• Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением). Использование препарата Брилинта® противопоказано у пациентов с активным патологическим кровотечением, внутричерепным кровоизлиянием в анамнезе, умеренной или тяжелой печеночной недостаточностью.
• Сопутствующее применение препаратов, которые могут повысить риск развития кровотечения (например, нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до приема препарата Брилинта®).
Отсутствуют данные о гемостатической эффективности трансфузий тромбоцитов при применении препарата Брилинта®; Брилинта® может ингибировать трансфузированные тромбоциты в крови. Так как при сопутствующем применении препарата Брилинта® и десмопрессина не уменьшалось стандартизированное время кровотечения, то маловероятно, что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия (аминокапроновая кислота или транексамовая кислота) и/или рекомбинантный фактор Vila могут усиливать гемостаз. После установления причины кровотечения и его купирования можно возобновить терапию препаратом Брилинта®.
Хирургические операции
Перед запланированной операцией или началом приема новых препаратов пациенту следует проинформировать врача о том, что он принимает препарат Брилинта®.
У пациентов, подвергающихся аортокоронарному шунтированию (АКШ), частота развития больших кровотечений при применении препарата Брилинта® была такой же, как при применении клопидогрела во все дни после отмены терапии, кроме дня 1, когда частота развития больших кровотечений была выше при приеме препарата Брилинта ® (см. раздел «Побочное действие»).
Если пациент подвергается плановой операции и не желателен
антитромботический эффект, то терапию препаратом Брилинта ® следует прекратить за 7 дней до операции.
Пациенты с риском развития брадикардии
В связи с выявлением в ранее проведенном клиническом исследовании, в основном, бессимптомных пауз, пациенты с повышенным риском развития брадикардии (например, больные без кардиостимулятора, у которых диагностирован синдром слабости синусового узла, атриовентрикулярная блокада сердца 2-ой или 3-ей степени; обморок, связанный с брадикардией) не были включены в основное исследование для оценки безопасности и эффективности препарата Брилинта®. Поэтому в связи с ограниченным клиническим опытом применения препарата у этих больных, рекомендуется с осторожностью назначать препарат Брилинта® таким пациентам (см. раздел «Фармакологические свойства»).
Дополнительная предосторожность должна соблюдаться при совместном применении препарата Брилинта® с препаратами, способными вызвать брадикардию. Однако не отмечалось клинически значимых побочных эффектов при совместном применении с одним или более препаратами, которые могут вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% блокаторы кальциевых каналов, включая дилтиазем и верапамил, и 4% дигоксин) (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
В ходе под-исследования с использованием суточного мониторирования ЭКГ по Холтеру в группе тикагрелора по сравнению с клопидогрелом больше пациентов в острой фазе ОКС имели желудочковые паузы > 3 секунд. Повышение числа желудочковых пауз, зарегистрированных с помощью суточного мониторирования по Холтеру, на фоне приема тикагрелора отмечалось чаще у пациентов с хронической сердечной недостаточностью по сравнению с общей популяцией в острой фазе ОКС, но не на первом месяце. Паузы у этих пациентов не сопровождались последующими нежелательными клиническими последствиями (обмороки и установка кардиостимулятора).
Одышка
Одышка при применении препарата Брилинта® обычно слабая или умеренная по своей интенсивности, часто проходит по мере продолжения терапии препаратом. Пациенты с бронхиальной астмой/ХОБЛ могут иметь повышенный абсолютный риск одышки на приеме препарата Брилинта® (см. раздел «Побочное действие»). У пациентов с бронхиальной астмой/ХОБЛ тикагрелор должен использоваться с осторожностью. Механизм одышки на приеме тикагрелора не выяснен. Если у пациента развился новый эпизод одышки, сохраняется или усилилась одышка во время применения препарата Брилинта®, то необходимо провести полноценное обследование, и в случае непереносимости, прием препарата следует прекратить.
Повышение уровня
креатинина
На приеме препарата Брилинта® уровень креатинина может увеличиться (см. раздел «Побочное действие»). Механизм этого эффекта не известен. Оценку почечной функции необходимо производить через месяц от начала приема препарата, а в последующем в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью и получающих терапию антагонистами рецепторов ангиотензина.
Повышение уровня мочевой кислоты
Пациенты на тикагрелоре имели более высокий риск гиперурикемии, чем
принимавшие клопидогрел (см. раздел «Побочное действие»). Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Другие
На основании наблюдаемого взаимодействия между поддерживающей дозой ацетилсалициловой кислоты и эффективностью тикагрелора по сравнению с клопидогрелом, совместное применение высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг) и препарата Брилинта® не рекомендуется (см. разделы «Фармакологические свойства», «С осторожностью»).
Совместное применение препарата Брилинта® с мощными ингибиторами CYP3A4 (например, кетоконазол, кларитромицин, нефазодон, ритонавир и атазанавир) противопоказано (см. раздел «Противопоказания»), так как оно может привести к значительному повышению экспозиции препарата Брилинта® (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
Совместное применение препарата Брилинта® с мощными индукторами CYP3A4 (например, рифампицин, фенитоин, карбамазепин и фенобарбитал) не рекомендуется, так как их совместный прием может снижать экспозицию и эффективность тикагрелора (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»). Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд и алкалоиды спорыньи) не рекомендовано, так как тикагрелор может увеличить экспозицию этих препаратов.
Совместное применение препарата Брилинта® с симвастатином или ловастатином в дозе более 40 мг не рекомендуется (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ АВТОМОБИЛЕМ И ДРУГИМИ МЕХАНИЗМАМИ
Не проводилось исследований влияния препарата Брилинта® на способность к вождению автотранспорта и управлению механизмами. Брилинта® не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Во время терапии острого коронарного синдрома сообщалось о головокружении и спутанности сознания. В случае развития данных явлений пациентам следует соблюдать осторожность при управлении автомобилем и другими механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые плёночной оболочкой, 90 мг. По 14 таблеток в блистере из Ал/ПВХ/ПВДХ. 1, 4 или 12 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30°С, в недоступном для детей месте.
СРОК ГОДНОСТИ
3 года. Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК
По рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Производитель и фасовщик (первичная упаковка)
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Упаковщик (вторичная (потребительская) упаковка) и выпускающий контроль качества
ООО «АстраЗенека Индастриз»
249006, Россия, Калужская область, Боровский район, деревня Добрино, 1-ый Восточный проезд, владение 8
Дополнительная информация предоставляется по требованию: ООО Астра Зенека Фармасьютикалз
125284 Москва, ул. Беговая д.3, стр. 1.
Купить Брилинта таблетки 90 мг в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Цитофлавин® (Cytoflavin®) инструкция по применению
📜 Инструкция по применению Цитофлавин®
💊 Состав препарата Цитофлавин®
✅ Применение препарата Цитофлавин®
📅 Условия хранения Цитофлавин®
⏳ Срок годности Цитофлавин®
Описание лекарственного препарата
Цитофлавин®
(Cytoflavin®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2021 года.
Дата обновления: 2020.11.08
Владелец регистрационного удостоверения:
Контакты для обращений:
ПОЛИСАН НТФФ ООО
(Россия)
Код ATX:
N07XX
(Прочие препараты для лечения заболеваний нервной системы)
Лекарственная форма
| Цитофлавин® |
Таб., покр. кишечнорастворимой оболочкой: 50 или 100 шт. рег. №: ЛП-(000923)-(РГ-RU) Предыдущий рег. №: ЛС-001767 |
Форма выпуска, упаковка и состав
препарата Цитофлавин®
Таблетки, покрытые кишечнорастворимой оболочкой красного цвета, круглые, двояковыпуклые; на поперечном срезе видны два слоя; ядро таблеток от желтого до желто-оранжевого цвета.
Вспомогательные вещества: повидон — 8.1 мг, кальция стеарат — 3.9 мг, гипромеллоза — 3.6 мг, полисорбат 80 — 0.4 мг.
Состав кишечнорастворимой оболочки: сополимер метакриловой кислоты и этилакрилата [1:1] — 29.02 мг, пропиленгликоль — 2.91 мг, краситель азорубин (кармуазин) (E122) — 0.07 мг.
10 шт. — упаковки ячейковые контурные (5) — пачки картонные×.
10 шт. — упаковки ячейковые контурные (10) — пачки картонные×.
20 шт. — упаковки ячейковые контурные (5) — пачки картонные×.
× Для контроля первого вскрытия боковые клапаны пачки могут быть заклеены с двух сторон этикетками.
Фармакологическое действие
Фармакологические эффекты обусловлены комплексным действием компонентов, входящих в состав препарата Цитофлавин®.
Янтарная кислота — эндогенный внутриклеточный метаболит цикла Кребса, выполняющий в клетках организма универсальную энергосинтезирующую функцию. При участии кофермента флавинадениндинуклеотида (ФАД) янтарная кислота митохондриальным ферментом сукцинатдегидрогеназой быстро трансформируется в фумаровую кислоту и далее в другие метаболиты цикла трикарбоновых кислот. Стимулирует аэробный гликолиз и синтез АТФ в клетках. Конечным продуктом метаболизма янтарной кислоты в цикле Кребса является двуокись углерода и вода. Янтарная кислота улучшает тканевое дыхание за счет активации транспорта электронов в митохондриях.
Инозин является производным пурина, предшественником АТФ. Обладает способностью активировать ряд ферментов цикла Кребса, стимулируя синтез ключевых ферментов-нуклеотидов — ФАД и НАД.
Никотинамид (витамин РР), амид никотиновой кислоты. Никотинамид в клетках, путем каскада биохимических реакций, трансформируется в форму никотинамидадениндинуклеотида (НАД) и его фосфата (НАДФ), активируя никотинамид-зависимые ферменты цикла Кребса, необходимых для клеточного дыхания и стимуляции синтеза АТФ.
Рибофлавин (витамин В2) является флавиновым коферментом (ФАД), активирующим сукцинатдегидрогеназу и другие окислительно-восстановительные реакции цикла Кребса.
Таким образом, все компоненты препарата Цитофлавин® являются естественными метаболитами организма и стимулируют тканевое дыхание. Метаболическая энергокоррекция, антигипоксическая и антиоксидантная активность препарата, определяющие фармакологические свойства и лечебную эффективность составляющих, обусловлена взаимодополняющим действием янтарной кислоты, инозина, никотинамида и рибофлавина.
Фармакокинетика
Цитофлавин® обладает высокой биодоступностью.
Янтарная кислота при приеме внутрь абсорбируется из ЖКТ, поступает в кровь и ткани, участвуя в реакциях энергетического обмена, и полностью распадается до конечных продуктов обмена (двуокись углерода и воду) через 30 мин.
Инозин хорошо абсорбируется из ЖКТ. Tmax в крови составляет 5 ч, среднее время удержания в крови — 5.5 ч, Vd в равновесном состоянии — около 20 л. Инозин метаболизируется в печени с образованием инозинмонофосфата с последующим его окислением до мочевой кислоты. В незначительном количестве выводится почками.
Никотинамид быстро распределяется во всех тканях (Vd в равновесном состоянии — около 500 л). Tmax в крови составляет 2 ч, среднее время удержания в крови — 4.5 ч. Метаболизируется в печени с образованием N-метилникотинамида. Выводится почками. Никотинамид проникает через плацентарный барьер, выделяется с грудным молоком.
Рибофлавин быстро абсорбируется из ЖКТ, распределяется неравномерно (наибольшее количество в миокарде, печени, почках), трансформируется во флавинаденинмононуклеотид (ФМН) и ФАД в митохондриях. Выводится почками, преимущественно в виде метаболитов. Проникает через плацентарный барьер, выделяется с грудным молоком.
Показания препарата
Цитофлавин®
В составе комплексной терапии у взрослых:
- последствия инфаркта мозга;
- цереброваскулярные заболевания (церебральный атеросклероз, гипертензивная энцефалопатия);
- неврастения (повышенная раздражительность, утомляемость, утрата способности к длительному умственному и физическому напряжению).
Режим дозирования
Препарат принимают внутрь по 2 таб. 2 раза/сут с интервалом 8-10 ч. Рекомендуется принимать Цитофлавин® утром и днем, не позднее 18 ч.
Таблетки следует принимать не менее чем за 30 мин до еды, не разжевывая, запивая водой (100 мл).
Продолжительность курса лечения составляет — 25 дней. Назначение повторного курса возможно с интервалом не менее 1 месяца.
Побочное действие
По данным ВОЗ побочные эффекты классифицированы в соответствии с их частотой развития следующим образом: очень часто (≥1/10); часто (≥1/100-<1/10); нечасто (≥1/1000-<1/100); редко (≥1/10000-<1/1000); очень редко (<1/10000); частота неизвестна (частота не может быть определена на основе имеющихся данных).
Со стороны нервной системы: очень редко — головная боль.
Со стороны сердечно-сосудистой системы: очень редко — гиперемия.
Со стороны пищеварительной системы: очень редко — боли в эпигастральной области, дискомфорт в эпигастральной области, тошнота.
Со стороны обмена веществ: очень редко — транзиторная гипогликемия, гиперурикемия, обострение сопутствующей подагры.
Со стороны кожи и подкожных тканей: очень редко — зуд, крапивница.
Если любые из указанных в инструкции побочных эффектов усугубляются или отмечаются любые другие побочные эффекты, не указанные в инструкции, пациенту необходимо сообщить об этом врачу.
Противопоказания к применению
- детский и подростковый возраст до 18 лет (в связи с недостаточностью данных об эффективности и безопасности);
- повышенная чувствительность к компонентам препарата.
С осторожностью следует назначать препарат пациентам с заболеваниями органов пищеварения (эрозии, язвы желудка и/или двенадцатиперстной кишки, гастриты, дуодениты) в фазе обострения, с артериальной гипотензией, при нерфролитиазе, сопутствующей подагре, гиперурикемии.
Применение при беременности и кормлении грудью
Не рекомендуется применять Цитофлавин® при беременности и в период лактации в связи с отсутствием клинических данных по эффективности и безопасности препарата у этой категории пациентов.
Применение при нарушениях функции почек
С осторожностью следует применять препарат при нефролитиазе.
Применение у детей
Противопоказан в детском и подростковом возрасте до 18 лет.
Особые указания
При артериальной гипертензии может потребоваться коррекция доз гипотензивных препаратов.
У больных сахарным диабетом лечение следует проводить под контролем концентрации глюкозы в крови.
В период лечения возможно интенсивное окрашивание мочи в желтый цвет.
Влияние на способность к управлению транспортными средствами и механизмами
Цитофлавин® не оказывает влияния на способность к управлению транспортными средствами и механизмами.
Передозировка
До настоящего времени случаев передозировки препарата Цитофлавин® установлено не было.
Лекарственное взаимодействие
Янтарная кислота, инозин и никотинамид совместимы с другими лекарственными средствами.
Рибофлавин уменьшает активность некоторых антибиотиков (тетрациклинов, эритромицина, линкомицина), несовместим со стрептомицином. Этанол, трициклические антидепрессанты, блокаторы канальцевой секреции снижают абсорбцию рибофлавина, а тиреоидные гормоны ускоряют его метаболизм.
Условия хранения препарата Цитофлавин®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре не выше 25°C.
Срок годности препарата Цитофлавин®
Срок годности — 3 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ПОЛИСАН НТФФ ООО
(Россия)

|
|
192102 Санкт-Петербург |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код