Капсулы твердые желатиновые цилиндрической формы с полусферическими концами бежевого цвета.
1 капсула содержит:
Активные вещества: Диосмин — 225,0 мг; Каштана конского семян экстракт сухой (12-15:1, экстрагент этанол 70% об/об) — 125,0 мг.
Вспомогательные вещества: магния стеарат, кремния диоксид коллоидный безводный, картофельный крахмал.
Состав желатиновой капсулы:
Желатин, вода очищенная, титана диоксид Е-171, железа оксид желтый Е-172.
Средства, снижающие проницаемость капилляров.
Код ATX: С05С
Диосмин плюс — комбинированный препарат, обладающий флеботонизирующим, ангиопротекторным, антиоксидантным, противоэкссудативным и противовоспалительным действием.
Диосмин обладает флеботонизирующим действием: уменьшает растяжимость вен, повышает тонус вен (дозозависимый эффект), уменьшает венозный застой; улучшает лимфатический дренаж (повышает тонус и частоту сокращения лимфатических капилляров, увеличивает их функциональную плотность, снижает лимфатическое давление), улучшает микроциркуляцию (повышает резистенстность капилляров (дозозависимый эффект), уменьшает их проницаемость); уменьшает адгезию лейкоцитов к венозной стенке и их миграцию в паравенозные ткани; улучшает диффузию кислорода и перфузию в кожной ткани, обладает противовоспалительным действием. Усиливает сосудосуживающее действие адреналина, норадреналина, блокирует выработку свободных радикалов, синтез простагландинов и тромбоксана.
Главный компонент Каштана конского семян экстракта сухого, тритерпенгликозид эсцин, оказывает противоэкссудативное, флеботонизирующее и противовоспалительное действие. Экстракт снижает концентрацию лизосомальных энзимов, в результате чего, предотвращается распад гликокаликса (мукополисахаридов) в стенках капилляров. Благодаря снижению проницаемости капилляров достигается нормализация патологически повышенной проницаемости сосудов, наблюдаемой при хронической венозной недостаточности. Это приводит к физиологическому балансу между фильтрацией и поглощением воды, отсутствие которого при повышенной скорости фильтрации из-за высокой проницаемости сосудов также приводит к возникновению отеков. Каштана конского экстракт снижает фильтрацию, предотвращает появление отеков и помогает достичь водного баланса на протяжении периода уменьшения отека.
— Лечение (в составе комплексной терапии) симптомов венозно-лимфатической недостаточности (тяжесть, отечность и боль в ногах, трофические нарушения).
Внутрь. Взрослым: по 1 капсуле 3 раза в день вместе с приемом пищи.
Продолжительность приема определяет лечащий врач.
Пожилые пациенты:
рекомендуется уменьшить дозу до 2 капсул в день.
Пациенты с почечной недостаточностью: нет данных о необходимости корректировки дозы.
Пациенты с печеночной недостаточностью: рекомендуется уменьшить дозу до 2 капсул в сутки.
Дети и подростки до 18 лет: не рекомендуется.
Нежелательные реакции классифицируют в зависимости от частоты их возникновения:
| Очень часто | ≥1/10 |
| Часто | от ≥1/100 до <1/10 |
| Нечасто | от ≥1/1000 до <1/100 |
| Редко | от ≥1/10000 до <1/1000 |
| Очень редко | от >1/10000 |
| Частота неизвестна | не может быть оценена на основе имеющихся данных. |
Диосмин:
Со стороны нервной системы: редко — головокружение, головная боль, общее недомогание.
Со стороны пищеварительной системы: часто — диарея, тошнота, рвота, диспепсия; нечасто — колит.
Нарушения со стороны кожных покровов и подкожной ткани: редко — сыпь, зуд, крапивница; неуточненной частоты — изолированный отек лица, губ, век; в исключительных случаях — ангионевротический отек.
Каштана конского семян экстракт сухой:
Со стороны пищеварительной системы: нечасто — тошнота, рвота, диарея, боли в желудке и животе.
Со стороны нервной системы: нечасто — головокружение, головная боль.
Со стороны сердечно-сосудистой системы: очень редко — артериальная гипертензия, тахикардия.
Реакции гиперчувствительности: редко — реакции гиперчувствительности со стороны кожи (зуд, сыпь, эритема, экзема); очень редко — тяжелые аллергические реакции (в некоторых случаях с кровотечением).
Со стороны половой системы: очень редко — гинекологические кровотечения между менструациями.
В случае появления любого из перечисленных побочных действий прекратите прием препарата и обратитесь к врачу.
— повышенная чувствительность к компонентам препарата
— беременность и лактация
— детский возраст до 18 лет
Не рекомендуется пациентам с тяжелой печеночной недостаточностью, нарушениями коагуляции.
Диосмин:
Случаи передозировки диосмина не описаны.
Каштана конского семян экстракт сухой:
Сапонины, содержащиеся в семенах конского каштана, при передозировке могут способствовать усилению побочного эффекта — тошноты, также могут вызывать рвоту и понос. Для принятия мер по устранению этих симптомов необходимо проконсультироваться с врачом.
Лечение:
— если после приема большого количества препарата рвота отсутствует, рекомендуется провести промывание желудка (например, 0,02%-ным раствором перманганата калия) и принять активированный уголь;
— в других случаях проводится симптоматическое лечение.
При нарушениях венозного кровообращения максимальный эффект лечения наблюдается при здоровом, сбалансированном образе жизни, при этом необходимо избегать длительного пребывания на солнце, длительного стояния на ногах, увеличения веса тела, совершать пешие прогулки.
Пациентам следует неукоснительно соблюдать назначенные врачом дополнительные лечебные меры, такие как ношение компрессионного лечебного трикотажа (гольфы, чулки), компрессы, прохладный душ на область нижних конечностей и т.д.
Если возникают аномально сильные жалобы, в особенности — на состояние ног, которые характеризуются воспалением, изменением цвета кожи, чувством напряжения или жара, уплотнениями под кожей, болями, язвами, тромбофлебитом, отеком одной или обеих ног, следует незамедлительно обратиться к врачу, так как данные симптомы могут являться признаками серьезного заболевания (тромбоза вен нижних конечностей). То же относится к признакам сердечной и почечной недостаточности.
При одновременном применении с антикоагулянтами следует регулярно контролировать параметры свертывания крови.
Применение у детей
Не применять у детей.
Препарат может усиливать действие антикоагулянтов при совместном применении из-за способности эсцина вытеснять антикоагулянты из связи с белками крови.
Применение при беременности и кормлении грудью не было достаточно исследовано. Не рекомендуется прием препарата во время беременности и в период лактации.
Нет данных об отрицательном влиянии препарата на способность управлять транспортными средствами и другими механизмами.
В защищенном от влаги и света месте при температуре не выше 25°C.
Хранить в недоступном для детей месте.
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
По 10 капсул в контурной ячейковой упаковке из пленки поливинилхлоридной и фольги алюминиевой. По 3 или по 6 контурных упаковок вместе с инструкцией по медицинскому применению помещают в пачку из картона.
Без рецепта врача
Производитель
Иностранное производственное унитарное предприятие «Мед-интерпласт», 222603, Минская область, г. Несвиж, ул. Ленинская, 115, ком. 204, Республика Беларусь.
Флексотрон плюс — инструкция по применению
Синонимы, аналоги
Статьи
Наименование медицинского изделия
Имплантат вязкоэластичный стерильный для внутрисуставных инъекций ФЛЕКСОТРОН® Плюс (FLEXOTRON® Plus), на основе гиалуроната натрия, 20 мг/мл, 3 мл.
Имплантат представляет собой бесцветный, прозрачный, вязкий и стерильный гель (гидрогель). Имплантат не включает в себя лекарственные средства, производные клеток и тканей человека, ткани животных. Не имеет радиационных и электромагнитных свойств.
Состав:
| Ингредиент | Содержание |
| гиалуронат натрия (C14H2DNNaO11)n | 2% |
| Солевой раствор фосфатного буфера: | |
| Na2HPO4*12H2O | 0,06% |
| NaH2PO4*2H2O | 0,0048% |
| Хлорид натрия | 0,89% |
| Вода для инъекций | сколько требуется до 100% (3 мл) |
Технические характеристики:
Описание
Имплантат для замещения синовиальной жидкости ФЛЕКСОТРОН® Плюс поставляется в стеклянном шприце и содержит гиалуроновую кислоту. Продукт представляет собой бесцветный, прозрачный, вязкоупругий и стерильный раствор. Гиалуроновую кислоту (молекулярная масса 650000-1200000 Да) экстрагируют из микроорганизмов. Продукт предназначен только для одноразового применения.
Гиалуроновая кислота является естественным полисахаридом, который входит в состав всех тканей организма, при этом в особенно большой концентрации гиалуроновая кислота содержится в коже, подкожных тканях, а также в соединительной ткани, такой как синовиальная жидкость. Гиалуроновая кислота принадлежит к небольшой группе веществ, одинаковых для всех живых организмов, поэтому она обладает высокой биосовместимостью. В 1 мл продукта содержится 20 мг натрия гиалуроната, растворенного в физиологическом растворе.
Не подлежит техническому обслуживанию.
Комплект поставки
Одна единица продукции включает:
Стерильность
Изделие проходит финишную стерилизацию автоклавированием в соответствии с EN 556-1. Валидация данного процесса осуществляется в соответствии со стандартами ISO 11138-3 и ISO 17665-1 для подтверждения стерильности.
Назначение
Вязкоэластичное протезирование синовиальной жидкости у пациентов с дегенеративно-дистрофическими и посттравматическими поражениями суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Показания к применению
Способ применения
Инъекции выполняются медицинскими специалистами в асептических условиях. Перед введением имплантата содержимое шприца должно быть визуально оценено на прозрачность и однородность. Помутнение, кристаллизация, появление окраски и/или инородных включений может свидетельствовать о нарушении правил транспортировки и хранения изделия. При появлении вышеуказанных признаков введение средства для замещения синовиальной жидкости запрещено.
Имплантат вводится внутрисуставно в асептических условиях процедурных и манипуляционных кабинетов.
Перед проведением инъекции необходимо удалить покрывающую мембрану и извлечь наполненный шприц с имплантатом из блистера.
Вручную прикрепить адаптер для пальцев к упору цилиндра шприца.
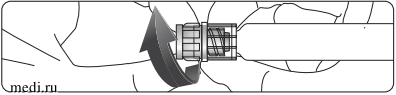
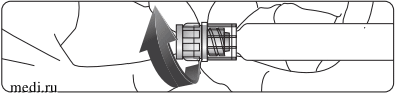
Придерживая люэровский наконечник, аккуратно открутить колпачок наконечника шприца (как показано ниже). Избегать чрезмерных нагрузок на шприц при фиксации иглы для предотвращения деформации механизма Луер-Лок.
Продолжая крепко удерживать люэровский наконечник, прикрутить стерильную иглу рекомендуемым размером 21G или 23G (не входят в комплект поставки) к защелке шприца до тех пор, пока она не будет закреплена. Длина иглы выбираться врачом в соответствии с конституцией человека и толщиной подкожной клетчатки в месте пункции. Перед инъекцией выпустить из шприца пузырьки воздуха в случае их наличия.
Вводить медленно. Пациент должен избегать любых физических нагрузок или весовых нагрузок в течение 48 часов после внутрисуставной инъекции.
На курс лечения рекомендуется 3 шприца. Для лечения остеоартрита / остеоартроза (OA) суставов у взрослых проводят 1 инъекцию в неделю. Количество и частота инъекций могут изменяться в зависимости от тяжести симптоматики.
Ожидаемая эффективность и принцип работы
Молекула гиалуроновой кислоты имеет спиральную длинноцепочечную структуру, которая позволяет удерживать или поглощать молекулы воды. Внутрисуставное обогащение синовиальной жидкости инъекциями гиалуроната натрия способствует улучшению или восстановлению вязкоупругих свойств естественной синовиальной жидкости. Гиалуронат натрия отвечает за вязкоупругие свойства синовиальной жидкости, таким образом вязкоэластичное протезирование позволяет компенсировать недостаточность гиалуроновой кислоты в синовиальной жидкости или снижение её вязкости, смягчить внешние нагрузки на сустав, обеспечивает смазывание, восстановление упругости и вязкости, амортизацию, увлажнение и обволакивание суставных поверхностей, покрывая смазывающим защитным слоем хрящ и рецепторы синовии. Это помогает увеличить объём движений и обеспечивает механическую защиту тканей полости сустава, что в свою очередь может улучшать течение остеоратроза / остеоартрита и других дегенеративно-дистрофических и посттравматических патологий суставов.
Ожидаемая продолжительность эффекта составляет 6 месяцев после проведения курса лечения.
Противопоказания
Меры предосторожности
По причине того, что септический артрит является серьезным побочным эффектом, необходимо соблюдать все стандартные меры предосторожности для хирургических вмешательств.
При получении аспирационной жидкости перед проведением вязкоэластичного протезирования следует провести соответствующие исследования для исключения бактериальной этиологии артрита.
Изделие предназначено для внутрисуставного введения. Необходимо избегать внутрисосудистого или внутритканевого введения изделия.
Изделие следует использовать до истечения срока годности, указанного на упаковке.
Применять с осторожностью у пациентов с аллергией, а также у пациентов с заболеваниями печени.
В первые дни после инъекции может быть рекомендован пероральный прием анальгетиков или противовоспалительных лекарственных средств. Применение изделия совместно с четвертичными соединениями аммония запрещено.
Только для одноразового использования. Повторная стерилизация и применение изделия запрещены по причине наличия риска возникновения инфекции, перекрестной инфекции и (или) дефекта изделия. Не использовать шприц из открытой и/или поврежденной стерильной упаковки. Не использовать шприц с открытым или поврежденным колпачком стерильного шприца. При нарушении стерильности или подозрении о нарушении стерильности имплантата изделие должно быть утилизировано.
Пожилые пациенты
Применять с осторожностью ввиду общего снижения функциональной активности органов и систем организма.
Беременность и лактация
Применять в случае, если преимущество лечения превышает риск развития нежелательных явлений. Во время лечения кормление грудью следует прекратить.
Дети
Безопасность применения продукта у детей изучена недостаточно, поэтому применять с осторожностью.
Возможные побочные эффекты
Применение внутрисуставных форм гиалуроновой кислоты при дегенеративно-дистрофических и посттравматических поражениях суставов является хорошо изученным методом с установленным профилем безопасности, применяющимся на протяжении нескольких десятилетий.
К основным побочным эффектам относятся боль, отек и скованность в суставе после инъекции.
В крайне редких случаях возможно проявление местных воспалительных симптомов (повышение температуры, покраснение и отечность, увеличение содержания экссудата в полости сустава). После внутрисуставной инъекции могут возникать такие обратимые местные реакции, как кратковременное ограничение подвижности, чувство дискомфорта или тяжести в суставе. Проявление данных симптомов можно уменьшить прикладыванием льда к месту инъекции в течение 5-10 минут.
Имеются сообщения о единичных случаях аллергических реакций (например, зуд, сыпь, крапивница) и анафилактических реакций, септического артрита, внутритканевых кровоизлияниях или кровоизлияниях в полость сустава, тендинитах, флебитах, парестезиях, головокружениях, головных болях, мышечных спазмах, чувстве жара, общем недомогании, периферических отеков при внутрисуставном введении растворов гиалуроновой кислоты.
При появлении местных или общих симптомов следует проконсультироваться с врачом.
Извлечение имплантата
В случае выраженных проявлений может быть рекомендовано удаление имплантата из полости сустава, в том числе с применением лаважа согласно действующим клиническим рекомендациям. Запрещаются повторные инъекции имплантатов синовиальной жидкости в сустав до купирования симптомов острого воспаления!
Хранение и транспортировка
Хранить и транспортировать при температуре от 2 °C до 30 °C, в оригинальной упаковке. Беречь от воздействия прямых солнечных лучей. Не замораживать.
Срок годности:
3 года.
Защита окружающей среды и утилизация
Содержание шприца не является токсичным или огнеопасным. Изделия при использовании, транспортировке и хранении не оказывают негативного воздействия на окружающую среду.
Неиспользованные шприцы могут быть утилизированы в качестве бытовых отходов. Стекло следует утилизировать с осторожностью.
Неиспользованное содержимое шприца до или после истечения срока годности может быть утилизировано в качестве бытовых отходов (слить с большим количеством воды).
Уничтожение использованных медицинских изделий осуществляется в соответствии с природоохранными требованиями национальных, местных и ведомственных руководящих положений о безопасном уничтожении и утилизации.
В соответствии с санитарно-эпидемиологическими правилами и нормативами СанПиН 2.1.7.2790-10 использованные медицинские изделия (шприцы с имплантатами) относятся к медицинским отходам класса Б (эпидемиологически опасные отходы).
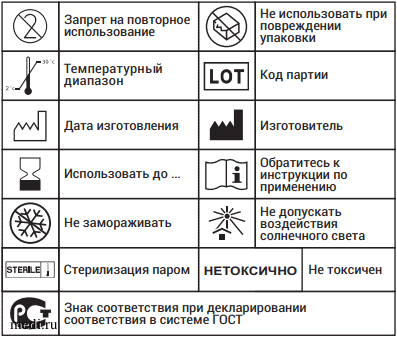
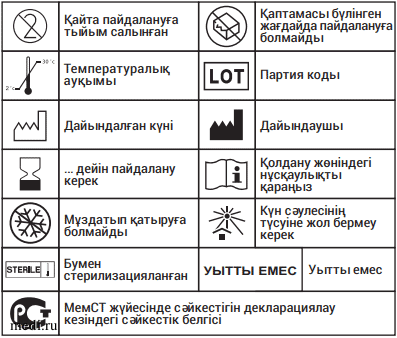
Расшифровка символов на упаковке
Гарантийные обязательства
Гарантийный срок соответствует сроку годности изделия. Срок годности медицинского изделия составляет 3 года.
Производитель гарантирует качество изделий и соответствие заявленным техническим спецификациям в течение всего срока годности при соблюдении условий эксплуатации, транспортирования и хранения. Производитель или его уполномоченный представитель предоставляет информацию и рекомендации в отношении рисков, а также предписания, методы и технические приемы для применения изделия.
Компания-производитель снимает с себя всю ответственность и отказывается от гарантийных обязательств в связи с травмами пациента или ущербом, который может иметь место в результате:
1. Выбранного способа применения и технического приема введения имплантата при несоблюдении установленных рекомендаций.
2. Неподходящего назначения, выбора использования для конкретного пациента.
3. Использования изделия после истечения указанного срока годности или при нарушениях правил хранения и транспортировки.
Производитель
«СайВижн Байотек Инк.», Тайвань.
(SciVision Biotech Inc., 9, South 6th Rd., K.E.P.Z., Kaohsiung 806, Taiwan, R.O.C.)
Уполномоченный представитель производителя
Общество с ограниченной ответственностью «МКНТ Импорт» (ООО «МКНТ Импорт»), 119071, город Москва, улица Орджоникидзе, дом 12, стр. 2, Российская Федерация
Уполномоченный представитель производителя в России наделен правами обеспечения процессов прослеживаемости продукции и послерегистрационного мониторинга безопасности медицинского изделия в целях выявления и предотвращения побочных действий, не указанных в инструкции по применению, нежелательных реакций при применении медицинского изделия, особенностей взаимодействия медицинских изделий между собой, фактов и обстоятельств, создающих угрозу жизни и здоровью граждан и медицинских работников. Для выполнения данных функций ООО «МКНТ Импорт», действуя в качестве уполномоченного представителя, или/и его доверенные лица наделены правом собирать послерегистрационные данные, доводить до субъектов обращения информацию по безопасности, вовлекаться в мероприятия по выполнению корректирующих и превентивных действий, а также заключать соответствующие соглашения по обмену данными в отношении этой продукции, если это не противоречит законодательству Российской Федерации и Евразийского Экономического Союза.
Уполномоченный представитель производителя и организация, отвечающая за пострегистрационное наблюдение за безопасностью и принимающая претензии от потребителей на территории Республики Казахстан: ТОО «ТопМед», Республика Казахстан, 050067, Алматы, Бостандыкский район, Садоводческое товарищество Природа, дом 49.
Изделие соответствует требованиям следующих национальных стандартов производителя ISO 13485: 2016; ISO 14630:2012; IEC 62366-1:2015; ISO 14602:2010; EN ISO 14971:2012; ISO 14155:2011; USP; Ph. Eur.; ISO 10993-1:2018; ISO 10993-3:2014; ISO 10993-5:2009; ISO 10993-6:2016; ISO 10993-10:2010; ISO 10993-11:2017; ISO 10993-12:2012; ISO 10993-18:2005; ASTM F1980-16:2016; EN 556-1:2001; ISO 11138-1:2017; ISO 11138-3:2017; ISO 11737-1:2018; ISO 11737-2:2009; ISO 17665-1:2006; ISO 14644-1:2015; ISO 14644-2:2015; ISO 13408-1:2008; ISO 11607-1:2019; ISO 11607-2:2019; ISO 11040-8:2016; ISO 80369-7:2016
Медициналық бұйымның атауы
Буынішілік инъекцияларға арналған, натрий гиалуронаты негізіндегі стерильді, тұтқыр созылғыш ФЛЕКСОТРОН® Плюс (FLEXOTRON® Plus) имплантаты, 20 мг/мл, 3 мл.
Имплантат түссіз, мөлдір, тұтқыр жане стерильді гель (гидрогель) болып табылады. Имплантаттың құрамында дәрілік заттар, адам жасушалары мен тіндерінің туындылары, жануарлар тіндері жоқ. Радиациялық жане электромагниттік қасиеттері жоқ.
Құрамы:
| Ингредиент | Құрамы |
| Натрий гиалуронаты (C14H2cNNaO11)n | 2% |
| Фосфатты буфердің тұзды ерітіндісі: | |
| Na2HPO4*12H2O | 0,06% |
| NaH2PO4*2H2O | 0,0048% |
| Натрий хлориді | 0,89% |
| Инъекцияға арналған су | 100% (3 мл) дейін қажетінше |
Техникалық сипаттамалары:*
Сипаттамасы
Синовиальді сұйықтықты алмастыруға арналған ФЛЕКСОТРОН® Плюс имплантаты шыны шприцте жеткізіледі жане құрамында гиалурон қышқылы бар. Өнім түссіз, мөлдір, тұтқыр серпімді жане стерильді ерітінді болып табылады. Гиалурон қышылы (молекулалық салмағы 650000-1200000 Да) микроорганизмдерден экстракцияланады. Өнім тек бір рет қолдануға арналған.
Гиалурон қышқылы организмнің барлық тіндерінің құрамына кіретін табиғи полисахарид болып табылады, сонымен қатар, асіресе, көп концентрациясында гиалурон қышқылы теріде, теріасты тіндерінде, сондай-ақ, синовиальді сұйықтық сияқты данекер тінде болады. Гиалурон қышқылы барлық тірі организмдер үшін бірдей заттардың шағын тобына жатады, сондықтан оның биоүйлесімділігі жоғары. 1 мл өнімнің құрамында физиологиялық ерітіндіде ерітілген 20 мг натрий гиалуронаты болады.
Техникалық қызмет көрсетілмейді.
Жеткізілім жиынтығы
Өнімнің бір бірлігі келесілерден құралған:
Стерильділігі
Бұйым EN 556-1ге сайкес автоклавтау арқылы ақырғы рет стерилизацилаудан өтеді. Бұл үдерісті валидациялау стерильділігін растау үшін ISO 11138-3 жане ISO 17665-1 стандарттарына сәйкес жүзеге асырылады.
Тағайындалуы
Буындардың дегенерациялық-дистрофиялық жане жарақаттан кейінгі зақымданулары бар пациенттерде, сондай-ақ, зақымданған буындарына көп күш түсетін адамдарда синовиальді сұйықтықты тұтқыр созылғыш протездеу үшін
Қолданылуы
Қолдану тәсілі
Инъекцияларды дарігер-мамандар асептикалық жағдайларда жүргізеді.
Имплантатты енгізер алдында шприцтің ішіндегісінің мөлдірлігі мен біртектілігі көзбен қарап бағалануы тиіс. Бұлыңғырлануы, кристалдануы, түсінің өзгеруі жане/немесе бөгде қосылыстардың пайда болуы бұйымды тасымалдау жане сақтау шарттарының бұзылғанын білдіруі мүмкін. Жоғарыда аталған белгілер пайда болған жағдайда, имплантатты енгізуге тыйым салынады.
Имплантат емшара жане манипуляция кабинеттерінде асептикалық жағдайларда буын ішіне енгізіледі.
Инъекция жүргізер алдында жауып тұрған жарғақшасын алып тастау жане имплантат толтырылған шприцті блистерден шығарып алыңыз.
Саусаққа арналған адаптерді шприц цилиндрінің түбіне қолмен бекемдеңіз.
Люэр ұштығынан ұстап тұрып, шприц ұштығының қалпақшасын абайлап бұрап ағытып алыңыз (төменде көрсетілгендей). Луер-Лок механизмінің деформациялануына жол бермеу үшін, инені бекемдеген кезде шприцке шамадан тыс күш салмаңыз.
Люэр ұштығын мықтап ұстап тұрып, ұсынылған 21G немесе 23G өлшемдегі (жеткізілім жиынтығына кірмейді) стерильді инені шприцтің ілмегіне бекемделгенге дейін бұрап кіргізіңіз. Иненің ұзындығын дарігер адамның конституциясына жане пункция орнындағы теріасты шелінің қалыңдығына сайкес таңдайды. Шприцте ауа көпіршіктері болса, инъекция алдында оларды шығарып жіберу керек.
Баяу енгізу керек. Пациент кез келген буынішілік инъекциядан кейінгі 48 сағат ішінде дене жүктемелерінен немесе салмақ жүктемелерінен сақтануы тиіс.
Бір емдеу курсына 3 шприц ұсынылады. Ересектерде буындардың остеоартритін / остеоартрозын (OA) емдеу үшін аптасына 1 инъекциясын жүргізеді. Инъекциялардың саны мен жиілігі симптоматиканың ауырлығына байланысты өзгеріп отыруы мүмкін.
Күтілетін тиімділігі және жұмыс істеу принципі
Гиалурон қышқылының молекуласы шиыршықты ұзын тізбекті құрылымыға ие, ол су молекулаларын ұстап тұруға немесе сіңіруге мүмкіндік береді. Буынішілік синовиальді сұйықтықтың натрий гиалуронаты инъекцияларымен байытылуы табиғи синовиальді сұйықтықтың тұтқыр серпімді қасиеттерінің жақсаруына немесе қалпына келуіне ықпал етеді. Натрий гиалуронаты синовиальді сұйықтықтың тұтқыр серпімді қасиеттерінне жауап береді, сол арқылы тұтқыр созылғыш протездеу синовиальді сұйықтықтағы гиалурон қышқылы жеткіліксіздігінің жане оның тұтқырлығы төмендеуінің орнын толтыруға, буынға түсетін сыртқы жүктемелерді жеңілдетуге мүмкіндік береді, шеміршек пен синовия рецепторларын майлағыш қорғағыш қабатпен жаба отырып, буын беткейлерінің майлануын, серпімділігі мен тұтқырлығының қалпына келуін, амортизациясын, ылғалдануы мен жабылуын қамтамасыз етеді. Бұл қимыл-қозғалыс көлемін арттыруға көмектеседі жане буын қуысы тіндерінің механикалық қорғанысын қамтамасыз етеді, ол өз кезегінде остеоратроз / остеоартрит және буындардың басқа дегенерациялық-дистрофиялық жане жарақаттан кейінгі патологияларының ағымын жақсартуы мүмкін.
Әсерінің күтілетін ұзақтығы емдеу курсын жүргізгеннен кейін 6 айды құрайды.
Қолдануға болмайтын жағдайлар
Сақтық шаралары
Сепсистік артрит ауыр жағымсыз эсер болып табылатындығы себепті, хирургиялық араласымдарға арналған барлық стандартты сақтық шараларын сақтау қажет.
Аспирациялық сұйықтық алу кезінде тұтқыр созылғыш протездеуді енгізер алдында артриттің бактериялық этиологиясы бар-жоқтығын анықтау үшін сэйкесінше зерттеулер жүргізу керек.
Бұйым буын ішіне енгізуге арналған. Бұйымды тамыр ішіне немесе тін ішіне енгізбеу қажет.
Бұйымды қаптамасында көрсетілген жарамдылық мерзімі өткенге дейін пайдалану керек.
Аллергиясы бар пациенттерде, сондай-ақ, бауыр ауруары бар пациенттерде сақтықпен қолдану керек.
Инъекциядан кейінгі алғашқы күндері анальгетиктерді немесе қабынуға қарсы дэрілік заттарды пероральді қабылдау пайдалы болуы мүмкін. Бұйымды төртіншілік аммоний қосылыстарымен бірге қолдануға тыйым салынады.
Тек бір рет пайдалануға арналған. Инфекцияның, айқаспалы инфекцияның жане (немесе) бұйым ақауының туындау қаупінің болуы себепті, бұйымды қайта стерилизациялауға жэне қолдануға тыйым салынады. Стерильді қаптамасы ашылған жане/немесе бүлінген шприцті пайдалануға болмайды. Стерильді шприцтің қалпақшасы ашылып қалған немесе бүлінген шприцті пайдалануға болмайды. Имплантаттың стерильділігі бұзылған немесе стерильділігі бұзылғандығына күдік болған жағдайда, бұйым утилизациялануы тиіс
Егде жастағы пациенттер
Организм ағзалары мен жүйелерінің функционалдық белсенділігінің жалпы төмендейтіндігіне байланысты, сақтықпен қолдану керек.
Жүктілік және лактация
Егер емдеудің артықшылығы жағымсыз құбылыстардың даму қаупінен асып түсетін болса ғана қолдану керек. Емдеу кезінде бала емізуді тоқтату керек.
Балалар
Өнімнің балаларда қолданылуының қауіпсіздігі жеткіліксіз зерттелген, сондықтан сақтықпен қолдану керек.
Болуы мүмкін жағымсыз әсерлері
Буындардың дегенерациялық-дистрофиялық жане жарақаттан кейінгі зақымданулары кезінде гиалурон қышқылының буынішілік түрерін қолдану қауіпсіздік бейіні анықталған, бірнеше онжылдықтар бойы қолданып келе жатқан, жақсы зерттелген адіс болып табылады.
Негізгі жағымсыз асерлеріне инъекциядан кейін буынның ауыруы, ісінуі жане құрысуы жатады.
Аса сирек жағдайларда жергілікті уақытша қабыну симптомдары (ауыру, температура жоғарылауы, қызару жане ісіну, буын қуысындағы экссудат мөлшерінің артуы) көрініс беруі мүмкін. Буынішілік инъекциядан кейін қимыл-қозғалыстың қысқа мерзімді шектелуі, буындағы жайсыздық немесе ауырлық сезімі, гематомалар сияқты қайтымды жергілікті реакциялар туындауы мүмкін. Ондай симптомдардың көрініс беруін инъекция орнына 5-10 минут бойы мұз басу арқылы азайтуға болады.
Гиалурон қышқылы ерітінділерін буын ішіне енгізген кездегі аллергиялық реакциялар (мысалы, қышыну, бөртпе, есекжем) мен анафилаксиялық реакциялардың бірен-саран жағдайлары, сепсистік артрит, тінішілік қан кетулер немесе буын қуысына қан құйылулар, тендениттер, флебиттер, парестезиялар, бас айналуы, бас ауыруы, бұлшықеттердің түйілулері, ысыну сезімі, жалпы дімкастану, шеткері ісінулер туралы хабарламалар бар.
Жергілікті немесе жалпы симптомдар пайда болған жағдайда, дарігермен кеңесу керек.
Имплантатты шығарып алу
Айқын көріністер болған жағдайда, имплантатты буын куысынан алып тастау, соның ішінде, қолданыстағы клиникалық ұсынымдарға сайкес лаважды қолданып алып тастау ұсынылуы мүмкін. Жедел қабыну симптомдары басылғанға дейін имплантаттарды буынға синовиальді сұйықтыққа қайта инъекциялауға тыйым салынады!
Сақтау және тасымалдау
2 °С-ден 30 °С-ге дейінгі температурада түпнұсқалық қаптамасында сақтау жане тасымалдау керек. Тікелей түсетін күн саулесінің асерінен қорғау керек. Мұздатып қатыруға болмайды.
Жарамдылық мерзімі:
3 жыл.
Қоршаған ортаны қорғау және утилизациялау.
Шприцтің ішіндегісі уытты немесе өртке қауіпті емес. Бұйымдар пайдалану, тасымалдау жане сақтау кезінде қоршаған ортаға теріс асер етпейді.
Пайдаланылмаған шприцтерді тұрмыстық қалдықтар ретінде утилизациялауға болады. Шыныларды сақтықпен утилизациялау керек. Пайдаланылмаған шприцтің ішіндегісін жарамдылық мерзімі өткенге дейін немесе өткеннен кейін тұрмыстық қалдықтар ретінде утилизациялауға (мол сумен ағызып жіберуге) болады.
Пайдаланылған медициналық бұйымдарды жою қауіпсіз жою жане утилизациялау туралы Ұлттық, жергілікті жэне ведомстволық басшылық ережелердің табиғат қорғау талаптарына сайкес жүзеге асырылады.
Санитарлық-эпидемиологиялық ережелер мен СанЕмН 2.1.7.2790-10 нормативтеріне сэйкес пайдаланылған медициналық бұйымдар (имплантанттары бар шприцтер) Б класының медициналық қалдықтарына (эпидемиологиялық қауіпті қалдықтар) жатады.
Қаптамасындағы символдардың түсіндірмесі
Кепілдік міндеттемелері
Кепілдік мерзімі бұйымның жарамдылық мерзіміне сайкес келеді. Медициналық бұйымның жарамдылық мерзімі 3 жылды құрайды.
Өндіруші бұйымдардың сапасына жэне пайдалану, тасымалдау жане сақтау шарттары сақталған жағдайда барлық жарамдылық мерзімі бойына, малімденген техникалық сипаттамаларына сайкес келетіндігіне кепілдік береді. Өндіруші немесе оның уакілетті өкілі бұйымды қолдану үшін қауіптеріне, сондай-ақ, кеңестер, адістері мен техникалық тасілдеріне қатысты ақпарат жане нұсқау береді.
Өндіруші компания келесілердің:
1. Таңдалған қолдану тасілінің жане имплантты енгізудің бекітілген ұсынымдары сақталмаған техникалық адісінің.
2. Үйлесімсіз тағайындалуының, пайдалану үшін нақты бір пациенттің таңдалуының.
3. Бұйымды жарамдылық мерзімі өткеннен кейін немесе сақтау жане тасымалдау ережелерін бұза отырып пайдаланудың, натижесінде орын алуы мүмкін пациенттің жарақаттануына немесе зиян шегуіне жауап бермейді жане сонымен байланысты кепілдік міндеттемелерінен бас тартады.
Өндіруші
«СайВижн Байотек Инк.», Тайвань. (SciVision Biotech Inc., 9, South 6th Rd., K.E.P.Z., Kaohsiung 806, Taiwan, R.O.C.)
Өндірушінің Ресейдегі уәкілетті өкілі
«МКНТ Импорт» жауапкершілігі шектеуі қоғамы («МКНТ Импорт» ЖШҚ) 119071, Маскеу қаласы, Орджоникидзе көшесі, 12 үй, 2 құр., Ресей Федерациясы
Өндірушінің Ресейдегі уакілетті өкіліне медициналық бұйымды қолдану кезінде қолдану жөніндегі нұсқаулықта көрсетілмеген жағымсыз асерлерін, медициналық бұйымдардың өзара арекеттесулерінің ерекшеліктерін, азаматтар мен медицина қызметкерлерінің өмірі мен денсаулығына қауіп төндіретін фактілер мен жағдайларды анықтау жане алдын алу мақсаттарында, өнімнің қадағалану үдерістерін жане медициналық бұйымның тіркеуден кейінгі қауіпсіздігін мониторингілеуді қамтамасыз ету құқықтары берілген. Аталған функцияларды атқару үшін, уакілетті өкіл ретінде арекет ететін «МКНТ
Импорт» ЖШК, жане/немесе оның сенімді тұлғаларына тіркеуден кейінгі деректерді жинақтап, қауіпсіздігі жөніндегі ақпараттар айналымы саласындағы субъектілерге хабарлау, түзетушілік жане превентивтік арекеттерді атқару шараларына қатысу, сондай-ақ, егер бұл Ресей Федерациясы мен Еуразиялық Экономикалық Одақтың заңдарына қайшы келмесе, осы өнімге қатысты деректер алмасу үшін тиісінше келісімдер жасасу құқығы берілген.
Бұйым өндірушінің келесі ұлттық стандарттарының талаптарына сайкес келеді ISO 13485: 2016; ISO 14630:2012; IEC 62366-1:2015; ISO 14602:2010; EN ISO 14971:2012; ISO 14155:2011; USP; Ph. Eur.; ISO 10993-1:2018; ISO 10993-3:2014; ISO 10993-5:2009; ISO 10993-6:2016; ISO 10993-10:2010; ISO 10993-11:2017; ISO 10993-12:2012; ISO 10993-18:2005; ASTM F1980-16:2016; EN 556-1:2001; ISO 11138-1:2017; ISO 11138-3:2017; ISO 11737-1:2018; ISO 11737-2:2009; ISO 17665-1:2006; ISO 14644-1:2015; ISO 14644-2:2015; ISO 13408-1:2008; ISO 11607-1:2019; ISO 11607-2:2019; ISO 11040-8:2016; ISO 80369-7:2016
Қазақтан Республикасы аумағында қолайсыз оқиғаларды (инциденттерді) мониторингілеу жөніндегі уәкілетті өкілдің байланыс деректері:
«ТопМед» жШс, Қазақстан Республикасы, 050067, Алматы, Бостандық ауданы, Природа бау-бақша серіктестігі 49 үй.
Осыған сәйкес медициналық мақсаттағы бұйым өндірілген нормативтік құжаттың атауы (белгіленуі ):
Техникалықфайл 30.07.2020
Купить Флексотрон плюс в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Бускопан® (Таблетки)
МНН: Гиосцина бутилбромид
Производитель: Делфарм Реймс С. А. С.
Анатомо-терапевтическо-химическая классификация: Butylscopolamine
Номер регистрации в РК:
№ РК-ЛС-5№016087
Информация о регистрации в РК:
12.05.2020 — бессрочно
Информация о реестрах и регистрах
- Скачать инструкцию медикамента
Торговое название
БУСКОПАН
Международное непатентованное название
Нет
Лекарственная форма
Таблетки, покрытые сахарной оболочкой, 10 мг
Состав
Одна таблетка содержит
активное вещество — гиосцина бутилбромид 10 мг,
вспомогательные вещества: кальция гидрофосфат безводный, крахмал кукурузный высушенный, крахмал растворимый, кремния диоксид коллоидный, кислота винная, кислота стеариновая/пальмитиновая,
состав оболочки: поливинилпирролидон, сахароза, тальк, гуммиарабик (аравийская камедь), титана диоксид, полиэтиленгликоль 6000, воск карнаубский, воск белый.
Описание.
Круглые, двояковыпуклые таблетки белого цвета, покрытые сахарной оболочкой, диаметром около 7.0 мм, толщиной около 3.7 мм.
Фармакотерапевтическая группа
Препараты для лечения функциональных расстройств желудочно-кишечного тракта. Полусинтетические алкалоиды белладонны, четвертичные аммониевые соединения.
Код АТХ А03ВВ01
Фармакологические свойства
Фармакокинетика
Всасывание и распределение. Как четвертичное аммониевое производное, гиосцина бутилбромид высоко полярен, вследствие чего при пероральном применении абсорбируется лишь частично (8%). После перорального применения однократных доз гиосцина бутилбромида в диапозоне от 20 до 400 мг средняя пиковая плазменная концентрация между 0.11 нг/мЛ и 2.04 нг/мЛ достигается в течении 2 часов. При том же диапазоне доз среднее значение АУК0-TZ варьируется от 0,37 до 10,7 нг ч/мЛ. Системная биодоступность различных лекарственных форм, таких как покрытые таблетки, суппозитории и оральный раствор, содержащих 100 мг гиосцина бутилбромида, cоставляет менее 1%.
Из-за высокого сродства с мускариновыми и никотиновыми рецепторами, гиосцина бутилбромид распределяется, в основном, в мышечных клетках брюшной и тазовой области и в интрамуральных ганглиях органов брюшной полости. Связь с белками плазмы составляет около 4,4%.
Метаболизм и выведение. После перорального применения однократных доз в диапазоне от 100 до 400 мг период полувыведения варьируется от 6,2 до 10,6 часов. Выводится, в основном, путем гидролитического расщепления эфирных связей.
После перорального применения от 2 до 5% остаточной дозы, определенной меченным радиоактивным изотопом гиосцина бутилбромида, выводится через почки и около 90% через ЖКТ. Выведение с мочой составляет менее 0,1% дозы. Общий клиренс составил от 881 л/мин до 1420 л/мин (при пероральных дозах от 100 до 400 мг), тогда как соответствующие объемы распределения варьируются от 6,13 до 11,3 х 105 л, что возможно связано с очень низкой системной биодоступностью.
Метаболиты, выводимые через почки, плохо связываются с мускариновыми рецепторами, вследствие чего не влияют на эффект гиосцина бутилбромида.
Фармакодинамика
БУСКОПАН оказывает спазмолитическое действие на гладкую мускулатуру желудочно-кишечного, желчного и мочеполового трактов. Как четвертичное аммониевое производное, он не проникает в центральную нервную систему. Поэтому антихолинергических побочных эффектов на ЦНС не возникает. Периферическое антихолинергическое действие возникает из-за ганглиоблокирующего действия внутри висцеральной стенки и антимускариновой активности.
Показания к применению
В составе комплексной терапии
— почечная колика, спазмы мочеточника, желчная колика, гипермоторная дискинезия желчевыводящих путей и желчного пузыря, холецистит, кишечная колика, пилороспазм, язвенная болезнь желудка и двенадцатиперстной кишки в фазе обострения дисменорея
Способ применения и дозы
Таблетки следует проглатывать полностью, запивая достаточным количеством воды.
Если врачом не назначено иначе, рекомендуется использовать следующие дозировки:
Взрослым по 2 таблетке 4 раза в день.
Детям старше 6 лет: по 1 таблетке 3 раз в день.
Продолжительность курса лечения определяется лечащим врачом индивидуально.
БУСКОПАН не следует принимать продолжительное время на ежедневной основе или на протяжении длительного времени без установления причины боли в животе.
Побочные действия
Многие из описанных ниже побочных действий могут быть отнесены к антихолинергическим свойствам БУСКОПАНА. Антихолинергические побочные эффекты БУСКОПАНА в основном умеренные и самокупирующиеся.
Нечасто
— тахикардия,
— сухость во рту
— дисгидроз
— анафилактический шок, включая летальный исход, анафилактоидные реакции, диспноэ, кожные реакции (например, крапивница, сыпь, эритема и зуд) и другие проявления гиперчувствительности
Редко
— задержка мочи
Противопоказания
— повышенная чувствительность к гиосцина бутилбромиду или любому другому компоненту препарата
— миастения гравис
— мегаколон
— наследственная непереносимость фруктозы
— детский возраст до 6 лет
Лекарственные взаимодействия
БУСКОПАН может усиливать антихолинергическое действие три- и тетрациклических антидепрессантов, антигистаминных и антипсихотических препаратов, хинидина, амантадина, дизопирамида и других холинолитиков (например, тиотропия, ипратропия, атропиноподобные соединения).
Одновременное назначение БУСКОПАНА и антагонистов допамина, например, метоклопрамида, может привести к ослаблению действия обоих препаратов на желудочно-кишечный тракт.
БУСКОПАН может усиливать тахикардию, вызываемую бета-адренергическими средствами.
Особые указания
В случае, если сильная боль в животе сохраняется или ухудшается, или протекает с такими симптомами, как лихорадка, тошнота, рвота, изменения перистальтики, болезненность живота, (при надавливании), снижение артериального давления, потеря сознания или кровь в стуле, необходимы соответствующие диагностические меры для исследования этиологии симптомов.
Вследствие потенциального риска антихолинергических осложнений следует соблюдать осторожность у следующих пациентов: с предрасположенностью к закрытоугольной глаукоме, с подозрением на кишечную непроходимость или обструкцию мочевыводящих путей, со склонностью к тахикардии.
Одна таблетка, покрытая сахарной оболочкой 10 мг, содержит 41,2 мг сахарозы, что дает в результате содержание 411,8 мг сахарозы в максимально рекомендованной дневной дозе. Пациенты с редкими наследственными состояниями непереносимости фруктозы не должны принимать этот препарат.
Беременность и период лактаци
Существует лишь ограниченная информация о применении гиосцина бутилбромида во время беременности. Нет достаточных данных по выведению БУСКОПАНА и его метаболитов в грудное молоко.
В качестве меры предосторожности предпочтительно избегать применения БУСКОПАНА во время беременности и грудного вскармливания.
Исследований по воздействию препарата на фертильность человека не проводилось.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Исследований о влиянии на способность управлять автомобилем и потенциально опасными механизмами не проводилось.
Передозировка
Симптомы: в случае передозировки могут наблюдаться антихолинергические эффекты.
Лечение: при необходимости следует применять парасимпатомиметические средства. В случае глаукомы необходима срочная консультация офтальмолога. Сердечно-сосудистые осложнения необходимо лечить согласно обычным терапевтическим принципам. При параличе дыхательной мускулатуры следует рассматривать применение интубации, искусственной вентиляции легких. В случае задержки мочи может потребоваться катетеризация мочевого пузыря. В дополнение, при необходимости следует использовать соответствующие поддерживающие меры.
Форма выпуска и упаковка
По 20 таблеток помещают в контурные ячейковые упаковки из пленки поливинилхлоридной и фольги алюминиевой.
По 1 контурной упаковке вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в пачку картонную.
Условия хранения
Хранить при температуре не выше 25ºС.
Хранить в недоступном для детей месте!
Срок хранения
5 лет
Не использовать после истечения срока годности.
Условия отпуска из аптек
Без рецепта
Производитель
Делфарм Реймс С.А.С., Франция
Наименование и страна владельца регистрационного удостоверения
Берингер Ингельхайм Интернешнл ГмбХ, Германия
Адрес организации, принимающей на территории Республики Казахстан, претензии от потребителей по качеству продукции
Представительство «Берингер Ингельхайм Фарма Гес мбХ» в РК
Адрес: г. Алматы, 050008, пр. Абая 52, Бизнес центр «Innova Tower», 7-й этаж
Тел: +7 (727) 250 00 77; факс: +7 (727) 244 51 77
e-mail: PV_local_Kazakhstan@boehringer-ingelheim.com
| 136727031477976413_ru.doc | 81.5 кб |
| 614869551477977663_kz.doc | 61 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Состав: метилсульфонилметан, глюкозамин сульфат, глюкозамин гидрохлорид, Н-ацетил Д-глюкозамин, витамин С, хондроитин сульфат, цинка бис-глицинат, меди бис-глицинат, желатин, Е171.
Для реализации населению в качестве биологически активной добавки к пище дополнительного источника витамина С, глюкозамина, меди и цинка, содержащей хондроитинсульфат, метилсульфонилметан.
Взрослым 1 капсулу в день во время приема пищи, запивая соком. Продолжительность приема — не более 4 недель. Повторный прием при необходимости через 2 недели.
Индивидуальная непереносимость компонентов, беременность, кормление грудью, лицам склонным к кровоточивости и страдающим тромбофлебитами.
Перед применением рекомендуется проконсультироваться с врачом.
Хранить в оригинальной упаковке в сухом, прохладном, защищенном от света и недоступном для детей месте.
Дата регистрации и переоформления
14.05.2015
Производители
Получатель
Таблетки 16 мг/12, 5 мг и 32 мг/12,5 мг
Одна таблетка содержит
активное вещество — кандесартана цилексетил 16 мг или 32 мг
гидрохлортиазид 12,5 мг,
вспомогательные вещества: лактоза моногидрат, кукурузный крахмал, полиэтиленгликоль 8000 Р, гидроксипропилцеллюлоза L, кальция карбоксиметилцеллюлоза, железа (III) оксид желтый (Е 172), магния стеарат.
Круглые таблетки желтого цвета, с двухсторонней фаской, с риской на одной стороне и с маркировкой знака «ɳ» на другой (для дозировки 16 мг/12,5 мг)
Круглые таблетки желтого цвета, с двухсторонней фаской, с риской на одной стороне (для дозировки 32 мг/12,5 мг).
Ангиотензина II антагонисты в комбинации с диуретиками. Кандесартан в
комбинации с диуретиками.
Код АТХ С09DА06
Фармакокинетика
Совместный прием кандесартана цилексетила и гидрохлортиазида не оказывает клинически значимого эффекта на фармакокинетику любого из этих лекарственных препаратов.
Всасывание и распределение
Кандесартана цилексетил
Кандесартана цилексетил является пролекарством для приема внутрь. Быстро превращается в активное вещество – кандесартан посредством эфирного гидролиза при всасывании из пищеварительного тракта, прочно связывается с АТ1- рецепторами и медленно диссоциирует, не имеет свойств агониста. Абсолютная биодоступность кандесартана после приема внутрь раствора кандесартана цилексетила составляет около 40%. Относительная биодоступность таблетированного препарата по сравнению с раствором для приема внутрь составляет приблизительно 34%. Максимальная концентрация в сыворотке крови (Сmax) достигается через 3 — 4 часа после приема таблетированной формы препарата. При увеличении дозы препарата в рекомендуемых пределах концентрация кандесартана повышается линейно. Фармакокинетические параметры кандесартана не зависят от пола пациента. Приём пищи не оказывает значимого влияния на площадь под кривой «концентрация — время» (AUC), т.е. пища существенно не влияет на биодоступность препарата. Кандесартан активно связывается с белками плазмы крови (более 99%). Плазменный объем распределения кандесартана составляет 0,1 л/кг.
Гидрохлортиазид
Гидрохлортиазид быстро всасывается из желудочно-кишечного тракта, биодоступность составляет примерно 70%. Сопутствующий прием пищи увеличивает всасывание примерно на 15%. Биодоступность может быть снижена у пациентов с сердечной недостаточностью и выраженными отеками. Связь с белками плазмы крови составляет примерно 60%. Видимый объем распределения составляет примерно 0,8 л/кг.
Метаболизм и выделение
Кандесартана цилексетил
Кандесартан, в основном, выводится из организма с мочой и желчью в неизмененном виде и лишь в незначительной степени метаболизируется в печени.
Имеющиеся исследования взаимодействия показали, что воздействие на CYP2C9 и CYP3A4 отсутствует. На основании данных, полученных в лабораторных условиях, не ожидается возникновение взаимодействия в организме с лекарственными препаратами, чей метаболизм зависит от изоферментов CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 или CYP3A4 цитохрома P450. Период полувыведения кандесартана составляет приблизительно 9 часов. Кумуляции препарата в организме не наблюдается. Период полувыведения кандесартана остается неизменным (приблизительно 9 часов) после приема кандесартана цилексетила совместно с гидрохлортиазидом. Не происходит дополнительного накопления кандесартана после многократного приема комбинированного препарата в сравнении с монотерапией.
Общий клиренс кандесартана составляет около 0,37 мл/мин/кг, при этом почечный клиренс – около 0,19 мл/мин/кг. Почечная экскреция кандесартана осуществляется путем клубочковой фильтрации и активной канальцевой секреции. При приёме внутрь радиоактивно-меченного кандесартана цилексетила около 26% от введенного количества выводится с мочой в виде кандесартана и 7% в виде неактивного метаболита, тогда как в кале обнаруживается 56% от введенного количества в виде кандесартана и 10% в виде неактивного метаболита.
Гидрохлортиазид
Гидрохлортиазид не метаболизируется и выделяется практически полностью в виде активной формы препарата путем клубочковой фильтрации и активной канальцевой секреции в проксимальном отделе нефрона. Период полувыведения составляет примерно 8 часов. Примерно 70% дозы принятой внутрь выводится с мочой в течение 48 часов. Период полувыведения не меняется при приеме совместно с кандесартаном. При использовании комбинации препаратов не выявлено дополнительного накопления гидрохлортиазида в сравнении с монотерапией.
Фармакокинетика кандесартана в особых группах
У пожилых пациентов (старше 65 лет) Cmax и AUC кандесартана увеличиваются на 50% и 80%, соответственно, по сравнению с молодыми пациентами. Однако, гипотензивный эффект и частота развития побочных эффектов при применении КАНТАБа Плюс не зависят от возраста пациентов.
У пациентов с легким и умеренным нарушением функции почек Cmax и AUC кандесартана увеличивались на 50% и 70% соответственно, тогда как период полувыведения препарата не изменяется по сравнению с больными с нормальной функцией почек. У пациентов с тяжелым нарушением функции почек Cmax и AUC кандесартана увеличивались на 50% и 110%, соответственно, а период полувыведения препарата увеличивался в 2 раза. У пациентов, находящихся на гемодиализе, были выявлены такие же фармакокинетические параметры кандесартана, как у пациентов с тяжелым нарушением функции почек.
У пациентов с легким и умеренным нарушением функции печени отмечалось повышение AUC кандесартана на 20% — 80% согласно данным клинических исследований.
Гидрохлортиазид
Период полувыведения более продолжителен у пациентов, страдающих почечной недостаточностью.
Фармакодинамика
КАНТАБ Плюс — является комбинацией непептидного селективного блокатора АТ1-рецепторов ангиотензина ІІ — кадесартана, который содержится в лекарственной форме в виде пролекарства (кадесартана цилексетила) и тиазидного диуретика — гидрохлортиазида.
Ангиотензин II – основной гормон ренин-ангиотензин-альдостероновой системы, который играет важную роль в патогенезе артериальной гипертензии, сердечной недостаточности и других сердечно-сосудистых заболеваний. Основными физиологическими эффектами ангиотензина II являются вазоконстрикция, стимуляция продукции альдостерона, регуляция водно-электролитного состояния и стимуляция клеточного роста. Все эти эффекты опосредованы взаимодействием ангиотензина II с ангиотензиновыми рецепторами 1 типа (АТ1 рецепторы).
Кандесартан – селективный антагонист рецепторов ангиотензина II 1 типа (АТ1 рецепторов), не ингибирует ангиотензин-превращающий фермент (АПФ), который осуществляет превращение ангиотензина I в ангиотензин II и разрушает брадикинин; не влияет на АПФ и не приводит к накоплению брадикинина или субстанции Р. Кандесартан не связывается с рецепторами других гормонов и не блокирует ионные каналы, участвующие в регуляции функций сердечно-сосудистой системы. В результате блокирования АТ1 рецепторов ангиотензина II происходит дозозависимое повышение уровня ренина, ангиотензина I, ангиотензина II и снижение концентрации альдостерона в плазме крови.
Гидрохлортиазид угнетает активную реабсорбцию натрия, в основном в дистальных отделах почечных канальцев и усиливает выделение ионов натрия, хлора и воды. Выделение калия и магния почками усиливается в зависимости от дозы, в то время как кальций начинает реабсорбироваться в больших количествах, чем раньше. Гидрохлортиазид уменьшает объем плазмы крови и внеклеточной жидкости и уменьшает интенсивность транспорта крови сердцем и АД. Во время долговременного лечения, гипотензивный эффект развивается за счет расширения артериол.
Показано, что при длительном применении гидрохлортиазида уменьшается риск сердечно-сосудистых заболеваний и смертность.
Кандесартан и гидрохлортиазид оказывают суммарное гипотензивное действие.
У пациентов, страдающих артериальной гипертензией, КАНТАБ Плюс вызывает эффективное и продолжительное снижение АД без увеличения частоты сердечных сокращений (ЧСС). Ортостатической гипотензии при первом приеме препарата не наблюдается, а также артериальная гипертензия не усиливается после окончания лечения. После однократного приема КАНТАБа Плюс основной гипотензивный эффект развивается в течение 2 часов. При продолжительном лечении стабильное снижение АД наступает в течение 4–х недель после начала приема препарата и может поддерживаться при длительном курсе лечения. КАНТАБ Плюс при приеме один раз в день эффективно и мягко снижает АД в течение 24 часов с незначительной разницей между максимальным и средним эффектом действия. Эффективность комбинации кандесартана и гидрохлортиазида не зависит от пола и возраста пациента.
— лечение артериальной гипертензии у пациентов‚ которым показана комбинированная терапия
Рекомендуемая доза — 1 таблетка 1 раз в сутки.
КАНТАБ Плюс следует принимать один раз в сутки вне зависимости от приема пищи.
Рекомендуется титрование дозы кандесартана перед переводом пациента на терапию КАНТАБом Плюс с. Основной гипотензивный эффект достигается, как правило, в первые 4 недели после начала лечения.
Пожилые пациенты
У пациентов пожилого возраста коррекции дозы не требуется.
Пациенты с почечной недостаточностью
У пациентов с нарушением функции почек предпочтительнее применение петлевых диуретиков по сравнению с тиазидными. До начала терапии препаратом КАНТАБ Плюс у пациентов с легким или умеренным нарушением функции почек (клиренс креатинина ≥ 30 мл/мин/1,73 м2), включая пациентов, находящихся на гемодиализе, рекомендуется титрование дозы кандесартана, начиная с 4 мг.
Препарат КАНТАБ Плюс противопоказан пациентам с тяжелой почечной недостаточностью (клиренс креатинина< 30 мл/мин/1,73 м2 BSA).
Пациенты со сниженным объемом циркулирующей крови
Для пациентов с риском артериальной гипотензии, например, для пациентов со сниженным объемом циркулирующей крови, рекомендуется титрование дозы кандесартана, начиная с 4 мг.
Пациенты с печеночной недостаточностью
Повышение дозы кандесартана цилексетила рекомендуется пациентам с легкой или умеренной печеночной недостаточностью для лечения препаратом КАНТАБ Плюс (рекомендуемая начальная доза кандесартан цилексетила – 4 мг у таких пациентов).
Часто (> 1/100, < 1/10)
— головная боль, головокружение
— инфекции дыхательных путей
Очень редко (< 1/10 000)
— тошнота
— кашель
— лейкопения, нейтропения и агранулоцитоз
— гиперкалиемия, гипонатриемия
— повышение активности «печеночных» ферментов, нарушение функции печени или гепатит
— ангионевротический отек, сыпь, крапивница, кожный зуд
— боль в спине, артралгия, миалгия
— нарушение функции почек, включая почечную недостаточность у предрасположенных пациентов
При терапии гидрохлортиазидом, обычно в дозе 25 мг или более, были отмечены следующие побочные эффекты: нечасто (>1/1000 и <1/100) или редко (<1/1000):
Нечасто(> 1/1000, < 1/100)
— реакции фотосенсибилизации
Редко (> 1/10 000, < 1/1 000)
— лейкопения, нейтропения/агранулоцитоз, тромбоцитопения, апластическая анемия
— анафилактические реакции
— некротический васкулит
— респиратоный дистресс-синдром (в том числе, пневмония и отек легких)
— панкреатит
— желтуха (внутрипеченочная холестатическая)
— токсический эпидермальный некролиз,
— нарушение функции почек и интерстициальный нефрит
— повышенная чувствительность к активным или вспомогательным компонентам, входящим в состав препарата, производным сульфонамидов
— тяжелая печеночная недостаточность и/или холестаз
— тяжелая почечная недостаточность (клиренс креатинина менее 30 мл/мин/1,73 м2)
— рефрактерная гипокалиемия и гиперкальциемия
— подагра
— беременность и период лактации
— детский возраст до 18 лет (эффективность и безопасность не установлены)
С осторожностью: тяжелая хроническая сердечная недостаточность, двухсторонний стеноз почечных артерий, стеноз артерии единственной почки, гемодинамически значимый стеноз аортального и митрального клапана, у больных с цереброваскулярными заболеваниями и ишемической болезнью сердца, гипертрофическая обструктивная кардиомиопатия, у больных со сниженным объемом циркулирующей крови, цирроз печени, у пациентов, страдающих непереносимостью лактозы, нарушением всасывания лактозы и галактозы, гипонатриемия, первичный гиперальдостеронизм, хирургическое вмешательство, у больных после трансплантации почки, почечная недостаточность, сахарный диабет.
В фармакокинетических исследованиях было изучено сочетанное применение КАНТАБа Плюс с варфарином, дигоксином, пероральными контрацептивами (этинилэстрадиол/левоноргестрел), глибенкламидом, нифедипином. Клинически значимых фармакокинетических взаимодействий выявлено не было.
Кандесартан метаболизируется в печени в незначительной степени (CYP2C9). Проведенные исследования по взаимодействию не выявили влияния препарата на CYP2C9 и CYP3A4. Совместное применение КАНТАБа Плюс с другими антигипертензивными средствами потенцирует гипотензивный эффект.
Следует ожидать, что действие гидрохлортиазида, приводящее к потере калия, может быть усилено другими средствами, приводящими к потере калия и гипокалиемии (например, диуретики, слабительные, амфотерицин, карбеноксолон, пенициллин G натрий, производные салициловой кислоты, стероиды, АКТГ).
Опыт применения других лекарственных средств, действующих на ренин-ангиотензин-альдостероновую систему, показывает, что сопутствующая терапия калийсберегающими диуретиками, препаратами калия, заменителями соли и другими средствами, которые могут повышать уровень калия в сыворотке крови (например, гепарин) может приводить к развитию гиперкалиемии.
Индуцированная диуретическими средствами гипокалиемия и гипомагниемия предрасполагают к возможному кардиотоксическому действию гликозидов наперстянки и антиаритмических средств. При приеме КАНТАБа Плюс параллельно с такими препаратами требуется контроль уровня калия в крови.
При сочетанном назначении препаратов лития с ингибиторами АПФ или гидрохлортиазидом сообщалось об обратимом повышении концентрации лития в сыворотке крови и развитии токсических реакций. Подобные реакции могут встречаться и при использовании антагонистов рецепторов ангиотензина II, в связи с чем рекомендуется контролировать уровень лития в сыворотке крови при комбинированном применении этих препаратов.
Биодоступность кандесартана не зависит от приема пищи.
Мочегонное, натрийуретическое и гипотензивное действия гидрохлортиазида ослабляются нестероидными противовоспалительными препаратами.
Всасывание гидрохлортиазида ослабляется при применении колестипола или холестирамина.
Действие не деполяризующих миорелаксантов (например, тубокурарина) может быть усилено гидрохлортиазидом.
Тиазидные диуретические средства могут вызывать повышение уровня кальция в крови в связи с уменьшением его экскреции. При необходимости приема кальцийсодержащих пищевых добавок или витамина D, следует контролировать уровень кальция в плазме крови и при необходимости скорректировать дозу.
Тиазиды усиливают гипергликемическое действие бета-адреноблокаторов и диазоксида.
Антихолинэргические средства (например, атропин, биперидин) могут увеличивать биодоступность мочегонных средств на основе тиазидов вследствие снижения моторики желудочно-кишечного тракта.
Тиазиды могут увеличить риск неблагоприятного действия амантадина.
Тиазиды могут замедлить выведение цитостатических средств (таких как циклофосфамид, метотрексат) из организма и усилить их миелоподавляющее действие.
Риск гипокалиемии может увеличиться при сопутствующем приеме стероидных лекарственных средств или адренокортикотропного гормона.
На фоне приема препарата может увеличиваться частота развития ортостатической гипотензии при приеме алкоголя, барбитуратов или анестетиков.
Лечение тиазидами может снижать толерантность к глюкозе. Может потребоваться подбор дозы противодиабетических препаратов, в том числе инсулина.
Гидрохлортиазид может уменьшить влияние сосудосуживающих аминов (например, эпинефрина (адреналина)).
Гидрохлортиазид может увеличить риск развития острой почечной недостаточности, особенно в совокупности с большими дозами йодированного контрастного вещества.
При сопутствующем применении с циклоспорином может повышаться риск гиперурикемии и подагры.
Сопутствующее применение баклофена, трициклических антидепрессантов или нейролептиков может привести к усилению антигипертензивного эффекта и может вызвать гипотензию.
Нарушение функции почек
В данной ситуации использование петлевых диуретиков предпочтительнее тиазидных. Для пациентов с почечной недостаточностью при использовании КАНТАБ Плюс рекомендуется постоянно контролировать уровень калия, креатинина и мочевой кислоты.
Пересадка почки
Данные о применении КАНТАБа Плюс у пациентов, недавно перенесших пересадку почки, отсутствуют.
Стеноз почечной артерии
Другие препараты, влияющие на ренин-ангиотензин-альдостероновую систему, например, ингибиторы АПФ, могут привести к повышению содержания мочевины в крови и уровня креатинина в сыворотке пациентов с двухсторонним стенозом почечной артерии или стенозом артерии единственной почки. Аналогичного эффекта следует ожидать и от антагонистов рецепторов ангиотензина II.
Снижение объема циркулирующей крови
У пациентов с дефицитом интраваскулярного объема и/или натрия возможно развитие симптоматической гипотензии, как описано для других препаратов, влияющих на ренин-ангиотензин-альдостероновую систему. Поэтому не рекомендуется применять КАНТАБ Плюс до исчезновения данных симптомов.
Анестезия и хирургическое вмешательство
У пациентов, получающих антагонисты ангиотензина II, во время анестезии и при хирургических вмешательствах может развиться артериальная гипотензия в результате блокады ренин-ангиотензиновой системы. Очень редко могут отмечаться случаи тяжелой артериальной гипотензии, требующей внутривенного введения жидкости и/или вазопрессоров.
Печеночная недостаточность
Пациентам, с нарушениям функции печени или прогрессирующей болезнью печени, следует применять тиазиды с осторожностью в виду того, что незначительные колебания объема жидкости и электролитного состава могут вызвать печеночную кому. Данные о применении КАНТАБа Плюс пациентами с печеночной недостаточностью отсутствуют.
Стеноз аортального и митрального клапана (гипертрофическая обструктивная кардиомиопатия)
При назначении КАНТАБа Плюс, как и других вазодилататоров, пациентам с обструктивной гипертрофической кардиомиопатией или гемодинамически значимым стенозом аортального или митрального клапана следует соблюдать осторожность.
Первичный гиперальдостеронизм
Пациенты с первичным гиперальдостеронизмом обычно резистентны к терапии антигипертензивными средствами, влияющими на ренин-ангиотензин-альдостероновую систему. В связи с этим не рекомендуется назначать таким пациентам КАНТАБ Плюс.
Нарушение водно-солевого баланса
Как и во всех случаях приема препаратов, обладающих мочегонным действием, следует контролировать электролиты в плазме крови.
Препараты на основе тиазидов, обладающие мочегонным действием, способны уменьшить выделение ионов кальция с мочой и могут вызвать периодическое и незначительное увеличение концентрации ионов кальция в плазме крови.
Тиазиды, в том числе и гидрохлортиазид, могут вызывать нарушения водно-солевого баланса (гиперкальциемия, гипокалиемия, гипонатриемия, гипомагниемия и гипохлоремический алкалоз).
Выявленная гиперкальциемия может быть признаком скрытого гиперпаратиреоза. Прием тиазидных средств следует прекратить до получения результатов анализов исследования паращитовидной железы.
Гидрохлортиазид дозозависимо увеличивает выделение калия, что может стать причиной гипокалиемии. Подобное действие гидрохлортиазида проявляется меньше, если применять его в сочетании с кандесартана цилексетилом. Риск гипокалиемии оказывается повышенным у пациентов, страдающих циррозом печени, у пациентов с повышенным диурезом и у пациентов, принимающих жидкость с пониженным содержанием солей, и у пациентов, проходящих параллельно курс лечения кортикостероидами или принимающих адренокортикотропный гормон.
На основании опыта применения препаратов, влияющих на ренин-ангиотензин-альдостероновую систему, параллельное применение КАНТАБа Плюс и увеличивающих выделение калия мочегонных средств можно компенсировать применением пищевых добавок, содержащих калий или других препаратов, способных повысить содержание калия в плазме крови.
Применение КАНТАБа Плюс с ингибиторами ангиотензин-превращающего фермента или ингибиторами рецепторов ангиотензина II может вызвать гипокалиемию, особенно если пациент страдает от сердечной недостаточности или почечной недостаточности, хотя подобные случаи документально не зарегистрированы.
Показано, что тиазиды увеличивают выделение магния, что может вызвать гипомагниемию.
Влияние на метаболизм и эндокринную систему
Лечение тиазидами может нарушить уровень глюкозы в крови. Может потребоваться подбор дозы гипогликемических средств, в том числе инсулина. Во время терапии тиазидом возможно проявление латентно протекающего сахарного диабета. С лечением тиазидом также связывают увеличение уровня холестерина и триглицеридов. Однако при использовании КАНТАБа Плюс, содержащего дозу в 12,5 мг, наблюдалось минимальное количество подобных эффектов. Тиазидные диуретики увеличивают концентрацию мочевой кислоты в плазме крови и могут способствовать возникновению подагры у предрасположенных больных.
Общие
Пациенты, у которых сосудистый тонус и функция почек преимущественно зависят от активности ренин-ангиотензин-альдостероновой системы (например, больные с тяжелой хронической сердечной недостаточностью или заболеваниями почек, включая стеноз почечной артерии), особенно чувствительны к препаратам, действующим на ренин-ангиотензин-альдостероновую систему. Назначение подобных препаратов сопровождается у этих больных острой артериальной гипотензией, азотемией, олигурией и реже – острой почечной недостаточностью. Возможность развития перечисленных эффектов не может быть исключена и при использовании антагонистов рецепторов ангиотензина II. Резкое снижение АД у больных с ишемической болезнью сердца или цереброваскулярными заболеваниями ишемического генеза, при использовании любых антигипертензивных средств, может приводить к развитию инфаркта миокарда или инсульта.
Проявление реакций повышенной чувствительности к гидрохлортиазиду возможно и у пациентов, не имевших ранее аллергии или бронхиальной астмы, но оно более вероятно для пациентов, имевших подобные симптомы.
При использовании тиазидных диуретиков отмечены случаи обострения или появления симптомов системного люпус-эритематоза.
Препарат содержит лактозу, поэтому его не следует принимать пациентам, страдающим от редких наследственных заболеваний, проявляющихся в непереносимости галактозы, врожденной лактазной недостаточности или глюкозогалактозной мальабсорбции.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Влияние на способность управлять автомобилем или работать с техникой не изучалось, но фармакодинамические свойства препарата указывают на то, что подобное влияние отсутствует. Пациентам следует быть острожными при управлении автотранспортом или работе с техникой, поскольку во время лечения может возникать головокружение и может наблюдаться повышенная усталость.
Симптомы: Были описаны отдельные случаи передозировки препарата (до 672 мг кандесартана цилексетила), закончившиеся выздоровлением пациентов без тяжелых последствий.
Основным проявлением передозировки гидрохлортиазидом является острая потеря жидкости и электролитов. Также наблюдались такие симптомы как головокружение, снижение АД, сухость во рту, тахикардия, желудочковая аритмия, седация, потеря сознания и мышечные судороги.
Лечение: При развитии клинически выраженного снижения АД необходимо проводить симптоматическое лечение и контролировать состояние пациента. Уложить пациента на спину и приподнять ноги. При необходимости следует увеличить объем циркулирующей крови, например, путем внутривенного введения изотонического раствора хлорида натрия. В случае необходимости могут быть назначены симпатомиметические средства. Выведение кандесартана и гидрохлортиазида с помощью гемодиализа маловероятно.
По 14 (для дозировки 16 мг/12,5 мг) или 7 (для дозировки 32 мг/12,5 мг) таблеток помещают в контурную ячейковую упаковку из пленки прозрачной ПВХ/ПЭ/ПВДХ и фольги алюминиевой печатной.
По 1 или 2 (для дозировки 16 мг/12,5 мг) или 2 или 4 (для дозировки 32 мг/12,5 мг) контурной упаковки вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку картонную с голограммой фирмы – производителя.
Хранить, в сухом, защищенном от света месте, при температуре не выше 25 0С.
Хранить в недоступном для детей месте!
2 года
Не применять после истечения срока годности.
АО «Нобел Алматинская Фармацевтическая Фабрика»
Республика Казахстан,
г. Алматы, ул. Шевченко 162 Е.