Дихлорацетат натрия представляет собой натриевую соль дихлоруксусной кислоты ( DCA ). Дихлоруксусная кислота имеет высокую кислотность, поэтому ее обычно хранят и продают в виде различных солей, которые снижают кислотность до приемлемого рН.
Дихлорацетат натрия это белый цвет, растворимый в кристаллическом порошке воды. Химическая формула — Cl2CHCOONa. Это простая молекула, которая имеет много применений.
Применение дихлорацетата натрия до открытия канадских ученых ограничивалось лечением детей с врожденными нарушениями метаболизма. Вещество было эффективным только при заболеваниях, вызванных нарушением функции митохондрий в клетках. Группа ученных пришла к выводу, что DCA является эффективным главным образом против раковых опухолей, которые поразили легкие, грудь и отделы головного мозга.
Дихлорацетат натрия не является ядом или химиопрепаратом, после действия которого происходит полное разрушение организма. Чтобы улучшить состояние здоровья и победить раковое заболевание, люди годами пьют препараты на основе DCA.
Преимуществом применения дихлорацетата натрия при раковой опухоли в том, что он имеет совсем другой механизм действия: он направлен на восстановление функций поврежденной митохондрии, в результате чего раковая клетка неизбежно гибнет.
DCA быстро разрушает злокачественную опухоль, а продукты ее распада проникают в кровь. Такой процесс может вызвать плохое самочувствие пациента, но симптомы интоксикации устраняются с помощью специальных капельниц, клизм и сорбентов.
Важно вовремя начать лечение DCA, если заболевание будет запущено, а внутренние органы пострадают от химиотерапии, никакие препараты уже не помогут. Иногда люди длительное время принимают дихлорацетат натрия, а состояние их здоровья остается на прежнем уровне. Тогда специалисты подбирают более высокую дозировку.
СОСТАВ
Дихлорацетат натрия (DCA).
ПОКАЗАНИЯ
- Неходжкинская лимфома;
- Острая лимфатическая лейкемия;
- Острая миелоцитическая лейкемия;
- Хроническая лимфатическая лейкемия;
- Рак груди;
- Рак яичек;
- Медуллобластома;
- Клеточная карцинома Меркеля;
- Нейробластома;
- Мелкоклетчатый рак лёгких.
- Заболевания, вызванные нарушением функции митохондрий в клетках.
Дозировка препарата должна быть назначена только специалистом, такое лечение невозможным становится при неврологических нарушениях. Побочных действий от приема дихлорацетата натрия не наблюдается, они могут возникать лишь при невропатии – дрожание пальцев рук и дрожь внутри, но через неделю после прекращения лечения побочные явления исчезают.
ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ
Дихлорацетат принимается из расчёта 12 — 25 мг порошка на 1 кг веса пациента — т.е. в сутки при весе 40 кг выходит около 1 гр. При весе 60 кг — 1,5 г ≈ 1/3 чай ложки. После еды. Также пьют «Нейромультивит» по 1 табл. три раза в день и 5-7 чашек чая, лучше нашего Живого Чая.
При дополнительных побочных действиях: тошнота, затруднённость дыхания, нарушения пищеварения, онемение в пальцах, тремор, головокружение, частое мочеиспускание, беспокойство, депрессия, сонливость – доза должна быть снижена до 10 мг/кг или прекращена на несколько дней, затем всё же желательно вернуться к дозе 25 мг/кг в день.
ПРОТИВОПОКАЗАНИЯ
Учеными замечено, что при других видах опухолей использование Дихлорацетата натрия приводило к ухудшению состояния. Причем, не просто вызывало побочные эффекты, а именно активизация онкологического процесса. В связи с этим существует ряд противопоказаний, а именно:
- Нарушение функций пищеварения;
- Высокая нагрузка на печень;
- Токсическое действие на нервную систему, вплоть, до появления полинейропатии, спутанности сознания, летаргии;
- Нарушение дыхания.
Хранить с плотно закрытой крышкой, в прохладном, защищенном от света месте.
Срок годности 3 года.
Мы готовы доставить Ваш заказ в любую страну и любой город, независимо от его размера.
Мы предлагаем следующие способы доставки:
- Доставка почтой России
- Курьерская доставка (до двери)
- Доставка транспортной компанией (СДЭК, Boxberry, ЦАП, Деловые Линии)
- Самовывоз по адресу г.Сочи, ул. Северная 6.
Мы рекомендуем доставку почтой России (наиболее экономный, но при этом быстрый вариант) или компанией СДЭК.
Обратите внимание, что у Почты России есть три тарифа: Обычная доставка, Ускоренная и EMS.
Ускоренная – на 80-100% дороже, в среднем посылка приходит на 2-3 дня быстрее.
EMS – доставка посылки до двери.
Вопросы по доставке вы можете задать по телефонам:
+7 (938) 467 78 06
+7 (928) 234 98 80
+7 (995) 003 74 85
Стоимость доставки
При заказе обычной доставки почты России у нас действует система скидок. Чем больше ваш заказ, тем ниже стоимость доставки. Обратите внимание, акция действует по только на территории РФ.
Сумма заказа
|
Сумма заказа |
Стоимость доставки |
|
До 800 рублей |
350 |
|
От 800 до 3500 рублей |
300 |
|
От 3500 до 6000 рублей |
250 |
|
От 6000 до 8000 рублей |
175 |
|
От 8000 до 11000 рублей |
100 |
|
От 11000 рублей |
Бесплатная доставка |
При ускоренной доставке Почты России, EMS или транспортной компании, Вы оплачиваете фактическую стоимость доставки. Она зависит от расстояния и размера заказа. Стоимость доставки рассчитает наш сотрудник, который с Вами свяжется.
Оплатить Ваш заказ можно следующими способами:
- Переводом на карту Сбербанка 4276 3000 5416 5108, владелец Геннадий Алексеевич Гарбузов. Платеж можно сделать с помощью приложения Сбербанк Online, через банкомат или в отделении Сбербанка (все варианты без комиссии). Или переводом с карты другого банка (размер комиссии уточняйте в вашем банке)
- Произвести оплату с вашей банковской карты при оформлении заказа (через сервис Robokassa)
- Произвести оплату с вашей банковской карты по выставленному счёту (через сервис Robokassa).
- Оплатить с помощью платёжных систем Золотая Корона (для жителей СНГ), Western Union и MoneyGram (для жителей дальнего зарубежья)
- Возможны иные способы оплаты по согласованию с вашим менеджером.
Обратите внимание! Заказы мы отправляем только по предоплате. Если Вам по какой-то причине это неудобно, мы готовы пойти на компромиссный вариант: Вы внесёте частичную небольшую предоплату, а остальную сумму оплатите при получении посылки.
Возврат и обмен товара
Возврат или обмен товара, который не подошел (не понравился), допускается, если с момента покупки прошло не более 7 дней (статья 26.1, пункт 4 ЗоЗПП) и он не входит в перечень товаров, не подлежащих возврату и обмену. Для проведения операции нужно позвонить по номеру +7(495)744-63-63 или отправить письмо на электронный адрес vitauct8@yandex.ru.
Обменять или вернуть товар можно в течение недели, если соблюдены условия:
- товар не использовался, не вскрывался;
- упаковка не повреждена;
- не нарушены технические, лечебные, другие свойства товара;
- сохранен товарный вид изделия;
- присутствуют ярлыки, пломбы;
- есть документация на продукцию, чек на покупку.
Обмен производится однократно на аналог такой же стоимости (без перерасчета) или на более дешевый/дорогой аналог с перерасчетом стоимости и возвратом/доплатой.
К сведению покупателей
При отказе от заказа Garbuzov.org обязуется вернуть уплаченную по договору сумму в течение 10 дней со дня предъявления требований по возврату, за исключением расходов на пересылку товара, которые оплачивает покупатель (статья 26.1). При ненадлежащем качестве продукции продавец берет на себя транспортные расходы в оба направления.
При 100 %-ной оплате заказ нужно получить до истечения срока хранения. Если заказчик не забирает посылку в установленные сроки хранения, товар возвращается отправителю. Транспортные расходы в этом случае оплачивает заказчик.
Подробную информацию можно узнать здесь.
Благодаря ученым из Университета Альберты в Канаде было изобретено средство, побеждающее раковую опухоль. Одолеть ее можно лишь активацией митохондрий, которые были подавлены болезнью. Изобретённый препарат «Дихлорацетат натрия», по утверждениям ученых, справляется с этой задачей и борется со многими типами рака.
Особую эффективность медикамента отмечают в борьбе с раком легких, отделов головного мозга и груди. Еще в 30-х годах ХХ века ученые пришли к выводу, что функциональные нарушения митохондрий клеток приводят к возникновению раковых опухолей. Митохондрии являются важнейшими органеллами живой клетки, и до недавнего времени ученые считали, что их разрушение — это не причина рака, а результат. Поэтому с 2005 года Мичелакис, который сомневался в этой гипотезе, начал тестовую работу над молекулами дихлорацетата натрия.
Лабораторные исследования препарата
Лабораторные испытания и тесты на животных показали, что лекарственное средство «Дихлорацетат натрия» является активатором фермента митохондрий, которые подавляются из-за возникших недугов независимо от типа онкологических заболеваний. Уменьшение раковых клеток достигается благодаря нормализации функций органелл. Препарат существенно отличается от химиотерапии тем, что не является токсичным и не воздействует угнетающе на здоровые клетки больного.
Профессор Мичелакис отмечает, что многопрофильность вещества, содержащегося в препарате, дает возможность бороться с большинством форм рака, за исключением сарком. Медикамент имеет влияние на онкологические образования, на которые нельзя воздействовать другими лекарствами. Вещество препарата не принадлежит ни одной из существующих фармацевтических компаний, поэтому медикамент не имеет патента. Это существенно сказывается на его ценовой доступности.
Лабораторные эксперименты показали, что препарат, оказывая уничтожающее действие на клетки злокачественной опухоли, не влияет при этом на здоровые части организма.
Когда начинать прием препарата?
Очень важно при лечении рака средство «Дихлорацетат натрия» принимать тогда, когда состояние организма еще удовлетворительное. Не стоит ждать прохождения нескольких курсов химиотерапии, которые оказывают существенные разрушения. К тому же раковые клетки имеют свойство вырабатывать иммунитет к химии. Это уже давно заметили медики. Первые несколько курсов химиотерапии действительно оказывают положительное влияние на протекание болезни, последующие же, наоборот, малоэффективны. Поэтому препарат нужно начинать принимать как можно раньше, даже совместно с курсами химии. Но дозировка должна составлять не более 15 мг на 1 кг веса.
Препарат «Дихлорацетат натрия»: состав
Состав лекарственного средства – натриевая соль дихлоруксусной кислоты. Соль находится в препарате в виде моногидрата, т. е. около 12% – кристаллизованная вода.
Ученые в настоящее время исследуют способы снижения токсичности рассматриваемого лекарственного средства и эффективность его в борьбе с раком.
Прием препарата
Это необходимо знать, если вы решили приобрести медикамент «Дихлорацетат натрия». Как принимать препарат для оказания помощи больному организму, ученые уже определили. Из расчета на 1 кг веса — по 25-50 мг в течение всего дня. Применение препарата в течение двух лет по 50 мг может вызвать периферическую невропатию, поэтому доза приема лекарственного средства была снижена до 25 мг, что способствовало прекращению неприятных явлений.
Если препарат при дозировке 25 мг на 1 кг веса вызывает нарушение пищеварения, тошноту, онемение в пальцах, затрудненность дыхания (также может спровоцировать депрессию, тремор, головокружение, сонливость, частое мочеиспускание, беспокойство), дозу необходимо снизить до 10 мг на 1 кг веса. Иногда рекомендуют вообще прекратить его прием на несколько дней. Затем снова необходимо вернуться к прежней дозировке – 25 мг на 1 кг веса в сутки. Отмечали случаи применения лимонной кислоты, которая оказывала снижение явлений периферической невропатии после приёма препарата «Дихлорацетат натрия». Инструкция по применению отмечает необходимость разбавлять рассматриваемый медикамент водой (100-150 мл). Это сделать несложно, так как лекарство имеет порошкообразную форму. Необходимо стараться избегать попадания препарата на кожу — он может вызвать раздражение.
Применение препарата при лизисе опухолей
Препарат может вызвать лизис злокачественной опухоли при острой лимфатической лейкемии, неходжкинской лимфоме, острой миелоцитической лейкемии, раке груди, клеточной карциноме, хронической лимфатической лейкемии, раке яичек, клеточной карциноме, медуллобластоме.
Лизисом злокачественной опухоли называется очень быстрый апоптоз раковых клеток (запрограммированная смерть), сопровождающийся резким ухудшением самочувствия (в исключительных случаях может вызвать летальный исход). В таких случаях необходимо сразу же прием препарата приостановить и проконсультироваться с врачом. Через несколько дней, возможно, разрешат возобновить применение препарата, при этом снизив дозу.
Данных о лекарственной несовместимости средства «Дихлорацетат натрия» с другими препаратами нет из-за его новизны (исключение – медикамент «Лазикс»).
Применение одновременно с кофеинизированными сортами чая, высокие дозы витамина В1, сочетание с лимонной кислотой, коэнзимом Q и альфа-липоидной кислотой добавляет эффективность препарату.
Эффективность препарата
Эффективность медикамента «Дихлорацетат натрия» зависит от некоторых факторов. Существенно снижает его лечебные свойства плохое состояние пациента. Например, когда у него из-за болезни затронуты жизненно важные органы, или разрушение произошло под воздействием химиотерапии. Также не рекомендуют применение средства, если больной не встает, постоянно испытывает боли, принимает наркотики.
Снижает эффективность препарата и сильное поражение недугом печени. Когда она не может справляться с погибшими раковыми клетками и продуктами распада, попадающими в кровь, ситуация усложняется.
При низкой дозировке эффективность препарата невысокая, при большой дозе результат становится заметнее. Но есть некоторые факторы риска. При большой дозировке может случиться так, что с продуктами распада опухоли печень не справится. Это вызовет интоксикацию организма, появление тошноты и рвоты. Поэтому дозировку нужно подбирать правильно.
Где приобрести?
Что делать, если кому-то необходимо приобрести препарат «Дихлорацетат натрия»? Где купить? Выпускается рассматриваемое лекарство в Канаде, поэтому можно заказать его, используя интернет-ресурсы, у производителей. Также существует возможность приобрести препарат у продавцов в России, закупающих его в Канаде. Цена на медикамент невысока, поэтому купить его могут позволить себе пациенты, принадлежащие к разным социальным слоям.
Отзывы о препарате
Положительный эффект лекарственного средства «Дихлорацетат натрия», отзывы о котором подтверждают его, прослеживается у многих больных раком. Препарат применяли одновременно и с курсом химеотерапии, и с иными лекарствами, что не снизило его эффективность.
Некоторые врачи не верили в выздоровление своих пациентов. Они были удивлены, когда больные шли на поправку. Многие отмечают отсутствие побочных эффектов при приеме препарата.
Отзывов отрицательных очень мало. Все они указывают на неэффективность медикамента «Дихлорацетат натрия». Что это? Известно, что некоторым пациентам препарат не помог избавиться от недуга. Некоторые люди отмечали появление рецидива болезни.
Как проверить подлинность препарата
На подлинность препарата «Дихлорацетат натрия» указывают некоторые факторы: он состоит из белых кристаллов, горьковатых на вкус. Если цвет кристаллов желтоватый, то медикамент имеет низкое качество, и применять его не рекомендуется. При растворении препарата в воде он не должен терять свой горьковатый вкус. Если разбавленный до кашицы порошок периодически наносить на кожу предплечья или внутреннюю поверхность плеча с интервалом в 1 минуту в течение 10 минут, то через какое-то время образуется малозаметное с окантовкой пятно. А через 5-10 часов это пятно станет более красным и четким. Спустя несколько дней на этом месте кожа может начать шелушиться.
Данный способ проверки рекомендуют использовать в крайнем случае: при добавлении в порошок серной кислоты, применяемой для аккумуляторов машин, произойдет реакция с выделением тепла и запаха дихлоруксусной кислоты. Само лекарство практически не имеет запаха. Чем выше качество препарата, тем меньше его запах. Если попробовать на вкус порошок, то он вызовет онемение, прохладу и вяжущий эффект.
1. Васляева С. Н., Люсов В. А., Цыганкова О. В., Гордеев И. Г., Волов Н. А. Безболевая ишемия миокарда: патогенетические и патофизиологические механизмы. Традиционные и метаболические аспекты терапии // Российский кардиологический журнал. – 2004. – № 4(48). – С. 74-83.
2. Мануйлов А. М., Попов К. А., Цымбалюк И. Ю., Литвинова М. Г., Хубиева Ф. У. Шестопалов А. В. Биологическая активность дихлорацетата натрия: концепции и механизмы (обзор литературы) // Кубанский научный медицинский вестник. – 2016. – № 6 (161). – С. 156–163.
3. Сорокіна Л., Бiлюк А., Хижняк С. Вплив натрій дихлорацетату на перебіг проокисно- антиоксидантних процесів в організмі мишей з саркомою 37 // Бiологiя. – 2011. – Випуск 57. – С. 35–37.
4. Сорокіна Л. В., Хижняк С. В., Дiденко Г. В., Степанова Л. I., Капля О. А. Структурний стан клітинних мембран саркоми 37 в динаміці росту // Фiзика живого. – 2010. – Т. 18. № 3. – С. 83–88.
5. Archer S. L., Weir E. K., Wilkins M. R. The basic science of pulmonary arterial hypertension for clinicians: new concepts and experimental therapies // Circulation. – 2010. – Vol. 121. № 18. – P. 2045–2066.
6. Barsan W. G. Treatment of cerebral ischemia with dichloroacetate // United States Patent Number: 4,631,294. – Date of Patent: Dec. 23, 1986. – Appl. No.: 752,091. – Filed: Jul. 5, 1985.
7. Bonnet S., Archer S. L., Allalunis-Turner J., Haromy A., Beaulieu C., Thompson R. et al. A mitochondria-K+ channel axis is suppressed in cancer and its normalization promotes apoptosis and inhibits cancer growth // Cancer Cell. – 2007. – Vol. 11. № 1. – P. 37–51.
8. Brandsma D., Dorlo T. P., Haanen J. H., Beijnen J. H., Boogerd W. Severe encephalopathy and polyneuropathy induced by dichloroacetate // Journal of Neurology. – 2010. – Vol. 257. № 12. – P. 2099–2100.
9. Cao W., Yacoub S., Shiverick K. T., Namiki K., Sakai Y., Porvasnik S. et al. Dichloroacetate (DCA) sensitizes both wild-type and over expressing Bcl-2 prostate cancer cells in vitro to radiation // The Prostate. – 2008. – Vol. 68. № 11. – P. 1223–1231.
10. De Stefano N., Matthews P. M., Ford B. et al. Short-term dichloroacetate treatment improves indices of cerebral metabolism in patients with mitochondrial disorders // Neurology. – 1995. – Vol.45. № 6. – P. 1193–1198.
11. Dhar S., Lippard S. J. Mitaplatin, a potent fusion of cisplatin and the orphan drug dichloroacetate // Proceedings of the National Academy of Sciences of the United States of America. – 2009. – Vol. 106. № 52. – P. 22199–22204.
12. Duncan G. E., Perkins L. A., Theriaque D. W., Neiberger R. E., Stacpoole P. W. Dichloroacetate therapy attenuates the blood lactate response to submaximal exercise in patients with defects in mitochondrial energy metabolism // The Journal of Clinical Endocrinology & Metabolism. – 2004. – Vol. 89. № 4. – P. 1733– 1738.
13. Fereidoonnezhad M., Faghih Z., Mojaddami A., Tabaei S. M. H., Rezaei Z. Novel approach synthesis, molecular docking and cytotoxic activity evaluation of N-phenyl-2,2- dichloroacetamide derivatives as anticancer agents // Journal of Sciences, Islamic Republic of Iran. – 2016. – Vol. 27. № 1. – P. 39–49.
14. Fiebiger W., Olszewski U., Ulsperger E., Geissler K., Hamilton G. In vitro cytotoxicity of novel platinum-based drugs and dichloroacetate against lung carcinoid cell lines // Clinical & translational oncology. – 2011. – Vol. 13. № 1. – P. 43–49.
15. Flavin D. Medullary thyroid carcinoma relapse reversed with dichloroacetate: a case report // Oncology Letters. – 2010. – Vol. 1. № 5. – P. 889–891.
16. Heshe D., Hoogestraat S., Brauckmann C., Karst U., Boos J., Lanvers-Kaminsky C. Dichloroacetate metabolically targeted therapy defeats cytotoxicity of standard anticancer drugs // Cancer Chemotherapy and Pharmacology. – 2011. – Vol. 67. № 3. – P. 647–655.
17. Ishiguro T., Ishiguro R., Ishiguro M., Iwai S. Co-treatment of dichloroacetate and omeprazole dramatically reduced the pain of pancreatic and bile duct cancer; possible blockade of their invasion // Abdominal Oncology. – 2013. – Vol. 1. – P. 1–4.
18. Ishiguro T., Ishiguro R., Ishiguro M., Iwai S. Co-treatment of dichloroacetate, omeprazole and tamoxifen exhibited synergistically antiproliferative effect on malignant tumors: in vivo experiments and a case report // Hepatogastroenterology. – 2012. – Vol. 59. № 116. – P. 994–996.
19. Jung G. -S., Jeon J. -H., Choi Y. -K., Jang S. Y., Park S. Y., Kim S. -W., Byun J. -K., Kim M. -K., Lee S., Shin E. -C., Lee I. -K., Kang Y. N., Park K. -G. Pyruvate dehydrogenase kinase regulates hepatitis C virus replication // Scientific Reports. – 2016. – Vol. 6. – Article number 30846.
20. Kaufmann P., Engelstad K., Wei Y., Jhung S., Sano M. C., Shungu D. C. et al. Dichloroacetate causes toxic neuropathy in MELAS: a randomized, controlled clinical trial // Neurology. – 2006. – Vol. 66. № 3. – P. 324–330.
21. Khan A. Case report of long term complete remission of metastatic renal squamous cell carcinoma after palliative radiotherapy and adjuvant dichloroacetate // Advances in Cancer: Research & Treatment. – 2012. – Vol. 2012. – Article ID 441895.
22. Khan A. Use of oral dichloroacetate for palliation of leg pain arising from metastatic poorly differentiated carcinoma: a case report // Journal of Palliative Medicine. – 2011. – Vol. 14. № 8. – P. 973–977.
23. Kinnaird A., Dromparis P., Haromy A., Bowers L., Hashimoto K., Sutendra G. et al. Dichloroacetate is a novel therapy for renal cell carcinoma // The Journal of Urology. – 2012. – Vol. 187. № 4. – P. e120–e121.
24. Kinnaird A., Dromparis P., Saleme B., Gurtu V., Watson K., Paulin R., Zervopoulos S., Stenson T., Sutendra G., Pink D. B., Carmine-Simmen K., Moore R., Lewis J. D., Michelakis E. D. Metabolic modulation of clear-cell renal cell carcinoma with dichloroacetate, an inhibitor of pyruvate dehydrogenase kinase // European Urology. – 2016. – Vol. 69. № 4. – P. 734–744.
25. Kluza J., Corazao-Rozas P., Touil Y., Jendoubi M., Maire C., Guerreschi P. et al. Inactivation of the HIF-1alpha/ PDK3 signaling axis drives melanoma toward mitochondrial oxidative metabolism and potentiates the therapeutic activity of pro-oxidants // Cancer Research. – 2012. – Vol. 72. № 19. – P. 5035–5047.
26. Kwitniewski M., Moan J., Juzeniene A. Metabolic-targeted therapy with dichloroacetate (DCA): a novel treatment strategy to improve the outcome of photodynamic therapy // Photochemical & Photobiological Sciences. – 2011. – Vol. 10. № 1. – P. 25–28.
27. Li T., Schultz I., Keys D. A., Campbell J. L., Fisher J. W. Quantitative evaluation of dichloroacetic acid kinetics in human – a physiologically based pharmacokinetic modeling investigation // Toxicology. – 2008. – Vol. 245. № 1–2. – P. 35–48.
28. Ludvik B., Peer G., Berzlanovich A., Stifter S., Graf H. Effects of dichloroacetate and bicarbonate on haemodynamic parameters in healthy volunteers // Clinical Science. – 1991. – Vol. 80. № 1. – P. 47–51.
29. Madhok B. M., Yeluri S., Perry S. L., Hughes T. A., Jayne D. G. Dichloroacetate induces apoptosis and cell-cycle arrest in colorectal cancer cells // British Journal of Cancer. – 2010. – Vol. 102. № 12. – P. 1746–1752.
30. Michelakis E. D., Sutendra G., Dromparis P., Webster L., Haromy A., Niven E. et al. Metabolic modulation of glioblastoma with dichloroacetate // Science Translational Medicine. – 2010. – Vol. 2. № 31. – P. 31ra34.
31. Michelakis E. D., Webster L., Mackey J. R. Dichloroacetate (DCA) as a potential metabolic-targeting therapy for cancer // British Journal of Cancer. – 2008. – Vol. 99. № 7. – P. 989–994.
32. Ohashi T., Akazawa T., Aoki M., Kuze B., Mizuta K., Ito Y., Inoue N. Dichloroacetate improves immune dysfunction caused by tumor-secreted lactic acid and increases antitumor immunoreactivity // International Journal of Cancer. – 2013. – Vol. 133. № 5. – P. 1107–1118.
33. Olszewski U., Poulsen T. T., Ulsperger E., Poulsen H. S., Geissler K., Hamilton G. In vitro cytotoxicity of combinations of dichloroacetate with anticancer platinum compounds // Clinical Pharmacology: Advances and Applications. – 2010. – Vol. 2. – P. 177–183.
34. Pfeffer G., Majamaa K., Turnbull D. M. et al. Treatment for mitochondrial disorders // Cochrane Database of Systematic Reviews. – 2012. – № 4. – CD004426.
35. Rajendran A., Bansal D., Marwaha R. K., Singhi S. C. Tumor lysis syndrome // The Indian Journal of Pediatrics. – 2013. – Vol. 80. № 1. – P. 50–54.
36. Ribes G., Valette G., Loubatieres-Mariani M. -M. Metabolic effects of sodium dichloroacetate in normal and diabetic dogs // Diabetes. – 1979. – Vol. 28. № 9. – P. 852–857.
37. Roh J. — L., Park J. Y., Kim E. H., Jang H. J., Kwon M. Activation of mitochondrial oxidation by PDK2 inhibition reverses cisplatin resistance in head and neck cancer // Cancer Letters. – 2016. – Vol. 371. № 1. – P. 20–29.
38. Rozier M. D., Zata V. J., Ellsworth M. L. Lactate interferes with ATP release from red blood cells // The American Journal of Physiology. Heart and Circulatory Physiology. – 2007. – Vol. 292. № 6. – P. H3038-H3042.
39. Saed G. M., Fletcher N. M., Jiang Z. L., Abu-Soud H. M., Diamond M. P. Dichloroacetate induces apoptosis of epithelial ovarian cancer cells through a mechanism involving modulation of oxidative stress // Reproductive Sciences. – 2011. – Vol. 18. № 12. – P. 1253–1261.
40. Shahrzad S., Lacombe K., Adamcic U., Minhas K., Coomber B. L. Sodium dichloroacetate (DCA) reduces apoptosis in colorectal tumor hypoxia // Cancer Letters. – 2010. – Vol. 297. № 1. – P. 75–83.
41. Shen H., Decollogne S., Dilda P. J., Hau E., Chung S. A., Luk P. P., Hogg P. J., McDonald K. L. Dual-targeting of aberrant glucose metabolism in glioblastoma // Journal of Experimental & Clinical Cancer Research. – 2015. – Vol. 34. № 1. – Article 14.
42. Shen Y., Fan H., Ou D., Liao S., Cheng A. et al. Dichloroacetate (DCA) enhances activities of sorafenib against hepatocellular carcinoma (HCC) via modulation of aberrant cellular metabolism of HCC cells // Molecular Cancer Therapeutics. – 2009. – Vol. 8. № 12 (Suppl.). – Abstract B97.
43. Shen Y. C., Ou D. L., Hsu C., Lin K. L., Chang C. Y., Lin C. Y. et al. Activating oxidative phosphorylation by a pyruvate dehydrogenase kinase inhibitor overcomes sorafenib resistance of hepatocellular carcinoma // British Journal of Cancer. – 2013. – Vol. 108. № 1. – P. 72–81.
44. Stacpoole P. W. Review of the pharmacologic and therapeutic effects of diisopropylammonium dichloroacetate (DIPA) // The Journal of Clinical Pharmacology. – 1969. – Vol. 9. № 5. – P. 282–291.
45. Stacpoole P. W. The pharmacology of dichloroacetate // Metabolism – Clinical and Experimental. – 1989. – Vol. 38. № 11. – P. 1124–1144.
46. Stacpoole P. W. Treatment of hyperlipoproteinemia with a dichloroacetate salt // United States Patent Number: 4,122,188. – Date of Patent: Oct. 24, 1978. – Appl. №: 828, 677. – Filed: Aug. 29, 1977.
47. Stacpoole P. W., Dunbar E. M., Shroads A. L., Coats B. S., Langaee T. Predictability of glutathione transferase zeta 1 haplotype on kinetics of dichloroacetate in human trials // Drug Metabolism Reviews. – 2011. – Vol. 43. – Suppl. 2. – P. 181–182.
48. Stacpoole P. W., Henderson G. N., Yan Z., Cornett R., James M. O. Pharmacokinetics, metabolism and toxicology of dichloroacetate // Drug Metabolism Reviews. – 1998. – Vol. 30. № 3. – P. 499–539.
49. Stacpoole P. W., Kerr D. S., Barnes C., Bunch S. T., Carney P. R., Fennell E. M. et al. Controlled clinical trial of dichloroacetate for treatment of congenital lactic acidosis in children // Pediatrics. – 2006. – Vol. 117. № 5. – P. 1519–1531.
50. Stacpoole P. W., Nagaraja N. V., Hutson A. D. Efficacy of dichloroacetate as a lactate- lowering drug // Journal of Clinical Pharmacology. – 2003. – Vol. 43. № 7. – P. 683–691.
51. Strum S. B., Adalsteinsson O., Black R. R., Segal D., Peress N. L., Waldenfels J. Case report: sodium dichloroacetate (DCA) inhibition of the «Warburg effect» in a human cancer patient: complete response in non-Hodgkin’s lymphoma after disease progression with rituximab-CHOP // Journal of Bioenergetics and Biomembranes. – 2013. – Vol. 45. № 3. – P. 307–315.
52. Sun R. C., Board P. G., Blackburn A. C. Targeting metabolism with arsenic trioxide and dichloroacetate in breast cancer cells // Molecular Cancer. – 2011. – Vol. 10. – Article 142.
53. Sun R. C., Fadia M., Dahlstrom J. E., Parish C. R., Board P. G., Blackburn A. C. Reversal of the glycolytic phenotype by dichloroacetate inhibits metastatic breast cancer cell growth in vitro and in vivo // Breast Cancer Research and Treatment. – 2010. – Vol. 120. № 1. – P. 253– 260.
54. Tong J., Xie G., He J., Li J., Pan F., Liang H. Synergistic antitumor effect of dichloroacetate in combination with 5-fluorouracil in colorectal cancer // Journal of Biomedicine & Biotechnology. – 2011. – Vol. 2011. – Article ID 740564.
55. Valauri-Orton A., Bschorer F., Bernd K. K. Dichloroacetate decreases cell health and activates oxidative stress defense pathways in rat alveolar type II pneumocytes // BioMed Research International. – 2015. – Vol. 2015. – Article ID 129031.
56. Vella S., Conti M., Tasso R., Cancedda R., Pagano A. Dichloroacetate inhibits neuroblastoma growth by specifically acting against malignant undifferentiated cells // International Journal of Cancer. – 2012. – Vol. 130. № 7. – P. 1484–1493.
57. Vissing J., Gansted U., Quistorff B. Exercise intolerance in mitochondrial myopathy is not related to lactic acidosis // Annals of Neurology. – 2001. – Vol. 49. № 5. – P. 672–676.
58. Wargovich T. J., MacDonald R. G., Hill J. A., Feldman R. L., Stacpoole P. W., Pepine C. J. Myocardial metabolic and hemodynamic effects of dichloroacetate in coronary artery disease // The American Journal of Cardiology. – 1988. – Vol. 61. № 1. – P. 65–70.
59. Washington J. T., Quintyne N. J. Dichloroacetate induces different rates of cell death in cancer and noncancer cell lines in vitro // Tumori. – 2012. – Vol. 98. № 1. – P. 142–151.
60. Wong J. Y., Huggins G. S., Debidda M., Munshi N. C., De Vivo I. Dichloroacetate induces apoptosis in endometrial cancer cells // Gynecologic Oncology. – 2008. – Vol. 109. № 3. – P. 394–402.
61. Xiao H., Yan L., Zhang Y., Qi R., Li W., Wang R. et al. A dual-targeting hybrid platinum (IV) prodrug for enhancing efficacy // Chemical Communications. – 2012. – Vol. 48. № 87. – P. 10730– 10732.
62. Xiao L., Li X., Niu N., Qian J., Xie G., Wang Y. Dichloroacetate (DCA) enhances tumor cell death in combination with oncolytic adenovirus armed with MDA-7/IL-24 // Molecular and Cellular Biochemistry. – 2010. – Vol. 340. № 1. – P. 31–40.
63. Xie J., Wang B. S., Yu D. H., Lu Q., Ma J., Qi H. et al. Dichloroacetate shifts the metabolism from glycolysis to glucose oxidation and exhibits synergistic growth inhibition with cisplatin in HeLa cells // International Journal of Oncology. – 2011. – Vol. 38. № 2. – P. 409–417.
64. Xue X., You S., Zhang Q., Wu Y., Zou G. Z., Wang P. C. et al. Mitaplatin increases sensitivity of tumor cells to cisplatin by inducing mitochondrial dysfunction // Molecular Pharmaceutics. – 2012. – Vol. 9. № 3. – P. 634–644.
65. Zajac J., Kostrhunova H., Novohradsky V., Vrana O., Raveendran R., Gibson D., Kasparkova J., Brabec V. Potentiation of mitochondrial dysfunction in tumor cells by conjugates of metabolic modulator dichloroacetate with a Pt(IV) derivative of oxaliplatin // Journal of Inorganic Biochemistry. – 2016. – Vol. 156. – P. 89–97.
66. Zhang N., Palmer A. F. Development of a dichloroacetic acid-hemoglobin conjugate as a potential targeted anti-cancer therapeutic // Biotechnology and Bioengineering. – 2011. – Vol.108. № 6. – P. 1413–1420.
Каждая таблетка 12,5 мг содержит:
Активное вещество: хлорталидон – 12,5 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая, крахмал прежелатинизированный (1500), хинолиновый желтый (Е104), натрия крахмала гликолят, кремния диоксид коллоидный, кислота стеариновая.
Каждая таблетка 25 мг содержит:
Активное вещество: хлорталидон – 25 мг
Вспомогательные вещества: целлюлоза микрокристаллическая, крахмал прежелатинизированный (1500), хинолиновый желтый (Е104), натрия крахмала гликолят, кремния диоксид коллоидный, кислота стеариновая.
Каждая таблетка 50 мг содержит:
Активное вещество: хлорталидон – 50 мг
Вспомогательные вещества: целлюлоза микрокристаллическая, крахмал прежелатинизированный (1500), хинолиновый желтый (Е104), натрия крахмала гликолят, кремния диоксид коллоидный, кислота стеариновая.
Дозировка 12,5 мг, 25 мг и 50 мг: круглые плоские таблетки желтого, цвета со скошенными краями с обеих сторон.
Диуретики. Сульфониламиды.
Код АТХ: С03ВА04
Фармакологические свойства
Фармакодинамика
Хлорталидон представляет собой бензотиадиазин (тиазидо)-подобный диуретик с длительным периодом действия. Тиазидные и тиазидоподобные диуретики действуют преимущественно на дистальные почечные канальцы (начальная извилистая часть), подавляя реабсорбцию NaCl (путем антагонизирования котранспортера Na+Cl–) и способствуя реабсорбции Ca++ (механизм неизвестен). Усиленная доставка Na+ и воды в кортикальный отдел собирающего почечного канальца и/или повышение скорости потока приводит к повышению секреций и выведению K+ и H+. У лиц с нормальной функцией почек диурез возникает после приема 12,5 мг хлорталидона. Усиление выведения натрия и хлора с мочой и менее выраженное повышение уровня калия в моче являются дозозависимыми и наблюдаются как у здоровых лиц, так и у пациентов с отеками. Диуретическое действие возникает спустя 2–3 часа, достигает максимума через 4–24 часа и может сохраняться в течение 2–3 дней. Вначале диурез, индуцированный приемом тиазидов, приводит к снижению объема плазмы, сердечного выброса и системного артериального давления. Вероятно, может быть активирована ренин-ангиотензиновая система. У пациентов с артериальной гипертензией хлорталидон обеспечивает постепенное снижение АД. При длительном применении поддержание гипотензивного эффекта обеспечивается, вероятно, за счет уменьшения периферического сосудистого сопротивления. Сердечный выброс возвращается к исходным значениям, сохраняется небольшое уменьшение объема плазмы, возможно увеличение активности ренина плазмы. При длительном приеме антигипертензивное действие хлорталидона зависит от дозы в диапазоне 12,5 и 50 мг/сутки. Превышение дозы 50 мг усиливает метаболические нарушения и редко оказывает благоприятный терапевтический эффект. Как и при приеме других диуретиков, когда хлорталидон назначают в качестве монотерапии; контроль артериального давления достигается приблизительно у половины пациентов с легкой и умеренной артериальной гипертензией. Как правило, пожилые и чернокожие пациенты хорошо реагируют на диуретики в качестве основной терапии. Рандомизированные клинические исследования пожилых пациентов показали, что терапия артериальной гипертензии или изолированной систолической гипертензии у пожилых людей, принимающих низкие дозы тиазидных диуретиков, включая хлорталидон, снижает заболеваемость и смертность от цереброваскулярного инсульта, ишемической болезни, а также общую сердечно-сосудистую смертность и заболеваемость. Комбинированная терапия с другими антигипертензивными средствами усиливает действие по снижению артериального давления. У большой части пациентов, которые не отреагировали должным образом на монотерапию, дальнейшее снижение артериального давления может быть достигнуто при назначении комбинированной схемы лечения. При почечном несахарном диабете хлорталидон парадоксальным образом снижает полиурию. Механизм действия не был выяснен.
Фармакокинетика
Всасывание и концентрация в плазме крови
Биодоступность пероральной дозы 50 мг хлорталидона составляет приблизительно 64 % с достижением максимальной концентрации в крови через 8–12 часов. Для дозы 25 и 50 мг значение Cmax в среднем составляет 1,5 мкг/мл (4,4 ммоль/л) и 3,2 мкг/мл (9,4 ммоль/л) соответственно. Для дозы до 100 мг наблюдается пропорциональное повышение значения AUC. При повторных ежедневных дозах 50 мг средняя равновесная концентрация 7,2 мкг/мл (21,2 ммоль/л) в конце интервала между приемом препарата, составляющего 24 часа, достигается через 1–2 недели.
Распределение
В крови только незначительная часть хлорталидона является свободной в связи с интенсивным накоплением в эритроцитах и связыванием с белками плазмы крови. Благодаря высокой степени связывания с карбоангидразой эритроцитов только 1,4 % общего количества хлорталидона в цельной крови отмечалось в плазме крови в равновесном состоянии в ходе терапии дозой 50 мг. Связывание с белками плазмы в условиях in vitro хлорталидона составляет приблизительно 76 %, основной связывающий белок – альбумин. Хлорталидон проникает через плацентарный барьер и попадает в грудное молоко. У матерей, получавших 50 мг хлорталидона ежедневно до и после родов, уровень хлорталидона в цельной крови плода составляет около 15 % от уровня, обнаруженного в крови матери. Концентрация хлорталидона в околоплодной жидкости и в материнском молоке составляет приблизительно 4 % соответствующего уровня в материнской крови.
Метаболизм
Метаболизм и выведение с желчью являются вспомогательными путями выведения. В течение 120 часов около 70 % дозы выводится с мочой и калом, как правило, в неизмененном виде.
Выведение
Хлорталидон выводится из цельной крови и плазмы с периодом полувыведения равным в среднем 50 часов. Период полувыведения не изменяется при длительном применении. Основная часть абсорбированной дозы хлорталидона выводится через почки со средним почечным клиренсом 60 мл/мин.
Особые группы пациентов
Нарушение функции почек не изменяет фармакокинетику хлорталидона. Вероятно, фактором, ограничивающим скорость выведения препарата из крови или плазмы, является его сродство с карбоангидразой эритроцитов. У пациентов с почечной недостаточностью корректировки дозировки не требуется. У пожилых пациентов хлорталидон выводится медленнее, чем у здоровых лиц молодого возраста, несмотря на одинаковую всасываемость. Следовательно, при проведении терапии хлорталидоном у пациентов пожилого возраста следует проводить тщательное медицинское обследование.
Хлорталидон показан:
В терапии артериальной гипертензии: эссенциальной, нефрогенной или изолированной систолической при клиренсе креатинина > 30 мл/мин;
В терапии стабильной хронической сердечной недостаточности от легкой до умеренной степени (II или III функциональный класс по классификации Нью-йоркской кардиологической ассоциации (ФК NYHA)) при клиренсе креатинина > 30 мл/мин;
В терапии отека специфического происхождения (при асците у стабильных пациентов с циррозом печени, под постоянным контролем; при отеке, обусловленным наличием нефротического синдрома: только у пациентов с нормальным уровнем калия в крови, без признаков гиповолемии или тяжелой гипоальбуминемии);
Несахарный диабет.
Хлорталидон противопоказан:
пациентам с известной гиперчувствительностью к хлорталидону или другим лекарственным средствам, производным сульфонамида;
при анурии;
при печеночной или почечной недостаточности тяжелой степени (клиренс креатинина < 30 мл/мин);
при резистентной гипокалиемии, гипонатриемии и гиперкальциемии;
при преренальной (кардиогенной) почечной недостаточности;
при состояниях, характеризующихся повышенной потерей калия (например, при некоторых видах нефропатии);
при симптоматической гиперурикемии (подагра или почечные камни мочевой кислоты в анамнезе);
при артериальной гипертензии во время беременности;
при нелеченой болезни Аддисона;
при сопутствующей терапии литием.
Дозу хлорталидона следует индивидуально титровать для получения наименьшей эффективной дозы, что позволяет свести к минимуму возникновение возможных побочных эффектов. Это особенно важно у пожилых людей.
Хлорталидон принимается внутрь, предпочтительно в виде одной суточной дозы во время завтрака.
Артериальная гипертензия
Терапевтические дозы варьируют от 12,5 до 50 мг в день. Рекомендуемая начальная доза составляет 12,5–25 мг/сут. Максимальный антигипертензивный эффект обычно достигается при приеме суточной дозы 25 мг. При рекомендованных режимах дозирования адекватный клинический эффект, как правило, достигается через 3–4 недели. Превышение суточной дозы 50 мг увеличивает риск возникновения осложнений, связанных с нарушением обмена веществ и электролитов.
Если артериальное давление недостаточно контролируется при использовании 25 мг или 50 мг в сутки, возможно назначение комбинированной терапии, например, с β-блокаторами или ингибиторами АПФ. В случае одновременного назначения ингибитора АПФ, следует либо уменьшить дозу хлорталидона, либо временно отменить его прием.
Стабильная хроническая сердечная недостаточность (II или III функциональный класс по классификации Нью-йоркской кардиологической ассоциации (NYHA))
Рекомендуемая начальная доза составляет 25–50 мг/сут, в тяжелых случаях возможно ее увеличение до 100 мг/сут. Максимально допустимая доза – 200 мг/сут. Для поддерживающей терапии используются наименьшие эффективные дозы; стандартная поддерживающая доза – 25–50 мг ежедневно или через день.
Если ответная реакция неудовлетворительная, допускается включение в схему лечения сердечных гликозидов (на основе дигиталиса) или ингибиторов АПФ.
Отечный синдром (см. показания к применению)
Следует определить минимально эффективную дозу, начав прием с 12,5–25 мг/сутки с последующим титрованием. Хлорталидон следует применять в течение ограниченного временного периода. Суточная доза не должна превышать 50 мг.
Несахарный диабет
Начальная доза составляет 100 мг два раза в сутки, постепенно уменьшая до поддерживающей дозы 50 мг один раз в сутки.
Особые категории пациентов
Пожилые пациенты: рекомендуется минимальная эффективная доза хлорталидона. У пожилых пациентов хлорталидон выводится медленнее, чем у здоровых лиц молодого возраста, несмотря на одинаковую всасываемость. Таким образом, может потребоваться снижение рекомендуемой дозы для взрослых. Во время терапии хлорталидоном следует проводить тщательное медицинское обследование пациентов пожилого возраста.
Применение у пациентов с почечной недостаточностью: пациентам с почечной недостаточностью легкой степени также рекомендуется минимальная эффективная доза хлорталидона.
У пациентов с клиренсом креатинина ниже 30 мл/мин хлорталидон и тиазидные диуретики утрачивают свой диуретический эффект.
Применение у детей возможно. Необходимо использовать наименьшую эффективную дозу. Рекомендуемая начальная доза – от 0,5–1,0 мг/кг/48 часов, максимально допустимая доза составляет 1,7 мг/кг/48 часов.
Частота возникновения: очень редко < 0,01 %, редко от < 0,01 % до < 0,1 %; иногда от < 0,1 % до < 1 %; часто от <1 % до < 10 %; очень часто > 10 %.
Нарушения со стороны обмена веществ и питания
Очень часто: преимущественно при высоких дозах, гипокалиемия, гиперурикемия и повышение липидов в крови; часто: гипонатриемия, гипомагнезиемия и гипергликемия; иногда: подагра; редко: гиперкальциемия, глюкозурия, ухудшение диабетического метаболического состояния; очень редко: гипохлоремический алкалоз.
Нарушения со стороны кожи и подкожных тканей
Часто: крапивница и другие формы кожной сыпи; редко: фоточувствительность.
Нарушения со стороны печени и желчевыводящих путей
Редко: внутрипеченочный холестаз или желтуха.
Нарушения со стороны сердца
Редко: нарушения ритма сердца
Нарушения со стороны сосудов
Часто: ортостатическая гипотензия; очень редко: васкулит.
Нарушения со стороны нервной системы
Часто: головокружение; редко: парестезия, головная боль.
Нарушения со стороны желудочно-кишечного тракта
Часто: потеря аппетита и незначительные расстройства ЖКТ; редко: тошнота и рвота, боль в желудке, запор и диарея; очень редко: панкреатит.
Нарушения со стороны крови и лимфатической системы
Редко: тромбоцитопения, лейкопения, агранулоцитоз и эозинофилия; неизвестно: апластическая анемия.
Нарушения со стороны органа зрения
Редко: нарушение остроты зрения
Иные явления
Часто: импотенция; редко: аллергический отек легких (расстройство дыхания), аллергический интерстициальный нефрит.
Пациент должен быть информирован, что в случае возникновения перечисленных или любых других побочных реакций, не указанных в данной инструкции, ему следует обратиться к врачу.
Медицинским работникам рекомендуется направлять информацию о любых подозреваемых нежелательных реакциях и неэффективности лекарственного средства по адресу: Республиканское унитарное предприятие «Центр экспертиз и испытаний в здравоохранении», веб-сайт: rceth.by.
Симптомы острой передозировки включают: тошноту, слабость, сонливость, гиповолемию, гипотензию, головокружение и нарушения электролитного баланса, ассоциированные с аритмией сердца и мышечными спазмами. ЛД50 средства при пероральном введении мышам и крысам превышает 25 000 мг/кг массы тела. Минимальная летальная доза (МЛД) для человека не установлена.
Специфического антидота хлорталидона при передозировке нет. Для снижения абсорбции следует промыть желудок, вызвать рвоту или принять активированный уголь. Следует осуществлять тщательный мониторинг артериального давления и водно-электролитного баланса и принять соответствующие корректирующие меры. В случае необходимости они включают осторожное введение внутривенного раствора декстрозы и солевого раствора с добавлением калия.
Взаимодействие с другими лекарственными средствами и иные формы взаимодействия
Хлорталидон способен оказывать дополнительное действие или усиливать действие других антигипертензивных лекарственных средств (например, гуанетидина, метилдопы, бета-блокаторов, сосудорасширяющих средств, антагонистов кальция и ингибиторов АПФ). Антигипертензивный эффект ингибиторов АПФ усиливают средства, повышающие активность ренина в плазме (диуретики). Рекомендуется снизить дозу диуретика или отменить его в течение 2–3 дней и/или начать терапию ингибитором АПФ с низкой начальной дозы. Следует осуществлять мониторинг пациентов в течение нескольких часов после приема первой дозы. Гипокалиемическое действие диуретиков усиливается при приеме кортикостероидов, адренокортикотропного гормона, G2-агониста, амфотерицина и карбеноксолона.
Потребности в инсулине у больных с диабетом могут увеличиться, снизиться или остаться неизменными. Может потребоваться увеличение дозы пероральных гипогликемических лекарственных средств.
Хлорталидон и аналогичные лекарственные средства могут увеличивать восприимчивость к тубокурарину, способны снижать восприимчивость к норадреналину. Такое снижение не является существенным, чтобы оказать влияние на прессорные системы на терапевтическом уровне.
Гипокалиемия или гипомагнезиемия, обусловленные приемом тиазидов, могут спровоцировать возникновение дигиталис-индуцированной сердечной аритмии.
Сопутствующий прием некоторых нестероидных противовоспалительных средств (например, индометацина) может снизить диуретическую и антигипертензивную активность хлорталидона. Сообщалось об отдельных случаях ухудшения функции почек у предрасположенных пациентов. Антихолинергические лекарственные средства (например, атропин, бипериден) могут повышать биодоступность тиазидоподобных диуретиков, что связано со снижением двигательной активности ЖКТ и скорости опорожнения желудка.
Всасывание тиазидных диуретиков нарушается в присутствии анионообменных смол, например, холестирамина. Предполагается снижение фармакологического эффекта.
Одновременное применение тиазидных диуретиков может увеличивать риск возникновения реакций повышенной чувствительности на аллопуринол, увеличивать риск побочного действия амантадина, усиливать гипергликемический эффект диазоксида, снижать почечную экскрецию цитотоксических средств (например, циклофосфамида, метотрексата) и усиливать их миелосупрессивное действие. Одновременный прием тиазидных диуретиков с витамином D или солями кальция может привести к их повышению до клинически значимых уровней. Возникшая гиперкальциемия, как правило, носит преходящий характер, однако у пациентов с гиперпаратиреозом возможен риск развития устойчивой гиперкальциемии, сопровождающейся симптомами (слабость, утомляемость, анорексия).
Одновременный прием циклоспорина может увеличивать риск гиперурикемии и подагры. Хлорталидон снижает почечный клиренс лития, повышая риск интоксикации литием. Пациентов следует предупредить о том, что прием алкоголя увеличивает риск развития головокружения.
Снижение объема циркулирующей жидкости, вызванное приемом диуретика, может усиливать нефротоксичность аминогликозидов. Хлорталидон снижает активность протромбина. Производные тиазида могут усиливать подавление деятельности костного мозга, вызванное химиотерапией при лечении рака (например, нейтропения).
Электролиты
Лечение тиазидными диуретиками ассоциируется с электролитными нарушениями, такими как гипокалиемия, гипомагниемия, гипергликемия и гипонатриемия. Поскольку экскреция электролитов увеличивается, следует избегать очень строгой диеты с ограничением соли.
Гипокалиемия может приводить к повышению чувствительности сердца на токсическое действие производных дигиталиса. Степень выведения калия, индуцированного приемом тиазидных диуретиков, зависит от дозы и варьирует у разных пациентов. При приеме хлорталидона в дозе от 25 до 50 мг/сут, снижение концентрации калия в сыворотке крови в среднем составляет 0,5 ммоль/л.
Периодически необходимо определять содержание электролитов в сыворотке крови. При длительном лечении рекомендуется определять концентрацию калия в сыворотке крови в начале лечения и через 3–4 недели, затем – через одинаковые промежутки времени (например, каждые 4–6 месяцев), если только баланс калия дополнительно не нарушается другими факторами, такими как рвота, парентеральное введение жидкости и пр.
Определение содержания электролитов особенно важно у пожилых пациентов, а также у пациентов, которые принимают сердечные гликозиды или страдают рвотой, диареей, имеют нарушения функции почек, асцит из-за цирроза печени, отек вследствие нефротического синдрома.
При необходимости хлорталидон можно комбинировать с пероральным приемом добавок, содержащих калий или с калийсберегающими диуретиками (например, триамтереном). Однако следует избегать данных комбинаций у пациентов, также получающих ингибиторы АПФ и блокаторы рецепторов ангиотензина II.
Если гипокалиемия сопровождается клиническими признаками (например, мышечная слабость, парез, изменения на ЭКГ), прием хлорталидона следует прекратить. При нефротическом синдроме использование хлорталидона возможно только под тщательным наблюдением у пациентов без признаков гиповолемии и с нормальным уровнем калия в сыворотке крови.
Рекомендуется регулярный мониторинг сывороточного натрия, так как тиазидные диуретики могут вызвать или усугубить существующую гипонатриемию. Имеются отдельные сообщения о возникновении гипонатриемии с такими клиническими симптомами, как тошнота, слабость, прогрессирующая дезориентация и апатия после лечения тиазидами. Тиазидные диуретики следует назначать только после коррекции дефицита натрия и/или объема жидкости, с большой осторожностью использовать у пожилых пациентов.
Тиазиды уменьшают секрецию кальция в моче и могут вызвать небольшое увеличение кальция в сыворотке в отсутствие известных аномалий в метаболизме кальция.
Поскольку хлорталидон может увеличить кальций в сыворотке, следует проявлять осторожность только при гиперкальциемии. Наличие чрезмерной гиперкальциемии, не имеющей связи с отменой тиазида, или если уровень кальция ≥ 12 мг/дл, может указывать на то, что в основе данных нарушений лежат другие причины. Поэтому при возникновении гиперкальциемии необходимы дополнительные диагностические действия, чтобы прояснить ее причину.
Метаболические эффекты
Хлорталидон может повышать уровень мочевой кислоты в сыворотке, но приступы подагры при длительном лечении случаются нечасто.
Как и при использовании других тиазидных диуретиков, может наблюдаться непереносимость глюкозы, которая проявляется в виде гипергликемии и гликозурии. Хлорталидон, как и другие тиазиды, очень редко провоцирует возникновение или усугубление сахарного диабета; изменения обычно носят обратимый характер при прекращении лечения.
При длительном лечении тиазидами и тиазидоподобными диуретиками у пациентов наблюдалось незначительное или частично обратимое увеличение концентрации в плазме общего холестерина, триглицеридов или холестерина липопротеинов низкой плотности.
Клиническая значимость данных фактов является предметом обсуждения.
Хлорталидон не следует использовать в качестве терапии первой линии для длительного лечения у пациентов с выраженным сахарным диабетом или у субъектов, получающих лечение для коррекции гиперхолестеринемии (диета или комбинированное лечение).
Нарушения со стороны органов зрения
Использование хлорталидона ассоциировалось с идиосинкразической реакцией, которая проявлялась возникновением временной острой близорукости и острой закрытоугольной (узкоугольной) глаукомы. Симптомы включают внезапное снижение остроты зрения или острую боль в глазах; они обычно возникают в течение нескольких часов после начала приема лекарственного средства. Отсутствие лечения глаукомы может привести к постоянной потере зрения. Первым шагом является прекращение использования хлорталидона как можно скорее. Если внутриглазное давление остается высоким, врачами-специалистами принимается решение о проведении медикаментозного или хирургического лечения. К факторам риска развития для острой глаукомы относят наличие в анамнезе аллергической реакции на сульфонамиды или пенициллин.
Дозирование, эффективность и другие эффекты
Как и при назначении других антигипертензивных средств, следует соблюдать осторожность и титровать дозы хлорталидона у пациентов с тяжелым коронарным или церебральным атеросклерозом.
Антигипертензивный эффект ингибиторов АПФ потенцируют агенты, повышающие активность ренина в плазме (диуретики). Поэтому рекомендуется снижать дозу диуретика или отменить его прием на 2–3 дня и/или начать терапию ингибитором АПФ с низкой начальной дозы. Следует осуществлять контроль состояния пациентов в течение нескольких часов после приема первой дозы.
Реакции гиперчувствительности могут развиваться у пациентов, имеющих в анамнезе аллергию или бронхиальную астму.
Имеется потенциал влияния тиазидов на обострение системной красной волчанки.
Следует избегать применения диуретиков в терапии отека или АГ во время беременности, поскольку их применение связывают с развитием гиповолемии, повышенной вязкости крови и снижением плацентарного кровотока. Сообщалось о нескольких случаях подавления деятельности костного мозга плода, тромбоцитопении, эмбриональной желтухи и желтухи новорожденных на фоне приема тиазидных диуретиков.
Хлорталидон проникает в грудное молоко. Матерям, принимающим хлорталидон, следует воздержаться от грудного вскармливания.
Применение в педиатрии
Применение у детей возможно. Необходимо использовать наименьшую эффективную дозу. Рекомендуемая начальная доза от 0,5–1,0 мг/кг/48 часов, максимально допустимая доза 1,7 мг/кг/48 часов.
Влияние на способность управлять автотранспортными средствами и другими механизмами
Не проводилось исследований по изучению влияния хлорталидона на способность управлять транспортным средством и использовать механизмы. Следует соблюдать осторожность при управлении автотранспортом или работе, связанной с повышенной концентрацией внимания и психомоторной реакцией (во время терапии может возникать головокружение).
По 10 таблеток в блистер ПВДХ/ПВХ.
По 3 блистера в картонную пачку вместе с инструкцией по применению.
Хранить в защищенном от влаги месте при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
2 года. Не использовать после истечения срока годности.
По рецепту врача.
Информация о производителе
«Ипка Лабораториз Лимитед», Индия
48, Kandivli Industrial Estate, Kandivli (West), Mumbai 400067 India
48, Кандивли Индастриал Эстейт, Кандивли (Вест), Мумбай 400067, Индия
Представительство КОО «Ипка Лабораториз Лимитед» в Республике Беларусь
220089, г. Минск, ул. Уманская, 54, оф. № 13, тел.+375 17 328 18 47
Статья на конкурс «Био/Мол/Текст»: Корректировка диеты часто применяется для лечения и профилактики заболеваний. Онкологические заболевания — не исключение: правильное питание может служить не только профилактической мерой, но и повышать эффективность терапии. Здесь мы предлагаем обсудить «вкусовые предпочтения» раковых клеток и разобраться в том, как отдельные питательные вещества могут помочь бороться с опухолью.
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2021/2022.
Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Введение: на вкус и цвет товарищей нет
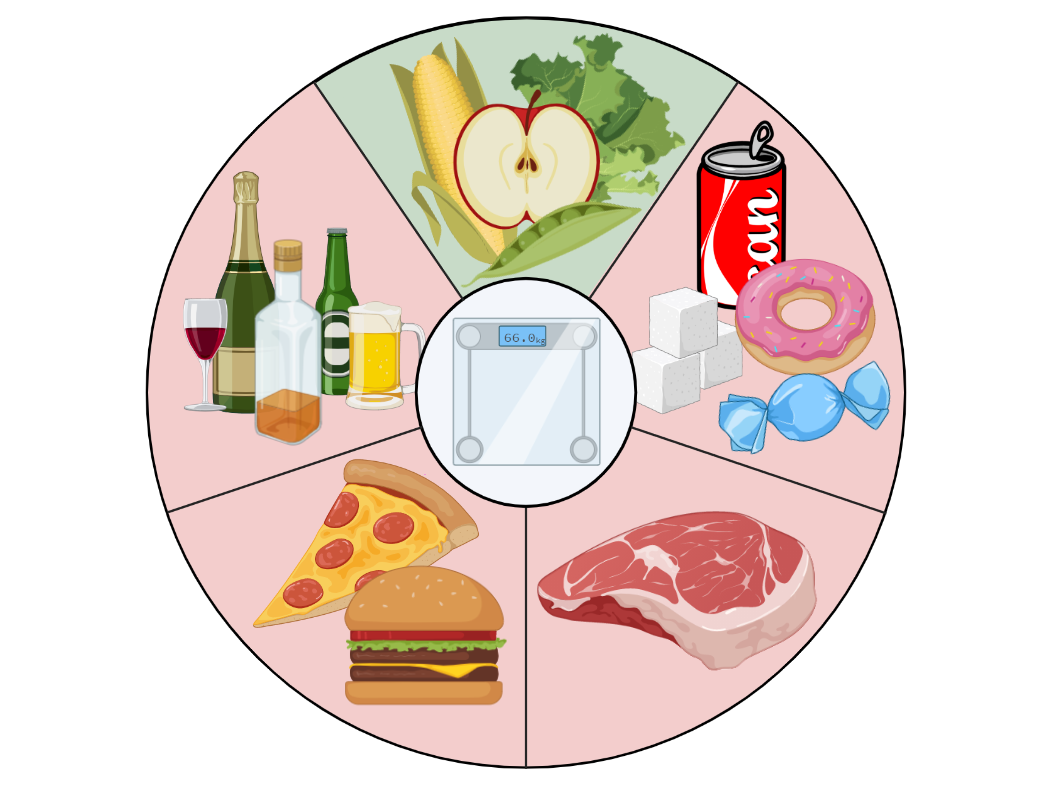
С начала 1980-х годов ведущие организации здравоохранения выпускают рекомендации по питанию и образу жизни, которые позволяют снизить индивидуальный риск развития рака. Данные рекомендации основаны на результатах метаанализов эпидемиологических исследований (иными словами, анализ многолетнего опыта миллионов людей, которые питались тем или иным образом). Эти рекомендации универсальны и просты в исполнении: они не требуют подсчета калорий, строгого контроля состава продуктов, а лишь предлагают общую схему и принцип питания для поддержания здорового веса (рис. 1).
Рисунок 1. Рекомендации по питанию, которые направлены на снижение вероятности возникновения онкологических заболеваний. Ежедневный рацион должен включать фрукты, овощи, бобовые культуры, цельнозерновые крупы. По возможности, необходимо ограничивать употребление красного мяса, сахара, сладких газированных напитков и алкоголя. Следование данным советам позволит поддерживать здоровый вес в течение всей жизни и снизить индивидуальный риск развития рака.
коллаж авторов статьи. Создан с помощью BioRender.com
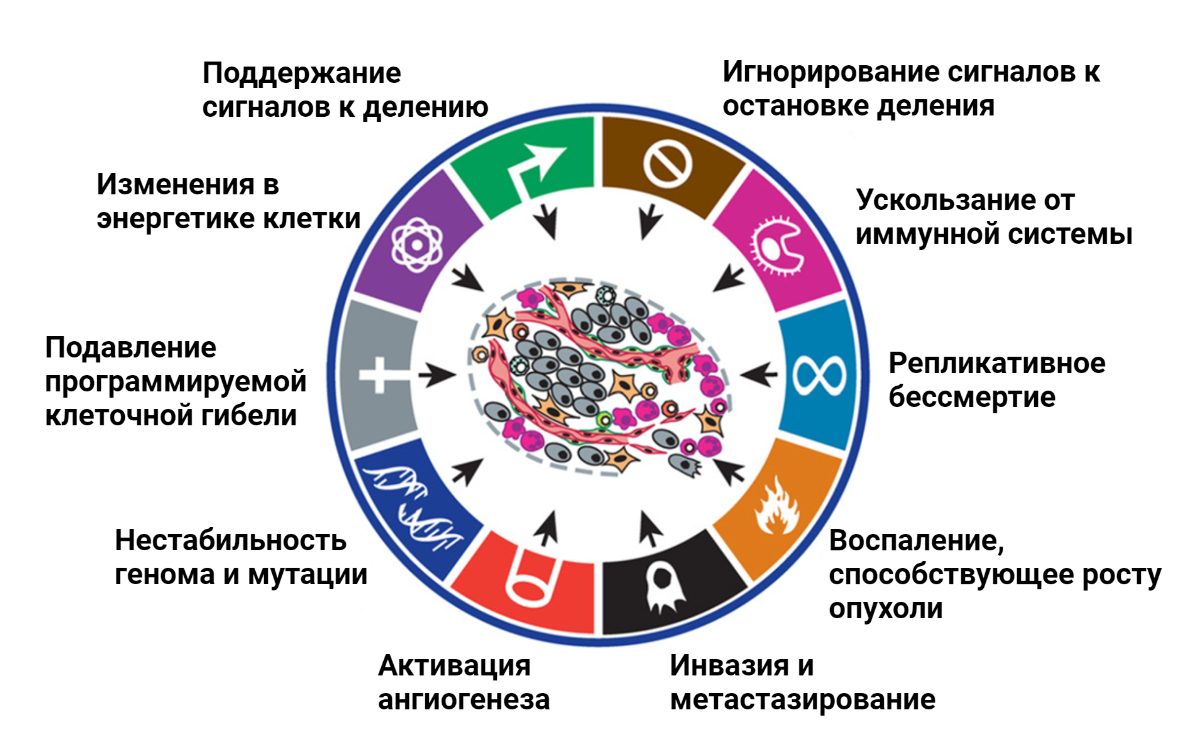
Подобного рода советы относятся к здоровым людям, тогда как для людей, страдающих онкологическими заболеваниями, стандартных рекомендаций по питанию не существует. В то же время, питание пациентов может сильно влиять на успешность терапии злокачественных образований [1]. Почему для людей, больных раком, нельзя составить универсальные рекомендации по составу пищи? Ответ на этот вопрос следует из принципов, согласно которым развиваются все опухоли [2]. Изначально клетка, которая в будущем даст начало опухоли, ничем не отличается от своих соседей. По мере накопления мутаций нормальные клетки могут постепенно эволюционировать и приобретать черты раковых клеток [3], [4]. В 2000 году среди многочисленных особенностей рака, в легендарном обзоре Hallmarks of cancer [3] были обозначены основные признаки, которые определяют биологию опухолевой клетки (рис. 2).
Рисунок 2. Особенности опухолевых клеток (hallmarks of cancer), которые отличают их от нормальных. Были сформулированы в 2000 году [3] и затем дополнены в 2011 [4].
адаптировано из [4]
Важнейшей особенностью всех раковых клеток является нестабильность генома, которая приводит к огромному генетическому разнообразию опухолей. Несмотря на ряд свойств, присущих всем раковым клеткам, каждая опухоль обладает уникальным набором мутаций, которые и определяют ее агрессивность, скорость роста, эффективность терапии. Генетическое разнообразие опухолей является основной преградой для составления универсальных рекомендаций по питанию для пациентов.
В последнее время исследователи активно изучают влияние питательных веществ на прогрессию опухоли и эффективность лечения. В основном проводятся экспериментальные работы на животных моделях, но есть и немногочисленные клинические исследования. Мы предлагаем читателям познакомиться поближе с особенностями метаболизма опухолевой клетки. Попытаемся разобраться, как вещества, потребляемые с пищей, могут влиять на опухоль и ее окружение. И, наконец, попробуем ответить на вопрос: может ли диета помочь в борьбе с раком?
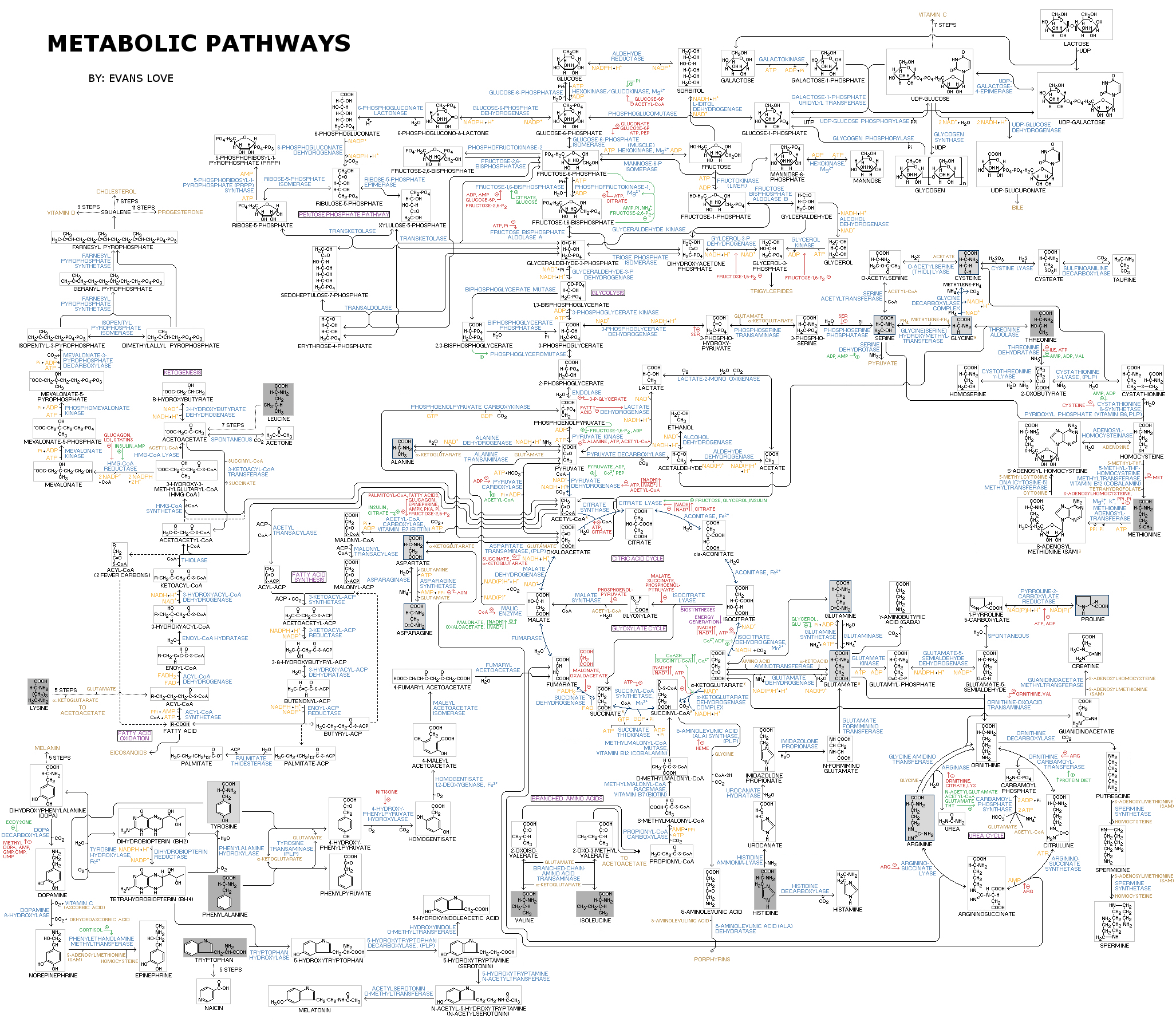
Для того, чтобы разобраться в тонкостях метаболизма раковой клетки, кратко вспомним основные принципы и термины биоэнергетики. Метаболизм — это совокупность химических превращений в клетке, которые направлены на получение энергии и необходимых веществ. Только посмотрите, какое бесчисленное количество реакций включает в себя метаболизм (рис. 3)! Все метаболические пути можно условно разделить на биодеградацию (катаболизм) и биосинтез (анаболизм) [5]. Катаболизм приводит к получению энергии в виде макроэргических соединений (таких как АТФ), а также NADH, NADPH и FADH2 — коферментов, участвующих в окислительно-восстановительных реакциях. Анаболические процессы используют запасенную энергию для синтеза молекул, необходимых для жизни клетки: жиров, нуклеотидов, белков, углеводов.
Рисунок 3. Метаболическая карта — схема, объединяющая основные метаболические пути в клетке.
Метаболизм тесно связан с питанием: ежедневно мы потребляем питательные вещества, которые, с одной стороны, участвуют в катаболических реакциях и поставляют энергию клеткам, а с другой — необходимы для синтеза собственных молекул. Углеводы, белки и жиры, которые мы потребляем, разрушаются в пищеварительном тракте до мономерных единиц: углеводы до моносахаридов (глюкоза, фруктоза и др.), жиры до жирных кислот и глицерина, белки до аминокислот. Эти молекулы поступают в клетки организма и принимают участие в метаболических процессах.
В раковой клетке зачастую увеличена активность некоторых метаболических ферментов или целых метаболических путей, а значит, и потребность в питательных веществах у клеток опухоли может отличаться от нормальных клеток [6]. Эти особенности могут быть учтены при лечении опухоли: исключение из рациона пациента определенных компонентов пищи приведет к понижению их содержания в плазме крови, а следовательно, и в окружении раковых клеток, что негативно скажется на их размножении. Кроме этого, некоторые элементы питания могут непосредственно влиять на противоопухолевый иммунитет, что также должно быть учтено при составлении диеты.
Глюкоза
Глюкоза является основным источником энергии для живых организмов. В нормальном рационе человека она встречается как в свободном виде, так и в составе олиго- и полисахаридов (например, в сахарозе, лактозе и мальтозе). Одним из важнейших биоэнергетических путей в клетке является гликолиз — последовательность химических реакций, в результате которых из 1 молекулы глюкозы получается 2 молекулы пировиноградной кислоты, 2 молекулы АТФ и 2 молекулы NADH. Затем пировиноградная кислота может быть вовлечена в цикл трикарбоновых кислот (цикл Кребса) — биохимический процесс, протекающий в митохондриях, который поставляет NADH и FADH2 что, в конечном счете, делает возможным синтез АТФ посредством окислительного фосфорилирования. При этом из 1 молекулы глюкозы можно получить приблизительно 36 молекул АТФ, что гораздо более выгодно с точки зрения энергетики, нежели просто гликолиз. Вследствие этого большинство клеток активно использует цикл трикарбоновых кислот и окислительное фосфорилирование для получения энергии.
Тем не менее, известно множество случаев, когда по разным причинам клетки смещают баланс в сторону гликолиза, используя этот путь в качестве основного источника энергии, ингибируя ферменты цикла трикарбоновых кислот или активируя ферменты гликолиза.
Давно известно, что опухолевые клетки активно используют гликолиз, несмотря на его относительно низкую эффективность с точки зрения энергетической выгоды. Это явление было открыто Отто Генрихом Варбургом в 1924 году. Сам Варбург считал, что нарушение клеточного дыхания — главная причина развития опухоли. Однако оказалось, что клеточное дыхание в большинстве опухолевых клеток не нарушено, а просто подавляется из-за активного гликолиза. Сейчас понятно, что активный гликолиз дает преимущество опухолевым клеткам. Во-первых, гликолиз протекает без кислорода, и, по-видимому, во многом является адаптацией к гипоксии, которая развивается по мере удаления опухолевых клеток от кровеносных сосудов. Частично эта проблема также решается тем, что раковые клетки могут способствовать ангиогенезу — прорастанию сосудов в опухоль за счет продукции ангиогенных факторов, например фактора роста эндотелия сосудов (VEGF, Vascular endothelial growth factor). Во-вторых, активный гликолиз сопряжен с образованием большого количества молочной кислоты, что приводит к закислению среды, тем самым способствуя инвазии опухоли за счет разрушения нормальных популяции клеток и деградации внеклеточного матрикса.
В то же время, нельзя не отметить тот факт, что эффект Варбурга наблюдается не только в опухолевых клетках, но и вообще во всех активно пролиферирующих клетках. Глюкоза — один из основных источников углерода в клетке, и ее полное окисление в цикле трикарбоновых кислот идет вразрез с потребностями пролиферирующей клетки. Некоторая часть глюкозы, а точнее, ее метаболитов, должна быть направлена на пути биосинтеза аминокислот, нуклеотидов и жирных кислот. Важную роль в производстве предшественников нуклеотидов и аминокислот, а также NADPH, необходимого для синтеза жирных кислот, играет пентозофосфатный путь — альтернативный путь окисления глюкозы, который также имеет ключевое значение в поддержании роста раковых клеток.
Итак, глюкоза особенно необходима раковым клеткам в связи с их активным размножением; при этом она служит не только источником энергии, но и важным предшественником для синтеза аминокислот, нуклеотидов и жирных кислот. Однако помимо непосредственной роли глюкозы в клеточном метаболизме, важным физиологическим аспектом также является эффект инсулина на опухолевые клетки.
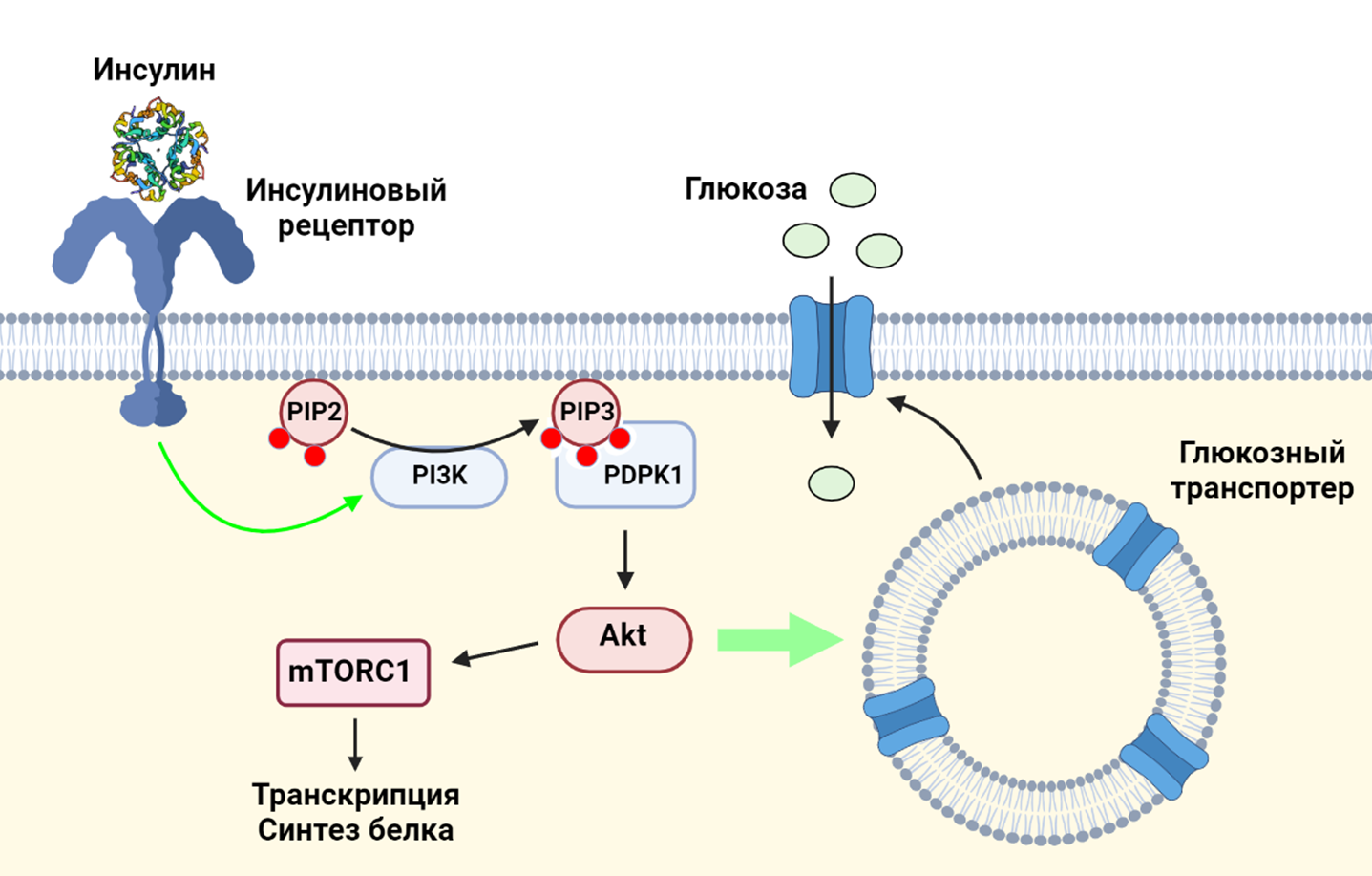
Как известно, повышение уровня глюкозы в крови вызывает секрецию гормона инсулина бета-клетками поджелудочной железы. Инсулин, в свою очередь, взаимодействует с инсулиновыми рецепторами на поверхностях клеток. Взаимодействие инсулина с его рецептором приводит к активации фосфатидилинозитол-3-киназы (PI3K) — ключевого фермента PI3K/AKT/mTOR сигнального пути: работа PI3K делает возможным фосфорилирование протеинкиназы Akt, что приводит, с одной стороны, к транслокации глюкозных транспортеров на клеточную мембрану (и, как следствие, к увеличению поглощения глюкозы клетками), а с другой стороны — к активации протеинкиназы mTORС1, важнейшего регулятора клеточного метаболизма и роста [1].
Рисунок 4. Взаимодействие инсулина и его рецептора приводит к активации фосфатидилинозитол-3-киназы (PI3K), которая фосфорилирует фосфатидилинозитолдифосфат (PIP2). Образовавшийся фосфатидилинозитолтрифосфат (PIP3) нужен для того, чтобы фосфоинозитид-зависимая киназа-1 (PDPK1) активировала протеинкиназу Akt. Akt необходима для стыковки внутриклеточных везикул, несущих глюкозный транспортер, с клеточной мембраной. Также Akt активирует mTORC1.
коллаж авторов статьи. Создан с помощью BioRender.com
Сигнальный путь PI3K/AKT/mTOR играет важную роль в раковых клетках, которые могут активно экспрессировать рецепторы к инсулину и, получая сигналы при их стимуляции, увеличивать темпы роста и размножения.
Снижение уровня глюкозы в крови пациентов рассматривается как одна из потенциальных диетических стратегий при терапии рака. Такой подход ограничит доступность глюкозы для раковых клеток и понизит секрецию инсулина бета-клетками поджелудочной железы. Как можно понизить содержание глюкозы в крови пациентов? Конечно, уменьшение калорийности пищи приведет к снижению уровня глюкозы в крови, но такой способ не может быть оптимальным, так как поставит под угрозу общее состояние пациента. Куда более выгодной стратегией может стать кетогенная диета, которая предполагает ограничение потребления углеводов с одновременным увеличением доли жиров в рационе. Действительно, есть данные доклинических исследований и немногочисленные клинические испытания, которые говорят, что такая диета может способствовать благоприятному исходу болезни — например, при глиобластоме [7]. Однако важно отметить, что некоторые типы опухолей, наоборот, зависят от жирных кислот, а значит, диета, богатая жирами, может опосредовать проканцерогенный эффект [1], о чем мы поговорим чуть далее.
А что насчет других углеводов?
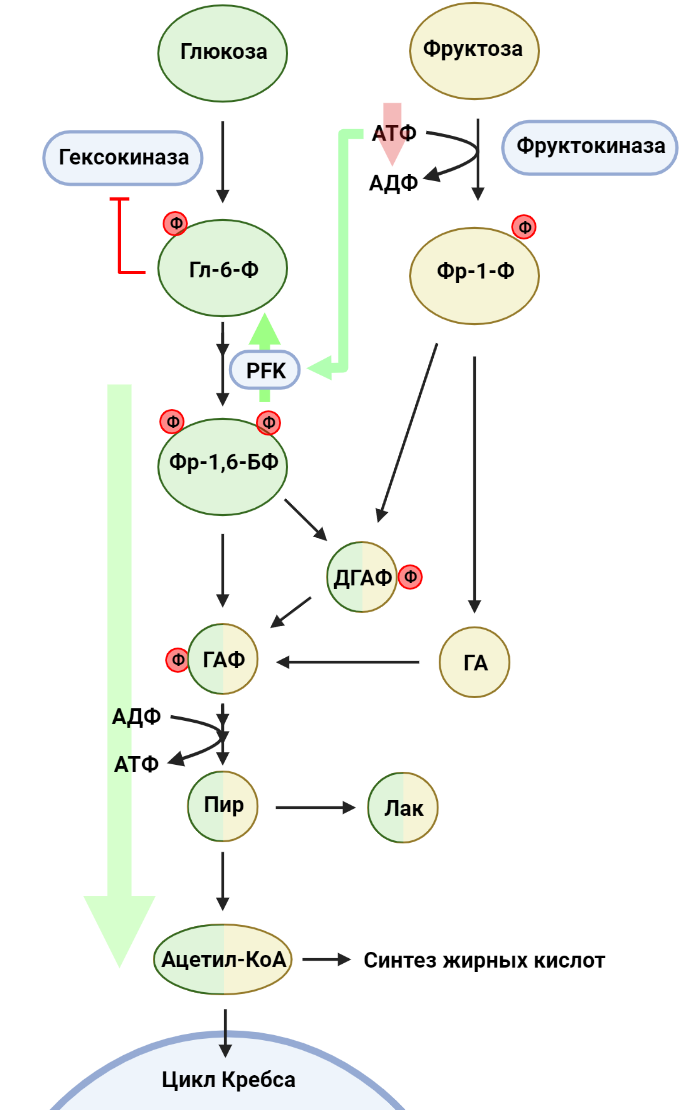
Рисунок 5. Метаболизм фруктозы. В первой стадии гликолиза глюкоза фосфорилируется до глюкозо-6-фосфата (Гл-6-Ф). Параллельно фруктоза фосфорилируется до фруктозо-1-фосфата (Фр-1-Ф). Фруктоза-1,6-бисфосфат (Фр-1,6-БФ), продукт фосфофруктокиназы (PFK), распадается на глицеральдегидфосфат (ГАФ) и дигидроксиацетонфосфат (ДГАФ), а Фр-1,6-БФ расщепляется на ДГАФ и глицеральдегид (ГА). ДГАФ и ГА переходят в ГАФ, который в оставшихся реакциях гликолиза превращается в пируват (ПИР). ПИР может восстановиться до лактата (ЛАК) или подвергаться превращению в ацетил-КоА, соединение, использующееся в многих биохимических процессах.
коллаж авторов статьи. Создан с помощью BioRender.com
Помимо глюкозы, в наш ежедневный рацион входит множество других углеводов. Например, фруктоза, один из наиболее распространенных в природе сахаров, встречается в пище как в свободном виде, так и в составе олигосахаридов, например, сахарозы. Эпидемиологи связывают рост потребления сахаросодержащих напитков с увеличением частоты заболеваемости раком [8]. Более того, оказывается, что даже умеренное потребление фруктозы (эквивалентное одной банке газировки в день) оказывает негативное воздействие и может способствовать росту опухоли, что было отмечено в экспериментах с мышами на примере колоректального рака [9]. Глюкоза эффективно поглощается эпителиальными клетками тонкого кишечника за счет специальных белков, осуществляющих совместный транспорт глюкозы и ионов натрия. При этом транспорт фруктозы опосредуется пассивным транспортером GLUT5 и потому менее эффективен. В результате значительная часть потребляемой фруктозы проходит тонкую кишку и попадает в толстый кишечник. В случае колоректального рака фруктоза становится одним из потенциальных питательных веществ для опухолевых клеток: действительно, раковые клетки в кишечнике активно экспрессируют как GLUT5, так и ферменты, метаболизирующие фруктозу. Глюкоза и фруктоза похожи между собой с точки зрения строения молекул, однако с точки зрения их метаболизма они немного отличаются (рис. 5). Если говорить про глюкозу, то первая стадия гликолиза представляет собой фосфорилирование глюкозы с затратой АТФ и образованием глюкозо-6-фосфата, причем активность гексокиназ (ферментов, осуществляющих эту реакцию) зависит от концентрации глюкозо-6-фосфата в среде: чем больше продукта для фермента, тем менее активно он работает. Это явление — пример отрицательной обратной связи, важного аспекта регуляции активности метаболических путей. Фруктоза же в первую очередь фосфорилируется фруктокиназой до фруктозо-1-фосфата (Фр-1-Ф), также с затратой АТФ, однако в данном случае активность фермента не зависит от концентрации продукта. Это значит, что киназа будет фосфорилировать всю доступную фруктозу, вне зависимости от того, сколько Фр-1-Ф уже было сделано. Следовательно, при повышенной концентрации фруктозы клетка будет тратить много АТФ на ее фосфорилирование. В ответ на понижение уровня АТФ активируется фермент глизолиза фосфофруктокиназа (PFK), а также, помимо этого, продукты расщепления Фр-1-Ф в конечном счете попадают в реакции гликолиза. Таким образом, фруктоза усиливает гликолиз, что на руку раковым клеткам: в случае колоректального рака активация гликолиза способствует индукции синтеза жирных кислот, необходимых для роста опухоли [9].
Надо отметить, что фруктоза, хоть и способствует росту опухолей в случае колоректального рака, для роста и выживания нормальных клеток вовсе не обязательна, так что фармакологическое подавление переносчиков фруктозы и ферментов, участвующих в ее метаболизме (например, фруктокиназы) может препятствовать прогрессии колоректального рака. И конечно же, исключение фруктозы из рациона пациента также может оказывать благотворный эффект на течение болезни. Однако клинических данных, подтверждающих это, пока недостаточно [1].
Еще один любопытный пример связан с маннозой, моносахаридом, который также часто встречается в рационе как в свободном виде, так и в составе полисахаридов. Манноза поглощается теми же транспортерами, что и глюкоза, но затем накапливается в клетках в виде маннозо-6-фосфата и дальше почти не метаболизируется. В то же время, маннозо-6-фосфат ингибирует некоторые ферменты гликолиза (гексокиназу и глюкозоизомеразу), а также глюкозо-6-фосфатдегидрогеназу — первый фермент пентозофосфатного пути, альтернативного способа окисления глюкозы. Таким образом, накопление маннозо-6-фосфат влечет за собой подавление метаболизма глюкозы, что негативно сказывается на жизнеспособности раковых клеток. Однако не все опухоли чувствительны к маннозе. Дело в том, что в клетках есть фермент маннозо-6-фосфат—изомераза (PMI), который катализирует превращение маннозо-6-фосфата в фруктозо-6-фосфат, метаболит гликолиза. Казалось бы, накопление маннозо-6-фосфата перестает быть проблемой для клетки, но дело в том, что разные опухоли имеют разную активность PMI, и если в каких-то опухолевых клетках его активность понижена, то манноза будет подавлять рост опухоли. Оказалось, что колоректальные опухоли обычно имеют очень низкие уровни PMI, и действительно, на мышиной модели колоректального рака было показано, что биодобавки, содержащие маннозу, значительно подавляют рост опухолей и не оказывают отрицательный эффект на здоровье и вес мышей [10]. Возможно, применение маннозы в виде добавок к пище будет повышать эффективность терапии колоректального рака и у людей, но клинических исследований на этот счет еще не проводилось [1].
Жирные кислоты
Жирные кислоты являются важнейшим источником энергии в клетке, особенно для «энергозатратных» тканей вроде скелетной и сердечной мышечных тканей. При окислении жирных кислот (которое в основном происходит в ходе процесса β-окисления) образуются NADH и FADH2, а также ацетил-КоА — вещества, необходимые для синтеза АТФ при окислительном фосфорилировании. Более того, если сравнить между собой жирные кислоты и углеводы, то окажется, что по отношению к своей сухой массе жирные кислоты обеспечивают больше АТФ, чем углеводы, а значит, они лучше подходят на роль запасного питательного вещества (жирные кислоты запасаются в форме триглицеридов в жировой ткани). Разумеется, не могло бы случиться такого, чтобы не нашлось опухолевых клеток, активно использующих жирные кислоты как источник энергии и восстановительных эквивалентов. Действительно, описаны процессы, когда раковая клетка переходит на β-окисление, а также отдельные опухоли, для которых основной источник энергии — это жиры, а не углеводы [1], [11].
Так, было показано, что окисление жирных кислот критично для клеток рака груди при их откреплении от матрикса. Протоки молочных желез выстланы слоем эпителиальных клеток, которые дают начало опухоли. На ранних стадиях развития рака молочной железы опухолевые клетки открепляются от матрикса, покидают свои ниши, начинают пролиферировать в просветах полых железистых структур, заполняя их. Эпителиальные клетки имеют на своей поверхности рецепторы эпидермального фактора роста (epidermal growth factor receptor, EGFR). При стимуляции EGFR, помимо прочего, происходит активация сигнального пути PI3K/AKT/mTOR, что приводит к росту, пролиферации, а также способствует поглощению глюкозы и подавлению апоптоза. Для эпителиальной клетки очень важен контакт с внеклеточным матриксом. Если клетка по какой-либо причине теряет контакт с матриксом, то экспрессия EGFR падает, и, как одно из следствий, клетка начинает испытывать дефицит в глюкозе. В норме эта череда событий непременно приведет к нехватке АТФ, окислительному стрессу, и наконец — к аноикису— гибели клетки, происходящей в ответ на открепление от матрикса. Но опухолевая клетка не так проста и активно пытается спастись от апоптоза. Активность ряда онкогенов в данном случае способствует активации окисления жирных кислот, что обеспечивает клетку энергией и предотвращает гибель [12].
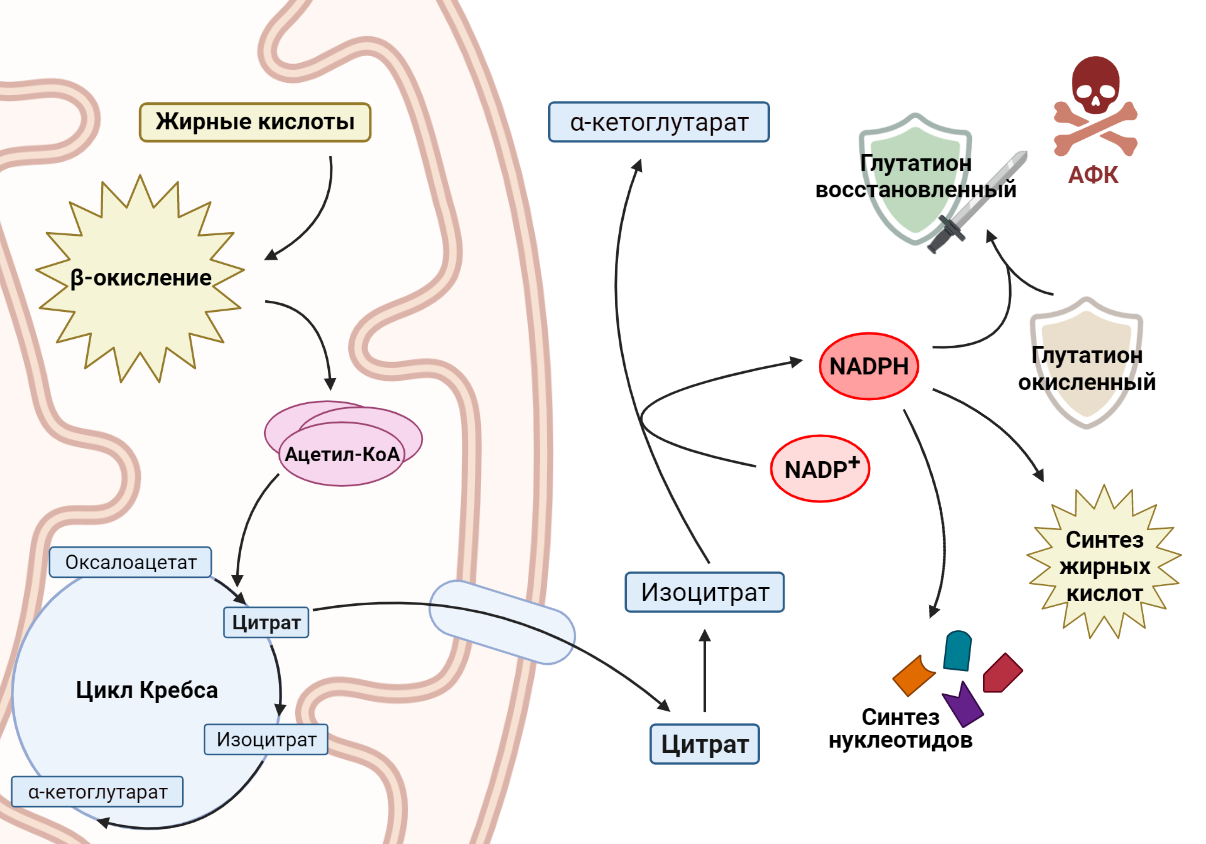
Другой важный пример роли жирных кислот в раковых клетках связан с никотинамидадениндинуклеотидфосфатом (NADPH) — веществом, которое выполняет две основные функции. С одной стороны, он участвует в защите клетки от токсичных активных форм кислорода (АФК), обеспечивая регенерацию антиоксиданта глутатиона (GSH), что особенно важно для выживания раковых клеток в условиях метаболического стресса. С другой стороны, NADPH необходим для синтеза жирных кислот и нуклеотидов, необходимых для поддержания роста и пролиферации клеток, что является неотъемлемой частью биологии опухолевой клетки. Зачастую рост раковой клетки ограничен уровнями NADPH, следовательно, изменения в метаболизме раковой клетки должны учитывать этот важный аспект. Как связаны между собой окисление жирных кислот и производство NADPH? Основным продуктом окисления жиров является ацетил-КоА, который вступает в цикл Кребса и превращается в цитрат. Цитрат может остаться воволеченным в цикл Кребса, а может покинуть митохондрию и выйти в цитоплазму. Там он превратится в изоцитрат, который является субстратом для NADP-зависимой изоцитратдегидрогеназы [13]. Этот фермент окисляет изоцитрат, при этом происходит перенос водорода на NADP+ и образуется NADPH, необходимый раковым клеткам. Например, в клетках глиомы, в которых ингибируется окисление жирных кислот, значительно понижается уровень NADPH, что приводит к накоплению АФК и, как следствие, клеточной гибели [14].
Рисунок 6. Ацетил-КоА, продукт окисления жирных кислот, поступает в цикл Кребса. В то же время цитрат, промежуточное соединение цикла Кребса, покидает митохондрию, где превращается в изоцитрат. При окислении изоцитрата происходит перенос водорода на NADP+, образуется NADPH, необходимый клеткам для множества процессов.
коллаж авторов статьи. Создан с помощью BioRender.com
Из данных примеров мы видим, что в некоторых случаях жирные кислоты способствуют выживанию и метастазированию опухолевых клеток. Это значит, что для отдельных пациентов диета с низким содержанием жиров может оказаться полезной. В то же время, кетогенная диета, которую мы обсуждали в главе про глюкозу, может вызывать непредвиденные проканцерогенные эффекты и способствовать росту опухоли. Таким образом, режим питания пациентов должен подбираться индивидуально с учетом стадии опухоли, ее локализации и особенностей метаболизма.
Аминокислоты
Как известно, белки принимают участие в большинстве клеточных процессов: поддерживают форму клетки, обеспечивают ее подвижность, контролируют работу генов, регулируют метаболические процессы и многое-многое другое. Аминокислоты являются строительными мономерными блоками для белков. Удивительно, что при огромном разнообразии белков, все они построены из довольно ограниченного набора аминокислот (рис. 7).
Рисунок 7. 20 классических аминокислот.
С пищей в организм попадают белки, после чего в желудочно-кишечном тракте они деградируют до отдельных аминокислот. Смесь аминокислот всасывается в тонком кишечнике, поступает в кровь и разносится к каждой клетке организма. В клетках аминокислоты используются уже для синтеза собственных белков, которые необходимы для нормального функционирования организма. Важно отметить, что некоторые из аминокислот клетки нашего организма умеют синтезировать сами (так называемые заменимые аминокислоты), а некоторые непременно должны поступать с пищей (незаменимые аминокислоты). Итак, аминокислоты, которые попали в клетку, могут войти в состав белков, но для нас более интересен тот факт, что отдельные аминокислоты могут выполнять специальные метаболические функции. Далее мы будем рассматривать роль конкретных аминокислот в метаболизме раковых клеток, а также возможные диетические стратегии для пациентов с онкологическими заболеваниями, основанные на ограничении или биодобавках данных аминокислот в рационе.
Метионин
Метионин относится к незаменимым аминокислотам для клеток человека. При этом раковые клетки для своего роста требуют бóльшие количества метионина по сравнению с нормальными клетками. Дело в том, что метионин выполняет ряд регуляторных функций. В клетке есть специальные сенсоры, которые в ответ на высокий уровень метионина (а точнее, его производного — S-аденозилметионина) способны активировать протеинкиназу mTORC1. Эта протеинкиназа крайне важна для раковых клеток: она активирует процесс синтеза белка и, как следствие, ускоряет рост и деление клетки [15]. Кроме этого, S-аденозилметионин является главным донором метильной группы в клетке, то есть обеспечивает метилирование. Метилирование ДНК и гистонов (белков, связанных с ДНК) позволяет «включать» и «выключать» определенные гены. Изменения статуса метилирования гистонов и ДНК регулируют экспрессию генов и вносят свой вклад в рост и развитие опухоли [16]. Начиная с 1990 года проводятся исследования на животных, которые демонстрируют, что ограничение потребления метионина улучшает исход лечения опухолей [1], [17]. Совсем недавно было проведено первое клиническое исследование, которое показало, что снижение количества метионина в рационе пациентов позволяет замедлить прогрессирование опухоли [18]. Таким образом, диетическое ограничение метионина у людей, страдающих онкологическими заболеваниями, является весьма многообещающим подходом [1]. Важно уточнить, что диетическое ограничение тех или иных аминокислот можно осуществить только за счет «искусственных» диет, при которых основным источником белковой пищи являются протеиновые напитки/батончики без содержания определенных аминокислот. Именно такой режим питания соблюдали пациенты, принявшие участие в клиническом испытании диеты с низким содержанием метионина: 75% белковой пищи представляли из себя протеиновые напитки без метионина [18].
Серин
Аминокислота серин принимает участие во множестве метаболических процессов: в синтезе нуклеотидов и липидов; она может превращаться в пируват и поступать в цикл Кребса, и так далее. Серин относится к заменимым аминокислотам и может синтезироваться в нормальных клетках из глюкозы и глицина (самой простой аминокислоты). Для раковых клеток, которые активно используют гликолиз и, соответственно, остро нуждаются в глюкозе, синтез серина из глюкозы непременно обернется потерями в количестве АТФ и скорости размножения. Именно поэтому можно сказать, что для опухолевых клеток серин является незаменимой аминокислотой, то есть обязательно должен поступать извне. Путь синтеза серина из глицина для раковых клеток тоже крайне нежелателен, так как глицин принимает непосредственное участие в синтезе нуклеотидов, а значит, превращение глицина в серин опять же ставит под угрозу скорость деления раковых клеток. Таким образом, ограничение потребление серина действительно может помочь в терапии опухолей. Эффективность такой диеты уже была показана в экспериментах на мышах, но клинических исследований пока не проводилось [1].
Аргинин
В нормальных клетках аргинин способен образовываться de novo, то есть является заменимой аминокислотой. В опухолевых клетках меланомы, гепатоцеллюлярной карциномы и рака простаты синтез аргинина сильно снижен. Это связано с низким уровнем фермента аргининосукцинатсинтетазы, участвующем в образовании аргиинина. Выходит, что некоторые раковые опухоли требуют поступление аргинина извне (для клеток этих опухолей аргинин — незаменимая аминокислота). «Аргининовая зависимость» опухолей может быть использована для терапии, причем как в фармакологических подходах, так и в простом диетическом ограничении аргинина. Про фармакологическое снижение аргинина в раковых клетках уже кое-что известно из научных работ: так, например, препараты, снижающие уровень аргинина в плазме крови пациентов, оказались эффективными при лечении гепатоцеллюлярной карциномы и меланомы [19].
Однако аргинин может негативно сказываться на противоопухолевом иммунитете. Важнейшими клетками, участвующими в борьбе с опухолью, являются T-лимфоциты. Аргинин активно поглощается активированными T-клетками, затем метаболизируется, что приводит к увеличению выживаемости клеток и усилению противоопухолевого Т-клеточного ответа. В мышиной модели рака кожи увеличение количества потребляемого с пищей аргинина привело к уменьшению размера опухолей, способствовало выживанию мышей [20].
Не менее важную роль в противоопухолевом иммунитете играют NK-клетки (Natural killer cells, натуральные киллеры) — иммунные клетки, способные уничтожать опухолевые клетки. Исследования показали, что потребление аргинина с пищей увеличивает количество и активность NK-клеток [21], и, наоборот, дефицит аргинина угнетает работу и жизнеспособность натуральных киллеров [22], что может негативно сказаться на борьбе с опухолью.
Таким образом, аргинин необходим как некоторым опухолям для роста, так и иммунным клеткам, сражающимся с опухолью. По-видимому, только масштабные клинические испытания помогут понять, в каких случаях стоит исключать или, наоборот, увеличивать содержание аргинина в пище для достижения максимального эффекта терапии.
Цистин и цистеин
Одна из важнейших функций аминокислоты цистеина в клетке — защита от активных форм кислорода (например, перекиси водорода), которые повреждают ДНК, липиды и белки, вызывая в клетке окислительный стресс. Раковые клетки, по сравнению с нормальными, испытывают сильный окислительный стресс и требуют большого количества цистеина. Действительно, для некоторых опухолевых клеток снижение уровня цистеина губительно: клетки «сгорают» из-за накопленных активных форм кислорода. Цистеин образуется из неклассической аминокислоты цистина, которая поступает в клетку из плазмы крови [1]. Препараты, снижающие уровень цистина в плазме крови, тормозят рост опухолей с мутантным рецептором эпидермального фактора роста (например, немелкоклеточного рака легких) у мышей [23]. Теоретически, достичь снижения уровня цистина в плазме крови пациентов можно при помощи корректировки диеты, без применения препаратов, но такой подход пока не исследован.
Гистидин
При деградации гистидина в клетке тратится тетрагидрофолат — кофактор, который необходим для синтеза нуклеотидов, а значит, определяет скорость деления раковых клеток. Чем больше в раковую клетку поступает гистидина, тем больше тетрагидрофолата тратится на распад гистидина и тем медленнее клетка делится. Применение гистидина вместе с пищей может помочь в терапии некоторых видов опухолей. В частности, такой диетический подход может стать особенно эффективным при лечении рака химиотерапевтическим агентом — метотрексатом (часто применяется для лечения злокачественных заболеваний крови). Метотрексат нарушает синтез тетрагидрофолата, что приводит к остановке синтеза нуклеотидов и к гибели раковых клеток. Оказалось, что эффективность лечения лейкемии метотрексатом заметно увеличивается при добавлении к пище аминокислоты гистидина — это было показано на мышиной модели [24].
Биодобавки фолиевой кислоты
В заключение мы хотим уделить внимание витаминам. Витамины необходимы для протекания многих биохимических реакций и должны поступать в организм с пищей. Существует распространенное заблуждение о том, что прием витаминных биодобавок может послужить защитой от рака и других заболеваний. На самом деле, витамины должны поступать исключительно с пищей, а дополнительный прием витаминов здоровым людям в основном не рекомендован (за некоторыми редкими исключениями). Регулярный прием биодобавок может оказаться не только неэффективными, но и вредным, особенно людям, страдающим онкологическими заболеваниями. Давайте рассмотрим пример того, как дополнительный прием витаминов способствует росту опухоли.
Фолиевая кислота (фолат, витамин B9) является необходимым веществом для синтеза нуклеотидов. Опухолевые клетки быстро делятся и нуждаются в больших количествах нуклеотидов для синтеза ДНК, поэтому активно потребляют фолат. Еще в 1948 году стало известно, что биодобавки фолиевой кислоты способствуют росту некоторых видов опухолей [25]. На сегодняшний день метаболизм фолиевой кислоты является фармакологической мишенью для терапии рака: упоминавшийся ранее химиотерапевтический препарат метотрексат нарушает метаболизм фолата и ингибирует пути синтеза нуклеотидов. Надо подчеркнуть, что антифолиевая терапия рака пока что является сугубо фармакологической и не предполагает корректировки диеты [1].
Однако потенциальные негативные эффекты фолата в опухолевой прогрессии на этом не заканчиваются. Ряд исследований показал, что присутствие в крови неметаболизированной фолиевой кислоты, связанное с ее избыточным потреблением, влекло за собой снижение количества и активности NK-клеток [26-28]. Упоминавшиеся ранее NK-клетки — это иммунные клетки, одна из основных функций которых состоит в защите организма от раковых клеток. Следовательно, снижение числа и подавление активности NK-клеток может повлечь за собой повышенный риск образования и прогрессии рака, хотя конкретных исследований о влиянии высоких доз фолата на противоопухолевый иммунитет не проводилось.
Таким образом, витамины необходимы для поддержания функций организма, однако чрезмерное потребление некоторых из них может привести к негативным последствиям, в том числе и к прогрессии опухоли, как в случае с витамином B9. Возможно, диета с низким содержанием фолата будет полезной для некоторых пациентов.
Заключение
Мы постарались кратко охарактеризовать некоторые особенности метаболизма опухолевых клеток и роль питательных веществ в прогрессии рака. В заключение мы хотели бы еще раз обратить внимание на то, что не существует какой-либо универсальной диеты для людей, страдающих онкологическими заболеваниями. Это связано с тем, что опухоли сильно различаются по своему метаболизму. Перечисленные диетические подходы пока что не могут использоваться повсеместно, так как перед внедрением любого из них для каждого типа рака, его локализации и стадии заболевания должны быть проведены масштабные клинические испытания, подтверждающие безопасность и эффективность нового метода лечения. Однако, ввиду многообещающих результатов исследований, модификации диеты являются перспективным подходом к лечению рака. Мы уверены, что в скором времени контроль состава диеты пациентов станет важной частью терапии онкологических заболеваний и поможет спасти многие жизни. А пока что давайте просто стараться питаться правильно и вести здоровый образ жизни. Будьте здоровы!
- Naama Kanarek, Boryana Petrova, David M. Sabatini. (2020). Dietary modifications for enhanced cancer therapy. Nature. 579, 507-517;
- Путь клетки «из греков в варяги». Малигнизация: причины и следствия;
- Douglas Hanahan, Robert A Weinberg. (2000). The Hallmarks of Cancer. Cell. 100, 57-70;
- Douglas Hanahan, Robert A. Weinberg. (2011). Hallmarks of Cancer: The Next Generation. Cell. 144, 646-674;
- Метаболизм клетки;
- Вослед Варбургу — последние достижения в изучении биоэнергетики рака;
- Colin E. Champ, Joshua D. Palmer, Jeff S. Volek, Maria Werner-Wasik, David W. Andrews, et. al.. (2014). Targeting metabolism with a ketogenic diet during the treatment of glioblastoma multiforme. J Neurooncol. 117, 125-131;
- Julie K. Bassett, Roger L. Milne, Dallas R. English, Graham G. Giles, Allison M. Hodge. (2020). Consumption of sugar‐sweetened and artificially sweetened soft drinks and risk of cancers not related to obesity. Int. J. Cancer. 146, 3329-3334;
- Marcus D. Goncalves, Changyuan Lu, Jordan Tutnauer, Travis E. Hartman, Seo-Kyoung Hwang, et. al.. (2019). High-fructose corn syrup enhances intestinal tumor growth in mice. Science. 363, 1345-1349;
- Pablo Sierra Gonzalez, James O’Prey, Simone Cardaci, Valentin J. A. Barthet, Jun-ichi Sakamaki, et. al.. (2018). Mannose impairs tumour growth and enhances chemotherapy. Nature. 563, 719-723;
- Arkaitz Carracedo, Lewis C. Cantley, Pier Paolo Pandolfi. (2013). Cancer metabolism: fatty acid oxidation in the limelight. Nat Rev Cancer. 13, 227-232;
- Zachary T. Schafer, Alexandra R. Grassian, Loling Song, Zhenyang Jiang, Zachary Gerhart-Hines, et. al.. (2009). Antioxidant and oncogene rescue of metabolic defects caused by loss of matrix attachment. Nature. 461, 109-113;
- Alessandra Castegna, Pasquale Scarcia, Gennaro Agrimi, Luigi Palmieri, Hanspeter Rottensteiner, et. al.. (2010). Identification and Functional Characterization of a Novel Mitochondrial Carrier for Citrate and Oxoglutarate in Saccharomyces cerevisiae. Journal of Biological Chemistry. 285, 17359-17370;
- Lisa S. Pike, Amy L. Smift, Nicole J. Croteau, David A. Ferrick, Min Wu. (2011). Inhibition of fatty acid oxidation by etomoxir impairs NADPH production and increases reactive oxygen species resulting in ATP depletion and cell death in human glioblastoma cells. Biochimica et Biophysica Acta (BBA) — Bioenergetics. 1807, 726-734;
- Xin Gu, Jose M. Orozco, Robert A. Saxton, Kendall J. Condon, Grace Y. Liu, et. al.. (2017). SAMTOR is an
S
-adenosylmethionine sensor for the mTORC1 pathway. Science. 358, 813-818; - Samantha J. Mentch, Mahya Mehrmohamadi, Lei Huang, Xiaojing Liu, Diwakar Gupta, et. al.. (2015). Histone Methylation Dynamics and Gene Regulation Occur through the Sensing of One-Carbon Metabolism. Cell Metabolism. 22, 861-873;
- Raghu Sinha, Timothy K. Cooper, Connie J. Rogers, Indu Sinha, William J. Turbitt, et. al.. (2014). Dietary methionine restriction inhibits prostatic intraepithelial neoplasia in TRAMP mice. Prostate. 74, 1663-1673;
- Xia Gao, Sydney M. Sanderson, Ziwei Dai, Michael A. Reid, Daniel E. Cooper, et. al.. (2019). Dietary methionine influences therapy in mouse cancer models and alters human metabolism. Nature. 572, 397-401;
- Francesco Izzo, Paolo Marra, Gerardo Beneduce, Giuseppe Castello, Paolo Vallone, et. al.. (2004). Pegylated Arginine Deiminase Treatment of Patients With Unresectable Hepatocellular Carcinoma: Results From Phase I/II Studies. JCO. 22, 1815-1822;
- Roger Geiger, Jan C. Rieckmann, Tobias Wolf, Camilla Basso, Yuehan Feng, et. al.. (2016). L-Arginine Modulates T Cell Metabolism and Enhances Survival and Anti-tumor Activity. Cell. 167, 829-842.e13;
- K.G.M. Park, P.D. Hayes, O. Eremin, H. Sewell, K.G.M. Park, P.J. Garlick. (1991). Stimulation of lymphocyte natural cytotoxicity by L-arginine. The Lancet. 337, 645-646;
- Bruno Lamas, Juliette Vergnaud-Gauduchon, Nicolas Goncalves-Mendes, Olivier Perche, Adrien Rossary, et. al.. (2012). Altered functions of natural killer cells in response to L-Arginine availability. Cellular Immunology. 280, 182-190;
- Ioannis Poursaitidis, Xiaomeng Wang, Thomas Crighton, Christiaan Labuschagne, David Mason, et. al.. (2017). Oncogene-Selective Sensitivity to Synchronous Cell Death following Modulation of the Amino Acid Nutrient Cystine. Cell Reports. 18, 2547-2556;
- Naama Kanarek, Heather R. Keys, Jason R. Cantor, Caroline A. Lewis, Sze Ham Chan, et. al.. (2018). Histidine catabolism is a major determinant of methotrexate sensitivity. Nature. 559, 632-636;
- Sidney Farber, Louis K. Diamond, Robert D. Mercer, Robert F. Sylvester, James A. Wolff. (1948). Temporary Remissions in Acute Leukemia in Children Produced by Folic Acid Antagonist, 4-Aminopteroyl-Glutamic Acid (Aminopterin). N Engl J Med. 238, 787-793;
- Hathairat Sawaengsri, Junpeng Wang, Christina Reginaldo, Josiane Steluti, Dayong Wu, et. al.. (2016). High folic acid intake reduces natural killer cell cytotoxicity in aged mice. The Journal of Nutritional Biochemistry. 30, 102-107;
- Aron M. Troen, Breeana Mitchell, Bess Sorensen, Mark H. Wener, Abbey Johnston, et. al.. (2006). Unmetabolized Folic Acid in Plasma Is Associated with Reduced Natural Killer Cell Cytotoxicity among Postmenopausal Women. The Journal of Nutrition. 136, 189-194;
- Clovis Paniz, Juliano Felix Bertinato, Maylla Rodrigues Lucena, Eduardo De Carli, Patrícia Mendonça da Silva Amorim, et. al.. (2017). A Daily Dose of 5 mg Folic Acid for 90 Days Is Associated with Increased Serum Unmetabolized Folic Acid and Reduced Natural Killer Cell Cytotoxicity in Healthy Brazilian Adults. The Journal of Nutrition. 147, 1677-1685.

Дихлорацетат натрия представляет собой натриевую соль дихлоруксусной кислоты. Это кристаллический порошок белого цвета, растворимый в воде и имеющий множество применений.
Дихлорацетат натрия мы производим и продаём в различных формах и упаковках. Вы можете приобрести капсулы, порошок и другие соли дихлоруксусной кислоты.

Все продукты, которые мы предлагаем, производятся нами в нашей собственной лаборатории. Мы находимся в ЕС, имеем строгий контроль качества и обеспечиваем продукцию наивысшего качества.
Мы предоставляем бесплатную и быструю доставку по всему миру. Для тех, кто в этом нуждается, мы включили возможность доставки DCA к Вашей двери за один рабочий день.
Мифы и правда о химиотерапии
14.03.2018
Правда ли, что химиотерапия «устарела»? Потому что больше вредит, чем помогает? А в прогрессивных клиниках рак давно лечат без «химии»? Комментирует резидент Высшей школы онкологии НМИЦ онкологии им. Н.Н. Петрова Катерина Коробейникова.
Миф 1: химиотерапия малоэффективна
В поддержку этого мнения ссылаются на цитируемое в интернете исследование профессора Гарвардского университета Джона Кэрнса, якобы опубликованное в «Scientific American» и в «Журнале клинической онкологии» в 2004 году, о том, что на самом деле химиотерапия помогает лишь 2,3-5% случаев (комментарий об источнике см. в конце нашего материала). Зато именно «химия» вызывает «сопротивление опухоли, которое выражается в метастазах».
Чтобы говорить об эффективности химиотерапии «при раке», надо уточнить, что понятие «онкология» включает в себя множество разных заболеваний.
Есть нейробластома у детей или хорионкарцинома матки. Их можно полностью излечить именно с помощью химиотерапии. Излечение означает, что у человека нет рецидивов в течении 5 лет.
Есть опухоли, высокочувствительные к химиотерапии – саркома Юинга, рак предстательной железы, рак мочевого пузыря. С помощью химиотерапии они поддаются контролю — возможно излечение, как минимум, можно добиться длительной ремиссии.
Есть промежуточная группа – рак желудка, рак почки, остеогенная саркома, при которых уменьшение опухоли от химиотерапии происходит в 75-50% случаев.
А есть рак печени, поджелудочной железы. Эти опухоли малочувительны к лекарственной терапии, но к ним сейчас применяют другие методы лечения – оперируют или облучают. И еще есть рак крови – понятие, которым пациенты называют острые лейкозы и лимфомы. Они вообще развиваются по другим законам.
Даже при запущенной стадии рака с метастазами, прогноз очень сильно зависит от того, какой у вас конкретно подтип опухоли. Например, гормоночувствительный подтип рака молочной железы даже с метастазами контролю поддается очень хорошо. Поэтому делать какие-то выводы о «химиотерапии при раке в целом» — некорректно.
В последнее время подход к лечению онкологических пациентов всё больше индивидуализируется. Совсем давно говорили: «У вас рак – какой ужас!», — потом: «У вас рак определенного органа – это плохо». А сейчас врач внимательно посмотрит на «паспорт» опухоли из гистохимических и иммунногенетических маркеров и характеристики опухоли, которую пациенту выдали при гистологическом исследовании (такое изучение опухоли теперь входит в стандарты обследования) и в зависимости от этого выберет тактику лечения.
Миф 2: срок жизни без химиотерапии длиннее, чем с химиотерапией
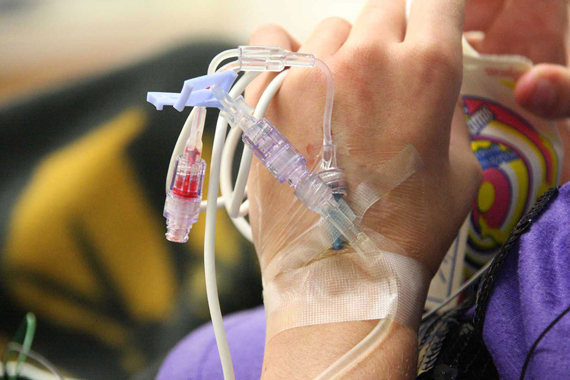
Источник: time.com
В интернете рассказывается, что это доказали некие доктор медицинских наук Алан Левин и профессор Шарль Матье. Якобы на самом деле большинство пациентов, получающих химиотерапию, умирает именно от химии, а не от рака.
Я не нашла подтверждающей информации, что врачи с такими именами (они есть, но они не онкологи) высказали такое мнение.
Сегодня Россия, как Европа и США, переходит к стандартам доказательной медицины. В этой системе все доказательства оцениваются по определенной шкале. И меньше всего доверия — аргументам из серии «профессор Иванов (или профессор Смит) сказал». Более серьезный уровень аргументов – метаанализы, то есть объединение нескольких, уже проведенных маленьких исследований в одно, когда их результаты складывают и считают вместе.
Химиотерапия – это лечение. И, как у всякого лечения, у нее бывают побочные эффекты. Они бывают от любых лекарств, они бывают после хирургических операций. Сама химиотерапия тоже бывает разной в зависимости от цели. Предоперационную химиотерапию применяют до хирургической операции, чтобы максимально уменьшить размер опухоли и сделать хирургическое вмешательство максимально щадящим.
Цель постоперационной «химии» – убрать отдельные опухолевые клетки, которые еще могут циркулировать в организме.
А бывает химиотерапия паллиативная. Ее применяют, когда опухоль запущена, со множественными метастазами, и вылечить больного невозможно, но возможно затормозить дальнейшее прогрессирование и попытаться контролировать опухоль. В этом случае химиотерапия призвана подарить пациенту время, но, как правило, она сопровождает его до конца. И тогда может создаться впечатление, что пациент умер не от рака, а от «химии», хотя это не так.
Кроме того, при предоперационной или послеоперационной «химии» часто врачи наблюдают пациента не только в тот момент, когда он получает капельницы с препаратами, но и между курсами. Поэтому смертельные случаи от побочных эффектов редки.
Миф 3: химиотерапия непоправимо «сажает» печень, кровь, нервы
Источник: npr.org
Главный механизм действия химиопрепаратов – воздействие на механизм деления клетки. Клетки раковых опухолей очень быстро делятся, поэтому, воздействуя на деление клеток, мы останавливаем рост опухоли.
Но, помимо опухоли, в организме много других быстро делящихся клеток. Они есть во всех системах, которые активно обновляются, — в крови, в слизистых. Те химиопрепараты, которые воздействуют не выборочно, действуют и на эти клетки.
Основные осложнения химиотерапии:
— падение показателей крови
— поражения печени
— изъязвление слизистых и связанные с этим тошнота и понос
— выпадение и ломкость ногтей.Такой эффект объясняется тем, что цитостатическая химиотерапия действует не только на клетки опухоли, но на все быстроделящиеся клетки организма.Также у отдельных препаратов, которые оказывают на организм токсичное действие, бывают специфические осложнения. (Часть препаратов химиотерапии сделана на основе платины – это тяжелый металл).
Токсичные препараты химиотерапии могут вызвать ряд неврологических симптомов – головные боли, бессонницу или сонливость, тошноту, депрессию, спутанность сознания. Иногда возникает ощущение онемения конечностей, «мурашки». Эти симптомы проходят после прекращения действия препарата.
После химиотерапии у пациента ожидаемо падают показатели крови. Обычно пик падения приходится на седьмой-четырнадцатый день, потому что «химия» как раз подействовала на все клетки, которые были в периферической крови, а новые костный мозг выработать еще не успел. Падение происходит в зависимости от препарата, который применялся; одни из них действует преимущественно на тромбоциты, другие – на лейкоциты и нейтрофилы, третьи – на эритроциты и гемоглобин.
Химиотерапевтическое лечение проходит циклами. В зависимости от схемы химиотерапии, человек может получить, например, три дня капельниц химиотерапии, а следующие будут через 21 день. Этот промежуток называется «один цикл», он дается специально, чтобы организм пациента восстановился.
Перед каждым новым сеансом химиотерапии состояние пациента контролируют, смотрят, что было с ним в этот промежуток – делают клинический и биохимический анализ крови. Пока человек не восстановился, новый цикл лечения не начинается.
Источник: verywell.com
Если кроме снижения показателей крови до определенного уровня в промежуток между «химиями» ничего плохого не происходило — кровь восстановится сама. Чрезмерное падение тромбоцитов создает угрозу кровотечения, пациенту с такими показателями делают переливание тромбоцитарной массы. Если упали лейкоциты, которые отвечают за иммунитет, а человек заразился какой-то инфекцией, начался кашель, насморк, поднялась температура, — сразу назначают антибиотики, чтобы инфекция не распространилась. Обычно все эти процедуры делаются амбулаторно.
В перерывах между курсами химиотерапии пациента ведет онколог из районного онкодиспансера или поликлиники.
Перед самым первым циклом химиотерапии пациенту должны объяснить все возможные осложнения, рассказать про каждый препарат и его воздействие; и пациент может проконсультироваться со своим онкологом. Взвешивание рисков – отправная точка химиотерапии. Врач и пациент выбирают между повреждением, которое может принести химиотерапия, и преимуществом, которое может за ней последовать, — а именно – продление жизни порой на десятки лет.
Это – ключевой момент в принятии решения о необходимости применения химиопрепаратов: если мы понимаем, что при назначении того или иного лекарства процент успеха будет ниже, чем побочные эффекты, применять его просто нет смысла.
Миф 4: метастазы вырастают из «стволовых клеток рака», которые «химия» все равно не убивает
Источник: independent.co.uk
Причины возникновения метастазов у разных опухолей очень разные, как именно возникают метастазы, мы пока не знаем. Единственное, что мы знаем – «стволовых клеток рака» не бывает.
Опухоль в разных своих фрагментах и клетки метастазов – это очень неоднородное образование, там все клетки разные, они быстро делятся и быстро мутируют. Но в любом случае химиотерапия воздействует на все метастазы, где бы они ни были. Исключение – метастазы в головном мозге, куда проникают не все препараты. В этих случаях назначают особое лечение, либо особое введение препаратов – в спинномозговой канал. Бывают даже такие опухоли, у которых нельзя найти первичный очаг, — то есть, все, что мы видим в организме – это метастазы. Но лечение все равно назначают, и оно, во многих случаях, успешно проводится.
Миф 5: химиотерапия – метод, поддерживаемый фарминдустрией
Источник: independent.co.uk
Якобы давно есть препараты эффективнее, безвреднее и дешевле, но о них не говорят, боятся обвалить фармрынок.
Этот миф существует и по поводу других заболеваний, особенно это касается ВИЧ.
«Альтернативные препараты», которые принимают онкологические пациенты, в лучшем случае оказываются безобидными травками, от которых нет заметного действия. Увы, бывает хуже. Например, иногда пациенты начинают пить чудодейственные лекарства на основе смеси разных масел, а ведь масло – это очень тяжелый продукт для печени. В итоге пациент буквально вызывает у себя воспаление печени, и мы не можем начать цикл химиотерапии, потому что «химия» на печень тоже воздействует. И хорошо, если пациент хотя бы рассказывает нам, что он принимал, и мы можем понять, что так ухудшило ситуацию. Но лечение в итоге откладывается, эффективность его понижается. Кроме того, ряд новых лекарств для лечения, например, рака молочной железы, сейчас основан на растительных компонентах. Например, препарат трабектедин содержит специальным образом обработанную вытяжку из морских тюльпанов. Так что иногда препараты, которые пациенты принимают в ходе официального лечения, сами по себе – «природные».
Что до «гигантских денег фарминдустрии», часть препаратов химиотерапии, например, метотрексат, — это очень старые, давно разработанные лекарства, они стоят буквально копейки. Никаким «обвалом» или «подъемом отрасли» уменьшение или увеличение их производства не грозит.
В любом случае препараты для лечения онкологических заболеваний пациенты в России получают бесплатно.
Новые лекарства при раке
В последнее время в дополнение к цитостатикам – препаратам химиотерапии, которые действовали на весь организм целиком, появились новые препараты. Это – новое поколение препаратов химиотерапии – таргетные препараты и лекарства, основанные на принципиально ином принципе действия – иммунопрепараты.
Таргетный препарат – это лекарство, воздействующее не на весь организм, а адресно на клетки опухоли. При этом важно – молекулы конкретного таргетного препарата могут присоединиться к рецепторам клетки только определенного вида опухоли. Конкретный подтип опухоли определяется генетическим анализом во время молекулярно-генетического исследования.
Иммунопрепараты воздействуют на иммунную систему организма и иммунные механизмы опухоли в её ядре. В результате в организме активизируется собственный иммунитет, который начинает бороться с раковыми клетками.
Однако чтобы получить иммунопрепарат и таргетный препарат, у пациента должна быть опухоль с определенными характеристиками, эти препараты действуют не на все опухоли, а на их определенные мутации. Патолог и молекулярный генетик должен подробно прописать паспорт опухоли, и записать в назначении, что пациенту необходим именно этот препарат.
Сравнительно новый метод — гормонотерапия, но здесь круг показаний еще уже – опухоль должна быть гормоночувствительная. Считается, что на гормонотерапию лучше всего реагируют опухоли молочной железы и предстательной железы, хотя и здесь гормоны можно использовать только при определенных показаниях.
Кстати, с гормонотерапией связан еще один миф: чаще всего она используется в форме таблеток, и пациенты считают, что таблетки – это «не лечение» при такой болезни, как рак.
Можно ли обойтись без химиотерапии

Катерина Коробейникова. Фото: Ольга Молостова
В случае, если опухоль чувствительна и реагирует на иммунотерапию или гормонотерапию, лечить онкобольного без химиотерапии можно.
Без химиотерапии, одними гормонами иногда лечат, например, рак молочной железы. Хотя понятно, что гормоны тоже небезобидны, от них бывают свои осложнения.
Вместе с тем надо понимать: мы изобретаем новые препараты, но и раковые клетки мутируют и к ним приспосабливаются. Даже у пациента, которому раньше лечение без «химии» помогало, опухоль может спрогрессировать и стать нечувствительной к лекарствам, которые сдерживали ее рост. В этом случае химиотерапия применяется как экстренное лечение.
Например, пациентка с раком молочной железы долгое время принимает гормоны, и опухоль не растет. Внезапно она чувствует слабость, появляются метастазы в печени. В этом случае мы проводим несколько циклов химиотерапии, возвращаем организм в состояние, когда опухоль вновь начинает реагировать на гормоны, и тогда пациентка возвращается к прежней схеме лечения.
Совсем без химиотерапии на нынешнем уровне развития онкологии мы не обойдемся. Но при этом развивается «сопроводительное лечение» — вместе с химиотерапией пациент получает целый набор лекарств, ослабляющих тошноту, ускоряющих восстановление клеток крови и нормализующих стул. Так что неприятные побочные эффекты химиотерапии удается значительно ослабить.
Сомнительный источник
Об исследовании «профессора Гарвардского университета Джона Кэрнса», которое озвучивает миф 1: химия малоэффективна, я слышу впервые. Единственный практикующий врач по имени Джон Кернс, которого удалось найти в интернете, — это невролог-радиолог, который занимается проблемами головного мозга, а про химиотерапию вообще ничего не писал.Возможно, речь идет о британском враче Джоне Кернсе (John Cairns), с 1991 года на покое – он 1923 года рождения. Кернс — автор книг «Рак: Наука и Общество» (1978) и «Вопросы жизни и смерти: взгляды на здравоохранение, молекулярную биологию, рак и перспективы человеческого рода» (1997). Годы работы Джона Кернса говорят о том, что он ссылался на статистику выживаемости 1970-1980-х годов, и публиковаться в научных журналах в начале 2000-х не мог.Если речь идет об этом Джоне Кернсе, то мы можем говорить лишь об устаревших исследованиях в онкологии: с 1970-х годов эффективность лекарств сильно изменилась.«Журнал клинической онкологии» в число современных авторитетных изданий не входит.
«Scientific American» — это американский научно-популярный журнал. Доверия к нему как к изданию, публикующему результаты научных исследований, никакого.Похожее скептическое исследование про химиотерапию выложил недавно портал geektimes.ru. Там сказано: «за период с 2009 по 2015 год было одобрено 48 различных противоопухолевых препаратов. Из них эффективны 10%, а 57% не дали вообще никакого эффекта». Здесь исследователи оценивали только два параметра – 5-летнюю выживаемость и качество жизни и смешали очень разные заболевания – рак желудка, рак легкого, и рак крови. Показатели по этим локализациям опухолей разные, механизм действия препаратов – тоже, и признаком эффективности лекарства будут разные показатели выживаемости. А у исследователей получилась просто «средняя температура по больнице».
Оригинал статьи опубликован на сайте Miloserdie.ru
В России у 3 762 218 человек диагностированы злокачественные новообразования и каждый год эта цифра увеличивается более чем на 600 000 новых случаев [1]. Всем онкопациентам необходимо противоопухолевое лечение, и многим из них – лекарственное.
Большую часть лекарственного противоопухолевого лечения пациенты, как правило, получают с помощью внутривенных инъекций. Это предполагает регулярное посещение онкологического учреждения для проведения очередного цикла терапии. Нередко это приносит неудобства, а инъекции могут быть болезненными. В некоторых случаях количество циклов не ограничено определенным числом, лечение может длиться месяцы или годы, вплоть до прогрессирования или развития непереносимой токсичности [2].
Чтобы пациент мог сократить количество визитов в больницу, все больше новых препаратов производится в пероральной форме.
Что такое пероральная лекарственная противоопухолевая терапия?
- Пероральная терапия – это любая терапия, которая принимается внутрь через рот в виде таблеток или капсул.
Безусловно такое лечение позволяет человеку вести активную жизнь и работать, что особенно актуально при длительной противоопухолевой терапии.
Таблетки – это только химиотерапия?
Не только. Ниже представлены основные препараты, которые можно использовать внутрь перорально:
- Химиотерапия: циклофосфамид, метотрексат, этопозид, капецитабин, винорелбин;
- Гормонотерапия: тамоксифен, торемифен, анастрозол, летрозол, эксеместан, мегестрол, медроксипрогестерон, бикалутамиб, энзалутамид, абиратерон;
- Таргетная терапия: регорафениб, сорафениб, сунитиниб, пазопаниб, акситиниб, гефитиниб, эрлотиниб, афатиниб, осимертиниб, кризотиниб, олапариб, палбоциклиб, рибоциклиб, лапатиниб, дабрафениб, траметиниб, вемурафениб, кобиметиниб.
Почему мне выписали таблетки, а моей знакомой с таким же диагнозом — капельницы?
Если вам назначили таблетки — это не значит, что исчерпаны все возможности вашего лечения.
Таблетки или капсулы могут назначаться как самостоятельное лечение, так и в качестве послеоперационного (после радикального удаления опухоли) профилактического (адъювантного) лечения. Пример таблетированной адъювантной терапии при раке молочной железы – тамоксифен или анастрозол в течение 5 лет [3].
В каких случаях могут назначить «химию» в таблетках?
Таблетки или капсулы назначают по определенным показаниям:
- Гистологический тип опухоли. Например, аденокарцинома.
- Рецепторный статус опухоли. Например, наличие рецепторов к эстрогену и прогестерону [3].
- Другие характеристики опухоли. Например, наличие определенной мутации, степень злокачественности, стадия распространения, наличие лимфоваскулярной инвазии и т.д.
- Важно и состояние вашего желудочно-кишечного тракта, а именно — возможность усвоить и произвести всасывание лекарственного препарата в системный кровоток.
Таблетки также могут применяться в следующих случаях:
- Пораженные вены;
- Невозможность внутривенного введения;
- Отек верхних конечностей;
- Поражение кожи грудной стенки, когда нет возможности установить порт-систему.
Например, пациенту может быть назначена поддерживающая лечебная химиотерапия капецитабином вместо внутривенного 5-фторурацила с лейковорином [4].
При опухолях каких органов могут назначить таблетки?
Рак молочной железы [5]:
- Химиотерапия (метастатический процесс): CMF (циклофосфамид внутрь + метотрексат в/в + 5-фторурацил в/в); Метрономный режим циклофосфамид + метотрексат; Капецитабин; Винорелбин (капсулы); Этопозид (капсулы).
- Гормонотерапия (послеоперационно или при метастатическом процессе): Тамоксифен, Анастрозол, Летрозол, Эксеместан, Мегестрол.
- Таргетная терапия (метастатический процесс): Рибоциклиб, Палбоциклиб, Лапатиниб.
- Остеомодифицирующий агент (при метастазах в костях): Клодроновая кислота.
Рак ободочной и прямой кишки [6,7]:
- Химиотерапия (послеоперационно или при метастатическом процессе): в схеме CapOX (XELOX) – Капецитабин внутрь + Оксалиплатин внутривенно, Капецитабин.
- Таргетная терапия (при метастатическом процессе): Регорафениб.
Рак яичников [8]:
- Химиотерапия (метастатический процесс): этопозид; циклофосфамид + метотрексат (метрономный режим).
- Гормонотерапия (метастатический процесс): летрозол, анастрозол, тамоксифен.
- Таргетная терапия (метастатический процесс или рецидив): Олапариб.
Рак тела матки (метастатический процесс) [9]: гормонотерапия (летрозол, анастрозол, тамоксифен).
Рак шейки матки (метастатический процесс) [10]: капецитабин.
Немелкоклеточный рак легкого (метастатический процесс) [11]: Гефитиниб, Эрлотиниб, Афатиниб, Осимертиниб, Кризотиниб.
Почечно-клеточный рак (метастатический процесс) [12]: Сорафениб, Сунитиниб, Пазопаниб и Акситиниб.
Меланома кожи (послеоперационно или при метастатическом процессе) [13]: Дабрафениб, Траметиниб, Вемурафениб, Кобиметиниб.
Меньше ли осложнений от таблеток или капсул?
Нет, таблетки и капсулы — это все равно противоопухолевая терапия. Она отличается лишь способом доставки лекарственного средства в организм. Осложнения и побочные эффекты такие же, как и при инъекциях.
Потеряю ли я волосы от противоопухолевой лекарственной терапии в таблетках?
Да, в некоторых случая это возможно [14], например:
- Этопозид вызывает обратимую алопецию у 8–66% пациентов, а иногда вызывает полную потерю волос;
- Метотрексат, Винорелбин и Циклофосфамид часто вызывают умеренную алопецию;
- Капецитабин редко вызывает выпадение волос.
Будет ли тошнота и рвота при пероральной противоопухолевой лекарственной терапии?
Да, некоторые препараты больше других вызывают рвоту [15]:
- Для Циклофосфамида, Винорелбина и Кризотиниба характерна умеренная эметогенность, т.е. рвота возникает у 30-90% пациентов. Для профилактики обязательно назначается противорвотная терапия.
- Капецитабин, этопозид и большинство таргетных препаратов относятся к препаратам с низкой эметогенностю, т.е. рвота возникает у 10-30% пациентов
- Метотрексат и Вемурафениб обладают минимальной эметогенностью (рвота у <10%) и не требуют назначения противорвотных средств.
- Еще реже вызывает рвоту гормональная терапия.
Какие еще осложнения возможны при приеме противоопухолевой терапии в таблетках и капсулах?
- Изменения со стороны крови: анемия, лейкопения, нейтропения, тромбоцитопения;
- Изменения кожи (капецитабин – ладонно-подошвенный синдром [16]; регорафениб, сорафениб, сунитиниб и акситиниб – ладонно-подошвенная кожная реакция [17]);
- Стоматит;
- Слабость;
- Диарея;
- Дисменорея, приливы, вагинальное кровотечение (гормональная терапия [18]).
О чем мне стоит знать до начала пероральной противоопухолевой лекарственной терапии?
- В каких дозах и когда принимать (сколько раз в день; после, до или во время еды);
- Сопутствующие мероприятия (пить много жидкости до, во время и после приема циклофосфамида [19]; с какими продуктами совместимо);
- Обязательно сообщить врачу, какие препараты вы принимаете по сопутствующим заболеваниям (артериальная гипертензия, сахарный диабет и т.д.), чтобы предусмотреть возможные взаимодействия;
- Ваш лечащий врач может не помнить все особенности приема всех пероральных средств. Нет ничего зазорного, чтобы уточнить особенности приема вашего препарата. Спрашивать не только можно, но и нужно!
Какие существуют особенности приема внутрь отдельных противоопухолевых препаратов?
- Этопозид: внутрь, натощак (можно принимать, запивая стаканом апельсинового сока). Избегать действий, которые могут привести к травмам и кровотечениям (включая бритье).
- Метотрексат: избегать действий, которые могут привести к травмам и кровотечениям (включая бритье); избегать солнца.
- Винорелбин: внутрь, целиком, не разжевывая и не рассасывая во рту, запивая водой. В связи с наличием сорбита, винорелбин не следует использовать у больных с наследственной непереносимостью фруктозы.
- Тамоксифен: внутрь, не разжевывая, запивая водой. В начале лечения в течение 2 недель возможно увеличение мягкотканных образований и эритема пораженных областей.
- Анастрозол, Летрозол: внутрь целиком, в одно и то же время, запивая водой. Применяется только в постменопаузе или у пациенток с овариальной супрессией.
- Эксеместан: внутрь, желательно после еды. Применяется только в постменопаузе или у пациенток с овариальной супрессией.
- Сунитиниб: внутрь, независимо от приема пищи. Может наблюдаться изменение окраски кожи вследствие наличия в препарате желтого красителя.
- Акситиниб: внутрь целиком, запивая стаканом воды, вне зависимости от приема пищи;
- Сорафениб: внутрь, в промежутках между приемами пищи или вместе с пищей, содержащей низкое или умеренное количество жира, запивая стаканом воды.
- Регорафениб: внутрь целиком, запивая водой, 1 раз в сутки в одно и то же время после приема пищи, содержащей низкое (<30%) количество жиров.
- Пазопаниб: внутрь целиком 1 раз в сутки, не менее чем за 1 час до или через 2 часа после приема пищи.
- Гефитиниб: внутрь, независимо от приема пищи, 1 раз в сутки. Можно также растворить (в течение 15 минут) в 100 мл питьевой (негазированной) воды и вводить внутрь через назогастральный зонд. N.B! В составе препарата – лактоза (необходимо учитывать непереносимость)!
- Эрлотиниб: внутрь, 1 раз в сутки, не менее чем за 1 час или через 2 часа после приема пищи. Курение снижает концентрацию эрлотиниба в плазме крови на 50–60%
- Афатиниб: внутрь, натощак, не менее чем за 1 ч до приема пищи или спустя 3 часа после приема пищи.
- Осимертиниб: внутрь целиком, 1 раз в сутки, в одно и то же время вне зависимости от приема пищи. Можно растворить в 15 мл питьевой (негазированной) воды и вводить через назогастральный зонд
- Кризотиниб: Внутрь целиком, вне зависимости от приема пищи. Избегать употребления грейпфрута и грейпфрутового сока
- Олапариб (табл., капс.): Внутрь целиком, через 1 час после или за 2 часа до приема пищи. B! Дозы таблеток и капсул не взаимозаменяемы!
- Палбоциклиб: внутрь целиком вместе с пищей в одно и то же время. Избегать грейпфрута или грейпфрутового сока, а также препаратов зверобоя.
- Рибоциклиб: внутрь целиком вне зависимости от приема пищи в одно и то же время.
- Лапатиниб: внутрь, за 1 час до или через 1 час после еды. Суточную дозу нельзя делить на приемы.
- Дабрафениб: внутрь 2 раза в сутки в одно и то же время через 1 час после или за 2 часа до приема пищи. Может быть повышение уровня глюкозы, что потребует изменения доз препаратов для лечения сахарного диабета.
- Траметиниб: внутрь 1 раз в сутки в одно и то же время, через 1 час после или за 2 часа до приема пищи.
- Вемурафениб: внутрь целиком 2 раза в сутки, вне зависимости от приема пищи, однако следует воздержаться от длительного приема обеих доз натощак.
- Кобиметиниб: внутрь целиком 1 раз в сутки, вне зависимости от приема пищи.
- Клодроновая кислота: внутрь. Суточная доза 1600 мг однократно утром натощак (за 1 час до еды), запивая стаканом воды (если >1600 мг, то в 2 приема). Нельзя принимать вместе с молоком, пищей и препаратами, содержащими двухвалентные катионы (кальций, препараты железа, антациды). Избегать стоматологических вмешательств во время приема клодроновой кислоты. До начала приема клодроновой кислоты следует санировать полость рта.
Что делать в случае пропуска приема таблетки(-ок)?
- Сообщить об этом вашему лечащему врачу
- В следующий прием НИКОГДА не принимайте дополнительно пропущенную дозу! *
* За исключением некоторых случаев. Необходимо ознакомиться с инструкцией к препарату.
Как не забыть принять противоопухолевые лекарства?
- Принимать таблетки в одно и то же время и при одних и тех же обстоятельствах каждый день.
- Поставьте напоминание на своем смартфоне.
- В путешествие возьмите с собой достаточно таблеток на случай непредвиденных задержек.
- Ведите дневник с информацией о вашем самочувствии. Держите дневник на видном месте.
- Просите родственников напоминать о приеме лекарств.
Что делать, если выпил двойную (и более) дозу?
- Немедленно сообщить об этом лечащему врачу.
- Тщательно следить за состоянием своего здоровья (вести дневник).
- В некоторых случаях потребуются срочные мероприятия (например, введение кальция фолината при передозировке метотрексата в течение первого часа).
Мне дали пачку таблеток – я могу просто пить таблетки и больше ничего не делать?
Нет, при каждом из препаратов требуется периодически выполнять обследования с целью выявления возможных осложнений лечения. Примеры:
- Клинический и биохимический анализы крови (ОАК и БАК): при химиотерапии – перед каждым циклом или каждые 2-3 недели;
- Капецитабин: периодически ЭКГ;
- Тамоксифен: ежегодный гинекологический осмотр; периодически ОАК и БАК (включая уровень кальция);
- Летрозол, Анастрозол, Эксеместан: ежегодная денситометрия;
- Сунитиниб, Сорафениб, Пазопаниб, Акситиниб: ежедневное измерение АД; ОАК, БАК, ОАМ перед каждым циклом или каждые 2-3 недели; периодически ЭКГ; ЭхоКГ каждые 12-24 недели;
- Регорафениб: обязательно АЛТ и АСТ не реже 1 раза в месяц, периодически ОАК и БАК, контроль АД, периодически ЭКГ;
- Гефитиниб, Эрлотиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин);
- Афатиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭхоКГ (ФВЛЖ) и осмотр офтальмолога;
- Осимертиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭКГ (интервал QT) и осмотр офтальмолога;
- Кризотиниб: периодически ОАК, оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭКГ (интервал QT) и осмотр офтальмолога;
- Олапариб: ежемесячно ОАК;
- Палбоциклиб: ОАК перед каждым циклом;
- Рибоциклиб: ОАК, АЛТ и АСТ перед каждым циклом, периодически ЭКГ, контроль электролитов (калия, кальция, фосфатов и магния) первые 6 циклов;
- Лапатиниб: ЭхоКГ (контроль ФВЛЖ), контроль показателей функции печени (АЛТ, АСТ, общего билирубина и ЩФ) до начала терапии, далее каждые 4–6 недель;
- Дабрафениб: креатинин после лихорадки, ЭКГ до лечения, через 1 месяц после начала лечения и после изменения дозы, контроль глюкозы при СД, осмотр кожных покровов;
- Траметиниб: креатинин после лихорадки, периодически ЭхоКГ (ФВЛЖ), контроль АД, осмотр офтальмолога при симптомах нарушения зрения, контроль функции печени каждые 4 недели в течение 6 месяцев после начала лечения, осмотр кожных покровов;
- Вемурафениб: ЭКГ и контроль электролитов 1 раз в месяц, осмотр офтальмолога, осмотр кожных покровов, контроль функции печени каждые 4 недель;
- Кобиметиниб: осмотр офтальмолога, контроль ЭхоКГ (ФВЛЖ) каждые 3 месяца, контроль функции печени, креатинина и КФК каждые 4 недели.
Заключение
- Пероральная противоопухолевая терапия – это терапия в форме таблеток или капсул.
- Это удобно (повышается социальная активность пациента, поскольку больше не требуется постоянное пребывание в больнице). Появляется все больше пероральных противоопухолевых препаратов.
- Пероральная противоопухолевая лекарственная терапия показана не для всех типов рака.
- Нужна ответственность со стороны пациента: не пропускать приемы лекарства, следить за состоянием своего здоровья.
- Необходимо наличие возможности связи с лечащим врачом при появлении осложнений.
Источники:
- Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2018 году (заболеваемость и смертность). Москва: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2019. 250 p.
- Руководство по химиотерапии опухолевых заболеваний. 4th ed. / ed. Переводчикова Н.И., Горбунова В.А. Москва: Практическая медицина, 2018. 688 p.
- Regan M.M. Predicting Benefit of Endocrine Therapy for Early Breast Cancer // Breast. 2015. Vol. 24, № 0 2. P. S129–S131.
- Luo H.Y. et al. Single-agent capecitabine as maintenance therapy after induction of XELOX (or FOLFOX) in first-line treatment of metastatic colorectal cancer: randomized clinical trial of efficacy and safety // Ann. Oncol. 2016. Vol. 27, № 6. P. 1074–1081.
- Клинические рекомендации: Рак молочной железы. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак ободочной кишки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак прямой кишки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак яичников/рак маточной трубы/первичный рак брюшины. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак тела матки и саркомы матки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак шейки матки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Злокачественное новообразование бронхов и легкого. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак паренхимы почки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Меланома кожи и слизистых оболочек. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Chon S.Y. et al. Chemotherapy-induced alopecia // J. Am. Acad. Dermatol. 2012. Vol. 67, № 1. P. e37-47.
- Aapro M. et al. MASCC/ESMO Antiemetic Guideline 2016 With Updates in 2019. Multinational Association of Supportive Care in Cancer. 2019. P. 55.
- Blum J.L. et al. Multicenter phase II study of capecitabine in paclitaxel-refractory metastatic breast cancer // J. Clin. Oncol. 1999. Vol. 17, № 2. P. 485–493.
- Bhojani N. et al. Toxicities associated with the administration of sorafenib, sunitinib, and temsirolimus and their management in patients with metastatic renal cell carcinoma // Eur. Urol. 2008. Vol. 53, № 5. P. 917–930.
- Тамоксифен (Tamoxifen®) — инструкция по применению, состав, аналоги препарата, дозировки, побочные действия [Electronic resource]. URL: https://www.rlsnet.ru/tn_index_id_3077.htm#pobochnye-dejstviya (accessed: 27.07.2020).
- Эндоксан® (Endoxan®) — инструкция по применению, состав, аналоги препарата, дозировки, побочные действия [Electronic resource]. URL: https://www.rlsnet.ru/tn_index_id_3690.htm (accessed: 27.07.2020).
В последнее время появилось множество публикаций на тему питания, которое помогает живому организму поддерживать кислотно-щелочное равновесие, не позволяя ему сдвигаться в кислую сторону [1, 2]. Такое питание включает в себя как рацион, насыщенный овощами и фруктами, так и употребление щелочной воды.
Кислотно-щелочной баланс внутренней среды организма поддерживается в достаточно жестких границах на уровне pH артериальной крови от 7,26 до 7,45 буферными системами организма [3], и принято считать, что он изменяется только при тяжелых заболеваниях. Однако анализ кислотно-щелочного равновесия крови, как правило, проводился у пациентов с выраженной патологией и мало изучался у практически здоровых людей, подверженных негативному влиянию экологии, стрессам, изменению в питании и проч. В настоящее время отрабатываются более чувствительные методы и модели, которые, возможно, помогут понять более тонкие, но весьма существенные для здоровья колебания pH [4, 5].
Есть исследование, убедительно доказывающее, что не только тяжелые состояния здоровья, но и условия работы в современной промышленности достоверно сдвигают традиционные показатели буферной системы крови (pH, РаCO2, РаO2 крови и HCO в плазме) у рабочих завода по производству пластмасс [6]. О более тонких изменениях кислотно-щелочного равновесия в связи с эволюцией питания людей в историческом разрезе изложено также в European Journal of Nutrition в 2001 г. [7]. Там же указано, что «во время высокоинтенсивной активности ацидоз ответственен за усталость и истощение рабочих мышц. Введение бикарбонатной добавки перед тренировкой улучшало показатели, задерживая начало усталости». Кислотно-щелочное равновесие зависит от питания перед высокоинтенсивной тренировкой. Низкое употребление углеводов перед тренировкой приводит после интенсивной нагрузки к его сдвигу в кислую сторону [8, 9]. Определение кислотно-щелочного равновесия по показателям мочи (pH, бикарбонаты, мочевина) также может показать баланс кислот и оснований в организме. Таким методом было выявлено негативное влияние западного стиля питания с большим количеством белка на изменение показателей мочи в кислую сторону [10]. Есть и другие работы, доказывающие влияние питания на кислотно-щелочной баланс как у людей, так и у животных, где подчеркивается, что несбалансированный рацион меняет кислотно-щелочное равновесие в кислую сторону [11–13].
Таким образом, роль питания в поддержании кислотно-щелочного баланса подтверждена и продолжает изучаться, и немалую долю в рационе составляет вода, оказывающая значимое влияние на здоровье наряду с пищей. В литературе накопилось немало данных о благоприятном воздействии на здоровье употребления питьевой щелочной воды, являющейся основой для коррекции кислотно-щелочного равновесия на фоне привычного для человека питания. Изучалось ее влияние на общее оздоровление, уровень глюкозы в крови, массу тела, восстановление спортсменов после напряженных тренировок и проч., что будет отдельно рассмотрено ниже.
Материалы и методы исследования
Были проанализированы рандомизированные клинические исследования, а также группы нерандомизированных исследований.
Результаты и обсуждения
Питьевая вода во всех странах регулируется по показателю pH, однако допустимый диапазон колебаний достаточно широкий. В Российской Федерации допустимыми параметрами для питьевой воды является pH в диапазоне 6–9 [14], охватывая диапазон от слабокислой до щелочной реакции. Питьевая вода с водородным показателем 8–9 является щелочной, находясь в нормируемых параметрах для ежедневного потребления.
Одним из самых спорных вопросов, возникающих при рассмотрении пользы питьевой щелочной воды, является сомнение в том, что она может полностью нейтрализоваться кислой средой желудка. Действительно, на первый взгляд этот вопрос очевиден, и есть предположение, что щелочная среда будет полностью инактивирована желудочным соком, потеряв свои полезные свойства. Однако ответ на этот вопрос не так прост, и было бы неправильно его рассматривать, опираясь только на физико-химические свойства двух сред, упуская из виду некоторые особенности эвакуации желудочного содержимого. Этот вопрос очень внимательно был рассмотрен некоторыми исследователями, так как в медицине всегда достаточно остро стоит вопрос, как избежать инактивации отдельных медицинских препаратов и снизить время их контакта с кислым содержимым желудка. Этот вопрос по отношению к щелочной воде в данном обзоре будет рассмотрен впервые.
Для понимания степени и времени контакта щелочной воды с кислотностью желудка необходимо рассмотреть особенности эвакуации жидкости и пищи из желудка. Методы изучения особенности эвакуации содержимого желудка включают методы взятия проб желудочно-кишечного тракта [15–18], сцинтиграфию [19, 20], фармакокинетический анализ маркерных веществ [21] и магнитно-резонансную томографию (МРТ) [22, 23].
Впервые механизм намного более быстрой эвакуации воды по сравнению с пищей был описан и изучен в 1908 г. Г. В. Вальдейером, который описал анатомическую структуру складок слизистой на малой кривизне желудка (рис.), выступающей в качестве пути для быстрой эвакуации жидкости [24], назвав ее «Magenstrasse» — желудочной дорожкой. Кстати, именно этот известнейший гистолог и анатом ввел термины «нейрон» и «хромосома».
Впоследствии феномен Вальдейера был неоднократно описан другими авторами [25, 26] и в 70-х годах прошлого столетия был окончательно подтвержден [27, 28]. В 2007 и 2015 гг. феномен быстрой эвакуации воды (в течение 10 мин) из желудка был подтвержден с помощью математических моделей [29, 30].
В 2017 г. группа немецких ученых опубликовала работу, где с помощью МРТ изучался механизм эвакуации воды, выпитой как натощак, так и после приема пищи, причем в данной работе исследовались различные виды пищи (твердость, калорийность, жирность) [31]. Несмотря на высокую вариабельность времени эвакуации воды у испытуемых, подтверждено, что большая часть воды не смешивается с химусом и эвакуируется значительно быстрее пищи. Более всего задерживает эвакуацию гомогенная нежирная пища, с которой происходит смешивание жидкости в желудке.
На скорость эвакуации воды влияет также ее температура — прохладные напитки (5–20 °C) проходят из желудка в двенадцатиперстную кишку быстрее, чем теплые (25–40 °C) [32, 33]. Следует отметить, что все исследования проводились на объемах 250–350 мл, то есть эвакуаторная функция желудка при употреблении больших объемов пищи не изучалась, вода также выпивалась в количестве 250 мл.
Несмотря на то, что вопрос особенностей эвакуации воды из желудка был достаточно хорошо изучен и подтвержден, он известен только определенному кругу исследователей и широко не обсуждается в кругах практических врачей. Хотя именно этот феномен помог бы понять механизм всасывания и расщепления некоторых лекарств и жидкостей, долгое соприкосновение которых с кислой средой желудка было бы нежелательно.
Ознакомление с феноменом Вальдейера дает понимание того, что значительная часть щелочной воды в желудке после ее употребления будет эвакуироваться в двенадцатиперстную кишку достаточно быстро по складкам малой кривизны и не будет соприкасаться с кислой средой желудочного сока, сосредоточенного в антральном отделе. Особенно быстро этот процесс происходит при пустом желудке. Другими словами, кислотность желудочного сока не влияет на сохранение щелочности жидкости. В качестве рекомендаций для максимального сохранения щелочной среды самым оптимальным будет режим, когда щелочная вода будет выпита натощак или между приемами пищи.
Воздействие на организм человека щелочной воды, полученной электролизом, изучалось отдельными авторами как в моделях на животных, так и у людей. Общеоздоровительный эффект от постоянного употребления такой воды рассматривался, в частности, с точки зрения воздействия на окислительные процессы, вызывающие обширное повреждение биологических макромолекул и ведущие к различным заболеваниям, старению и мутациям. В частности, были рассмотрены механизмы защиты от окисления и повреждения РНК, ДНК и белков как in vitro [34–37], так и in vivo у лабораторных крыс [38]. Предполагалось, что щелочная вода является идеальным поглотителем активного кислорода, являющегося одним из мощных повреждающих факторов в живых системах. Результаты исследований подтвердили данный тезис. Все эти исследования установили, что щелочная вода имела тенденцию подавлять одноцепочечный разрыв ДНК, РНК и защищать белок от воздействия окислительного стресса. Доказано также, что щелочная вода повышает активность ключевого детоксифицирующего фермента в организме, супероксиддисмутазы, который является основной защитой от повреждения свободными радикалами [34, 35].
Вода с щелочным диапазоном (pH 8,5–9,5) хорошо продемонстрировала свое антиоксидантное действие у пациентов, находящихся на диализе. K. C. Huang и соавт. изучили активные формы кислорода в плазме этих пациентов и обнаружили, что такая вода снижает уровень пероксида, повышенный гемодиализом, и минимизирует маркеры воспаления (С-реактивный белок и интерлейкин-6) после 1 месяца употребления. Эти данные показывают, что сердечно-сосудистые осложнения (инсульт и сердечный приступ) у пациентов, находящихся на гемодиализе, могут быть предотвращены или отсрочены с помощью такого безобидного питья [39]. Причем по активности и результатам анализов употребление щелочной воды у этой группы пациентов сравнимо с действием инъекционного витамина С, но, в отличие от последнего, без риска образования оксалатов [40]. В этой же статье отмечено, что шестимесячный прием щелочной воды увеличил гематокрит и уменьшил количество цитокинов, обеспечивающих мобилизацию воспалительного ответа.
Известно, что именно свободнорадикальное окисление приводит к развитию многих возрастных болезней, поэтому антиоксиданты могут быть полезными для смягчения разрушительного действия старения и, возможно, для его замедления. G. Fernandes из Университета Техаса сообщил, что различные виды лабораторных мышей, получавших щелочную воду с рождения, живут на 20–50% дольше контрольной группы, употреблявшей водопроводную воду. Он также обнаружил снижение уровня пероксида в сыворотке опытных мышей по сравнению с контрольными [41]. Исследование, проведенное на нематодах, у которых в качестве водной среды использовалась щелочная вода, показало, что она значительно продлила продолжительность жизни червей, что было интерпретировано как проявление поглощающего действия активных форм кислорода [42].
Оздоровительный эффект при приеме щелочной воды зарегистрирован и описан у людей в исследовании Н. В. Воробьевой (МГУ им. М. В. Ломоносова) при изучении микрофлоры кишечника. Отмечалась стимуляция роста нормальной анаэробной флоры. Положительное воздействие трактовалось автором как улучшение среды обитания и благоприятного микроэкологического фона для роста аутомикрофлоры [43].
Исследование, проведенное в Китае в 2001 г. с людьми, продемонстрировало, что прием щелочной воды на протяжении от 3 до 6 месяцев снижал вплоть до нормальных значений гиперлипидемию, уровень глюкозы крови при сахарном диабете 2 типа легкой степени и регулировал уровень артериального давления [44]. Аналогичные результаты с регуляцией сахара крови были получены и в других исследованиях. Другое исследование 2006 г., проведенное на лабораторных крысах с экспериментальным диабетом, подтвердило данные результаты [45]. Через 12 недель употребления щелочной воды снижались уровни холестерина, триглицеридов и сахара в крови.
Поскольку сахарный диабет 2 типа является достаточно актуальной проблемой в современном обществе, ему уделяется много внимания различными исследователеми. Интересные результаты были получены на людях, больных диабетом 2 типа, которые были разбиты на группы и получали воду с различным pH (7,0; 8,0; 9,5 и 11,5) в течение 14 дней. Было обнаружено, что сахароснижающее свойство проявляет вода с pH 9,5 и 11,5, тогда как более низкие значения не оказывают статистически достоверного влияния на глюкозу в крови [46]. Авторы также отмечают, что наряду с сахароснижающим эффектом щелочная вода проявляет выраженное антиоксидантное действие, которое необходимо больным сахарным диабетом, а также выраженный детоксикационный эффект, проявляющийся в учащенном мочеиспускании. Корейское исследование, проведенное на мышах с диабетом, подтвердило, что питье щелочной воды значительно снижало концентрацию глюкозы в крови и улучшало толерантность к глюкозе [47]. Однако не было выявлено воздействия на уровень инсулина. Еще два исследования подтвердили не только способствование снижению глюкозы в крови и нормализации толерантности к глюкозе, но и лучшее сохранение β-клеток поджелудочной железы, активно разрушающихся при прогрессировании данного заболевания [48, 49].
Исследования, посвященные действию щелочной воды на организм, были также проведены среди спортсменов и среди людей, получавших интенсивные физические нагрузки. Предполагается, что интенсивные физические нагрузки провоцируют окислительный стресс в организме [50]. Дегидратация после тренировок также провоцирует повышение уровня малонового альдегида, являющегося одним из маркеров окислительного стресса [51]. К окислению весьма чувствительны эритроциты. Насыщенный железом гемоглобин разлагается, выделяя супероксид [49, 52]. Когда активные формы кислорода инициируют перекисное окисление липидных мембран, белки клеточных мембран часто становятся сшитыми, а эритроциты становятся более жесткими с меньшей подвижностью [53]. Эти механизмы изменяют свойства эритроцитов, в том числе снижают текучесть крови и повышают агрегацию ее клеток, что приводит к увеличению вязкости крови и нарушению кровотока [54]. Аналогичные изменения под действием окислителей происходят и с тромбоцитами [55]. Агрегацию тромбоцитов усиливает и финибриноген, испытывающий действие окислительного стресса [56]. Поэтому одним из показателей выраженного окислительного стресса у спортсменов можно рассматривать повышение вязкости крови, которую усугубляет дегидратация после интенсивных тренировок.
Быстрое восстановление после интенсивных физических нагрузок является актуальной проблемой в спортивной медицине. J. Weidman и соавт. провели двойное слепое рандомизированное исследование для сравнения эффективности регидратации после тренировок с применением стандартной питьевой и щелочной воды (pH 9,5), полученной электролизом, в котором изучали показатели вязкости крови [57]. В этом исследовании была обнаружена значительная разница в вязкости цельной крови при оценке употребления воды с высоким pH по сравнению со стандартной очищенной водой во время фазы восстановления (120 мин) после интенсивной дегидратации, вызванной физической нагрузкой. Авторы объясняют полученные результаты нейтрализацией окислительных процессов, выявленных после интенсивных физических нагрузок в организме спортсменов. Исследование, проведенное с тремя видами воды: минеральной (pH 6,1), щелочной с низким содержанием минералов (pH 
В другом исследовании D. P. Heil продемонстрировал более быструю и лучшую регидратацию с бутылочной щелочной водой (pH 10), чем со стандартной питьевой водой у десяти велосипедистов мужского пола. Маркерами регидратации были удельный вес мочи, диурез, концентрация сывороточного белка и восстановление водного баланса [59]. Бикарбонатная бутылочная щелочная вода с микроэлементами (pH 9,1) показала также лучшие восстановительные свойства по сравнению с питьевой водой и у спортсменов боевых искусств после ограничения воды для быстрой потери веса перед соревнованиями [60]. Перечисленные исследования демонстрируют, что лучшие восстановительные свойства показывает вода со щелочным pH по сравнению с нейтральной питьевой водой, независимо от того, получена она электролизом или это бутылочный вариант.
Выводы
Таким образом, вода с pH 9–10 может рассматриваться как дополнительный фактор оздоровления. Растущий объем научных исследований не выявил негативных отрицательных воздействий на организм. Из рассмотренных публикаций очевидно, что употребление щелочной воды может быть дополнительной антиоксидантной поддержкой, благоприятно сказывается на состоянии здоровья при диабете и гиперлипидемии и может улучшать реологию крови в случае, когда она нарушена из-за интенсивных физических нагрузок. Применение щелочной воды в спорте для более активного восстановления после тренировок может дать дополнительный безопасный инструмент сохранения здоровья спортсменов.
Литературные данные, приведенные в обзоре, также могут помочь выработать рекомендации по приему щелочной воды для максимального сохранения ее полезных свойств. Особенности эвакуаторной функции желудка при употреблении пищи объемом до 250 мл позволяют большей ее части не смешиваться с его содержимым. Однако это касается не всего объема выпитой воды. Часть ее все-таки смешивается, особенно если пища является гомогенной и полужидкой. Наиболее полно сохранение свойств с наибольшей вероятностью произойдет при употреблении щелочной воды натощак или между приемами пищи. Следует также принимать во внимание, что исследования касались объема жидкости до 250 мл. Каким образом эвакуируются из желудка большие объемы воды, на сегодняшний день остается не изученным.
В заключение следует отметить, что сохраняется высокая актуальность исследований воздействия щелочной воды на здоровье, поскольку есть перспективы дополнительного безопасного алиментарного фактора питания, благотворно влияющего на организм и доступного для широких кругов населения.
Литература
- Riond J. L. Animal nutrition and acid-base balance // Eur J Nutr. 2001. № 40 (5). P. 245–254.
- Gannon R. H., Millward D. J., Brown J. E. et al. Estimates of daily net endogenous acid production in the elderly UK population: analysis of the National Diet and Nutrition Survey (NDNS) of British adults aged 65 years and over // Br J Nutr. 2008, Sep; 100 (3): 615–623.
- Adrogué H. E., Adrogué H. J. Acid-base physiology // Respir Care. 2001. Apr; 46 (4). Р. 328–341.
- Adrogué H. J., Madias N. E. Assessing Acid-Base Status: Physiologic Versus Physicochemical Approach // Kidney Dis. 2016. Nov; 68 (5). Р. 793–802.
- Todorovic J., Nešovic-Ostojic J., Milovanovic A. et al. The assessment of acid-base analysis: comparison of the «traditional» and the «modern» approaches // Med Glas (Zenica). 2015. Feb; 12 (1). Р. 7–18.
- Prakova G. Monitoring of acid-base status of workers at a methyl methacrylate and polymethyl methacrylate production plant in Bulgaria // RAIHA J (Fairfax, Va). 2003. Jan-Feb; 64 (1). Р. 11–16.
- Manz F. History of nutrition and acid-base physiology // Eur J Nutr. 2001. Oct; 40 (5). P. 189–199.
- Greenhaff P. L., Gleeson M., Maughan R. J. The effects of dietary manipulation on blood acid-base status and the performance of high intensity exercise // Eur J Appl Physiol Occup Physiol. 1987. 56 (3). Р. 331–337.
- Greenhaff P. L., Gleeson M., Whiting P. H. et al. Dietary composition and acid-base status: limiting factors in the performance of maximal exercise in man? // Eur J Appl Physiol Occup Physiol. 1987. 56 (4). Р. 444–450.
- Remer T. Influence of nutrition on acid-base balance — metabolic aspects // Eur J Nutr. 2001. Oct; 40 (5). Р. 214–220.
- Remer T. Influence of diet on acid-base balance // Semin Dial. 2000, Jul-Aug; 13 (4): 221–226.
- Riond J. L. Animal nutrition and acid-base balance // Eur J Nutr. 2001 Oct; 40 (5): 245–254.
- Akter S., Eguchi M., Kurotani K. High dietary acid load is associated with increased prevalence of hypertension: the Furukawa Nutrition and Health Study // Nutrition. 2015 Feb; 31 (2): 298–303.
- СанПиН 2.1.4.10749–01 «Питьевая вода. Гигиенические требования к качеству воды».
- Malagelada J. R., Longstreth G. F., Summerskill W. H. et al. Measurement of Gastric Functions during Digestion of Ordinary Solid Meals in Man // Gastroenterology. 1976, 70 (2), 203–210.
- Hens B., Corsetti M., Brouwers J. et al. Gastrointestinal and Systemic Monitoring of Posaconazole in Humans After Fasted and Fed State Administration of a Solid Dispersion // J. Pharm. Sci. 2016, 105 (9), 2904–2912.
- Hunt J. N., Macdonald I. The Influence of Volume on Gastric Emptying // J. Physiol. 1954, 126 (3), 459–474.
- Rubbens J., Brouwers J., Wolfs K. et al. Ethanol Concentrations in the Human Gastrointestinal Tract after Intake of Alcoholic Beverages // Eur. J. Pharm. Sci. 2016, 86, 91–95.
- Feinle C., Kunz P., Boesiger P. et al. Scintigraphic Validation of a Magnetic Resonance Imaging Method to Study Gastric Emptying of a Solid Meal in Humans // Gut. 1999, 44 (1), 106–111.
- Coupe A. J., Davis S. S., Evans D. F. et al. Do Pellet Formulations Empty from the Stomach with Food? // Int. J. Pharm. 1993, 92 (1), 167–175.
- Heading R. C., Nimmo J., Prescott L. F. et al. The Dependence of Paracetamol Absorption on the Rate of Gastric Emptying // Br. J. Pharmacol. 1973, 47 (2), 415–421.
- Koziolek M., Grimm M., Garbacz G. et al. Intragastric Volume Changes after Intake of a High-Caloric, HighFat Standard Breakfast in Healthy Human Subjects Investigated by MRI // Mol. Pharmaceutics. 2014, 11 (5), 1632–1639.
- Mudie D. M., Murray K., Hoad, C. L. et al. Quantification of Gastrointestinal Liquid Volumes and Distribution Following a 240 mL Dose of Water in the Fasted State // Mol. Pharmaceutics. 2014, 11 (9), 3039–3047.
- Waldeyer H. W. Die Magenstraße. Sitzungsberichte der Koniglich — Preussischen Akademie der Wissenschaften; Verlag der Ko?niglich Preussischen Akademie der Wissenschaften: Berlin, 1908.
- Jefferson G. The Human Stomach and the Canalis Gastricus (Lewis) // J. Anat. Physiol. 1915, 49 (Part 2), 165–181.
- Baastrup C. I. Roentgenological Studies of the Inner Surface of the Stomach and of the Movements of the Gastic Contents // Acta Radiol. 1924, 3 (2–3), 180–204.
- Malagelada J. R., Go V. L., Summerskill W. H. Different gastric, pancreatic, and biliary responses to solid-liquid or homogenized meals // Dig. Dis. Sci. 1979, 24 (2), 101–110.
- Malagelada J. R. Quantification of gastric solid-liquid discrimination during digestion of ordinary meals // Gastroenterology. 1977, 72 (6), 1264–1267.
- Pal A., Brasseur J. G., Abrahamsson B. A stomach road or «Magenstrasse» for gastric emptying // J. Biomech. 2007, 40 (6), 1202–1210.
- Ferrua M. J., Singh R. P. Computational modelling of gastric digestion: current challenges and future directions // Curr. Opin. Food Sci. 2015, 4, 116–123.
- Grimm M., Scholz E., Koziolek M. et al. Gastric Water Emptying under Fed State Clinical Trial Conditions Is as Fast as under Fasted Conditions // Mol Pharm. 2017, Dec 4; 14 (12): 4262–4271.
- Bateman D. N. Effects of meal temperature and volume on the emptying of liquid from the human stomach // J Physiol. 1982, Oct; 331: 461–467.
- Ritschel W. A., Erni W. The influence of temperature of ingested fluid on stomach emptying time // Int J Clin Pharmacol Biopharm. 1977 Apr; 15 (4): 172–175.
- Park E. J., Ryoo K. K., Lee Y. B. et al. Protective effect of electrolyzed reduced water on the paraquat-induced oxidative damage of human lymphocyte DNA // J. Korean Soc. Appl. Biol. Chem. 2005, 48, 155–160.
- Hanaoka K., Sun D., Lawrence R. et al. The mechanism of the enhanced antioxidant effects against superoxide anion radicals of reduced water produced by electrolysis // Biophys Chem. 2004, Jan 1; 107 (1): 71–82.
- Shirahata S., Kabayama S., Nakano M. et al. Electrolyzed-reduced water scavenges active oxygen species and protects DNA from oxidative damage // Biochem Biophys Res Commun. 1997, May 8; 234 (1): 269–274.
- Lee M. Y., Kim Y. K., Ryoo K. K. et al. Electrolyzed-reduced water protects against oxidative damage to DNA, RNA, and protein // Appl Biochem Biotechnol. 2006, Nov; 135 (2): 133–144.
- Yanagihara T., Arai K., Miyamae K. et al. Electrolyzed hydrogen-saturated water for drinking use elicits an antioxidative effect: a feeding test with rats // Biosci Biotechnol Biochem. 2005, Oct; 69 (10): 1985–1987.
- Huang K. C., Lee K. T., Chien C. T. Reduced hemodialysis-induced oxidative stress in end-stage renal disease patients by electrolyzed reduced water // Kidney International. 2003, 64 (2), p. 704–714.
- Huang K. C., Yang C. C., Hsu S. P. et al. Electrolyzed-reduced water reduced hemodialysis-induced erythrocyte impairment in end-stage renal disease patients // Kidney Int. 2006, Jul; 70 (2): 391–398.
- Rubik B. Studies and observations on the health effects of drinking electrolyzed-reduced alkaline water // WIT Transactions on Ecology and The Environment. 2011. Vol. 153, 317–327.
- Landis G. N., Tower J. Superoxide dismutase evolution and life span regulation // Mech. Ageing Dev. 2005. Vol. 126, № 3. P. 365–379.
- Vorobjeva N. V. Selective stimulation of the growth of anaerobic microflora in the human intestinal tract by electrolyzed reducing water // Medical Hypotheses. 2005. 64 (3), p. 543–546,
- Wang Yu-Lian. Preliminary observation on changes of blood pressure, blood sugar and blood lipids after using alkaline ionized drinking water // Shanghai Journal of Preventive Medicin. 2001, 12.
- Jin D., Ryu S. H., Kim H. W. et al. Anti-diabetic effect of alkaline-reduced water on OLETF rats // Biosci Biotechnol Biochem. 2006, Jan; 70 (1): 31–37.
- Edy Siswantoro, Nasrul Hadi Purwanto, Sutomo Effectiveness of Alkali Water Consumption to Reduce Blood Sugar Levels in Diabetes Mellitus Type 2 // JDM. 2017, Nov, vol. 7, № 4, р. 249–264.
- Kim M. J., Kim H. K. Anti-diabetic effects of electrolyzed reduced water in streptozotocin-induced and genetic diabetic mice // Life Sci. 2006, Nov 10; 79 (24): 2288–2292.
- Kim M. J., Jung K. H., Uhm Y. K. et al. Preservative effect of electrolyzed reduced water on pancreatic beta-cell mass in diabetic db/db mice // Biol. Pharm. Bull. 2007, Feb; 30 (2): 234–236
- Li Y., Nishimura T., Teruya K. et al. Protective mechanism of reduced water against alloxan-induced pancreatic beta-cell damage: Scavenging effect against reactive oxygen species // Cytotechnology. 2002, vol. 40, № 1–3, p. 139–149.
- Oostenbrug G. S., Mensink R. P., Hardeman M. R. et al. Exercise performance, red blood cell deformability, and lipid peroxidation: effects of fish oil and vitamin E // J Appl Physiol. 1997, Sep; 83 (3): 746–752.
- Paik I. Y., Jeong M. H., Jin H. E. et al. Fluid replacement following dehydration reduces oxidative stress during recovery // Biochem Biophys Res Commun. 2009; 383 (1): 103–107.
- Baskurt O. K., Meiselman H. J. Blood rheology and hemodynamics. Semin Thromb Hemost. 2003; 29 (5): 435–450.
- Halliwell B., Gutteridge J. Free radicals in medicine and biology. Oxford: Clarendon, 1999.
- Nwose E. U., Jelinek H. F., Richards R. S., Kerr P. G. Erythrocyte oxidative stress in clinical management of diabetes and its cardiovascular complications // Br J Biomed Sci. 2007; 64 (1): 35–43.
- https://www.lvrach.ru/2003/04/4530251/.
- Azizova O. A., Aseichev A. V., Piryazev A. P. et al. Effects of oxidized fibrinogen on the functions of blood cells, blood clotting, and rheology // Bull Exp Biol Med. 2007, Sep; 144 (3): 397–407.
- Weidman J., Holsworth R. E. Jr., Brossman B. et al. Effect of electrolyzed high-pH alkaline water on blood viscosity in healthy adults // J Int Soc Sports Nutr. 2016, Nov 28; 13: 45.
- Chycki J., Zajac T., Maszczyk A. et al. The effect of mineral-based alkaline water on hydration status and the metabolic response to short-term anaerobic exercise // Biol Sport. 2017, Sep; 34 (3): 255–261.
- Heil D., Seifert J. Influence of bottled water on rehydration following a dehydrating bout of cycling exercise // J Int Soc Sports Nutr. 2009; 6 (Suppl 1): 1–2.
- Chycki J., Kurylas A., Maszczyk A. et al. Alkaline water improves exercise-induced metabolic acidosis and enhances anaerobic exercise performance in combat sport athletes // PLoS One. 2018, Nov 19; 13 (11).
Е. А. Хохлова, доктор медицинских наук
ООО «Медицинский центр «Август», Чебоксары
Контактная информация: helenkhokhlova@rambler.ru
DOI: 10.26295/OS.2019.16.75.011
Питьевая щелочная вода – насколько благотворно ее влияние на организм? Обзор литературы/ Е. А. Хохлова
Для цитирования: Лечащий врач № 6/2019; Номера страниц в выпуске: 44-49
Теги: физические нагрузки, кислотно-щелочной баланс, диабет