20.06.2022
Описание препарата Эфлейра® (раствор для подкожного введения, 60 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 20.06.2022
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для п/к введения | 1 мл |
| активное вещество: | |
| нетакимаб | 60 мг |
| вспомогательные вещества: натрия ацетата тригидрат — 1,74 мг; трегалозы дигидрат — 80 мг; полоксамер 188 — 0,5 мг; уксусная кислота ледяная — до pH 5; вода для инъекций — до 1 мл |
Описание лекарственной формы
Раствор для п/к введения: прозрачный или слегка опалесцирующий от бесцветного до светло-желтого или светло-желтого с коричневатым оттенком цвета.
Фармакологическое действие
Фармакологическое действие
—
дерматотропное.
Фармакодинамика
Нетакимаб является рекомбинантным гуманизированным моноклональным антителом, в терапевтических концентрациях специфически связывающим ИЛ-17А, находящийся непосредственно в тканях или крови и других биологических жидкостях. ИЛ-17А — провоспалительный цитокин, гиперпродукция которого преимущественно обусловлена активацией Th17-лимфоцитов. В рамках врожденного иммунитета ИЛ-17А выполняет защитную роль. При хронических иммуновоспалительных заболеваниях патологическая активация Th17-лимфоцитов и гиперпродукция ИЛ-17 стимулирует Т-клеточный ответ и усиленную продукцию других медиаторов воспаления: ИЛ-1, ИЛ-6, ФНО-α, факторов роста (G-CSF, GM-CSF) и различных хемокинов.
Нетакимаб обладает высокой термодинамической константой специфического связывания с ИЛ-17А человека. По данным доклинических исследований, специфическое связывание нетакимаба в нормальных тканях человека ограничено тканями легкого, тимуса, лимфатических узлов, миндалин, что согласуется с данными об экспрессии ИЛ-17 клетками этих тканей.
Применение нетакимаба не сопровождается статистически значимым изменением уровня Т-лимфоцитов и не влияет на уровень и соотношение Ig классов А, G и М.
Специфическая противовоспалительная активность нетакимаба продемонстрирована в тестах in vitro и in vivo. Нетакимаб дозозависимо ингибирует ИЛ-17 и ФНО-α-зависимую продукцию ИЛ-6 на культуре клеток при IC50 40 pM. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (1 раз в нед в течение 4 нед) п/к введение нетакимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (суставной хрящ остается интактным, синовиальные оболочки — без признаков поражения и воспалительной реакции, пролиферации синовиоцитов не отмечено).
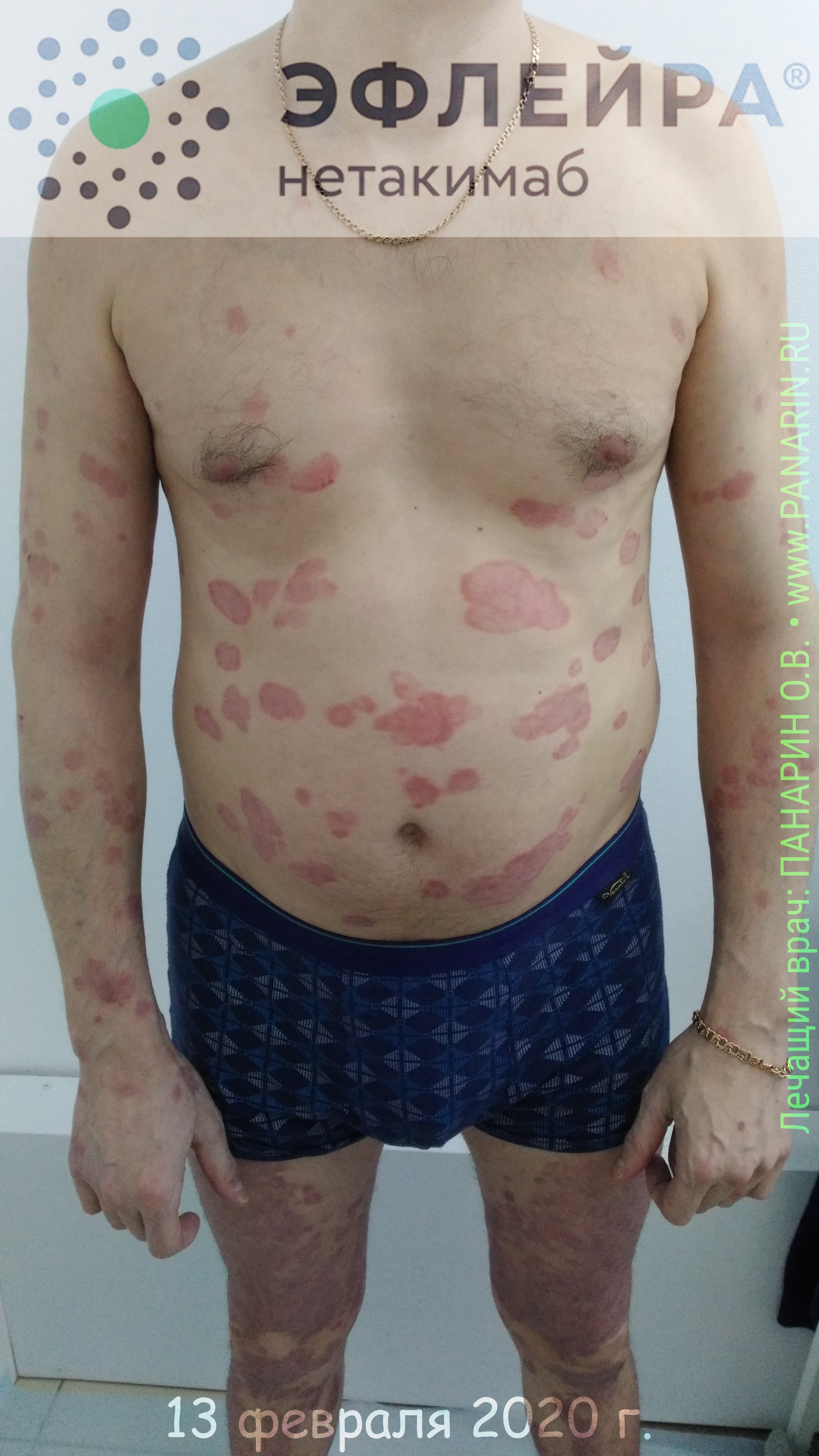
У больных псориазом использование нетакимаба сопровождается угасанием явлений воспаления и гиперкератоза в коже, достоверным снижением уровня С-реактивного белка и СОЭ.
У пациентов с активным анкилозирующим спондилитом и псориатическим артритом на фоне применения нетакимаба отмечается уменьшение симптомов воспаления в позвоночнике, энтезисах и суставах, а также быстрое снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание/распределение. Изменение концентрации нетакимаба после его п/к введения является дозозависимым (значения Сmax, Cmax–mult, AUC0–t находятся в прямой зависимости от дозы). Препарат характеризуется медленной фазой абсорбции с постепенным линейным нарастанием концентрации в сыворотке крови.
При однократном п/к введении нетакимаба в дозе 120 мг пациентам с бляшечным псориазом препарат начинал обнаруживаться в сыворотке крови в течение 0,5–4 ч после введения; Cmax нетакимаба составляла 15,1 (7,7–19,3) мкг/мл, Tmax — 144 (72–168) ч, AUC0–168 — 1667,8 (932,2–2270,8) мкг/мл·ч.
При повторных введениях отмечено накопление препарата в сыворотке крови с ростом концентрации в 1,8–3,6 раза. Cmax при многократном введении (Cmax–mult) составляла 33,0 (23,1–44) мкг/мл и достигалась (Tmax–mult) через 1680 (672–2016) ч.
Выведение. Характеристики выведения нетакимаба являются типичными для препаратов на основе моноклональных антител: показатели Kel (константа элиминации), T1/2, MRT (среднее время пребывания препарата в организме), клиренса не зависят от дозы вводимого препарата, T1/2 после однократного введения составляет около 16 сут.
Средний клиренс нетакимаба при однократном введении дозы 120 мг пациентам с бляшечным псориазом составил 1,8 л/сут.
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Особые группы пациентов
Почечная и печеночная недостаточность. Фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Возраст старше 65 лет. Фармакокинетические данные у лиц старше 65 лет отсутствуют.
Показания
лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия;
лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию;
лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию.
Противопоказания
гиперчувствительность к нетакимабу, а также к любому из вспомогательных веществ препарата;
клинически значимые инфекционные заболевания в острой фазе, включая туберкулез;
беременность;
период грудного вскармливания;
возраст до 18 лет.
С осторожностью: пациенты с хроническими и рецидивирующими инфекциями или анамнестическими указаниями на них, в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний, а также после недавно проведенной вакцинации живыми вакцинами; пациенты старше 65 лет (в связи с отсутствием данных клинических исследований о применении нетакимаба); больные с воспалительными заболеваниями кишечника, в т.ч. с болезнью Крона или язвенным колитом (в связи с отсутствием сведений о применении нетакимаба).
Применение при беременности и кормлении грудью
Беременность. При применении нетакимаба у животных не выявлено отрицательного влияния на репродуктивную функцию, эмбриотоксичности или тератогенных эффектов. Исследований влияния на плод у беременных женщин не проводилось. Препарат противопоказан к применению во время беременности.
Период грудного вскармливания. Нет данных о проникновении нетакимаба в грудное молоко. Учитывая, что IgG, к которым относится нетакимаб, при циркуляции в крови матери могут выделяться с грудным молоком, применение в период грудного вскармливания противопоказано. Во избежание негативного воздействия на ребенка следует прекратить либо грудное вскармливание, либо терапию, учитывая соотношение риска и пользы для матери и ребенка.
Фертильность. В исследованиях у животных не обнаружено негативного воздействия нетакимаба на фертильность. Данные о влиянии препарата на фертильность у людей отсутствуют.
Способ применения и дозы
П/к.
Применение препарата Эфлейра® должно осуществляться под наблюдением врачей, имеющих опыт лечения заболеваний, при которых показан препарат Эфлейра®. После соответствующего обучения возможно самостоятельное введение препарата пациентом при условии динамического наблюдения со стороны лечащего врача. Препарат Эфлейра® может применяться как в стационарных, так и в амбулаторных условиях.
Препарат Эфлейра® вводится в дозе 120 мг в виде 2 п/к инъекций по 1 мл препарата с концентрацией 60 мг/мл.
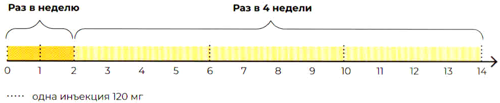
Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия. Рекомендуемая доза — 120 мг в виде 2 п/к инъекций по 1 мл (60 мг) препарата, каждая вводится 1 раз в нед на неделях 0, 1 и 2, затем 1 раз каждые 4 нед.
Лечение активного анкилозирующего спондилита при недостаточном ответе на стандартную терапию. Рекомендуемая доза — 120 мг в виде двух п/к инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в нед на неделях 0, 1 и 2, затем — каждые 2 нед.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию. Рекомендуемая доза — 120 мг в виде двух п/к инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в нед на неделях 0, 1 и 2, затем каждые 2 нед до недели 10 включительно. Далее с недели 14 препарат вводится в дозе 120 мг в виде двух п/к инъекций по 1 мл (60 мг) каждая 1 раз в 4 нед.
| Показание | Разовая доза, мг | Индукция | Поддерживающая терапия |
| Бляшечный псориаз | 120 | 0, 1, 2 недели | 1 раз в 4 нед, начиная с недели 6 |
| Анкилозирующий спондилит | 120 | 0, 1, 2 недели | 1 раз в 2 нед, начиная с недели 4 |
| Псориатический артрит | 120 | 0, 1, 2 недели | 1 раз в 2 нед, начиная с недели 4 по неделю 10 включительно, далее 1 раз в 4 нед с недели 14 |
При пропуске очередного введения по любой причине инъекция препарата Эфлейра® должна быть произведена как можно быстрее. Дата следующего введения рассчитывается исходя из продолжительности задержки с введением препарата: если со времени пропуска введения прошло не более 3 дней, то следующую инъекцию препарата необходимо выполнить по текущему графику; если с момента пропуска дозы прошло более 3 дней, то новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Эфлейра®.
Подготовка к проведению подкожной инъекции (на данном этапе не следует снимать колпачок шприца/автоинжектора)
1. Тщательно вымыть руки
Рисунок 1.
2. Достать упаковку с двумя шприцами/автоинжекторами с препаратом Эфлейра® из холодильника, затем извлечь из картонной пачки и ячейковой упаковки два шприца/автоинжектора и положить на чистую поверхность. Убедиться, что срок хранения препарата, указанный на картонной пачке и шприце/автоинжекторе, не истек.
Рисунок 2. Препарат Эфлейра® в преднаполненном шприце.
Рисунок 3. Препарат Эфлейра® в автоинжекторе.
3. Осмотреть шприцы/автоинжекторы, а также лекарственный препарат, находящийся в них. Препарат Эфлейра® представляет собой прозрачный, от бесцветного до светло-желтого цвета раствор. Нельзя использовать препарат в случае помутнения раствора, наличия в препарате посторонних видимых частиц; изменения цвета; повреждения любых частей шприца/автоинжектора; истечения срока годности («годен до…»), указанного на картонной пачке, а также на этикетке шприца/автоинжектора.
4. Перед введением шприцы/автоинжекторы с препаратом Эфлейра® следует довести до комнатной температуры, для этого необходимо оставить шприц при комнатной температуре в течение приблизительно 25–30 мин. Не следует согревать шприц/автоинжектор каким-либо другим способом.
Рисунок 4.
5. Подготовить салфетку/ватный тампон, спиртовой раствор.
Техника выполнения п/к инъекции препарата Эфлейра® в преднаполненном шприце
Выбор и подготовка места для инъекции
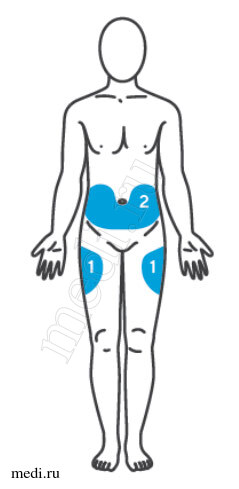
1. Выбрать место инъекции (передняя брюшная стенка, отступая не менее 5 см от пупка), передняя и боковая поверхность бедра или средняя треть наружной части плеча (возможные места для инъекций закрашены на рисунке ниже).
Рисунок 5.
2. Места инъекций и стороны следует менять с каждой последующей процедурой инъекции. Расстояние между двумя введениями должно составлять как минимум 5 см.
3. Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек (эти признаки могут указывать на наличие инфекции). По возможности не следует вводить препарат в псориатическую бляшку.
4. Место для укола необходимо обработать спиртовой салфеткой/ватным тампоном круговыми движениями.
Рисунок 6.
5. Шприц не встряхивать.
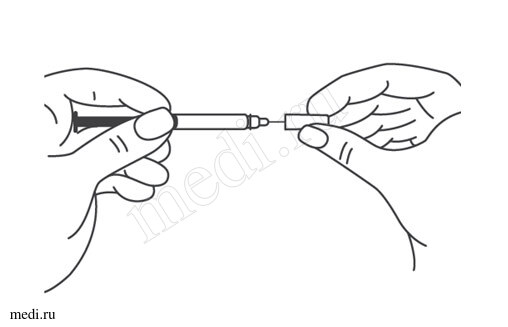
6. Снять колпачок с иглы, не дотрагиваясь до иглы и избегая ее прикосновения к другим поверхностям.
Рисунок 7.
7. Большим и указательным пальцами одной руки взять в складку обработанную кожу.
Рисунок 8.
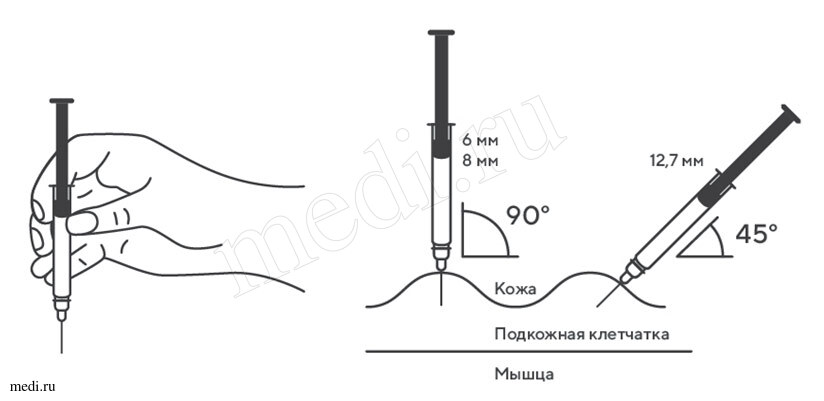
8. В другую руку взять шприц, держа его градуированной поверхностью вверх. Введение препарата необходимо осуществлять под углом 45 или 90° к поверхности кожи в зависимости от толщины кожи и выраженности подкожно-жирового слоя (у худощавых пациентов введение препарата осуществляется под углом 45°, у пациентов с толщиной кожной складки более 1,5 см допустимо введение под углом 90°).
Рисунок 9.
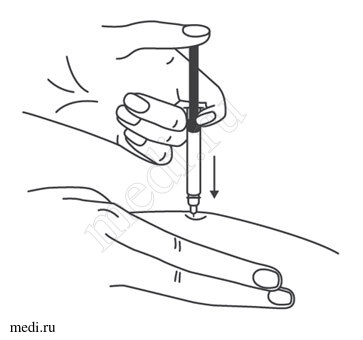
9. Одним быстрым движением полностью ввести иглу в кожную складку.
Рисунок 10.
10. После введения иглы складку кожи отпустить.
Рисунок 11.
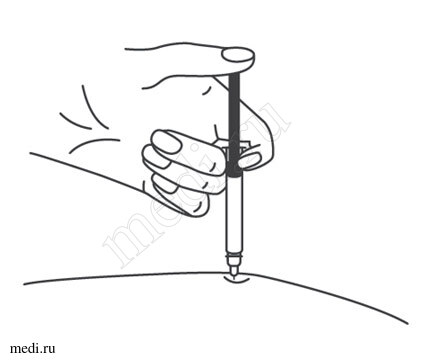
11. Ввести весь раствор медленным постоянным надавливанием на поршень шприца в течение 2–5 с.
Рисунок 12.
12. Когда шприц будет пустым, вынуть иглу из кожи под тем же углом.
Рисунок 13.
13. Сухой стерильной салфеткой/ватным шариком слегка прижать область инъекции, но не растирать область выполненной инъекции. Из места инъекции может выделиться небольшое количество крови. При необходимости можно воспользоваться пластырем.
14. Ввести вторую дозу препарата Эфлейра® аналогичным образом предпочтительно в ту же анатомическую область при условии, что место последующей инъекции должно быть не ближе 5 см от предыдущей. Время выполнения 2 инъекций не должно превышать 10 мин.
15. После инъекции шприц повторно не использовать.
Техника выполнения подкожной инъекции препарата Эфлейра® в автоинжекторе
Рисунок 14. Устройство автоинжектора.
Автоинжектор не встряхивать.
Не снимать защитный колпачок с автоинжектора до выполнения инъекции.
Проверить срок годности препарата по маркировке на упаковке, оценить целостность автоинжектора и состояние раствора через зону контроля автоинжектора. Не использовать автоинжектор в случае его повреждения, изменения цвета и прозрачности раствора, а также при истечении срока годности.
Рисунок 15.
1. Разместить автоинжектор на чистой горизонтальной поверхности.
2. Выбрать место введения (область брюшной стенки, отступая не менее 5 см от пупка, или передняя поверхность бедра) и обработать кожу в области введения спиртовой салфеткой.
Рисунок 16.
3. Непосредственно перед инъекцией одной рукой снять колпачок с автоинжектора, удерживая другой рукой его корпус.
Рисунок 17.
4. Одной рукой взять в складку обработанную спиртовой салфеткой кожу и удерживать в течение всей процедуры инъекции.
5. В другую руку взять автоинжектор, удерживая его за корпус. Введение препарата необходимо осуществлять, плотно прижав автоинжектор под углом 90° к поверхности кожи. Надавливание автоинжектором на поверхность кожной складки приведет к разблокированию кнопки.
Рисунок 18.
6. Удерживая автоинжектор под углом 90° к поверхности кожной складки, надавить до упора на кнопку автоинжектора. Пациент услышит щелчок, указывающий на начало инъекции. Не изменять положение автоинжектора. Необходимо удерживать кнопку в течение 10 с до окончания инъекции.
Рисунок 19.
7. Если инъекция не запустилась, следует отпустить кнопку и проверить, плотно ли прижат автоинжектор к кожной складке. Прижать плотно автоинжектор к коже и повторить процедуру инъекции, вновь нажав на кнопку.
8. Удерживать автоинжектор плотно прижатым к коже еще несколько секунд для полного введения лекарственного вещества. Осмотрев зону контроля, убедиться, что вся доза препарата введена и контейнер пуст.
Рисунок 20.
9. После окончания инъекции следует извлечь автоинжектор, игла автоматически закроется защитным цилиндром.
Рисунок 21.
10. Сухой стерильной салфеткой/ватным шариком слегка прижать область инъекции, не растирая кожу. Из места инъекции может выделиться небольшое количество крови. При необходимости можно воспользоваться пластырем.
11. Ввести вторую дозу препарата Эфлейра® аналогичным образом предпочтительно в ту же анатомическую область при условии, что место последующей инъекции должно быть не ближе 5 см от предыдущей. Время выполнения 2 инъекций не должно превышать 10 мин.
12. После инъекции автоинжектор повторно не использовать.
Утилизация расходного материала
Неиспользованный раствор препарата, использованные шприцы/автоинжекторы, салфетки/ватные тампоны и другие расходные материалы подлежат утилизации с применением закрывающегося, устойчивого к проколам контейнера для острых предметов из пластика или стекла.
Не допускать хранения использованных шприцев/автоинжекторов в местах, доступных для детей.
Рисунок 22.
Побочные действия
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений, связанных с приемом препарата Эфлейра®, имели легкую или среднюю степень тяжести, определяемую по СТСАЕ v.4.03., и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (≤10000).
Инфекционные и инвазии: часто — инфекции верхних дыхательных путей; нечасто — инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Желудочно-кишечные нарушения: нечасто — боль в животе, диарея.
Со стороны печени и желчевыводящих путей: нечасто — гипербилирубинемия.
Со стороны кожи и подкожной клетчатки: нечасто — экзема, дерматит, сыпь, зуд, крапивница.
Со стороны крови и лимфатической системы: часто — нейтропения, лейкопения, лимфоцитоз; нечасто — тромбоцитопения, лимфопения.
Со стороны иммунной системы: нечасто — гиперчувствительность.
Со стороны органа зрения: нечасто — эписклерит.
Со стороны нервной системы: нечасто — головная боль, головокружение, парестезия, поражение лицевого нерва.
Со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Со стороны сосудов: нечасто — гипертензия (в т.ч. изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**.
Нарушения метаболизма и питания: нечасто — гипергликемия.
Со стороны почек и мочевыводящих путей: нечасто — протеинурия.
Лабораторные и инструментальные данные: часто — повышение активности АЛТ, АСТ, положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто — повышение ГГТ, повышение уровня Хс в крови, увеличение веса.
Травмы, интоксикации и осложнения процедур: нечасто — головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто — инфицированный невус.
Со стороны репродуктивной системы и молочных желез: нечасто — фиброзно-кистозная болезнь молочных желез.
*Гриппоподобное заболевание характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
**Местные реакции могут включать в себя любые неблагоприятные проявления, возникающие в месте инъекции.
Взаимодействие
Сведений о наличии неблагоприятных лекарственных взаимодействий нетакимаба с другими лекарственными препаратами до настоящего времени не получено.
Предполагается, что препарат нетакимаб может усиливать иммуносупрессивное действие ГКС, метотрексата, сульфасалазина, лефлуномида и других базисных противовоспалительных препаратов.
Смешивание препарата с другими ЛС, введение в виде инфузии строго запрещено.
Передозировка
Клинические данные о передозировке отсутствуют. Максимальная переносимая доза для человека не установлена. В клинических исследованиях явлений дозолимитирующей токсичности не зарегистрировано: при п/к введении нетакимаба в максимальной дозе 3 мг/кг (195–355 мг для взрослого человека с весом 65–85 кг) патологических отклонений не было выявлено.
Лечение: симптоматическое. Специфический антидот отсутствует.
Особые указания
Наличие таких потенциально тяжелых инфекций, как ВИЧ, активный гепатит В и/или С, сифилис, туберкулез, относится к противопоказаниям для назначения нетакимаба. Применение нетакимаба у данной группы больных не изучено. Учитывая иммуносупрессивное действие нетакимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования. Необходимо проводить скрининг и оценивать соотношение риска и пользы терапии нетакимабом у этих пациентов.
Пациентам с активным туберкулезом терапия препаратом Эфлейра® противопоказана. Перед назначением препарата Эфлейра® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Эфлейра®.
При реактивации гепатита В терапия нетакимабом должна быть прекращена и назначена соответствующая противовирусная терапия.
Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии.
При использовании нетакимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований нетакимаба анафилактических реакций не зарегистрировано, нечасто отмечались реакции гиперчувствительности и крапивница. Однако при использовании других ингибиторов ИЛ-17 крапивница и анафилактические реакции отмечались в редких и очень редких случаях. При возникновении анафилактических или других серьезных аллергических реакций применение препарата Эфлейра® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения нетакимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходим более тщательный мониторинг за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований на данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность. В ходе клинических исследований препарата Эфлейра® при лечении псориаза, псориатического артрита и анкилозирующего спондилита выработка связывающих антител к нетакимабу была зарегистрирована менее чем в 0,5% случаев. Нейтрализующих антител выявлено не было. Полученные данные демонстрируют низкую иммуногенность нетакимаба у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом.
Возраст старше 65 лет. Данные об эффективности и безопасности препарата у пациентов старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Нарушение функций почек и печени. Эффективность и безопасность препарата у данной категории пациентов не изучались.
Дети. Исследование эффективности и безопасности препарата у детей и лиц моложе 18 лет не проводилось.
Вакцинация. Не следует проводить иммунизацию живыми вакцинами в ходе лечения препаратом Эфлейра®, т.к. клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми вакцинами до начала терапии препаратом Эфлейра®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям. Иммунизация инактивированными вакцинами во время терапии нетакимабом должна выполняться с осторожностью.
Влияние на способность управлять транспортными средствами и механизмами. Отсутствуют данные о влиянии препарата Эфлейра® на способность управлять транспортными средствами и работать с машинами и/или механизмами.
Форма выпуска
Раствор для подкожного введения, 60 мг/мл.
Преднаполненные шприцы
По 1 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса. Шприц с одной стороны имеет впаянную иглу для инъекций из нержавеющей стали, которая защищена жестким колпачком. С другой стороны шприц укупорен поршнем, шток которого изготовлен из полипропилена; на конце поршня имеется уплотнитель из бутилкучука, ламинированный фторполимером. На каждый шприц наклеивают самоклеящуюся этикетку.
По 1 шприцу помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ. По 2 контурные ячейковые упаковки помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Автоинжектор
По 1 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса. Шприц с препаратом встроен в пластиковый автоинжектор, состоящий из защитного колпачка, корпуса с прозрачной зоной контроля, верхнего корпуса и кнопки активации. Внутреннее устройство автоинжектора имеет цилиндр, защищающий иглу, и поршень, который через систему механического пуска соединен с кнопкой активации. На каждый автоинжектор наклеивают самоклеящуюся этикетку.
По 1 автоинжектору помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ. По 2 контурные ячейковые упаковки помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Производитель
АО «БИОКАД». 143422, Россия. Московская обл., Красногорский р-н, с. Петрово-Дальнее.
Владелец регистрационного удостоверения. АО «БИОКАД». 198515, Россия. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, 34, лит. А.
Организация, принимающая претензии потребителей. АО «БИОКАД». 198515, Россия. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, 34, лит. А.
Тел.: (812) 380-49-33; факс: (812) 380-49-34.
e-mail: biocad@biocad.ru
Информацию о развитии нежелательных реакций направлять по адресу: safety@biocad.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Эфлейра — инструкция по применению
Синонимы, аналоги
Статьи
Внимательно прочтите эту инструкцию перед тем, как начать прием/использование лекарственного средства.
Сохраните инструкцию, она может потребоваться вновь.
Если у Вас возникли вопросы, обратитесь к врачу.
Это лекарственное средство назначено лично Вам, и его не следует передавать другим лицам, поскольку оно может причинить им вред даже при наличии тех же симптомов, что и у Вас.
Регистрационный номер:
ЛП-005439
Торговое наименование препарата:
Эфлейра®
Международное непатентованное наименование:
нетакимаб
Лекарственная форма:
раствор для подкожного введения
Состав:
1 мл раствора содержит:
Действующее вещество: нетакимаб – 60 мг;
Вспомогательные вещества: натрия ацетата тригидрат – 1,74 мг, трегалозы дигидрат – 80 мг, полоксамер 188 – 0,5 мг, уксусная кислота ледяная – до pH 5,0, вода для инъекций – до 1,0 мл.
Описание:
Прозрачный или слегка опалесцирующий от бесцветного до светло-желтого или светло-желтого с коричневатым оттенком цвета раствор.
Фармакотерапевтическая группа:
Интерлейкина ингибитор
Код АТХ:
L04AC
Фармакологические свойства
Фармакодинамика
Нетакимаб является рекомбинантным гуманизированным моноклональным антителом, в терапевтических концентрациях специфически связывающим интерлейкин-17А (ИЛ-17А), находящийся непосредственно в тканях или в крови и других биологических жидкостях. ИЛ-17А – провоспалительный цитокин, гиперпродукция которого преимущественно обусловлена активацией Th17-лимфоцитов. В рамках врожденного иммунитета ИЛ-17А выполняет защитную роль. При хронических иммуновоспалительных заболеваниях патологическая активация Th17-лимфоцитов и гиперпродукция ИЛ-17 стимулирует Т-клеточный ответ и усиленную продукцию других медиаторов воспаления: ИЛ-1, ИЛ-6, фактора некроза опухоли альфа (ФНО-α), факторов роста (Г-КСФ, ГМ-КСФ) и различных хемокинов.
Нетакимаб обладает высокой термодинамической константой специфического связывания с ИЛ-17А человека. По данным доклинических исследований специфическое связывание нетакимаба в нормальных тканях человека ограничено тканями легкого, тимуса, лимфатического узла, миндалин, что согласуется с данными об экспрессии ИЛ-17 клетками этих тканей.
Применение нетакимаба не сопровождается статистически значимым изменением уровня Т-лимфоцитов и не влияет на уровень и соотношение иммуноглобулинов классов А, G и М.
Специфическая противовоспалительная активность нетакимаба продемонстрирована в тестах in vitro и in vivo. Нетакимаб дозозависимо ингибирует ИЛ-17 и ФНОα-зависимую продукцию интерлейкина-6 на культуре клеток при IC50 40 pM. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (один раз в неделю в течение 4-х недель) подкожное введение нетакимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (суставной хрящ остается интактным, синовиальные оболочки — без признаков поражения и воспалительной реакции, пролиферации синовиоцитов не отмечено).
У больных псориазом использование нетакимаба сопровождается угасанием явлений воспаления и гиперкератоза в коже, достоверным снижением уровня С-реактивного белка и СОЭ. У пациентов с активным анкилозирующим спондилитом и псориатическим артритом на фоне применения нетакимаба отмечается уменьшение симптомов воспаления в позвоночнике, энтезисах и суставах, а также быстрое снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание/распределение
Изменение концентрации нетакимаба после его подкожного введения является дозозависимым (значения Сmax, Cmax-mult, AUC0-t находятся в прямой зависимости от дозы). Препарат характеризуется медленной фазой абсорбции с постепенным линейным нарастанием концентрации в сыворотке крови.
При однократном подкожном введении нетакимаба в дозе 120 мг пациентам с бляшечным псориазом препарат начинал обнаруживаться в сыворотке крови в течение 0,5 — 4 часов после введения; максимальная концентрация нетакимаба (Сmax) составляла 15,1 [7,7-19,3] мкг/мл, время ее достижения – 144 [72-168] ч, AUC0-168 – 1667,8 [932,2-2270,8] (мкг/мл)*ч.
При повторных введениях отмечено накопление препарата в сыворотке крови с ростом концентрации в 1,8-3,6 раза. Максимальная концентрация при многократном введении (Cmax-mult) составляла 33,0 [23,1-44,0] мкг/мл и достигалась (Tmax-mult) через 1680 [672-2016] часов.
Выведение
Характеристики выведения нетакимаба являются типичными для препаратов на основе моноклональных антител: показатели Kel, T½, MRT, Cl не зависят от дозы вводимого препарата, период полувыведения после однократного введения составляет около 16 суток.
Средний клиренс нетакимаба при однократном введении в дозе 120 мг пациентам с бляшечным псориазом составил 1,8 л/сутки.
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Пациенты с почечной и печеночной недостаточностью: фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания к применению
- Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия.
- Лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
- Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию.
Противопоказания
- Гиперчувствительность к нетакимабу, а также к любому из вспомогательных веществ препарата.
- Клинически значимые инфекционные заболевания в острой фазе, включая туберкулез.
- Детский и подростковый возраст до 18 лет.
- Беременность, грудное вскармливание.
С осторожностью
Следует соблюдать осторожность при назначении нетакимаба пациентам с хроническими и рецидивирующими инфекциями или с анамнестическими указаниями на них, в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний, а также после недавно проведенной вакцинации живыми вакцинами.
В связи с ограниченными данными клинических исследований о применении нетакимаба у пациентов в возрасте старше 65 лет, следует соблюдать осторожность при назначении препарата пациентам указанной возрастной группы.
В связи с отсутствием сведений о применении нетакимаба у больных воспалительными заболеваниями кишечника, следует избегать его назначения пациентам с болезнью Крона или язвенным колитом.
Применение при беременности и в период грудного вскармливания
Применение при беременности
При применении нетакимаба у животных не выявлено отрицательного влияния на репродуктивную функцию, эмбриотоксичности или тератогенных эффектов.
Исследований влияния на плод у беременных женщин не проводилось. Препарат противопоказан к применению во время беременности.
Применение при грудном вскармливании
Нет данных о проникновении нетакимаба в грудное молоко. Учитывая, что иммуноглобулины класса G, к которым относится нетакимаб, при циркуляции в крови матери могут выделяться с грудным молоком, применение в период грудного вскармливания противопоказано. Во избежание негативного воздействия на ребенка следует прекратить либо грудное вскармливание, либо терапию, учитывая соотношение риска и пользы для матери и ребенка.
Влияние на фертильность
В исследованиях у животных не обнаружено негативного воздействия нетакимаба на фертильность. Данные о влиянии препарата на фертильность у людей отсутствуют.
Способ применения и дозы
Применение препарата Эфлейра® должно осуществляться под наблюдением врачей, имеющих опыт лечения заболеваний, при которых показан препарат Эфлейра®. После соответствующего обучения возможно самостоятельное введение препарата пациентом при условии динамического наблюдения со стороны лечащего врача. Препарат Эфлейра® может применяться как в стационарных, так и в амбулаторных условиях.
Препарат Эфлейра® вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл препарата с концентрацией 60 мг/мл.
Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая вводится 1 раз в неделю на неделях 0, 1 и 2, затем 1 раз каждые 4 недели.
Лечение активного анкилозирующего спондилита при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели до недели 10 включительно. Далее с недели 14 препарат вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) каждая 1 раз в 4 недели.
| Показание | Разовая доза | Индукция | Поддерживающая терапия |
| Бляшечный псориаз | 120 мг | 0, 1, 2 недели |
1 раз в 4 недели, начиная с недели 6 |
| Анкилозирующий спондилит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 |
| Псориатический артрит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 по неделю 10 включительно, далее 1 раз в 4 недели с недели 14 |
При пропуске очередного введения по любой причине инъекция препарата Эфлейра® должна быть произведена как можно быстрее. Дата следующего введения рассчитывается исходя из продолжительности задержки с введением препарата: если со времени пропуска введения прошло не более 3 дней, то следующую инъекцию препарата необходимо выполнить по текущему графику, если с момента пропуска введения прошло более 3 дней, то новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Эфлейра®.
Указания по применению
Подготовка к проведению подкожной инъекции

Препарат Эфлейра ® в автоинжекторе
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца/автоинжектора;
- истечения срока годности (годен до…), указанного на картонной пачке, а также на этикетке шприца/автоинжектора.
На данном этапе не следует снимать колпачок шприца/автоинжектора
1. Техника выполнения подкожной инъекции препарата Эфлейра® в преднаполненном шприце
Выбор и подготовка места для инъекции



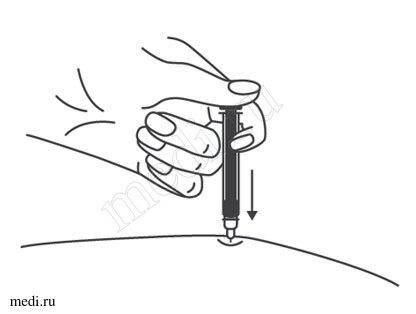
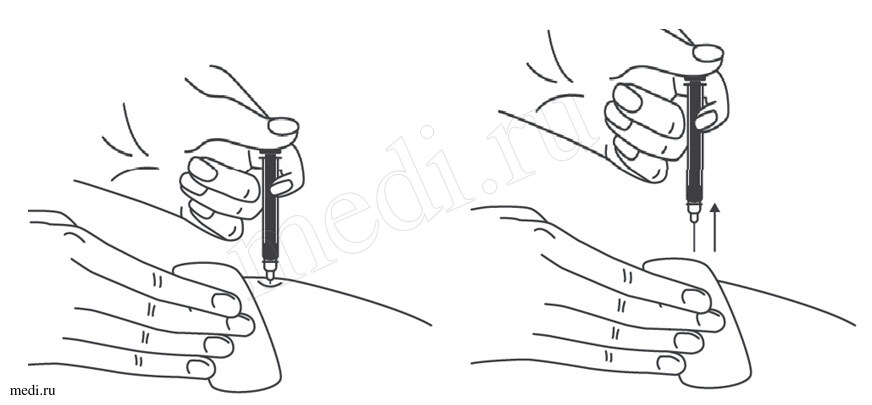
После инъекции шприц повторно не использовать
2. Техника выполнения подкожной инъекции препарата Эфлейра® в автоинжекторе
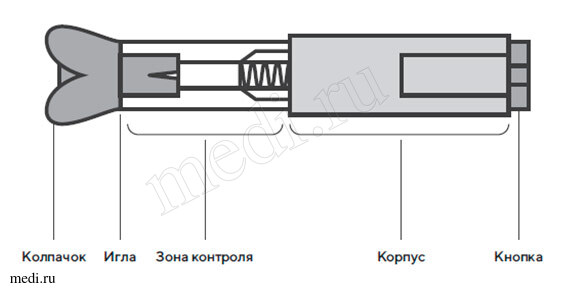
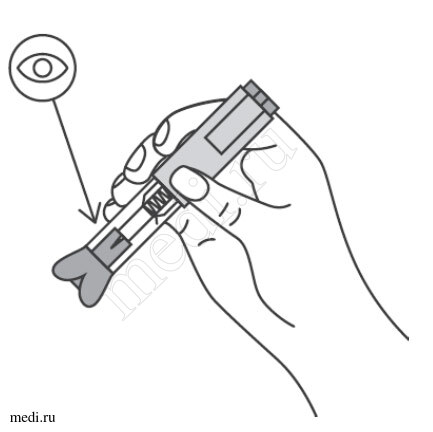



После инъекции автоинжектор повторно не использоватьУтилизация расходного материала

Побочное действие
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений (НЯ), связанных с применением препарата Эфлейра®, имели легкую или среднюю степень тяжести и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000), очень редко (<10000).
Инфекции и инвазии: часто – инфекции верхних дыхательных путей; нечасто – инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Нарушения со стороны печени и желчевыводящих путей: нечасто – гипербилирубинемия.
Желудочно-кишечные нарушения: нечасто – боль в животе, диарея.
Нарушения со стороны кожи и подкожной клетчатки: нечасто – экзема, дерматит, сыпь, зуд, крапивница.
Нарушения со стороны крови и лимфатической системы: часто – нейтропения, лейкопения, лимфоцитоз; нечасто – тромбоцитопения, лимфопения.
Нарушения со стороны иммунной системы: нечасто – гиперчувствительность.
Нарушения со стороны органа зрения: нечасто – эписклерит.
Нарушения со стороны нервной системы: нечасто – головная боль, головокружение, парестезия, поражение лицевого нерва.
Нарушения со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Нарушения со стороны сосудов: нечасто — гипертензия (в том числе изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**.
Нарушения метаболизма и питания: нечасто – гипергликемия.
Нарушения со стороны почек и мочевыводящих путей: нечасто – протеинурия.
Лабораторные и инструментальные данные: часто – повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто – повышение гамма-глутамилтрансферазы (ГГТ), повышение уровня холестерина в крови, увеличение веса.
Травмы, интоксикации и осложнения процедур: нечасто – головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто – инфицированный невус.
Нарушения со стороны репродуктивной системы и молочных желез: нечасто – фиброзно-кистозная болезнь молочных желез.
* «Гриппоподобное заболевание» характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
** Местные реакции могут включать в себя любые неблагоприятные проявления, возникающие в месте инъекции.
Передозировка
Клинические данные о передозировке отсутствуют. Максимальная переносимая доза для человека не установлена. В клинических исследованиях явлений дозолимитирующей токсичности не зарегистрировано: при подкожном введении нетакимаба в максимальной дозе 3 мг/кг (195 – 355 мг для взрослого человека с весом 65 – 85 кг) патологических отклонений не было выявлено.
Специфический антидот отсутствует. Лечение симптоматическое.
Взаимодействие с другими лекарственными средствами
Сведений о наличии неблагоприятных лекарственных взаимодействий нетакимаба с другими лекарственными препаратами до настоящего времени не получено. Предполагается, что нетакимаб может усиливать иммуносупрессивное действие глюкокортикоидов, метотрексата, сульфасалазина, лефлуномида и других базисных противовоспалительных препаратов.
Смешивание препарата с другими лекарственными средствами, введение в виде инфузии строго запрещено.
Особые указания
Наличие таких потенциально тяжелых инфекций как ВИЧ, активный гепатит В и/или С, сифилис, туберкулез, относится к противопоказаниям для назначения нетакимаба. Применение нетакимаба у данной группы больных не изучено. Учитывая иммуносупрессивное действие нетакимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования. Необходимо проводить скрининг и оценивать соотношение риска и пользы терапии нетакимабом у этих пациентов.
Пациентам с активным туберкулезом терапия препаратом Эфлейра® противопоказана. Перед назначением препарата Эфлейра® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Эфлейра®.
При реактивации гепатита В терапия нетакимабом должна быть прекращена и назначена соответствующая противовирусная терапия.
Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии.
При использовании нетакимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований нетакимаба анафилактических реакций не зарегистрировано, нечасто отмечались реакции гиперчувствительности и крапивница. Однако при использовании других ингибиторов ИЛ17 крапивница и анафилактические реакции отмечались в редких и очень редких случаях. При возникновении анафилактических или других серьёзных аллергических реакций применение препарата Эфлейра® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения нетакимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходим более тщательный мониторинг за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований на данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Эфлейра® при лечении псориаза, псориатического артрита и анкилозирующего спондилита выработка связывающих антител к нетакимабу была зарегистрирована менее чем в 0,5 % случаев. Нейтрализующих антител выявлено не было. Полученные данные демонстрируют низкую иммуногенность нетакимаба у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Пациенты моложе 18 лет, дети
Исследование эффективности и безопасности препарата у детей и лиц моложе 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми вакцинами в ходе лечения препаратом Эфлейра®, так как клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми вакцинами до начала терапии препаратом Эфлейра®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям. Иммунизация инактивированными вакцинами во время терапии нетакимабом должна выполняться с осторожностью.
Влияние на способность управлять транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Эфлейра® на способность управлять транспортными средствами и работать с машинами и (или) механизмами.
Форма выпуска
Раствор для подкожного введения 60 мг/мл.
Преднаполненные шприцы
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса. Шприц с одной стороны имеет впаянную иглу для инъекций из нержавеющей стали, которая защищена жестким колпачком. С другой стороны шприц укупорен поршнем, шток которого изготовлен из полипропилена; на конце поршня имеется уплотнитель из бутилкучука, ламинированный фторполимером.
На каждый шприц наклеивают самоклеящуюся этикетку.
По 1 шприцу помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Автоинжектор
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса.
Шприц с препаратом встроен в пластиковый автоинжектор, состоящий из защитного колпачка, корпуса с прозрачной зоной контроля, верхнего корпуса и кнопки активации. Внутреннее устройство автоинжектора имеет цилиндр, защищающий иглу, и поршень, который через систему механического пуска соединен с кнопкой активации.
На каждый автоинжектор наклеивают самоклеящуюся этикетку.
По 1 автоинжектору помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Условия хранения
При температуре от 2 до 8°С в защищенном от света месте. Не замораживать!
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Производитель
ЗАО «БИОКАД», Россия, 143422, Московская обл., Красногорский р-н, с. Петрово-Дальнее.
Владелец регистрационного удостоверения
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Организация, принимающая претензии потребителей
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакологическое действие
Нетакимаб является рекомбинантным гуманизированным моноклональным антителом, в терапевтических концентрациях специфически связывающим интерлейкин-17А (ИЛ-17А), находящийся непосредственно в тканях или в крови и других биологических жидкостях. ИЛ-17А – провоспалительный цитокин, гиперпродукция которого преимущественно обусловлена активацией Th17-лимфоцитов. В рамках врожденного иммунитета ИЛ-17А выполняет защитную роль. При хронических иммуновоспалительных заболеваниях патологическая активация Th17-лимфоцитов и гиперпродукция ИЛ-17 стимулирует Т-клеточный ответ и усиленную продукцию других медиаторов воспаления: ИЛ-1, ИЛ-6, ФНОα, факторов роста (Г-КСФ, ГМ-КСФ) и различных хемокинов.
Нетакимаб обладает высокой термодинамической константой специфического связывания с ИЛ-17А человека. По данным доклинических исследований специфическое связывание нетакимаба в нормальных тканях человека ограничено тканями легкого, тимуса, лимфатического узла, миндалин, что согласуется с данными об экспрессии ИЛ-17 клетками этих тканей.
Применение нетакимаба не сопровождается статистически значимым изменением уровня Т-лимфоцитов и не влияет на уровень и соотношение иммуноглобулинов классов А, G и М.
Специфическая противовоспалительная активность нетакимаба продемонстрирована в тестах in vitro и in vivo. Нетакимаб дозозависимо ингибирует ИЛ-17 и ФНОα-зависимую продукцию ИЛ-6 на культуре клеток при IC50 40 pM. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (1 раз в неделю в течение 4 недель) п/к введение нетакимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (суставной хрящ остается интактным, синовиальные оболочки — без признаков поражения и воспалительной реакции, пролиферации синовиоцитов не отмечено).
У больных псориазом использование нетакимаба сопровождается угасанием явлений воспаления и гиперкератоза в коже, достоверным снижением уровня С-реактивного белка и СОЭ.
У пациентов с активным анкилозирующим спондилитом и псориатическим артритом на фоне применения нетакимаба отмечается уменьшение симптомов воспаления в позвоночнике, энтезисах и суставах, а также быстрое снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание/распределение
Изменение концентрации нетакимаба после п/к введения препарата является дозозависимым (значения Сmax, Cmax—mult, AUC0-t находятся в прямой зависимости от дозы). Препарат характеризуется медленной фазой абсорбции с постепенным линейным нарастанием концентрации в сыворотке крови.
При однократном п/к введении нетакимаба в дозе 120 мг пациентам с бляшечным псориазом препарат начинал обнаруживаться в сыворотке крови в течение 0.5-4 ч после введения; Сmax составляла 15.1 (7.7-19.3) мкг/мл, Тmax – 144 (72-168) ч, AUC0-168 – 1667.8 (932.2–2270.8) (мкг/мл)×ч.
При повторных введениях отмечено накопление препарата в сыворотке крови с ростом концентрации в 1.8-3.6 раза. Максимальная концентрация при многократном введении (Cmax-mult) составляла 33.0 (23.1-44.0) мкг/мл и достигалась (Tmax—mult) через 1680 (672-2016) ч.
Выведение
Характеристики выведения нетакимаба являются типичными для препаратов на основе моноклональных антител: показатели Kel, T1/2, MRT, Cl не зависят от дозы вводимого препарата. Т1/2 после однократного введения составляет около 16 суток.
Средний клиренс нетакимаба при однократном введении в дозе 120 мг пациентам с бляшечным псориазом составил 1.8 л/сут.
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Фармакокинетика в особых клинических случаях
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Пациенты с почечной и печеночной недостаточностью: фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания препарата
Эфлейра®
- лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия;
- лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию;
- лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию.
Режим дозирования
Применение препарата Эфлейра® должно осуществляться под наблюдением врачей, имеющих опыт лечения заболеваний, при которых показан препарат Эфлейра®. После соответствующего обучения возможно самостоятельное введение препарата пациентом при условии динамического наблюдения со стороны лечащего врача.
Препарат Эфлейра® можно применять как в стационарных, так и в амбулаторных условиях.
Препарат вводят в дозе 120 мг в виде двух п/к инъекций по 1 мл препарата с концентрацией 60 мг/мл.
Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия
Рекомендуемая доза — 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата, каждая вводится 1 раз в неделю на неделях 0, 1 и 2, затем 1 раз каждые 4 недели.
Лечение активного анкилозирующего спондилита при недостаточном ответе на стандартную терапию
Рекомендуемая доза — 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию
Рекомендуемая доза — 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели до недели 10 включительно. Далее с недели 14 препарат вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) каждая 1 раз в 4 недели.
При пропуске очередного введения по любой причине инъекция препарата Эфлейра® должна быть произведена как можно быстрее. Дата следующего введения рассчитывается исходя из продолжительности задержки с введением препарата: если со времени пропуска введения прошло не более 3 дней, следующую инъекцию препарата необходимо выполнить по текущему графику, если с момента пропуска дозы прошло более 3 дней, то новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Эфлейра®.
Указания по применению
Подготовка к проведению п/к инъекции
Тщательно вымыть руки.
Достать упаковку с двумя шприцами/автоинжекторами с препаратом Эфлейра® из холодильника, затем извлечь из картонной пачки и ячейковой упаковки два шприца/автоинжектора и положить на чистую поверхность. Убедиться, что срок хранения препарата, указанный на картонной пачке и шприце/автоинжекторе не истек.
Препарат Эфлейра® в преднаполненном шприце
Препарат Эфлейра® в автоинжекторе
Осмотреть шприцы/автоинжекторы, а также лекарственный препарат, находящийся в них. Препарат Эфлейра® представляет собой прозрачный, от бесцветного до светло-желтого цвета раствор. Нельзя использовать препарат в случае:
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца/автоинжектора;
- истечения срока годности (годен до…), указанного на картонной пачке, а также на этикетке шприца/автоинжектора.
Перед введением шприцы/автоинжекторы с препаратом Эфлейра® следует довести до комнатной температуры, для этого необходимо оставить шприц при комнатной температуре в течение приблизительно 25-30 мин. Не следует согревать шприц/автоинжектор каким-либо другим способом.
Подготовить салфетку/ватный тампон, спиртовой раствор.
На данном этапе не следует снимать колпачок шприца/автоинжектора.
Техника выполнения п/к инъекции препарата Эфлейра® в преднаполненном шприце
Выбор и подготовка места для инъекции
Выбрать место инъекции (передняя брюшная стенка (отступая не менее 5 см от пупка), передняя и боковая поверхность бедра или средняя треть наружной части плеча (возможные места для инъекций закрашены на рисунке ниже)).
Места инъекций и стороны следует менять при каждой последующей инъекции. Расстояние между двумя введениями должно составлять как минимум 5 см.
Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек (эти признаки могут указывать на наличие инфекции). По возможности не следует вводить препарат в псориатическую бляшку.
Место для укола необходимо обработать спиртовой салфеткой/ватным тампоном круговыми движениями.
Шприц не встряхивать.
Снять колпачок с иглы, не дотрагиваясь до иглы и избегая ее прикосновения к другим поверхностям.
Большим и указательным пальцами одной руки взять в складку обработанную кожу.
В другую руку взять шприц, держа его градуированной поверхностью вверх. Введение препарата необходимо осуществлять под углом 45 или 90 градусов к поверхности кожи в зависимости от толщины кожи и выраженности подкожно-жирового слоя (у худощавых пациентов введение препарата осуществляется под углом 45 градусов, у пациентов с толщиной кожной складки более 1.5 см допустимо введение под углом 90 градусов).
Одним быстрым движением полностью ввести иглу в кожную складку.
После введения иглы складку кожи следует отпустить.
Ввести весь раствор медленным постоянным надавливанием на поршень шприца в течение 2-5 сек.
Когда шприц будет пустым, вынуть иглу из кожи под тем же углом.
Сухой стерильной салфеткой/ватным шариком слегка прижать область инъекции, но не растирать. Из места инъекции может выделиться небольшое количество крови. При необходимости можно воспользоваться пластырем.
Ввести вторую дозу препарата Эфлейра® аналогичным образом предпочтительно в ту же анатомическую область при условии, что место последующей инъекции должно быть не ближе 5 см от предыдущей. Время выполнения двух инъекций не должно превышать 10 мин.
После инъекции шприц повторно не использовать.
Техника выполнения п/к инъекции препарата Эфлейра® в автоинжекторе
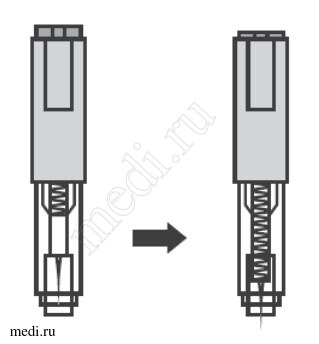
Устройство автоинжектора:
Автоинжектор не встряхивать.
Не следует снимать защитный колпачок с автоинжектора до выполнения инъекции.
Необходимо проверить срок годности препарата по маркировке на упаковке, оценить целостность автоинжектора и состояние раствора через зону контроля автоинжектора. Не следует использовать автоинжектор в случае его повреждения, изменения цвета и прозрачности раствора, а также при истечении срока годности.
Разместить автоинжектор на чистой горизонтальной поверхности.
Выбрать место введения (область брюшной стенки (отступая не менее 5 см от пупка) или передняя поверхность бедра) и обработать кожу в области введения спиртовой салфеткой.
Непосредственно перед инъекцией одной рукой снять колпачок с автоинжектора, удерживая другой рукой его корпус.
Одной рукой взять в складку обработанную спиртовой салфеткой кожу и удерживать в течение всей процедуры инъекции.
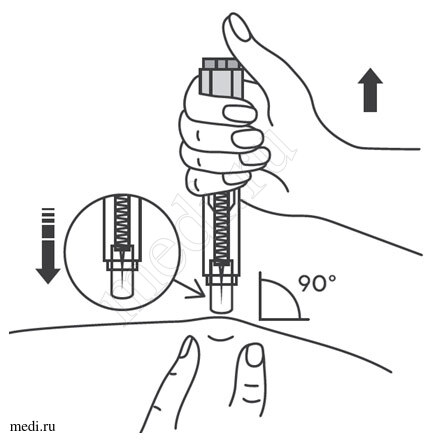
В другую руку взять автоинжектор, удерживая его за корпус. Введение препарата необходимо осуществлять, плотно прижав автоинжектор под углом 90 градусов к поверхности кожи. Надавливание автоинжектором на поверхность кожной складки приведет к разблокированию кнопки.
Удерживая автоинжектор под углом 90 градусов к поверхности кожной складки, надавить до упора на кнопку автоинжектора. Послышится щелчок, указывающий на начало инъекции. Не следует изменять положение автоинжектора. Необходимо удерживать кнопку в течение 10 сек до окончания инъекции.
Если инъекция не запустилась, следует отпустить кнопку и проверить, плотно ли прижат автоинжектор к кожной складке. Необходимо прижать плотно автоинжектор к коже и повторить процедуру инъекции, вновь нажав на кнопку.
Следует удерживать автоинжектор плотно прижатым к коже еще несколько секунд для полного введения лекарственного вещества. Осмотрев зону контроля, необходимо убедиться, что вся доза препарата введена и контейнер пуст.
После окончания инъекции извлечь автоинжектор, игла автоматически закроется защитным цилиндром.
Сухой стерильной салфеткой/ватным шариком слегка прижать область инъекции, но не растирать область выполненной инъекции. Из места инъекции может выделиться небольшое количество крови. При необходимости можно воспользоваться пластырем.
Ввести вторую дозу препарата Эфлейра® аналогичным образом предпочтительно в ту же анатомическую область при условии, что место последующей инъекции должно быть не ближе 5 см от предыдущей. Время выполнения двух инъекций не должно превышать 10 мин.
После инъекции автоинжектор повторно не использовать.
Утилизация расходного материала
Неиспользованный раствор препарата, использованные шприцы/автоинжекторы, салфетки/ватные тампоны и другие расходные материалы подлежат утилизации с применением закрывающегося, устойчивого к проколам контейнера для острых предметов из пластика или стекла. Не допускать хранения использованных шприцев/автоинжекторов в местах, доступных для детей.
Побочное действие
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений, связанных с приемом препарата Эфлейра®, имели легкую или среднюю степень тяжести и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (≤10000).
Инфекции и инвазии: часто – инфекции верхних дыхательных путей; нечасто – инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Со стороны печени и желчевыводящих путей: часто — гипербилирубинемия.
Со стороны ЖКТ: нечасто — боль в животе, диарея.
Со стороны кожи и подкожной клетчатки: нечасто – экзема, дерматит, сыпь, зуд, крапивница.
Со стороны крови и лимфатической системы: часто — нейтропения, лейкопения, лимфоцитоз; нечасто – тромбоцитопения, лимфопения.
Со стороны иммунной системы: нечасто — гиперчувствительность.
Со стороны органа зрения: нечасто – эписклерит.
Со стороны нервной системы: нечасто — головная боль, головокружение, парестезия, поражение лицевого нерва.
Со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Со стороны сосудов: нечасто — гипертензия (в т.ч. изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**
Со стороны метаболизма и питания: нечасто – гипергликемия.
Со стороны почек и мочевыводящих путей: нечасто — протеинурия.
Лабораторные и инструментальные данные: часто – повышение активности АЛТ, АСТ, положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто – повышение ГГТ, повышение уровня холестерина в крови, увеличение массы тела.
Травмы, интоксикации и осложнения процедур: нечасто – головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто – инфицированный невус.
Со стороны репродуктивной системы и молочных желез: нечасто – фиброзно-кистозная болезнь молочных желез.
* Гриппоподобное заболевание характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры тела, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
** Местные реакции могут включать любые неблагоприятные проявления, возникающие в мете инъекции.
Противопоказания к применению
- гиперчувствительность к нетакимабу, а также к любому из вспомогательных веществ препарата;
- клинически значимые инфекционные заболевания в острой фазе, включая туберкулез;
- детский и подростковый возраст до 18 лет;
- беременность;
- период грудного вскармливания.
С осторожностью
Следует соблюдать осторожность при назначении препарата пациентам с хроническими и рецидивирующими инфекциями или с указаниями на них в анамнезе, в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний, а также после недавно проведенной вакцинации живыми вакцинами.
В связи с ограниченными данными клинических исследований о применении нетакимаба у пациентов в возрасте старше 65 лет следует соблюдать осторожность при назначении препарата пациентам указанной возрастной группы.
В связи с отсутствием сведений о применении нетакимаба у больных воспалительными заболеваниями кишечника следует избегать его назначения пациентам с болезнью Крона или язвенным колитом.
Применение при беременности и кормлении грудью
Беременность
При применении нетакимаба у животных не выявлено отрицательного влияния на репродуктивную функцию, эмбриотоксичности или тератогенных эффектов. Исследований влияния на плод у беременных женщин не проводилось. Препарат противопоказан к применению во время беременности.
Грудное вскармливание
Нет данных о выделении нетакимаба с грудным молоком. Учитывая, что иммуноглобулины класса G, к которым относится нетакимаб, при циркуляции в крови матери могут выделяться с грудным молоком, применение в период грудного вскармливания противопоказано. Во избежание негативного воздействия на ребенка следует прекратить либо грудное вскармливание, либо терапию, учитывая соотношение риска и пользы для матери и ребенка.
Фертильность
В исследованиях у животных не обнаружено негативного воздействия нетакимаба на фертильность. Данные о влиянии препарата на фертильность у человека отсутствуют.
Применение при нарушениях функции печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Применение при нарушениях функции почек
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Применение у детей
Противопоказано применение препарата в возрасте до 18 лет.
Применение у пожилых пациентов
В связи с ограниченными данными клинических исследований о применении нетакимаба у пациентов в возрасте старше 65 лет следует соблюдать осторожность при назначении препарата пациентам указанной возрастной группы.
Особые указания
Наличие таких потенциально тяжелых инфекций, как ВИЧ, активный гепатит В и/или С, сифилис, туберкулез, относится к противопоказаниям для назначения нетакимаба. Применение нетакимаба у данной группы пациентов не изучено. Учитывая иммуносупрессивное действие нетакимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования. Необходимо проводить скрининг и оценивать соотношение риска и пользы терапии нетакимабом у этих пациентов.
Пациентам с активным туберкулезом терапия препаратом Эфлейра® противопоказана. Перед назначением препарата Эфлейра® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Эфлейра®.
При реактивации гепатита В лечение нетакимабом следует прекратить и назначить соответствующую противовирусную терапию.
Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии.
При применении нетакимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований нетакимаба анафилактические реакции не зарегистрированы, нечасто отмечались реакции гиперчувствительности и крапивница. Однако при применении других ингибиторов ИЛ-17 крапивница и анафилактические реакции отмечались в редких и очень редких случаях. При возникновении анафилактических или других серьезных аллергических реакций применение препарата Эфлейра® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения нетакимабом, что, в свою очередь, может привести к снижению эффективности терапии. Необходим более тщательный мониторинг за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований на данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Эфлейра® при лечении псориаза, псориатического артрита и анкилозирующего спондилита формирование связывающих антител к нетакимабу было зарегистрировано менее чем в 0.5% случаев. Нейтрализующих антител выявлено не было. Полученные данные демонстрируют низкую иммуногенность нетакимаба у пациентов с псориазом, псориатическим артритом и пациентов с анкилозирующим спондилитом.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Использование в педиатрии
Исследование эффективности и безопасности препарата у детей и подростков в возрасте до 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми вакцинами в ходе лечения препаратом Эфлейра®, т.к. клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми вакцинами до начала терапии препаратом Эфлейра®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям. Иммунизацию инактивированными вакцинами во время терапии нетакимабом необходимо выполнять с осторожностью.
Влияние на способность к управлению транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Эфлейра® на способность управлять транспортными средствами и работать с машинами и/или механизмами.
Передозировка
Клинические данные о передозировке отсутствуют. Максимальная переносимая доза для человека не установлена. В клинических исследованиях явлений дозолимитирующей токсичности не зарегистрировано: при п/к введении препарата нетакимаб в максимальной дозе 3 мг/кг (195–355 мг для взрослого человека с массой тела 65–85 кг) патологических отклонений не было выявлено.
Лечение: специфический антидот отсутствует; проводят симптоматическую терапию.
Лекарственное взаимодействие
Сведений о наличии неблагоприятного лекарственного взаимодействия нетакимаба с другими лекарственными препаратами до настоящего времени не получено. Предполагается, что нетакимаб может усиливать иммуносупрессивное действие ГКС, метотрексата, сульфасалазина, лефлуномида и других базисных противовоспалительных препаратов.
Смешивание препарата с другими лекарственными средствами и введение в виде инфузии строго запрещено.
Условия хранения препарата Эфлейра®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Эфлейра®
Срок годности — 2 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускается по рецепту.
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений (НЯ), связанных с применением препарата Эфлейра®, имели легкую или среднюю степень тяжести и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (≤10000).
Инфекции и инвазии: часто – инфекции верхних дыхательных путей; нечасто – инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Нарушения со стороны печени и желчевыводящих путей: нечасто – гипербилирубинемия.
Желудочно-кишечные нарушения: нечасто – боль в животе, диарея.
Нарушения со стороны кожи и подкожной клетчатки: нечасто – экзема, дерматит, сыпь, зуд, крапивница.
Нарушения со стороны крови и лимфатической системы: часто – нейтропения, лейкопения, лимфоцитоз; нечасто – тромбоцитопения, лимфопения.
Нарушения со стороны иммунной системы: нечасто – гиперчувствительность.
Нарушения со стороны органа зрения: нечасто – эписклерит.
Нарушения со стороны нервной системы: нечасто – головная боль, головокружение, парестезия, поражение лицевого нерва.
Нарушения со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Нарушения со стороны сосудов: нечасто — гипертензия (в том числе изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**.
Нарушения метаболизма и питания: нечасто – гипергликемия.
Нарушения со стороны почек и мочевыводящих путей: нечасто – протеинурия.
Лабораторные и инструментальные данные: часто – повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто – повышение гамма-глутамилтрансферазы (ГГТ), повышение уровня холестерина в крови, увеличение веса.
Травмы, интоксикации и осложнения процедур: нечасто – головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто – инфицированный невус.
Нарушения со стороны репродуктивной системы и молочных желез: нечасто – фиброзно-кистозная болезнь молочных желез.
*«Гриппоподобное заболевание» характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
**Местные реакции могут включать в себя любые неблагоприятные проявления, возникающие в месте инъекции.
ЭФЛЕЙРА › Нетакимаб – подавляющий иммунитет биопрепарат для лечения тяжёлого и среднетяжёлого бляшечного псориаза, когда показаны ультрафиолетовая или системная (таблетки, капсулы, инъекции) терапия.
Эфлейра выпускается в форме раствора для подкожного введения (60 мг Нетакимаба в 1 мл). В одной упаковке находятся два уже заполненных шприца (по 1 мл каждый) в автоинжекторах („ручках“ для автоматических уколов).
Обновлено: 08-02-2023
Содержание
МЕХАНИЗМ ДЕЙСТВИЯ
- Активный компонент биопрепарата Эфлейра?
- Откуда возникает ИЛ-17А в организме? Какую роль играет?
- К чему ведёт избыток ИЛ-17А при псориазе?
- Насколько сильно Эфлейра (Нетакимаб) блокирует ИЛ-17А?
АНАЛОГИ
- В аптеках России какие ещё имеются в наличии ингибиторы интерлейкина (аналоги), предназначенные для лечения псориаза? Их цена?
- Козэнтикс или Талс более действенны, чем Эфлейра?
- Если у пациента есть финансовая возможность купить любой ингибитор ИЛ-17А, то Вы ему всё равно назначите Эфлейру?
КАК ПРОВОДИТСЯ ЛЕЧЕНИЕ ПСОРИАЗА КОЖИ
- Что включают 2 этапа лечения биопрепаратом Эфлейра?
- Разовая доза?
- Длительность лечения?
- Можно вводить моноклональное антитело Нетакимаб реже, чем 1 раз в 4 недели?
- Где лучше делать первые инъекции биопрепарата Эфлейра?
ЭФФЕКТИВНОСТЬ
- Эфлейра излечивает псориаз?
- Насколько эффективен Нетакимаб для лечения псориаза?
- Может ли со временем пропадать эффект от лечения псориаза биопрепаратом Эфлейра?
- По отзывам, через какое время обычно возникает рецидив псориаза у большинства пациентов после прекращения лечения Эфлейрой?
БЕЗОПАСНОСТЬ
- Согласно инструкции, пока какие побочные действия зафиксированы у больных псориазом, которым проводили инъекции биопрепарата Эфлейра?
- Как именно может проявиться аллергическая реакция (гиперчувствительность) после введения Эфлейры?
- При возникновении каких симптомов инфекции нужно прекратить лечение моноклональным антителом Нетакимаб и срочно обратиться к врачу?
- Нетакимаб избирательно, но всё равно угнетает иммунитет… Может ли это привести к возникновению рака?
- Эфлейра (Нетакимаб) может вызвать избыточный вес (ожирение)?
- Прекращать ли лечение биопрепаратом Эфлейра (Нетакимаб) перед хирургической операцией?
ПЕРЕД НАЧАЛОМ ЛЕЧЕНИЯ
- Что нужно обязательно сообщить врачу (что должен узнать врач) при рассмотрении возможности лечения псориаза биопрепаратом Эфлейра?
- Какие анализы крови нужно провести перед планированием лечения псориаза биопрепаратом Нетакимаб (или другим ингибитором интерлейкина 17А)?
- Нужно ли провериться на туберкулёз перед лечением биопрепаратом Эфлейра?
- Перед лечением биологическим препаратом Эфлейра (Нетакимаб) обязательно ли проводить УЗИ органов брюшной полости + (женщинам) УЗИ малого таза, эзофагогастродуоденоскопию (ФГДС)?
- Требуется ли вакцинация?
ПОКУПКА, ЦЕНА
- Эфлейру можно купить без рецепта?
- Как купить лекарство Эфлейра с максимальной скидкой (25%)?
- Во сколько обойдётся лечение псориаза этим иммунодепрессантом в первые 6 недель?
- Начиная с 7-й недели?
- Сколько упаковок биопрепарата Эфлейра нужно купить для проведения лечения псориаза кожи на протяжении первых 12 недель?
- Как получить социальный вычет по НДФЛ (минус 13% – минимум 1950 р. за пачку) на биопрепарат Эфлейра?
- Что делать, если сейчас из-за высокой цены я не могу купить биологический препарат Эфлейра (Нетакимаб) или Малую молекулу?
ХРАНЕНИЕ И ПЕРЕВОЗКА
- Как можно испортить Эфлейру (или другой биопрепарат)?
- Сколько времени можно перевозить биопрепарат Эфлейра в термопакете с хладоэлементом?
- В аптеке мне выдадут в чём перевозить Эфлейру?
СРАВНЕНИЕ С «МАЛЫМИ МОЛЕКУЛАМИ» И ТРЕМФЕЕЙ
- Таблетки для лечения псориаза Отесла менее эффективны, чем Эфлейра?
- Таблетки Яквинус в сравнении с Эфлейрой?
- Нетакимаб лучше, чем Тремфея (ингибитор ИЛ-23)?
- Как перейти с лечения псориаза биологическим препаратом Эфлейра (Нетакимаб) на более совершенный биологический препарат Тремфея (Гуселькумаб)?
РАЗНОЕ
- Можно ли ставить прививку для профилактики коронавируса („КОВИД-19“) при лечении псориаза препаратом ЭФЛЕЙРА (Нетакимаб)?
- Какие сайты продвигают биологический препарат Эфлейра (Нетакимаб)?
- Почему на официальном сайте препарата Эфлейра (Нетакимаб) ни разу не указано, что он относится к группе лекарственных средств, подавляющих иммунитет (иммунодепрессантов, иммуносупрессантов)?
- Когда показаны ультрафиолетовая или системная (таблетки, капсулы, инъекции) терапия псориаза?
- Где производится Эфлейра?
- Нетакимаб – генно-инженерное лекарственное средство?
- Нетакимаб одобрен FDA?
- При каких инфекциях противопоказан биопрепарат Эфлейра?
- Если у меня только псориаз ногтей или ладонно-подошвенный или каплевидный псориаз, при отсутствии противопоказаний дерматолог может назначить мне биопрепарат Эфлейра?
- Где почитать краткую инструкцию иммунодепрессанта Эфлейра?
- Как можно будет получить бесплатное лечение Эфлейрой?
- У меня поднялась температура от инфекции (гриппа, простуды, воспаления лёгких). Можно ли мне проводить инъекцию биопрепарата Эфлейра?
- Хочу поставить прививку от гриппа. Это возможно во время курса лечения препаратом Эфлейра?
- Как ожирение может повлиять на эффективность лечения псориаза биопрепаратом Эфлейра?
- Через какой промежуток времени после последней инъекции биопрепарата Эфлейра можно начать лечение псориаза другим биологическим биопрепаратом?
- Можно ли лечить псориаз у детей биопрепаратом Эфлейра?
- Что такое PASI 75?
- За эту веб-страницу и/или за назначения биопрепарата Эфлейра Вы получали денежные средства, подарки?
- Как можно поблагодарить Вас за информацию о препарате Эфлейра (Нетакимаб)?
- Для повышения эффективности лечения псориаза с чем ещё можно сочетать применение биопрепарата Эфлейра?
- Где почитать про биологическую терапию псориаза?
ЛИТЕРАТУРА
ОТВЕТЫ НА ПРИСЛАННЫЕ ВОПРОСЫ
Механизм действия
Активный компонент биопрепарата Эфлейра?
Нетакимаб – моноклональное антитело, которое ингибирует (связывает/блокирует/нейтрализует) вещество, вызывающее воспаление в поражённой псориазом коже и суставах – ИнтерЛейкин-17А (ИЛ-17А). (Inhibition – подавление.)
Откуда возникает ИЛ-17А в организме? Какую роль играет?
ИЛ-17А синтезируют клетки иммунной системы (Th17). ИЛ-17А защищает организм от инфекций на слизистых оболочках (например, грибов рода Candida, нередко вызывающих „молочницу“), по-разному влияет на злокачественные новообразования (может способствовать как прогрессированию, так и подавлять их развитие). При псориазе и некоторых других заболеваниях слишком много ИЛ-17А.
К чему ведёт избыток ИЛ-17А при псориазе?
К возникновению воспаления, признаки (симптомы) которого на коже следующие: очаги с покраснением, утолщением/инфильтрацией, шелушением. Клетки кожи имеют рецепторы к ИЛ-17А. Установлено, что чем больше ИЛ-17А в крови, тем тяжелей псориаз (PASI). Блокада ИЛ-17А приводит к снижению скорости деления клеток кожи поверхностного слоя кожи (эпидермиса), уменьшению количества воспалительных иммунных T-клеток в глубоком слое кожи (дерме), уменьшает экспрессию (проявление) генов псориаза.
Psoriasis and beyond: targeting the IL-17 pathway
Насколько сильно Эфлейра (Нетакимаб) блокирует ИЛ-17А?
Неизвестно (в инструкции не написано). Не исключено, что если Эфлейра заблокирует слишком много ИЛ-17А, то это может способствовать возникновению тяжёлых заболеваний (в том числе рака). Поэтому рационально было бы до и в процессе лечения псориаза проводить исследование сыворотки крови для определения активного и связанного/заблокированного моноклональным антителом Нетакимаб интерлейкина, и, учитывая эффект от терапии, персонально подбирать каждому пациенту дозу и частоту введения биопрепарата (это уменьшит цену лечения для многих пациентов). По аналогии, если пациенту с низким сердечно-сосудистым риском достаточно 1 таблетки для контроля артериального давления, зачем принимать две, что может вызвать слишком низкое давление (следствием чего, как установлено, могут стать инсульты и инфаркты)? Производителям ГИБП экономически невыгодна такая персонализированная медицина.
↑ Содержание
Аналоги
В аптеках России какие ещё имеются в наличии ингибиторы интерлейкина (аналоги), предназначенные для лечения псориаза? Их цена?
- Раствор для подкожного введения Козэнтикс (активное вещество: Секукинумаб) производства Швейцарии. Стоимость* разовой дозы (2 шприца по 150 мг) в аптеках около 80 000 ₽.
- Раствор для подкожного введения Талс (активное вещество: Иксекизумаб) производства США. Цена* первой разовой дозы (2 шприца по 80 мг) составляет ориентировочно 162 000 ₽.
- Раствор для подкожного введения Стелара (активное вещество: Устекинумаб) производства Швейцарии. Цена* разовой дозы (1 шприц 45 мг) приблизительно 215 000 ₽.
*Стоимость первого месяца лечения псориаза ингибиторами интерлейкина (до 24-фев-2022)
| Козэнтикс | 8 инъекций | ~ 320 000 р. (без скидки) |
| Талс | 4 инъекции | ~ 325 000 р. |
| Стелара | 2 инъекции | ~ 430 000 р. |
| Эфлейра | 6 инъекций | 15 000 р. (со скидкой) |
Стоимость ежемесячного лечения псориаза спустя 12 недель после его начала*
| Козэнтикс | 2 инъекции | ~ 80 000 р. (без скидки) |
| Талс | 1 инъекция | ~ 81 000 р. |
| Эфлейра | 2 инъекции | 15 000 р. (со скидкой) |
Козэнтикс или Талс более действенны, чем Эфлейра?
При непрямом сравнении Талс больше всего очищает кожу от псориаза, лечебная эффективность биопрепаратов Эфлейра и Козэнтикс примерно одинаковая.
По отзывам дерматологов, скорость очищения кожи от псориаза при использовании ингибиторов ИЛ-17А наиболее быстрая (в отличие от ингибитора ИЛ-23 › биопрепарата Тремфея или, тем более, „старого“ биопрепарата, ингибирующего ИЛ-12 и ИЛ-23 › Стелара).
Если у пациента есть финансовая возможность купить любой ингибитор ИЛ-17А, то Вы ему всё равно назначите Эфлейру?
Разумеется, что нет. Если есть финансовая возможность, всегда выбирайте лекарственные средства, не изготовленные в таких странах, как Китай, Индия или Россия. Для достижения быстрого лечебного эффекта может быть вначале назначен больше изученный (чем Эфлейра) в отношении эффективности и побочных действий, долгосрочности действия ингибитор ИЛ-17А европейского или американского производства: Козэнтикс или Талс (на данный наиболее эффективный ингибитор ИЛ-17А в России), а затем – более совершенное моноклональное антитело – ингибитор ИЛ-23 (Тремфея или ещё лучше Скайризи).
У многих пациентов спустя более года лечения происходит „привыкание“ к препарату Эфлейра (Нетакимаб), чего не отмечается у больных псориазом, которые вводили зарубежный ингибитор интерлейкина…
↑ Содержание
 Как проводится лечение псориаза кожи
Как проводится лечение псориаза кожи
Что включают 2 этапа лечения биопрепаратом Эфлейра?
1-й этап (индукция, нагрузочная доза) → В первые 15 дней проводятся 3 введения биопрепарата 1 раз в неделю (⓿, ❶ и ❷ недели; например, в три понедельника подряд).
2-й этап (поддержание) → Начиная с ❻-й недели с момента первого (то есть спустя 4 недели после предыдущего) введения осуществляется 1 введение в 4 недели.
Разовая доза?
Разовая доза = 120 мг Нетакимаба = Одна упаковка биопрепарата Эфлейра (с 2-мя шприцами) = 1 введение = 2 последовательные инъекции по 1 мл.
Длительность лечения?
Раствор Эфлейра можно вводить пожизненно (в том числе для уменьшения вероятности рецидива) или хотя бы до достижения PASI 100 или PASI 75, при последнем варианте при возникновении рецидива псориаза нужно будет вновь проводить индукцию (3 еженедельных введения).
Можно вводить моноклональное антитело Нетакимаб реже, чем 1 раз в 4 недели?
Ряду больных псориазом кожи для поддержания ремиссии будет достаточно более редкого введения моноклонального антитела и/или меньшей ежемесячной дозы (чем указано в инструкции) на поддерживающем (втором) этапе. Эта группа пациентов выделяется мной в процессе наблюдения в динамике. Я за персонализированный (индивидуальный) подход к лечению псориаза.
При псориазе суставов или наличии предикторов псориаза суставов (псориаз ногтей, складок, волосистой части головы) вводить препарат на втором этапе желательно согласно инструкции (то есть 1 раз в 4 недели).
Где лучше делать первые инъекции биопрепарата Эфлейра?
В кабинете дерматолога, назначившего данное моноклональное антитело, имеющего навыки проведения инъекций с помощью автоинжектора или преднаполненных шприцов. Более 80% пациентов без обучения неправильно самостоятельно проводят инъекции. Отличный вариант: Первые инъекции совершает врач, а последующие – пациент под контролем врача, обучившего пациента технике инъекции.
↑ Содержание
Эффективность
Эфлейра излечивает псориаз?
К сожалению, как и другое современное лечение, нет. Достижимыми целями терапии псориаза в настоящий момент развития медицины являются уменьшение признаков (симптомов) поражения кожи (вплоть до „чистой кожи“), ногтей и суставов, снижение частоты рецидивов, повышение качества жизни, уменьшение риска возникновения поражения суставов, а также нередко ассоциированных с псориазом депрессии и сердечно-сосудистых заболеваний.
Насколько эффективен Нетакимаб для лечения псориаза?
Согласно отзывам врачей, предоставленных производителем (2019 г.), спустя 12 недель после начала лечения биопрепаратом Эфлейра PASI 75 зафиксирован примерно у 8 из 10 пациентов, при этом у каждого 3-го пациента отмечалось полное очищение кожи от признаков (симптомов) псориаза (PASI 100).
| PASI 75 | PASI 100 |
| 85% пациентов | 34% пациентов |
Клинический случай (отзыв) лечения псориаза биопрепаратом Эфлейра (Нетакимаб)
БЫЛО:
Как СТАЛО смотрите на YouTube:
ЭФЛЕЙРА (Нетакимаб): ОТЗЫВ врача
Может ли со временем пропадать эффект от лечения псориаза биопрепаратом Эфлейра?
Да, и это, назначая препарат уже более 2-х лет, отмечаю у многих пациентов. Иммунная система может начать вырабатывать антитела против биологического биопрепарата (иммуногенность) → пытаться „нейтрализовать“ препарат, что способствует потере эффективности лечения псориаза (не исчезновению присутствующих, появлению новых бляшек). В инструкции производитель утверждает, что образование связывающих антител к активному веществу биопрепарата Эфлейра (Нетаимабу) было зафиксировано менее, чем в 1% случаев, и можно было сделать (не соответствующий действительности) вывод, что „привыкание“ навряд ли возникнет, однако нередко наблюдаю снижение эффективности данного российского ГИБП с течением времени.
По отзывам, через какое время обычно возникает рецидив псориаза у большинства пациентов после прекращения лечения Эфлейрой?
У моих пациентов длительность ремиссии псориаза кожи составляла 2–3 месяца – это означает, что очень высока вероятность возвращения псориаза кожи спустя всего 3 месяца после последней инъекции биопрепарата Эфлейра.
Вероятность рецидива псориаза после окончания лечения биопрепаратом зависит от многих индивидуальных факторов, например, времени от дебюта псориаза до начала биологической терапии (чем позже начато лечение, тем короче период ремиссии), распространённости и тяжести псориаза к началу лечения, динамики регресса элементов псориаза в процессе курса лечения, распространённости и тяжести псориаза к окончанию лечения и др.
Некоторые факторы, часто поддерживающие патологический кожный процесс при псориазе, например, очаги хронической инфекции (кариес, тонзиллит/фарингит/гайморит, инфекция Helicobacter pylori, урогенитальный хламидиоз и др.), ожирение, инсулинорезистентность, психоэмоциональные нарушения (депрессию и/или тревогу) можно выявлять и устранять.
↑ Содержание
Безопасность
Согласно инструкции, пока какие побочные действия зафиксированы у больных псориазом, которым проводили инъекции препарата Эфлейра?
Часто (у от 1 до 9 из 100 пациентов)
- Инфекции верхних дыхательных путей;
- Кровь: Гипербилирубинемия, нейтропения лёгкой или средней степени тяжести (наиболее частая преходящая нежелательная реакция), лейкопения, повышение АлАТ, повышение АсАТ.
Нечасто (у менее чем 10 из 1000 пациентов)
- Инфекции нижних дыхательных путей;
- Инфекции мочевыводящих путей;
- Конъюнктивит;
- Фурункул;
- Экзема;
- Дерматит;
- Кровь: Повышение ГГТ;
- Гриппоподобный синдром, боль в животе.
Таким образом, согласно инструкции, моноклональное антитело Нетакимаб (Эфлейра) обладает относительно благоприятным профилем безопасности, серьёзные побочные эффекты возникают редко и очень редко.
Для установления долгосрочной безопасности генно-инженерного биологического препарата требуется не менее 5 лет после поступления его в продажу. Эфлейра появилась в аптеках в июне 2019 г., поэтому отдалённые последствия введения её в организм неизвестны.
Как именно может проявиться аллергическая реакция (гиперчувствительность) после введения Эфлейры?
- Затруднение дыхания (вызвать бригаду скорой медицинской помощи по тел.: 103)
- Отёк лица, языка или горла (вызвать бригаду скорой медицинской помощи по тел.: 103)
- Кожная сыпь
При возникновении каких симптомов инфекции нужно прекратить лечение моноклональным антителом Нетакимаб и срочно обратиться к врачу?
- Кашель.
- Одышка.
- Кровь в мокро́те.
- Высокая температура.
- Повышенная потливость.
- Боль в мышцах.
- Потеря веса.
- Понос и/или боль в животе.
- Частое мочеиспускание и/или жжение (боль) при мочеиспускании.
- Изменения кожи, не характерные для псориаза (например, красная и болезненная кожа, язвы).
Нетакимаб избирательно, но всё равно угнетает иммунитет… Может ли это привести к возникновению рака?
См. Плейлист на YouTube «Эфлейра (Нетакимаб)»
Прекращать ли лечение биопрепаратом Эфлейра (Нетакимаб) перед хирургической операцией?
Да, если это операция с высоким риском развития инфекционных осложнений, так как угнетающий иммунитет биологический препарат может утяжелить течение инфекции (это может закончиться смертью). Целесообразность перерыва следует индивидуально обсудить с врачом, который будет проводить операцию. Следует прекратить введение биопрепарата Эфлейра (Нетакимаб) за 7 недель (примерно 3 периода полувыведения) до операции; если не будет осложнений, возобновление лечения возможно уже через 1–2 недели после оперативного вмешательства [2].
↑ Содержание
Покупка, Цена
Эфлейру можно купить без рецепта?
Биопрепарат отпускается из аптек строго по рецепту врача; хранится и транспортируется при температуре от 2 до 8 °С. Поэтому фармацевт не продаст Эфлейру, если пациент не покажет ему рецепт на иммунодепрессант + термоконтейнер или термопакет с замороженным (при положительных температурах окружающей среды) или охлаждённым (при отрицательных температурах окружающей среды) хладоэлементом.
Как купить лекарство Эфлейра с максимальной скидкой (25%)?
Зайти на сайт программы „Курс на выздоровление“ от БИОКАД, где зарегистрироваться и оставить заявку на препарат, при этом 1 упаковка (2 шприца) обойдётся в 15 000 р.
Во сколько обойдётся лечение псориаза этим иммунодепрессантом в первые 6 недель?
При приобретении лекарства Эфлейра со скидкой по программе „Курс на выздоровление“ цена терапии составит 45 000 ₽ (3 упаковки).
Начиная с 7-й недели?
При наивысшей скидке цена лечения составит 15 000 ₽ в 4 недели (1 упаковка).
Сколько упаковок биопрепарата Эфлейра нужно купить для проведения лечения псориаза кожи на протяжении первых 12 недель?
5 упаковок (с предельной скидкой будут стоить всего 75 000 ₽).
Как получить социальный вычет по НДФЛ (минус 13% – минимум 1950 р. за пачку) на биопрепарат Эфлейра?
Попросите дерматолога выписать два (2) рецепта: один для аптеки, а другой должен быть со штампом (или напечатанной надписью) «Для налоговых органов Российской Федерации, ИНН налогоплательщика». Последний вместе с чеками на покупку и декларацией 3-НДФЛ представьте в Федеральную налоговую службу (можно сделать в течение трех лет со дня оплаты лекарства). Подробности на на Госуслугах.
Что делать, если сейчас из-за высокой цены я не могу купить биологический препарат Эфлейра (Нетакимаб)?
Пожалуйста, рассмотрите с лечащим врачом-дерматологом более доступные, альтернативные варианты лечения тяжёлого и среднетяжёлого псориаза: ультрафиолетовое облучение, Ацитретин и различные не-биологические иммунодепрессанты › Псориаз: Лечение тяжёлого, среднетяжёлого, устойчивого к наружным препаратам.
Эфлейра (Нетакимаб) может вызвать избыточный вес (ожирение)?
Не исключаю (не все побочные эффекты новых биопрепаратов известны). Некоторые мои пациентки отметили увеличение массы тела после начала лечения биопрепаратом Эфлейра (Нетакимаб). Так, у одной из пациенток зафиксировано повышение веса на 15 кг (!). В экспериментальных исследованиях на животных установлено, что дефицит ИЛ-17 ускорял накопление жира даже при диете с низким содержанием жира [3]. Рекомендую пациентам периодически взвешиваться.
↑ Содержание
Перед началом лечения
Что нужно обязательно сообщить врачу (что должен узнать врач) при рассмотрении возможности лечения псориаза биопрепаратом Эфлейра?
- Есть симптомы инфекции (например, высокая температура тела, кашель).
- Имеется инфекционное заболевание (туберкулёз, гепатит, ВИЧ и др.)
- О тесном контакте с больным туберкулёзом.
- Проводится вакцинация или недавно была вакцинация (прививка).
- Наличие беременности, её планирование, кормление грудью.
- О всех принимаемых лекарствах и БАДах.
- Об аллергических реакциях на лекарства.
Какие анализы крови нужно провести перед планированием лечения псориаза биопрепаратом Нетакимаб (или другим ингибитором интерлейкина 17А)?
Минимум: Клинический анализ крови, комплексная метаболическая панель (глюкоза, АлАТ, АсАТ, ЩФ, билирубин, креатинин и др.), тесты на ВИЧ, гепатиты B и C.
Требуется ли вакцинация?
Пациентам, которым проводится или планируется лечение моноклональным антителом Нетакимаб желательно проводить вакцинацию для профилактики пневмококковой (бактериальной) пневмонии («Превенар 13», «Пневмовакс» 23», «Пневмо» 23»), гепатита B, гриппа. Рекомендую применять вакцину против гриппа без иммуномодулятора «Полиоксидоний» (может ухудшить течение псориаза), и она должна содержать антигены вируса гриппа в адекватном количестве (каждый тип не по 5, а по 10 мкг).
Нужно ли провериться на туберкулёз перед лечением биопрепаратом Эфлейра?
Обязательно, так как Нетакимаб, ослабляя иммунитет, может ухудшить течение туберкулёза. До сих пор фиксируется высокая заболеваемость этим заболеванием жителей России. Для выявления (в том числе бессимптомного) туберкулёза требуется провести «Диаскинтест» или тест «T-SPOT.TB» + рентгенологическое исследование органов грудной клетки (прицельную рентгенографию органов грудной клетки или МСКТ) с последующей консультацией врача-фтизиатра.
Перед лечением биологическим препаратом Эфлейра (Нетакимаб) обязательно ли проводить УЗИ органов брюшной полости + (женщинам) УЗИ малого таза, эзофагогастродуоденоскопию (ФГДС)?
Согласно одобренным Научно-практическим Советом Минздрава РФ Клиническим рекомендациям Общероссийской общественная организация «Российское общество дерматовенерологов и косметологов [4] – необходимо. Очевидно, что эти исследования нужны с целью исключения злокачественных опухолей, которые могут начать прогрессировать после начала лечения биологическим препаратом, подавляющим иммунитет. Однако непонятно, почему в таком случае нет указаний на то, что нужно ещё провести следующие исследования для исключения распространённых злокачественных опухолей: УЗИ щитовидной железы (рак щитовидной железы), УЗИ молочных желез и/или с 40 лет – маммографию (рак груди), колоноскопию или хотя бы тест анализ кала на скрытую кровь (рак кишечника), цитологическое исследование соскоба из шейки матки (рак шейки матки), УЗИ простаты + анализ сыворотки для определения уровня ПСА (рак простаты).
↑ Содержание
Хранение и перевозка
Как можно испортить Эфлейру (или другой биопрепарат)?
- Перевезти не в термоконтейнере/термопакете (даже в течение короткого периода времени).
- Хранить на полке дверцы холодильника (значительные колебания температуры) или в самом низу холодильника.
- Заморозить:
- Перевезти при температуре воздуха ниже 0 °C не в термоконтейнере/термопакете (1 мл биопрепарата может быстро заморозиться);
- Положить биопрепарат в холодильник в непосредственной близости потока холодного воздуха.
- Потрясти (биопрепараты – это белки, которые могут повредиться даже при тряске). Многие инъекционные препараты перед введением нужно встряхивать, и медсестра процедурного кабинета может сделать это «по привычке“.
- После нагревания до комнатной температуры (для этого достаточно менее 30 минут) положить в холодильник.
Сколько времени можно перевозить биопрепарат Эфлейра в термопакете с хладоэлементом?
Недолго: Обычно от 30 минут до 2-х часов (зависит от используемого хладоэлемента и температуры окружающей среды). Желательно использовать термоконтейнер.
В аптеке мне выдадут в чём перевозить Эфлейру?
Моим пациентам фармацевты аптек выдавали с биопрепаратом только картонную коробку (или простой пакет) с одним или двумя хладоэлементами. Перевозка биопрепарата Эфлейра даже с хладоэлементом, но не в термопакете (термоконтейнере) может привести к порче биопрепарата!
↑ Содержание
Сравнение с «Малыми молекулами» и Тремфеей
Таблетки для лечения псориаза Отесла менее эффективны, чем Эфлейра?
Да. PASI 75 отмечался спустя только 16 недель и у 33% пациентов с псориазом, принимавших таблетки Отесла (клиническое исследование ESTEEM 1). (PASI 75 зафиксирован у 85% пациентов через 12 недель после первой инъекции раствора Эфлейра.)
Таким образом, Нетакимаб оказывает лечебное влияние скорее и гораздо больше уменьшает распространённость и тяжесть псориаза, кроме того, после второго месяца лечение псориаза будет дешевле примерно в 3 раза, чем иммунодепрессантом Отесла, который нужно принимать внутрь 2 раза в день, а биопрепарат вводится всего 1 раз в 4 недели.
Таблетки Яквинус в сравнении с Эфлейрой?
Кроме России, нигде не одобренный для лечения псориаза кожи (из-за неблагоприятного соотношения польза/риск) иммунодепрессант для приёма внутрь Яквинус (Тофацитиниб) существенно более эффективен, чем Отесла, но всё равно проигрывает новым биопрепаратам для лечения псориаза. В клиническом исследовании OPT Pivotal 2 при приёме внутрь таблеток Яквинус 10 мг 2 раза в день PASI 75 наблюдался у 53% пациентов через 12 недель терапии псориаза (у проходивших лечение Эфлейрой – у 85%).
| PASI 75 | |
| Яквинус | 53% пациентов |
| Эфлейра | 85% пациентов |
В настоящее время в России цена 4-недельного курса лечения псориаза таблетками Яквинус (требуется 104 табл. по 5 мг) составляет около 93 000 р., что дороже, чем применение большинства биологических препаратов на поддерживающем этапе (в 6 раз дороже, чем ежемесячные инъекции Эфлейры).
Нетакимаб лучше, чем Тремфея (ингибитор ИЛ-23)?
В отношении быстроты лечебного действия – несомненно, но ингибиторы ИЛ-23 очищают кожу от псориаза значительнее по сравнению с ингибиторами ИЛ-17А. Однако для этого требуется более продолжительное время. Тремфея удобней в применении: На втором этапе лечения псориаза она вводится 1 раз в 8 недель (1 шприц – 1 инъекция), а Эфлейра – 1 раз в 4 недели (2 шприца – 2 инъекции). Как вариант, можно начать терапию псориаза ингибитором ИЛ-17А для достижения быстрого лечебного эффекта, а затем перейти на ингибитор ИЛ-23.
Как перейти с лечения псориаза биологическим препаратом Эфлейра (Нетакимаб) на более совершенный биологический препарат Тремфея (Гуселькумаб)?
После последней инъекции моноклонального антитела Нетакимаб (Эфлейра) рекомендуется сделать перерыв в 7 недель (что составит примерно 3 периода полувыведения этого лекарственного средства из организма), затем под контролем врача можно начинать лечение более эффективным препаратом Тремфея (Гуселькумаб).
↑ Содержание
Разное
Можно ли ставить прививку для профилактики коронавируса („КОВИД-19“) при лечении псориаза препаратом ЭФЛЕЙРА (Нетакимаб)?
Вакцины формируют иммунитет в отношении коронавирусной инфекции. Препарат Эфлейра (Нетакимаб) угнетает иммунитет, следовательно, возможно снижение эффективности вакцинации ➜ увеличение вероятности заразиться.
⠀
Эфлейра (Нетакимаб) подавляет звено иммунитета, которое, видимо, участвует в реакции на внедрение коронавируса, поэтому при наличии ряда признаков для предупреждения „цитокинового шторма“ этот препарат даже рекомендован актуальными Временными методическими рекомендациями «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)».
⠀
В инструкциях к вакцинам «Гам-КОВИД-Вак» и «Гам-КОВИД-Вак-Лио» („Sputnik V“), «КовиВак», «Спутник Лайт» особо указано, что приём препаратов, угнетающих функцию иммунной системы, ПРОТИВОПОКАЗАН в течение как минимум 1 месяца до и после вакцинации из-за риска снижения иммуногенности. В новосибирской вакцине «ЭпиВакКорона» таких указаний нет.
⠀
Таким образом, если следовать инструкциям к вакцинам (исключение: «ЭпиВакКорона»), нужно делать перерыв в лечении препаратом Эфлейра (Нетакимаб) на 3 месяца. Рецидив псориаза у большинства моих пациентов возникал примерно спустя 2 месяца после последнего введения…
Какие сайты продвигают биологический препарат Эфлейра (Нетакимаб)?
Сайты от производителя биопрепарата: Efleira.ru и Psoriaz.life
Почему на официальном сайте препарата Эфлейра (Нетакимаб) ни разу не указано, что он относится к группе лекарственных средств, подавляющих иммунитет (иммунодепрессантов, иммуносупрессантов)?
Действительно, если в поиске Google или Яндекс сделать поиск слов «иммунодепрессант» или «иммуносупрессант» на сайте efleira.ru («иммунодепрессант site:efleira.ru» или «иммуносупрессант site:efleira.ru), то обнаружите, что таких слов там нет, и это подтверждает то, что официальный сайт не предоставляет исчерпывающую информацию о препарате Эфлейра (Нетакимаб)…
Кроме того, в инструкции указано, что российское лекарственное средство Эфлейра (Нетакимаб) относится к фармакотерапевтической подгруппе Ингибиторы интерлейкина (код по АТХ – Анатомо-Терапевтической Химической классификации: L04AC), но не уточняется, что эта подгруппа включена в группу Иммунодепрессанты (код по АТХ: L04A). Напротив, в инструкциях к зарубежным биологическим препаратам Талс и Тремфея эта информация не скрывается, добросовестно указано, что они являются Иммуносупрессорами (Иммунодепрессантами), ингибиторами интерлейкина:
●
●
Когда показаны ультрафиолетовая или системная (таблетки, капсулы, инъекции) терапия псориаза?
Ультрафиолетовое или системное лечение псориаза назначается при среднетяжёлом или тяжёлом псориазе кожи.
В Клинических рекомендациях Российского общества дерматовенерологов и косметологов [4] для оценки тяжести псориаза предлагается (см. Приложение Г) использовать только индекс PASI: Если он составит до 10 баллов, то это следует интерпретировать как лёгкий псориаз (следовательно, лечение биологическим препаратом не показано, даже если псориаз существенно снизил качество жизни и/или другое лечение не дало эффекта).
Таким образом, если псориазом поражены только ногти или волосистая часть головы или ладони/подошвы или половые органы (то есть PASI менее 10 баллов), то такой псориаз, в соответствии с Клиническими рекомендациями Российского общества дерматовенерологов и косметологов, не является среднетяжёлым или тяжёлым, и его неправомерно* (пациент может инициировать судебное разбирательство в том числе при развитии осложнений) лечить** моноклональным антителом Нетакимаб (Эфлейра).
*„Медицинская помощь оказывается на основе клинических рекомендаций“ – ФЗ от 21.11.2011 N 323-ФЗ (ред. от 08.06.2020) «Об основах охраны здоровья граждан в Российской Федерации».
**„Медицинским работникам запрещается оформлять рецепты при отсутствии у пациента медицинских показаний“ – Приказ Минздрава России от 14.01.2019 N 4н (ред. от 11.12.2019) «Об утверждении порядка назначения лекарственных препаратов, форм рецептурных бланков на лекарственные препараты, порядка оформления указанных бланков, их учета и хранения».
Где производится Эфлейра?
Производителем оригинальной фармацевтической субстанции (Нетакимаб) и готовой лекарственной формы (раствора для подкожного введения) является биотехнологическая компания «БИОКАД» (Россия).
Нетакимаб – генно-инженерное лекарственное средство?
Верно, генно-инженерный биологический препарат (ГИБП) Эфлейра создан с помощью технологии рекомбинантной ДНК (в составе части ДНК человека и животного ламы), является моноклональным антителом (netakiMAB – Monoclonal AntiBody).
Нетакимаб одобрен FDA?
Нет. FDA (U.S. Food and Drug Administration) одобрило 11 биологических препаратов для лечения псориаза, моноклонального антитела Нетакимаб в их числе нет.
При каких инфекциях противопоказан биопрепарат Эфлейра?
Активные туберкулёз, ВИЧ-инфекция, гепатит B и/или гепатит C.
Если у меня только псориаз ногтей или ладонно-подошвенный или каплевидный псориаз, при отсутствии противопоказаний дерматолог может назначить мне биопрепарат Эфлейра?
К сожалению, нет, несмотря на то, что ингибиторы ИЛ-17А эффективны при перечисленных формах псориаза (для лечения ладонно-подошвенного псориаза могут потребоваться бóльшие, а каплевидного – меньшие однократные дозы.). Согласно инструкции, биопрепарат Эфлейра показан для лечения только двух форм псориаза: бляшечного, или обыкновенного (код по международной классификации болезней 10-го пересмотра: L40.0) и артропатического (код по международной классификации болезней 10-го пересмотра: L40.5). В настоящее время в России за назначение лекарственного средства не строго по инструкции врачу потенциально грозит судебное преследование. Навряд ли в ближайшем будущем в инструкцию будут добавлены другие формы псориаза.
Где почитать краткую инструкцию иммунодепрессанта Эфлейра?
Эфлейра (Нетакимаб): Краткая Инструкция
Как можно будет получить бесплатное лечение Эфлейрой?
При наличии показаний пациент с псориазом может (теоретически) получить назначение на бесплатное лечение моноклональным антителом Нетакимаб от врача-дерматолога государственной медицинской организации (например, кожно-венерологического диспансера). (Схема пути пациента.) Однако сейчас в России бесплатная генно-инженерная биологическая терапия псориаза назначается достаточно редко. Согласно Клиническим рекомендациям [4], лечение биологическим препаратом может быть назначено при распространённом псориазе (средняя или тяжёлая степень тяжести) и неэффективности токсичных недорогих системных препаратов (например, Метотрексата, вызывающего цирроз печени; канцерогенным Циклоспорином), канцерогенной ПУВА-терапии или если есть непереносимость или противопоказания к их применению:
Не уточняется, что значит “отсутствие клинического эффекта” (насколько именно должна уменьшиться степень тяжести псориаза через конкретный промежуток времени). Таким образом, сейчас врач-дерматолог государственной медицинской организации во многих случаях может отказать в бесплатном лечении псориаза, ссылаясь на эти Клинические рекомендации.
У меня поднялась температура от инфекции (гриппа, простуды, воспаления лёгких). Можно ли мне проводить инъекцию биопрепарата Эфлейра?
Нет. Можно только после нормализации температуры тела и окончания курса приёма антибиотика.
Хочу поставить прививку от гриппа. Это возможно во время курса лечения биопрепаратом Эфлейра?
Допускается, так как вакцина для профилактики гриппа является инактивированной (не „живой“).
Как ожирение может повлиять на эффективность лечения псориаза биорепаратом Эфлейра?
В дорегистрационном клиническом исследовании не выявлено снижения лечебной эффективности Эфлейры у пациентов с повышенным весом.
У некоторых зарубежных ингибиторов интерлейкина 17А у пациентов с ожирением (индекс массы тела более 30 кг/м²) отмечалась меньшая эффективность лечения псориаза.
Через какой промежуток времени после последней инъекции биопрепарата Эфлейра можно начать лечение псориаза другим биологическим препаратом?
Минимум 48 суток. Между введением разных биопрепаратов желательно (необязательно) должен пройти промежуток, составляющий не менее трёх (3) периодов их полувыведения из организма. Согласно инструкции, для биопрепарата Нетакимаб период полувыведения равен около 16 суток.
Можно ли лечить псориаз у детей биопрепаратом Эфлейра?
Моноклональное антитело Нетакимаб в настоящее время противопоказано пациентам младше 18 лет (не опубликованы результаты клинических исследований относительно эффективности и безопасности у детей).
См. Какими биопрепаратами можно лечить псориаз у детей?
Что такое PASI 75?
Уменьшение индекса выраженности и распространённости псориаза (PASI – Psoriasis Area and Severity Index) приблизительно на 75% → Пример (фото).
За эту веб-страницу и/или за назначения биопрепарата Эфлейра Вы получали денежные средства, подарки?
Нет, я работаю в интересах пациентов, независим от фармацевтических компаний, не заключал соглашений с компанией (или представителем компании) о назначении пациентам препарата Эфлейра (Нетакимаб) или любого другого, не скрываю сведений о наличии в обращении аналогичных лекарственных средств.
На консультативном приёме пациенту предоставляется информация обо всех зарегистрированных в России биопрепаратах для лечения псориаза, обсуждаются другие альтернативные, более доступные варианты терапии.
Как можно поблагодарить Вас за информацию о препарате Эфлейра (Нетакимаб)?
ПОБЛАГОДАРИТЬ
Для повышения эффективности лечения псориаза с чем ещё можно сочетать применение биопрепарата Эфлейра?
У моих пациентов элементы псориаза на голенях хуже всего поддавались лечению биопрепаратом Нетакимаб, поэтому на эти области желательно наносить наружные лекарственные препараты (подбираются индивидуально).
Где почитать про биологическую терапию псориаза?
Псориаз: Моноклональные антитела
↑ Содержание
Литература
① Долгосрочная эффективность и безопасность препарата нетакимаб у пациентов со среднетяжелым и тяжелым вульгарным псориазом. Результаты открытого продленного клинического исследования II фазы BCD-085-2-ext. Бакулев АЛ, Самцов АВ, Кубанов АА и др. Вестник дерматологии и венерологии. 2019;95(3):54–64.
② Joint AAD-NPF guidelines of care for the management and treatment of psoriasis with biologics. Menter A, Strober BE, Kaplan DH et al. J Am Acad Dermatol. 2019 Apr;80(4):1029–1072.
③ IL-17 Regulates Adipogenesis, Glucose Homeostasis, and Obesity. Luis A. Zúñiga, Wen-Jun Shen, Barbara Joyce-Shaikh et al. J Immunol. 2010 Dec 1; 185(11): 6947–6959.
④ Псориаз: Клинические рекомендации, утверждённые в 2020 г. Общероссийская общественная организация «Российское общество дерматовенерологов и косметологов». Одобрено Научно-практическим Советом Минздрава РФ.
Эфлейра (Нетакимаб): Задать вопрос
Ответы на присланные Вопросы
19.07.2020 г.
У меня псориаз ногтей, после долгого лечения разными способами попробовала Эфлейру. Уже почти 9 месяцев прохожу лечение, результат есть, однако полной ремиссии нет, процесс очень медленный. Думаю попробовать Козэнтикс, но он в 2 раза дороже, чем Эфлейра, даже для участников программы.
Буду рада вашей рекомендации – стоит попробовать и инвестировать в Козэнтикс? Или вообще Талс?) Спасибо!
Анастасия, 37
Уважаемая Анастасия! Эфлейра, Талс и Козэнтикс являются ингибиторами интерлейкина-17А, поэтому нельзя дать гарантию, что эффективность лечения псориаза ногтей существенно увеличится при переходе с одного ингибитора интерлейкина-17А на другой (если выбирать из этих 3-х биопрепаратов, рекомендую отдать предпочтение Талс). Что касается ингибитора интерлейкина-23 (Тремфея), то он не показал впечатляющих результатов в лечении псориаза ногтей. Пожалуйста, обсудите с лечащим врачом-дерматологом следующие варианты лечения псориаза ногтей: импульсный лазер на красителе с длиной волны 595-нм или фотодинамическая терапия, капсулы Отесла, капсулы Неотигазон (если никогда больше не планируете беременеть). Другими вариантами лечения псориаза являются капсулы Циклоспорин и старые биологические препараты – ингибиторы ФНО-альфа, но из-за возможных серьёзных побочных действий я бы не стал их назначать пациенту только с псориазом ногтей.
Олег Валерьевич,
Спасибо большое за рекомендации!
Думаю попробовать Козэнтикс и Талс, ваши рекомендации также обсужу со своим врачом!
Анастасия.
12.06.2020 г.
Нахожусь в Израиле после операции на сердце. Кололи Стелару бесплатно 90 мг 1 раз в 3 месяца. Еду домой в Крым. Могу ли я колоть Эфлейру? И как часто, сколько? Спасибо.
Анна, 71
Уважаемая Анна! Скорей всего, Вам можно будет перейти на лечение препаратом Эфлейра (Нетакимаб). Между последней инъекцией раствора Стелара и первой инъекцией раствора Эфлейра (Нетакимаб) должно пройти минимум 9 недель (то есть примерно 3 периода полувыведения из организма Стелары). Если к моменту первого введения Эфлейры псориаз не будет прогрессировать (появление новых элементов и/или рост существующих), то я бы назначил введение Нетакимаба 1 раз в 4 недели. Лечение биопрепаратом должно проводиться при периодическом наблюдении врачом-дерматологом, для получения рецепта нужно обратиться к нему.
18.04.2020 г.
Здравствуйте, Олег Валерьевич.
Псориаз стал быстро прогрессировать в течение 2-3 лет. Локти, голени, кисти рук, ногти, уши, перианальная область, наблюдаю высыпания на волосистой части головы. Без ремиссий. Каждый день новые очаги.
Можно ли в данной ситуации начать применять Эфлейру? Мой врач в КВД говорит, что назначит биопрепарат только когда поражение кожных покровов превысит 50% тела.
Alex, 50
Уважаемый Alex! Согласно инструкции, препарат Эфлейра показан для для лечения тяжёлого (PASI 10–19 баллов) или среднетяжёлого (PASI от 20 баллов) бляшечного псориаза. Думаю, что в Вашем случае PASI составляет более 10 баллов, поэтому моноклональное антитело Нетакимаб при отсутствии противопоказаний может быть назначено, тем более, что имеется псориаз ногтей, который нередко предшествует псориазу суставов, и есть шанс предотвратить его развитие.
Добрый день! Можно ли начать лечение моей дочери 17 лет, хотя в инструкции написано только с 18 лет?
Владимир Валериевич
Уважаемый Владимир Валериевич! Формально противопоказано (сейчас в РФ за назначение препарата не согласно инструкции врача могут засудить). Если бы у меня была пациентка 17 лет (с адекватными родителями), которой показано лечение препаратом Эфлейра (Нетакимаб), то возраст не стал бы помехой для назначения этого биопрепарата.
Добрый день! Возможна ли транспортировка Эфлейры без термоконтейнера? Можно ли держать Эфлейру какое-то время без холодильника по аналогии с Козэнтиксом? Заранее благодарна за ответ.
Светлана, 26
Уважаемая Светлана!
Действительно, раствор Козэнтикс навряд ли испортится вне холодильника при температуре до 30° С (в течение не более 4-х суток). Что касается Эфлейры, устойчивость этого препарата к комнатной температуре мне неизвестна (если производитель даст информацию по этому вопросу, то она будет размещена на этой странице). Нетакимаб желательно перевозить в термоконтейнере, или хотя бы в термопакете – одна пачка Эфлейры помещается в термопакет «ХолодОк» (с хладоэлементом «ХолодОк М-100»), который можно купить, например, в «Аптеке от Склада» менее чем за 100 руб. (подробности).
Беременность наступила вовремя лечения. Необходимо ли ее прерывать? Какова вероятность родить нездорового малыша?
Людмила, 34
Уважаемая Людмила!
Введение моноклонального антитела Нетакимаб животным не выявило вредного воздействия на плод, на людях таких исследований не проводилось. Поэтому прерывать беременность не нужно, при наличии проявлений псориаза на коже можно перейти на (не противопоказанную во время беременности) узкополосную средневолновую терапию с длиной волны 311 нм. Вероятно (пока до конца не изучено), наиболее безопасным генно-инженерным препаратом для лечения псориаза у беременных является Симзия.
Добрый день. Очень хорошо все у Вас написано. Препарат быстро и полностью помог очиститься (болею с 1996), хотя с каждым годом ситуацию ухудшалась и на пляже уже нельзя было появляться. Хочу попробовать колоть (сделал на данный момент 4 упаковки — 1,5 месяца) Эфлейру 60 мг 1 раз в 4 недели или лучше 1 раз в 3 недели. Считаете возможным так сделать или риск возврата бляшек большой?
Вадим, 57
Уважаемый Вадим!
При описанном быстром и полном (или почти полном) очищении кожи от псориаза, а также при отсутствии псориатического артрита (и/или псориаза ногтей, нередко предшествующему ему) у большинства пациентов удаётся поддерживать достигнутый эффект более редким введением моноклонального антитела Нетакимаб и/или меньшей дозировкой, например, вводить его 60 мг (1 мл) один раз в 4 недели. Индивидуальный подбор дозы (1 или 2 шприца), частоты введения генно-инженерного биологического препарата (ГИБП) Эфлейра я подбираю в ходе динамического наблюдения за пациентом. Обращаю Ваше внимание на то, что терапия псориаза ГИБП должно проводиться только под периодическим контролем врача-дерматолога, самолечение недопустимо.
Эфлейра (Нетакимаб): Задать вопрос
(заочные консультации для назначения лекарства не проводятся)
Информация для образовательных целей; не должна использоваться для самостоятельной диагностики и лечения, не может служить заменой персональной консультации врача. Есть противопоказания.


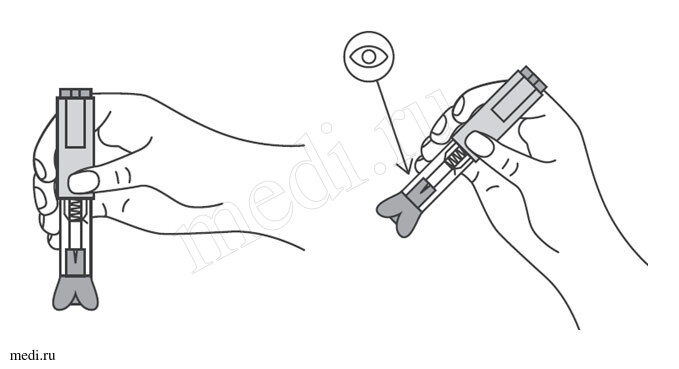
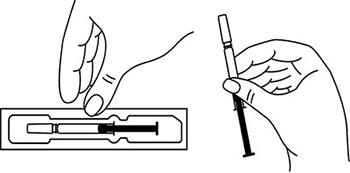
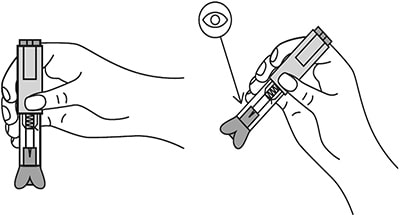
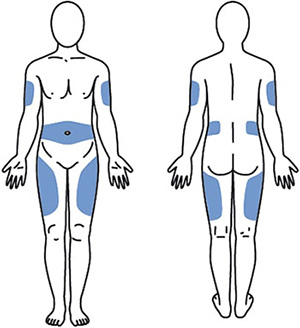
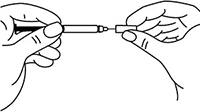
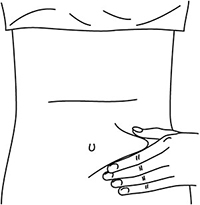
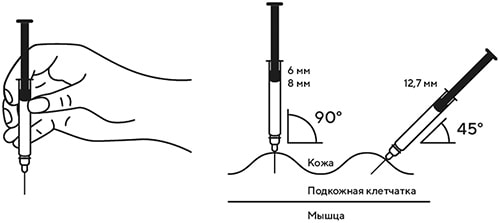
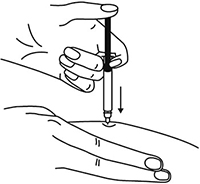
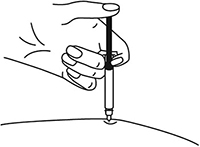
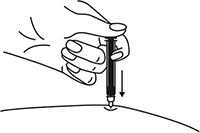
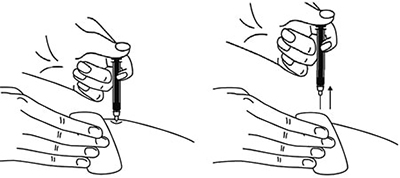
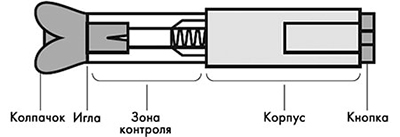
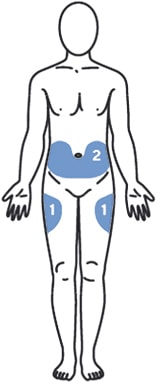
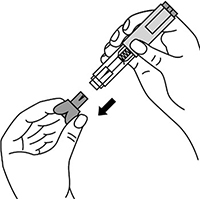
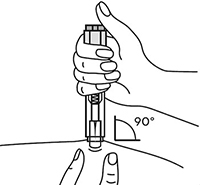
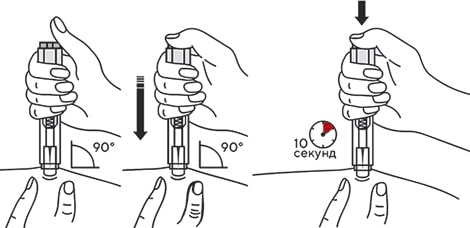
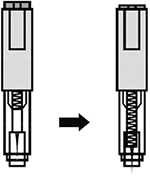
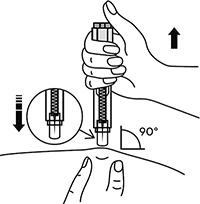
 Как проводится лечение псориаза кожи
Как проводится лечение псориаза кожи