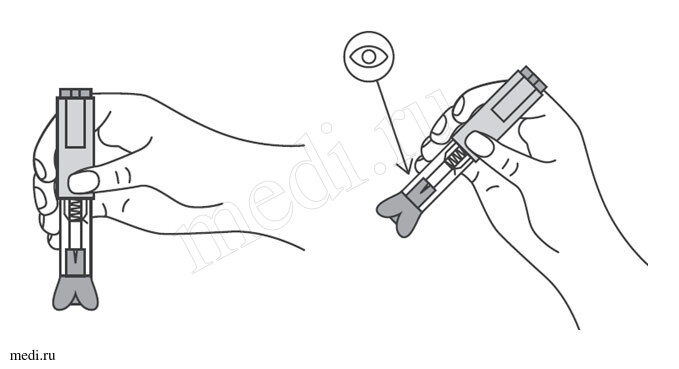
Эйлеа® (Eylea®)
💊 Состав препарата Эйлеа®
✅ Применение препарата Эйлеа®
Описание активных компонентов препарата
Эйлеа®
(Eylea®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2021.02.16
Владелец регистрационного удостоверения:
Вторичная упаковка и выпускающий контроль качества:
BAYER, AG
(Германия)
Код ATX:
S01LA05
(Афлиберцепт)
Лекарственная форма
| Эйлеа® |
Р-р д/внутриглазного введения 40 мг/мл: фл. 0.1 мл рег. №: ЛП-003544 |
Форма выпуска, упаковка и состав
препарата Эйлеа®
Раствор для внутриглазного введения прозрачный или слегка опалесцирующий, бесцветный или светло-желтого цвета.
Вспомогательные вещества: натрия дигидрофосфата моногидрат, натрия гидрофосфата гептагидрат, натрия хлорид, сахароза, полисорбат 20, вода д/и.
Один флакон содержит (0.1 мл) 100 мкл раствора (извлекаемый объем), что эквивалентно 4 мг афлиберцепта. Данный извлекаемый объем раствор позволяет обеспечить введение разовой дозы 2 мг афлиберцепта, что составляет 50 мкл раствора.
0.1 мл (100 мкл) извлекаемого объема* — флаконы бесцветного стекла (1) в комплекте с фильтровальной иглой — пачки картонные с контролем первого вскрытия (перфорация и/или стикер).
* Препарат производится с избытком наполнения в целях обеспечения извлекаемого объема не менее 0.1 мл (100 мкл).
Фармакологическое действие
Афлиберцепт — рекомбинантный гибридный белок, состоящий из связывающихся с VEGF (эндотелиальными факторами роста сосудов) частей внеклеточных доменов рецептора VEGF 1 и рецептора VEGF 2, соединенных с доменом Fc (фрагмента способного к кристаллизации) иммуноглобулина G1 (IgG1). Афлиберцепт производится с помощью технологии рекомбинантной ДНК с использованием экспрессионной системы клеток яичника китайского хомячка (СНО) К-1.
Афлиберцепт действует как растворимый рецептор-ловушка, который связывает VEGF-A (сосудистый эндотелиальный фактор роста А) и P1GF (плацентарный фактор роста) с более высокой аффинностью, чем их естественные рецепторы, и, таким образом, может ингибировать связывание и активацию этих родственных рецепторов VEGF.
Эндотелиальный фактор роста сосудов A (VEGF-A), эндотелиальный фактор роста сосудов В (VEGF-B) и плацентарный фактор роста (PlGF) относятся к VEGF-семейству ангиогенных факторов, которые могут действовать как сильные митогенные, хемотаксические и влияющие на сосудистую проницаемость факторы для эндотелиальных клеток. Действие VEGF осуществляется через две рецепторные тирозинкиназы — VEGFR-1 и VEGFR-2, находящиеся на поверхности эндотелиальных клеток. P1GF связывается только с VEGFR-1, которые также присутствуют на поверхности лейкоцитов. Избыточная активация VEGF-А этих рецепторов может приводить к патологической неоваскуляризации и избыточной проницаемости сосудов. В этих процессах P1GF может проявлять синергизм с VEGF-А, а также стимулирует инфильтрацию лейкоцитов и сосудистое воспаление.
Фармакокинетика
Вводят непосредственно в стекловидное тело для оказания локального воздействия. После интравитреального введения афлиберцепт медленно всасывается в системный кровоток, где обнаруживается в основном в виде неактивного стабильного комплекса с VEGF; при этом только свободный афлиберцепт может связывать эндогенный VEGF. Афлиберцепт не кумулирует в плазме крови при интравитреальном введении каждые 4 недели. Развитие системных фармакодинамических эффектов, таких как изменения АД, маловероятно. Величина средней Cmax свободного афлиберцепта в плазме согласно результатам фармакокинетических дополнительных исследований находилась в диапазоне от 0.03 до 0.05 мкг/мл, индивидуальные значения не превышали 0.14 мкг/мл. Впоследствии плазменные концентрации свободного афлиберцепта снижались до значений ниже или близких к нижнему пределу количественного определения, как правило, в течение одной недели. Ожидается, что как и другие крупные белки, и свободный, и связанный афлиберцепт будет выводиться из организма путем протеолитического катаболизма.
Показания активных веществ препарата
Эйлеа®
Для лечения неоваскулярной возрастной макулярной дегенерации («влажной» формы ВМД); снижения остроты зрения, вызванного макулярным отеком вследствие окклюзии вен сетчатки (центральной вены (ОЦВС) или ее ветвей (ОВЦВС)); снижения остроты зрения, вызванного диабетическим макулярным отеком (ДМО); снижения остроты зрения, вызванного миопической хориоидальной неоваскуляризацией (миопической ХНВ).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Средство предназначено для введения в стекловидное тело. Рекомендуемая доза афлиберцепта составляет 2 мг. Интервал между введениями должен составлять не менее одного месяца. Количество инъекций и интервалы между инъекциями устанавливают в зависимости от показаний, результатов изменения остроты зрения и/или анатомических показателей.
Побочное действие
Со стороны иммунной системы: нечасто — реакции гиперчувствительности.
Со стороны органа зрения: очень часто — снижение остроты зрения, субконъюнктивальное кровоизлияние, боль в глазу; часто — разрыв пигментного эпителия сетчатки, отслойка пигментного эпителия сетчатки, дегенерация сетчатки, кровоизлияние в стекловидное тело, катаракта, кортикальная катаракта, ядерная катаракта, субкапсулярная катаракта, эрозия роговицы, микроэрозии роговицы, повышение внутриглазного давления, затуманивание зрения, плавающие помутнения стекловидного тела, отслойка стекловидного тела, боль в месте введения, чувство инородного тела в глазу, слезотечение, отек века, кровоизлияния в месте введения, точечный кератит, инъекция конъюнктивы век, инъекция конъюнктивы глазного яблока; нечасто — эндофтальмит, отслойка сетчатки, разрыв сетчатки, ирит, увеит, иридоциклит, помутнение хрусталика, дефект эпителия роговицы, раздражение в месте введения, аномальная чувствительность тканей глаза, раздражение века, воспалительная реакция во влаге передней камеры, отек роговицы; редко — слепота, ятрогенная травматическая катаракта, воспалительная реакция со стороны стекловидного тела (витреит), гипопион.
Противопоказания к применению
Повышенная чувствительность к афлиберцепту; активная или подозреваемая интра- или периокулярная инфекция; активное тяжелое внутриглазное воспаление; беременность и период грудного вскармливания, за исключением случаев, когда потенциальная польза для матери превышает потенциальный риск для плода; возраст до 18 лет.
С осторожностью: при лечении пациентов с плохо контролируемой глаукомой (не следует вводить афлиберцепт при внутриглазном давлении >30 мм рт.ст.); у пациентов, перенесших инсульт, транзиторную ишемическую атаку или инфаркт миокарда в течение последних 6 месяцев; у пациентов с факторами риска нарушения целостности пигментного эпителия сетчатки.
Применение при беременности и кормлении грудью
Афлиберцепт не следует применять при беременности, за исключением случаев, когда потенциальная польза для матери превышает потенциальный риск для плода.
Афлиберцепт не рекомендуется применять при грудном вскармливании. Необходимо принять решение о прерывании грудного вскармливания или воздержаться от терапии афлиберцептом, принимая во внимание пользу грудного вскармливания для ребенка и пользу лечения для матери.
Женщины репродуктивного возраста должны использовать эффективные средства контрацепции в период лечения и, по крайней мере, в течение 3 месяцев после последней интравитреальной инъекции афлиберцепта.
Применение при нарушениях функции печени
Коррекции дозы у пациентов с печеночной недостаточностью не требуется.
Применение при нарушениях функции почек
Коррекции дозы у пациентов с почечной недостаточностью не требуется.
Применение у детей
Противопоказано применение у детей и подростков в возрасте до 18 лет.
Применение у пожилых пациентов
У пациентов пожилого возраста соблюдения каких-либо специальных условий не требуется.
Особые указания
Была выявлена связь интравитреальных инъекций, включая инъекции афлиберцепта, с развитием эндофтальмита, воспалительной реакции со стороны стекловидного тела, регматогенной отслойки сетчатки, разрыва сетчатки, ятрогенной травматической катаракты. При введении афлиберцепта всегда следует строго соблюдать соответствующую технику асептического проведения инъекций. Пациенты должны находиться под наблюдением в течение 1 недели после проведенной инъекции для выявления первых признаков воспаления и своевременного назначения необходимой терапии. Следует информировать пациентов о необходимости немедленно сообщать врачу о любых симптомах, свидетельствующих о развитии эндофтальмита или любой другой реакции, указанной выше.
Наблюдались случаи повышения внутриглазного давления в первые 60 мин после интравитреальных инъекций, включая инъекции афлиберцепта. При лечении пациентов с плохо контролируемой глаукомой необходимы особые меры предосторожности (не следует вводить афлиберцепт при внутриглазном давлении >30 мм рт. ст.). Во всех случаях необходим контроль внутриглазного давления и перфузии диска зрительного нерва с назначением соответствующей состоянию терапии.
Поскольку афлиберцепт представляет собой белок с терапевтическими свойствами, существует вероятность проявления иммуногенности. Следует информировать пациентов о необходимости сообщать врачу о любых признаках или симптомах внутриглазного воспаления, таких как боль, светобоязнь или конъюнктивальная или перикорнеальная инъекция, которые могут быть клиническими проявлениями гиперчувствительности.
После интравитреальных инъекций ингибиторов VEGF были отмечены системные нежелательные явления, в т.ч. кровоизлияния вне органа зрения и тромбоэмболия артерий. Существует теоретический риск связи этих явлений с ингибированием VEGF. Имеются ограниченные данные по безопасности применения афлиберцепта пациентами с ОЦВС, ОВЦВС, ДМО или миопической ХНВ, имеющими в анамнезе инсульт, транзиторную ишемическую атаку или инфаркт миокарда за период в 6 мес до начала терапии. При лечении таких пациентов следует соблюдать осторожность.
При введении афлиберцепта одновременно в оба глаза возможно повышение его системной экспозиции, что, в свою очередь, повышает риск возникновения системных нежелательных явлений.
Факторы риска, связанные с нарушением целостности слоя пигментных клеток после анти-VEGF терапии «влажной» формы ВМД, включают обширную и/или выраженную отслойку пигментного эпителия сетчатки. В начале терапии афлиберцептом следует соблюдать осторожность при его назначении пациентам с факторами риска развития разрывов пигментного эпителия сетчатки.
Пациентам с регматогенной отслойкой сетчатки или с макулярными разрывами 3 или 4 стадии не рекомендуют терапию афлиберцептом.
В случае разрыва сетчатки инъекцию афлиберцепта следует отменить, лечение не следует возобновлять до адекватного восстановления разрыва.
От инъекции следует воздержаться до следующей запланированной по графику инъекции в случае снижения МКОЗ >30 букв по сравнению с последней оценкой остроты зрения; субретинальных кровоизлияний, затрагивающих центральную ямку, или если размер кровоизлияния составляет >50% от общей области поражения.
От инъекции следует воздержаться на период 28 дней до планируемого и 28 дней после проведенного интраокулярного хирургического вмешательства.
При наличии у пациентов клинических признаков необратимых изменений зрительных функций на фоне ишемической ОЦВС и ОВЦВС терапия афлиберцептом не рекомендована.
Влияние на способность к управлению транспортными средствами и механизмами
Применение афлиберцепта оказывает минимальное влияние на способность управлять транспортными средствами и использовать механизмы вследствие возможных временных нарушений зрения, связанных как с инъекцией, так и с процедурой обследования. Если после проведения инъекции у пациента возникли временные нарушения зрения, не рекомендуется управлять автомобилем или работать с механизмами до восстановления четкости зрительного восприятия.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Обобщенные научные материалы по действующему веществу препарата Эйлеа® (раствор для внутриглазного введения, 40 мг/мл)
Дата последней актуализации: 06.03.2017
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Характеристика
- Фармакология
- Показания к применению
- Нозологическая классификация (МКБ-10)
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Владелец РУ
Байер АГ
Условия хранения
При температуре 2–8 °C в оригинальной упаковке (пачка картонная) для защиты от света.
Перед использованием невскрытый флакон может храниться при температуре не выше 25 °C до 24 ч.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2016.
Фармакологическая группа
Характеристика
Афлиберцепт производится с помощью технологии рекомбинантной ДНК с использованием экспрессионной системы клеток яичника китайского хомячка (СНО) К-1.
Афлиберцепт является химерным гликопротеином с молекулярной массой 97 кДа, гликозилирование белка добавляет 15% к общей молекулярной массе, в результате чего общая молекулярная масса афлиберцепта составляет 115 кДа.
Фармакология
Фармакодинамика
Афлиберцепт — это рекомбинантный гибридный белок, состоящий из связывающихся с VEGF (vascular endothelial growth factor, эндотелиальный фактор роста сосудов) частей внеклеточных доменов рецептора VEGF-1 и VEGF-2, соединенных с доменом Fc (фрагмент, способный к кристаллизации) IgG1 человека.
Эндотелиальный фактор роста сосудов A (VEGF-A), эндотелиальный фактор роста сосудов В (VEGF-B) и плацентарный фактор роста (PLGF) относятся к VEGF-семейству ангиогенных факторов, которые могут действовать как сильные митогенные, хемотаксические и влияющие на сосудистую проницаемость факторы для эндотелиальных клеток. Действие VEGF-A осуществляется через две рецепторные тирозинкиназы — VEGFR-1 и VEGFR-2, находящиеся на поверхности эндотелиальных клеток. PLGF и VEGF-B связываются только с рецепторной тирозинкиназой VEGFR-1, которая, кроме локализации на поверхности эндотелиальных клеток, присутствует еще и на поверхности лейкоцитов. Чрезмерная активация этих рецепторов VEGF-A может приводить к патологической неоваскуляризации и повышению проницаемости сосудов. PLGF также имеет отношение к развитию патологической неоваскуляризации и инфильтрации опухоли клетками воспаления.
Афлиберцепт действует как растворимый «рецептор-ловушка», который связывается с VEGF-A с большей аффинностью, чем нативные рецепторы VEGF-A, кроме этого он также связывается с родственными лигандами VEGF-B и PLGF. Афлиберцепт связывается с человеческими VEGF-A, VEGF-B и PLGF с образованием стабильных инертных комплексов, не обладающих биологической активностью. Действуя в качестве «ловушки» для лигандов, афлиберцепт предотвращает связывание эндогенных лигандов с соответствующими им рецепторами и благодаря этому блокирует передачу сигналов через эти рецепторы.
Афлиберцепт блокирует активацию рецепторов VEGF и пролиферацию эндотелиальных клеток, тем самым подавляя образование новых сосудов, снабжающих опухоли кислородом и питательными веществами.
Афлиберцепт связывается с VEGF-A человека (равновесная константа диссоциации (Кд) — 0,5 пмоля для VEGF-A165 и 0,36 пмоля для VEGF-A121); с PLGF человека (Кд — 39 пмоля для PLGF-2); с VEGF-B человека (Кд — 1,92 пмоля) с образованием стабильного инертного комплекса, не обладающего биологической активностью, поддающейся определению.
Применение афлиберцепта у мышей с ксенотрансплантированными или аллотрансплантированными опухолями ингибировало рост различных типов аденокарцином.
Метастатический колоректальный рак (МКРР)
У пациентов с МКРР, которым ранее проводилась оксалиплатинсодержащая химиотерапия (с предшествующим введением бевацизумаба или без предшествующего введения бевацизумаба), химиотерапевтическая схема афлиберцепт/FOLFIRI (фторурацил, иринотекан, кальция фолинат) продемонстрировала статистически достоверное увеличение продолжительности жизни по сравнению с химиотерапевтической схемой FOLFIRI.
Неоваскулярная (влажная) возрастная макулярная дегенерация (влажная ВМД)
Влажная ВМД характеризуется патологической неоваскуляризацией хориоидеи. Просачивание крови и жидкости из патологически неоваскуляризированной хориоидеи может вызвать утолщение сетчатки или отек и/или кровоизлияния в сетчатку/субретинальное пространство, что приводит к снижению остроты зрения. Безопасность и эффективность афлиберцепта при интравитреальном введении при влажной ВМД оценивалась в двух рандомизированых многоцентровых двойных слепых исследованиях с активным контролем VIEW-1 и VIEW-2. В этих исследованиях 2412 пациентов были рандомизированы в соотношении 1:1:1:1 на получение афлиберцепта или ранибизумаба в следующих режимах: афлиберцепт 2 мг каждые 8 нед после 3 первоначальных ежемесячных инъекций; афлиберцепт 2 мг каждые 4 нед; афлиберцепт 0,5 мг каждые 4 нед; ранибизумаб 0,5 мг каждые 4 нед.
В исследования были включены пациенты в возрасте от 49 до 99 лет, средний возраст составил 76 лет.
На 2-м году исследований пациенты продолжали получать средства в той же дозе, которая была назначена им исходно, но в модифицированном режиме дозирования, который, согласно протоколу, основывался на результатах изменения остроты зрения и анатомических показателей, при этом максимальный интервал между инъекциями составлял не более 12 нед.
В обоих исследованиях первичной конечной точкой эффективности была доля пациентов, у которых поддерживалась достигнутая острота зрения, что подразумевало потерю <15 букв по шкале ETDRS (Early Treatment Diabetic Retinopathy Study, Исследование Раннего Лечения Диабетической Ретинопатии) на 52-й нед по сравнению с исходным состоянием.
В исследовании VIEW-1 на 52-й нед достигнутое улучшение остроты зрения поддерживалось у 95,1% пациентов, получавших афлиберцепт 2 мг каждые 8 нед после 3 первоначальных ежемесячных инъекций, по сравнению с 94,4% пациентов, получавших ранибизумаб 0,5 мг каждые 4 нед.
В исследовании VIEW-2 на 52-й нед достигнутое улучшение остроты зрения поддерживалось у 95,6% пациентов, получавших афлиберцепт 2 мг каждые 8 нед после 3 первоначальных ежемесячных инъекций, по сравнению с 94,4% пациентов, получавших ранибизумаб 0,5 мг каждые 4 нед.
В обоих исследованиях было показано, что афлиберцепт и ранибизумаб, применявшийся в дозе 0,5 мг каждые 4 нед, сопоставимы по клинической эффективности.
Подробное описание результатов анализа объединенных данных обоих исследований приведено в таблице 1.
Таблица 1
Оценка эффективности на 52-й и 96-й нед; комбинированные данные исследований VIEW-1 и VIEW-2
|
Оценка эффективности |
Афлиберцепт 2 мг каждые 8 нед после 3 первоначальных ежемесячных инъекций (N=607) | Ранибизумаб 0,5 мг каждые 4 нед (N=595) | ||
| 52-я нед | 96-я нед1 | 52-я нед | 96-я нед1 | |
| Среднее число инъекций | 7,6 | 11,2 | 12,3 | 16,5 |
| Среднее число инъекций в течение второго года (недели 52–96) | 4,2 | 4,7 | ||
| Доля пациентов, у которых поддерживалось достигнутое улучшение остроты зрения (потеря <15 букв для остроты зрения с максимальной коррекцией) | 95,33% | 92,42% | 94,42% | 91,6% |
| Среднее изменение остроты зрения с максимальной коррекцией, измеренной по шкале ETDRS, по сравнению с исходным состоянием | 8,4 | 7,62 | 8,74 | 7,89 |
| Доля пациентов, прибавивших по крайней мере 15 букв по шкале ETDRS по сравнению с исходным состоянием | 30,97% | 33,44% | 32,44% | 31,6% |
1Начиная с 52-й нед лечение проводилось в модифицированном режиме дозирования, при котором пациенты могли получать средство каждые 4 нед, но не реже чем 1 раз в 12 нед, в соответствии с определенными критериями продолжения лечения.
На 96-й нед исследований доля пациентов, прибавивших не менее 15 букв по шкале ETDRS по сравнению с исходным состоянием, составляла 33,44% в группе афлиберцепта 2 мг каждые 8 нед после 3 первоначальных ежемесячных инъекций и 31,6% в группе ранибизумаба 0,5 мг каждые 4 нед.
В обоих исследованиях было отмечено уменьшение зоны патологической неоваскуляризации во всех группах с разными режимами дозирования.
У пациентов, получавших терапию афлиберцептом (1 инъекция в месяц в течение 3 последовательных месяцев, затем одна инъекция каждые 2 мес), толщина сетчатки и средний размер области патологической неоваскуляризации уменьшились вскоре после начала лечения, что соответствует результатам, полученным при применении ранибизумаба в дозе 0,5 мг каждый месяц.
Достигнутое уменьшение размера зоны патологической неоваскуляризации и толщины сетчатки оставалось стабильным на втором году исследований.
Макулярный отек, развившийся вследствие окклюзии центральной вены сетчатки (ОЦВС) или ее ветвей (ОВВС)
При ОЦВС и ОВВС развивается ишемия сетчатки, что является сигналом к высвобождению VEGF, что в свою очередь приводит к дестабилизации плотных контактов и стимулирует пролиферацию эндотелиальных клеток. Повышенная экспрессия VEGF связана с нарушением гематоофтальмического барьера, повышением проницаемости сосудов, что приводит к отеку сетчатки, стимуляции роста эндотелиальных клеток и неоваскуляризации.
Безопасность и эффективность афлиберцепта оценивались в двух рандомизированных многоцентровых двойных слепых контролируемых исследованиях COPERNICUS и GALILEO, включавших 358 пациентов с макулярным отеком, развившимся вследствие ОЦВС. В обоих исследованиях пациенты были рандомизированы в соотношении 3:2 для получения 2 мг афлиберцепта каждые 4 нед или в контрольную группу для получения имитаций инъекций каждые 4 нед.
После 6 ежемесячных инъекций пациенты продолжали получать лечение только в том случае, если они соответствовали заранее определенным критериям для продолжения терапии, за исключением пациентов контрольной группы в исследовании GALILEO, которые продолжали получать имитации инъекций до 52-й нед. С этого момента всем пациентам терапия проводилась в том случае, если они соответствовали заранее определенным критериям.
В исследования были включены пациенты в возрасте от 22 до 89 лет, средний возраст составил 64 года.
В обоих исследованиях первичной конечной точкой эффективности являлась доля пациентов, у которых острота зрения с максимальной коррекцией увеличилась по крайней мере на 15 букв через 24 нед по сравнению с исходным состоянием.
Различия между группами были статистически значимыми в пользу афлиберцепта в обоих исследованиях. В обоих исследованиях улучшение остроты зрения с максимальной коррекцией было достигнуто через 3 мес с последующей стабилизацией эффекта до 6 мес, как в отношении остроты зрения, так и толщины сетчатки в центральной зоне. Статистически значимые различия сохранялись вплоть до 52-й нед.
Описание результатов анализа обоих исследований приведено в таблице 2.
Таблица 2
Оценка эффективности в исследованиях COPERNICUS и GALILEO на 24, 52 и 76/110-й нед
| Оценка эффективности | Доля пациентов, у которых острота зрения с максимальной коррекцией увеличивалась на ?15 букв по сравнению с исходным состоянием |
Среднее изменение остроты зрения с максимальной коррекцией по шкале ETDRS по сравнению с исходным состоянием (SD1) |
||
| COPERNICUS | 24-я нед | Контроль (N=73) | 12% | ?4 (18) |
| Афлиберцепт 2 мг каждые 4 нед (N=114) |
56% | 17,3 (12,8) | ||
| 52-я нед | Контроль2 (N=73) | 30% | 3,8 (17,1) | |
| Афлиберцепт 2 мг (N=114) | 55% | 16,2 (17,4) | ||
| 100-я нед | Контроль2,3 (N=77) | 23,3% | 1,5 (17,7) | |
| Афлиберцепт3 2 мг (N=114) | 49,1% | 13 (17,7) | ||
| GALILEO | 24-я нед | Контроль (N=68) | 22% | 3,3 (14,1) |
| Афлиберцепт 2 мг каждые 4 нед (N=103) | 60% | 18 (12,2) | ||
| 52-я нед | Контроль (N=68) | 32% | 3,8 (18,1) | |
| Афлиберцепт 2 мг (N=103) | 60% | 16,9 (14,8) | ||
| 76-я нед | Контроль4 (N=68) | 29,4% | 6,2 (17,7) | |
| Афлиберцепт4 2 мг (N=103) | 57% | 13,7 (17,8) |
1SD: Standard Deviation, стандартное отклонение.
2В исследовании COPERNICUS пациенты контрольной группы могли получать афлиберцепт по потребности каждые 4 нед в течение периода с 24-й до 52-й нед; пациенты посещали врача каждые 4 нед.
3В исследовании COPERNICUS и контрольная группа, и группа афлиберцепта 2 мг получали афлиберцепт 2 мг по потребности каждые 4 нед с 52-й по 96-ю нед: пациенты в обязательном порядке посещали врача каждый квартал, но при необходимости могли приходить на прием каждые 4 нед.
4В исследовании GALILEO с 52-й по 68-ю нед и контрольная группа, и группа афлиберцепта 2 мг получали афлиберцепт 2 мг по потребности каждые 8 нед; пациенты приходили на прием в обязательном порядке каждые 8 нед.
Безопасность и эффективность афлиберцепта оценивались в рандомизированном многоцентровом двойном слепом контролируемом исследовании VIBRANT, включавшем 181 пациента с макулярным отеком, развившимся вследствие ОВВС, в т.ч. гемиокклюзии центральной вены сетчатки. В данном исследовании пациенты были рандомизированы в соотношении 1:1 для получения афлиберцепта в дозе 2 мг каждые 8 нед после 6 первоначальных ежемесячных инъекций, или в группу пациентов, изначально получавших лазерную фотокоагуляцию (активный контроль). Начиная с 12-й нед при необходимости пациенты группы активного контроля могли получать дополнительную лазерную фотокоагуляцию (резервное лазерное лечение). Минимальный интервал между сеансами лазерной фотокоагуляции составлял 12 нед. Начиная с 24-й нед пациенты группы активного контроля, удовлетворяющие заранее определенным критериям, могли получать резервное лечение афлиберцептом в дозе 2 мг каждые 4 нед в течение 3 мес, затем интравитреальные инъекции каждые 8 нед.
В исследование были включены пациенты в возрасте от 42 до 94 лет, средний возраст составил 65 лет.
В исследовании VIBRANT первичной конечной точкой эффективности являлась доля пациентов, у которых острота зрения с максимальной коррекцией увеличилась по крайней мере на 15 букв через 24 нед по сравнению с исходным состоянием. На 24-й нед этот показатель в группе афлиберцепта превосходил показатель в группе активного контроля.
В исследовании VIBRANT вторичной конечной точкой эффективности была толщина сетчатки, по результатам оптической когерентной томографии (ОКТ) на 24-й нед, по сравнению с исходными показателями. Различия между группами были статистически значимыми в пользу данных группы афлиберцепта. Улучшение зрения происходило быстро, и максимальное улучшение остроты зрения достигалось через 3 мес с последующей стабилизацией достигнутых значений остроты зрения и толщины сетчатки в центральной зоне до 6 мес и последующим сохранением достигнутых значений до 12 мес.
Начиная с 24-й нед 67 пациентов группы активного контроля получали резервное лечение афлиберцептом (группа активный контроль/афлиберцепт 2 мг). У пациентов этой группы острота зрения увеличилась в среднем на 5 букв с 24-й нед по 52-ю нед.
Описание результатов анализа обоих исследований приведено в таблице 3.
Таблица 3
Оценка эффективности в исследовании VIBRANT на 24-й и 52-й нед
| Оценка эффективности | Доля пациентов, у которых острота зрения с максимальной коррекцией увеличилась на ?15 букв по сравнению с исходным состоянием |
Среднее изменение остроты зрения с максимальной коррекцией по шкале ETDRS по сравнению с исходным состоянием (SD1) |
|
| 24-я нед | Афлиберцепт 2 мг каждые 4 нед (N=91) | 52,7% | 17 (11,9) |
| Активный контроль (N=90) | 26,7% | 6,9 (12,9) | |
| 52-я нед | Афлиберцепт 2 мг каждые 8 нед (N=91)2 | 57,1% | 17,1 (13,1) |
| Активный контроль Афлиберцепт 2 мг (N=90)3 | 41,1% | 12,2 (11,9) |
1SD: Standard Deviation, стандартное отклонение.
2Интервал лечения для всех пациентов группы афлиберцепта был увеличен до 8 нед в течение периода с 24-й по 48-ю нед.
3Начиная с 24-й нед пациенты группы активного контроля, удовлетворяющие по крайней мере одному из заранее определенных критериев приемлемости, могли получать резервное лечение афлиберцептом (всего 67 пациентов). Фиксированный режим резервного лечения афлиберцептом — афлиберцепт в дозе 2 мг каждые 4 нед в течение 3 мес, затем интравитреальные инъекции каждые 8 нед.
Пожилые пациенты. В исследованиях по показанию ОВВС примерно 58% пациентов, рандомизированных в группу афлиберцепта, были в возрасте 65 лет или старше, и примерно 23% — в возрасте 75 лет или старше.
В исследованиях COPERNICUS и GALILEO (ОЦВС) и VIBRANT (ОВВС) вторичной конечной точкой эффективности была толщина сетчатки по результатам ОКТ на 24-й нед по сравнению с исходными показателями. В трех исследованиях среднее изменение толщины сетчатки в центральной зоне на 24-й нед при применении афлиберцепта статистически значимо превосходило исходные значения.
У пациентов, получавших афлиберцепт (одна ежемесячная инъекция в течение 6 мес), отмечался постоянный, быстрый и выраженный ответ со стороны морфологических показателей (толщина сетчатки в центральной зоне по результатам ОКТ). Улучшение средних показателей толщины сетчатки в центральной зоне сохранялось до 24-й нед.
Диабетический макулярный отек (ДМО)
ДМО характеризуется повышением проницаемости сосудов и повреждением капилляров сетчатки, что может привести к потере остроты зрения.
Безопасность и эффективность афлиберцепта у пациентов с ДМО оценивались в двух рандомизированных многоцентровых двойных слепых исследованиях с активным контролем. Всего было рандомизировано 862 пациента. Из них 576 пациентов были рандомизированы в группы афлиберцепта в двух исследованиях (VIVID-DME и VISTA-DME). В каждом исследовании пациенты были случайным образом распределены на три группы в соотношении 1:1:1 — афлиберцепт 2 мг каждые 8 нед в течение первых 5 мес; афлиберцепт 2 мг каждые 4 нед; лазерная фотокоагуляция макулярной зоны (активный контроль).
Начиная с 24-й нед пациенты, удовлетворяющие заранее определенным пороговым значениям потери зрения, могли получать дополнительную терапию: пациенты в группах афлиберцепта могли получать лазерную фотокоагуляцию, а пациенты в группе лазерной фотокоагуляции — терапию афлиберцептом.
В исследования были включены пациенты в возрасте от 23 до 87 лет; средний возраст составил 63 года.
В обоих исследованиях первичной конечной точкой эффективности являлось среднее значение изменения остроты зрения с максимальной коррекцией по шкале ETDRS на 52-й нед по сравнению с исходным состоянием. Показатели эффективности лечения в группах афлиберцепта 2 мг каждые 8 нед в течение первых 5 мес и 2 мг каждые 4 нед статистически значимо превосходили показатели в группе лазерной терапии. Подробное описание результатов исследований VIVID-DME и VISTA-DME приведено в таблице 4.
Таблица 4
Оценка эффективности на 52-й нед в исследованиях VIVID-DME и VISTA-DME
|
Оценка эффективности |
VIVID-DME | VISTA-DME | ||||
| 52-я нед | 52-я нед | |||||
| Афлиберцепт 2 мг каждые 8 нед в течение первых 5 мес1(N=135) | Афлиберцепт 2 мг каждые 4 нед (N=136) | Активный контроль (лазер) (N=132) | Афлиберцепт 2 мг каждые 8 нед в течение первых 5 мес1(N=151) | Афлиберцепт 2 мг каждые 4 нед (N=154) | Активный контроль (лазер) (N=154) | |
| Среднее изменение остроты зрения с максимальной коррекцией по шкале ETDRS по сравнению с исходным состоянием | 10,7 | 10,5 | 1,2 | 10,7 | 12,5 | 0,2 |
| Доля пациентов, у которых улучшение остроты зрения с максимальной коррекцией составило ?15 букв по шкале ETDRS по сравнению с исходным состоянием | 33% | 32% | 9% | 31% | 42% | 8% |
1После 5 первоначальных ежемесячных инъекций.
Исходы лечения на втором году исследования VISTA-DME согласуются с результатами, полученными на 52-й нед.
Пациенты с билатеральным поражением могли получать анти-VEGF-терапию другого глаза, если лечащий врач считал это необходимым. В исследовании VISTA-DME 198 пациентам (65%), получавшим афлиберцепт, выполнялись инъекции афлиберцепта в оба глаза; в исследовании VIVID-DME 70 (26%) пациентам, получавшим афлиберцепт, выполнялись инъекции различных анти-VEGF-средств в другой глаз.
Пожилые пациенты. В исследованиях III фазы по показанию диабетический макулярный отек примерно 47% пациентов, рандомизированных в группу афлиберцепта, были в возрасте 65 лет или старше, и примерно 9% — в возрасте 75 лет и старше. Параметры эффективности и безопасности были сопоставимы с таковыми для общей популяции.
Вскоре после начала терапии у пациентов, получавших терапию афлиберцептом, наблюдался быстрый и выраженный ответ со стороны морфологических показателей (толщина сетчатки в центральной зоне) по результатам ОКТ. Среднее изменение толщины сетчатки в центральной зоне по сравнению с исходными показателями на 52-й нед было более выражено в группе афлиберцепта.
В исследовании VIVID-DME на 52-й нед толщина сетчатки в центральной зоне по результатам ОКТ уменьшилась в среднем на 192,4 мкм в группе афлиберцепта 2 мг каждые 8 нед в течение первых 5 мес и на 66,2 мкм в группе лазерной терапии. В исследовании VISTA-DME также отмечалось уменьшение толщины сетчатки в центральной зоне по результатам ОКТ (на 183,1 и 73,3 мкм для афлиберцепта 2 мг каждые 8 нед в течение первых 5 мес и группы лазерной терапии соответственно).
Фармакокинетика
Абсорбция. В доклинических исследованиях, проведенных на моделях опухолей, биологически активные дозы афлиберцепта коррелировали с дозами, необходимыми для создания концентраций циркулирующего в системном кровотоке свободного афлиберцепта, превышающих концентрации циркулирующего в системном кровотоке афлиберцепта, связанного с VEGF. После в/в введения концентрации циркулирующего в системном кровотоке связанного с VEGF афлиберцепта при повышении его дозы увеличиваются до тех пор, пока бoльшая часть VEGF не оказывается связанной. Дальнейшее увеличение дозы афлиберцепта приводит к дозозависимому увеличению концентрации циркулирующего в системном кровотоке свободного афлиберцепта и только к небольшому дальнейшему возрастанию концентрации связанного с VEGF афлиберцепта.
У пациентов афлиберцепт вводится в/в в дозе 4 мг/кг в/в каждые 2 нед, в течение которых имеет место избыток концентрации циркулирующего свободного афлиберцепта над концентрацией афлиберцепта, связанного с VEGF.
При рекомендованной дозе 4 мг/кг 1 раз в 2 нед концентрации свободного афлиберцепта, близкие к величинам Css, достигались в течение второго цикла лечения практически без накопления (коэффициент накопления 1,2 в равновесном состоянии по сравнению с концентрацией свободного афлиберцепта при первом введении).
После интравитреального введения афлиберцепт медленно всасывается в системный кровоток, где обнаруживается в основном в виде неактивного, стабильного комплекса с VEGF; при этом только свободный афлиберцепт может связывать эндогенный VEGF.
В исследовании фармакокинетики с частым отбором проб у 6 пациентов с неоваскулярной ВМД Cmax свободного афлиберцепта (системная Сmax) в течение 1–3 дней после интравитреальной инъекции дозы 2 мг была низка, составляла в среднем примерно 0,02 мкг/мл (диапазон от 0 до 0,054) и была неопределима через 2 нед после интравитреальной инъекции практически у всех пациентов. Афлиберцепт не кумулировал в плазме крови при интравитреальном введении каждые 4 нед.
Распределение. После в/в введения Vss свободного афлиберцепта составляет 8 л.
После интравитреального введения средняя Сmax свободного афлиберцепта примерно в 50–500 раз ниже, чем концентрация, необходимая для ингибирования биологической активности VEGF в системном кровотоке на 50% на моделях у животных, у которых изменения АД наблюдались после достижения концентрации свободного афлиберцепта в системном кровотоке около 10 мкг/мл, давление возвращалось к нормальным значениям при снижении концентрации ниже 1 мкг/мл. Ожидается, что средняя Сmax свободного афлиберцепта после интравитреальной инъекции 2 мг афлиберцепта пациентам будет более чем в 100 раз ниже, чем концентрация афлиберцепта, необходимая для связывания половины системного VEGF (2,91 мкг/мл) у здоровых добровольцев. Таким образом, развитие системных фармакодинамических эффектов, таких как изменения АД, маловероятно.
Величина средней Сmax свободного афлиберцепта в плазме, согласно результатам дополнительных фармакокинетических исследований с участием пациентов с ОЦВС, ОВВС и ДМО, находилась в диапазоне от 0,03 до 0,05 мкг/мл, индивидуальные значения не превышали 0,14 мкг/мл. Впоследствии плазменные концентрация свободного афлиберцепта снижались до значений ниже или близких к нижнему пределу количественного определения, как правило, в течение одной недели. По истечении 4 нед, перед следующим применением у всех пациентов концентрация была неопределяема.
Метаболизм. Так как афлиберцепт является белком, исследования его метаболизма не проводились. Ожидается, что афлиберцепт будет расщепляться на небольшие пептиды и отдельные аминокислоты.
Элиминация. Циркулирующий в системном кровотоке свободный афлиберцепт главным образом связывается с VEGF-семейством с образованием стабильных неактивных комплексов. Ожидается, что, как и другие крупные белки, связанный с VEGF и свободный афлиберцепт будет постепенно выводиться из системного кровотока за счет других биологических механизмов, таких как протеолитический катаболизм.
При дозах, превышающих 2 мг/кг (в/в введение), клиренс свободного афлиберцепта составлял 1 л/сут с конечным T1/2 6 дней.
Высокомолекулярные белки не выводятся почками, поэтому ожидается, что почечное выведение афлиберцепта будет минимальным.
Линейность/нелинейность элиминации. В связи с целевым связыванием афлиберцепта с его мишенью (эндогенный VEGF) свободный афлиберцепт при дозах ниже 2 мг/кг (в/в введение) показал быстрое (нелинейное) снижение его концентраций в системном кровотоке, по-видимому связанное с его высокоаффинным связыванием с эндогенным VEGF. В диапазоне доз от 2 до 9 мг/кг клиренс свободного афлиберцепта становится линейным, по-видимому за счет ненасыщаемых биологических механизмов выведения, таких как катаболизм белка.
Особые группы пациентов
Дети. При в/в введении афлиберцепт в дозах 2; 2,5 и 3 мг/кг каждые 2 нед 8 пациентам детского возраста с сoлидными опухолями (от 5 до 17 лет) средний T1/2 свободного афлиберцепта, определяемый после введения первой дозы, составлял приблизительно 4 дня (от 3 до 6 дней).
Афлиберцепт для интравитреального введения не применяется у данной группы пациентов по показаниям влажная ВМД, ОЦВС, ОВВС и ДМО.
Пациенты пожилого возраста. Возраст не влияет на фармакокинетику афлиберцепта при в/в введении.
Соблюдения каких-либо специальных условий применения афлиберцепта для интравитреального введения не требуется. Опыт применения у пациентов с ДМО старше 75 лет ограничен.
Половая принадлежность. Несмотря на различия в клиренсе свободного афлиберцепта и Vd у мужчин и женщин, не наблюдались связанные с половой принадлежностью различия в его системной экспозиции при в/в применении в дозе 4 мг/кг.
Масса тела. Масса тела влияла на клиренс свободного афлиберцепта и Vd после в/в введения; так у пациентов с массой тела более 100 кг наблюдалось увеличение системной экспозиции афлиберцепта на 29%.
Расовая принадлежность. Расовая и этническая принадлежность не оказывала влияние на фармакокинетику афлиберцепта.
Печеночная недостаточность. Официальные исследования по применению афлиберцепта для в/в введения у пациентов с печеночной недостаточностью не проводились.
У пациентов с легкой (концентрация общего билирубина в крови ?1,5 ВГН при любых значениях активности ACT) и средней (концентрация общего билирубина в крови >1,5–3 ВГН при любых значениях активности ACT) печеночной недостаточностью не было выявлено изменение клиренса афлиберцепта. Отсутствуют данные по фармакокинетике афлиберцепта у пациентов с тяжелой степенью печеночной недостаточности (концентрация общего билирубина в крови >3 ВГН при любых значениях активности ACT).
Почечная недостаточность. Официальные исследования по применению афлиберцепта для в/в введения у пациентов с почечной недостаточностью не проводились.
Не обнаружены различия в системной экспозиции (AUC) свободного афлиберцепта у пациентов с почечной недостаточностью различных степеней тяжести при применении афлиберцепта для в/в введения в дозе 4 мг/кг.
Никаких специальных исследований с участием пациентов с нарушенной функцией почек, получающих афлиберцепт для интравитреального введения, не проводилось.
Анализ фармакокинетических данных исследования VIEW-2 показал, что у 40% пациентов с нарушениями функции почек (24% — легкой степени, 15% — умеренной степени и 1% — тяжелой степени) после интравитреального введения каждые 4 или 8 нед различий в плазменных концентрациях этого средства не отмечалось.
Схожие результаты были получены у пациентов с ОЦВС в исследовании GALILEO и пациентов с ДМО в исследовании VIVID-DME.
Показания к применению
Метастатический колоректальный рак (взрослые пациенты), резистентный к оксалиплатинсодержащей химиотерапии или прогрессирующий после ее применения (в комбинации с режимом, включающим иринотекан, фторурацил, кальция фолинат (FOLFIRI).
Неоваскулярная (влажная) возрастная макулярная дегенерация; снижение остроты зрения, вызванное макулярным отеком вследствие окклюзии вен сетчатки (центральной вены или ее ветвей); снижение остроты зрения, вызванное диабетическим макулярным отеком.
Противопоказания
Для в/в введения: гиперчувствительность к афлиберцепту; тяжелые кровотечения; артериальная гипертензия, не поддающаяся медикаментозной коррекции; хроническая сердечная недостаточность III–IV класса (по классификации NYHA); тяжелая степень печеночной недостаточности (отсутствие данных по применению); офтальмологическое применение или введение в стекловидное тело; беременность; период грудного вскармливания; детский и подростковый возраст до 18 лет (в связи с отсутствием достаточного опыта применения).
Для интравитреального введения: повышенная чувствительность к афлиберцепту; беременность и период грудного вскармливания, за исключением случаев, когда потенциальная польза для матери превышает потенциальный риск для плода (см. «Применение при беременности и кормлении грудью»); возраст до 18 лет.
Ограничения к применению
Для в/в введения: тяжелая степень почечной недостаточности; артериальная гипертензия; клинически значимые заболевания ССС (ишемическая болезнь сердца, хроническая сердечная недостаточность I–II класса по классификации NYHA); пожилой возраст; общее состояние >2 баллов по оценочной шкале общего состояния пациента ECOG (Eastern Cooperative Oncology Group, Восточная Объединенная Группа Онкологов).
Для интравитреального введения: плохо контролируемая глаукома (не следует вводить при ВГД ≥30 мм рт.ст.) (см. «Меры предосторожности»); перенесенные инсульт, транзиторная ишемическая атака или инфаркт миокарда в течение последних 6 мес (при лечении ОЦВС, ОВВС или ДМО) (см. «Меры предосторожности»); наличие факторов риска нарушения целостности пигментного эпителия сетчатки (см. «Меры предосторожности»).
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.
Данные по применению афлиберцепта у беременных женщин отсутствуют. Исследования, проведенные у животных, выявили у афлиберцепта эмбриотоксическое и тератогенное действие. Так как ангиогенез имеет большое значение для развития эмбриона, ингибирование ангиогенеза при введении афлиберцепта может привести к неблагоприятным для развития беременности эффектам. Применение афлиберцепта во время беременности и у женщин, у которых возможно наступление беременности, противопоказано.
Женщинам детородного возраста следует рекомендовать избегать наступления беременности во время лечения афлиберцептом, и они должны быть проинформированы о возможности неблагоприятного воздействия этого средства на плод.
Женщины детородного возраста и фертильные мужчины должны использовать эффективные способы контрацепции во время лечения и как минимум в течение до 6 мес после последней в/в дозы или 3 мес после последней интравитреальной инъекции афлиберцепта (см. «Меры предосторожности»).
Имеется возможность нарушения фертильности у мужчин и женщин во время лечения афлиберцептом (исходя из данных, полученных в исследованиях, проведенных на обезьянах, у самцов и самок которых афлиберцепт вызывал нарушения фертильности, полностью обратимые через 8–18 нед).
Клинические исследования для оценки воздействия афлиберцепта на выработку грудного молока, выделение афлиберцепта в грудное молоко и его влияния на грудных детей не проводились.
Неизвестно, выделяется ли афлиберцепт в женское грудное молоко. Однако из-за того что нельзя пока исключить возможность проникновения афлиберцепта в грудное молоко, а также из-за возможности развития серьезных нежелательных реакций, вызываемых афлиберцептом у грудных детей, необходимо или отказаться от грудного вскармливания, или не применять афлиберцепт (в зависимости от важности применения средства для матери).
Побочные действия
Клинические исследования безопасности при в/в введении. Наиболее часто встречающимися нежелательными реакциями (HP) (всех степеней тяжести, с частотой ≥20%), наблюдавшимися по крайней мере на 2% чаще при применении химиотерапевтической схемы афлиберцепт/FOLFIRI, чем при применении химиотерапевтической схемы FOLFIRI, были следующие HP (в порядке снижения частоты возникновения): лейкопения, диарея, нейтропения, протеинурия, повышение активности ACT, стоматит, утомляемость, тромбоцитопения, повышение активности АЛТ, повышение АД, снижение массы тела, уменьшение аппетита, носовые кровотечения, абдоминальные боли, дисфония, повышение концентрации креатинина в сыворотке крови и головная боль.
Наиболее часто встречающимися HP 3–4-й степени тяжести (с частотой ≥5%), наблюдавшимися по крайней мере на 2% чаще при применении химиотерапевтической схемы афлиберцепт/FOLFIRI по сравнению с химиотерапевтической схемой FOLFIRI, были следующие HP (в порядке снижения частоты возникновения): нейтропения, диарея, повышение АД, лейкопения, стоматит, утомляемость, протеинурия и астения.
В целом прекращение терапии в связи с возникновением нежелательных явлений (всех степеней тяжести) наблюдалось у 26,8% пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, по сравнению с 12,1% пациентов, получавших химиотерапевтическую схему FOLFIRI. Наиболее часто встречающимися НР, которые послужили причиной для отказа от терапии у ≥1% пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, были: астения/утомляемость, инфекции, диарея, дегидратация, повышение АД, стоматит, венозные тромбоэмболические осложнения, нейтропения и протеинурия.
Коррекция дозы афлиберцепта (уменьшение дозы и/или пропуски введения) проводилась у 16,7%. Отсрочки последующих циклов терапии, превышающие 7 дней, наблюдались у 59,7% пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, по сравнению с 42,6% пациентов, получавших химиотерапевтическую схему FOLFIRI.
Смерть от других причин, кроме прогрессирования заболевания, наблюдавшаяся в течение 30 дней после последнего цикла изучаемой химиотерапевтической схемы, была зафиксирована у 2,6% пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, и у 1% пациентов, получавших химиотерапевтическую схему FOLFIRI. Причиной смерти пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, были: инфекция (в т.ч. нейтропенический сепсис) у 4 пациентов; дегидратация у 2 пациентов; гиповолемия у 1 пациента; метаболическая энцефалопатия у 1 пациента; заболевания дыхательных путей (острая дыхательная недостаточность, аспирационная пневмония и ТЭЛА) у 3 пациентов; расстройства со стороны ЖКТ (кровотечение из язвы двенадцатиперстной кишки, воспаление ЖКТ, полная непроходимость кишечника) у 3 пациентов; летальный исход от неизвестных причин у 2 пациентов.
Ниже представлены HP и отклонения от нормы лабораторных показателей, наблюдавшиеся у пациентов, получавших химиотерапевтическую схему афлиберцепт/FOLFIRI, с разделением их по системно-органным классам в соответствии с классификацией MedDRA.
Представленные ниже HP определялись как любые нежелательные клинические реакции или отклонения от нормы лабораторных показателей, имеющие на ≥2% бóльшую частоту (для HP всех степеней тяжести) в группе лечения афлиберцептом по сравнению с группой плацебо, в исследовании, проведенном у пациентов с МКРР. Интенсивность HP классифицировалась в соответствии с NCI CTC (National Cancer Institute Common Terminology Criteria, оценочная шкала Общих Критериев Токсичности Национального Института Рака США), версия 3.0.
Частота возникновения HP определялась в соответствии с классификацией ВОЗ следующим образом: очень часто (≥10%); часто (≥1, <10%); нечасто (≥0,1, <1%); редко (≥0,01, <0,1%); очень редко (<0,01%); частота неизвестна (по имеющимся данным определить частоту встречаемости не представляется возможным).
Инфекционные и паразитарные заболевания: очень часто — инфекции (всех степеней тяжести), включая инфекции мочевыводящих путей, назофарингит, инфекции верхних дыхательных путей, пневмонию, инфекции в месте введения катетера, зубные инфекции; часто — нейтропенические инфекции/сепсис (всех степеней тяжести, в т.ч. ≥3-й степени).
Со стороны крови и лимфатической системы: очень часто — лейкопения (всех степеней тяжести, в т.ч. ≥3-й степени), нейтропения (всех степеней тяжести, в т.ч. ≥3-й степени), тромбоцитопения (всех степеней тяжести); часто — фебрильная нейтропения (всех степеней тяжести, в т.ч. ≥3-й степени), тромбоцитопения (≥3-й степени тяжести).
Со стороны иммунной системы: часто — реакции гиперчувствительности (всех степеней тяжести); нечасто — реакции гиперчувствительности (≥3-й степени тяжести).
Нарушения обмена веществ и питания: очень часто — снижение аппетита (всех степеней тяжести); часто — дегидратация (всех степеней тяжести и в т.ч. ≥3-й степени), снижение аппетита (≥3-й степени тяжести).
Со стороны нервной системы: очень часто — головная боль (всех степеней тяжести); часто — головная боль (≥3-й степени тяжести); нечасто — синдром обратимой задней лейкоэнцефалопатии (СОЗЛ).
Со стороны сосудов: очень часто — повышение АД (всех степеней тяжести) (у 54% пациентов, у которых наблюдалось повышение АД (≥3-й степени тяжести), повышение АД развивалось в течение двух первых циклов лечения), кровотечения/кровоизлияния (всех степеней тяжести), причем наиболее частым видом кровотечений были малые носовые кровотечения (1–2-й степени тяжести); часто — артериальные тромбоэмболические осложнения (АТЭО) (такие как острые нарушения мозгового кровообращения (включая транзиторные цереброваскулярные ишемические атаки) стенокардию, внутрисердечный тромб, инфаркт миокарда, артериальную тромбоэмболию и ишемический колит) (всех степеней тяжести), венозные тромбоэмболические осложнения (тромбоз глубоких вен и ТЭЛА) всех степеней тяжести, кровотечения (≥3-й степени тяжести, иногда с летальным исходом), включая желудочно-кишечные кровотечения, гематурию, кровотечения после медицинских процедур; частота неизвестна — у пациентов, получавших афлиберцепт, сообщалось о развитии тяжелых внутричерепных кровоизлияний и легочных кровотечений/кровохарканья, в т.ч. с летальным исходом.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — одышка (всех степеней тяжести), носовое кровотечение (всех степеней тяжести), дисфония (всех степеней тяжести); часто — боль в области ротоглотки (всех степеней тяжести), ринорея (наблюдалась ринорея только 1–2-й степени тяжести); нечасто — одышка (≥3-й степени тяжести), носовое кровотечение (≥3-й степени тяжести), дисфония (≥3-й степени тяжести), боль в области ротоглотки (≥3-й степени тяжести).
Со стороны ЖКТ: очень часто — диарея (всех степеней тяжести, в т.ч. ≥3-й степени), стоматит (всех степеней тяжести, в т.ч. ≥3-й степени), абдоминальные боли (всех степеней тяжести), боли в верхнем отделе живота (всех степеней тяжести); часто — абдоминальные боли (≥3-й степени тяжести), боли в верхнем отделе живота (≥3-й степени тяжести), геморрой (всех степеней тяжести), кровотечение из прямой кишки (всех степеней тяжести), боли в прямой кишке (всех степеней тяжести), зубная боль (всех степеней тяжести), афтозный стоматит (всех степеней тяжести), образование свищей (анальный, тонкокишечно-мочепузырный, наружный тонкокишечный (тонкокишечно-кожный), толстокишечно-влагалищный, межкишечный) (всех степеней тяжести); нечасто — образование желудочно-кишечных свищей (≥3-й степени тяжести), перфорации стенок ЖКТ (всех степеней тяжести в т.ч. ≥3-й степени), включая фатальные перфорации стенок ЖКТ, кровотечение из прямой кишки (≥3-й степени тяжести), афтозный стоматит (≥3-й степени тяжести), боли в прямой кишке (≥3-й степени тяжести).
Со стороны кожи и подкожных тканей: очень часто — синдром ладонно-подошвенной эритродизестезии (всех степеней тяжести); часто — гиперпигментация кожи (всех степеней тяжести), синдром ладонно-подошвенной эритродизестезии (≥3-й степени тяжести).
Со стороны почек и мочевыводящих путей: очень часто — протеинурия (по объединенным клиническим и лабораторным данным) (всех степеней тяжести), увеличение концентрации креатинина в сыворотке крови (всех степеней тяжести); часто — протеинурия (≥3-й степени тяжести); нечасто — нефротический синдром. Одному пациенту с протеинурией и повышением АД из 611 пациентов, получавших лечение по химиотерапевтической схеме афлиберцепт/FOLFIRI, был поставлен диагноз тромботической микроангиопатии.
Общие расстройства и реакции в месте введения: очень часто — астеническое состояние (всех степеней тяжести), чувство усталости (всех степеней тяжести, в т.ч. ≥3-й степени); часто — астеническое состояние (≥3-й степени тяжести); нечасто — нарушение заживления ран (расхождение краев раны, несостоятельность анастомозов) (всех степеней тяжести, в т.ч. ≥3-й степени).
Лабораторные и инструментальные данные: очень часто — повышение активности ACT, АЛТ (всех степеней тяжести), снижение массы тела (всех степеней тяжести); часто — повышение активности ACT, АЛТ (≥3-й степени тяжести), снижение массы тела (≥3-й степени тяжести).
Частота HP у особых групп пациентов
Пожилой возраст. У пациентов пожилого возраста (≥65 лет) частота возникновения диареи, головокружения, астении, уменьшения массы тела и дегидратации была более чем на 5% выше, чем у пациентов более молодого возраста. Пациенты пожилого возраста должны находиться под тщательным наблюдением на предмет развития диареи и/или возможной дегидратации.
Почечная недостаточность. У пациентов с нарушениями функции почек легкой степени на момент начала применения афлиберцепта частота возникновения HP была сопоставима с таковой у пациентов без нарушения функции почек на момент начала применения этого средства. У пациентов со средней и тяжелой степенью нарушений функции почек возникновение HP не со стороны почек в целом было сопоставимо с таковым у пациентов без почечной недостаточности, за исключением >10% превышения частоты развития дегидратации (всех степеней тяжести).
Иммуногенность. Как у всех других белковых ЛС, у афлиберцепта существует потенциальный риск иммуногенности. В целом, по результатам всех онкологических клинических исследований, ни у одного из пациентов не было обнаружено высокого титра антител к афлиберцепту.
Постмаркетинговое применение афлиберцепта
Со стороны сердца: частота неизвестна — сердечная недостаточность, снижение фракции выброса левого желудочка.
Со стороны скелетно-мышечной и соединительной ткани: частота неизвестна — остеонекроз челюсти. У пациентов, принимающих афлиберцепт, сообщалось о случаях развития остеонекроза челюсти, особенно у тех пациентов, которые имели определенные факторы риска развития остеонекроза челюсти, такие как применение бисфосфонатов и/или инвазивные стоматологические процедуры.
Клинические исследования безопасности при интравитреальном введении. 2957 пациентов, принимавших участие в семи исследованиях III фазы, составили популяцию по оценке безопасности. Из них 2356 пациентов получали рекомендованную дозу 2 мг.
Серьезные НР, связанные с процедурой введения, отмечались менее чем в 1 случае на 2200 интравитреальных инъекций афлиберцепта и включали слепоту, эндофтальмит, отслойку сетчатки, ятрогенную травматическую катаракту, кровоизлияние в стекловидное тело, катаракту, отслойку стекловидного тела и повышение ВГД (см. «Меры предосторожности»).
Наиболее распространенные НР (по крайней мере у 5% пациентов, получавших терапию афлиберцептом) включали субконъюнктивальное кровоизлияние (24,9%), снижение остроты зрения (10,7%), боль в глазу (9,9%), повышение ВГД (7,1%), отслойку стекловидного тела (6,8%), плавающие помутнения стекловидного тела (6,6%) и катаракту (6,6%).
Данные по безопасности, приведенные ниже, включают все НР, отмеченные в семи исследованиях III фазы при лечении по показаниям влажная ВМД, ОЦВС, ОВВС и ДМО с указанием возможности наличия причинно-следственной связи с процедурой введения или ЛС.
НР, представленные ниже, перечислены в соответствии с частотой встречаемости в клинических исследованиях и системно-органным классом. Частота встречаемости HP определялась в соответствии с классификацией ВОЗ следующим образом: очень часто (≥10%); часто (≥1, <10%); нечасто (≥0,1, <1%); редко (≥0,01, <0,1%); очень редко (<0,001%).
В пределах каждой системы НР реакции представлены в порядке уменьшения их тяжести.
Со стороны иммунной системы: нечасто — гиперчувствительность1.
Со стороны органа зрения: очень часто — кровоизлияния в сетчатку, снижение остроты зрения; часто — разрыв пигментного эпителия сетчатки2, отслойка пигментного эпителия сетчатки, дегенерация сетчатки, кровоизлияние в стекловидное тело, катаракта, ядерная катаракта, субкапсулярная катаракта, кортикальная катаракта, эрозия роговицы, микроэрозии роговицы, повышение ВГД, затуманивание зрения, плавающие помутнения стекловидного тела, отек роговицы, отслойка стекловидного тела, боль в месте введения, боль в глазу, чувство инородного тела в глазу, слезотечение, отек век, кровоизлияния в месте введения, точечный кератит, инъекция конъюнктивы век, инъекция конъюнктивы глазного яблока; нечасто — слепота, эндофтальмит3, отслойка сетчатки, разрыв сетчатки, ирит, увеит, иридоциклит, помутнение хрусталика, дефект эпителия роговицы, раздражение в месте введения, аномальная чувствительность тканей глаза, раздражение век, взвесь форменных элементов крови в передней камере; редко — ятрогенная травматическая катаракта, воспалительная реакция со стороны стекловидного тела (витреит), гипопион.
1Включая аллергические реакции.
2Состояние, связанное, как известно, с влажной ВМД. Наблюдалось только в исследованиях с влажной ВМД.
3Эндофтальмит с высевающейся и невысевающейся культурой.
Описание отдельных НР
В исследованиях фазы III при влажной ВМД отмечено повышение частоты возникновения субконъюнктивальных кровоизлияний у пациентов, получающих антитромботические средства. Повышение частоты возникновения данного явления было сопоставимым у пациентов, получающих ранибизумаб и афлиберцепт.
Артериальная тромбоэмболия (АТЭ) является НР, потенциально связанной с системным ингибированием VEGF. Теоретически существует риск АТЭ после интравитреального введения ингибиторов VEGF.
В соответствии с критериями Рабочей группы специалистов по антиагрегантной терапии (Antiplatelet Trialists’ Collaboration), под термином АТЭ подразумеваются инфаркт миокарда без смертельного исхода, инсульт без смертельного исхода, смерть вследствие нарушений кровообращения (в т.ч. синдром внезапной необъяснимой смерти).
Распространенность АТЭ в исследованиях III фазы по показанию влажная ВМД (VIEW-1 и VIEW-2) за 96 нед исследования составляла 3,3% (суммарно 60 из 1824) в группе пациентов, получавших препарат афлиберцепт, по сравнению с 3,2% (19 из 595) у пациентов, получавших ранибизумаб (см. «Фармакодинамика»). Соответствующая величина в исследованиях III фазы по показанию ДМО (VISTA-DME и VIVID-DME) за первые 52 нед исследования составляла 3,3% (19 из 578) в группе пациентов, получавших препарат афлиберцепт, по сравнению с 2,8% (8 из 287) в контрольной группе (см. «Фармакодинамика»).
Распространенность АТЭ в исследованиях III фазы по показанию ОЦВС (GALILEO и COPERNICUS) за 76/100 нед исследования составляла 0,6% (2 из 317) у пациентов, получивших по крайней мере одну дозу афлиберцепта, по сравнению с 1,4% (2 из 142) в группе пациентов, которым проводилась только имитация инъекций (см. «Фармакодинамика»), в то время как в исследовании фазы III по показанию ОВВС (VIBRANT) за 52 нед исследования эта величина составляла 0% (0 из 92) у пациентов, получавших лечение афлиберцептом, по сравнению с 2,2% (2 из 92) в контрольной группе (см. «Фармакодинамика»). Один из этих пациентов контрольной группы получал резервное лечение афлиберцептом.
Как и все терапевтические белки, афлиберцепт обладает иммуногенным потенциалом.
Взаимодействие
Официальные исследования по взаимодействию с афлиберцептом при в/в введении не проводились.
В сравнительных исследованиях концентрации свободного и связанного афлиберцепта в комбинации с другими средствами были сходными с концентрациями афлиберцепта при монотерапии, что указывает на то, что данные комбинации (оксалиплатин, цисплатин, фторурацил, иринотекан, доцетаксел, пеметрексед, гемцитабин и эрлотиниб) не влияли на фармакокинетику афлиберцепта.
В свою очередь, афлиберцепт не влиял на фармакокинетику иринотекана, фторурацила, оксалиплатина, цисплатина, доцетаксела, пеметрекседа, гемцитабина и эрлотиниба.
Исследования взаимодействия при интравитреальном введении не проводились.
Сочетанное применение фотодинамической терапии вертепорфином и афлиберцепта не изучалось, следовательно профиль безопасности неизвестен.
Передозировка
Информация о безопасности применения афлиберцепта в дозах, превышающих 7 мг/кг 1 раз в 2 нед или 9 мг/кг 1 раз в 3 нед в/в, отсутствует.
Симптомы: наиболее часто встречающиеся HP, наблюдавшиеся при этих режимах дозирования, были сходны с HP, наблюдавшимися при применении средства в терапевтических дозах.
Лечение: требуется поддерживающая терапия, в частности мониторинг и лечение повышения АД и протеинурии. Специфический антидот афлиберцепта отсутствует. Пациент должен находиться под тщательным медицинским наблюдением для выявления и контроля любых HP, описанных в разделе «Побочные действия».
В клинических исследованиях при интравитреальном введении применялись дозы до 4 мг с интервалом 1 мес. Наблюдались отдельные случаи передозировки при применении дозы 8 мг.
Симптомы: передозировка с введением большего объема раствора может приводить к повышению ВГД.
Лечение: следует контролировать ВГД, при необходимости — адекватная терапия по его коррекции.
Способ применения и дозы
В/в, в виде 1-часовой инфузии с последующим введением химиотерапевтического режима FOLFIRI (см. «Фармакодинамика»). Рекомендованная доза афлиберцепта, применяемого в сочетании с химиотерапевтическим режимом FOLFIRI, составляет 4 мг/кг.
Интравитреально. Рекомендованная доза афлиберцепта составляет 2 мг.
Меры предосторожности
Перед началом лечения и каждого нового цикла лечения афлиберцептом рекомендуется проводить общий анализ крови с определением лейкоцитарной формулы. При первом развитии нейтропении ≥3-й степени тяжести следует рассмотреть вопрос о терапевтическом применении гранулацитарного колониестимулирующего фактора (Г-КСФ, филграстим), кроме этого, у пациентов, которые имеют повышенный риск развития нейтропенических осложнений, рекомендуется введение Г-КСФ для профилактики нейтропении.
Пациенты должны находиться под постоянным наблюдением на предмет выявления признаков и симптомов желудочно-кишечных и других тяжелых кровотечений. Нельзя вводить афлиберцепт пациентам с тяжелыми кровотечениями.
У пациентов, получавших лечение афлиберцептом, сообщалось о развитии сердечной недостаточности и снижении фракции выброса левого желудочка. Пациенты должны находиться под постоянным наблюдением на предмет выявления признаков и симптомов сердечной недостаточности и снижения фракции выброса левого желудочка. У пациентов, у которых возникает сердечная недостаточность или снижение фракции выброса левого желудочка, применение афлиберцепта должно быть прекращено.
Пациенты должны находиться под наблюдением на предмет выявления признаков и симптомов перфорации стенок ЖКТ. В случае развития перфорации стенок ЖКТ лечение афлиберцептом следует прекратить.
При развитии свищей лечение афлиберцептом должно быть прекращено.
Рекомендуется контролировать АД каждые 2 нед, включая контроль АД перед введением афлиберцепта, или чаще — по клиническим показаниям во время лечения афлиберцептом. В случае повышения АД во время лечения афлиберцептом необходимо применять соответствующую антигипертензивную терапию и регулярно контролировать АД. При чрезмерном повышении АД лечение афлиберцептом следует приостановить до снижения АД до целевых значений и в последующих циклах дозу афлиберцепта — снизить до 2 мг/кг. В случае развития гипертонического криза или гипертонической энцефалопатии введение афлиберцепта необходимо прекратить.
Следует соблюдать осторожность при введении афлиберцепта пациентам с клинически выраженной сердечно-сосудистой патологией, такой как ИБС и сердечная недостаточность. Данные клинических исследований по введению афлиберцепта пациентам с сердечной недостаточностью III и IV функционального класса по классификации NYHA отсутствуют.
В случае развития у пациента АТЭО лечение афлиберцептом следует прекратить.
Перед каждым введением афлиберцепта следует определять величину протеинурии с помощью индикаторной тест-полоски или путем определения соотношения белок/креатинин в моче для выявления развития или увеличения протеинурии. Пациентам с соотношением белок/креатинин в моче >1 следует провести определение количества белка в суточной моче.
При развитии нефротического синдрома или тромботической микроангиопатии лечение афлиберцептом следует прекратить.
В случае развития тяжелой реакции гиперчувствительности (включая бронхоспазм, одышку, ангионевротический отек и анафилаксию) необходимо прекратить лечение и начать соответствующую терапию, направленную на купирование этих реакций.
В случае развития умеренно выраженной реакции гиперчувствительности на афлиберцепт (включая гиперемию кожных покровов, сыпь, крапивницу, зуд) следует временно приостановить лечение до разрешения реакции. В случае клинической необходимости для купирования этих реакций можно применять ГКС и/или антигистаминные средства. В последующих циклах можно рассмотреть вопрос о проведении премедикации ГКС и/или антигистаминными средствами. При возобновлении лечения пациентов, имевших ранее реакции гиперчувствительности, следует соблюдать осторожность, т.к. у некоторых пациентов наблюдалось повторное развитие реакций гиперчувствительности несмотря на их профилактику, включающую применение ГКС.
Применение афлиберцепта должно быть приостановлено в течение не менее 4 нед после крупных хирургических вмешательств и до тех пор, пока не заживет полностью операционная рана. При небольших хирургических вмешательствах, таких как установка центрального венозного катетера, биопсия, экстракция зубов, лечение афлиберцептом может быть начато/возобновлено после полного заживления операционной раны. У пациентов с нарушением заживления раны, потребовавшим медицинского вмешательства, применение афлиберцепта следует прервать.
СОЗЛ может проявляться изменением психического состояния, эпилептическими припадками, тошнотой, рвотой, головными болями и зрительными расстройствами. Диагноз СОЗЛ подтверждается исследованием головного мозга с помощью МРТ.
У пациентов с СОЗЛ применение афлиберцепта следует прекратить.
Пациенты пожилого возраста. У пациентов пожилого возраста (≥65 лет) имеется повышенный риск развития диареи, головокружения, астении, снижения массы тела и дегидратации. С целью минимизации риска такие пациенты нуждаются в тщательном медицинском наблюдении для раннего выявления и лечения признаков и симптомов диареи и дегидратации.
Общее состояние и сопутствующие заболевания. Пациенты, имеющие индекс общего состояния пациента ≥2 баллов (по пятибалльной (0–4 балла) оценочной шкале ECOG) или значимые сопутствующие заболевания, могут иметь более высокий риск неблагоприятного клинического исхода и нуждаются в тщательном медицинском наблюдении для раннего выявления клинического ухудшения.
Афлиберцепт для в/в введения несовместим с введением во внутриглазное пространство и его нельзя вводить в стекловидное тело.
Реакции, обусловленные интравитреальным введением. Была выявлена связь интравитреальных инъекций, включая инъекции афлиберцепта, с развитием эндофтальмита, воспалительной реакции со стороны стекловидного тела, регматогенной отслойки сетчатки, разрыва сетчатки, ятрогенной травматической катаракты (см. «Побочные действия»). При введении афлиберцепта всегда следует соблюдать соответствующую технику асептического проведения инъекций. Кроме того, пациенты должны находиться под наблюдением в течение недели после проведенной инъекции для выявления первых признаков воспаления и своевременного назначения необходимой терапии. Следует информировать пациентов о необходимости немедленно сообщать врачу о любых симптомах, свидетельствующих о развитии эндофтальмита или любой другой реакции, указанной выше.
Наблюдались случаи повышения ВГД в первые 60 мин после интравитреальных инъекций, включая инъекции афлиберцепта (см. «Побочные действия»). При лечении пациентов с плохо контролируемой глаукомой необходимы особые меры предосторожности (не следует вводить афлиберцепт при ВГД ≥30 мм рт.ст.). Во всех случаях необходим контроль ВГД и перфузии диска зрительного нерва с назначением соответствующей состоянию терапии.
Иммуногенность. Поскольку афлиберцепт представляет собой белок с терапевтическими свойствами, существует вероятность проявления иммуногенности (см. «Побочные действия»). Следует информировать пациентов о необходимости сообщать врачу о любых признаках или симптомах внутриглазного воспаления, таких как боль, светобоязнь или конъюнктивальная или перикорнеальная инъекция, которые могут быть клиническими проявлениями гиперчувствительности к афлиберцепту.
Системные эффекты. После интравитреальных инъекций ингибиторов VEGF были отмечены системные НР, в т.ч. кровоизлияния вне органа зрения и тромбоэмболия артерий. Существует теоретический риск связи этих явлений с ингибированием VEGF. Имеются ограниченные данные по безопасности применения афлиберцепта пациентами с ОЦВС, ОВВС или ДМО с анамнестическими сведениями об инсульте, транзиторной ишемической атаке или инфаркте миокарда за период в 6 мес перед началом терапии. При лечении таких пациентов следует соблюдать осторожность.
Прочее. Как и в случае интравитреального введения других анти-VEGF-средств при ВМД, ОЦВС, ОВВС и ДМО следует принять во внимание нижеследующее.
Безопасность и эффективность афлиберцепта при введении одновременно в оба глаза систематически не изучалась (см. «Фармакодинамика»). Одновременное билатеральное введение может привести к повышению системной экспозиции средства, что, в свою очередь, повышает риск системных НР.
Отсутствуют сведения об одновременном применении афлиберцепта с другими анти-VEGF-средствами (системными или глазными).
Факторы риска, связанные с нарушением целостности слоя пигментных клеток после анти-VEGF-терапии влажной ВМД, включают распространенную и/или локализованную в верхних отделах сетчатки отслойку пигментного эпителия. В начале терапии афлиберцептом следует соблюдать осторожность при его назначении пациентам с факторами риска развития разрывов пигментного эпителия сетчатки.
Пациентам с регматогенной отслойкой сетчатки или с макулярными разрывами 3-й или 4-й стадии от лечения следует воздержаться.
В случае разрыва сетчатки инъекция должна быть отменена, лечение не следует возобновлять до адекватного восстановления разрыва.
От инъекции следует воздержаться до следующей запланированной по графику инъекции в случае: снижения остроты зрения с максимальной коррекцией ≥30 букв по сравнению с последней оценкой остроты зрения; субретинальных кровоизлияний, затрагивающих центральную ямку, или если размер кровоизлияния составляет ≥50% от общей области поражения.
От инъекции следует воздержаться на периоды 28 дней до планируемого и 28 дней после проведенного интраокулярного хирургического вмешательства.
Афлиберцепт не следует применять при беременности, за исключением случаев, когда потенциальная польза для матери превышает потенциальный риск для плода (см. «Применение при беременности и кормлении грудью»).
Женщины репродуктивного возраста должны использовать эффективные средства контрацепции в период лечения и по крайней мере в течение 3 мес после последней интравитреальной инъекции афлиберцепта (см. «Применение при беременности и кормлении грудью»).
Опыт лечения пациентов с ишемической ОЦВС и ОВВС ограничен. При наличии у пациентов клинических признаков необратимых изменений зрительных функций на фоне ишемии терапия афлиберцептом не рекомендована.
Популяции с ограниченными данными. Опыт лечения ДМО у пациентов с сахарным диабетом типа 1 и уровнем гликированного Hb более 12% и/или с пролиферативной диабетической ретинопатией ограничен.
Применение афлиберцепта у пациентов с активными системными инфекциями или сопутствующими заболеваниями глаз, такими как отслойка сетчатки или разрыв макулы, не изучалось. Опыт лечения афлиберцептом пациентов с сахарным диабетом и неконтролируемой гипертензией отсутствует. Это должно учитываться лечащим врачом при ведении таких пациентов.
Данные, полученные из доклинических исследований. В доклинических исследованиях при изучении токсичности повторных доз эффекты афлиберцепта наблюдались только при системной экспозиции, существенно превышающей максимальную экспозицию у человека после интравитреального введения в дозе, предназначенной для клинического применения, что указывает на малую значимость этих результатов в клинической практике.
Исследований по изучению мутагенного или канцерогенного потенциала афлиберцепта не проводилось.
Влияние на способность управлять транспортными средствами и работать с механизмами. Не проводились исследования по влиянию афлиберцепта на способность управлять автомобилем или заниматься другими потенциально опасными видами деятельности при в/в введении. Если у пациентов появляются симптомы, влияющие на зрение и способность к концентрации, а также замедляющие психомоторные реакции, им следует воздержаться от управления транспортными средствами и других потенциально опасных видов деятельности.
При интравитреальном введении афлиберцепт оказывает минимальное влияние на способность управлять транспортными средствами и использовать механизмы вследствие возможных временных нарушений зрения, связанных как с инъекцией, так и с процедурой обследования. Если после проведения инъекции у пациента возникли временные нарушения зрения, то пациенту не рекомендуется управлять автомобилем или работать с механизмами до восстановления четкости зрительного восприятия.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Эфлейра — инструкция по применению
Синонимы, аналоги
Статьи
Внимательно прочтите эту инструкцию перед тем, как начать прием/использование лекарственного средства.
Сохраните инструкцию, она может потребоваться вновь.
Если у Вас возникли вопросы, обратитесь к врачу.
Это лекарственное средство назначено лично Вам, и его не следует передавать другим лицам, поскольку оно может причинить им вред даже при наличии тех же симптомов, что и у Вас.
Регистрационный номер:
ЛП-005439
Торговое наименование препарата:
Эфлейра®
Международное непатентованное наименование:
нетакимаб
Лекарственная форма:
раствор для подкожного введения
Состав:
1 мл раствора содержит:
Действующее вещество: нетакимаб – 60 мг;
Вспомогательные вещества: натрия ацетата тригидрат – 1,74 мг, трегалозы дигидрат – 80 мг, полоксамер 188 – 0,5 мг, уксусная кислота ледяная – до pH 5,0, вода для инъекций – до 1,0 мл.
Описание:
Прозрачный или слегка опалесцирующий от бесцветного до светло-желтого или светло-желтого с коричневатым оттенком цвета раствор.
Фармакотерапевтическая группа:
Интерлейкина ингибитор
Код АТХ:
L04AC
Фармакологические свойства
Фармакодинамика
Нетакимаб является рекомбинантным гуманизированным моноклональным антителом, в терапевтических концентрациях специфически связывающим интерлейкин-17А (ИЛ-17А), находящийся непосредственно в тканях или в крови и других биологических жидкостях. ИЛ-17А – провоспалительный цитокин, гиперпродукция которого преимущественно обусловлена активацией Th17-лимфоцитов. В рамках врожденного иммунитета ИЛ-17А выполняет защитную роль. При хронических иммуновоспалительных заболеваниях патологическая активация Th17-лимфоцитов и гиперпродукция ИЛ-17 стимулирует Т-клеточный ответ и усиленную продукцию других медиаторов воспаления: ИЛ-1, ИЛ-6, фактора некроза опухоли альфа (ФНО-α), факторов роста (Г-КСФ, ГМ-КСФ) и различных хемокинов.
Нетакимаб обладает высокой термодинамической константой специфического связывания с ИЛ-17А человека. По данным доклинических исследований специфическое связывание нетакимаба в нормальных тканях человека ограничено тканями легкого, тимуса, лимфатического узла, миндалин, что согласуется с данными об экспрессии ИЛ-17 клетками этих тканей.
Применение нетакимаба не сопровождается статистически значимым изменением уровня Т-лимфоцитов и не влияет на уровень и соотношение иммуноглобулинов классов А, G и М.
Специфическая противовоспалительная активность нетакимаба продемонстрирована в тестах in vitro и in vivo. Нетакимаб дозозависимо ингибирует ИЛ-17 и ФНОα-зависимую продукцию интерлейкина-6 на культуре клеток при IC50 40 pM. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (один раз в неделю в течение 4-х недель) подкожное введение нетакимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (суставной хрящ остается интактным, синовиальные оболочки — без признаков поражения и воспалительной реакции, пролиферации синовиоцитов не отмечено).
У больных псориазом использование нетакимаба сопровождается угасанием явлений воспаления и гиперкератоза в коже, достоверным снижением уровня С-реактивного белка и СОЭ. У пациентов с активным анкилозирующим спондилитом и псориатическим артритом на фоне применения нетакимаба отмечается уменьшение симптомов воспаления в позвоночнике, энтезисах и суставах, а также быстрое снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание/распределение
Изменение концентрации нетакимаба после его подкожного введения является дозозависимым (значения Сmax, Cmax-mult, AUC0-t находятся в прямой зависимости от дозы). Препарат характеризуется медленной фазой абсорбции с постепенным линейным нарастанием концентрации в сыворотке крови.
При однократном подкожном введении нетакимаба в дозе 120 мг пациентам с бляшечным псориазом препарат начинал обнаруживаться в сыворотке крови в течение 0,5 — 4 часов после введения; максимальная концентрация нетакимаба (Сmax) составляла 15,1 [7,7-19,3] мкг/мл, время ее достижения – 144 [72-168] ч, AUC0-168 – 1667,8 [932,2-2270,8] (мкг/мл)*ч.
При повторных введениях отмечено накопление препарата в сыворотке крови с ростом концентрации в 1,8-3,6 раза. Максимальная концентрация при многократном введении (Cmax-mult) составляла 33,0 [23,1-44,0] мкг/мл и достигалась (Tmax-mult) через 1680 [672-2016] часов.
Выведение
Характеристики выведения нетакимаба являются типичными для препаратов на основе моноклональных антител: показатели Kel, T½, MRT, Cl не зависят от дозы вводимого препарата, период полувыведения после однократного введения составляет около 16 суток.
Средний клиренс нетакимаба при однократном введении в дозе 120 мг пациентам с бляшечным псориазом составил 1,8 л/сутки.
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Пациенты с почечной и печеночной недостаточностью: фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания к применению
- Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия.
- Лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
- Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию.
Противопоказания
- Гиперчувствительность к нетакимабу, а также к любому из вспомогательных веществ препарата.
- Клинически значимые инфекционные заболевания в острой фазе, включая туберкулез.
- Детский и подростковый возраст до 18 лет.
- Беременность, грудное вскармливание.
С осторожностью
Следует соблюдать осторожность при назначении нетакимаба пациентам с хроническими и рецидивирующими инфекциями или с анамнестическими указаниями на них, в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний, а также после недавно проведенной вакцинации живыми вакцинами.
В связи с ограниченными данными клинических исследований о применении нетакимаба у пациентов в возрасте старше 65 лет, следует соблюдать осторожность при назначении препарата пациентам указанной возрастной группы.
В связи с отсутствием сведений о применении нетакимаба у больных воспалительными заболеваниями кишечника, следует избегать его назначения пациентам с болезнью Крона или язвенным колитом.
Применение при беременности и в период грудного вскармливания
Применение при беременности
При применении нетакимаба у животных не выявлено отрицательного влияния на репродуктивную функцию, эмбриотоксичности или тератогенных эффектов.
Исследований влияния на плод у беременных женщин не проводилось. Препарат противопоказан к применению во время беременности.
Применение при грудном вскармливании
Нет данных о проникновении нетакимаба в грудное молоко. Учитывая, что иммуноглобулины класса G, к которым относится нетакимаб, при циркуляции в крови матери могут выделяться с грудным молоком, применение в период грудного вскармливания противопоказано. Во избежание негативного воздействия на ребенка следует прекратить либо грудное вскармливание, либо терапию, учитывая соотношение риска и пользы для матери и ребенка.
Влияние на фертильность
В исследованиях у животных не обнаружено негативного воздействия нетакимаба на фертильность. Данные о влиянии препарата на фертильность у людей отсутствуют.
Способ применения и дозы
Применение препарата Эфлейра® должно осуществляться под наблюдением врачей, имеющих опыт лечения заболеваний, при которых показан препарат Эфлейра®. После соответствующего обучения возможно самостоятельное введение препарата пациентом при условии динамического наблюдения со стороны лечащего врача. Препарат Эфлейра® может применяться как в стационарных, так и в амбулаторных условиях.
Препарат Эфлейра® вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл препарата с концентрацией 60 мг/мл.
Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая вводится 1 раз в неделю на неделях 0, 1 и 2, затем 1 раз каждые 4 недели.
Лечение активного анкилозирующего спондилита при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели до недели 10 включительно. Далее с недели 14 препарат вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) каждая 1 раз в 4 недели.
| Показание | Разовая доза | Индукция | Поддерживающая терапия |
| Бляшечный псориаз | 120 мг | 0, 1, 2 недели |
1 раз в 4 недели, начиная с недели 6 |
| Анкилозирующий спондилит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 |
| Псориатический артрит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 по неделю 10 включительно, далее 1 раз в 4 недели с недели 14 |
При пропуске очередного введения по любой причине инъекция препарата Эфлейра® должна быть произведена как можно быстрее. Дата следующего введения рассчитывается исходя из продолжительности задержки с введением препарата: если со времени пропуска введения прошло не более 3 дней, то следующую инъекцию препарата необходимо выполнить по текущему графику, если с момента пропуска введения прошло более 3 дней, то новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Эфлейра®.
Указания по применению
Подготовка к проведению подкожной инъекции
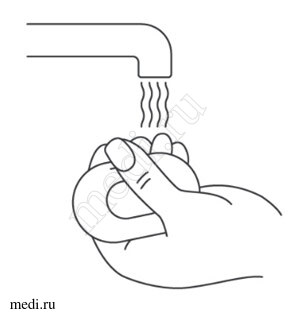

Препарат Эфлейра ® в автоинжекторе
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца/автоинжектора;
- истечения срока годности (годен до…), указанного на картонной пачке, а также на этикетке шприца/автоинжектора.
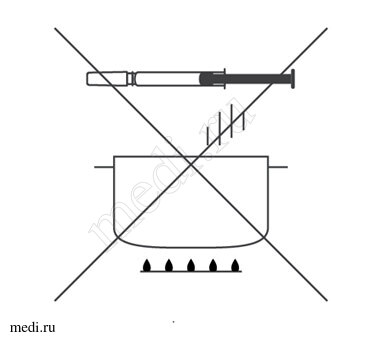
На данном этапе не следует снимать колпачок шприца/автоинжектора
1. Техника выполнения подкожной инъекции препарата Эфлейра® в преднаполненном шприце
Выбор и подготовка места для инъекции


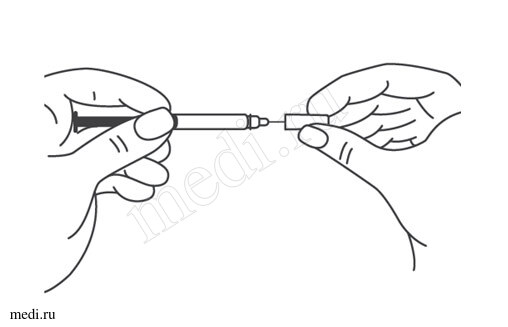

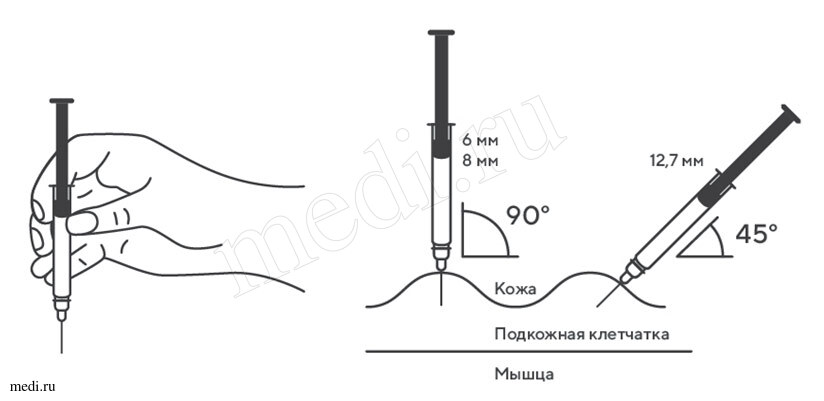
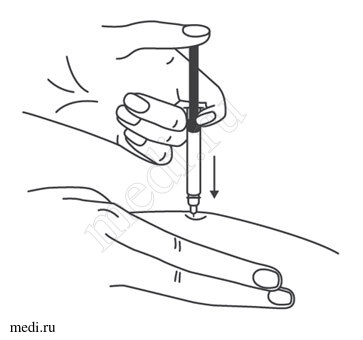
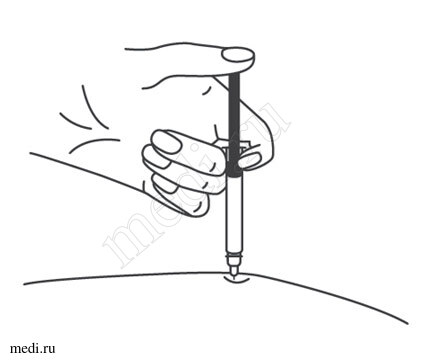
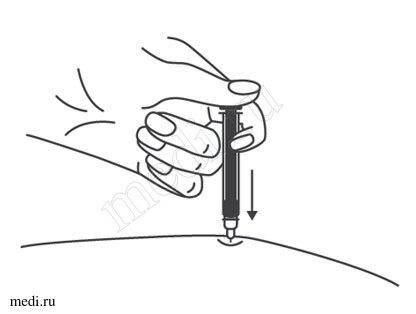
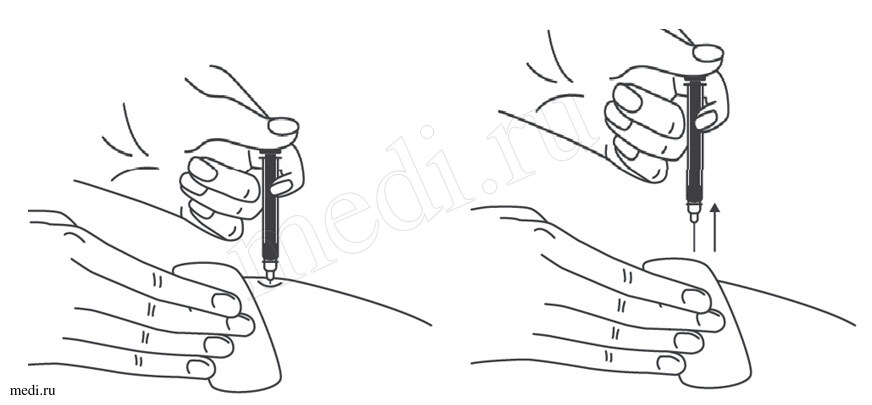
После инъекции шприц повторно не использовать
2. Техника выполнения подкожной инъекции препарата Эфлейра® в автоинжекторе
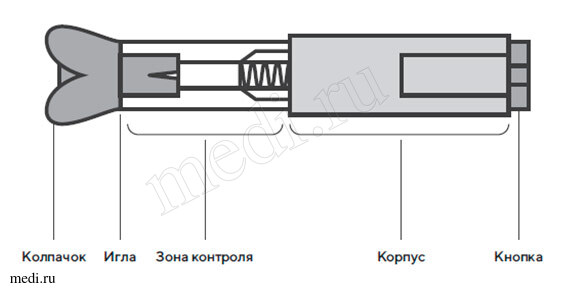
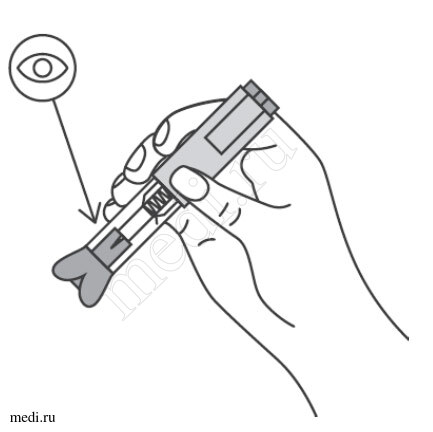
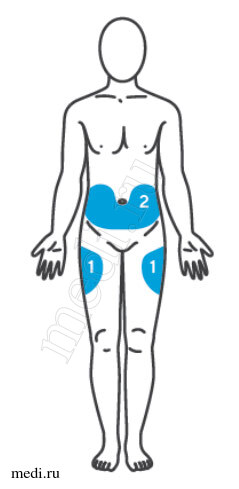



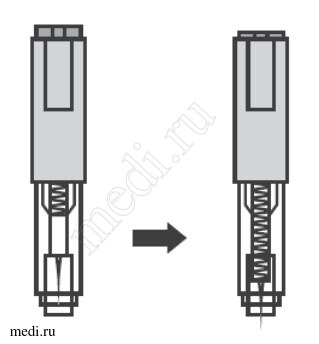
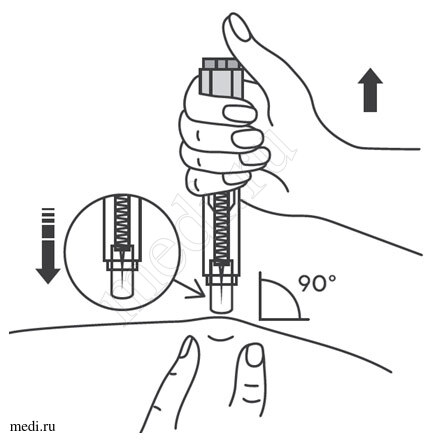
После инъекции автоинжектор повторно не использоватьУтилизация расходного материала

Побочное действие
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений (НЯ), связанных с применением препарата Эфлейра®, имели легкую или среднюю степень тяжести и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000), очень редко (<10000).
Инфекции и инвазии: часто – инфекции верхних дыхательных путей; нечасто – инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Нарушения со стороны печени и желчевыводящих путей: нечасто – гипербилирубинемия.
Желудочно-кишечные нарушения: нечасто – боль в животе, диарея.
Нарушения со стороны кожи и подкожной клетчатки: нечасто – экзема, дерматит, сыпь, зуд, крапивница.
Нарушения со стороны крови и лимфатической системы: часто – нейтропения, лейкопения, лимфоцитоз; нечасто – тромбоцитопения, лимфопения.
Нарушения со стороны иммунной системы: нечасто – гиперчувствительность.
Нарушения со стороны органа зрения: нечасто – эписклерит.
Нарушения со стороны нервной системы: нечасто – головная боль, головокружение, парестезия, поражение лицевого нерва.
Нарушения со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Нарушения со стороны сосудов: нечасто — гипертензия (в том числе изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**.
Нарушения метаболизма и питания: нечасто – гипергликемия.
Нарушения со стороны почек и мочевыводящих путей: нечасто – протеинурия.
Лабораторные и инструментальные данные: часто – повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто – повышение гамма-глутамилтрансферазы (ГГТ), повышение уровня холестерина в крови, увеличение веса.
Травмы, интоксикации и осложнения процедур: нечасто – головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто – инфицированный невус.
Нарушения со стороны репродуктивной системы и молочных желез: нечасто – фиброзно-кистозная болезнь молочных желез.
* «Гриппоподобное заболевание» характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
** Местные реакции могут включать в себя любые неблагоприятные проявления, возникающие в месте инъекции.
Передозировка
Клинические данные о передозировке отсутствуют. Максимальная переносимая доза для человека не установлена. В клинических исследованиях явлений дозолимитирующей токсичности не зарегистрировано: при подкожном введении нетакимаба в максимальной дозе 3 мг/кг (195 – 355 мг для взрослого человека с весом 65 – 85 кг) патологических отклонений не было выявлено.
Специфический антидот отсутствует. Лечение симптоматическое.
Взаимодействие с другими лекарственными средствами
Сведений о наличии неблагоприятных лекарственных взаимодействий нетакимаба с другими лекарственными препаратами до настоящего времени не получено. Предполагается, что нетакимаб может усиливать иммуносупрессивное действие глюкокортикоидов, метотрексата, сульфасалазина, лефлуномида и других базисных противовоспалительных препаратов.
Смешивание препарата с другими лекарственными средствами, введение в виде инфузии строго запрещено.
Особые указания
Наличие таких потенциально тяжелых инфекций как ВИЧ, активный гепатит В и/или С, сифилис, туберкулез, относится к противопоказаниям для назначения нетакимаба. Применение нетакимаба у данной группы больных не изучено. Учитывая иммуносупрессивное действие нетакимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования. Необходимо проводить скрининг и оценивать соотношение риска и пользы терапии нетакимабом у этих пациентов.
Пациентам с активным туберкулезом терапия препаратом Эфлейра® противопоказана. Перед назначением препарата Эфлейра® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Эфлейра®.
При реактивации гепатита В терапия нетакимабом должна быть прекращена и назначена соответствующая противовирусная терапия.
Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии.
При использовании нетакимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований нетакимаба анафилактических реакций не зарегистрировано, нечасто отмечались реакции гиперчувствительности и крапивница. Однако при использовании других ингибиторов ИЛ17 крапивница и анафилактические реакции отмечались в редких и очень редких случаях. При возникновении анафилактических или других серьёзных аллергических реакций применение препарата Эфлейра® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения нетакимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходим более тщательный мониторинг за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований на данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Эфлейра® при лечении псориаза, псориатического артрита и анкилозирующего спондилита выработка связывающих антител к нетакимабу была зарегистрирована менее чем в 0,5 % случаев. Нейтрализующих антител выявлено не было. Полученные данные демонстрируют низкую иммуногенность нетакимаба у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Пациенты моложе 18 лет, дети
Исследование эффективности и безопасности препарата у детей и лиц моложе 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми вакцинами в ходе лечения препаратом Эфлейра®, так как клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми вакцинами до начала терапии препаратом Эфлейра®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям. Иммунизация инактивированными вакцинами во время терапии нетакимабом должна выполняться с осторожностью.
Влияние на способность управлять транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Эфлейра® на способность управлять транспортными средствами и работать с машинами и (или) механизмами.
Форма выпуска
Раствор для подкожного введения 60 мг/мл.
Преднаполненные шприцы
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса. Шприц с одной стороны имеет впаянную иглу для инъекций из нержавеющей стали, которая защищена жестким колпачком. С другой стороны шприц укупорен поршнем, шток которого изготовлен из полипропилена; на конце поршня имеется уплотнитель из бутилкучука, ламинированный фторполимером.
На каждый шприц наклеивают самоклеящуюся этикетку.
По 1 шприцу помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Автоинжектор
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса.
Шприц с препаратом встроен в пластиковый автоинжектор, состоящий из защитного колпачка, корпуса с прозрачной зоной контроля, верхнего корпуса и кнопки активации. Внутреннее устройство автоинжектора имеет цилиндр, защищающий иглу, и поршень, который через систему механического пуска соединен с кнопкой активации.
На каждый автоинжектор наклеивают самоклеящуюся этикетку.
По 1 автоинжектору помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Условия хранения
При температуре от 2 до 8°С в защищенном от света месте. Не замораживать!
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Производитель
ЗАО «БИОКАД», Россия, 143422, Московская обл., Красногорский р-н, с. Петрово-Дальнее.
Владелец регистрационного удостоверения
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Организация, принимающая претензии потребителей
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Эйлеа®
МНН: Афлиберцепт
Производитель: Регенерон Фармасьютикалс, Инк.
Анатомо-терапевтическо-химическая классификация: Афлиберцепт
Номер регистрации в РК:
№ РК-ЛС-5№020045
Информация о регистрации в РК:
02.10.2018 — бессрочно
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
319 827.2 KZT
- Скачать инструкцию медикамента
Торговое название
Эйлеа®
Международное непатентованное название
Афлиберцепт
Лекарственная форма
Раствор для инъекций, 40 мг/мл
Состав
1 мл препарата содержит
активное вещество — афлиберцепта 40 мг,
вспомогательные вещества: натрия хлорид, натрия дигидрофосфат моногидрат, натрия гидрофосфат гептагидрат, сахароза, полисорбат 20, вода для инъекций.
Описание
Прозрачный, слегка опалесцирующий раствор.
Фармакотерапевтическая группа
Препараты для лечения заболеваний глаз. Средства для лечения сосудистых расстройств окологлазного пространства. Антинеоваскулярные средства. Афлиберцепт.
Код АТХ S01LA05
Фармакологические свойства
Фармакокинетика
Абсорбция / распределение
После интравитреального введения афлиберцепт медленно проникает в системный кровоток и находится, главным образом в виде неактивного стабильного комплекса с VEGF (фактор роста эндотелия сосудов), однако только «свободный афлиберцепт» может связываться с эндогенным VEGF.
Максимальная концентрация свободного афлиберцепта в плазме крови (системный Cmax) низкая и в среднем составляет приблизительно 0,02 микрограмма/мл (в диапазоне от 0 до 0,054) в течение 1-3 дней после интравитреального введения 2 мг, а через две недели после введения дозы не обнаруживается в плазме. При интравитреальном введении каждые 4 недели афлиберцепт не кумулирует в плазме.
Предполагается, что после интравитреального введения пациентам 2 мг препарата, средняя максимальная концентрация свободного афлиберцепта в плазме крови более чем в 100 раз ниже концентрации афлиберцепта, необходимой для связывания половины максимального уровня системного VEGF. Таким образом, системный фармакодинамический эффект (такой как, изменения АД) маловероятен.
Экскреция
Свободный афлиберцепт связывается с VEGF для формирования стабильного инертного комплекса. Как и в случае с другими крупными белками предполагается, что свободный и связанный афлиберцепт будет выводиться путем протеолитического катаболизма.
Фармакодинамика
Афлиберцепт представляет собой рекомбинантный гибридный белок, состоящий из фрагментов внеклеточных доменов рецепторов VEGF (фактора роста эндотелия сосудов) 1 и 2, соединенных с Fc-фрагментом человеческого IgG1.
Афлиберцепт вырабатывается в клетках K1 яичника китайского хомячка (CHO/ЯКХ) путем рекомбинантной ДНК-технологии.
Механизм действия
Эндотелиальный сосудистый фактор роста А (VEGF-A) и плацентарный фактор роста (PIGF) относятся к семейству ангиогенных факторов, которые могут действовать в качестве активного митогенного, хемотаксического фактора и фактора сосудистой проницаемости для эндотелиальных клеток. VEGF действует посредством тирозинкиназы двух рецепторов, VEGFR-1 и VEGFR-2, которые присутствуют на поверхности эндотелиальных клеток. PIGF связывается только с фактором VEGFR-1, который также присутствует на поверхности лейкоцитов. Излишняя активация рецепторов VEGF-А может привести к патологической неоваскуляризации и повышенной проницаемости сосудов.
Возможен синергизм между фактором PIGF и VEGF-A в этих процессах, также известно, что фактор PIGF способствует лейкоцитарной инфильтрации и сосудистому воспалению. Множество глазных болезней связаны с патологической неоваскуляризацией, сосудистым пропотеванием, которые могут привести к утолщению или отеку сетчатки, что, как полагают, способствует потере зрения.
Афлиберцепт действует как растворимый рецептор-«ловушка», который связывает все изоформы VEGF-A и PIGF с большей аффинностью, чем их природные рецепторы, и таким образом ингибирует связывание и активацию нативных рецепторов VEGF. Константа равновесной диссоциации (КD) для связывания афлиберцепта, с человеческим VEGF-A165 составляет 0,5 промилле, а для человеческого VEGF-A121 составляет 0,36 промилле. Константа KD для связывания с человеческим PIGF-2 составляет 39 промилле.
Исследования на животных показали, что афлиберцепт может предотвращать патологическую неоваскуляризацию и пропотевание жидкости из сосудов на ряде различных моделей глазных болезней. Например, интравитреальное введение афлиберцепта обезьянам предотвращало развитие выраженной хориоидальной неоваскуляризации ( ХНВ/CNV) после повреждения лазерным лучом, и способствовало уменьшению пропотевания жидкости через сосуды на установленных участках патологической хориоидальной неоваскуляризации.
Фармакодинамические эффекты
Неоваскулярная влажная возрастная макулярная дегенерация (влажная ВМД) характеризуется патологической хориоидальной неоваскуляризацией (ХНВ). Пропотевание крови или жидкости из участков ХНВ может вызывать отек сетчатки и/или суб- /интраретинальное кровоизлияние, приводящее к потере остроты зрения.
У пациентов, получающих препарат Эйлеа® (одна инъекция в месяц в течение трех первых месяцев, с последующей одной инъекцией каждые 2 месяца), отмечалось уменьшение толщины сетчатки вскоре после начала лечения и уменьшение среднего размера патологического участка ХНВ, что соответствует результатам, полученным у пациентов на фоне ежемесячного введения ранибизумаба в дозе 0,5 мг.
Макулярный отек вследствие окклюзии центральной вены сетчатки или ее ветвей
При окклюзии центральной вены сетчатки или ее ветвей возникает ишемия сетчатки, провоцирующая высвобождение VEGF, которые в свою очередь дестабилизируют плотные соединения и способствуют пролиферации эндотелиальных клеток. Повышение активности VEGF приводит к нарушению гематоретинального барьера, и такая повышенная сосудистая проницаемость приводит к отеку сетчатки, стимулированию роста эндотелиальных клеток и неоваскуляризации.
У пациентов, получающих лечение Эйлеа®, (одна инъекция раз в месяц на протяжении шести месяцев) наблюдалась постоянная, быстрая и устойчивая ответная реакция в отношении морфологии ( толщина центральной зоны сетчатки (ТЦЗС) по данным ОКТ (оптической когерентной томографии). Улучшение среднего показателя ТЦЗС сохранялось на протяжении 24 недель.
Диабетический макулярный отек
Диабетический макулярный отек характеризуется повышенной проницаемостью сосудов и повреждением капилляров сетчатки, что может вызвать потерю остроты зрения.
У пациентов, получавших препарат Эйлеа®, вскоре после начала лечения наблюдался быстрый и устойчивый морфологический ответ (толщина центральной зоны сетчатки [ТЦЗС]), согласно оценке данных ОКТ. Среднее изменение в ТЦЗС от исходного уровня значения к 52 неделе было статистически значимым в пользу Эйлеа®.
Миопическая хориоидальная неоваскуляризация
Миопическая хориоидальная неоваскуляризация является частой причиной потери зрения у взрослых с патологической миопией.
Она развивается как ранозаживляющий механизм вследствие разрыва мембраны Бруха и представляет собой наиболее угрожающее зрению событие при патологической миопии.
Показания к применению
— неоваскулярная (влажная) возрастная макулярная дегенерация (ВМД)
— нарушение зрения вследствие макулярного отека, обусловленного окклюзией вен сетчатки (центральной вены сетчатки (ОЦВС) и ее ветвей (ОВВС))
— нарушение зрения вследствие диабетического макулярного отека (ДМО) — нарушение зрения вследствие миопической хориоидальной неоваскуляризации (миопической ХНВ)
Способ применения и дозы
Эйлеа® предназначен только для интравитреального введения.
Препарат должен вводиться только квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций.
Каждый флакон содержит 0.278 мл раствора для интравитреального введения, что предоставляет извлекаемый объем 0.1 мл.
Разовая доза препарата во флаконе составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора для инъекций.
Режим дозирования
Неоваскулярная возрастная макулярная дегенерация
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора для инъекций.
Лечение Эйлеа® начинают с трех последовательных инъекций 1 раз в месяц (каждые 4 недели в течение первых 12 недель) с дальнейшей инъекцией 1 раз каждые 2 месяца. Нет необходимости в проведении мониторинга между инъекциями.
После первых 12 месяцев лечения Эйлеа®, интервал между инъекциями может быть продлен на основании визуальных и анатомических результатов. В этом случае график обследований должен устанавливаться лечащим врачом и при этом он может быть чаще, чем график инъекций.
Макулярный отек вследствие окклюзии вен сетчатки (центральной вены сетчатки или ее ветвей)
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора для инъекций.
После начальной инъекции препарата лечение проводят каждый месяц. Интервал между двумя инъекциями не должен быть короче одного месяца.
Если визуальные и анатомические результаты не указывают на пользу проводимой непрерывной терапии, инъекции Эйлеа® следует прекратить.
Лечение продолжают до достижения максимальной остроты зрения и/или отсутствия признаков активности заболевания. Возможна необходимость в выполнении 3-х или более последовательных ежемесячных инъекций.
Лечение затем можно продолжить в режиме treat-and-extend (лечить-и-увеличивать) с постепенным увеличением интервалов между инъекциями для поддержания стабильных визуальных и/или анатомических результатов, однако имеется недостаточно данных, чтобы сделать заключение о длительности этих интервалов. Если отмечается ухудшение визуальных и/или анатомических результатов необходимо сократить интервал в лечении, соответственно.График мониторинга и лечения должен определяться лечащим врачом на основании индивидуальной реакции пациента.
Мониторинг активности заболевания включает в себя проведение клинического обследования, функциональных тестов или методов визуализации (например, оптической когерентной томографии или флуоресцентной ангиографии).
Диабетический макулярный отек
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора для инъекций.
Лечение Эйлеа® начинают с пяти последовательных инъекций 1 раз в месяц с дальнейшим интервалом лечения 1 инъекция в 2 месяца. Нет необходимости в проведении мониторинга между инъекциями.
После первых 12 месяцев лечения Эйлеа®, интервал между инъекциями может быть продлен на основании визуальных и анатомических результатов. График обследований должен устанавливаться лечащим врачом.
Если визуальные и анатомические результаты не указывают на пользу проводимой непрерывной терапии, инъекции Эйлеа® следует прекратить.
Миопическая хориоидальная неоваскуляризация
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора в виде однократной интравитреальной инъекции.
Дополнительные дозы могут вводиться, если визуальные и/или анатомические результаты свидетельствуют о сохранении признаков заболевания. При развитии рецидива необходимо лечение как в случае новой манифестации заболевания.
График обследований должен устанавливаться лечащим врачом.
Интервал между двумя инъекциями не должен быть короче одного месяца.
Дополнительная информация для особых категорий пациентов
Пациенты с нарушениями функции печени и/или почек
Не проводилось каких-либо специальных исследований Эйлеа® у больных с нарушениями функции печени и почек. Доступные данные не предполагают коррекции дозы у таких пациентов.
Пожилые пациенты
Специальных предостережений не существуют. Имеется ограниченный опыт применения у больных старше 75 лет с диабетическим макулярным отеком.
Дети и подростки
Безопасность и эффективность в данной возрастной группе не установлена.
Нет обоснования для применения Эйлеа® в педиатрической популяции по показаниям ВМД, ОЦВС и ОВВС, ДМО, миопической ХНВ
Техника введения
Интравитреальные введения должны осуществляться квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций в соответствии с медицинскими стандартами и действующими руководящими положениями. В целом, должна обеспечиваться адекватная анестезия и асептика, включая наружные бактерицидные средства широкого спектра (например, повидон-йод), наносимые на кожу вокруг глаза, веко и поверхность глаза. Рекомендуется применять хирургическую дезинфекцию рук, использовать стерильные перчатки, стерильные салфетки, стерильные векорасширители (или эквивалент).
Иглу для инъекций следует вводить на 3,5–4 мм кзади от лимба в полость стекловидного тела, избегая области горизонтальной меридианы и направляя иглу к центру глазного яблока. Затем следует выполнить инъекцию 0.05 мл раствора; для последующих инъекций следует использовать разные места склеры.
Сразу после интравитреальной инъекции должно быть начато наблюдение за пациентами на предмет выявления возможного повышения внутриглазного давления. Надлежащий мониторинг может состоять из проверки перфузии диска зрительного нерва или тонометрии. При необходимости следует обеспечить доступ к стерильному оборудованию для проведения парацентеза.
После интравитреальной инъекции пациентов необходимо проинструктировать о том, что они должны без промедления сообщать о каких-либо симптомах эндофтальмита (например, глазная боль, покраснение глаза, светобоязнь, нечеткость зрения).
Каждый флакон должен применяться только для лечения одного глаза.
После инъекции любой неиспользованный продукт должен быть утилизирован.
Инструкция по введению изложена в отдельном разделе.
Побочные действия
Серьезные побочные реакции, связанные с инъекцией Эйлеа® наблюдались менее чем в одной из 2200 проведенных интравитреальных инъекций, и включали слепоту, эндофтальмит, отслойку сетчатки, травматическую катаракту, кровоизлияния в стекловидное тело, катаракту, отслойку стекловидного тела, и повышение внутриглазного давления (смотрите раздел «Особые указания»).
Наиболее частыми побочными реакциями (как минимум у 5% пациентов, получивших терапию Эйлеа®) были кровоизлияние под конъюнктиву (24%), снижение остроты зрения (10%), боль в глазу (10%), повышение внутриглазного давления (7%), отслойка стекловидного тела (7%), плавающие помутнения стекловидного тела (6%) и катаракта (6%).
Перечисленные ниже данные по безопасности препарата включают в себя все побочные реакции, основанные на исследованиях фазы III, с допустимой возможностью их взаимосвязи с процедурой инъекции или с самим препаратом
Очень часто (1/10)
— снижение остроты зрения
— кровоизлияние под конъюнктиву
— боль в глазу
Часто (1/100, 1/10)
— разрыв пигментного эпителия сетчатки⃰, отслойка пигментного эпителия сетчатки, дегенерация сетчатки, кровоизлияние в стекловидное тело, катаракта, ядерная катаракта, субкапсулярная катаракта, эрозия роговицы, повреждение роговицы, повышение внутриглазного давления, нечеткость зрения, плавающие помутнения стекловидного тела, отек роговицы, отслойка стекловидного тела, боль в месте введения, ощущение инородного тела в глазах, повышенное слезоотделение, отек век, кровоизлияние в месте введения, точечный кератит, гиперемия конъюнктивы, окулярная гиперемия
Нечасто (1/1 0001/100)
— реакции гиперчувствительности
— эндофтальмит**, отслойка сетчатки, разрыв сетчатки, ирит, иридоциклит, кортикальная катаракта, помутнение хрусталика, отек роговицы, повреждение эпителия роговицы, раздражение в месте введения, ощущение дискомфорта в глазу, раздражение век, воспаление передней камеры глаза.
Редко (1/10 000, 1/1 000)
— слепота, увеит, травматическая катаракта, воспаление стекловидного тела, гипопион
*Состояния, о которых известно, что они связаны с влажной ВМД. Наблюдались только в исследованиях влажной ВМД.
**Эндофтальмит с положительной и отрицательной культурой.
Описание отдельных побочных реакций
Артериальные тромбоэмболические явления
Артериальные тромбоэмболические явления (АТЯ)– это побочные реакции, потенциально связанные с ингибированием системного эндотелиального фактора роста сосудов (VEGF). Существует теоретический риск развития АТЯ после интравитреального применения ингибиторов VEGF.
АТЯ, как это определено критериями Сотрудничества Антитромбоцитарных исследователей (АРТС), включают в себя нефатальный инфаркт миокарда, нефатальный инсульт или сосудистую смерть (включая смерть неизвестной этиологии)
Частота АТЯ у больных с ВМД в исследованиях III фазы в течение 96 недель была 3,3% (60 из 1,824) в комбинированной группе пациентов, получавших Эйлеа® по сравнению с 3,2% (19 из 595) у пациентов, получавших ранибизумаб (см. раздел «Фармакодинамические свойства»). Соответствующие цифры в исследованиях отмечались у пациентов с ДМО в течение первых 52 недель как 3,3% (19 из 578) на фоне Эйлеа® и 2,8% (8 из 287) в контрольной группе) (см. раздел «Фармакодинамические свойства»).
Частота АТЯ у больных с ОЦВС в исследованиях III фазы продолжительностью 76/100 недель была 0,6% (2 из 317) у пациентов, получавших, по крайней мере, одну дозу Эйлеа® по сравнению с 1,4% (2 из 142) в группе пациентов, получавших только имитацию инъекции (см. раздел «Фармакодинамические свойства»). Частота АТЯ у больных с ОВВС в исследованиях III фазы продолжительностью 52 недели была 0% (0 из 91) у пациентов, получавших Эйлеа® сравнению с 2,2% (2 из 92) в контрольной группе (см. раздел «Фармакодинамические свойства»).
Один из пациентов в контрольной группе получил лечение препаратом Эйлеа® в качестве «терапии спасения».
Частота АТЯ у больных с миопической ХНВ в исследовании продолжительностью 48 недель была 1,1% (1 из 91) на фоне Эйлеа® по сравнению с 0% (0 из 31) в контрольной группе).
Как и для других препаратов белковой природы существует вероятность развития иммуногенности на введение препарата Эйлеа®.
Противопоказания
— гиперчувствительность к афлиберцепту или вспомогательным компонентам препарата
— активная окулярная или периокулярная инфекция или подозрение на них
— активное тяжелое интраокулярное воспаление.
Лекарственные взаимодействия
Исследования на лекарственные взаимодействия не проводились.
Особые указания
Эндофтальмит
Побочные действия
При введении Эйлеа® всегда необходимо применять соответствующую технику проведения асептических инъекций. Кроме того, необходимо наблюдать за состоянием пациента в течение недели после проведения инъекции для обеспечения своевременного лечения при появлении признаков инфекционного процесса. Пациентов необходимо проинструктировать о том, что они должны без промедления сообщать при подозрении на какие-либо симптомы эндофтальмита или других вышеуказанных нарушений.
После проведения интравитреальных инъекций, в том числе препарата Эйлеа®, в течение первых 60 мин. наблюдается повышение внутриглазного давления (смотрите раздел «Побочные действия»). Пациенты с плохо контролируемой глаукомой нуждаются в особых мерах предосторожности. Эйлеа® не вводят когда внутриглазное давление ≥ 30 мм рт. ст. Во всех случаях необходимо проводить наблюдение за внутриглазным давлением и перфузией диска зрительного нерва и принимать соответствующие меры терапии.
Иммуногенность
Как и для других препаратов белковой природы существует вероятность развития иммуногенности на введение препарата Эйлеа®.
Пациенты должны быть проинструктированы о необходимости сообщать о любых признаках или симптомах интраокулярного воспаления, таких как боль, светобоязнь, покраснение, что может быть клиническим признаком повышенной чувствительности.
Системные эффекты
После интравитреальных инъекций ингибиторов VEGF отмечались системные побочные эффекты, включая внеглазные кровоизлияния и артериальные тромбоэмболические явления, которые теоретически могут быть обусловлены ингибированием VEGF. Данные о безопасности применения у пациентов с ДМО, ОЦВС, ОВВС, а также миопической ХНВ, имевших в анамнезе инсульт или транзиторные ишемические атаки в течение последних 6 месяцев, ограничены. Следовательно, при лечении таких пациентов следует соблюдать осторожность.
Другие
Как и при лечении другими ингибиторами VEGF для терапии ВМД, ОЦВС, ОВВС, ДМО и миопической ХНВ, следующие предостережения также применимы и к Эйлеа®.
-
Безопасность и эффективность терапии с Эйлеа® при введении в оба глаза систематически не изучалась. Если лечение проводится одновременно в оба глаза, это может привести к повышенному воздействию препарата, что может повысить риск развития системных побочных эффектов.
-
Одновременное применение с другими анти-VEGF препаратами, (ингибиторами фактора роста эндотелия сосудов).
Доступных данных об одновременном применении Эйлеа® с другими анти-VEGF препаратами (для системного или окулярного применения), нет.
-
Факторы риска, связанные с развитием разрыва пигментного эпителия сетчатки после терапии анти-VEGF препаратами для лечения влажной ВМД, включают обширную и/или высокую отслойку пигментного эпителия сетчатки. Перед началом лечения Эйлеа® следует проявлять осторожность пациентам, имеющим указанные факторы риска разрыва пигментного эпителия сетчатки.
-
Необходимо воздержаться от проведения лечения пациентам с регматогенной отслойкой сетчатки или с макулярным разрывом 3-4 степени.
-
В случае разрыва сетчатки следует воздержаться от введения дозы и не возобновлять его до тех пор, пока разрыв не будет устранен должным образом.
-
При нижеуказанных состояниях необходимо прекратить введение дозы и не возобновлять его ранее следующей запланированной инъекции препарата:
— снижение показателя наилучшей корригированной остроты зрения (НКОЗ) ≥30 букв по сравнению с показателем при последней оценке остроты зрения
— субретинальное кровоизлияние с вовлечением центра фовеа или, если размер кровоизлияния составляет ≥50% общей области поражения
-
Если проведено или запланировано хирургическое вмешательство на глазах необходимо воздержаться от введения дозы за 28 дней до и после операции.
-
Не cледует назначать Эйлеа® во время беременности, за исключением тех случаев, когда потенциальная польза от лечения превышает потенциальный риск для плода.
-
Женщинам репродуктивного возраста во время лечения препаратом необходимо использовать эффективную контрацепцию, по крайней мере в течение 3 месяцев после последней интравитреальной инъекции Эйлеа®.
-
Имеется ограниченный опыт применения препарата у пациентов с ишемической окклюзией центральной вены сетчатки и ее ветвей. Не рекомендуется применять препарат пациентам, имеющим клинические признаки необратимой потери функции зрения ишемического характера.
Популяции с ограниченными данными
Имеется ограниченный опыт применения препарата для лечения ДМО у пациентов с сахарным диабетом 1 типа или у диабетических пациентов с уровнем гликозилированного гемоглобина более 12% или с пролиферативной диабетической ретинопатией.
Эйлеа® не изучался у пациентов с активными системными инфекциями или у пациентов с сопутствующими заболеваниями глаз, такими как, отслойка сетчатки или макулярный разрыв. Также не имеется опыта применения препарата у диабетических пациентов с неконтролируемой артериальной гипертензией. Лечащий врач должен принимать во внимание недостаток данной информации при лечении таких пациентов.
Нет опыта применения препарата в лечении миопической ХНВ у лиц не азиатской популяции, пациентов, ранее получавших лечение по поводу миопической ХНВ, а также с экстрафовеальной локализацией поражения.
Беременность и период лактации
Беременность
Данные об использовании афлиберцепта у беременных женщин отсутствуют.
Доклинические исследования продемонстрировали эмбриофетальную токсичность.
Хотя системное воздействие после окулярного введения является очень низким, не cледует назначать Эйлеа® во время беременности, за исключением тех случаев, когда потенциальная польза от лечения превышает потенциальный риск для плода.
Лактация
Неизвестно, проникает ли афлиберцепт в грудное молоко. Нельзя исключить существование риска для ребенка находящегося на грудном вскармливании.
Не рекомендуется принимать Эйлеа® в период кормления грудью. Необходимо принять решение о прекращении кормления грудью или воздержании от приема препарата с учетом пользы от кормления для ребенка и пользы от терапии для женщины.
Фертильность
Результаты исследований на животных при высоком системном воздействии препарата свидетельствуют о том, что афлиберцепт может оказывать неблагоприятное влияние на фертильность у женщин и мужчин. Не ожидается подобных эффектов после окулярного введения препарата с очень низким системным воздействием.
Применение в педиатрии
Безопасность и эффективность препарата у детей и подростков не изучались.
Особенности влияния лекарственного средства на способность управлять транспортным средством и потенциально опасными механизмами
После инъекций Эйлеа® отмечается незначительное влияние на способность управлять транспортным средством и потенциально опасными механизмами вследствие возможных временных нарушений зрения после проведения интравитреальных инъекций препарата или сопутствующего обследования зрения.
Пациентам не следует управлять автомобилем или сложными механизмами до тех пор, пока зрительная функция не будет в достаточной степени восстановлена.
Передозировка
В клинических исследованиях дозы до 4 мг с интервалом в 1 месяц и отдельные случаи передозировки в дозе 8 мг в целом хорошо переносились.
Симптомы: передозировка в результате повышенного объема введения может привести к повышению внутриглазного давления.
Лечение: в случаях передозировки необходимо проводить наблюдение за внутриглазным давлением и при необходимости лечащий врач должен назначить адекватное лечение.
Форма выпуска и упаковка
По 0.278 мл раствора во флакон из бесцветного стекла типа I вместимостью 2 мл, укупоренный пробкой из бутилкаучука, фольгированный фторполимером; обжатый алюминиевым кольцом и полипропиленовым колпачком.
По 1 флакону, 1 фильтровальной игле вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
Условия хранения
Хранить при температуре от 2°С до 8°С. Не замораживать.
Хранить в картонной пачке для предотвращения воздействия света.
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту
Производитель
Регенерон Фармасьютикалс, Инк.,
Нью-Йорк 12144, США
Владелец регистрационного удостоверения
Байер Фарма АГ, Берлин, Германия.
Упаковщик
Байер Фарма АГ, Берлин, Германия.
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукта (товара)
ТОО «Байер КАЗ»
ул. Тимирязева, 42, бизнес-центр «Экспо-Сити», пав. 15
050057 Алматы, Республика Казахстан,
тел. +7 727 258 80 40, факс: +7 727 258 80 39,
e-mail: kz.claims@bayer.com
Инструкции по введению
Флакон предназначен только для однократного использования.
Перед введением следует визуально осмотреть флакон. Нельзя использовать флакон при наличии частиц, хлопьев или изменения цвета раствора.
Перед применением неоткрытый флакон может храниться при комнатной температуре (25 °C / 77°F) в течение максимум 24 часов. Все манипуляции с открытым флаконом следует проводить в асептических условиях.
Для интравитреального введения необходимо использовать иглу для инъекций размером 30 G x ½.
-
Снимите пластиковый колпачок и продезинфицируйте наружную часть резиновой пробки флакона
| 073721241477976842_ru.doc | 323.5 кб |
| 075162901477978000_kz.doc | 351.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
1 мл лекарственного средства содержит: активное вещество — афлиберцепта 40 мг,
вспомогательные вещества: натрия хлорид, натрия дигидрофосфат моногидрат, натрия гидрофосфат гептагидрат, сахароза, полисорбат 20, вода для инъекций.
Прозрачный, слегка опалесцирующий раствор.
Препараты для лечения заболеваний глаз. Средства для лечения сосудистых расстройств окологлазного пространства. Антинеоваскулярные средства. Афлиберцепт. Код ATX S01LA05.
Фармакологические свойства
Фармакокинетика
Лекарственное средство Эйлеа® вводится непосредственно в стекловидное тело для оказания локального воздействия.
Абсорбция / распределение
После интравитреального введения афлиберцепт медленно проникает в системный кровоток, где обнаруживается в основном в виде неактивного стабильного комплекса с VEGF (фактор роста эндотелия сосудов), при этом только «свободный афлиберцепт» может связывать эндогенный VEGF.
В исследовании фармакокинетики с частым отбором проб у 6 пациентов с неоваскулярной влажной возрастной макулярной дегенерацией (влажной ВМД) максимальная концентрация свободного афлиберцепта в плазме (системная Смакс) была низкой и составляла в среднем около 0,02 мкг/мл (в диапазоне от 0 до 0.054) в течение 1-3 дней после интравитреального введения 2 мг афлиберцепта, и через две недели после введения дозы, афлиберцепт вовсе не обнаруживался практически у всех пациентов. Афлиберцепт не кумулирует в плазме крови при интравитреальном введении каждые 4 недели.
Средняя максимальная концентрация свободного афлиберцепта в плазме крови примерно в 50-500 раз ниже, чем концентрация, необходимая для ингибирования биологической активности VEGF в системном кровотоке на 50% на животных моделях, у которых изменения артериального давления наблюдались после достижения концентрации свободного афлиберцепта в системном кровотоке около 10 мкг/мл, давление возвращалось к нормальным значениям при снижении концентрации ниже приблизительно 1 мкг/мл. В исследовании на здоровых добровольцах было установлено, что после интравитреального введения 2 мг афлиберцепта пациентам, средняя максимальная концентрация в плазме крови свободного афлиберцепта более чем в 100 раз ниже концентрации, необходимой для связывания половины максимального уровня системного VEGF (2.91 мкг/мл). Таким образом, развитие системных фармакодинамических эффектов, таких как изменения артериального давления, маловероятно.
Экскреция
Поскольку Эйлеа® — белковое лекарственное средство, никаких исследований метаболизма не проводилось.
Свободный афлиберцепт связывается с VEGF с образованием стабильного инертного комплекса. Ожидается, что, как и другие крупные белки, и свободный и связанный афлиберцепт будет выводиться из организма путем протеолитического катаболизма.
Нарушение функции почек
Никаких специальных исследований лекарственного средства Эйлеа® с участием пациентов с нарушенной функцией почек не проводилось.
Фармакодинамика
Афлиберцепт представляет собой рекомбинантный гибридный белок, состоящий из фрагментов внеклеточных доменов человеческих рецепторов VEGF (фактора роста эндотелия сосудов) 1 и 2, соединенных с Fc-фрагментом человеческого IgGl.
Афлиберцепт вырабатывается в клетках К1 яичника китайского хомячка (СНО/ЯКХ) по технологии рекомбинантной ДНК.
Афлиберцепт действует как растворимый рецептор-ловушка, связывающийся с VEGF-А и P1GF с большим сродством, чем их естественные рецепторы, и, таким образом, может ингибировать связывание и активацию этих родственных VEGF рецепторов.
Механизм действия
Эндотелиальный сосудистый фактор роста А (VEGF-А) и плацентарный фактор роста (P1GF) относятся к семейству VEGF ангиогенных факторов, которые обладают мощным митогенным, хемотаксическим действием в отношении эндотелиальных клеток и повышают проницаемость сосудов. VEGF действует посредством двух типов тирозинкиназных рецепторов, VEGFR-1 и VEGFR-2, которые присутствуют на поверхности эндотелиальных клеток. P1GF связывается только с фактором VEGFR-1, который также присутствует на поверхности лейкоцитов. Избыточная активация VEGF-А этих рецепторов может привести к патологической неоваскуляризации и избыточной проницаемости сосудов. В этих процессах P1GF может проявлять синергизм с VEGF-А и стимулировать инфильтрацию лейкоцитов и сосудистое воспаление.
Фармакодинамические эффекты
Неоваскулярная влажная возрастная макулярная дегенерация (влажная ВМД)
Влажная ВМД характеризуется патологической хориоидальной неоваскуляризацией (ХНВ). Просачивание крови и жидкости из участков ХНВ может вызвать утолщение или отек сетчатки и/или суб-/интраретинальное кровоизлияние, что приводит к снижению остроты зрения.
У пациентов, получавших лекарственное средство Эйлеа® (одна инъекция в месяц в течение трех первых месяцев, с последующей одной инъекцией каждый месяц или каждые 2 месяца), отмечалось уменьшение толщины центральной зоны сетчатки (ТЦЗС) вскоре после начала лечения и уменьшение среднего размера патологического участка ХНВ, что соответствует результатам, полученным у пациентов на фоне ежемесячного введения ранибизумаба в дозе 0.5 мг.
Макулярный отек вследствие окклюзии центральной вены сетчатки (ОЦВС) или ее ветвей (ОВВС)
При ОЦВС и ОВВС развивается ишемия сетчатки, провоцирующая высвобождение VEGF, которые в свою очередь дестабилизируют плотные соединения и стимулируют пролиферацию эндотелиальных клеток. Повышение активности VEGF приводит к нарушению гематоретинального барьера, повышенной проницаемости сосудов, отеку сетчатки и неоваскуляризации.
У пациентов, получавших терапию лекарственным средством Эйлеа® (одна инъекция раз в месяц на протяжении шести месяцев), наблюдалась постоянная, быстрая и устойчивая ответная реакция в отношении морфологии (ТЦЗС по данным ОКТ). Улучшение среднего показателя ТЦЗС сохранялось на протяжении 24 недель.
Диабетический макулярный отек (ДМО)
ДМО является последствием диабетической ретинопатии и характеризуется повышенной проницаемостью сосудов и повреждением капилляров сетчатки, что может привести к потере остроты зрения.
У пациентов, получавших лекарственное средство Эйлеа®, большинство из которых страдали диабетом II типа, вскоре после начала лечения наблюдался быстрый и устойчивый морфологический ответ (ТЦЗС согласно оценке данных ОКТ).
Миопическая хориоидальная неоваскуляризация (миопическая ХНВ)
Миопическая ХНВ является частой причиной потери зрения у взрослых людей с патологической миопией. Она развивается как механизм заживления ран вследствие разрывов мембран Бруха и представляет собой наиболее опасное для зрения явление в патологической миопии.
Лекарственное средство Эйлеа® показано взрослым пациентам для лечения:
неоваскулярной (влажной) возрастной макулярной дегенерации (влажной ВМД);
снижения остроты зрения, вызванного макулярным отеком вследствие окклюзии вен сетчатки (центральной вены (ОЦВС) или ее ветвей (ОВВС));
снижения остроты зрения, вызванного диабетическим макулярным отеком (ДМО);
снижения остроты зрения, вызванного миопической хориоидальной неоваскуляризацией (миопической ХНВ).
Способ применения и дозировка
Лекарственное средство Эйлеа® предназначено только для интравитреального введения.
Лекарственное средство должно вводиться только квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций.
Режим дозирования
Неоваскулярная возрастная макулярная дегенерация
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл раствора для инъекций.
Лечение Эйлеа® начинают с трех последовательных инъекций 1 раз в месяц. Затем интервал между инъекциями увеличивают до двух месяцев.
На основании заключения врача о результатах изменения остроты зрения и/или анатомических показателей интервал между инъекциями может поддерживаться на уровне двух месяцев или впоследствии увеличиваться при лечении в режиме «лечить и увеличивать интервал», при котором интервалы между введениями доз препарата увеличиваются с шагом в 2 или 4 недели для поддержания достигнутых стабильных остроты зрения и/или анатомических показателей. В случае ухудшения остроты зрения и/или анатомических показателей интервалы между инъекциями должны быть соответственно сокращены до минимума — два месяца в течение первых 12 месяцев лечения.
Нет необходимости в проведении мониторинга между инъекциями. На основании заключения врача контрольные обследования могут выполняться чаще, чем визиты для проведения инъекций.
Интервалы лечения больше четырех месяцев между инъекциями не изучались.
Макулярный отек, разившийся вследствие ОЦВС или ОВВС
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл раствора для инъекций.
После начальной инъекции лекарственного средства лечение проводят каждый месяц. Интервал между двумя инъекциями должен быть не менее одного месяца.
Если не наблюдается улучшение остроты зрения и анатомических показателей после непрерывного лечения, терапия лекарственным средством Эйлеа® должна быть прекращена.
Ежемесячная терапия продолжается до достижения максимально возможной остроты зрения в отсутствие признаков активности заболевания. Для этого может потребоваться
три или более последовательных ежемесячных инъекции.
Затем лечение может быть продолжено в режиме «лечить и увеличивать интервал» при постепенном увеличении интервалов времени между инъекциями для поддержания достигнутых стабильных остроты зрения и /или анатомических показателей, однако имеющихся данных недостаточно для того, чтобы сделать вывод о продолжительности этих интервалов. В случае ухудшения остроты зрения и (или) анатомических показателей интервалы между инъекциями должны быть соответствующим образом сокращены.
График мониторинга и лечения должен определяться лечащим врачом индивидуально, на основании ответа пациента.
Мониторинг проявлений активности заболевания может включать в себя стандартный офтальмологический осмотр, функциональную диагностику или проведение визуальных методов исследования (например, оптическую когерентную томографию или флуоресцеиновую ангиографию).
ДМО
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, (эквивалентно 50 мкл раствора для инъекций) интравитреально в виде первых пяти последовательных ежемесячных инъекций, с дальнейшим интервалом лечения 1 инъекция в 2 месяца. Нет необходимости в проведении мониторинга между инъекциями.
Через 12 месяцев лечения Эйлеа® интервал между инъекциями может быть увеличен на основании результатов изменения остроты зрения и анатомических показателей; при лечении в режиме «лечить и увеличивать интервал» интервалы между введениями доз препарата постепенно увеличиваются для поддержания достигнутых стабильных остроты зрения и/или анатомических показателей, однако данных для установления длины таких интервалов недостаточно. В случае ухудшения остроты зрения и анатомических показателей интервалы между инъекциями должны быть соответственно сокращены. В этом случае лечащий врач должен составить график контрольных обследований, которые могут быть более частыми, чем инъекции.
Если результаты остроты зрения и анатомические показатели указывают на отсутствие эффекта от проводимого лечения, терапию лекарственным средством Эйлеа® следует прекратить.
Миопическая ХНВ
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 50 мкл раствора для инъекций.
Дополнительные дозы могут вводиться, если результаты остроты зрения и/или анатомические показатели показывают, что заболевание сохраняется. Рецидивы следует рассматривать как новое проявление заболевания.
График мониторинга определяется лечащим врачом.
Интервал между двумя инъекциями должен составлять не менее одного месяца.
Дополнительная информация для особых категорий пациентов
Пациенты с нарушениями функции печени и/или почек
Какие — либо специальные исследования Эйлеа® у больных с нарушениями функции печени и почек не проводились. На основании доступных данных, коррекции дозы у таких пациентов не требуется.
Пожилые пациенты
Особых мер предосторожности не требуется. Опыт применения у пациентов старше 75 лет с диабетическим макулярным отеком ограничен.
Применение в педиатрии
Безопасность и эффективность лекарственного средства у детей и подростков не изучалась. Лекарственное средство Эйлеа® не показано к применению у данной группы пациентов при влажной ВМД, ОЦВС, ОВВС, ДМО и миопической ХНВ.
Техника введения
Интравитреальные введения должны осуществляться квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций в соответствии с медицинскими стандартами и действующими руководящими положениями. В целом должны обеспечиваться адекватная анестезия и асептические условия, включая применение наружных бактерицидных средств широкого спектра действия (например, наносить повидон-йод на кожу вокруг глаза, веко и поверхность глаза). Рекомендуется дезинфекция рук хирурга, использование стерильных перчаток и салфеток, стерильного векорасширителя (или его эквивалента).
Инъекционную иглу следует вводить в стекловидное тело на 3.5-4.0 мм кзади от лимба, избегая горизонтального меридиана и направляя ее к центру глазного яблока. Объем введенного препарата составляет 0.05 мл. Следующая инъекция лекарственного средства проводится в другой участок склеры.
Сразу после интравитреальной инъекции состояние пациента необходимо контролировать на предмет повышения внутриглазного давления. Надлежащий мониторинг может состоять из проверки перфузии диска зрительного нерва или офтальмотонометрии. При необходимости следует обеспечить доступ к стерильному оборудованию для проведения парацентеза.
После интравитреальной инъекции пациентам необходимо без промедления сообщать о каких-либо симптомах эндофтальмита (например, боль в глазу, покраснение глаза, светобоязнь, нечеткость зрения).
Каждый флакон должен применяться только для лечения одного глаза. Извлечение нескольких доз из флакона может увеличить риск загрязнения и последующего инфицирования.
Флакон содержит дозу афлиберцепта, превышающую рекомендованную дозу 2 мг. Извлекаемый из флакона объем (100 мкл) не следует использовать целиком. Избыточный объем следует выпустить из шприца до инъекции. Ввод всего объема флакона может привести к передозировке. Для удаления пузырьков воздуха и избыточного объема лекарственного средства, медленно нажимайте на поршень шприца, чтобы совместить цилиндрическое основание поршня с черной меткой дозы на шприце (эквивалентной 50 микролитрам, т.е. 2 мг афлиберцепта).
После инъекции все неиспользованное лекарственное средство должно быть утилизировано.
О любых побочных эффектах, развившихся на фоне применения лекарственного средства, в том числе и не описанных в инструкции, необходимо сообщить врачу.
Оценка безопасности применения лекарственного средства Эйлеа® осуществлялась в ходе исследований фазы III с участием 3102 пациентов. Из них 2501 пациентов получали рекомендованную дозу 2 мг.
Серьезные офтальмологические нежелательные реакции, связанные с инъекцией Эйлеа® наблюдались менее чем в одной из 1900 проведенных интравитреальных инъекций, и включали слепоту, эндофтальмит, отслойку сетчатки, травматическую катаракту, катаракту, кровоизлияние в стекловидное тело, отслойку стекловидного тела и повышение внутриглазного давления (смотрите раздел «Меры предосторожности»). Наиболее распространенными нежелательными реакциями (как минимум у 5 % пациентов, получивших терапию Эйлеа®) были субконъюнктивальное кровоизлияние (25%), снижение остроты зрения (11%), боль в глазу (10%), катаракта (8%), повышение внутриглазного давления (8 %), отслойка стекловидного тела (7 %), плавающие помутнения стекловидного тела (7 %).
Перечисленные ниже данные по безопасности лекарственного средства включают в себя все нежелательные реакции, основанные на исследованиях фазы III по показаниям влажная ВМД, ОЦВС, ОВВС, ДМО и миопическая ХНВ с указанием возможности наличия причинно-следственной связи с процедурой введения или с лекарственным средством.
Нежелательные лекарственные реакции классифицированы в соответствии с системно-органными классами: очень часто (> 1/10), часто (> 1/100, < 1/10), нечасто (> 1/1 000, < 1/100), редко (> 1/10 000, < 1/1 000). В рамках каждой группы нежелательные реакции представлены в порядке уменьшения степени тяжести.
| Системно-органные классы | Очень часто | Часто | Нечасто | Редко |
| Нарушения со стороны иммунной системы | реакции гиперчувствительности*** | |||
| Нарушения со стороны органа зрения | снижение остроты зрения, субконъюнктивальное кровоизлияние, боль в глазу | разрыв пигментного эпителия сетчатки*, отслойка пигментного эпителия сетчатки, дегенерация сетчатки, кровоизлияние в стекловидное тело, катаракта, кортикальная катаракта, ядерная катаракта, субкапсулярная катаракта, эрозия роговицы, повреждение роговицы, повышение внутриглазного давления, нечеткость зрения, плавающие помутнения стекловидного тела, отслойка стекловидного тела, боль в месте введения, ощущение инородного тела в глазах, повышенное слезоотделение, отек век, кровоизлияние в месте введения, точечный кератит, гиперемия конъюнктивы, окулярная гиперемия | эндофтальмит* *, отслойка сетчатки, разрыв сетчатки, ирит, увеит, иридоциклит, помутнение хрусталика, повреждение эпителия роговицы, раздражение в месте введения, аномальная чувствительность тканей глаза, покраснение век, воспаление передней камеры глаза, отек роговицы | слепота, травматическая катаракта, воспаление стекловидного тела, гипопион |
* Состояния, как известно, связанные, с влажной ВМД. Наблюдались только в исследованиях с влажной ВМД.
** Эндофтальмит с положительной и отрицательной культурой.
*** В пострегистрационном периоде сообщения о реакциях гиперчувствительности включали сыпь, зуд, крапивницу и в отдельных случаях — тяжелые анафилактические/анафилактоидные реакции.
Описание отдельных нежелательных реакций
Артериальная тромбоэмболия (АТЯ) является нежелательным явлением, потенциально связанным с системным ингибированием эндотелиального фактора роста сосудов (VEGF). Теоретически существует риск развития АТЯ после интравитреального применения ингибиторов VEGF, включая инфаркт миокарда и инсульт.
Как и все лекарственные средства белковой природы Эйлеа® обладает иммуногенным потенциалом.
повышенная чувствительность к афлиберцепту или вспомогательным компонентам лекарственного средства;
активная или подозреваемая окулярная или периокулярная инфекция;
активное тяжелое внутриглазное воспаление.
Лекарственные взаимодействия
Исследования в отношении лекарственных взаимодействий не проводились. Осуществление вспомогательной фотодинамической терапии с применением вертепорфина (PDT) и Эйлеа не изучалось, поэтому, профиль безопасности не был установлен.
Реакции, обусловленные интравитреальным введением
Интравитреальные инъекции, включая инъекции лекарственного средства Эйлеа®, могут вызвать развитие эндофтальмита, внутриглазное воспаление, регматогенную отслойку сетчатки, разрыв сетчатки и ятрогенную травматическую катаракту (см. раздел «Побочное действие»).
При введении лекарственного средства Эйлеа® всегда необходимо соблюдать соответствующую технику асептического проведения инъекций. Кроме того, необходим мониторинг пациентов в течение недели после инъекции, для выявления первых признаков воспаления и своевременного назначения необходимой терапии.
При появлении каких-либо симптомов, свидетельствующих о развитии эндофтальмита или любой другой реакции, указанной выше, необходимо немедленно сообщить врачу. Наблюдались случаи повышения внутриглазного давления в первые 60 минут после интравитреальных инъекций, включая инъекции лекарственного средства Эйлеа® (смотрите раздел «Побочное действие»). Пациенты с плохо контролируемой глаукомой нуждаются в особых мерах предосторожности. Лекарственное средство Эйлеа® не следует вводить при внутриглазном давлении > 30 мм рт. ст. Во всех случаях необходим контроль внутриглазного давления и перфузии диска зрительного нерва с назначением соответствующей состоянию терапии.
Иммуногенность
Так как Эйлеа® представляет собой белок с терапевтическими свойствами, существует вероятность проявления иммуногенности (см. раздел «Побочное действие»). При появлении признаков или симптомов внутриглазного воспаления, таких как боль, светобоязнь или покраснение, которые могут являться клиническими проявлениями гиперчувствительности к лекарственному средству, необходимо сообщить врачу.
Системные эффекты
После интравитреальных инъекций ингибиторов VEGF были отмечены системные нежелательные явления, включая кровоизлияния вне органа зрения и тромбоэмболии артерий. Существует теоретический риск связи этих явлений с ингибированием VEGF. Имеются ограниченные данные относительно безопасности применения афлиберцепта пациентами с ОЦВС, ОВВС, ДМО или миопической ХНВ с анамнестическими сведениями об инсульте, транзиторной ишемической атаке или инфаркте миокарда за период в 6 месяцев перед началом терапии. Указанным пациентам следует соблюдать осторожность при терапии лекарственным средством Эйлеа®.
Прочее
Как и в случае интравитреального введения других анти-VEGF препаратов при влажной ВМД, ОЦВС, ОВВС, ДМО и миопической ХНВ, следует принять во внимание следующее:
Безопасность и эффективность лекарственного средства Эйлеа® при введении одновременно в оба глаза систематически не изучались (см. раздел «Фармакодинамика»). Одновременное билатеральное введение может привести к повышению системной экспозиции лекарственного средства, что, в свою очередь, повышает риск системных нежелательных явлений.
Сопутствующее применение других анти-VEGF (фактор роста эндотелия сосудов). Отсутствуют данные об одновременном применении лекарственного средства Эйлеа® с другими анти-VEGF препаратами (системными или глазными).
Факторы риска, связанные с нарушением целостности слоя пигментных клеток после анти-VEGF терапии влажной ВМД, включают распространенную и/или локализованную в верхних отделах отслойку пигментного эпителия сетчатки. Пациентам с факторами риска развития разрывов пигментного эпителия сетчатки следует соблюдать осторожность в начале терапии лекарственным средством Эйлеа®.
Пациентам с регматогенной отслойкой сетчатки или макулярными разрывами 3 или 4 стадии от лечения следует воздержаться.
В случае разрыва сетчатки введение дозы следует остановить и не возобновлять лечение до достаточного восстановления места разрыва.
От инъекции следует воздержаться до следующей запланированной по графику инъекции в случае:
снижения наилучшей корригированной остроты зрения (BCVA) более чем на 30 букв, по сравнению с последней оценкой остроты зрения;
субретинальных кровоизлияний, затрагивающих центральную ямку, или в случае размера кровоизлияния >50% общей площади поражения.
Следует воздержаться от введения дозы лекарственного средства в течение предыдущих или последующих 28 дней в случае выполнения или планирования операции на глазу.
Лекарственное средство Эйлеа® не следует использовать во время беременности, за исключением случаев, когда потенциальная выгода превышает потенциальный риск для плода (см. раздел «Беременность и период лактации»).
Женщинам репродуктивного возраста следует использовать эффективные способы контрацепции в период лечения и в течение, по меньшей мере, 3 месяцев после последней интравитреальной инъекции афлиберцепта.
Имеется ограниченный опыт лечения пациентов с ишемическим макулярным отеком вследствие окклюзии ветви вены сетчатки и ишемическим макулярным отеком вследствие окклюзии центральной вены сетчатки. Пациентам с клиническими признаками необратимой ишемической потери зрительной функции терапия афлиберцептом не рекомендована.
Группы пациентов с ограниченными данными
Имеется только ограниченный опыт лечения ДМО у пациентов с сахарным диабетом типа I, у пациентов с уровнем гликированного гемоглобина более 12 %, или у пациентов с пролиферативной диабетической ретинопатией. Лекарственное средство Эйлеа® не изучалось у пациентов с активными системными инфекциями или у пациентов с сопутствующими заболеваниями глаз, такими как отслойка сетчатки или разрыв макулы. Также отсутствует опыт лечения лекарственным средством Эйлеа® пациентов с сахарным диабетом и неконтролируемой гипертензией. При лечении таких пациентов врач должен учитывать этот дефицит информации.
Отсутствует опыт лечения миопической ХНВ у пациентов не азиатской популяции, пациентов ранее проходивших лечение миопической ХНВ, и пациентов с экстрафовеальными поражениями.
Женщины репродуктивного возраста
Женщинам репродуктивного возраста во время терапии лекарственным средством Эйлеа® необходимо использовать эффективную контрацепцию, по крайней мере, в течение 3 месяцев после последней интравитреальной инъекции.
Беременность
Данные по применению афлиберцепта у беременных женщин отсутствуют.
В исследования на животных была продемонстрирована эмбрио-фетотоксичность.
Несмотря на то, что системная экспозиция после внутриглазного введения Эйлеа® очень мала, лекарственное средство не следует применять при беременности, за исключением тех случаев, когда потенциальная польза от лечения превышает потенциальный риск для плода.
Период грудного вскармливания
Неизвестно, проникает ли афлиберцепт в грудное молоко. Нельзя исключить существование риска для ребенка находящегося на грудном вскармливании.
Не рекомендуется принимать лекарственное средство Эйлеа® в период грудного вскармливания. Необходимо принять решение о прерывании грудного вскармливания или воздержании от приема лекарственного средства, принимая во внимание пользу грудного вскармливания для ребенка и пользу лечения для матери.
Фертильность
Результаты исследований на животных с высокой системной экспозицией показывают, что афлиберцепт может нарушать мужскую и женскую фертильность. Подобные эффекты маловероятны после внутриглазного введения лекарственного средства с учетом очень низкой системной экспозиции.
Влияние лекарственного средства на способность управлять транспортными средствами и потенциально опасными механизмами
У пациентов могут наблюдаться временные нарушения зрения, связанные как с инъекцией, так и с процедурой обследования.
Пациентам не следует управлять автомобилем или сложными механизмами до восстановления четкости зрительного восприятия.
В клинических исследованиях применялись дозы до 4 мг с интервалом в 1 месяц, наблюдались отдельные случаи передозировки при применении дозы 8 мг.
Симптомы: передозировка в результате введения большего объема может привести к повышению внутриглазного давления.
Лечение: в случаях передозировки следует контролировать внутриглазное давление, при необходимости лечащий врач должен назначить адекватную терапию по его коррекции.
Форма выпуска и упаковка
По 0.278 мл раствора во флакон из бесцветного стекла типа I, вместимостью 2 мл. укупоренный пробкой из бутилкаучука, фольгированный фторполимером, обжатый алюминиевым кольцом и полипропиленовым колпачком.
По 1 флакону, 1 фильтровальной игле вместе с инструкцией по медицинскому применению помещают в пачку из картона.
Хранить при температуре от 2 °C до 8 °C. Не замораживать.
Хранить в картонной пачке для предотвращения воздействия света.
Хранить в недоступном для детей месте!
Перед использованием невскрытый флакон может храниться при температуре не выше 25°С до 24 часов. После вскрытия флакона необходимо соблюдать асептические условия.
Срок хранения
2 года.
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту
Информация о производителе
Владелец регистрационного удостоверения:
Байер АГ, Германия.
Производитель готовой лекарственной формы:
Регенерон Фармасьютикалс, Инк.,
Нью-Йорк 12144, США.
Выпускающий контроль качества/Упаковка:
Байер АГ, Германия
13353 Берлин, Мюллерштрассе 178, Германия.
Дополнительную информацию можно получить по адресу: 220089, Минск, пр-т Дзержинского 57, 14 эт.
Тел.: +375(17) 239-54-20 (30).
Факс. +375(17) 336-12-36.
Инструкции по введению
Флакон предназначен только для однократного использования (для одного глаза).
Флакон содержит 100 мкл извлекаемого объема лекарственного средства, что превышает рекомендованную дозу в 50 мкл. Извлекаемый из флакона объем (100 мкл) не следует использовать целиком, часть его должна быть отброшена перед применением.
Перед введением следует визуально осмотреть флакон. Нельзя использовать флакон при наличии посторонних частиц и/или изменения цвета раствора или при любом изменении внешнего вида раствора.
Для интравитреального введения необходимо использовать иглу для инъекций размером 30 G × 1/2.
Снимите пластиковый колпачок и продезинфицируйте наружную часть резиновой пробки флакона.
Соедините иглу 18G с 5-микронным фильтром, вложенную в картоннуюупаковку с 1-милиллитровым стерильным шприцем с замком Люэра.
Вводите фильтровальную иглу в центр пробки флакона, пока она полностью не войдет во флакон, а кончик не достигнет дна или нижнего края флакона.
В асептических условиях извлеките все содержимое флакона лекарственного средства Эйлеа® в шприц, удерживая флакон в вертикальном положении, слегка наклонив его для полного извлечения лекарственного средства. Чтобы предотвратить попадание воздуха необходимо обеспечить погружение косого края фильтровальной иглы в жидкость. Продолжайте наклонять флакон во время отбора лекарственного средства, удерживая срез фильтровальной иглы погруженным в жидкость.
Удостоверьтесь в том, что шток поршня при заборе раствора из флакона в достаточной степени поднят, и игла с фильтром пустая.
Снимите фильтровальную иглу и утилизируйте ее надлежащим образом.
Примечание: фильтровальная игла не предназначена для интравитреальных инъекций.
В условиях асептики, скручивающим движением наденьте крепко иглу для инъекций 30G × 1/2 дюйма на переходную канюлю шприца с люэровским замком.
8. Удерживая шприц с поднятой вверх иглой, проверьте его на наличие пузырьков. Если есть пузырьки, мягко постучите по шприцу пальцем до тех пор, пока все пузырьки не поднимутся вверх.
9. Устраните все пузырьки и удалите излишки лекарственного средства, медленно нажимая на поршень шприца так, чтобы его конец совпал с линией на отметке 0,05 мл на шприце.
10. Флакон предназначен только для одноразового использования.
Извлечение нескольких доз из флакона может увеличить риск загрязнения и последующего инфицирования.
Весь неиспользованный объем лекарственного препарата или отходы должны быть утилизированы.

Товары из категории — Лекарства для глаз
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 43 050
Немного фактов
Лекарственное средство применяется для внутриглазного метода ввода, чтобы воспрепятствовать новообразованию сосудов в органах зрения. Эйлеа вводится непременно в стекловидное тело глазного яблока для более эффективного локального воздействия.
Состав и форма выпуска
Для препарата эйлеа активным веществом является афлиберцепт. Для полноценного раскрытия всех лекарственных свойств основы, применяются сопутствующие элементы: моногидрат дигидрофосфата натрия, хлорид натрия, полисорбат, сахароза, гептагидрат гидрофосфата натрия, вода для инъекций.
Средство выпускается во флаконе 0,1 мл готового раствора, афлиберцепт присутствует в количестве 4 мг. Это прозрачная, слегка вязкая жидкость, с легким желтым оттенком.
Показания к применению
Эйлеа предназначен, как лекарственное средство для следующих заболеваний:
- влажная макулодистрофия — поражение области сетчатки, искажение видимых образов и линий, затруднения в чтении, быстрое образование новых сосудов, распространяющихся к желтому пятну, нарушение нормальной работы центрального зрения;
- центральная окклюзия вен сетчатки — закупоривание центральной артерии и вен, которые выступаю, как единственный источник получения крови для сетчатки, вследствие чего нарушается острота зрения, частично повреждается сетчатка, может пропасть зрение или развиться глаукома.
- диабетический макулярный отек — чрезмерное накопление в желтом пятне и под ним жидкости и белковых образований, вследствие чего пятно разбухает и искажает центральное поле зрения и его остроту.
Побочные эффекты
В ходе курса использования данного препарата могут возникнуть боли в глазном яблоке, повысится внутриглазное давление, снизиться острота зрения, отслоится сетчатка, появиться кровоизлияния, гнойные образования на оболочках глаза, развиться катаракта.
Для иммунной системы есть риск возникновения гиперчувствительности, как к применяемому веществу (эйлеа) и другим, более привычным элементам.
Для органов зрения, как было указано ранее, это опасность развития болезненных процессов связанных с сетчаткой, кровяным снабжением, общим восприятием объектов.
В медицинской практике описаны случаи разрыва тканей глазного яблока, значительного помутнения стекловидного тела и хрусталика, слезотечения и общая воспаленнность глаза.
В период лечения на кожных покровах может проступить сыпь, значительный зуд, крапивница, головная боль, пониженное настроение, упадок сил.
При влажной макулодистрофии, отмечаются частые кровотечения у пациентов, дополнительно принимающих препараты, противодействующие образованию тромбов. Это возникает потому что, афлиберцепт, зачастую дает негативные последствия при воздействии с ранибизумабом.
Также, вещества, замедляющие и прекращающие работу фактора роста эндотелия сосудов, могут спровоцировать возникновение кризиса, который приведет к инсульту или инфаркту миокарда.
Как и все белки, применяющиеся в терапии, эйлеа способен активировать иммунный ответ без учета иммунной специфичности антигена.
Противопоказания
Употребление данного препарата первоочередно не рекомендовано пациентам, которые не переносят афлиберцепт и другие компоненты средства в любых дозировках.
Эйлеа не должен быть использован при периокулярном дерматите или подозрении на возникновение этой инфекции. В значительной степени, это запрет распространяется на случай периокулярного дерматита, при поражении кожи на веках.
При анамнезе стоит взять анализы и исследовать глазное яблоко на предмет воспалительных реакций. При выявлении тяжелых воспалительных процессов, препарат не принимать до устранения усугубляющих факторов.
В очень редких случаях, действие лекарства снижает возможность взрослого организма производить полноценное здоровое потомство, как у мужчин, так и у женщин.
Препарат не рекомендован для применения при лечении пациентов, которым не исполнилось 18 лет, поскольку он оказывает сильное воздействие на неокрепший организм.
Объективных данных по применение эйлеа для беременных женщин и кормящих матерей нет, есть лишь единичные тяжелые случаи. Поэтому, для профилактических мер, не стоит планировать беременность в период активного лекарственного курса, а также в течении трех месяцев после его окончания, поскольку есть вероятность негативного воздействия на развитие плода. Эта же причина относится к женщинам в лактационный период. Все употребляемые вещества попадают в молоко в полном количестве, поэтому ребенок может получить огромную дозу вещества. Единственно возможным случаем использования лекарства для беременных и кормящих женщин, является положительный эффект для выздоровления, который превышает возможные риски.
Особо осторожным следует быть при использовании эйлеа в лечении больных, у которых есть глаукома, практически не контролируемая медикаментозным лечением, сердечная или почечная недостаточность, нарушенная пигментная целостность эпителия на сетчатке, в течении последнего полугодия был инсульт, инфаркт миокарда или ишемическая атака.
Особых ограничений для людей пожилого возраста нет, но после 75 лет необходимо особо оценивать риски и пользу, которую даст препарат эйлеа.
Приобретение и хранение
Средство продается в специализированной аптеке по рецептному бланку вашего лечащего врача. Для сохранения лечебных свойств препарата эйлеа, его необходимо поместить в темное место с температурой от 2 до 8 градусов тепла. Лекарство действительно до двух лет от даты производства, а при открытии — до 24 часов при температуре 20-25 градусов тепла. Эйлеа ни в коем случае не стоит замораживать.
МКБ-10
Средство применяется в лечебном курсе для следующих болезней:
- Н34 — нарушение проходимости сосудов сетчатки;
- Н35.3 — дегенерация желтого пятна и заднего полюса;
- Н36 — диабетическое поражение сосудов в сетчатой оболочке глазного яблока;
- Н58.1 — нарушения нормального функционирования зрения, которое усугублено предыдущими болезнями.
Аналоги
Если препарат эйлеа невозможно задействовать в лечении из-за непереносимости, либо же по иным объективным причинам, то рекомендуются следующие альтернативные средства:
- офтоципро;
- миртилене форте;
- сигницеф;
- тобразон.
Способ и особенности применения препарата
Средство эйлеа используется исключительно для введения в стекловидное тело глаза. Количество, содержащееся во флаконе, рассчитано на 1 дозу для взрослого человека, не имеющего сопутствующих болезни осложнений. Для прочих пациентов доза должна быть рассчитана исходя из анамнеза и показателей анализов.
Период лечения препаратом начинается с трех месяцев по одному уколу ежемесячно, далее, каждые два месяца. После годового курса возможно увеличение интервала введения эйлеа, если видна тенденция нормализации здоровья.
При отсутствии улучшения остроты зрения хотя бы на какой-то уровень, рекомендуется прервать лечение этим средством.
Имеется незначительное влияние препарата эйлеа на водителей автомобилей.
Инъекцию препарата эйлеа должен осуществлять опытный специалист.
Передозировка
Случаи превышения рекомендованной дозы в 4мг, приводят к значительному увеличению давления внутри глаза. При подобных симптомах, следует проводить терапию по контролю давления и его постепенному понижению. Пациентов с усугубляющими болезнь факторами следует поместить под особый контроль.
Следует помнить, негативное воздействие не всегда является причиной прерывать лечение и проводить терапевтические меры по выводу препарата из организма. У многих пациентов отмечено небольшое увеличение артериального давления в течения часа после ввода инъекции, но оно самостоятельно нормализуется, в большинстве случаев.
Совместимость с алкоголем
Инструкция не дает однозначного запрета на употребления алкоголя и данного лекарства. Но известно, что эйлеа не влияет на метаболические процессы в организме, лишь на давление в глазном яблоке и некоторые другие реакции. Поэтому не следует употреблять алкоголь в период 3-5 дней до и после инъекции.
Взаимодействие с другими лекарствами
Средство нередко применяется в комплексе с вертепорфином, объективных данных по их пагубности или улучшения терапии не имеется. Впрочем, не нужно увеличивать количество активного элемента в эйлеа с другими лекарствами. При возникшей ситуации лучше всего подобрать альтернативу.
Терапия должна проходить в постоянном увеличении интервала ввода лекарства. Побочные эффекты могут быть устранены терапевтическими методами, либо рациональным комплексным подходом к лечебному курсу, либо же прекращению применения данного средства.
Важно помнить о других болезнях и побочных факторах, на которые может воздействовать описываемое лекарство. Хотя объективных данных для пациентов с дисфункцией почечной системы, нарушении работы печени, нет, все же следует проявить к этим людям особое внимание во избежание негативного действия.
Побочные эффекты возникают в первые дни, поэтому контроль на протяжении всего периода между инъекциями не требуется, если пациент не ощущает осложнений.
дко применяется в комплексе с вертепорфином, объективных данных по их пагубности или улучшения терапии не имеется. Впрочем, не нужно увеличивать количество активного элемента в эйлеа с другими лекарствами. При возникшей ситуации лучше всего подобрать альтернативу.
Терапия должна проходить в постоянном увеличении интервала ввода лекарства. Побочные эффекты могут быть устранены терапевтическими методами, либо рациональным комплексным подходом к лечебному курсу, либо же прекращению применения данного средства.
Важно помнить о других болезнях и побочных факторах, на которые может воздействовать описываемое лекарство. Хотя объективных данных для пациентов с дисфункцией почечной системы, нарушении работы печени, нет, все же следует проявить к этим людям особое внимание во избежание негативного действия.
Побочные эффекты возникают в первые дни, поэтому контроль на протяжении всего периода между инъекциями не требуется, если пациент не ощущает осложнений.
Цены на Эйлеа в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 43 050 руб.
Сертификаты и лицензии
Один мл препарата содержит
активное вещество – афлиберцепт, 40 мг,
вспомогательные вещества: натрия хлорид, натрия дигидрофосфата моногидрат, натрия гидрофосфата гептагидрат, сахароза, полисорбат 20, вода для инъекций.
Прозрачный, слегка опалесцирующий раствор.
Органы чувств. Офтальмологические препараты. Средства для лечения сосудистых расстройств окологлазного пространства. Антинеоваскулярные средства. Афлиберцепт.
Код АТХ S01LA05
Эйлеа® показан для лечения взрослых при:
— неоваскулярной (влажной) возрастной макулярной дегенерации (ВМД)
— нарушении зрения вследствие макулярного отека, обусловленного окклюзией вен сетчатки (центральной вены сетчатки (ОЦВС) или ее ветвей (ОВВС))
— нарушении зрения вследствие диабетического макулярного отека (ДМО)
— нарушении зрения вследствие миопической хориоидальной неоваскуляризации (миопической ХНВ)
— гиперчувствительность к афлиберцепту или к любому из вспомогательных веществ
— активная окулярная или периокулярная инфекция или подозрение на них
— активное тяжелое интраокулярное воспаление.
Прослеживаемость
Для того чтобы улучшить прослеживаемость биологических лекарственных препаратов следует четко записывать название и номер серии вводимого препарата.
Реакции, связанные с процедурой интравитреальной инъекции
Интравитреальные инъекции, включая инъекции Эйлеа®
были ассоциированы с эндофтальмитом, интраокулярным воспалением, регматогенной отслойкой сетчатки глаза, разрывом сетчатки глаза и ятрогенной травматической катарактой.
При введении Эйлеа® всегда необходимо применять надлежащую технику проведения асептических инъекций. Кроме того, необходимо наблюдать за состоянием пациента в течение недели после проведения инъекции для обеспечения своевременного лечения при появлении признаков инфекционного процесса. Пациентов необходимо проинструктировать о том, что они должны без промедления сообщать при подозрении на какие-либо симптомы эндофтальмита или других вышеуказанных явлений.
Объем препарата во флаконе превышает рекомендованную дозу, составляющую 2 мг афлиберцепта (что эквивалентно 0,05 мл). Избыточный объем необходимо удалить до проведения инъекции.
После проведения интравитреальных инъекций, в том числе препарата Эйлеа®, в течение первых 60 мин. наблюдается повышение внутриглазного давления. Пациенты с плохо контролируемой глаукомой нуждаются в особых мерах предосторожности. Эйлеа® не вводят когда внутриглазное давление ≥ 30 мм рт. ст. Во всех случаях необходимо проводить наблюдение за внутриглазным давлением и перфузией диска зрительного нерва и принимать соответствующие меры терапии.
Иммуногенность
Как и для других препаратов белковой природы существует вероятность развития иммуногенности на введение препарата Эйлеа®.
Пациенты должны быть проинструктированы о необходимости сообщать о любых признаках или симптомах интраокулярного воспаления, таких как боль, светобоязнь, или покраснение, что может быть клиническим признаком повышенной чувствительности.
Системные эффекты
После интравитреальных инъекций ингибиторов VEGF отмечались системные побочные эффекты, включая внеглазные кровоизлияния и артериальные тромбоэмболические явления, которые теоретически могут быть обусловлены ингибированием VEGF. Данные о безопасности применения у пациентов с ДМО, ОЦВС, ОВВС, а также миопической ХНВ, имевших в анамнезе инсульт, транзиторные ишемические атаки или инфаркт миокарда в течение 6 месяцев до лечения, ограничены. Следовательно, при лечении таких пациентов следует соблюдать осторожность.
Другие
Как и при лечении другими ингибиторами VEGF для терапии ВМД, ОЦВС, ОВВС, ДМО и миопической ХНВ, следующие предостережения также применимы и к Эйлеа®.
· Безопасность и эффективность терапии с Эйлеа® при введении в оба глаза одновременно систематически не изучалась.
Если лечение проводится одновременно в оба глаза, это может привести к повышенному системному воздействию препарата, что может повысить риск развития системных побочных эффектов.
· Одновременное применение с другими анти-VEGF препаратами, (ингибиторами фактора роста эндотелия сосудов).
· Доступных данных об одновременном применении Эйлеа®
с другими анти-VEGF препаратами (для системного или окулярного применения), нет.
·Факторы риска, связанные с развитием разрыва пигментного эпителия сетчатки после терапии анти-VEGF препаратами для лечения влажной ВМД, включают обширную и/или высокую отслойку пигментного эпителия сетчатки. При начале терапии Эйлеа®
следует проявлять осторожность у пациентов, имеющих факторы риска разрыва пигментного эпителия сетчатки.
· Необходимо воздержаться от проведения лечения пациентам с регматогенной отслойкой сетчатки или с макулярным разрывом 3-4 степени.
· В случае разрыва сетчатки следует воздержаться от введения дозы и не возобновлять его до тех пор, пока разрыв не будет устранен должным образом.
· При нижеуказанных состояниях необходимо прекратить введение дозы и не возобновлять его ранее следующей запланированной инъекции препарата:
— снижение показателя наилучшей корригированной остроты зрения (НКОЗ) ≥30 букв по сравнению с показателем при последней оценке остроты зрения
— субретинальное кровоизлияние с вовлечением центра фовеа или, если размер кровоизлияния составляет ≥50% общей области поражения
· Если проведено или запланировано хирургическое вмешательство на глазах необходимо воздержаться от введения дозы за 28 дней до и после операции.
· Не cледует назначать Эйлеа® во время беременности, за исключением тех случаев, когда потенциальная польза от лечения превышает потенциальный риск для плода.
· Женщинам репродуктивного возраста необходимо использовать эффективную контрацепцию во время лечения препаратом и, по крайней мере, в течение 3 месяцев после последней интравитреальной инъекции Эйлеа® .
· Имеется ограниченный опыт применения препарата у пациентов с ишемической окклюзией центральной вены сетчатки и ее ветвей. Не рекомендуется применять препарат пациентам, имеющим клинические признаки необратимой потери функции зрения ишемического характера.
Популяции с ограниченными данными
Имеется ограниченный опыт применения препарата для лечения ДМО у пациентов с сахарным диабетом 1 типа или у диабетических пациентов с уровнем гликозилированного гемоглобина HbA1c более 12% или с пролиферативной диабетической ретинопатией.
Эйлеа® не изучался у пациентов с активными системными инфекциями или у пациентов с сопутствующими заболеваниями глаз, такими как, отслойка сетчатки или макулярный разрыв. Также не имеется опыта применения препарата у диабетических пациентов с неконтролируемой артериальной гипертензией. Лечащий врач должен принимать во внимание недостаток данной информации при лечении таких пациентов.
Нет опыта применения препарата в лечении миопической ХНВ у лиц не азиатской популяции, пациентов, ранее получавших лечение по поводу миопической ХНВ, а также у пациентов с экстрафовеальной локализацией поражения.
Содержание натрия
Данный лекарственный препарат содержит менее 1 ммоль натрия (23 мг) в разовой дозе, то есть считается препаратом, свободным от натрия.
Исследования на лекарственные взаимодействия не проводились.
Смежное применение фотодинамической терапии (ФДТ) вертепорфином и препарата Эйлеа® не изучалось, поэтому профиль безопасности для данного взаимодействия не установлен.
Применение в педиатрии
Безопасность и эффективность препарата Эйлеа®
у детей и подростков не установлена.
Нет обоснования для применения Эйлеа® в педиатрической популяции по показаниям влажная ВМД, ОЦВС и ОВВС, ДМО, миопическая ХНВ.
Женщины репродуктивного возраста
Женщины репродуктивного возраста должны использовать эффективные средства контрацепции в период лечения и по крайней мере в течение 3 месяцев после последней интравитреальной инъекции афлиберцепта.
Данные об использовании афлиберцепта у беременных женщин отсутствуют.
Хотя системное воздействие после окулярного введения является очень низким, не cледует назначать Эйлеа®
во время беременности, за исключением тех случаев, когда потенциальная польза от лечения превышает потенциальный риск для плода.
Неизвестно, проникает ли афлиберцепт в грудное молоко. Нельзя исключить существование риска для ребенка находящегося на грудном вскармливании.
Не рекомендуется принимать Эйлеа®
в период кормления грудью. Необходимо принять решение о прекращении кормления грудью или воздержании от приема препарата с учетом пользы от кормления для ребенка и пользы от терапии для женщины.
После инъекций Эйлеа® отмечается незначительное влияние на способность управлять транспортным средством и потенциально опасными механизмами вследствие возможных временных нарушений зрения, связанных с инъекцией или обследованием глаза.
Пациентам не следует управлять автомобилем или сложными механизмами до тех пор, пока зрительная функция не будет в достаточной степени восстановлена.
Эйлеа®
предназначен только для интравитреального введения.
Препарат должен вводиться только квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций.
Каждый флакон содержит 0.278 мл раствора для интравитреального введения, что предоставляет извлекаемый объем 0.1 мл.
Разовая доза препарата во флаконе составляет 2 мг афлиберцепта, что эквивалентно 50 мкл (0.05 мл) раствора для инъекций.
Один флакон содержит извлекаемый объем, по меньшей мере, 0,1 мл, эквивалентный, по меньшей мере, 4 мг афлиберцепта. Это обеспечивает применимое для использования количество для доставки однократной дозы 0,05 мл, содержащей 2 мг афлиберцепта.
Режим дозирования
Влажная возрастная макулярная дегенерация
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 0.05 мл раствора для инъекций.
Лечение Эйлеа® начинают с трех последовательных инъекций 1 раз в месяц. Затем интервал в лечении продлевают до двух месяцев.
По решению врача, основанного на зрительных и анатомических результатах интервал между инъекциями можно поддерживать в течение двух месяцев или в дальнейшем продлевать в режиме treat-and-extend (лечить-и-увеличивать) с увеличением интервалов между инъекциями до 2 или 4 недель для поддержания стабильных зрительных и/или анатомических результатов. В случае ухудшения зрительных и анатомических результатов интервал в лечении следует соответственно сократить.
Нет необходимости проводить мониторинг между инъекциями. Исходя из решения врача, график мониторинга может быть чаще, чем график инъекций.
Интервалы в лечении, превышающие четыре месяца или меньше 4 недель между инъекциями, не изучались.
Макулярный отек вследствие окклюзии вен сетчатки (центральной вены сетча тки или ее ветвей )
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 0.05 мл раствора для инъекций.
После начальной инъекции препарата лечение проводят каждый месяц. Интервал между двумя инъекциями не должен быть короче одного месяца.
Если зрительные и анатомические результаты не указывают на пользу проводимой терапии, инъекции Эйлеа® следует прекратить.
Ежемесячное введение продолжают до достижения максимальной остроты зрения и/или отсутствия признаков активности заболевания. Возможна необходимость в выполнении 3-х или более последовательных ежемесячных инъекций.
Лечение затем можно продолжить в режиме treat-and-extend (лечить-и- увеличивать) с постепенным увеличением интервалов между инъекциями для поддержания стабильных зрительных и/или анатомических результатов, однако имеется недостаточно данных, чтобы сделать заключение о длительности этих интервалов. Если отмечается ухудшение зрительных и/или анатомических результатов необходимо сократить интервал в лечении, соответственно.
График мониторинга и лечения должен определяться лечащим врачом на основании индивидуальной реакции пациента.
Мониторинг активности заболевания включает в себя проведение клинического обследования, функциональных тестов или методов визуализации (например, оптической когерентной томографии или флуоресцентной ангиографии).
Диабетический макулярный отек
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 0.05 мл раствора для инъекций.
Лечение Эйлеа®
начинают с пяти последовательных инъекций 1 раз в месяц с дальнейшим интервалом лечения 1 инъекция в 2 месяца. Нет необходимости в проведении мониторинга между инъекциями.
После первых 12 месяцев лечения Эйлеа® и по решению врача, основанного на зрительных и/или анатомических результатах интервал между инъекциями может быть продлен, например, в режиме treat-and-extend (лечить-и-увеличивать) со стандартным увеличением интервалов в 2 недели между инъекциями для поддержания стабильных зрительных и/или анатомических результатов. Имеются ограниченные данные для интервалов лечения более 4 месяцев. В случае ухудшения зрительных и/или анатомических результатов, интервал в лечении следует соответственно сократить.
Следовательно, график мониторинга должен устанавливаться лечащим врачом и может быть чаще, чем график инъекций.
Если зрительные и анатомические результаты не указывают на пользу проводимой непрерывной терапии, инъекции Эйлеа® следует прекратить.
Интервалы лечения менее 4 недель между инъекциями, не изучались.
Миопическая хориоидальная неоваскуляризация
Рекомендованная доза Эйлеа® составляет 2 мг афлиберцепта, что эквивалентно 0.05 мл раствора в виде однократной интравитреальной инъекции.
Дополнительные дозы могут вводиться, если зрительные и/или анатомические результаты свидетельствуют о сохранении признаков заболевания. При развитии рецидива необходимо лечение как в случае новой манифестации заболевания.
График обследований должен устанавливаться лечащим врачом.
Интервал между двумя инъекциями не должен быть короче одного месяца.
Дополнительная информация для особых категорий пациентов Пациенты с нарушениями функции печени и/или почек
Не проводилось каких-либо специальных исследований Эйлеа® у больных с нарушениями функции печени и почек. Доступные данные не предполагают коррекции дозы у таких пациентов.
Пациенты пожилого возраста
Специальных предостережений не существуют. Имеется ограниченный опыт применения у больных старше 75 лет с диабетическим макулярным отеком.
Дети и подростки
Безопасность и эффективность препарата Эйлеа®
у детей и подростков не установлена.
Нет обоснования для применения Эйлеа® в педиатрической популяции по показаниям влажная ВМД, ОЦВС и ОВВС, ДМО, миопическая ХНВ.
Метод и путь введения
Интравитреальные инъекции должны осуществляться квалифицированным врачом, имеющим опыт проведения интравитреальных инъекций в соответствии с медицинскими стандартами и действующими руководящими положениями. В целом, должна обеспечиваться адекватная анестезия и асептика, включая наружные бактерицидные средства широкого спектра (например, повидон-йод), наносимые на кожу вокруг глаза, веко и поверхность глаза. Рекомендуется применять хирургическую дезинфекцию рук, использовать стерильные перчатки, стерильные салфетки, стерильные векорасширители (или эквивалент).
Иглу для инъекций следует вводить на 3,5–4.0 мм кзади от лимба в полость стекловидного тела, избегая горизонтального меридиана и направляя иглу к центру глазного яблока. Затем следует выполнить инъекцию 0.05 мл раствора; для последующих инъекций следует использовать другие участки склеры.
Сразу после интравитреальной инъекции должно быть начато наблюдение за пациентами на предмет возможного повышения внутриглазного давления. Надлежащий мониторинг может состоять из проверки перфузии диска зрительного нерва или тонометрии. При необходимости стерильное оборудование для проведения парацентеза должно быть доступно.
После интравитреальной инъекции пациентов необходимо проинструктировать о том, что они должны без промедления сообщать о каких-либо симптомах, которые могут свидетельствовать о развитии эндофтальмита (например, глазная боль, покраснение глаза, светобоязнь, размытое зрение).
Каждый флакон должен применяться только для лечения одного глаза.
Извлечение нескольких доз из флакона может увеличить риск заражения и последующей инфекции.
Флакон содержит дозу афлиберцепта, превышающую рекомендованную дозу 2 мг. Извлекаемый объем флакона (100 мкл) не используется полностью. Избыточный объем должен быть удален до инъекции.
Введение полного объема флакона может привести к передозировке. Для удаления пузырьков воздуха и избыточного объема лекарственного препарата следует медленно нажать на поршень шприца и передвинуть цилиндрическое основание купола поршня до черной метки на шприце (эквивалентной 50 мкл, т.е. 2 мг афлиберцепта).
После инъекции любой неиспользованный препарат должен быть утилизирован.
Флакон предназначен исключительно для однократного использования, т.е. для введения одной инъекции в один глаз.
Флакон содержит больше рекомендованной дозы 2 мг афлиберцепта (что эквивалентно 0,05 мл). Избыточный объем должен быть удален до инъекции.
Перед инъекцией выполняется визуальная проверка раствора на наличие инородных механических включений и/или на предмет изменения его окраски или любых изменений внешнего вида. В любом из рассмотренных выше случаев лекарственный препарат забраковывается.
Фильтровальная игла:
BD Blunt Filter (Fill) игла не предназначена для кожных инъекций. Нельзя стерилизовать в автоклаве.
Фильтровальная игла является апирогенной. Нельзя использовать иглу при повреждении индивидуальной упаковки.
Использованную фильтровальную иглу BD Blunt Filter (Fill) необходимо утилизировать в специальном контейнере для острых медицинских предметов.
Внимание: Повторное использование фильтровальной иглы может привести к развитию инфекции или другой патологии /повреждению.
Для выполнения интравитреальной инъекции используется игла для инъекций размером 30 G x ½ дюйма.
В клинических исследованиях использовались дозы до 4 мг с интервалом в 1 месяц и отдельные случаи передозировки в дозе 8 мг.
Передозировка с повышенным объемом введения может привести к повышению внутриглазного давления.
Следовательно, в случаях передозировки необходимо проводить наблюдение за внутриглазным давлением и при необходимости лечащий врач должен назначить адекватное лечение.
Меры, необходимые при пропуске одной или нескольких доз лекарственного препарата
В случае пропуска инъекции Эйлеа®
необходимо записаться к врачу для обследования и инъекции.
Указание на наличие риска симптомов отмены
Необходимо проконсультироваться с врачом, прежде чем прекратить лечение.
Рекомендации по обращению за консультацией к медицинскому работнику для разъяснения способа применения лекарственного препарата
При возникновении какие-либо дополнительных вопросов по использованию этого лекарства, необходимо обратиться к врачу.
В общей сложности 3 102 пациента, принимавших участие в восьми исследованиях III фазы, составили популяцию по оценке безопасности. Из них 2 501 пациент получал рекомендованную дозу 2 мг.
Серьезные глазные побочные реакции в исследуемом глазу, связанные с процедурой инъекции наблюдались менее чем в одной из 1900 интравитреальных инъекций, и включали слепоту, эндофтальмит, отслойку сетчатки, травматическую катаракту, кровоизлияния в стекловидное тело, катаракту, отслойку стекловидного тела, и повышение внутриглазного давления.
Наиболее частыми побочными реакциями (как минимум у 5% пациентов, получивших терапию Эйлеа®) были кровоизлияние под конъюнктиву (25 %), кровоизлияние в сетчатку (11 %), снижение остроты зрения (11 %), боль в глазу (10 %), катаракта (8 %), повышение внутриглазного давления (8 %), отслойка стекловидного тела (7 %), плавающие помутнения стекловидного тела (7 %).
Перечисленные ниже данные по безопасности препарата включают в себя все побочные реакции, основанные на отчетах полученных из 8 исследований фазы III по показаниям влажная ВМД, ОЦВС, ОВВС, ДМО и миопическая ХНВ и данных постмаркетинговых наблюдений, с допустимой возможностью их взаимосвязи с процедурой инъекции или с самим препаратом.
В рамках каждой группы побочные реакции представлены в порядке убывания серьезности.
Все побочные реакции, возникшие во время лечения и зарегистрированные у участников исследований III фазы (объединенные данные исследований III фазы при лечении по показаниям ВМД, ОЦВС, ОВВС, ДМО и миопическая ХНВ) или в рамках пострегистрационного наблюдения.
Очень часто
— снижение остроты зрения, кровоизлияние в сетчатку, кровоизлияние под конъюнктиву, боль в глазу
Часто
— разрыв пигментного эпителия сетчатки⃰, отслойка пигментного эпителия сетчатки, дегенерация сетчатки, кровоизлияние в стекловидное тело, катаракта, кортикальнгая катаракта, ядерная катаракта, субкапсулярная катаракта, эрозия роговицы, повреждение роговицы, повышение внутриглазного давления, нечеткость зрения, плавающие помутнения стекловидного тела, отслойка стекловидного тела, боль в месте введения, ощущение инородного тела в глазах, повышенное слезоотделение, отек века, кровоизлияние в месте введения, точечный кератит, гиперемия конъюнктивы, окулярная гиперемия
Нечасто
— реакции гиперчувствительности***
— эндофтальмит**, отслойка сетчатки, разрыв сетчатки, ирит, увеит, иридоциклит, помутнение хрусталика, отек роговицы, повреждение эпителия роговицы, раздражение в месте введения, ощущение дискомфорта в глазу, раздражение век, воспаление передней камеры глаза.
Редко
— слепота, травматическая катаракта, воспаление стекловидного тела, гипопион
*Состояния, о которых известно, что они связаны с влажной ВМД. Наблюдались только в исследованиях влажной ВМД.
**Инфекционный и неинфекционный эндофтальмит.
***В постмаркетинговый период сообщения о реакциях гиперчувствительности включали в себя сыпь, зуд, крапивницу и изолированные случаи анафилактических/анафилактоидных реакций.
Описание отдельных побочных реакций
При «влажной» форме ВМД отмечено повышение частоты возникновения субконъюнктивальных кровоизлияний у пациентов, получающих антитромботические препараты в исследованиях фазы III. Повышение частоты возникновения данного явления было сопоставимым у пациентов, получающих ранибизумаб и препарат Эйлеа®.
Артериальные тромбоэмболические явления (АТЯ) – это побочные реакции, потенциально связанные с ингибированием системного эндотелиального фактора роста сосудов (VEGF). Существует теоретический риск развития АТЯ, включая инсульт и инфаркт миокарда после интравитреального применения ингибиторов VEGF.
Низкая частота АТЯ наблюдалась в клинических исследованиях Эйлеа®
у пациентов с ВМД, ДМО, ОЦВС и ОВВС, миопической ХНВ. При всех показаниях не отмечалось заметных различий между группами пациентов, получавших Эйлеа® и в соответствующих группах сравнения.
Как и для других препаратов белковой природы существует вероятность развития иммуногенности на введение препарата Эйлеа®.
При возникновении нежелательных лекарственных реакций обращаться к медицинскому работнику, фармацевтическому работнику или напрямую в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов
РГП на ПХВ «Национальный центр экспертизы лекарственных средств и медицинских изделий» Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан http://www.ndda.kz
По 0.278 мл раствора во флакон из бесцветного стекла типа I вместимостью 2 мл, укупоренный пробкой из бутилкаучука, фольгированный фторполимером; обжатый алюминиевым кольцом и полипропиленовым колпачком.
По 1 флакону, 1 фильтровальной игле вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
2 года
Не применять по истечении срока годности.
Хранить при температуре от 2°С до 8°С. Не замораживать.
Хранить в картонной пачке для предотвращения воздействия света. Хранить в недоступном для детей месте!
По рецепту
Сведения о производителе
Байер АГ, Берлин, Германия
Мюллерштрассе 178
тел.: +49 214-30 56150
Держатель регистрационного удостоверения
Байер АГ, Леверкузен, Германия
тел.: 0214/30 51 348
факс: 0214/30 51 603
e-mail: medical-information@bayer.com
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей
ТОО «Байер КАЗ»
ул. Тимирязева, 42, павильон 15, офис 301
050057 Алматы, Республика Казахстан,
тел. +7 727 258 80 40, факс: +7 727 258 80 39,
e-mail: kz.claims@bayer.com
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «Байер КАЗ»
ул. Тимирязева 42, павильон 15, офис 301
050057, Алматы, Республика Казахстан
тел: +7 701 715 78 46 (круглосуточно)
тел:+7 727 258 80 40, вн. 106 (в рабочие часы)
факс: +7 727 2588 039
e-mail: pv.centralasia@bayer.com
Перед применением неоткрытый флакон может храниться при комнатной температуре (25 °C / 77°F) в течение максимум 24 часов. Все манипуляции с открытым флаконом следует проводить в асептических условиях.
1. Снимите пластиковый колпачок и продезинфицируйте наружную часть резиновой пробки флакона
.png)
2. Соедините иглу 18G c 5-микронным фильтром, предлагаемую в картонной упаковке с 1-милиллитровым стерильным шприцем с замком Люэра.
.png)
3. Вводите фильтровальную иглу в центр пробки флакона, пока она не достигнет края дна.
4. В асептических условиях извлеките все содержимое флакона Эйлеа в шприц, удерживая флакон в вертикальном положении, слегка его наклонив для того, чтобы облегчить полное опорожнение. Для предотвращения попадания воздуха необходимо убедиться, что скошенный конец иглы погружен в жидкость. Продолжайте наклонять флакон во время вывода следя за тем, чтобы скошенный конец фильтровальной иглы был погружен в жидкость.
.png)
.png)
5. Удостоверьтесь в том, что шток поршня при опорожнении флакона в достаточной степени поднят, и игла с фильтром пустая.
6. Снимите фильтровальную иглу и утилизируйте ее надлежащим образом.
Примечание:
фильтровальная игла не предназначена для интравитреальных инъекций.
7. В условиях асептики, скручивающим движением наденьте крепко иглу для инъекций 30G x ½ дюйма на переходную канюлю шприца с люэровским замком.
.png)
8. Удерживая шприц с поднятой вверх иглой, проверьте его на наличие пузырьков. Если есть пузырьки, мягко постучите по шприцу пальцем до тех пор, пока все пузырьки не поднимутся вверх.
.png)
9. Устраните все пузырьки и удалите излишки лекарства, медленно нажимая на поршень шприца так, чтобы его плоский край совпал с линией на отметке 0,05 мл на шприце.
.png)
.png)
10. Флакон предназначен исключительно для однократного использования. Извлечение нескольких доз из одного флакона может привести к увеличению риска контаминации и последующей инфекции.
Весь неиспользованный объем лекарственного средства или отходы должны быть утилизированы в соответствии с национальными требованиями.