Элигард (Eligard) инструкция по применению
📜 Инструкция по применению Элигард
💊 Состав препарата Элигард
✅ Применение препарата Элигард
📅 Условия хранения Элигард
⏳ Срок годности Элигард
Описание лекарственного препарата
Элигард
(Eligard)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.04.08
Владелец регистрационного удостоверения:
Производство готовой лекарственной формы/первичная упаковка:
Tolmar, Inc.
(США)
Код ATX:
L02AE02
(Лейпрорелин)
Лекарственные формы
| Элигард |
Лиофилизат д/пригот. раствора для п/к введения 7.5 мг: шприцы 2 шт. в компл. с растворителем, иглой инъекц. и пакетиком с влагопоглотителем рег. №: ЛСР-006156/09 |
|
|
Лиофилизат д/пригот. раствора для п/к введения 22.5 мг: шприцы 2 шт. в компл. с растворителем, иглой инъекц. и пакетиком с влагопоглотителем рег. №: ЛСР-006156/09 |
||
|
Лиофилизат д/пригот. раствора для п/к введения 45 мг: шприцы 2 шт. в компл. с растворителем, иглой инъекц. и пакетиком с влагопоглотителем рег. №: ЛСР-006156/09 |
Форма выпуска, упаковка и состав
препарата Элигард
Лиофилизат для приготовления раствора для п/к введения (шприц Б) от белого до почти белого цвета, без видимых посторонних частиц. Приложенный растворитель (шприц А) — от светло-желтой до светло-желтой с коричневатым оттенком, прозрачная, вязкая жидкость без видимых посторонних частиц; допускается наличие пузырьков воздуха. Восстановленный раствор — вязкая жидкость от светло-желтого до светло-желтого с коричневатым оттенком цвета, без видимых посторонних частиц; допускается наличие пузырьков воздуха.
Растворитель (шприц А): (сополимер поли-D,L-лактид-ко-гликолид: ПЛГХ (50:50) — 117 мг, N-метил-2-пирролидон — 226 мг) — 343 мг.
Шприцы из полипропилена или сополимера циклического олефина [шприц А в комплекте с поршнем для шприца Б и пакетиком с влагопоглотителем, помещенный в контурную ячейковую упаковку из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) и [шприц Б в комплекте с иглой инъекционной и пакетиком с влагопоглотителем, помещенный в упаковку ячейковую контурную из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) — пачки картонные.
Лиофилизат для приготовления раствора для п/к введения (шприц Б) от белого до почти белого цвета, без видимых посторонних частиц. Приложенный растворитель (шприц А) — от бесцветной до светло-желтой, прозрачная, вязкая жидкость без видимых посторонних частиц; допускается наличие пузырьков воздуха. Восстановленный раствор — вязкая жидкость от бесцветной до светло-желтого цвета, без видимых посторонних частиц; допускается наличие пузырьков воздуха.
Растворитель (шприц А): (сополимер поли-D,L-лактид-ко-гликолид: ПЛГ (75:25) — 206 мг, N-метил-2-пирролидон — 251 мг) — 457 мг.
Шприцы из полипропилена или сополимера циклического олефина [шприц А в комплекте с поршнем для шприца Б и пакетиком с влагопоглотителем, помещенный в контурную ячейковую упаковку из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) и [шприц Б в комплекте с иглой инъекционной и пакетиком с влагопоглотителем, помещенный в упаковку ячейковую контурную из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) — пачки картонные.
Лиофилизат для приготовления раствора для п/к введения (шприц Б) от белого до почти белого цвета, без видимых посторонних частиц. Приложенный растворитель (шприц А) — от бесцветной до светло-желтой, прозрачная, вязкая жидкость без видимых посторонних частиц; допускается наличие пузырьков воздуха. Восстановленный раствор — вязкая жидкость от бесцветной до светло-желтого цвета, без видимых посторонних частиц; допускается наличие пузырьков воздуха.
Растворитель (шприц А): (сополимер поли-D,L-лактид-ко-гликолид: ПЛГ (85:15) — 217 мг, N-метил-2-пирролидон — 217 мг) — 434 мг.
Шприцы из полипропилена или сополимера циклического олефина [шприц А в комплекте с поршнем для шприца Б и пакетиком с влагопоглотителем, помещенный в контурную ячейковую упаковку из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) и [шприц Б в комплекте с иглой инъекционной и пакетиком с влагопоглотителем, помещенный в упаковку ячейковую контурную из полиэфира, покрытую алюминиевой фольгой ламинированной] (1) — пачки картонные.
* избыток лейпрорелина ацетата компенсирует потери в шприце и игле. Восстановленный раствор (вводимая доза) содержит 7.5 мг, 22.5 мг или 45 мг лейпрорелина ацетата.
Фармакологическое действие
Лейпрорелин является синтетическим непептидным аналогом естественного гонадотропин-рилизинг гормона (ГнРГ), который при длительном применении ингибирует секрецию гипофизарного гонадотропина и подавляет тестикулярный стероидогенез у мужчин. Аналог обладает большей эффективностью, чем естественный гормон, и его воздействие обратимо при прекращении лечения. Однако время восстановления концентрации тестостерона может варьировать среди пациентов.
Применение лейпрорелина сначала приводит к повышению концентрации циркулирующего ЛГ и ФСГ, в результате чего временно повышается концентрация гонадных стероидов, тестостерона и дигидротестостерона у мужчин. При продолжительном применении лейпрорелина содержание ЛГ и ФСГ снижается. У мужчин содержание тестостерона снижается до кастрационного уровня (≤50 нг/дл) в течение 3-5 недель после начала лечения. Среднее содержание тестостерона через 6 месяцев лечения составляет 6.1 (±0.4) нг/дл для дозировки 7.5 мг; 10.1 (±0.7) нг/дл для дозировки 22.5 мг и 10.4 (±0.53) нг/дл для дозировки 45 мг. Эти значения сопоставимы с содержанием тестостерона после выполнения билатеральной орхиэктомии.
Все пациенты в клиническом исследовании препарата Элигард 7.5 мг достигли кастрационных уровней тестостерона на 6-й неделе лечения; 94% пациентов — к 28 дню и 98% пациентов — к 35 дню. Все пациенты в клиническом исследовании препарата Элигард 22.5 мг достигли кастрационных уровней тестостерона на 5-й неделе; 99% пациентов — к 28 дню. Все пациенты (за исключением одного) в клиническом исследовании препарата Элигард 45 мг достигли кастрационных уровней тестостерона на 4-й неделе. У подавляющего большинства пациентов концентрации тестостерона уменьшались ниже 20 нг/дл, хотя полноценное преимущество данных низких уровней тестостерона пока еще не было установлено.
Концентрации ПСА снизились на 94% через 6 месяцев лечения при применении препарата Элигард 7.5 мг, на 98% — при применении препарата Элигард 22.5 мг, на 97% — при применении препарата Элигард 45 мг.
Длительные исследования показали, что постоянная терапия поддерживает концентрацию тестостерона ниже кастрационного уровня на протяжении до 7 лет и, по всей видимости, на неопределенный срок.
Фармакокинетика
Всасывание
После первой инъекции через 4-8 ч средний уровень концентрации лейпрорелина (Cmax), определяемой в сыворотке крови, повышается до 25.3 нг/дл, 127 нг/дл и 82 нг/дл при применении лейпрорелина в дозе 7.5 мг, 22.5 мг и 45 мг соответственно. После первоначального повышения (фаза плато составляет от 2 до 28 дней для дозировки 7.5 мг; от 3 до 84 дней — для дозировки 22.5 мг, от 3 до 168 дней — для дозировки 45 мг) уровень лейпрорелина в сыворотке оставался относительно стабильным: 0.28-1.67 нг/мл для дозировки 7.5 мг и 0.2-2 нг/мл для дозировок 22.5 и 45 мг. Данные о накоплении вещества при повторных инъекциях отсутствуют.
Распределение
Средний Vd в равновесном состоянии после в/в однократного введения лейпрорелина здоровым добровольцам мужчинам составлял 27 л. По данным исследований in vitro связывание с белками плазмы составляет от 43% до 49%.
Выведение
При введении 1 мг лейпрорелина ацетата в/в здоровым добровольцам мужчинам выяснилось, что при применении двухкамерной модели средний клиренс составил 8.34 л/ч с конечным T1/2 приблизительно 3 ч. Исследований по выведению препарата Элигард не проводилось. Исследований по лекарственному метаболизму препарата Элигард не проводилось.
Показания препарата
Элигард
- гормонозависимый рак предстательной железы.
Режим дозирования
Элигард следует применять только под контролем специалиста здравоохранения, имеющего достаточный опыт для оценки эффективности лечения.
Элигард назначают в виде подкожной инъекции один раз в месяц при дозировке 7.5 мг, 1 раз в 3 месяца при дозировке 22.5 мг и 1 раз в 6 месяцев при дозировке 45 мг. Содержимое двух заранее наполненных стерильных шприцев должно быть смешано непосредственно перед п/к введением препарата Элигард. Введенный раствор образует депо препарата, обеспечивающее постоянное высвобождение лейпрорелина в течение указанного периода.
Как правило, терапия распространенного рака предстательной железы с использованием препарата Элигард предусматривает длительное лечение и не должна прекращаться при наступлении улучшения или ремиссии. Элигард может применяться в качестве неоадъювантной или адъювантной терапии в сочетании с лучевой терапией у пациентов с локализованным раком высокого риска и местно-распространенным раком предстательной железы.
Место инъекции следует периодически менять. Необходимо избегать попадания препарата в артерию или вену.
Ответ на терапию препаратом Элигард необходимо контролировать по клиническим параметрам и измерению концентрации ПСА в сыворотке крови. Результаты клинических исследований показали, что концентрация тестостерона увеличивалась в течение первых 3 дней лечения у большинства пациентов, не подвергавшихся орхиэктомии, а затем снижалась до уровней ниже таковых при медикаментозной кастрации в течение 3-4 недель. После достижения данные показатели остаются неизменными при продолжении терапии лекарственным препаратом (<1.0% случаев прорывного повышения концентраций тестостерона). Если ответ пациента на терапию является недостаточным, необходимо убедиться, что концентрация тестостерона в сыворотке крови достигла или остается на кастрационном уровне. В случае предполагаемой или известной ошибки при смешивании у пациента должна быть определена концентрация тестостерона в связи с тем, что в результате неправильного приготовления, смешивания или введения препарата могут наблюдаться случаи отсутствия клинической эффективности.
У пациентов с метастатическим кастрационно-резистентным раком предстательной железы, не подвергавшихся хирургической кастрации и получающих агонисты ГнРГ, такие как лейпрорелин, лечение агонистами ГнРГ может быть продолжено на фоне применения ингибиторов биосинтеза андрогенов или ингибиторов андрогенных рецепторов.
Коррекция доз для особых популяций пациентов
Клинических данных по применению препарата Элигард у пациентов с печеночной или почечной недостаточностью нет.
В случае предполагаемой или известной ошибки при смешивании у пациента должна быть определена концентрация тестостерона в связи с тем, что в результате неправильного приготовления, смешивания или введения препарата могут наблюдаться случаи отсутствия клинической эффективности.
Рекомендации по приготовлению раствора для введения
Если препарат был приготовлен с нарушением инструкций, его не следует использовать в связи с тем, что при неправильном приготовлении раствора для п/к введения могут наблюдаться случаи отсутствия клинической эффективности.
Сначала рекомендуется подготовить пациента к введению препарата, а затем приступить к приготовлению раствора в соответствии с рекомендациями, представленными ниже.
Упаковку достают из холодильника примерно за 30 мин до использования и выдерживают при комнатной температуре.
После извлечения из холодильника препарат может храниться в оригинальной упаковке при комнатной температуре (не выше 25°С) до 4 недель.
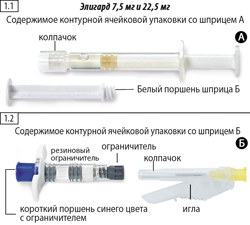
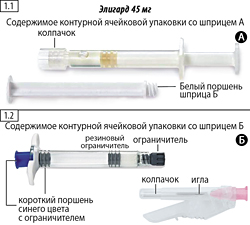
Шаг 1. Извлечь из коробки две контурные ячейковые упаковки и открыть их, потянув за свободный край алюминиевой фольги, извлечь содержимое ячейковых упаковок (рис. 1.1 и 1.2) и положить на чистую поверхность. Следует выбросить пакетики с влагопоглотителем.
Шаг 2. Взять шприц Б и извлечь из него короткий поршень синего цвета вместе с прикрепленным ограничителем серого цвета (не следует выкручивать поршень из ограничителя), следует выбросить их (рис. 2).
Не следует смешивать содержимое шприцев пока синий короткий поршень с прикрепленным ограничителем серого цвета не будет извлечен из шприца Б.
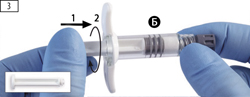
Шаг 3. Взять белый поршень для шприца Б и вставить его в шприц Б со стороны оставшегося серого ограничителя (рис. 3, шаг 1), провернуть поршень по часовой стрелке до ограничителя (рис. 3, шаг 2).
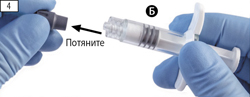
Шаг 4. Снять серый резиновый колпачок со шприца Б и отложить шприц (рис. 4).
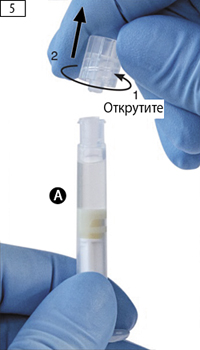
Шаг 5. Взять шприц А и, удерживая его в вертикальном положении, чтобы избежать протечки растворителя, открутить прозрачный колпачок со шприца А (рис. 5).
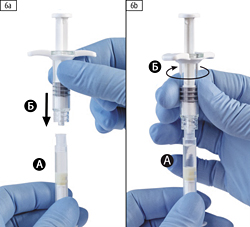
Шаг 6. Соединить два шприца вместе, шприц А снизу, и вкрутить шприц Б в шприц А по часовой стрелке до полной фиксации (рисунки 6а, 6b).
Не следует закручивать шприцы слишком плотно.
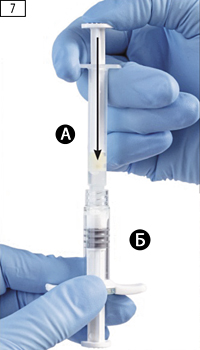
Шаг 7. Перевернуть соединенные шприцы так, чтобы шприц Б оказался снизу, и нажать на поршень шприца А до момента полного ввода содержимого шприца А (растворитель) в шприц Б (содержащий порошок лейпрорелина ацетата), шприцы следует держать вертикально (рис. 7).
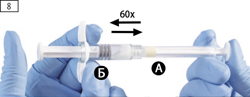
Шаг 8. Держа шприцы в строго горизонтальном положении, тщательно перемешать содержимое обоих шприцев,
поочередно нажимая осторожным движением на поршень то одного, то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного вязкого раствора (рис. 8).
Следует избегать перегиба системы (это может стать причиной протечки, поскольку шприцы могут быть недостаточно плотно закручены).
После тщательного перемешивания получается вязкий раствор от бесцветного до светло-коричневого цвета (могут наблюдаться оттенки белого или светло-желтого цвета).
Важно: необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать готовый продукт запрещено.
Следует помнить о том, что препарат нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
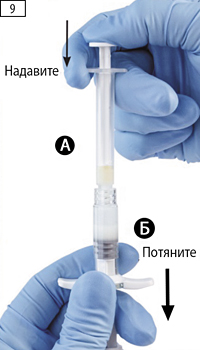
Шаг 9. Держать шприцы вертикально, шприц Б — снизу. Шприцы должны быть надежно закреплены. Нажимая на поршень шприца А, и слегка оттягивая вниз поршень шприца Б, переместить все содержимое в шприц Б (рис. 9).
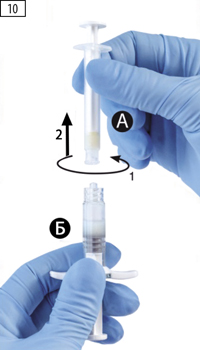
Шаг 10. Открутить шприц А, продолжая нажимать на поршень шприца А (рис. 10). Необходимо убедиться, что содержимое не вытекает из шприца, т.к. не удастся закрепить иглу надлежащим образом в случае утечки.
Внимание: в растворе могут присутствовать один большой или несколько маленьких пузырьков воздуха, это допустимо.
Не следует пытаться удалять пузырьки из шприца Б на этом этапе, поскольку это может привести к потере препарата.
Шаг 11
- Держать шприц Б вертикально и оттянуть поршень белого цвета, чтобы не допустить потери препарата.
- Открыть упаковку со стерильной иглой, сняв бумажный клапан, и извлечь безопасную иглу. Не следует удалять откидное защитное устройство.
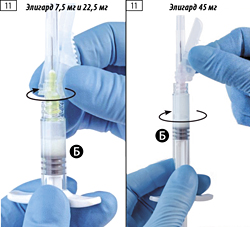
- Прикрепить безопасную иглу к шприцу Б, удерживая шприц и осторожно закручивая иглу по часовой стрелке приблизительно на три четверти оборота до закрепления иглы (рис. 11).
Важно: не перетягивать иглу слишком сильно, так как может треснуть разъем иглы, что приведет к утечке препарата во время инъекции.
В случае если разъем иглы треснул, имеет внешние признаки повреждения или если произошла утечка, препарат не следует использовать. Замена поврежденной иглы на аналогичную недопустима, препарат вводить не следует. Весь препарат следует безопасно утилизировать.
В случае повреждения разъема иглы следует использовать новую дополнительную упаковку препарата.
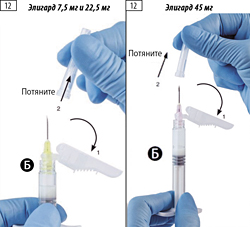
Шаг 12. Переместить защитное устройство в направлении от иглы и перед введением препарата снять защитный колпачок с иглы (рис. 12).
Важно: не следует приводить в действие защитное устройство иглы до введения препарата.
Шаг 13. До начала введения удалить большие пузырьки воздуха из шприца Б. Ввести препарат подкожно, параллельно удерживая защитное устройство на расстоянии от иглы. Необходимо убедиться в том, что введен весь препарат из шприца Б.
Шаг 14. После инъекции необходимо незамедлительно активировать защитное устройство иглы любым из двух способов, описанных ниже.
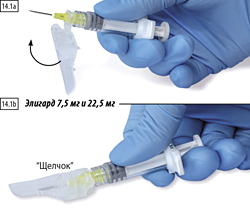
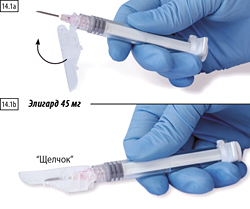
1 способ. Закрытие на плоской поверхности
Положить шприц с иглой на плоскую поверхность вниз рычагом защитного устройства и нажатием на рычаг активировать защитный механизм (рис. 14.1а).
Необходимо убедиться, что рычаг переведен в закрытое положение и кончик иглы полностью закрыт (до характерного щелчка) (рис. 14.1b).
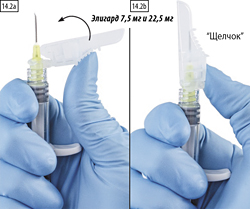
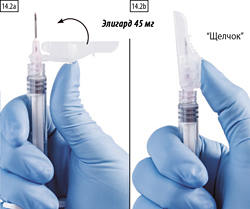
2 способ. Закрытие большим пальцем
Поместить большой палец на защитное устройство (рис. 14.2а), накрыть наконечник иглы и активировать защитный механизм. Необходимо убедиться, что рычаг переведен в закрытое положение и кончик иглы полностью закрыт (до характерного щелчка) (рис. 14.2b).
Шаг 15. После закрытия защитного механизма немедленно поместить иглу и шприц в соответствующий контейнер для острых предметов.
Побочное действие
Нежелательные явления, вызванные приемом препарата Элигард, обусловлены главным образом специфическим фармакологическим действием лейпрорелина, вызывающим увеличение и снижение концентрации гормонов. Самыми распространенными побочными эффектами являлись: «приливы», недомогание, тошнота и слабость, раздражение в месте введения препарата. Слабые или умеренно выраженные «приливы» наблюдались у приблизительно 58% пациентов.
Следующие нежелательные явления были зафиксированы во время проведения клинических исследований препарата Элигард у пациентов с распространенным раком предстательной железы. Частота побочных реакций, приведенных ниже, изложена в соответствии со следующей градацией: очень часто (>1/10), часто (>1/100, <1/10); нечасто (>1/1000, <1/100); редко (>1/10 000, <1/1000); очень редко (<1/10000), неизвестно (невозможно оценить на основании имеющихся данных).
Инфекционные и паразитарные заболевания: часто — назофарингит; нечасто — инфекция мочевыводящих путей, ограниченная инфекция кожных покровов.
Со стороны обмена веществ и питания: нечасто — ухудшение течения сахарного диабета.
Психические нарушения: нечасто — необычные сновидения, депрессия, снижение либидо.
Со стороны нервной системы: нечасто — головокружение, головная боль, гипестезия, бессонница, нарушение вкусовых ощущений, нарушение обоняния, вертиго; редко — непроизвольные патологические движения.
Со стороны сердца: неизвестно — удлинение интервала QT.
Со стороны сосудистой системы: очень часто — «приливы»; нечасто — повышение АД, снижение АД; редко — обморок, коллапс.
Со стороны дыхательной системы, органов грудной клетки и средостения: нечасто — ринорея, диспноэ; неизвестно — интерстициальное заболевание легких.
Со стороны желудочно-кишечного тракта: часто — тошнота, диарея, гастроэнтерит, колит; нечасто — запор, сухость во рту, диспепсия, рвота; редко — метеоризм, отрыжка.
Со стороны кожи и подкожной клетчатки: очень часто — экхимозы, эритема; часто — зуд, ночная потливость; нечасто — холодный пот, повышенное потоотделение; редко — алопеция, кожный зуд.
Со стороны скелетно-мышечной и соединительной ткани: часто — артралгия, боль в конечностях, миалгия, дрожь, слабость; нечасто — боль в спине, мышечные судороги.
Со стороны почек и мочевыводящих путей: часто — нарушение мочеиспускания, затрудненное мочеиспускание, дизурия, никтурия, олигурия; нечасто — спазм мочевого пузыря, гематурия, увеличение частоты мочеиспускания, задержка мочеиспускания.
Со стороны половых органов и молочной железы: часто — болезненность грудных желез, боль в яичках, атрофия яичек, гипертрофия грудных желез, бесплодие, эректильная дисфункция, уменьшение размеров полового члена; нечасто — гинекомастия, импотенция, тестикулярные нарушения; редко — боль в грудной железе.
Общие расстройства и нарушения в месте введения: очень часто — повышенная утомляемость, жжение в месте введения, парестезия в месте введения; часто — недомогание, боль в месте введения, кровоподтек, жжение (ощущение покалывания в месте инъекции); нечасто — зуд в месте введения, уплотнение в месте введения, заторможенность, болевые ощущения, пирексия; редко — образование язвы в месте введения; очень редко — некроз в месте введения.
Со стороны крови и лимфатической системы: часто — гематологические изменения, анемия.
Со стороны показателей лабораторных и инструментальных исследований: часто — повышение активности КФК, увеличение времени коагуляции; нечасто — повышение активности АЛТ, гипертриглицеридемия, увеличение протромбинового времени, увеличение массы тела.
К другим нежелательным явлениям при приеме лейпрорелина ацетата относятся: периферические отеки, эмболия легочной артерии, ощущение сердцебиения, миалгия, мышечная слабость, нарушение кожной чувствительности, озноб, головокружение, кожная сыпь, амнезия и нарушение зрения. При продолжительном применении препаратов данного класса отмечали атрофию мышц. Редко поступали сообщения о случаях возникновения инфаркта, вызванного гипофизарной апоплексией после приема антагонистов ГнРГ краткосрочного и длительного действия. Также были зафиксированы случаи возникновения тромбоцитопении и лейкопении, изменения толерантности к глюкозе.
После введения аналога агониста ГнРГ редко были описаны случаи возникновения судорог.
После введения агониста ГнРГ редко были описаны случаи развития анафилактических/анафилактоидных реакций.
Местные реакции после введения препарата Элигард такие же, как и при п/к введении других препаратов. В целом, местные реакции после введения препарата носят умеренный характер и являются краткосрочными.
Изменение плотности костной ткани
В публикациях отмечалось уменьшение плотности костей у мужчин после орхиэктомии или терапии аналогами ГнРГ. Можно предположить, что долгосрочная терапия лейпрорелином приводит к усилению симптомов остеопороза, что повышает риск переломов.
Усиление симптомов и признаков заболевания
Терапия лейпрорелина ацетатом может привести к усилению симптомов заболевания в течение первых недель лечения. В случае заболеваний с метастазами в позвоночник и/или обструкцией мочевых путей или гематурией возможно возникновение таких неврологических осложнений, как слабость и/или парестезия нижних конечностей или ухудшение симптомов нарушения мочеиспускания.
Противопоказания к применению
- повышенная чувствительность к лейпрорелину, другим агонистам ГнРГ или к любому вспомогательному веществу, входящему в состав лекарственной формы;
- хирургическая кастрация;
- в качестве единственного лечения у пациентов с раком предстательной железы со сдавлением спинного мозга или наличием метастазов в позвоночник.
Противопоказан женщинам и детям.
Применение при беременности и кормлении грудью
Препарат противопоказан женщинам.
Применение при нарушениях функции печени
Клинических данных по применению Элигарда у больных с печеночной недостаточностью нет.
Применение при нарушениях функции почек
Клинических данных по применению Элигарда у больных с почечной недостаточностью нет.
Применение у детей
Препарат противопоказан детям.
Особые указания
При неправильном приготовлении раствора для п/к введения могут наблюдаться случаи отсутствия клинической эффективности.
Элигард должен применяться под наблюдением врача, имеющего опыт проведения противоопухолевой терапии.
Ответ на терапию препаратом Элигард необходимо контролировать по клиническим параметрам и измерению концентрации ПСА в сыворотке крови. Результаты клинических исследований показали, что концентрация тестостерона увеличивается в первые 3 дня лечения у большинства пациентов без орхиэктомии, а затем снижается до уровня медикаментозной кастрации в течение 3-4 недель. Впоследствии данные показатели остаются неизменными при продолжении терапии лекарственным препаратом. В случае, если ответ пациента на терапию является недостаточным, необходимо убедиться, что концентрация тестостерона в сыворотке крови достигла или остается на кастрационном уровне.
Андрогенная депривационная терапия может удлинять интервал QT. Перед назначением препарата Элигард следует оценивать соотношение пользы и риска (включая возникновение желудочковой тахикардии типа «пируэт») у пациентов с указаниями в анамнезе или факторами риска удлинения интервала QT, принимающих препараты, которые могут удлинять интервал QT.
Заболевания сердечно-сосудистой системы
Сообщалось о повышенном риске развития инфаркта миокарда, внезапной сердечной смерти и инсульта при приеме мужчинами препаратов-агонистов ГнРГ. Такой риск не подкреплен достаточным количеством результатов в пределах обобщенного соотношения показателей, поэтому его следует внимательно оценивать вместе с риском развития сердечно-сосудистых заболеваний при принятии решения о выборе метода лечения для пациентов, страдающих раком простаты. Пациенты, принимающие препараты-агонисты ГнРГ, должны проходить обследование на предмет появления симптомов и признаков, свидетельствующих о развитии сердечно-сосудистых заболеваний, а также проходить лечение, основанное на современных принципах клинической практики.
Временное повышение содержания тестостерона
Элигард, как и другие препараты-агонисты ГнРГ, в течение первой недели лечения вызывает кратковременное повышение концентрации тестостерона, дигидротестостерона и кислой фосфатазы в сыворотке крови, в связи с чем у пациентов могут усилиться симптомы или возникнуть новые, такие как боль в костях, неврологические расстройства, гематурия, обструкция мочеточника или инфравезикальная обструкция. Эти симптомы обычно проходят при продолжении терапии.
Дополнительное применение соответствующего антиандрогена за 3 дня до начала терапии препаратом Элигард и продолжение его приема в течение первых 2 или 3 недель лечения предупреждает последствия первоначального повышения концентрации тестостерона.
После выполнения кастрации хирургическим путем применение препарата Элигард не приводит к дальнейшему снижению тестостерона в сыворотке крови.
Изменения плотности костей
В публикациях отмечалось уменьшение плотности костей у мужчин после орхиэктомии или терапии агонистом ГнРГ.
Антиандрогенная терапия значительно повышает риск переломов костей в результате возникновения остеопороза. Информация по данному вопросу в настоящее время ограничена. Переломы, связанные с развитием остеопороза, отмечались у 5% пациентов, получавших антиандрогенную терапию на протяжении 22 месяцев, а также у 4% больных при продолжительности лечения от 5 до 10 лет. В целом, риск переломов костей в результате возникновения остеопороза выше такового для патологических переломов. Помимо продолжительного дефицита тестостерона на развитие остеопороза может влиять преклонный возраст, курение, потребление алкоголя, лишний вес и недостаточные физические нагрузки.
Гипофизарная апоплексия
В течение пострегистрационного периода применения препарата, поступали сообщения о случаях возникновения гипофизарной апоплексии (редко) (клинический синдром, возникающий после инфаркта гипофиза), у большинства пациентов симптомы проявлялись после приема препаратов-агонистов ГнРГ через 2 недели после приема первой дозы, у некоторых — в течение первого часа. В данном случае, гипофизарная апоплексия проявляется в виде таких симптомов как головная боль, рвота, нарушение зрения, офтальмоплегия, изменение психического состояния и сердечно-сосудистой недостаточности, и требует немедленного оказания медицинской помощи.
Гипергликемия и сахарный диабет
Гипергликемия и повышенный риск развития сахарного диабета отмечались у мужчин, принимавших препараты-агонисты ГнРГ. Гипергликемия может свидетельствовать о развитии сахарного диабета или ухудшении гликемического контроля у пациентов с сахарным диабетом. Следует периодически производить мониторинг концентрации глюкозы в крови и/или гликированного гемоглобина (HbA1c) у пациентов, принимающих препараты-агонисты ГнРГ, а также осуществлять подбор необходимых современных методов лечения гипергликемии или сахарного диабета.
Судороги
В течение пострегистрационного периода поступали сообщения о возникновении судорог у пациентов, получавших лечение лейпрорелина ацетатом при наличии или в отсутствие в анамнезе предрасполагающих факторов. При судорогах следует проводить лечение, основанное на современных клинических рекомендациях.
Другие явления
При применении агонистов ГнРГ сообщалось также о случаях возникновения обструкции мочевыводящих путей и компрессии спинного мозга, что может привести к параличу как с развитием фатальных осложнений, так и без них. В случае компрессии спинного мозга или развитии нарушения функции почек следует прибегнуть к стандартной терапии этих осложнений.
За пациентами с метастазами в позвоночник и/или головной мозг, а также за пациентами с обструкцией мочевыводящих путей следует вести тщательное наблюдение в течение нескольких первых недель лечения.
Влияние на способность к управлению транспортными средствами и механизмами
Некоторые побочные реакции препарата, такие как повышенная усталость, головокружение, нарушения зрения, могут отрицательно влиять на способность к управлению автомобилем и выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Передозировка
Данных относительно передозировки не имеется. В случае передозировки больному следует проводить симптоматическое лечение.
Лекарственное взаимодействие
Исследований по изучению фармакокинетического взаимодействия препарата Элигард с другими препаратами не проводилось. О взаимодействии препарата Элигард с другими лекарственными препаратами не сообщалось.
В связи с тем, что андрогенная депривация может удлинять интервал QT, следует тщательно взвесить одновременное применение препарата Элигард с другими препаратами, удлиняющими интервал QT, или препаратами, способными вызывать желудочковую тахикардию типа «пируэт», такими как антиаритмические препараты класса IА (например, хинидин, дизопирамид) или класса III (например, амиодарон, соталол, дофетилид, ибутилид), метадон, моксифлоксацин, нейролептики и т.д.
Условия хранения препарата Элигард
Препарат следует хранить в оригинальной упаковке в недоступном для детей месте при температуре от 2° до 8°С.
Срок годности препарата Элигард
Срок годности — 2 года. Не использовать препарат по истечении срока годности.
Готовый раствор стабилен химически и физически в течение 30 минут при температуре 25°С.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
РУСФИК ООО, ГРУППА КОМПАНИЙ RECORDATI
(Россия)

|
|
РУСФИК ООО, 123610 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Состав
1 доза содержит лейпрорелина ацетата 7,5, 22,5 или 45 мг.
Форма выпуска
Лиофилизат в шприце (Б) и растворитель в другом шприце (А).
Фармакологическое действие
Противоопухолевое.
Фармакодинамика и фармакокинетика
Фармакодинамика
Лейпрорелин — аналог ГнРГ (гонадотропин-рилизинг гормона), вырабатываемого в организме. Подавляет секрецию гонадотропина гипофизом. Синтетический аналог более эффективен, чем естественный гормон.
Лейпрорелин сначала вызывает повышение уровня ЛГ и ФСГ и временное повышение гонадных стероидов, дигидротестостерона и тестостерона. При длительном применении (3-5недель) снижается уровень ЛГ и ФСГ и, соответственно, тестостерона до кастрационного уровня. При применении этого препарата в 95% случаев достигается этот уровень, по сравнению с аналогами.
Фармакокинетика
Средний уровень концентрации через 5-8 ч после инъекции — 25,3, 127 и 82 нг/дл при использовании в дозах 7,5, 22,5 и 45 мг. Первоначальное повышение концентрации лейпрорелина сменяется стабильной концентрацией 0.2-2 нг/мл. Накопление вещества при последующих инъекциях не зарегистрировано. Связывается с белками плазмы на 45-49%.
Показания к применению
Рак предстательной железы (гормонозависимый).
Противопоказания
- при хирургической кастрации;
- повышенная чувствительность;
- применение у женщин и детей.
Побочные действия
- колебания АД, приливы жара, обморок, отеки, одышка, сердцебиение;
- головокружение, бессонница, расстройства вкуса и обоняния, депрессия, амнезия, расстройство зрения;
- тошнота, диарея или запор, отрыжка, сухость во рту, вздутие кишечника;
- насморк, затрудненное дыхание;
- дизурические расстройства, затрудненное мочеиспускание и задержка мочи, боль в яичках и мочевом пузыре, снижение либидо;
- гинекомастия;
- боль в спине и суставах, мышечные боли и судороги, мышечная слабость;
- снижение плотности кости;
- снижение эритроцитов, гемоглобина;
- зуд, жжение и покалывание в месте инъекции, уплотнение тканей.
Элигард, инструкция по применению (Способ и дозировка)
Препарат применяется в виде подкожных инъекций в клетчатку брюшной стенки, которые выполняются 1 раз в месяц (Элигард 7,5 мг), раз в полгода (Элигард 45 мг) и раз в 3 месяца (Элигард 22,5 мг). Из созданных депо препарат постоянно высвобождается. Лечение проводится длительно. Рекомендуется менять место инъекции и не допускать попадания в кровеносные сосуды. Если на фоне снижения тестостерона повышается простатспецифический антиген (ПСА), лечение Элигардом прекращают.
Как приготовить раствор для инъекций.
Содержимое шприца А и шприца Б смешивают непосредственно перед введением, соединяя шприцы. Раствор смешивается попеременным нажатием на поршень шприца А и Б. Готовая смесь имеет светло-желтый цвет, ее вводят в шприц Б и вставляют стерильную иглу.
Передозировка
Случаев передозировки не зарегистрировано. В случае передозировки проводится симптоматическое лечение.
Взаимодействие
Исследований по фармакокинетическому взаимодействию препарата с другими ЛС не проводилось.
Условия продажи
По рецепту.
Условия хранения
Температура 2-6°C.
Срок годности
2 года.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Люкрин депо, Простап.
Отзывы об Элигарде
По отзывам этот препарат на первой неделе лечения вызывал усиление симптомов заболевания, а также появление болей в костях, неврологических расстройств и появление крови в моче. Эти симптомы объясняются вспышкой секреции гонадотропных гормонов, которая при дальнейшем лечении сменяется их подавлением. При длительном приеме больные отмечали слабовыраженные и средне выраженные приливы, жжение месте инъекции, тошноту и гинекомастию.
Уникальность препарата заключается в использовании системы Атригель — это биодеградирующий полимер, используемый в виде растворителя и позволяющий создать депо препарата в подкожной клетчатке на 1-3-6 месяцев и стабильный эффект. Эта система обеспечивает эффективное снижение тестостерона у 95% пациентов, а применение 6-месячного депо очень удобно: уменьшается частота местных реакций, не требуется частых посещений врача.
Цена, где купить
Купить препарат по рецепту врача можно во многих аптеках Москвы, Санкт — Петербурга и других городов России.
Цена на Элигард зависит от дозы. Элигард 7,5 мг можно приобрести за 9095 руб. Препарат в дозе 22,5 мг стоит 22731 руб., а стоимость лиофилизата в дозе 45 мг колеблется от 32931 до 34804 руб.
Введение препарата Элигард должно осуществляться под руководством медицинского работника, имеющего соответствующий опыт для оценки эффекта лечения.
Элигард назначают в виде подкожной инъекции один раз в месяц при дозировке 7,5 мг, один раз в три месяца при дозировке 22,5 мг и один раз в шесть месяцев при дозировке 45 мг. Введенный раствор образует депо препарата, обеспечивающее постоянное высвобождение лейпрорелина в течение указанного периода.
Как правило, терапия распространённого рака предстательной железы с использованием Элигарда предусматривает длительное лечение и не должна прекращаться при наступлении улучшения или ремиссии.
Препарат Элигард можно использовать в качестве неоадъювантной или адъювантной терапии в сочетании с лучевой терапией у пациентов с локализованным раком высокого риска и местно-распространённым раком простаты.
Реакцию на лечение препаратом следует контролировать путем наблюдения за клиническими проявлениями болезни и измерения уровня простатспецифического антигена (ПСА) в сыворотке крови. В клинических исследованиях показано, что в большинстве случаев у пациентов без орхидэктомии уровень тестостерона повышается в течение первых трех дней лечения и затем снижается в течение 3-4 недель ниже уровней медицинской кастрации. Кастрационный уровень тестостерона поддерживается при длительном применении лекарственного средства (достигается уровня тестостерона <1%). Если ответ пациента на лечение недостаточный, желательно проверить, достиг ли уровень тестостерона кастрационного уровня или продолжает находиться на нем.
Отсутствие клинической эффективности может наблюдаться при неправильном приготовлении, восстановлении и введении препарата; в случае предполагаемой или известной ошибки необходимо оценить уровни тестостерона.
У пациентов с метастатическим кастрационно-резистентным раком предстательной железы, не подвергавшихся хирургической кастрации и получающих агонисты ГнРГ, такие как лейпрорелин, лечение агонистами ГнРГ может быть продолжено на фоне применения ингибиторов биосинтеза андрогенов или ингибиторов андрогенных рецепторов.
Педиатрическая популяция
Безопасность и эффективность у детей в возрасте до 18 лет не установлена.
Коррекция доз для особых популяций пациентов
Клинических данных по применению Элигарда у больных с печёночной или почечной недостаточностью нет.
Рекомендации по приготовлению раствора для введения
Важно: При неправильном приготовлении раствора для подкожного введения могут наблюдаться случаи отсутствия клинической эффективности. Перед использованием продукт достают из холодильника и в течение 30 минут выдерживают при комнатной температуре. Сперва подготовьте пациента к введению препарата, а затем приступите к приготовлению раствора в соответствии с ниже представленными рекомендациями.
Важно:
Следующие шаги касаются только дозировок 7,5 мг и 22,5 мг! Шаги для дозировки 45 мг представлены ниже в отдельном разделе.
Шаг 1. Откройте внешнюю упаковку (оторвите фольгу от уголка, место отрыва обозначено) и извлеките содержимое упаковки А (рисунок 1.1) и упаковки Б (рисунок 1.2), положите на стерильную поверхность. Выбросьте пакетики с влагопоглотителем.
Шаг 2. Выньте из шприца Б (не выкручивать) короткий поршень синего цвета со вторым ограничителем серого цвета (рисунок 2).
Не смешивайте продукт с двумя ограничителями внутри шприца.
Шаг 3. Аккуратно выньте белый поршень из упаковки со шприцем А и вставьте его в ограничитель серого цвета шприца Б (рисунок 3).
Шаг 4. Снимите серый резиновый колпачок со шприца Б и отложите шприц (рисунок 4).
Шаг 5. Держите шприц А вертикально, чтобы избежать протечки, а затем открутите прозрачный колпачок со шприца А (рисунок 5).
Шаг 6. Соедините два шприца вместе, надавливая и вкручивая шприц Б в шприц А до полной фиксации (рисунки 6а, 6b). Не закручивайте шприцы слишком плотно.
Шаг 7. Переверните соединённые шприцы и держите шприцы вертикально (шприц Б снизу) до момента полного ввода содержимого лейпрорелина ацетата из шприца А в шприц Б (рисунок 7).
Шаг 8. Тщательно перемешайте содержимое обоих шприцев, держа их в горизонтальном положении и поочередно осторожным движением нажимая на поршень то одного то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного раствора (рисунок 8). Не наклонять шприцы (следует обратить внимание, что это может привести к вытеканию жидкости, поскольку шприцы могут частично открутиться).
После тщательного смешивания вязкий раствор приобретёт цвет от светло-жёлтого до светло-жёлтого с коричневым оттенком (для дозировки7,5 мг) или от бесцветной до светло-жёлтого цвета (для дозировки 22,5 мг).
Важно: Необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать готовый продукт запрещено.
Помните: Продукт нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
Шаг 9. Держите шприцы вертикально, шприц Б — снизу. Шприцы должны быть четко закреплены. Нажимая на поршень шприца А, и слегка подтягивая поршень шприца Б, переместите все содержимое в шприц Б (рисунок 9).
Шаг 10. Открутите шприц А, продолжая нажимать на поршень шприца (рисунок 10). Убедитесь, что содержимое не вытекает из шприца, поскольку в данном случае вы не сможете закрепить иглу надлежащим образом.
Помните: наличие маленьких пузырьков воздуха допустимо. Пожалуйста, не пытайтесь удалять пузырьки из шприца Б на этом этапе, поскольку это может привести к потере продукта.
Шаг 11.
•Держите шприц Б вертикально и удерживайте белый поршень во избежание потери препарата
•Откройте упаковку со стерильной иглой (отогнув бумажную этикетку) и извлеките иглу. •Присоедините безопасную иглу к шприцу Б, удерживая шприц и аккуратно поворачивая иглу по часовой стрелке приблизительно на три четверти оборота до полной фиксации (рис. 11).
Не перекручивайте иглу, поскольку это может привести к образованию трещин на переходнике иглы и последующей утечке препарата во время инъекции.
Если переходник иглы сломан, имеет видимые повреждения или протекает, препарат использовать не следует.
Замена повреждённой иглы, а также инъекционное введение препарата недопустимы. Весь препарат необходимо утилизировать с соблюдением мер безопасности.
В случае повреждения переходника иглы необходимо использовать новый препарат.
Шаг 12. Перед инъекцией снимите защитный колпачок с иглы (рисунок 12).
Важно: не используйте иглу до установки на шприц.
Шаг 13. До начала введения удалите большие пузырьки воздуха из шприца Б. Вводите препарат подкожно. Пожалуйста, убедитесь в том, что введен весь препарат из шприца Б.
Шаг 14. После инъекции, закройте защитную крышку в соответствии с рекомендациями, представленными ниже.
1. Закрытие на плоской поверхности
Нажмите на защитную крышку, рычаг опустите вниз, на плоской поверхности (рисунки 14.1а, b), чтобы закрыть иглу и крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.1b).
2. Закрытие большим пальцем.
Поместите большой палец на рычаг, слегка нагните его по направлению к кончику иглы (рисунки 14.2а, b), чтобы закрыть иглу и защитную крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.2b).
Шаг 15. Как только вы закрыли защитную крышку, немедленно выбросьте иглу и шприц в соответствующий контейнер для острых предметов.
Важно:
Следующие шаги касаются только дозировки 45 мг!
Шаг 1. Откройте внешнюю упаковку (оторвите фольгу от уголка, место отрыва обозначено) и извлеките содержимое упаковки А (рисунок 1.1) и упаковки Б (рисунок 1.2), положите на стерильную поверхность. Выбросьте пакетики с влагопоглотителем.
Шаг 2. Выньте из шприца Б (не выкручивать) короткий поршень синего цвета со вторым ограничителем серого цвета (рисунок 2).
Не смешивайте продукт с двумя ограничителями внутри шприца.
Шаг 3. Аккуратно выньте белый поршень из упаковки со шприцем А и вставьте его в ограничитель серого цвета шприца Б (рисунок 3).
Шаг 4. Снимите серый резиновый колпачок со шприца Б и отложите шприц (рисунок 4).
Шаг 5. Держите шприц А вертикально, чтобы избежать протечки, а затем открутите прозрачный колпачок со шприца А (рисунок 5)
Шаг 6. Соедините два шприца вместе, надавливая и вкручивая шприц Б в шприц А до полной фиксации (рисунки 6а, 6Ь). Не закручивайте шприцы слишком плотно.
Шаг 7. Переверните соединённые шприцы и держите шприцы вертикально (шприц Б снизу) до момента полного ввода содержимого лейпрорелина ацетата из шприца А в шприц Б (рисунок 7).
Шаг 8. Тщательно перемешайте содержимое обоих шприцев, держа их в горизонтальном положении и поочередно осторожным движением нажимая на поршень то одного то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного раствора (рисунок 8). Не наклонять шприцы (следует обратить внимание, что это может стать причиной протечки, поскольку шприцы могут частично открутиться).
После тщательного смешивания вязкий раствор приобретёт цвет от бесцветной до светло-жёлтого цвета.
Важно: Необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать Готовый продукт запрещено.
Помните: Продукт нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
Шаг 9. Держите шприцы вертикально, шприц Б — снизу. Шприцы должны быть четко закреплены. Нажимая на поршень шприца А, и слегка подтягивая поршень шприца Б, переместите все содержимое в шприц Б (рисунок 9).
Шаг 10. Открутите шприц А, продолжая нажимать на поршень шприца (рисунок 10). Убедитесь, что содержимое не вытекает из шприца, поскольку вы не сможете закрепить иглу надлежащим образом в случае вытекания.
Помните: наличие маленьких пузырьков воздуха допустимо. Не пытайтесь удалять пузырьки из шприца Б на этом этапе, поскольку это может привести к потере продукта.
Шаг 11.
Держите шприц Б вертикально и удерживайте белый поршень во избежание потери препарата
Откройте упаковку со стерильной иглой (отогнув бумажную этикетку) и извлеките иглу.
•Присоедините безопасную иглу к шприцу Б, удерживая шприц и аккуратно поворачивая иглу по часовой стрелке приблизительно на три четверти оборота до полной фиксации (рис. 11).
Не перекручивайте иглу, поскольку это может привести к образованию трещин на переходнике иглы и последующей утечке препарата во время инъекции.
Если переходник иглы сломан, имеет видимые повреждения или протекает, препарат использовать не следует.
Замена повреждённой иглы, а также инъекционное введение препарата недопустимы. Весь препарат необходимо утилизировать с соблюдением мер безопасности.
В случае повреждения переходника иглы необходимо использовать новый препарат.
Шаг 12. Перед инъекцией снимите защитный колпачок с иглы (рисунок 12).
Важно: не используйте иглу до установки на шприц.
Шаг 13. До начала введения удалите большие пузырьки воздуха из шприца Б. Вводите препарат подкожно. Убедитесь в том, что введен весь препарат из шприца Б.
Шаг 14. После инъекции, закройте защитную крышку в соответствии с рекомендациями, представленными ниже.
1. Закрытие на плоской поверхности
Нажмите на защитную крышку, рычаг опустите вниз, на плоской поверхности (рисунки 14.1а, b), чтобы закрыть иглу и крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.1b).
2. Закрытие большим пальцем.
Поместите большой палец на рычаг, слегка нагните его по направлению к кончику иглы (рисунки 14.2а, b), чтобы закрыть иглу и защитную крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.2b).
Шаг 15. Как только вы закрыли защитную крышку, немедленно выбросьте иглу и шприц в соответствующий контейнер для острых предметов.
Информация для работников здравоохранения
Если раствор был приготовлен неправильно, его не следует вводить, поскольку в связи с неправильным приготовлением раствора может наблюдаться отсутствие клинической эффективности.
Элигард® (45 мг)
МНН: Лейпрорелин
Производитель: Толмар Инк.
Анатомо-терапевтическо-химическая классификация: Leuprorelin
Номер регистрации в РК:
№ РК-ЛС-5№018819
Информация о регистрации в РК:
25.10.2017 — 25.10.2022
Информация о реестрах и регистрах
- Скачать инструкцию медикамента
Торговое название
Элигард®
Международное непатентованное название
Лейпрорелин
Лекарственная форма
Лиофилизат для приготовления раствора для подкожного введения 7,5 мг, 22,5 мг, 45 мг в комплекте с растворителем
Состав
1 шприц с препаратом (шприц Б) содержит, в миллиграммах
активное вещество: лейпрорелина ацетат 10.6* 29.2* 59.2*
(7.5) (22.5) (45)
1 шприц с растворителем (шприц А) содержит, в миллиграммах
Для Для Для
дозировки дозировки дозировки
7,5 мг 22,5 мг 45 мг
Сополимер поли-D,L-лактид-гликолид:
PLGH (50: 50) 117* — —
PLG (75: 25) — 206* —
PLG (85: 15) — — 217*
N-метил-2-пирролидон 226* 251* 217*
*Избыток веществ компенсирует потери в шприце и игле
Описание
Лиофилизат для приготовления раствора (шприц Б). Содержимое шприца: порошок от белого до почти белого цвета, без признаков оплавления.
Растворитель (шприц А). Вязкая прозрачная жидкость от светло-жёлтого до светло-жёлтого с коричневатым оттенком цвета (для дозировки 7.5 мг). Вязкая прозрачная жидкость от бесцветного до светло-жёлтого цвета (для дозировок 22.5 мг и 45 мг).
Приготовленный раствор. Вязкая прозрачная жидкость от светло-жёлтого до светло-жёлтого с коричневатым оттенком цвета (для дозировки 7.5 мг). Вязкая прозрачная жидкость от бесцветного до светло-жёлтого цвета (для дозировок 22.5 мг и 45 мг.
Фармакотерапевтическая группа
Противоопухолевые гормональные препараты. Гормоны и их производные. Гонадотропин – рилизинг гормона аналоги. Лейпрорелин.
Код АТХ L02AE02
Фармакологические свойства
Фармакокинетика
Абсорбция
После подкожного введения любой из форм депо Элигарда® отмечается первоначальная фаза подъема, которая характеризуется высокой концентрацией лейпрорелина в сыворотке крови. Она сменяется фазой плато, в ходе которой сывороточные концентрации лейпрорелина остаются относительно
постоянными в течение всего оставшегося временного промежутка между инъекциями. После повторного введения признаки кумуляции не выявлены: профиль Элигарда® в сыворотке крови одинаков как после первого, так и каждого последующего введения.
Фармакокинетические свойства Элигарда® у пациентов с прогрессирующим раком предстательной железы были изучены: для Элигарда® в дозе 22,5, 30 и 45 мг за два временных промежутка между введениями, для Элигарда® в дозе 7,5 мг – за три временных промежутка между введениями. Профиль лейпрорелина в сыворотке крови на фоне повторного введения Элигарда® пациентам с прогрессирующим раком предстательной железы через определенные временные интервалы соответствовал таковому для других существующих форм депо лейпрорелина. В редких случаях концентрация лейпрорелина в сыворотке крови в фазу плато оказывалась ниже порога чувствительности лабораторных тест-систем, что не влияло на подавление уровня тестостерона. Для каждой формы Элигарда® фармакокинетический профиль замедленного высвобождения действующего вещества соответствовал непрерывному подавлению уровня тестостерона почти у 100% пациентов в течение месячного, трёхмесячного, четырёхмесячного или шестимесячного интервала между введениями препарата.
Средняя концентрация лейпрорелина в сыворотке крови после первоначальной инъекции увеличилась до 25,3 нг/мл (Сmax) в среднем через 5 часов после введения. После первоначального повышения на фоне каждой инъекции сывороточные концентрации лейпрорелина оставались относительно стабильными (0,28-2,00 нг/мл).
Распределение
Средний равновесный объем распределения после внутривенного введения составляет 27 л. Связь с белками плазмы составляет 43 — 49 %.
Метаболизм
После внутривенного введения 1 мг лейпрорелина, системный клиренс
составляет 8,34 л/ч с периодом полувыведения приблизительно 3 часа. Исследования по метаболизму Элигарда® не проводились. Лейпрорелина ацетат подвергается метаболической деградации, главным образом до более коротких неактивных пептидов – пентапептида (метаболит I), трипептида (метаболиты II и III) и дипептида (метаболит IV). Концентрация основного метаболита М-1 достигает максимального уровня в течение 2-6 часов и составляет 6 % от максимального уровня лейпрорелина. Через неделю после инъекции средняя концентрация М- I в плазме составляет 20 % от средней концентрации лейпрорелина.
Выведение
Через 27 дней после назначения лейпрорелина ацетата 3,75 мг в моче определялось менее 5 % дозы родительского вещества и метаболита М- I.
Фармакокинетика у пациентов с почечной и печеночной недостаточностью не определялась.
Фармакодинамика
Лейпрорелин — активное вещество препарата Элигард® является синтетическим нонапептидным агонистом гонадотропин-рилизинг гормона (ГнРГ).
После первоначального введения лейпрорелина ацетат вызывает повышение уровней циркулирующего лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ), что приводит к временному повышению уровней половых стероидов (тестостерона и дигидротестостерона у мужчин). Последующее введение препарата в терапевтических дозах угнетает выработку гипофизарных гонадотропинов и подавляет тестикулярный и овариальный стероидогенез. У мужчин содержание тестостерона снижается до кастрационного уровня (<50 нг/дл) в течение 3 – 5 недель после начала лечения.
Средний уровень тестостерона через 6 месяцев лечения составляет 6.1 (± 0.4) нг/дл для дозировки 7.5 мг; 10.1 (± 0.7) нг/дл для дозировки 22.5 мг и 10.4 (± 0.53) нг/дл для дозировки 45 мг. Эти значения сопоставимы с уровнем тестостерона после выполнения билатеральной орхиэктомии.
Показания к применению
— распространённый гормонозависимый рак предстательной железы.
Способ применения и дозы
Перед использованием температура препарата должна достичь комнатной. Препарат необходимо ввести в течение 30 минут после смешивания. Содержимое двух стерильных предварительно заполненных шприцев необходимо смешать непосредственно перед инъекцией. Препарат вводится подкожно в область с достаточным количеством подкожно-жировой клетчатки (например, в переднюю брюшную стенку), где отсутствует выраженная пигментация, узелки, патологические изменения кожи или волосы. Места инъекций необходимо периодически менять.
Элигард® не следует вводить в руку.
Два шприца соединяются, а их содержимое смешивается путем перемещения из одного шприца в другой (см. ниже) до получения гомогенной смеси. Далее следует разъединить шприцы, и надеть иглу непосредственно перед инъекцией. Элигард® необходимо вводить под наблюдением медицинского работника.
Элигард® в дозе 7,5 мг рекомендуется вводить один раз в месяц.
Элигард® в дозе 22,5 мг рекомендуется вводить один раз каждые три месяца. Элигард® в дозе 45 мг рекомендуется вводить один раз каждые шесть месяцев.
Только для одноразового применения. Неиспользованный раствор должен быть уничтожен.
После вскрытия ячейковой упаковки или внешней упаковки из алюминиевой фольги, необходимо сразу же смешать лиофилизат и растворитель для получения инъекционного раствора и ввести его в организм пациента.
Несмотря на то, что химическая стабильность готового к применению раствора сохраняется в течение 30 минут при температуре 25°C, вязкость растворенного препарата с течением времени увеличивается. Поэтому препарат следует вводить непосредственно после приготовления рабочего раствора.
-
Расположив упаковку на чистой рабочей поверхности, вскрыть все защитные оболочки (фольгу следует снимать от угла, помеченного небольшим вздутием) и достать ее содержимое. Удалить пакетик (и) с влагопоглощающим веществом.
-
Вынуть из шприца Б короткий шток-поршень с голубым наконечником (не выворачивать) и прикрепленный к нему ограничитель и выбросить. Аккуратными закручивающими движениями прикрепить длинный белый заместительный шток-поршень к серому основному ограничителю, который остался в шприце Б.
-
Отвинтить защитную крышку со шприца А, держа его в вертикальном положении, чтобы убедиться в отсутствии утечки растворителя. Удалить серую каучуковую крышку со шприца Б.
-
Плотно соединить два шприца вместе путем поступательно-вращательных движений. Избегать чрезмерного закручивания элементов шприцев. При утечке какого-либо количества растворителя невозможно будет должным образом закрепить иглу.
-
Ввести жидкое содержимое шприца А в шприц Б, содержащий лейпрорелина ацетат. В горизонтальном положении тщательно смешать компоненты препарата, попеременно нажимая на поршни обоих шприцев (всего около 60 раз), для получения однородного раствора (суспензии Элигард® в дозе 45 мг). Избегать перегибов системы шприцев. При правильном смешивании раствор (суспензия Элигард® 45 мг) представляется собой: для Элигард® 7,5 мг – светло-желтую или желтоватую с коричневым оттенков жидкость; для Элигард® 22,5/45 мг – бесцветную или белую, или бледно-желтую жидкость. Важно помнить, что препарат следует смешивать только согласно данной инструкции; взбалтывание не обеспечивает достаточного смешивания компонентов препарата.
-
Держать шприцы вертикально; при этом шприц Б находится внизу. Соединение шприцев должно быть прочным. Ввести весь готовый препарат в шприц Б (короткий широкий шприц), нажимая на поршень шприца А и аккуратно оттягивая поршень шприца Б назад. Отсоединить шприц А, продолжая нажимать на его поршень. Важно помнить: готовый препарат может содержать небольшие пузырьки, что не влияет на его действие. (Применимо к препарату, укомплектованному иглой инъекционной).
-
Расположить шприц Б вертикально. Удалить колпачок с основания стерильного картриджа иглы, поворачивая его. Прикрепить картридж иглы к концу шприца Б, толкая его и поворачивая иглу, пока она прочно не встанет на место. Не навинчивайте иглу на шприц до снятия упаковки. Перед введением препарата снимите защитный колпачок с картриджа иглы.
(Применимо к препарату, укомплектованному безопасной иглой инъекционной).
Процедура введения
ВАЖНО: Перед использованием дайте препарату нагреться до комнатной температуры. После смешивания препарат должен быть введён в течение 30 минут.
-
Выбрать соответствующее место для инъекции на передней брюшной стенке, в верхнем ягодичном квадранте или любом другом участке с достаточным количеством подкожной жировой клетчатки, где отсутствует выраженная пигментация, узелки, патологические изменения кожи или волосы. Поскольку зоны подкожного введения препарата необходимо периодически менять, то следует выбирать именно те участки кожи, куда инъекция еще не проводилась.
-
Протереть место инъекции смоченным в спирте ватным тампоном.
-
С помощью большого и указательного пальцев недоминантной (нерабочей) руки собрать складку кожи в месте проведения инъекции.
-
Доминантной (рабочей) рукой быстро воткните иглу под углом 90. Примерный угол, используемый Вами, будет зависеть от количества и полноты подкожной ткани и длины иглы. После введения иглы освободить кожную складку, собранную нерабочей рукой.
-
Введите препарат медленным равномерным толчком. Нажимайте на поршень, пока шприц не опустеет.
-
Быстро выньте иглу под тем же углом, под которым она была вставлена.
-
Сразу после того, как игла будет вынута, приведите в действие защитный щиток на игле большим пальцем руки (Рисунок 1) или пальцем (Рисунок 2) или плоской поверхностью (Рисунок 3), чтобы сдвинуть защитный щиток вперёд, пока он полностью не закроет кончик иглы и не защелкнется на место. Слышимый и ощутимый “щелчок” свидетельствует о том, что защитный щиток находится в зафиксированном положении (Рисунок 4). [Шаг 7 применим только к препарату, укомплектованному безопасной иглой инъекционной]
ИЛИ ИЛИ
Рисунок 1 Рисунок 2
Рисунок 3
Рисунок 4
-
Все элементы инъекционной системы следует выбросить в соответствующую емкость для биологически опасных материалов. Только для одноразового применения. Неиспользованный раствор должен быть уничтожен.
-
Снять перчатки и вымыть руки. Зафиксировать процесс введения препарата и реакцию пациента на инъекцию.
Побочные действия
Частота нежелательных явлений классифицируется как: очень частые (>1/10), частые (>1/100, <1/10), нечастые (>1/1,000, <1/100), редкие (>1/10,000, <1/1,000) и очень редкие (<1/10,000).
Очень часто
— приливы a b; чувство жара d
— обморок и острая сосудистая недостаточность a b d
— экхимозы, эритема a b d
— ощущение жжения и парестезии в месте введения препарата a b d, общее недомогание и повышенная утомляемость d
Часто
— одышка, кровохарканье, эмфизема легких
— назофарингит d
— гипестезия a b
— зуд кожи a b d, ночная потливость d
— задержка мочеиспусканий, затруднение мочеиспусканий, дизурия, никтурия, олигурия a b d
— болезненность грудных желез, бесплодие, гипертрофия грудных желез a b d, атрофия яичек, боли в яичках a b d, эректильная дисфункция, уменьшение размеров полового члена a b d
— слабость a b d, повышенная утомляемость a b, общее недомогание d, боли и кровоподтеки в месте введения препарата a b d, покалывание в месте инъекции d, ознобы a b d
— уменьшение количества эритроцитов, снижение гематокрита и гемоглобина, гематологические изменения a b d
— повышение уровня креатинфосфокиназы, удлинение времени свертывания крови a b d
— боли в костях , артралгии, миалгии a b d
— поллакиурия, гематурия a b d
Нечасто
— ринорея a b d, диспноэ d
— инфекция мочевыводящих путей a b, местная инфекция кожи a b
— ухудшение течения сахарного диабета a b d
— необычные сновидения, депрессия, снижение полового влечения a b d
— головокружение, головная боль, бессонница, нарушение вкуса, нарушение обоняния, вестибулярное головокружение a b d
— гипертензия, гипотония a b d
— запоры, сухость во рту a b d, диспепсия d, рвота d
— повышенная общая потливость и потливость ладоней, ночная потливость a b d
— боли в спине a b d, судороги в мышцах, тремор, мышечная атрофия a b
— спазм мочевого пузыря, чрезмерно учащение мочеиспусканий, задержка мочи a b d
— гинекомастия, импотенция, нарушение функции яичек a b d
— зуд в месте введения препарата a b d, заторможенность, боли, лихорадка, индурация в месте введения препарата a b d
— повышение уровня аланинаминотрансферазы, триглицеридов сыворотки крови, удлинение протромбинового времени, увеличение массы тела a b d
Редко
— гипестезия d
— патологические непроизвольные движения a b d
— метеоризм, отрыжка a b d; боли в животе на фоне вздутия a
— алопеция, кожные высыпания b d
— боли в грудных железах a b d
— образование язв в месте введения препарата d
Очень редко
— некроз тканей в месте введения препарата d
а Элигард в дозе 7,5 мг, b Элигард в дозе 22,5 мг, d Элигард в дозе 45 мг
К ожидаемым последствиям фармакологического подавления выработки тестостерона относятся приливы жара, повышенная потливость/ночная потливость, потеря/снижение полового влечения, импотенция, гинекомастия, болезненность/чувствительность грудных желез, атрофия яичек, эректильная дисфункция, уменьшение размеров полового члена, нарушение функции полового члена.
Кровоизлияние в гипофиз: в ходе пострегистрационных наблюдений появлялись сообщения о редких случаях кровоизлияния в гипофиз (клинический синдром, возникающий на фоне инфаркта гипофиза), которое развивалось после введения агонистов гонадотропин-рилизинг гормона.
Чаще всего это явление возникало в течение двух недель после первого введения, а в некоторых случаях – в течение нескольких часов. Клиническая картина кровоизлияния в гипофиз представлена внезапной головной болью, рвотой, нарушением зрения, параличом глазодвигательных мышц, иногда – острой сердечно-сосудистой недостаточностью. При этом состоянии требуется немедленное медицинское вмешательство.
Также сообщалось о развитии анафилактических/анафилактоидных реакций на введение агонистов ГнРГ.
Судороги: в ходе пострегистрационных наблюдений были отмечены случаи судорог у некоторых пациентов, получавших лечение аналогами агонистов гонадотропин-рилизинг гормона.
Противопоказания
-
повышенная чувствительность к активному веществу или любому другому компоненту препарата, в том числе к полисорбату 80
-
исходное число нейтрофилов <1500/мкл
-
выраженные нарушения функции печени
-
гормононезависимый рак предстательной железы
-
хирургическая кастрация
-
женщины и дети
-
наличие компрессии спинного мозга, наличие метастазов в спинной мозг
Лекарственные взаимодействия
Исследований по изучению фармакокинетического взаимодействия препарата Элигард® с другими препаратами не проводилось.
О взаимодействии Элигарда® с другими лекарственными препаратами не сообщалось.
Особые указания
Элигард® должен применяться под наблюдением врача, имеющего опыт применения противоопухолевой терапии.
Как и другие агонисты ГнРГ, Элигард®в первую неделю лечения вызывает кратковременное повышение концентрации тестостерона в сыворотке крови.
В связи с этим в течение первой недели лечения пациенты могут отметить усиление симптомов или появление новых признаков и симптомов, таких как боли в костях, неврологическая симптоматика, гематурия или обструкция выходного отверстия мочевого пузыря. При паллиативном лечении прогрессирующего рака предстательной железы с помощью агонистов ГнРГ наблюдались отдельные случаи обструкции мочеточника и/или компрессии спинного мозга, которая может привести к развитию паралича с возможными осложнениями и летальным исходом. Пациенты с метастатическими поражениями позвоночника и/или обструкцией мочевыводящих путей нуждаются в тщательном наблюдении в течение первых нескольких недель лечения. При развитии компрессии спинного мозга или нарушении функции почек необходимо провести стандартное лечение данных осложнений.
Включение в терапию нестероидных антиандрогенов и их одновременное введение с Элигардом® доказано снижает остроту реакций на препарат (то есть, усиление симптомов в ответ на кратковременное повышение тестостерона сыворотки крови) у пациентов из группы риска (а именно, при наличии выпячивания мозговых оболочек, что создает риск компрессии спинного мозга, или у пациентов с обструкцией выходного отверстия мочевого пузыря). За три дня до первой инъекции Элигарда® следует начать дополнительное введение соответствующего антиандрогена, которое должно продолжаться в течение первых двух-трех недель лечения. Это позволяет предотвратить последствия первоначального подъёма уровня тестостерона сыворотки крови.
Следует контролировать ответ на лечение Элигардом® путем периодических измерений концентрации тестостерона и простатспецифического антигена (ПСА) в сыворотке крови. Результаты измерений уровня тестостерона зависят от методики исследования. Для принятия правильных клинических и терапевтических решений рекомендуется учитывать вид и точность методики лабораторного исследования.
У пациентов мужского пола применение Элигарда® после хирургической кастрации не приводит к дальнейшему снижению уровня тестостерона сыворотки крови.
У некоторых пациентов опухоль оказывается нечувствительной к гормональному лечению. Диагностическим критерием данного состояния является отсутствие клинического улучшения, несмотря на достаточное подавление уровня тестостерона. Дальнейшее применение Элигарда® у таких пациентов бесполезно.
Влияние на эндокринную систему и метаболизм.
Изменение минеральной плотности костей: потеря костной ткани является частью естественного процесса старения, а также возникает на фоне гипоандрогенного состояния при длительном применении лейпрорелина ацетата. У пациентов с высоким риском снижения минеральной плотности костей и/или массы костной ткани, например, при наличии в семейном анамнезе остеопороза, при длительном использовании кортикостероидов или противосудорожных препаратов, при злоупотреблении алкоголем или табаком, применение Элигарда® может внести дополнительный риск. У данных пациентов перед началом лечения с помощью лейпрорелина ацетата следует очень внимательно оценить соотношение «риск-польза».
Длительное применение Элигарда® вызывает подавление гипофизарных гонадотропинов и выработки половых гормонов, что приводит к развитию симптомов гипогонадизма. Отмечено, что после прекращения лечения эти изменения подвергаются обратному развитию. Тем не менее, до сих пор точно не установлено, у всех ли пациентов купируются клинические симптомы гипогонадизма.
Применение антиандрогенов существенно увеличивает риск развития переломов на фоне остеопороза. Данные по этому вопросу крайне ограничены. Переломы на фоне остеопороза наблюдались у 5% пациентов через 22 месяца фармакологического подавления активности андрогенов и у 4% пациентов через 5-10 лет лечения. Риск переломов на фоне остеопороза в целом выше риска возникновения патологических переломов.
У некоторых пациентов, получающих лечение агонистами ГнРГ, возникают изменения толерантности к глюкозе. Поэтому на фоне лечения рекомендуется более частое наблюдение за пациентами с сахарным диабетом.
Сердечно-сосудистые заболевания.
Сообщается о повышенном риске развития инфаркта миокарда, внезапной смерти и инсульта, связанных с применением агонистов ГнРГ. Следует тщательно взвешивать соотношение имеющихся у пациента факторов сердечно-сосудистого риска при назначении лечения рака простаты агонистами ГнРГ. Пациенты, получающие лечение агонистами ГнРГ, должны находиться под наблюдением врача.
Было зарегистрировано удлинение интервала QT при длительном подавлении андрогенов. Врач должен оценить соотношение польза/риск при длительном подавлении андрогенов у пациенов с врожденным синдромом удлинения интервала QT, у пациентов с нарушением уровня электролитов в крови или у пациентов с застойной сердечной недостаточностью, а также у пациентов, получающих антиаритмические препараты класса IА (напр. гуанидин, прокаинамид) или класса III (напр. амиодарон, соталол).
Применение у пожилых пациентов
Возраст большинства пациентов (около 70%), которые участвовали в клинических исследованиях, соответствовал 70 годам и старше.
Почечная/Печеночная недостаточность
Фармакокинетические свойства Элигарда® у пациентов с печеночной или почечной недостаточностью не установлены. Все клинические исследования и оценка кинетики препарата проводились с участием пациентов с нормальной функцией печени и почек.
В постмаркетинговой практике сообщалось о судорогах у пациентов женского пола, детей, которые получали терапию лейпрорелина ацетатом. Эти случаи наблюдались у пациентов с судорогами, эпилепсией, цереброваскулярными расстройствами в анамнезе, аномалиями или новообразованиями центральной нервной системы, у пациентов с сопутствующей терапией, которая была ассоциирована с судорогами, например, бупропионом и ингибиторами обратного захвата серотонина. О судорогах также сообщалось у пациентов, у которых отсутствовали состояния, перечисленные выше.
Особенности влияния лекарственного средства на способность управлять транспортными средствами или потенциально опасными механизмами
Учитывая побочные эффекты препарата (головокружение, головная боль, расстройства зрения) следует соблюдать осторожность при управлении транспортом или другими потенциально опасными механизмами.
Передозировка
Симптомы: данных относительно передозировки не имеется.
Возможно усиление побочных эффектов.
Лечение: симптоматическая и поддерживающая терапия.
Форма выпуска и упаковка
По 343 мг (для дозировки 7.5 мг), по 457 мг (для дозировки 22.5 мг) или по 434 мг (для дозировки 45 мг) растворителя в полипропиленовый шприц с поршнем и навинчивающейся крышкой (шприц А). По 1 шприцу А вместе с поршнем для шприца Б и пакетиком с влагопоглотителем в поддон и пластиковую ячейковую упаковку, покрытую алюминиевой ламинированной фольгой.
По 10.6 мг (для дозировки 7.5 мг), по 29.2 мг (для дозировки 22.5 мг), или по 59.2 мг (для дозировки 45 мг) лейпрорелина ацетата в полипропиленовый шприц (шприц Б). По 1 шприцу Б вместе с иглой инъекционной в пенале из прозрачного пластика или безопасной иглой инъекционной с колпачком из прозрачного пластика, помещённой в пластиковую ячейковую упаковку, покрытую ламинированной бумагой, вместе с пакетиком с влагопоглотителем в поддон, или без поддона, и пластиковую ячейковую упаковку, покрытую алюминиевой ламинированной фольгой.
По 1 ячейковой упаковке со шприцем А в комплекте с поршнем и пакетиком с влагопоглотителем и по 1 ячейковой упаковке со шприцем Б в комплекте с иглой инъекционной или безопасной иглой инъекционной и пакетиком с влагопоглотителем вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную пачку.
Условия хранения
Хранить при температуре от 2 ºС до 8 ºС.
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту
Производитель
«Толмар Инк.», США
Адрес: 701 Центр Авеню, Форт Коллинс, Колорадо 80526 США
Владелец регистрационного удостоверения
«Толмар Инк.», США
Адрес: 701 Центр Авеню, Форт Коллинс, Колорадо 80526 США
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции:
ИП Тлеубергенова Г.С., Республика Казахстан, 010000, Акмолинская область, г. Астана, ул. Бозинген, д.8.
aldoninakbar@mail.ru
| 426513371477977101_ru.doc | 409.5 кб |
| 376716441477978259_kz.doc | 326.74 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Товары из категории — Препараты для лечения онкологических заболеваний
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 13 300
Описание препарата
Элигард является противоопухолевым препаратам, который создан для лечения онкологических заболеваний предстательной железы у мужчин. Действующий компонент является синтетическим гормоном и обладает повышенной активностью в сравнении с натуральным гормоном мужчиной. Основная связь активного компонента происходит в гипофизе.
После поступления в организм мужчины действующий компонент повышает физиологическую реакцию в течение первых семи дней. Через двадцать один день концентрация начинает снижаться. Снижается уровень гормонов. Следующая инъекция лекарство вызывает разрушение опухоли, которая зависит от уровня гормонов мужчины. После прекращения лечения гормональный уровень восстанавливается до физиологической нормы. Биологическая доступность составляет девяносто восемь процентов у мужчин, у женщин семьдесят пять процентов. Действующий компонент связывается с белками крови до сорока девяти процентов. Через семь дней после инъекции средняя концентрация действующего вещества составляет двадцать процентов. После доставки в кровь одного миллилитра лекарства средняя скорость очищения крови составляет восемь часов. Период выведения из организма составляет три часа. Действующий компонент подвергается процессу метаболизмом до образования коротких пептидов. Выведение из организма происходит через двадцать семь дней, концентрация действующего вещества составляет пять процентов от дозировки. При постановке семи с половиной миллиграммов лекарства уровень тестостерона в крови через шесть месяцев составляет шесть нанограмм на децилитр. Действующий компонент не вызывает толерантности. У большинства больных переносится хорошо.
Форма выпуска и состав препарата
Лекарство выпускается в виде лиофилизата. Он создан для приготовления раствора, который используется для подкожных инъекций. В состав препарата входят действующий компонент Лейпрорелин ацетат. Его доза составляет семь с половиной миллиграммов. Растворитель содержит сополимер ПЛГХ соотношение 50/50, n-метилпирролидон, его доза двести двадцать шесть мг. Лекарство упаковано в коробку, в которой содержится два шприца с маркировкой А и Б, игла.
Цена Элигарда зависит миллиграммов действующего вещества. Лекарство выпускается в комплекте шприц семь с половиной миллиграммов, сорок пять миллиграммов, двадцать два с половиной миллиграммов. Элигард купить можно только по рецепту врача. На каждую инъекцию выдается один рецепт. Аналога у лекарства нет.
Показания
Лекарство показано для лечения новообразований предстательной железы, которые являются гормонозависимыми образованиями.
Противопоказания
Препарат не используются у пациентов с повышенной чувствительностью к действующему компоненту, также к аналогам синтетического гормона. Не рекомендуется использовать у пациентов после хирургического удаления репродуктивных органов. Лекарства используются для лечения только у мужчин. Женщинам и детям до восемнадцати лет лекарства запрещено для использования.
Дозировка
Препарат назначается в виде инъекций. Инъекции ставится подкожно один раз в тридцать дней. Инъекция ставится подкожно в область, где имеется достаточное количество подкожно-жировой клетчатки. Местом инъекции может быть передняя брюшная стенка, верхний наружный квадрант ягодицы. Но следует проследить чтобы на месте не было патологических изменений, повышенного волосяного покрова, пигментации. Нельзя вводить лекарство в руку. Первоначальная дозировка составляет семь с половиной миллиграммов. Доза двадцать два миллиграмма ставится один раз в девяноста дней. А дозировка сорок пять миллиграммов ставится один раз в полгода. Лекарство вводится подкожно, при этом образуется депо действующего вещества, которая освобождается постепенно. Длительность высвобождения соответствует интервалу через сколько ставится инъекция:тридцать дней, девяноста дней, полгода. Длительность постановки инъекций зависит от ответной реакции на лечение. Если происходит повышение уровня мужского гормона на фоне терапии, то ей нужно остановить. Инъекция каждый раз ставится в разные места. Не допускать попадания лекарства в крупные кровеносные сосуды. Перед использованием лекарство нужно предварительно приготовить. Для этого нужно лиофилизат нагреть до комнатной температуры. После чего для работы нужен шприц с маркировкой А и Б. Шприц А с длинным поршнем вставляется с коротким поршнем шприц Б. Затем убирается крышечка с растворителем и водится шприц бы, в котором содержится действующий компонент. Медленно смешивается раствор с действующим компонентом до образования однородной консистенции. Раствор будет готов только после того как он станет бесцветный (слегка желтоватым) раствором. После чего шприц убирается. На шприц Б помещается специальная игла, которая является полностью стерильной иглой. Раствор готов. Его можно вводить подкожно. Перед манипуляцией место постановки обрабатывается спиртовым раствором. Манипуляция выполняется в стерильных перчатках. Для подкожного введения нужно рукой собрать кожу в складку, а доминирующей рукой под углом девяноста градусов ввести иглу. Опустить складку и медленно вести препарат. После процедуры на иглу поместить защитный колпачок. Затем зафиксировать в журнале дату и время постановки. Разведённое лекарство является одноразовым, неиспользованные раствор утилизируется. Остальные компоненты от лекарства утилизируются в соответствующие емкости с дезинфекционным раствором. Хранение Элигард в разведенном виде составляет тридцать минут при температуре двадцать пять градусов. Через тридцать минут у раствора повышается вязкость, он становится не пригодным для инъекции. Цена Элигарда зависит от производителя.
Побочные действия
При длительном применении лекарства может проявлять нежелательные реакции на организм. Исходя из отзывов пациентов были зафиксированы основные симптомы. Влияние на сердечно сосудистую систему заключается в появлении приливов и жара, изменение артериального давления, обморочного состояния, отечности нижних конечностей, ощущение биение сердца, нехватка воздуха. Влияние на нервную систему заключается в виде кружения головы, болезненности головы, нарушенного сна, изменённого вкусом, депрессивного состояния, изменение зрения, изменения обоняния. Влияние на желудочно-кишечный тракт проявляется в виде периодической тошноты, расстройство пищеварения, нарушенного акта дефекации, сухость слизистой ротовой полости, повышенного газообразования. Влияние на органы дыхания заключается в виде заложенности носа, нарушенного дыхания. Влияние на мочевую систему заключается в виде нарушенного мочеиспускания, воспаление мочевого пузыря, спастические боли, появление крови в моче, болезненность в области яичек, нарушенная репродуктивная функция, снижение либидо. Влияние на костную систему проявляется болезненностью в костях, мышцах, судорожные сокращения, слабость мышц. Влияние на кровеносную систему заключается в виде снижения уровня гемоглобина, эритроцитов, тромбоцитов. Влияние на лабораторные анализы заключается в виде изменения показателей триглицеридов в крови. У некоторых пациентов может отмечаться жжение и болезненное ощущение в месте инъекции, краснота покрова, зуд, уплотнение места введения. Побочные эффекты Элигард могут проявиться через семь дней после начала лечения в виде обострения болезни.
Особые указания
Элигард в Москве может быть использован для лечения только под наблюдением опытного врача. Лекарство после постановки инъекции в течение семи дней вызывает нестойкое увеличение уровня тестостерона и фосфатазы в крови. Из-за этого у больного могут усилиться симптомы заболеванием, появляется болезненность в костях, кровь в моче, депрессивное состояние. Перечисленные симптоматические описания проходят походу лечения. Наблюдению подлежат пациенты, у которых имеются метастазы в спинном или головном мозге. Пациенту можно дополнительно назначить антиандрогены, чтобы избежать повышения уровня гормонов. Антиандрогены назначается за три дня до лечения. Но такая терапия повышает вероятность перелома костной ткани, так как у мужчин снижается плотность кости. Действующий компонент понижает толерантность к сахару. Больным с сахарным диабетом нужно проводить тщательный контроль анализов и учесть данный факт. Во время лечения нужно проводить контроль тестостерона в ответ на влияние действующего вещества. Действующий компонент вызывает нежелательные реакции в виде кружения головы, изменения зрения, поэтому во время терапии следует ограничить деятельность, требующая концентрации внимания. Нежелательно во время лечения управлять автомобилем. Если у пациента на фоне лечения нет улучшения, следовательно, опухоль является негормонзависимой и использование лекарства нецелесообразно. Такому пациенту требуется провести дополнительную диагностику.
Беременность и лактация
Лекарство не используются у женщин во время беременности и лактации. Препарат создан для лечения мужчин, из-за этого нецелесообразно использовать раствор для терапии женщин.
При нарушениях функции почек
Лекарственное средство у пациентов с нарушенной функцией почек используется крайне осторожно. Действующий компонент может вызвать нежелательную реакцию на функцию мочевой и почечной системы. На фоне терапии может нарушиться процесс мочеиспускания, может возникнуть преобладание ночного диуреза над дневным объемом мочи. У больного может отмечаться снижение количества мочи, наличие крови в моче или возникнуть задержка мочеиспускания. Во время лечения таким пациентам нужно проводить тщательный контроль работы почек. Сдавать анализы не реже чем один раз в тридцать дней. Если у пациента отмечается выраженная болезненность или обострение заболевание почек, то он врачу нужно решить вопрос о дальнейшей тактике лечения.
Применение в пожилом возрасте
Инструкция по применению Элигард в пенсионном возрасте показывает, лекарственное средство эффективно борется с новообразованиями предстательной железы. Но данная группа пациентов находится на тщательном контроле из-за вероятности развития побочного воздействия на организм. В ходе медицинской практики установлено, что семьдесят процентов пациентов имели возраст семидесяти лет. Стоит учитывать лекарственное взаимодействие препаратов у пожилых пациентов. Нежелательного лекарственного взаимодействия с изменением фармакологических свойств не сообщалось. На фоне терапии больным проводится электрокардиограмма для контроля работы сердца.
Цены на Элигард в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 13 300 руб.
Сертификаты и лицензии
Элигард, инструкция по применению
- Производитель
- Страна происхождения
- Группа препаратов
- Действующее вещество
- Формы выпуска
- Упаковка
- Состав
- Дозировка
- Показания к применению
- Передозировка
- Противопоказания
- Побочные действия
- Способ применения
- Применение при беременности и кормлении грудью
- Фармакологическое действие
- Синонимы
- Фармакокинетика
- Взаимодействие с другими лекарствами
- Лекарственная форма
- Условия хранения
- Срок годности
- Особые условия
- Условия отпуска из аптек
Элигард — лекарственное средство, используемое для лечения гормонозависимого рака простаты.
Производитель
Производитель: «Толмар ИНК», США.
Владелец регистрационного удостоверения: «Астеллас Фарма Юроп Б.В.», Нидерланды.
Страна происхождения
США, Нидерланды.
Группа препаратов
Относится к фармакологической группе «Противоопухолевое средство, аналог гонадотропин-рилизинг-гормона (ГнРГ)»
Действующее вещество
Основным действующим веществом является лейпрорелин (Leuprorelinum). Брутто-формула C59H84N16O12. Является синтетическим аналогом гонадотропин-рилизинг-гормона. В препарате используется в виде ацетата. Молекулярная масса — 1269,47.
Код ATX: L02AE02
Формы выпуска
Препарат Элигард производится в виде лиофилизата и растворителя в трех дозировках (7,5, 22,5 и 45 мг), которые помещаются в разные шприцы. В шприце А находится прозрачный растворитель вязкой консистенции, у которого цвет немного различается в зависимости от дозировки (7,5 мг — светло-желтого цвета с возможным коричневатым оттенком, 22,5/45 мг — от бесцветного до светло-желтого). Посторонние частицы недопустимы. Могут присутствовать пузырьки воздуха. Шприц Б содержит лиофилизат лейпрорелина ацетата белого цвета без других частиц.
Восстановленный раствор также сохраняет консистенцию и цвет растворителя, возможно наличие пузырьков воздуха.
Упаковка
В одной картонной упаковке одна ячейковая упаковка, содержащая шприц А (с поршнем и влагопоглотителем) и шприц Б (вместе с инъекционной иглой и влагопоглотителем), а также инструкцию по применению с подробным описанием показаний к применению, противопоказаний и др.
Состав
| Компоненты | Дозировка препарата, мг | ||
| 7,5 | 22,5 | 45 | |
| 1 шприц А (растворитель) сополимер поли-D,L-лактид-ко-гликолид: ПЛГХ (50:50) ПЛГ (75:25) ПЛГ (85:15) N-метил-2-пирролидон |
117 — — 226 |
— 206 — 251 |
— — 217 217 |
| 1 шприц Б лейпрорелина ацетат |
10,6 | 29,2 | 59,2 |
Дозировка
Элигард должен применяться только под контролем специалиста здравоохранения, имеющего достаточный опыт для оценки эффекта лечения.
Элигард назначают в виде подкожной инъекции один раз в месяц при дозировке 7,5 мг, один раз в три месяца при дозировке 22,5 мг и один раз в 6 месяцев при дозировке 45 мг. Содержимое двух заранее наполненных стерильных шприцов должно быть смешано непосредственно перед подкожным введением препарата Элигард. Введенный раствор образует депо препарата, обеспечивающее постоянное высвобождение лейпрорелина в течение указанного периода. Как правило, терапия распространенного рака предстательной железы с использованием Элигарда предусматривает длительное лечение и не должна прекращаться при наступлении улучшения или ремиссии. Элигард может использоваться в качестве неоадъювантной или адъювантной терапии в сочетании с лучевой терапией у пациентов с локализованным раком высокого риска и местно-распространенным раком простаты.
Место инъекции следует периодически менять. Избегать попадания препарата в артерию или вену.
Ответ на терапию препаратом Элигард необходимо контролировать по клиническим параметрам и измерению концентрации простат-специфического антигена (ПСА) в сыворотке крови. Результаты клинических исследований показали, что концентрация тестостерона увеличивалась в течение первых трех дней лечения у большинства пациентов, не подвергавшихся орхиэктомии, а затем снижалась до уровней ниже таковых при медикаментозной кастрации в течение 3–4 недель. После достижения данные показатели остаются неизменными при продолжении терапии лекарственным препаратом (<1,0% случаев прорывного повышения концентраций тестостерона). Если ответ пациента на терапию является недостаточным, необходимо убедиться, что концентрация тестостерона в сыворотке крови достигла или остается на кастрационном уровне. В случае предполагаемой или известной ошибки при смешивании у пациента должна быть определена концентрация тестостерона в связи с тем, что в результате неправильного приготовления, смешивания или введения препарата могут наблюдаться случаи отсутствия клинической эффективности.
У пациентов с метастатическим кастрационно-резистентным раком предстательной железы, не подвергавшихся хирургической кастрации и получающих агонисты ГнРГ, такие как лейпрорелин, лечение агонистами ГнРГ может быть продолжено на фоне применения ингибиторов биосинтеза андрогенов или ингибиторов андрогенных рецепторов.
Коррекция доз для особых популяций пациентов
Клинических данных по применению Элигарда у больных с печеночной или почечной недостаточностью нет.
В случае предполагаемой или известной ошибки при смешивании у пациента должна быть определена концентрация тестостерона в связи с тем, что в результате неправильного приготовления, смешивания или введения препарата могут наблюдаться случаи отсутствия клинической эффективности.
Показания к применению
Гормонозависимый рак предстательной железы.
Передозировка
Нет зарегистрированных случаев передозировки. При ее возникновении назначается симптоматическое лечение.
Противопоказания
- Непереносимость компонентов, входящих в состав.
- Хирургическая кастрация.
- Женский пол.
- Детский возраст.
- При раке предстательной железы с компрессией спинного мозга/наличием метастазов в позвоночнике (в качестве единственного лечения).
Побочные действия
Очень часто: ощущение «приливов», эритема, экхимозы, повышенная утомляемость, раздражение/парестезии в месте инъекции.
Часто: назофарингит, тошнота, диарея, гастроэнтерит/колит, зуд, потливость по ночам, боли в суставах и мышцах, дрожь, слабость, нарушение мочеиспускания, дизурия, никтурия, олигурия, болезненность/гипертрофия грудных желез, боль/атрофия яичек, бесплодие, импотенция, уменьшение размеров полового члена, недомогание, реакции в месте введения (боль, кровоподтеки, жжение), анемия, гематологические изменения, увеличение активности КФК, времени свертываемости крови.
Нечасто: инфекции мочеполовых путей, ограниченная инфекция кожи, ухудшение течения сахарного диабета, головокружение, головная боль, гипестезия, вертиго, нарушения сна, вкусовых ощущений, обоняния, нарушение АД, ринорея, диспноэ, запор, сухость во рту, диспепсия, рвота, холодный пот, повышенная потливость.
Самые распространенные нежелательные эффекты: ощущение «приливов», тошнота, недомогание и слабость.
Применение при беременности и кормлении грудью
Запрещен для назначения женщинам.
Фармакологическое действие
Лейпрорелин является синтетическим непептидным аналогом естественного гонадотропин-рилизинг-гормона (ГнРГ), который при длительном применении ингибирует секрецию гипофизарного гонадотропина и подавляет тестикулярный стероидогенез у мужчин. Аналог обладает большей эффективностью, чем естественный гормон, и его воздействие обратимо при прекращении лечения. Однако время восстановления концентрации тестостерона может варьироваться среди пациентов.
Применение лейпрорелина сначала приводит к повышению концентрации циркулирующего лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ), в результате чего временно повышается концентрация гонадных стероидов, тестостерона и дигидротестостерона у мужчин. При продолжительном применении лейпрорелина содержание ЛГ и ФСГ снижается. У мужчин содержание тестостерона снижается до кастрационного уровня (< 50 нг/дл) в течение 3–5 недель после начала лечения. Среднее содержание тестостерона через 6 месяцев лечения составляет 6,1 (± 0,4) нг/дл для дозировки 7,5 мг; 10,1 (± 0,7) нг/дл для дозировки 22,5 мг и 10,4 (± 0,53) нг/ДЛ для дозировки 45 мг. Эти значения сопоставимы с содержанием тестостерона после выполнения билатеральной орхиэктомии.
Все пациенты в клиническом исследовании Элигарда 7,5 мг достигли кастрационных уровней тестостерона на 6-ой неделе лечения; 94% пациентов — к 28-му дню и 98% пациентов — к 35-му дню. Все пациенты в клиническом исследовании Элигарда 22,5 мг достигли кастрационных концентраций тестостерона на 5-ой неделе; 99% пациентов — к 28-му дню. Все пациенты (за исключением одного) в клиническом исследовании Элигарда 45 мг достигли кастрационных концентраций тестостерона на 4-ой неделе. У подавляющего большинства пациентов концентрации тестостерона уменьшались ниже 20 нг/дл, хотя полноценное преимущество данных низких концентраций тестостерона пока не было установлено.
Концентрации ПСА снизились на 94% через 6 месяцев лечения при использовании Элигарда 7,5 мг, на 98% — при использовании Элигарда 22,5 мг, на 97% — при использовании Элигарда 45 мг. Длительные исследования показали, что постоянная терапия поддерживает концентрацию тестостерона ниже кастрационного уровня на протяжении до 7 лет и, по всей видимости, на неопределенный срок.
Синонимы
Известен один аналог — Люкрин депо.
Фармакокинетика
После первой инъекции через 4–8 часов средний уровень концентрации лейпрорелина (Сmax), определяемой в сыворотке крови, повышается до 25,3 нг/дл, 127 НГ/ДЛ и 82 нг/дл — при применении лейпрорелина в дозе 7,5 мг, 22,5 мг и 45 мг соответственно.
После первоначального повышения (фаза плато составляет от 2 до 28 дней для дозировки 7,5 мг, от 3 до 84 дней для дозировки 22,5 мг, от 3 до 168 дней для дозировки 45 мг) концентрация лейпрорелина в сыворотке оставалась относительно стабильной: 0,28–1,67 нг/мл для дозировки 7,5 мг и 0,2–2 нг/мл для дозировок 22,5 и 45 мг. Данные о накоплении вещества при повторных инъекциях отсутствуют.
Средний объем распределения в равновесном состоянии после внутривенного однократного введения лейпрорелина здоровым добровольцам-мужчинам составлял 27 литров. По данным исследований in vitro, связь с белками плазмы составляет от 43% до 49%.
При введении 1 мг лейпрорелина ацетата внутривенно здоровым добровольцам мужчинам выяснилось, что при применении двухкамерной модели средний клиренс составил 8,34 л/ч с конечным периодом полувыведения приблизительно 3 часа.
Исследований по выведению препарата Элигард не проводилось.
Исследований по лекарственному метаболизму препарата Элигард не проводилось.
Взаимодействие с другими препаратами
Исследований по изучению фармакокинетического взаимодействия препарата Элигард с другими препаратами не проводилось. О взаимодействии Элигарда с другими лекарственными препаратами не сообщалось.
В связи с тем, что андрогеная депривация может удлинять интервал QT, должно быть тщательно взвешено одновременное применение препарата Элигард с другими препаратами, удлиняющими интервал QT, или препаратами, способными вызывать желудочковую тахикардию типа «пируэт», такими как антиаритмические препараты класса IА (например, хинидин, дизопирамид) или класса III (например, амиодарон, соталол, дофетилид, ибутилид), метадон, моксифлоксацин, нейролептики и т.д.
Лекарственная форма
Лиофилизат для приготовления раствора для подкожного введения 7,5 мг, 22,5 мг, 45 мг.
Условия хранения
Хранить в оригинальной упаковке в недоступном для детей месте при соблюдении температурного режима 2–8 °C.
Срок годности
Составляет 2 года. Не использовать по его истечении. Приготовленный раствор сохраняет свойства и эффективность в течение 30 минут при температуре 25 °C.
Особые условия
При неправильном приготовлении раствора для подкожного введения может наблюдаться отсутствие клинической эффективности.
Элигард должен применяться под наблюдением врача, имеющего опыт применения противоопухолевой терапии.
Ответ на терапию препаратом Элигард необходимо контролировать по клиническим параметрам и измерению концентрации простат-специфического антигена (ПСА) в сыворотке крови. Результаты клинических исследований показали, что концентрация тестостерона увеличивается в первые 3 дня лечения у большинства пациентов без орхиэктомии, а затем снижается до уровня медикаментозной кастрации в течение 3–4 недель. Впоследствии данные показатели остаются неизменными при продолжении терапии лекарственным препаратом. В случае если ответ пациента на терапию является недостаточным, необходимо убедиться, что концентрация тестостерона в сыворотке крови достигла или остается на кастрационном уровне.
Андрогенная депривационная терапия может удлинять интервал QT. Перед назначением препарата Элигард врачи должны оценивать соотношение пользы и риска (включая возникновение желудочковой тахикардии типа «пируэт») у пациентов с анамнезом или факторами риска удлинения интервала QT, принимающих препараты, которые могут удлинять интервал QT.
Заболевания сердечно-сосудистой системы:
Сообщалось о повышенном рирке развития инфаркта миокарда, внезапной сердечной смерти и инсульта при приеме мужчинами препаратов-агонистов ГнРГ. Такой риск не подкреплен достаточным количеством результатов в пределах обобщенного соотношения показателей, поэтому его следует внимательно оценивать вместе с риском развития сердечно-сосудистых заболеваний при принятии решения о выборе метода лечения для пациентов, страдающих раком простаты. Пациенты, принимающие препараты-агонисты ГнРГ, должны проходить обследование на предмет появления симптомов и признаков, свидетельствующих о развитии сердечно-сосудистых заболеваний, а также проходить лечение, основанное на современных принципах клинической практики.
Временное повышение содержания тестостерона:
Элигард, как и другие препараты-агонисты ГнРГ, в течение первой недели лечения вызывает кратковременное повышение концентрации тестостерона, дигидротестостерона и кислой фосфатазы в сыворотке крови, в связи с чем у пациентов могут усилиться симптомы или возникнуть новые, такие как боль в костях, неврологические расстройства, гематурия, обструкция мочеточника или инфравезикальная обструкция. Эти симптомы обычно проходят при продолжении терапии. Дополнительное применение соответствующего антиандрогена за три дня до начала терапии Элигардом и продолжение его приема в течение первых двух или трех недель лечения предупреждает последствия первоначального повышения концентрации тестостерона. После выполнения кастрации хирургическим путем применение Элигарда не приводит к дальнейшему снижению тестостерона в сыворотке крови.
Изменения плотности костей:
В публикациях отмечалось уменьшение плотности костей у мужчин после орхиэктомии или терапии агонистом ГнРГ.
Антиандрогенная терапия значительно повышает риск переломов костей в результате возникновения остеопороза. Информация по данному вопросу в настоящее время ограничена. Переломы, связанные с развитием остеопороза, отмечались у 5% пациентов, получавших антиандрогенную терапию на протяжении 22 месяцев, а также у 4% больных при продолжительности лечения от 5 до 10 лет. В целом риск переломов костей в результате возникновения остеопороза выше такового для патологических переломов. Помимо продолжительного дефицита тестостерона, на развитие остеопороза могут влиять преклонный возраст, курение, употребление алкоголя, лишний вес и недостаточные физические нагрузки.
Гипофизарная апоплексия:
В течение пострегистрационного периода применения препарата редко поступали сообщения о случаях возникновения гипофизарной апоплексии (клинический синдром, возникающий после инфаркта гипофиза), у большинства пациентов симптомы проявлялись после приема препаратов-агонистов ГнРГ через 2 недели после приема первой дозы, у некоторых — в течение первого часа. В данном случае гипофизарная апоплексия проявляется в виде таких симптомов, как головная боль, рвота, нарушение зрения, офтальмоплегия, изменение психического состояния и сердечно-сосудистой недостаточности, и требует немедленного оказания медицинской помощи.
Гипергликемия и сахарный диабет:
Гипергликемия и повышенный риск развития сахарного диабета отмечались у мужчин, принимавших препараты-агонисты ГнРГ. Гипергликемия может свидетельствовать о развитии сахарного диабета или ухудшении гликемического контроля у пациентов с сахарным диабетом. Следует периодически проводить мониторинг концентрации глюкозы в крови и/или гликированного гемоглобина (HbA1с) у пациентов, принимающих препараты-агонисты ГнРГ, а также осуществлять подбор необходимых современных методов лечения гипергликемии или сахарного диабета.
Судороги:
В течение пострегистрационного периода поступали сообщения о возникновении судорог у пациентов, получавших лечение лейпрорелина ацетатом, при наличии или отсутствии в анамнезе предрасполагающих факторов. При судорогах следует проводить лечение, основанное на современных клинических рекомендациях.
Другие явления:
При применении агонистов ГнРГ сообщалось также о случаях возникновения обструкции мочевыводящих путей и компрессии спинного мозга, что может привести к параличу как с развитием осложнений со смертельным исходом, так и без них. В случае компрессии спинного мозга или развитии нарушения функции почек следует назначать стандартную терапию этих осложнений.
За пациентами с метастазами в позвоночнике или головном мозге, а также за пациентами с обструкцией мочевыводящих путей следует вести тщательное наблюдение в течение нескольких первых недель лечения.
Из-за наличия таких нежелательных реакций, как повышенная усталость, головокружение и нарушения зрения, следует избегать ситуаций, требующих повышенной концентрации внимания и быстрой реакции. Речь идет об управлении автомобилем и других опасных видах деятельности.
Условия отпуска из аптек
Возможно приобретение Элигарда только при наличии рецептурного бланка.
1 шприц А содержит:
активное вещество: нет
вспомогательные вещества: растворитель, состоящий из:
| Название компонента | Дозировка 7,5 мг | Дозировка 22,5 мг | Дозировка 45 мг |
| Сополимер поли-D,L- лактид- ко- гликолид: ПЛГХ (50:50) ПЛГ (75:25) ПЛГ (85:15) |
117 мг — — |
— 206 мг — |
— |
| N-метил-2- пирролидон | 226 мг | 251 мг | 217 мг |
1 шприц Б содержит:
активное вещество: лейпрорелина ацетат*
дозировка 7,5 мг: 10,6 мг
дозировка 22,5 мг: 29,2 мг
дозировка 45 мг: 59,2 мг
вспомогательные вещества: нет
*Избыток лейпрорелина ацетата компенсирует потери в шприце и игле. Восстановленный раствор (вводимая доза) содержит 7,5 мг, 22,5 мг или 45 мг лейпрорелина ацетата.
Шприц А (растворитель)
Дозировка 7,5 мг: От светло-желтой до светло-желтой с коричневатым оттенком прозрачная, вязкая жидкость, без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Дозировки 22,5 мг и 45 мг: От бесцветной до светло-желтой, прозрачная, вязкая жидкость, без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Шприц Б (лиофилизат лейпрорелина ацетата)
Лиофилизат от белого до почти белого цвета, без видимых посторонних частиц.
Восстановленный раствор
Дозировка 7,5 мг: от светло-желтой до светло-желтой с коричневатым оттенком вязкая жидкость без видимых посторонних частиц. Допускается наличие пузырьков воздуха. Дозировки 22,5 мг и 45 мг: от бесцветной до светло-желтого цвета вязкая жидкость без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Противоопухолевое средство, гонадотропин-рилизинг гормона аналог.
Код ATX
L02A Е02
Фармакодинамика
Лейпрорелин является синтетическим непептидным аналогом естественного гонадотропин-рилизинг-гормона (ГнРГ), который при длительном применении ингибирует секрецию гипофизарного гонадотропина и подавляет тестикулярный стероидогенез у мужчин. Аналог обладает большей эффективностью, чем естественный гормон и его воздействие обратимо при прекращении лечения. Однако время восстановления концентрации тестостерона может варьировать среди пациентов.
Назначение лейпрорелина сначала приводит к повышению уровня циркулирующего лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ), в результате чего временно повышается уровень гонадных стероидов, тестостерона и дигидротестостерона у мужчин. При продолжительном применении лейпрорелина уровень ЛГ и ФСГ снижается. У мужчин уровень тестостерона снижается до кастрационного уровня (? 50 нг/дл) в течение 3 — 5 недель после начала лечения. Средний уровень тестостерона через 6 месяцев лечения составляет 6,1 (± 0,4) нг/дл для дозировки 7,5 мг; 10,1 (± 0,7) нг/дл для дозировки 22,5 мг и 10.4 (± 0,53) нг/дл для дозировки 45 мг. Эти значения сопоставимы с уровнем тестостерона после выполнения билатеральной орхиэктомии. Все пациенты в клиническом исследовании Элигарда 7,5 мг достигли кастрационных уровней тестостерона на 6 неделе лечения; 94% пациентов — к 28 дню и 98% пациентов — к 35 дню. Все пациенты в клиническом исследовании Элигарда 22.5 мг достигли кастрационных уровней тестостерона на 5 неделе; 99% пациентов — к 28 дню. Все пациенты (за исключением одного) в клиническом исследовании Элигарда 45 мг достигли кастрационных уровней тестостерона на 4 неделе. У подавляющего большинства пациентов концентрации тестостерона уменьшались ниже 20 нг/дл, хотя полноценное преимущество данных низких уровней тестостерона пока еще не было установлено. Концентрации ПСА снизились на 94% через 6 месяцев лечения при использовании Элигарда 7,5 мг, на 98% — при использовании Элигарда 22,5 мг, на 97% — при использовании Элигарда 45 мг.
Длительные исследования показали, что постоянная терапия поддерживает концентрацию тестостерона ниже кастрационного уровня на протяжении до 7 лет и по всей видимости на неопределенный срок.
Фармакокинетика
После первой инъекции через 4-8 часов средний уровень концентрации лейпрорелина (Сmаx), определяемой в сыворотке крови, повышается до 25,3 нг/дл, 127 нг/дл и 82 нг/дл при применении лейпрорелина в дозе 7,5 мг, 22,5 мг и 45 мг соответственно.
После первоначального повышения (фаза плато составляет от 2 до 28 дней для дозировки 7,5 мг; от 3 до 84 дней для дозировки 22,5 мг, от 3 до 168 дней для дозировки 45 мг) уровень лейпрорелина в сыворотке оставался относительно стабильным: 0,28 — 1,67 нг/мл для дозировки 7,5 мг и 0,2 — 2 нг/мл для дозировок 22.5 и 45 мг. Данные о накоплении вещества при повторных инъекциях отсутствуют.
Средний объем распределения в равновесном состоянии после внутривенного однократного введения лейпрорелина здоровым добровольцам мужчинам составлял 27 литров. По данным исследований in vitro связь с белками плазмы составляет от 43% до 49%.
При введении 1 мг лейпрорелина ацетата внутривенно здоровым добровольцам мужчинам выяснилось, что при применении двухкамерной модели средний клиренс составил 8,34 л/ч с конечным периодом полувыведения приблизительно 3 часа.
Исследований по выведению препарата Элигард не проводилось.
Исследований по лекарственному метаболизму препарата Элигард не проводилось.
Гормонозависимый рак предстательной железы.
Повышенная чувствительность к лейпрорелину, другим агонистам ГнРГ или к любому вспомогательному веществу, входящему в состав лекарственной формы.
Хирургическая кастрация.
Противопоказан женщинам и детям.
В качестве единственного лечения у пациентов с раком предстательной железы со сдавлением спинного мозга или наличием метастазов в позвоночник.
Способ применения и дозировка
Элигард должен применяться только под контролем специалиста здравоохранения, имеющего достаточный опыт для оценки эффекта лечения.
Элигард назначают в виде подкожной инъекции один раз в месяц при дозировке 7,5 мг, один раз в три месяца при дозировке 22,5 мг и один раз в шесть месяцев при дозировке 45 мг. Содержимое двух заранее наполненных стерильных шприцев должно быть смешано непосредственно перед подкожным введением препарата Элигард. Введенный раствор образует депо препарата, обеспечивающее постоянное высвобождение лейпрорелина в течение указанного периода. Как правило, терапия распространенного рака предстательной железы с использованием Элигарда предусматривает длительное лечение и не должна прекращаться при наступлении улучшения или ремиссии. Элигард может использоваться в качестве неоадъювантной или адъювантной терапии в сочетании с лучевой терапией у пациентов с локализованным раком высокого риска и местно-распространенным раком простаты.
Место инъекции следует периодически менять. Избегать попадания препарата в артерию или вену.
Коррекция доз для особых популяций пациентов
Клинических данных по применению Элигарда у больных с печеночной или почечной недостаточностью нет.
В случае предполагаемой или известной ошибки при смешивании у пациента должна быть определена концентрация тестостерона в связи с тем, что в результате неправильного приготовления, смешивания или введения препарата могут наблюдаться случаи отсутствия клинической эффективности.
Рекомендации по приготовлению раствора для введения
Если препарат был приготовлен с нарушением инструкций, он не должен использоваться в связи с тем, что при неправильном приготовлении раствора для подкожного введения могут наблюдаться случаи отсутствия клинической эффективности.
Сначала рекомендуется подготовить пациента к введению препарата, а затем приступить к приготовлению раствора в соответствии с рекомендациями, представленными ниже.
Упаковку достают из холодильника примерно за 30 минут до использования и выдерживают при комнатной температуре.
После извлечения из холодильника препарат может храниться в оригинальной упаковке при комнатной температуре (не выше 25 °С) до 4 недель.
Шаг 1
Извлеките из коробки две контурные ячейковые упаковки и откройте их, потянув за свободный край алюминиевой фольги, извлеките содержимое ячейковых упаковок (рис. 1.1 и 1.2) и положите на чистую поверхность. Выбросьте пакетики с влагопоглотителем.
Шаг 2
Возьмите шприц Б и извлеките из него короткий поршень синего цвета вместе с ограничителем (не выкручивайте поршень из ограничителя) (рис. 2).
Не смешивайте содержимое шприцев пока синий короткий поршень не будет извлечен из шприца Б.
Шаг 3
Возьмите белый поршень для шприца Б и вставьте его в шприц Б со стороны оставшегося серого ограничителя (рис. 3, шаг 1), проверните поршень по часовой стрелке до ограничителя (рис.З, шаг 2).
Шаг 4
Снимите серый резиновый колпачок со шприца Б и отложите шприц (рис. 4).
Шаг 5
Возьмите шприц А и, удерживая его в вертикальном положении, чтобы избежать протечки растворителя, открутите прозрачный колпачок со шприца А (рис. 5).
Шаг 6
Соедините два шприца, шприц А снизу, и вкрутите шприц Б в шприц А по часовой стрелке до полной фиксации (рисунки 6а, 6б). Не закручивайте шприцы слишком плотно.
Шаг 7
Переверните соединенные шприцы так, чтобы шприц Б оказался снизу, и нажмите на поршень шприца А до момента полного ввода содержимого шприца А (растворитель) в шприц Б (содержащий порошок лейпрорелина ацетата), шприцы держите вертикально (рис. 7).
Шаг 8
Держа шприцы в строго горизонтальном положении, тщательно перемешайте содержимое обоих шприцев, поочередно нажимая осторожным движением на поршень то одного то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного вязкого раствора (рис. 8).
Избегайте перегиба системы (помните, что это может стать причиной протечки, поскольку шприцы могут быть недостаточно плотно закручены).
После тщательною перемешивания готовая к применению смесь должна быть бесцветной или светло-желтой (может наблюдаться опенок белого или бледно-желтого).
Важно: Необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать готовый продукт запрещено.
Помните: Препарат нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
Шаг 9
Держите шприцы вертикально, шприц Б — снизу. Шприцы должны быть надежно закреплены. Нажимая на поршень шприца А, и слегка оттягивая вниз поршень шприца Б, переместите все содержимое в шприц Б (рис. 9).
Шаг 10
Выверните шприц А, продолжая нажимать на поршень шприца А (рис. 10). Убедитесь, что содержимое не вытекает из шприца, поскольку вы не сможете закрепить иглу надлежащим образом в случае утечки.
Шаг 11
Держите шприц Б вертикально. Откройте упаковку со стерильной иглой (отогнув бумажную этикетку) и извлеките иглу. Приставьте картридж иглы к основанию шприца Б и аккуратно соедините, закручивая иглу по часовой стрелке (рис. 11).
Не перетягивайте.
Шаг 12
Перед инъекцией снимите защитный колпачок с иглы (рис. 12).
Важно: не приводите в действие защитное устройство иглы до введения препарата.
Шаг 13
До начала введения удалите большие пузырьки воздуха из шприца Б. Введите препарат подкожно. Пожалуйста, убедитесь в том, что введен весь препарат из шприца Б.
Шаг 14
После инъекции незамедлительно активируйте защитное устройство иглы любым из двух способов, описанных ниже.
1 способ
Закрытие на плоской поверхности.
Положите шприц с иглой на плоскую поверхность вниз рычагом защитного устройства и нажатием на рычаг активируйте защитный механизм (рис. 14.1а) Затем переведите рычаг в переднее положение до тех пор, пока кончик иглы не будет полностью закрыт. Убедитесь, что рычаг переведен в крайнее положение и кончик иглы полностью закрыт (до характерного щелчка) (рис. 14.1б).
2 способ
Закрытие рукой.
Поместите большой палец на рычаг, слегка надавите на него по направлению к кончику иглы с переводом рычага в крайнее переднее положение до тех пор, пока кончик иглы не будет полностью закрыт (рис. 14.2а-2б).
Убедитесь, что рычаг переведен в крайнее положение и кончик иглы полностью закрыт (до характерного щелчка) (рис. 14.2б).
Шаг 15
Немедленно поместите иглу и шприц в соответствующий контейнер для острых предметов.
Нежелательные явления, вызванные приемом препарата Элигард, обусловлены главным образом специфическим фармакологическим действием лейпрорелина, вызывающим увеличение и снижение уровня гормонов. Самыми распространенными побочными эффектами являлись: «приливы», недомогание, тошнота и слабость, местное раздражение в месте введения препарата. Слабые или умеренные «приливы» наблюдались у приблизительно 58% пациентов.
Следующие нежелательные явления были зафиксированы во время проведения клинических исследований препарата Элигард у пациентов с распространенным раком предстательной железы. Частота побочных реакций, приведенных ниже, изложена в соответствии со следующей градацией: очень часто (>1/10), часто (> 1/100, < 1/10); нечасто (> 1/1000, < 1/100); редко (>1/10000, <1/1000); очень редко (< 1/10000), неизвестно (невозможно оценить на основании имеющихся данных).
Таблица 1
Нежелательные явления в ходе клинических исследований препарата Элигард
|
Инфекционные и паразитарные заболевания |
|
| часто | назофарингит |
| нечасто | инфекция мочевыводящих путей, ограниченная инфекция кожных покровов |
| Нарушения питания и обмена веществ | |
| нечасто | ухудшение течения сахарного диабета |
| Психические нарушения | |
| нечасто | нарушения сна, депрессия, снижение либидо |
| Нарушения со стороны нервной системы | |
| нечасто | головокружение, головная боль, гипестезия, бессонница, нарушение вкусовых ощущений, нарушение обоняния |
| редко | непроизвольные патологические движения |
| Нарушения со стороны сердца | |
|
Не известно |
удлинение интервала QТ |
| Нарушения со стороны сосудистой системы | |
|
очень часто |
«приливы» |
| нечасто | повышение артериального давления, снижение артериального давления |
| редко | обморок, коллапс |
| Респираторные, торакальные и медиастинальные нарушения | |
| нечасто | ринорея, диспноэ |
| Нарушения со стороны пищеварительной системы | |
| часто | тошнота, диарея |
| нечасто | запор, сухость во рту, диспепсия, рвота |
| редко | метеоризм, отрыжка |
| Нарушения со стороны кожи и подкожной клетчатки | |
|
очень часто |
экхимозы, эритема |
|
часто |
зуд, ночная потливость |
|
нечасто |
холодный пот, повышенное потоотделение |
| редко | алопеция, кожный зуд |
| Нарушения со стороны костно-мышечной системы и соединительной ткани | |
|
часто |
артралгия, боль в конечностях, миалгия |
| нечасто | боли в спине, мышечные судороги |
| Нарушения со стороны мочевыделительной системы | |
|
часто |
нарушение мочеиспускания, затрудненное мочеиспускание, дизурия, никтурия, олигурия |
| нечасто | спазм мочевого пузыря, гематурия, увеличение частоты мочеиспускания, задержка мочеиспускания |
|
Нарушения со стороны репродуктивной системы и молочной железы |
|
|
часто |
болезненность грудных желез, боль в яичках, гипертрофия грудных желез, атрофия яичек, бесплодие |
|
нечасто |
гинекомастия, импотенция, тестикулярные нарушения |
| редко | боль в грудной железе |
|
Системные нарушения и осложнения в месте введения |
|
|
очень часто |
повышенная утомляемость, жжение в месте введения, парестезия в месте введения |
|
часто |
недомогание, боль в месте введения, кровоподтек, жжение, мышечная ригидность, слабость |
|
нечасто |
зуд в месте введения, летаргия, болевые ощущения, пирексия |
|
редко |
образование язвы в месте введения |
| очень редко | некроз в месте введения |
|
Нарушения со стороны крови и лимфатической системы |
|
| часто |
гематологические изменения (отклонение от нормы количества клеток крови, отклонение от нормы показателя МНО (международное нормализованное отношение)) |
| Отклонения от нормы, выявленные в лабораторных исследованиях | |
| часто | повышение концентрации креатинина и активности креатинфосфокиназы, увеличение времени коагуляции |
|
нечасто |
повышение активности аланинаминотрансферазы, гипертриглицеридемия, увеличение протромбинового времени, увеличение веса |
К другим нежелательным явлениям при приеме лейпрорелина ацетата относятся: периферический отек, эмболия легких, ощущение сердцебиения, миалгия, мышечная слабость, нарушение кожной чувствительности, озноб, головокружение, зуд, амнезия и нарушение зрения. Редко поступали сообщения о случаях возникновения инфаркта, вызванного гипофизарной апоплексией после приема антагонистов ГнРГ краткосрочного и длительного действия. Также были зафиксированы случаи возникновения тромбоцитопении и лейкопении, изменения толерантности к глюкозе.
Местные реакции после введения препарата Элигард такие же, как и при подкожном введении других препаратов.
В целом, местные реакции после введения препарата носят умеренный характер и являются краткосрочными.
Изменения в плотности костей
В публикациях отмечалось уменьшение плотности костей у мужчин после орхиэктомии или терапии аналогами ГнРГ. Можно предположить, что долгосрочная терапия лейпрорелином приводит к усилению симптомов остеопороза, что повышает риск переломов.
Усиление симптомов и признаков заболевания
Терапия лейпрорелина ацетатом может привести к усилению симптомов заболевания в течение первых недель лечения. В случае заболеваний с метастазами в позвоночник и/или обструкцией мочевых путей или гематурией, возможно возникновение таких неврологических осложнений, как слабость и/или парестезия нижних конечностей или ухудшение симптомов нарушения мочеиспускания.
Данных относительно передозировки у людей не имеется. В случае передозировки больному следует назначить симптоматическое лечение.
Взаимодействие с другими лекарственными препаратами и другие формы взаимодействия
Исследований по изучению фармакокинетического взаимодействия препарата Элигард с другими препаратами не проводилось. О взаимодействии Элигарда с другими лекарственными препаратами не сообщалось.
В связи с тем, что андрогенная депривация может удлинять интервал QТ, должно быть тщательно взвешено одновременное применение препарата Элигард с другими препаратами, удлиняющими интервал QТ, или препаратами, способными вызывать желудочковую тахикардию типа «пируэт», такими как антиаритмические препараты класса IА (например, хинидин, дизопирамид) или класса III (например, амиодарон, соталол, дофетилид, ибутилид), метадон, моксифлоксацин, нейролептики и т.д.
При неправильном приготовлении раствора для подкожного введения могут наблюдаться случаи отсутствия клинической эффективности. Элигард должен применяться под наблюдением врача, имеющего опыт применения противоопухолевой терапии.
Ответ на терапию препаратом Элигард необходимо контролировать по клиническим параметрам и измерению концентрации простат-специфического антигена (ПСА) в сыворотке крови. Результаты клинических исследований показали, что концентрация тестостерона увеличивается в первые 3 дня лечения у большинства пациентов без орхиэктомии, а затем снижается до уровня медикаментозной кастрации в течение 3-4 недель. Впоследствии данные показатели остаются неизменными при продолжении терапии лекарственным препаратом. В случае, если ответ пациента на терапию является недостаточным, необходимо убедиться, что концентрация тестостерона в сыворотке крови достигла или остается на кастрационном уровне.
Андрогенная депривационная терапия может удлинять интервал QТ. Перед назначением препарата Элигард врачи должны оценивать соотношение пользы и риска (включая возникновение желудочковой тахикардии типа «пируэт») у пациентов с анамнезом или факторами риска удлинения интервала QТ, принимающих препараты, которые могут удлинять интервал QТ.
Элигард, как и другие препараты-агонисты ГнРГ, в течение первой недели лечения вызывает кратковременное повышение концентрации тестостерона, дигидротестостерона и кислой фосфатазы в сыворотке крови, в связи с чем у пациентов могут усилиться симптомы или возникнуть новые, такие как боль в костях, неврологические расстройства, гематурия, обструкция мочеточника или инфравезикальная обструкция. Эти симптомы обычно проходят при продолжении терапии.
Дополнительное назначение соответствующего антиандрогена за три дня до начала терапии Элигардом и продолжение его приема в течение первых двух или трех недель лечения предупреждает последствия первоначального повышения концентрации тестостерона.
После выполнения кастрации хирургическим путем применение Элигарда не приводит к дальнейшему снижению тестостерона в сыворотке крови.
При применении агонистов ГнРГ сообщалось также о случаях возникновения обструкции мочевых путей и компрессии спинного мозга, что может привести к параличу как с, так и без фатальных осложнений. В случае компрессии спинного мозга или развития почечной недостаточности следует прибегнуть к стандартной терапии.
За пациентами с метастазами в позвоночник и/или головной мозг, а также за пациентами с обструкцией мочевых путей должно вестись тщательное наблюдение в течение первых нескольких недель лечения.
У определенного процента пациентов опухоли резистентны к гормональной терапии. Отсутствие улучшения клинических показателей, несмотря на подавление выработки тестостерона, диагностируется, как отсутствие эффективности при дальнейшей терапии препаратом Элигард.
Антиандрогенная терапия значительно повышает риск переломов костей в результате возникновения остеопороза. Информация по данному вопросу в настоящее время ограничена. Переломы, связанные с развитием остеопороза, отмечались у 5% пациентов, получавших антиандрогенную терапию на протяжении 22 месяцев, а также у 4% больных при продолжительности лечения от 5 до 10 лет. В целом, риск переломов костей в результате возникновения остеопороза выше такового для патологических переломов. Помимо продолжительного дефицита тестостерона на развитие остеопороза может влиять преклонный возраст, курение, потребление алкоголя, лишний вес и недостаточные физические нагрузки.
В течение пострегистрационного периода применения препарата, поступали сообщения о случаях возникновения гипофизарной апоплексии (редко) (клинический синдром, возникающий после инфаркта гипофиза), у большинства пациентов симптомы проявлялись после приема препаратов-агонистов ГнРГ через 2 недели после приема первой дозы, у некоторых — в течение первого часа. В данном случае, гипофизарная апоплексия проявляется в виде таких симптомов как головная боль, рвота, нарушение зрения, офтальмоплегия, изменение психического состояния и сердечнососудистой недостаточности и требует немедленного оказания медицинской помощи.
Гипергликемия и сахарный диабет: гипергликемия и повышенный риск развития сахарного диабета отмечались у мужчин, принимавших препараты-агонисты ГнРГ. Гипергликемия может свидетельствовать о развитии сахарного диабета или ухудшении гликемического контроля у пациентов с сахарным диабетом. Следует периодически производить мониторинг концентрации глюкозы в крови и/или гликированного гемоглобина (НЬА1с) у пациентов, принимающих препараты-агонисты ГнРГ, а также осуществлять подбор необходимых современных методов лечения гипергликемии или сахарного диабета.
Заболевания сердечно-сосудистой системы: сообщалось о повышенном риске развития инфаркта миокарда, внезапной сердечной смерти и инсульта при приеме мужчинами препаратов-агонистов ГнРГ. Такой риск не подкреплен достаточным количеством результатов в пределах обобщенного соотношения показателей, поэтому его следует внимательно оценивать вместе с риском развития сердечно-сосудистых заболеваний при принятии решения о выборе метода лечения для пациентов, страдающих раком простаты. Пациенты, принимающие препараты-агонисты ГнРГ, должны проходить обследование на предмет появления симптомов и признаков, свидетельствующих о развитии сердечно-сосудистых заболеваний, а также проходить лечение, основанное на современных принципах клинической практики.
Влияние на способность водить автомобиль и управлять механизмами
Некоторые побочные действия препарата, такие как повышенная усталость, головокружение, нарушения зрения, могут отрицательно влиять на способность к управлению автомобилем и выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Лиофилизат для приготовления раствора для подкожного введения 7,5 мг, 22,5 мг, 45 мг.
Два стерильных заранее наполненных шприца из полипропилена или сополимера циклического олефина, в одном (шприц Б) содержится лиофилизат лейпрорелина ацетата (10,6 мг для дозировки 7,5 мг; 29,2 мг для дозировки 22,5 мг, 59,2 мг для дозировки 45 мг), в другом (шприц А) — растворитель (343 мг для дозировки 7,5 мг; 457 мг для дозировки 22,5 мг; 434 мг для дозировки 45 мг). Содержимое двух шприцев представляет собой комбинированную систему.
Шприц А вместе с поршнем для шприца Б и пакетиком с влагопоглотителем помещен в контурную ячейковую упаковку из полиэфира, покрытую алюминиевой фольгой ламинированной.
Шприц Б вместе с иглой инъекционной и пакетиком с влагопоглотителем помещен в контурную ячейковую упаковку из полиэфира, покрытую алюминиевой фольгой ламинированной.
По одной контурной ячейковой упаковке со шприцом А в комплекте с поршнем для шприца Б и пакетиком с влагопоглотителем и по одной контурной ячейковой упаковке со шприцом Б в комплекте с иглой инъекционной и пакетиком с влагопоглотителем вместе с инструкцией в картонной пачке.
При температуре от 2 °С до 8 °С в оригинальной упаковке.
Хранить в недоступном для детей месте.
2 года.
Не использовать препарат по истечении срока годности, указанного на упаковке.
Готовый раствор стабилен химически и физически в течение 30 минут при температуре 25 °С.
Условия отпуска из аптек
По рецепту.
Владелец регистрационного удостоверения
«Астеллас Фарма Юроп Б.В.», Нидерланды Силвиусвег 62, 2333 ВЕ, Лейден, Нидерланды
Производитель
Шприц А: «Толмар Инк.», США
Шприц Б: «Толмар Инк.», США или
«Кангене биоФарма Инк.», США
Упаковщик (вторичная упаковка)
Толмар Инк., США или
Астеллас Фарма Юроп Б.В., Нидерланды
Выпускающий контроль качества
МедиГене АГ, Германия или
Астеллас Фарма Юроп Б.В., Нидерланды
Претензии по качеству направлять по адресу
Представительство Частной компании с ограниченной ответственностью «Астеллас Фарма Юроп Б.В.» (Нидерланды)
г. Москва: 109147, Россия, г. Москва, Марксистская ул., 16 «Мосаларко Плаза-1» бизнес-центр, этаж 3.