Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Иммунодепрессант, ингибитор передачи пролиферативного сигнала. Иммуносупрессивное действие обусловлено ингибированием антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими интерлейкинами Т-клеток, например, интерлейкином-2 и интерлейкином-15. Эверолимус ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием этих факторов роста Т-клеток с соответствующими рецепторами. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
На молекулярном уровне эверолимус образует комплекс с цитоплазматическим белком FKBP-12. В присутствии эверолимуса происходит ингибирование фосфорилирования р70 S6 киназы, стимулируемой фактором роста. Поскольку фосфорилирование р70 S6 киназы находится под контролем FRAP (так называемого m-TOR ), эти данные позволяют предположить, что комплекс эверолимус-РКВР-12 связывается с FRAP. FRAP — это ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией; нарушение функции FRAP, таким образом, объясняет остановку клеточного цикла, вызываемую эверолимусом. Эверолимус имеет, таким образом, отличный от циклоспорина механизм действия. В доклинических моделях аллотрансплантации была показана более высокая эффективность комбинации эверолимуса с циклоспорином, чем при изолированном использовании каждого из них.
Помимо влияния на Т-клетки, эверолимус ингибирует стимулируемую факторами роста пролиферацию как гемопоэтических, так и негемопоэтических клеток (например, гладкомышечных клеток). Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, которая запускается при повреждении эндотелиальных клеток и приводит к образованию неоинтимы, играет ключевую роль в патогенезе хронического отторжения.
Эверолимус является активным ингибитором роста и пролиферации опухолевых клеток, эндотелиальных клеток, фибробластов и гладкомышечных клеток кровеносных сосудов.
У пациентов с распространенным и/или метастатическим почечно-клеточным раком, прогрессирующим после предшествующей терапии ингибиторами тирозиновых киназ и/или цитокинами, эверолимус достоверно снижал риск прогрессирования заболевания и смерти больных на 67%. При применении эверолимуса выживаемость больных без прогрессирования заболевания составила 4.9 месяцев. В течение 6 месяцев у 36% больных, получавших эверолимус, не отмечалось прогрессирования заболевания. Считается, что применение эверолимуса позволяет значительно улучшить качество жизни пациентов (оценивалось влияние симптомов заболевания на различные сферы жизни пациента).
Фармакокинетика
После приема внутрь Cmax достигается через 1-2 ч. У пациентов после пересадки концентрация эверолимуса в крови пропорциональна дозе в диапазоне доз от 0.25 мг до 15 мг.
Соотношение концентрации эверолимуса в крови и его концентрации в плазме находится в пределах от 17% до 73% и зависит от значений концентрации в диапазоне от 5 до 5000 нг/мл. У здоровых добровольцев и пациентов с умеренными нарушениями функции печени связывание с белками плазмы составляет приблизительно 74%. Vd в конечной фазе у пациентов после трансплантации почки, находящихся на поддерживающей терапии, составляет 342±107 л.
Эверолимус является субстратом CYP3A4 и Р-гликопротеина. Основными путями метаболизма, выявленными у человека, были моногидроксилирование и O-деалкилирование. Два основных метаболита образуются путем гидролиза циклического лактона. Ни один из них не имеет существенной иммуносупрессивной активности. В системном кровотоке находится в основном эверолимус.
После введения однократной дозы меченого радиоактивной меткой эверолимуса пациентам после трансплантации, получающим циклоспорин, большая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось с мочой. Неизмененное вещество не определялось ни в моче, ни в кале.
У пациентов с умеренно выраженными нарушениями функции печени (класс В по шкале Чайлд-Пью) AUC эверолимуса увеличивалась. Показатель AUC положительно коррелировал с концентрацией сывороточного билирубина и увеличением протромбинового времени и отрицательно коррелировал с концентрацией сывороточного альбумина. Если концентрация билирубина составляла > 34 мкмоль/л, протромбиновое время >1.3 INR (пролонгирование > 4 сек) и/или концентрация альбумина составляла < 35 г/л, то наблюдалась тенденция к увеличению показателя AUC у пациентов с умеренно выраженной печеночной недостаточностью. При тяжелой печеночной недостаточности (класс С по шкале Чайлд-Пью) изменения AUC не изучены, но, вероятно, они такие же или более выраженные, чем при умеренной печеночной недостаточности.
Клиренс эверолимуса повышался в линейной зависимости от возраста пациента (от 1 до 16 лет), площади поверхности тела (0.49-1.92 м2) и массы тела (11-77 кг). В равновесном состоянии клиренс составлял 10.2±3.0 л/ч/м2, T1/2 — 30±11 ч.
У реципиентов почки и сердца в течение 6 мес после трансплантации была выявлена связь между базальной концентрацией эверолимуса и частотой подтвержденного биопсией острого отторжения и тромбоцитопении.
Показания активного вещества
ЭВЕРОЛИМУС
Профилактика отторжения трансплантата почки и сердца у взрослых реципиентов с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию (циклоспорин и ГКС).
Распространенный и/или метастатический почечно-клеточный рак (при неэффективности антиангиогенной терапии).
Режим дозирования
Принимают внутрь.
В качестве средства профилактики отторжения трансплантата рекомендуемая начальная доза для взрослых с почечными и сердечными трансплантатами составляет по 750 мкг 2 раза/сут. Применение следует начинать как можно скорее после трансплантации. Принимают в одно и то же время с циклоспорином в специальной лекарственной форме. Может потребоваться коррекция режима дозирования эверолимуса с учетом достигнутых концентраций в плазме крови, переносимости, индивидуального ответа на лечение, изменений сопутствующей медикаментозной терапии и клинической ситуации. Коррекцию режима дозирования можно проводить с интервалами 4-5 дней.
В качестве противоопухолевого средства применяют в дозе 10 мг 1 раз/сут ежедневно. Лечение проводят до тех пор, пока сохраняется клинический эффект. При развитии тяжелых и/или труднопереносимых побочных реакций следует снизить дозу до 5 мг/сут и/или временно прекратить терапию. При применении одновременно с умеренными ингибиторами CYP3A4 и ингибиторами Р-гликопротеина дозу эверолимуса следует уменьшить до 5 мг/сут. При развитии тяжелых и/или труднопереносимых побочных реакций у пациентов, получающих препарат одновременно с умеренными ингибиторами CYP3A4 и ингибиторами Р-гликопротеина, дозу эверолимуса следует уменьшить до 5 мг/сут через день. При одновременном применении эверолимуса с сильными индукторами CYP3A4 или индукторами Р-гликопротеина доза может быть повышена постепенно с 10 мг/сут до 20 мг/сут (величина пошагового увеличения дозы — 5 мг). При прекращении терапии сильными индукторами CYP3A4 или индукторами Р-гликопротеина эверолимус следует применять в дозе, которая применялась до начала лечения индукторами CYP3A4 или индукторами Р-гликопротеина.
У пациентов с нарушениями функции печени умеренной степени (класс В по классификации Чайлд-Пью) дозу следует уменьшить до 5 мг/сут.
Побочное действие
Со стороны системы кроветворения и лимфатической системы: очень часто — лейкопения; часто — тромбоцитопения, анемия, коагулопатия, тромботическая тромбоцитопеническая пурпура/гемолитический уремический синдром; иногда — гемолиз.
Со стороны эндокринной системы: иногда — гипогонадизм у мужчин (снижение уровня тестостерона, повышение уровня ЛГ).
Со стороны обмена веществ: очень часто — гиперхолестеринемия, гиперлипидемия; часто — гипертриглицеридемия.
Со стороны сердечно-сосудистой системы: часто — повышение АД, лимфоцеле, венозный тромбоз.
Со стороны дыхательной системы: часто — пневмония; иногда — пневмонит.
Со стороны пищеварительной системы: часто — боли в животе, диарея, тошнота, рвота; иногда — гепатит, нарушения функции печени, желтуха, повышение АЛТ, ACT , ГГТ.
Со стороны кожи и подкожной клетчатки: часто — ангионевротический отек, акне, осложнения со стороны хирургической раны; иногда — сыпь.
Со стороны костно-мышечной системы: иногда — миалгия.
Со стороны мочевыделительной системы: часто — инфекции мочевых путей; иногда — некроз почечных канальцев, пиелонефрит.
Прочие: часто — отек, боль, вирусные, бактериальные и грибковые инфекции, сепсис; иногда — раневая инфекция.
В контролируемых клинических исследованиях, в которых пациентов наблюдали не менее одного года, сообщалось о возникновении лимфом или лимфопролиферативного заболевания в 1.4% случаев при применении эверолимуса с другими иммунодепрессантами; злокачественные новообразования кожи (1.3%); другие типы малигнизации (1.2%).
Противопоказания к применению
Повышенная чувствительность к эверолимусу, сиролимусу.
Применение при беременности и кормлении грудью
Данные по применению при беременности отсутствуют. Не следует применять эверолимус при беременности за исключением тех случаев, когда ожидаемая польза для матери превышает потенциальный риск для плода.
Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения и в течение 8 недель после окончания терапии.
Неизвестно, выделяется ли эверолимус с грудным молоком у человека. При необходимости применения эверолимуса в период лактации следует решить вопрос о прекращении грудного вскармливания.
В экспериментальных исследованиях показано наличие токсического влияния на репродуктивность, включая эмбриотоксичность и фетотоксичность. Неизвестно, существует ли потенциальный риск для человека. Показано, что эверолимус и/или его метаболиты быстро проникали в молоко лактирующих крыс.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени умеренной степени (класс В по классификации Чайлд-Пью) дозу следует уменьшить до 5 мг/сут. Эверолимус не изучен у пациентов с тяжелой печеночной недостаточностью. Рекомендуется тщательно мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
Применение при нарушениях функции почек
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Особые указания
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Не рекомендуется одновременное применение с сильными ингибиторами CYP3A4 (например, кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (например, рифампицин, рифабутин), за исключением случаев, когда ожидаемая польза такой терапии превышает потенциальный риск. Рекомендуется контролировать концентрации эверолимуса в цельной крови при одновременном применении с индукторами или ингибиторами CYP3A4 и после их отмены.
Эверолимус не изучен у пациентов с тяжелой печеночной недостаточностью. Рекомендуется тщательно мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
В период лечения следует контролировать состояние пациентов для выявления кожных новообразований. Следует регулярно контролировать состояние пациентов для выявления кожных новообразований, рекомендовать сведение к минимуму воздействие ультрафиолетового излучения, солнечного света и использовать соответствующие солнцезащитные средства.
С осторожностью применять у пациентов с гиперлипидемией. В период лечения следует контролировать содержание в крови холестерина и триглицеридов. Следует оценивать соотношение риск/польза продолжения терапии эверолимусом у пациентов с тяжелой рефрактерной гиперлипидемией. Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития нежелательных реакций, вызванных применением указанных лекарственных средств.
Чрезмерная иммуносупрессия предрасполагает к развитию инфекций (в т.ч. оппортунистических). Имеются сообщения о развитии фатальных инфекций и сепсиса.
В течение 3 мес после трансплантации рекомендуется профилактика развития цитомегаловирусной инфекции, особенно у пациентов с повышенным риском ее развития.
Пациентам, получающим ингибиторы ГМГ-КоА-редуктазы, требуется клинический контроль с целью своевременного выявления рабдомиолиза.
В период лечения эверолимусом не следует применять живые вакцины.
Лекарственное взаимодействие
На абсорбцию и последующую элиминацию эверолимуса могут оказывать влияние препараты, взаимодействующие с CYP3A4 и/или Р-гликопротеином. Сочетанное применение эверолимуса с сильными ингибиторами или индукторами CYP3A4 не рекомендуется. Ингибиторы Р-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить концентрацию эверолимуса в сыворотке. In vitro эверолимус являлся конкурентным ингибитором CYP3A4 и CYP2D6, потенциально увеличивающим концентрации в плазме препаратов, выводящихся при участии этих ферментов.
Биодоступность эверолимуса значительно увеличивалась при одновременном применении циклоспорина (ингибитор CYP3A4/Р-гликопротеина).
При изучении лекарственного взаимодействия у здоровых добровольцев, получавших предшествующую терапию многократными дозами рифампицина (индуктор CYP3A4), при последующем применении эверолимуса в однократной дозе наблюдалось почти 3-кратное повышение клиренса эверолимуса и уменьшение Сmax на 58% и AUC — на 63% (данная комбинация не рекомендуется).
Умеренные ингибиторы CYP3A4 и Р-гликопротеина могут повышать концентрацию эверолимуса в крови, в т.ч. противогрибковые средства: флуконазол; антибиотики группы макролидов (эритромицин); блокаторы кальциевых каналов (верапамил, никардипин, дилтиазем); ингибиторы протеазы (нелфинавир, индинавир, ампренавир).
Индукторы CYP3A4 могут повышать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови, в т.ч. зверобой продырявленный, противосудорожные средства (карбамазепин, фенобарбитал, фенитоин); препараты для лечения ВИЧ (эфавиренз, невирапин).
Грейпфрут и грейпфрутовый сок влияют на активность изоферментов CYP и Р-гликопротеина, поэтому следует избегать употребления этих соков на фоне применения эверолимуса.
Поскольку иммунодепрессанты могут оказывать влияние на ответ при вакцинации, на фоне лечения эверолимусом вакцинация может быть менее эффективной.
Новости онкологии
27.08.2012
Эверолимус в практике онколога. Клинические случаи
В настоящей статье представлены клинические случаи победителей конкурса, который проводился Обществом онкологов-химиотерапевтов. Наградой является поездка на конгресс ESMO в Вену.
Опыт применения препарата эверолимус в качестве четвертой линии лекарственной терапии метастатического почечноклеточного рака
А.И. Семенова, С.А. Проценко
ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
Больной ГОВ, 52 года, впервые обратился в НМИЦ онкологии им. Н.Н. Петрова в июле 2005 г. Из анамнеза: 02.09.2005 г. в Санкт-Петербурге по поводу опухоли правой почки (размерами до 12×13 см) выполнена правосторонняя нефрэктомия. Гистологическое заключение – светлоклеточный почечноклеточный рак. По данным дополнительного обследования выявлены множественные метастазы в легких (до 15 мм в диаметре), костях таза, позвонках, правой плечевой кости.
С октября 2005 г. начата первая линия лекарственного лечения интерфероном (по 9 МЕ 3 раза в неделю, внутримышечно) в сочетании с бисфосфонатами, достигнута стабилизация. С сентября 2006 г. выявлено прогрессирование болезни в виде увеличения размеров и количества метастазов в легких. Завершена иммунотерапия интерфероном, начата вторая линия лечения антиэстрогенами в высокой дозе (тамоксифен 120 мг/сут, внутрь). В течение 2 лет (до ноября 2008 г.) сохранялась стабилизация метастатического процесса. По поводу очередного прогрессирования метастазов в легких начата третья линия лекарственного лечения: таргетная терапия сорафенибом (800 мг/сут, внутрь). В марте 2009 г. зарегистрирован частичный регресс в виде уменьшения размеров и количества метастазов в легких, сохранявшийся до августа 2010 г.
По данным КТ органов грудной клетки (от 18.08.2010 г.) – очередное прогрессирование процесса в виде увеличения количества метастазов в легких, появления метастазов в лимфатических узлах средостения. Больному назначена четвертая линия лекарственной терапии эверолимусом (по 10 мг/сут, внутрь). Начал прием препарата с октября 2010 г. В ноябре 2010 г. после незначительной физической нагрузки произошел патологический перелом правой плечевой кости в средней трети, по поводу которого в РНИИТО им. Р.Р. Вредена в феврале 2011 г. выполнена операция остеосинтеза с практически полным восстановлением функции конечности. По поводу метастаза в теле 4-го поясничного позвонка в сентябре 2011 г. произведена пункционная чрезкожная вертебропластика костным цементом.
На момент последнего осмотра в мае 2012 г. больной продолжает прием эверолимуса в прежней дозе, общая продолжительность приема составляет 19 месяцев. Клинически значимых осложнений не отмечено, перерывов в лечении не было. По данным обследования (май 2012 г.) сохраняется стабилизация метастатического процесса в легких. Обращает внимание хорошее качество жизни больного (работоспособен, физически активен, полностью социально адаптирован). Планируется продолжение непрерывного приема эверолимуса (до возникновения серьезных осложнений или исчерпания эффекта лечения).
Эффективность комбинации эверолимуса с анастрозолом в качестве третьей линии гормонотерапии
М.А. Фролова1, А. Мелхем-Бертрандт2
1ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва; 2Онкологический Центр MD Anderson, Хьюстон
Пациентка Х., 44 лет, наблюдается в Онкологическом Центре MD Anderson, Хьюстон, США. В сентябре 2010 г. был диагностирован рак левой молочной железы, T1N2MX. Через месяц была выполнена резекция левой молочной железы с подмышечной лимфаденэктомией. При гистологическом исследовании – инфильтративный протоковый рак 3 степени злокачественности с метастазами в 4 л/лимфатических узлах. При иммуногистохимическом исследовании: ER 90%, PR-, Her2neu-, Ki67 48%. При дополнительном исследовании в MD Anderson были выявлены метастазы в кости. Пациентку беспокоили периодические умеренные боли в спине. В декабре 2010 г. начат прием тамоксифена, инъекции золедроновой кислоты, выполнена овариоэктомия. В мае 2011 г. выявлен новый литический очаг в ключице с патологическим переломом, однако продолжена терапия тамоксифеном.
В июне 2011 г. появились боли в грудном отделе позвоночника. При обследовании обнаружены новые литические очаги в ребрах, грудном отделе позвоночника. Был назначен летрозол, продолжены введения золедроновой кислоты. В августе 2011 г. пациентка отметила усиление болей в спине и ребрах. При обследовании выявлен новый очаг в правой вертлужной впадине. Продолжен прием летрозола, назначены обезболивающие препараты. В сентябре 2011 г. отмечено усиление болей, по поводу чего назначены наркотические аналгетики.
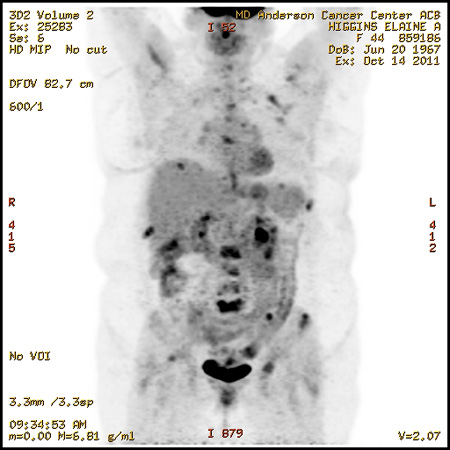
В октябре 2011 г. было зафиксировано прогрессирование заболевания (появление новых очагов в подвздошных костях). Боли перестали купироваться наркотическими аналгетиками. Была проведена лучевая терапия на Th12-L5 позвонки, где локализовался наиболее выраженный болевой синдром. 20.10.11 г. больная была переведена на лечение по схеме эверолимус 10 мг/сут. в сочетании с анастрозолом 1 мг/сут. На момент начала данной схемы у пациентки имелись множественные метастазы в позвоночник, кости таза, левую ключицу и отдельные ребра (рис. 1). После 3 недель приема отмечено значительное уменьшение болевого синдрома до 1 степени.
Рисунок 1. Исследование ПЭТ-КТ от 14.10.11 г.
Множественные метастазы во всех отделах позвоночника, костях таза, ребрах, левой ключице.
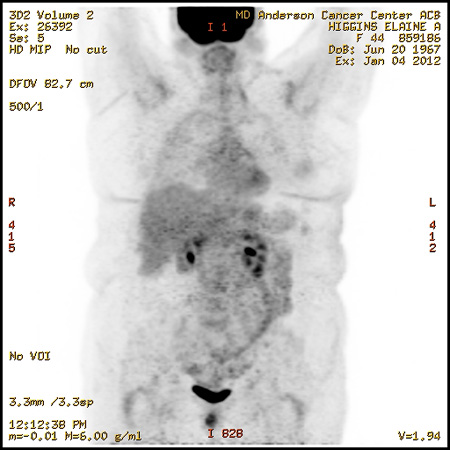
При контрольном обследовании в январе 2012 г. по данным ПЭТ был отмечен полный метаболический ответ метастатического процесса в костях (рис. 2). К этому времени полностью купировался болевой синдром. Лечение характеризовалось хорошей переносимостью, отмечалось лишь развитие кожной сыпи 1 ст. Пациентка продолжила лечение по схеме анастрозол в сочетании с эверолимусом. При повторных обследованиях в марте и в июне 2012 г. сохранялась полная регрессия метастатического процесса в костях.
Рисунок 2. Исследование ПЭТ-КТ от 4.01.12 г.
Без признаков метастатического поражения костей.
Заключение
Данный случай демонстрирует возможность достижения быстрого выраженного ответа при сочетании эверолимуса с ингибиторами ароматазы у пациентки, ранее получившей ингибиторы ароматазы. Введение в клиническую практику эверолимуса позволило существенно расширить возможности гормонотерапии метастатического рака молочной железы за счет появления данной малотоксичной, амбулаторной, пероральной комбинации.
Преодоление резистентности к сунитинибу после терапии эверолимусом
И.С. Шумская, О.В. Исаченкова
Нижегородская государственная медицинская академия, Нижний Новгород
В иностранной литературе содержится информация о возможном восстановлении чувствительности опухоли к ингибиторам тирозинкиназ после терапии ингибиторами mTOR. Представленный клинический случай продемонстрировал справедливость этих данным. Пациент, 49 лет, наблюдается в онкологическом диспансере с сентября 2010 года с диагнозом: рак левой почки T3N×M1, метастазы в легкие, мягкие ткани боковой поверхности брюшной стенки слева.
Из анамнеза: в сентябре 2009 года выполнена нефрэктомия по поводу рака левой почки. Гистологическое исследование: светлоклочный ПКР, с глубоким инфильтративным ростом через стенку лоханки в паранефральную клетчатку. На фоне терапии интерфероном альфа в течение 3 месяцев отмечен рост образований на брюшной стенке. В сентябре 2010 г. по данным КТ органов грудной клетки – метастатическое поражение бронхопульмональных лимфатических узлов, легких, отрицательная динамика.
С сентября 2010 г. начата терапия сунитинибом в дозе 50 мг 4 недели с перерывом в 2 недели. На фоне лечения сунитинибом отмечен частичный регресс метастазов в легких, уменьшение размера мягкотканых образований на брюшной стенке. Лечение сунитинибом проводилось в течение 11 месяцев. В сентябре 2011 по данным УЗИ органов брюшной полости отмечается рост мягкотканых очагов в области послеоперационного рубца, отрицательная динамика по данным КТ грудной клетки в виде увеличения размеров и количества метастатических очагов.
В связи с прогрессированием был назначен эверолимус в дозе 10 мг ежедневно. На фоне лечения зарегистрированы следующие побочные эффекты: через месяц после начала приема препарата впервые был выявлен диабет 2 типа инсулинозависимый, плохо контролируемый сочетанием инсулина и пероральных сахароснижающих препаратов; стоматит 2 степени, появившийся еще на фоне приема сунитиниба; через два месяца после приема препарата появилась нарастающая одышка в покое, кашель. По данным КТ грудной клетки от ноября 2011 размеры и количество метастатических очагов в легких не изменились, однако появились явления лимфангоита. Данное состояние не позволяло исключить медикаментозный пульмонит, в связи с чем была продолжена терапия эверолимусом в дозе 5 мг на фоне глюкокортикостероидов. В результате этого лечения было достигнуто некоторое субъективное улучшение – уменьшилась одышка. Однако после 3 месяцев приема препарата выявлен рост мягкотканых очагов в области послеоперационного рубца, увеличение метастазов в легких по данным КТ грудной клетки. Эверолимус был отменен. После отмены препарата нормализовались показатели глюкозы, в настоящее время никакой сахароснижающей терапии больной не получает.
В связи с прогрессированием заболевания сделана попытка вернуться к терапии сунитинибом в дозе 50 мг. На фоне лечения отмечено значительное уменьшение одышки и уменьшение мягкотканых метастазов. По данным КТ грудной клетки на протяжении последних 8 месяцев наблюдается стабилизация процесса. Статус по шкале ECOG 2.
Николимус — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-006455
Торговое наименование:
Николимус
Международное непатентованное наименование:
эверолимус
Лекарственная форма:
таблетки
Состав на одну таблетку:
| Действующее вещество: | |||
| Эверолимус | 2,5 мг | 5,0 мг | 10,0 мг |
| Вспомогательные вещества: | |||
| Бутилгидрокситолуол | 0,05 мг | 0,1 мг | 0,2 мг |
| Гипромеллоза Е15 | 22,5 мг | 45,0 мг | 90,0 мг |
| Кремния диоксид коллоидный | 2,5 мг | 5,0 мг | 10,0 мг |
| Кросповидон | 25,0 мг | 50,0 мг | 100,0 мг |
| Лактозы моногидрат | 5,0 мг | 10,0 мг | 20,0 мг |
| Лактоза безводная | 50,0 мг | 100,0 мг | 200,0 мг |
| Натрия стеарилфумарат | 0,75 мг | 1,5 мг | 3,0 мг |
| Целлюлоза микрокристаллическая тип 112 | 16,7 мг | 33,4 мг | 66,8 мг |
Описание
Таблетки 2,5 мг: круглые плоскоцилиндрические таблетки от белого до белого с желтоватым оттенком цвета с фаской и риской;
Таблетки 5,0 мг: круглые плоскоцилиндрические таблетки от белого до белого с желтоватым оттенком цвета с фаской;
Таблетки 10,0 мг: двояковыпуклые капсуловидные таблетки от белого до белого с желтоватым оттенком цвета.
Фармакотерапевтическая группа:
противоопухолевое средство, ингибитор протеинкиназы
Код ATX:
L01XE10
Фармакологические свойства
Механизм действия
Эверолимус является избирательным ингибитором серин-треониновой киназы mTOR (мишень рапамицина млекопитающих), специфически воздействующим на комплекс mTORCl сигнал-преобразующей mTOR-киназы и регуляторного raptor-протеина (regulatory associated protein of mTOR). Эверолимус проявляет свою активность за счет высоко аффинного взаимодействия с внутриклеточным рецепторным белком FKBP12. Комплекс FКВР12-эверолимус связывается с mTORCl, ингибируя его способность к передаче сигналов. mTOR является ключевой серин-треониновой киназой, играющей центральную роль в регуляции клеточного роста, пролиферации и выживаемости. Регуляция сигнального пути mTORCl является сложным процессом, зависящим от митогенов, факторов роста, энергетической составляющей и питательных веществ.
Комплекс mTORCl является важнейшим регулятором синтеза белка в дистальной части Р13К/АКТ-зависимого каскада, регуляция которого нарушена в большинстве злокачественных опухолей человека, а также при генетических заболеваниях, таких как туберозный склероз (ТС).
Сигнальная функция mTORCl реализуется через модулирование фосфорилирования дистальных эффекторов, из которых наиболее полно охарактеризованы регуляторы трансляции: киназа рибосомального белка S6 (S6K1) и фактор инициации эукариотных клеток, 4Е-связывающий белок (4Е-ВР1). Нарушение функции S6K1 и 4Е-ВР1 вследствие ингибирования mTORCl нарушает трансляцию кодируемых мРНК основных белков, участвующих в регуляции клеточного цикла, гликолиза и адаптации клеток к низкому уровню кислорода (гипоксии). Это подавляет рост опухоли и экспрессию индуцируемых гипоксией факторов (например, транскрипционного фактора HIF-1). Последнее приводит к уменьшению экспрессии факторов, обеспечивающих усиление процессов ангиогенеза в опухоли (например, сосудистого эндотелиального фактора роста – VEGF) во множественных опухолях, таких как почечно-клеточный рак и ангиомилипома. Сигнальная передача через mTORCl регулируется генами-супрессорами опухолевого роста: генами туберозного склероза 1 и 2 (TSC1, TSC2). Отсутствие или инактивация TSC1 или TSC2 приводит к повышению уровня RHEB-GTP (гуанозинтрифосфат-связывающий белок, ГТФ-связывающий белок), относящийся к Ras семейству ГТФаз, который взаимодействует с комплексом mTORCl, вызывая его активацию. Активация mTORCl приводит к нисходяще-направленному сигнальному каскаду, в том числе активации S6K1, фосфорилирует рецептор эстрогена, который отвечает за лиганд-независимую активацию рецептора.
Эверолимус является активным ингибитором роста и пролиферации опухолевых клеток, эндотелиальных клеток, фибробластов и гладкомышечных клеток кровеносных сосудов.
Соответственно центральному регуляторному действию комплекса mTORCl, эверолимус уменьшает пролиферацию клеток, гликолиз и ангиогенез в солидных опухолях in vivo, таким образом реализуя два независимых пути подавления роста опухоли: прямая противоопухолевая активность и ингибирование стромальной составляющей опухоли.
Активация mTOR сигнального пути – ключевой адаптивный механизм развития резистентности к эндокринной терапии у пациенток с раком молочной железы. Различные пути передачи сигнала активируются при развитии устойчивости к эндокринной терапии. Основным из них является PI3K/AKT/mTOR путь, который активизирован в клетках рака молочной железы, резистентных к ингибиторам ароматазы и длительно находящихся в состоянии эстрогенной депривации. В исследованиях in vitro показано, что клетки опухоли при гормонозависимом и НЕК2+раке молочной железы чувствительны к ингибирующим эффектам эверолимуса, а противоопухолевая активность комбинированной терапии эверолимусом и ингибитором ароматазы усиливает таковую активность эверолимуса вследствие синергии. Резистентность клеток рака молочной железы к ингибиторам ароматазы вследствие активации АКТ может быть преодолена посредством комбинирования с эверолимусом. Комбинированная терапия эверолимусом и ингибитором ароматазы позволяет увеличить медиану выживаемости без прогрессирования в 2,7 раза и на 62% снизить вероятность прогрессирования заболевания и смерти.
При ТС, генетически обусловленном заболевании, инактивирующие мутации генов TSC1 или TSC2 приводят к образованию гамартом различной локализации.
У пациентов с субэпендимальными гигантоклеточными астроцитомами (СЭГА), ассоциированными с ТС, после 6 месяцев лечения эверолимусом отмечалось статистически значимое уменьшение объема опухоли, при этом у 75% пациентов объем опухоли сократился не менее чем на 30%, а у 32% пациентов – не менее чем на 50%. При этом новых очагов, усиления гидроцефалии, признаков повышения внутричерепного давления и необходимости в хирургическом лечении СЭГА не возникло.
Продолжительное наблюдение за пациентами с СЭГА, ассоциированными с ТС, подтвердили устойчивую эффективность эверолимуса.
Фармакодинамика
После ежедневного применения эверолимуса в дозе 5 мг или 10 мг отмечалась умеренная зависимость уменьшения фосфорилирования белка 4Е-ВР1 опухолевой ткани от средней минимальной концентрации (Cmin) эверолимуса в крови в равновесном состоянии.
Дополнительные данные свидетельствуют о том, что уменьшение фосфорилирования киназы S6 крайне чувствительно к ингибированию mTOR эверолимусом. Ингибирование фосфорилирования elF-4G было полным при всех значениях Cmin после ежедневного применения эверолимуса в дозе 10 мг.
Имелась тенденция к увеличению срока выживаемости без прогрессирования заболевания при увеличении Cmin эверолимуса, нормализованной по времени (определяемой по формуле: (площадь под кривой Cmin-время от начала исследования до времени события)/(время от начала исследования до события)) у пациентов с распространенными нейроэндокринными опухолями поджелудочной железы (отношение рисков 0,73) и у пациентов с распространенными карциноидами (отношение рисков 0,66). Величина Cmin эверолимуса повлияла на вероятность уменьшения размера опухоли (р <0,001) при изменении экспозиции от 5 до 10 нг/мл у пациентов с распространенными нейроэндокринными опухолями поджелудочной железы и у пациентов с распространенными карциноидами (отношение шансов 1,62 и 1,46 соответственно).
Эверолимус достоверно снижал риск прогрессирования заболевания и смерти пациентов с распространенным и/или метастатическим почечно-клеточным раком после прогрессии на антиангиогенной терапии на 67%, медиана выживаемости пациентов без прогрессирования заболевания составила 4,9 месяцев. В течение 6 месяцев у 36% пациентов, получавших эверолимус, не отмечалось прогрессирования заболевания. Применение эверолимуса позволяет значительно улучшить качество жизни пациентов (оценивалось влияние симптомов заболевания на различные сферы жизни пациента).
При применении эверолимуса у пациентов с распространенными и/или метастатическими нейроэндокринными опухолями выживаемость без прогрессирования в течение 18 месяцев составила 34,2%.
У пациентов с СЭРА, ассоциированными с ТС, увеличение Cmin в 2 раза ведет к уменьшению объема опухоли на 13%.
Фармакокинетика
Всасывание
Максимальная концентрация (Сmax) эверолимуса в крови у пациентов с распространенными солидными опухолями после приема эверолимуса в форме таблеток внутрь в дозах от 5 до 70 мг (натощак или с небольшим количеством нежирной пищи) достигается через 1-2 часа. Сmax при ежедневном приеме препарата изменяется пропорционально дозе в диапазоне от 5 до 10 мг. При приеме однократной дозы эверолимуса 20 мг и выше возрастание Сmax происходит менее чем пропорционально дозе, однако значение площади под фармакокинетической кривой «концентрация-время» (AUC) увеличивается пропорционально дозе при приеме от 5 мг до 70 мг препарата.
При приеме эверолимуса в дозе 10 мг в форме таблеток с пищей с высоким содержанием жиров AUC и Сmax препарата снижались соответственно на 22% и 54%. Одновременный прием пищи с низким содержание жиров снижал AUC и Сmax на 32% и 42%, соответственно. Одновременный прием пищи, однако, не оказывал значимого влияния на профиль концентрация-время после всасывания в течение 24 часов.
Распределение
Процентное отношение концентрации эверолимуса в крови и плазме крови, которое является зависимым от концентрации соединения в диапазоне от 5 до 5000 нг/мл, изменяется от 17% до 73%. Концентрация эверолимуса в плазме крови составляет примерно 20% от его концентрации в цельной крови при концентрациях вещества, регистрируемых в крови онкологических пациентов, принимающих эверолимус по 10 мг в день. Связь с белками плазмы крови составляет примерно 74% как у здоровых добровольцев, так и у пациентов с нарушением функции печени средней степени тяжести.
В экспериментальных исследованиях было показано, что после внутривенного введения проникновение эверолимуса через гематоэнцефалический барьер зависит от дозы нелинейно, что предполагает насыщение насоса гематоэнцефалического барьера, обеспечивающего попадание препарата из крови в ткани мозга. Проникновение эверолимуса через гематоэнцефалический барьер продемонстрировано также у животных, получавших препарат внутрь.
Метаболизм
Эверолимус является субстратом изофермента CYP3A4 и Р-гликопротеина (Р-ГП). После приема препарата внутрь в крови эверолимус циркулирует в основном в неизмененном виде. В крови человека определены шесть основных метаболитов эверолимуса, представленных тремя моногидроксилированными метаболитами, двумя продуктами гидролитического превращения с открытым кольцом и фосфатидилхолиновым конъюгатом эверолимуса. Указанные метаболиты по активности уступали эверолимусу примерно в 100 раз. Поэтому принято считать, что большая часть общей фармакологической активности эверолимуса обусловлена действием неизмененного соединения.
Выведение
Специальных исследований по изучению выведения эверолимуса у онкологических пациентов не проводилось; однако имеются соответствующие данные у пациентов, принимающих препарат после трансплантации органов. После введения однократной дозы меченого радиоактивной меткой эверолимуса большая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось почками. Неизмененное вещество не определялось ни в моче, ни в кале.
Фармакокинетика в равновесном состоянии
После ежедневного приема эверолимуса величина площади под фармакологической кривой «концентрация-время» от момента приема препарата до момента отбора пробы (AUC0-τ) была пропорциональна дозе препарата при его применении в дозах от 5 до 10 мг в день. Равновесное состояние достигалось в пределах двух недель. Сmax эверолимуса была пропорциональна дозе при применении препарата в дозах от 5 до 10 мг в день. Время достижения максимальной концентрации в плазме крови (Тmax) составляло 1-2 часа.
При ежедневном приеме эверолимуса по достижении равновесного состояния имелась достоверная корреляция между величиной AUC0-τ И концентрацией препарата в крови перед приемом очередной дозы. Период полувыведения эверолимуса составляет около 30 часов.
Фармакокинетика у отдельных групп пациентов
Пациенты с нарушениями функции печени
При приеме эверолимуса пациентами с нарушениями функции печени системное воздействие препарата повышается в 1,6; 2,0-3,3 и 3,6 раз, соответственно, при печеночной недостаточности легкой степени тяжести (класс А по классификации Чайлд-Пью), средней степени тяжести (класс В по классификации Чайлд-Пью) и тяжелой степени (класс С по классификации Чайлд-Пью). Необходима коррекция дозы эверолимуса при нарушении функции печени (см. «Способ применения и дозы»).
Пациенты с нарушением функции почек
Существенного влияния величины клиренса креатинина (от 25 до 178 мл/мин) на клиренс (CL/F) эверолимуса не выявлено у пациентов с распространенными солидными опухолями. Посттрансплантационные нарушения функции почек (клиренс креатинина от 11 до 107 мл/мин) не влияли на фармакокинетику эверолимуса у пациентов после трансплантации органов.
Пациенты в возрасте ≤18 лет
- Применение эверолимуса у детей и подростков до 18 лет противопоказано по показаниям: распространенный и/или метастатический почечно-клеточный рак и распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы, ангиомиолипома почки, ассоциированная с ТС при отсутствии СЭГА.
- У пациентов с СЭГА минимальная концентрация (Cmin) эверолимуса при применении в форме таблеток была приблизительно пропорциональна суточной дозе и находилась в пределах 1,35-14,4 мг/м².
- У пациентов с СЭГА среднее геометрическое значение Cmin эверолимуса нормализованное к дозе в мг/м² у пациентов младше 10 лет и от 10 до 18 лет статистически значимо ниже, чем у взрослых пациентов, что может указывать на повышенный клиренс эверолимуса у молодых пациентов.
Пациенты в возрасте ≥65 лет
Существенного влияния возраста пациентов (от 27 до 85 лет) на клиренс эверолимуса (CL/F от 4,8 до 54,7 л/ч) после приема препарата внутрь не было выявлено.
Влияние расовой принадлежности
Клиренс эверолимуса (CL/F) после приема препарата внутрь у лиц европеоидной и монголоидной рас при сходной функции печени не различается.
По данным популяционного фармакокинетического анализа у лиц негроидной расы после пересадки органов клиренс эверолимуса (CL/F) (после приема внутрь) был в среднем на 20% больше, чем у представителей европеоидной.
Показания к применению
- Распространенный и/или метастатический почечно-клеточный рак при неэффективности антиангиогенной терапии.
- Распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы.
- Гормонозависимый распространенный рак молочной железы у пациенток в постменопаузе в комбинации с ингибитором ароматазы после предшествующей эндокринной терапии.
- Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом у пациентов в возрасте старше 3-х лет при невозможности выполнения хирургической резекции опухоли.
- Ангиомиолипома почки, ассоциированная с туберозным склерозом, не требующая немедленного хирургического вмешательства.
Противопоказания
- Повышенная чувствительность к эверолимусу, другим производным рапамицина или любому из вспомогательных компонентов препарата.
- Беременность и период грудного вскармливания.
- Нарушение функции печени (класс А, В, С по классификации Чайлд-Пью) у пациентов от 3-х до 18 лет с СЭГА.
- Возраст до 3-х лет (СЭГА), до 18 лет (по остальным показаниями).
Следует избегать одновременного применения с мощными ингибиторами изофермента CYP3A4 и/или Р-ГП.
Следует избегать одновременного применения с мощными индукторами изофермента CYP3A4 или индукторами Р-ГП.
С осторожностью
- При одновременном применении эверолимуса с умеренными ингибиторами CYP3A4 или ингибиторами Р-ГП.
- У пациентов >18 лет с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Нью) в случае, когда польза от приема препарата превышает возможный риск.
- У пациентов до и после хирургических вмешательств.
- У пациентов с непереносимостью лактозы, тяжелой лактазной недостаточностью или глюкозо-галактозной мальабсорбцией.
Применение при беременности и в период грудного вскармливания
Беременность
Сводная характеристика рисков
Нет данных о применении эверолимуса у беременных женщин. Потенциальный риск для человека не известен. В исследованиях у животных выявлена репродуктивная токсичность, включая эмбрио- и фетотоксичность.
Препарат Николимус противопоказан к применению во время беременности.
Исследования у животных
При применении эверолимуса внутрь у самок крыс в дозе >0,1 мг/кг (приблизительно 4% от суточной AUC у пациентов, принимающих препарат в дозе 10 мг/сут) частота преимплантационных потерь увеличивалась. Эверолимус проходит через гематоплацентарный барьер и оказывает токсическое действие на оплодотворенную яйцеклетку. У крыс эверолимус проявлял эмбрио- и фетотоксичность при системной экспозиции ниже терапевтической, что приводило к увеличению смертности или уменьшению массы тела плода. Частота возникновения вариантов развития скелета и скелетных мальформаций (например, расщелина грудной клетки) увеличивалась при применении эверолимуса в дозах 0,3 и 0,9 мг/кг. У кроликов эмбриотоксичность проявлялась увеличением частоты поздней резорбции плода при применении эверолимуса в дозе 0,8 мг/кг (9,6 мг/м²), что приблизительно в 1,6 раз выше дозы 10 мг для взрослых при применении по показанию СЭГА и в 1,3 раз выше средней дозы, применяемой при ТС и рефрактерной эпилепсии, рассчитанной по площади поверхности тела. Не было выявлено побочных действий на эмбрион и плод при применении эверолимуса у самцов крыс.
Исследования у человека
Описаны случаи воздействия эверолимуса на плод во время беременности в результате приема препарата как матерью, так и отцом (беременность у женщины, являвшейся партнером пациента, принимавшего эверолимус). Сообщений о возникновении пороков развития плода не зарегистрировано. В некоторых случаях беременность протекала без осложнений и закончилась родами здоровым плодом без какой-либо патологии.
Лактация
Сводная характеристика рисков
Не известно проникает ли эверолимус в грудное молоко человека. Не зарегистрировано случаев воздействия эверолимуса на ребенка в период грудного вскармливания у человека. В исследованиях у животных эверолимус и/или его метаболиты легко и быстро проникали в молоко крыс в концентрации, в 3,5 раза превосходящей концентрацию в плазме крови матери. Женщинам, получающим эверолимус, не следует кормить грудью во время терапии и спустя 2 недели после приема последней дозы.
Женщины и мужчины с сохраненным репродуктивным потенциалом
Контрацепция
Пациенток с сохраненным репродуктивным потенциалом следует проинформировать, что в исследованиях у животных было выявлено неблагоприятное влияние эверолимуса на развивающийся плод. Пациенткам с сохраненным репродуктивным потенциалом, ведущим активную половую жизнь, необходимо применять надежные способы контрацепции (при правильном и длительном применении которых частота наступления беременности составляет <1%) во время терапии препаратом и минимум в течение 8 недель после ее завершения. Пациентам мужского пола, принимающим эверолимус, не следует отказываться от попыток зачатия.
Фертильность
Исследования у животных
В исследованиях у животных фертильность самок не изменялась, однако были зарегистрированы случаи преимплантационных потерь. У самцов крыс наблюдались морфологические изменения в яичках при применении эверолимуса в дозе 0,5 мг/кг и выше, а также снижение подвижности и уменьшение количества сперматозоидов и активности тестостерона при применении дозы 5 мг/кг, что соответствует терапевтической концентрации (52 нг*ч/мл и 414 нг*ч/мл соответственно в сравнении с терапевтической концентрацией 560 нг*ч/мл при применении препарата у человека в дозе 10 мг/сут) и приводит к снижению фертильности у самцов. Имеются данные об обратимости данного эффекта.
Исследования у человека
Терапия эверолимусом может отрицательно сказаться на фертильности у пациентов мужского и женского пола.
У пациенток, принимавших эверолимус, отмечались нерегулярный менструальный цикл, вторичная аменорея и нарушение баланса лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). У пациентов мужского пола на фоне применения эверолимуса отмечалось повышение активности ФСГ и ЛГ, снижение активности тестостерона, азооспермия.
Способ применения и дозы
Лечение препаратом Николимус следует проводить только под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами или лечения пациентов с туберозным склерозом.
Препарат Николимус следует принимать внутрь один раз в день ежедневно в одно и то же время (предпочтительно утром) натощак или после приема небольшого количества пищи, не содержащей жира. Таблетки следует проглатывать целиком, запивая стаканом воды, их не следует разжевывать или дробить. Для пациентов с СЭГА, ассоциированными с ТС, которые не могут проглотить таблетку целиком, таблетку препарата Николимус непосредственно перед приемом можно полностью растворить в стакане воды (примерно 30 мл), осторожно помешивая содержимое стаканчика до полного распадения таблетки (примерно 7 минут). Для обеспечения приема полной дозы следует еще раз набрать в стаканчик такой же объем воды (примерно 30 мл), смыть со стенок оставшиеся частицы препарата и выпить получившийся раствор.
Лечение препаратом проводят до тех пор, пока сохраняется клиническая эффективность и нет признаков непереносимой токсичности.
Смена лекарственной формы препарата эверолимуса
Нельзя комбинировать разные лекарственные формы препарата эверолимуса (таблетки и диспергируемые таблетки) для достижения необходимой дозы. Следует всегда использовать одну и ту же лекарственную форму в соответствии с показанием к применению.
При смене лекарственной формы (только для пациентов с СЭГА, ассоциированными с ТС) следует подбирать дозу препарата, максимально близкую к применяемой ранее. Следует проконтролировать Cmin эверолимуса приблизительно через 1 или 2 недели после смены лекарственной формы.
В случае пропуска приема очередной дозы препарата, ее можно принять в течение 6 часов после запланированного времени, по истечении 6 часов после запланированного времени дозу следует пропустить. На следующий день дозу препарата следует принять в запланированное время. Недопустим прием двойной дозы препарата с целью восполнения пропущенной.
Распространенный и/или метастатический почечно-клеточный рак при неэффективности антиангиогенной терапии: распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы, ангиомиолипома почки, не требующая немедленного хирургического вмешательства, у пациентов с туберозным склерозом.
Рекомендуемая доза препарата Николимус составляет 10 мг один раз в сутки.
Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом, у пациентов в возрасте старше 3-х лет при невозможности выполнения хирургической резекции опухоли
Дозу препарата Николимус для лечения пациентов с СЭГА, ассоциированными с ТС, определяют исходя из площади поверхности тела (BSA, м²), рассчитанной по формуле Дюбуа.
Начальная доза препарата Николимус и целевая Cmin эверолимуса в крови у пациентов с СЭГА, ассоциированными с ТС
Рекомендуемая начальная доза препарата Николимус для лечения пациентов с СЭГА, составляет 4,5 мг/м², округленная до ближайшей дозировки препарата Николимус. Таблетки препарата Николимус различных дозировок одной лекарственной формы можно комбинировать для получения необходимой дозы, однако комбинировать разные лекарственные формы эверолимуса с этой целью нельзя.
Контроль концентрации эверолимуса в крови
У пациентов, получающих терапию эверолимусом по поводу СЭГА, следует контролировать Cmin эверолимуса в крови. Определять Cmin эверолимуса в крови следует через 1-2 недели после начала терапии и/или любой коррекции дозы. Дозу корректируют для поддержания целевой Cmin эверолимуса в крови в диапазоне 5-15 нг/мл.
Подбор дозы
Для оптимального клинического ответа дозу препарата следует подбирать индивидуально, увеличивая на 2,5 мг для достижения целевой Cmin эверолимуса в крови. При планировании подбора дозы следует принимать во внимание эффективность и безопасность проводимого лечения, одновременно проводимую медикаментозную терапию и текущую Сmin эверолимуса в крови. Индивидуальный подбор дозы может быть проведен исходя из следующей формулы:
новая доза эверолимуса = применяемая доза × (целевая Сmin / текущая Сmin эверолимуса)
Например, применяемая доза препарата, рассчитанная исходя из площади поверхности тела, в настоящее время составляет 2,5 мг, Cmin эверолимуса в крови в равновесном состоянии составляет 4 нг/мл. Для достижения целевой Cmin эверолимуса в крови составляющей >5нг/мл, например, 8 нг/мл, новая скорректированная доза препарата должна составлять 5 мг (применяемая суточная доза 2,5 мг, увеличенная на 2,5 мг). После коррекции дозы следует определить Cmin в крови через 1-2 недели.
Долгосрочный контроль дозы
У пациентов с СЭГА, ассоциированными с ТС, объем опухоли следует измерить через 3 месяца после начала терапии препаратом Николимус с последующей коррекцией дозы с учетом изменения объема опухоли на фоне лечения, Cmin эверолимуса в крови и индивидуальной переносимости препарата.
После достижения стабильной дозы препарата при СЭГА, ассоциированными с ТС, следует контролировать Cmin эверолимуса в крови на протяжении всего срока лечения каждые 3-6 месяцев у пациентов с меняющейся площадью поверхности тела и каждые 6-12 месяцев у пациентов с неизменной площадью поверхности тела.
Рекомендации по коррекции дозы препарата Николимус при развитии нежелательных явлений
Коррекция тяжелых и/или труднопереносимых нежелательных лекарственных реакций (НЛР) может потребовать временного прекращения терапии с/без уменьшения дозы. Если требуется снижение дозы препарата, рекомендуется применять дозу приблизительно на 50% меньше предыдущей. В таблице № 1 отражены рекомендации по коррекции дозы препарата при развитии НЛР. У пациентов, получающих препарат Николимус в наименьшей доступной дозировке, дальнейшее снижение дозы при необходимости возможно при приеме препарата через день. Тактика ведения пациента должна основываться на индивидуальной оценке пользы и риска с учетом особенностей каждого пациента.
Таблица 1. Рекомендации по коррекции дозы препарата Николимус при развитии нежелательных явлений
| Нежелательная реакция | Степень тяжести1 | Рекомендации по изменению дозы и коррекции нежелательных явлений2 |
| Неинфекционный пневмонит | Степень 1 Субклинические, отдельные признаки или симптомы; вмешательство не показано |
Коррекции дозы не требуется. Контроль состояния. |
| Степень 2 Проявляющийся клинически; показано вмешательство; ограничение бытовой ежедневной активности |
Рассмотреть возможность прерывания терапии, исключение инфекционного процесса, при необходимости рассмотреть возможность применения глюкокортикостероидов до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в сниженной дозе. Прекращение терапии, если снижения степени тяжести симптомов до 1 степени не наступило в течение 4 недель. |
|
| Степень 3 Тяжелые симптомы; ограничение способности к самообслуживанию; показана кислородотерапии |
Прерывание терапии до снижения степени тяжести симптомов до 1 степени, исключение инфекционного процесса, при необходимости применение глюкокортикостероидов. Рассмотреть возможность возобновления терапии в сниженной дозе. При повторном развитии симптомов 3 степени рассмотреть возможность прекращения терапии. |
|
| Степень 4 Жизнеугрожающая дыхательная недостаточность; показано экстренное вмешательство (например, трахеотомия или интубация) |
Прекращение терапии, исключение инфекционного процесса, при необходимости применение глюкокортикостероидов. | |
| Стоматит | Степень 1 Субклинические симптомы, или симптомы легкой степени; вмешательство не показано |
Коррекции дозы не требуется. Полоскание рта бесспиртовым или водно-солевым (0,9%) раствором несколько раз в день. |
| Степень 2 Умеренные болевые ощущения, не препятствующие приему пищи; показана специальная диета |
Прекращение терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии препаратом Николимус в прежней дозе. При повторном развитии симптомов стоматита до 2 степени – прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в сниженной дозе. Лечение анальгетиками для местного применения (например, бензокаин, бутил-аминобензоат, тетракаина гидрохлорид, ментол или фенол) с/без глюкокортикостероидов для местного применения3. |
|
| Степень 3 Тяжелые болевые ощущения, препятствующие приему пищи |
Прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в сниженной дозе. Лечение анальгетиками для местного применения (например, бензокаин, бутил-аминобензоат, тетракаина гидрохлорид, ментол или фенол) с/без глюкокортикостероидов для наружного применения3. |
|
| Степень 4 Жизнеугрожающее последствия, показано экстренное вмешательство |
Прекращение терапии, лечение стоматита соответствующими методами. | |
| Другая не гематологическая токсичность (исключая метаболические нарушения) | Степень 1 | Коррекции дозы не требуется при переносимости симптомов. Лечение соответствующими методами и контроль состояния. |
| Степень 2 | Коррекции дозы не требуется при переносимости симптомов. Лечение соответствующими методами и контроль состояния. При непереносимости симптомов – прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в прежней дозе. При повторном развитии симптомов 2 степени – прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в сниженной дозе. |
|
| Степень 3 | Прерывание терапии до снижения степени тяжести симптомов до 1 степени. Лечение соответствующими методами и контроль состояния. Рассмотреть возможность возобновления терапии препаратом Николимус в сниженной дозе. При повторном развитии симптомов до 3 степени – рассмотреть возможность прекращение терапии. |
|
| Степень 4 | Прекращение терапии, лечение соответствующими методами. | |
| Метаболические нарушения (например, гипергликемия, дислипидемия) | Степень 1 | Коррекции дозы не требуется. Лечение соответствующими методами и контроль состояния. |
| Степень 2 | Коррекции дозы не требуется. Лечение соответствующими методами и контроль состояния. |
|
| Степень 3 | Прерывание терапии. Возобновление терапии в сниженной дозе. Лечение соответствующими методами и контроль состояния. |
|
| Степень 4 | Прекращение терапии, лечение соответствующими методами. | |
| Тромбоцитопения (уменьшение количества тромбоцитов) | Степень 1 (<НГН (нижняя граница нормы) – 75000/мм³; <НГН – 75,0×109/л) |
Коррекция дозы не требуется. |
| Степень 2 (<75000-50000/мм³;75,0-50,0×109/л) |
Прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в прежней дозе. | |
| Степень 3 (<50000-25000/мм³;50,0-25,0×109/л) или Степень 4 (<25000/мм³; <25,0×109/л) |
Прерывание терапии до снижения степени тяжести симптомов до 1 степени. Возобновление терапии в прежней дозе. | |
| Нейтропения (уменьшение количества нейтрофилов) | Степень 1 (<НГН-1500/мм³; <НГН – 1,5×109/л) или Степень 2 (<1500-1000/мм³; 1,5-1,0×109/л) |
Коррекции дозы не требуется. |
| Степень 3 (<1000-500/мм³; 1,0-0,5×109/л) |
Прерывание терапии до снижения степени тяжести симптомов до 2 степени. Возобновление терапии в прежней дозе. | |
| Степень 4 (<500/мм³; <0,5×109/л) |
Прерывание терапии до снижения степени тяжести симптомов до 2 степени. Возобновление терапии в прежней дозе. | |
| Фебрильная нейтропения | Степень 3 (АЧН (абсолютное число нейтрофилов) <1000/мм³ при однократном повышении температуры тела >38,3°С или при продолжительном повышении температуры тела ≥38 °С, сохраняющемся более 1 часа |
Прерывание терапии до снижения степени тяжести симптомов до 2 степени и отсутствия лихорадки. Возобновление терапии в сниженной дозе. |
| Степень 4 Жизнеугрожающее последствия; показано экстренное вмешательство |
Прекращение терапии. | |
| 1 Степени тяжести: 1 = минимальные симптомы; 2 = умеренные симптомы; 3 = выраженные симптомы; 4 = жизнеугрожающие симптомы. Оценочная шкала основана на рекомендованных Национальным институтом онкологии США стандартных терминологических критериях оценки нежелательных явлений (NCI СТСАЕ v4.03) 2 Если требуется снижение дозы препарата, рекомендуется применять дозу приблизительно на 50% меньше предыдущей. 3 Избегать применения препаратов, содержащих спирт, пероксид водорода, йод и производные чабреца (тимьяна) в лечении стоматита (могут провоцировать усиление изъязвления в ротовой полости). |
Одновременная терапия умеренными ингибиторами изофермента CYP3A4 или Р-ГП
Следует соблюдать осторожность, в случае если невозможно избежать совместного применения препарата Николимус и умеренных ингибиторов CYP3A4 или Р-ГП.
Распространенный и/или метастатический почечно-клеточный рак при неэффективности антиангиогенной терапии; распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы, ангиомиолипома почки, не требующая немедленного хирургического вмешательства, у пациентов с туберозным склерозом
Если пациентам показано одновременное применение препаратов, которые являются умеренными ингибиторами CYP3A4 или Р-ГП, доза препарата Николимус в большинстве случаев должна быть снижена до 5 мг или 2,5 мг в сутки. Однако точные клинические данные по корректировке дозы отсутствуют, рекомендуемая коррекция дозы может варьировать у отдельных групп пациентов, поэтому рекомендуется проведение тщательного лекарственного мониторинга с целью своевременного выявления возможных побочных эффектов. В случае прекращения одновременного применения умеренных ингибиторов CYP3A4 или Р-ГП, следует учитывать продолжительность «отмывочного» периода препаратов, который в среднем составляет от 2 до 3 дней, перед возобновлением применения препарата Николимус в дозе, применяемой исходно, до начала совместного применения препарата Николимус и умеренных ингибиторов CYP3A4 или Р-ГП.
Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом, у пациентов в возрасте старше 3-х лет при невозможности выполнения хирургической резекции опухоли
Если пациентам показано одновременное применение препаратов, которые являются умеренными ингибиторами CYP3A4 или Р-ГП, доза препарата Николимус в большинстве случаев должна быть снижена на 50%. При возникновении побочных эффектов может потребоваться дополнительное снижение дозы. Следует определить Cmin эверолимуса в крови по меньшей мере через 1 неделю после начала одновременного применения умеренного ингибитора изофермента CYP3A4 или Р-ГП. При отмене одновременно применяемых ингибиторов изофермента CYP3A4 или Р-ГП дозу препарата Николимус следует вернуть к исходной после 2-3 дней «отмывочного» периода и, по меньшей мере, через 1 неделю определить Cmin эверолимуса в крови.
Применение одновременно с мощными индукторами изофермента CYP3A4
Несмотря на то, что одновременного применения препарата с мощными индукторами следует избегать, имеются данные по коррекции режима дозирования препарата в случае, если невозможно избежать одновременного приема препаратов.
Распространенный и/или метастатический почечно-клеточный рак при неэффективности антиангиогенной терапии; распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы, ангиомиолипома почки, не требующая немедленного хирургического вмешательства, у пациентов с туберозным склерозом
При применении препарата Николимус одновременно с мощными индукторами изофермента CYP3A4 на основании фармакокинетических данных может потребоваться увеличение суточной дозы в 2 раза с шагом в 5 мг или меньше. Предполагается, что при указанном изменении дозы препарата Николимус значение AUC будет соответствовать AUC, наблюдаемому без приема индукторов изофермента, однако клинические данные с подобным изменением дозы у пациентов, получающих мощные индукторы изофермента CYP3A4, отсутствуют.
При прекращении приема мощного индуктора изофермента CYP3A4 следует обеспечить 3-5 дней «отмывочного» периода (адекватный период для значительного снижения индукции изофермента), до снижения дозы препарата Николимус к исходной дозе.
Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом, у пациентов в возрасте старше 3-х лет при невозможности выполнения хирургической резекции опухоли
- При применении препарата Николимус одновременно с мощными индукторами изофермента CYP3A4 (например, противоэпилептическими препаратами, такими как карбамазепин, фенобарбитал, фенитоин) может потребоваться увеличение начальной дозы препарата Николимус для достижения терапевтической концентрации 5-15 нг/мл; следует увеличить суточную дозу препарата Николимус в 2 раза и оценить переносимость лечения. Приблизительно через 2 недели следует измерить Cmin эверолимуса в крови. При необходимости следует скорректировать дозу препарата Николимус на 2,5 мг для достижения терапевтической концентрации 5-15 нг/мл. При прекращении приема мощного индуктора изофермента CYP3A4 дозу препарата Николимус следует вернуть к исходной после 3-5 дней «отмывочного» периода, и приблизительно через 2 недели измерить Cmin эверолимуса в крови.
- При добавлении к терапии эверолимусом мощного индуктора изофермента CYP3A4 может потребоваться увеличение дозы препарата Николимус. Дозу следует увеличить в 2 раза и оценить переносимость терапии. Приблизительно через 2 недели после удваивания дозы следует определить Cmin эверолимуса в крови. Далее при необходимости дозу следует корректировать на 2,5 мг для поддержания целевой Cmin эверолимуса в крови.
- Добавление еще одного мощного индуктора изофермента CYP3A4 к уже проводимой одновременной терапии препаратом Николимус и мощным индуктором изофермента CYP3A4 может не потребовать дополнительной коррекции дозы препарата Николимус. Приблизительно через 2 недели после добавления еще одного мощного индуктора изофермента CYP3A4 следует определить Cmin эверолимуса в крови и при необходимости дозу следует изменить на 2,5 мг для поддержания целевой Cmin эверолимуса в крови.
- Отмена терапии одним из нескольких мощных индукторов изофермента CYP3A4, применяемых одновременно с препаратом Николимус, может не потребовать дополнительной коррекции дозы препарата Николимус. Следует определить Cmin эверолимуса в крови приблизительно через 2 недели после прекращения одновременной терапии одним из нескольких мощных индукторов изофермента CYP3A4. При отмене всех одновременно применяемых мощных индукторов изофермента CYP3A4 дозу препарата Николимус следует вернуть к исходной после 3-5 дней «отмывочного» периода, и приблизительно через недели определить Cmin эверолимуса в крови.
Пациенты в возрасте <18 лет
Препарат Николимус не показан для лечения онкологических заболеваний у детей и подростков.
Препарат Николимус не показан для лечения детей и подростков с ангиомиолипомой почки, ассоциированной с ТС.
Препарат Николимус в таблетках не показан для лечения детей с СЭГА в возрасте <3 лет. Для лечения пациентов данной категории следует применять эверолимус в форме диспергируемых таблеток.
При лечении СЭГА у детей и подростков рекомендованные дозы такие же, как для лечения взрослых пациентов с СЭГА, за исключением пациентов с нарушениями функции печени.
Не рекомендуется применение препарата Николимус у пациентов <18 лет с СЭГА и нарушением функции печени.
Пациенты в возрасте ≥65 лет: коррекции дозы препарата не требуется.
Пациенты с нарушениями функции почек: коррекции дозы препарата не требуется.
Пациенты с нарушениями функции печени
При распространенном и/или метастатическом почечно-клеточном раке или метастатических нейроэндокринных опухолях желудочно-кишечного тракта, легкого и поджелудочной железы, при гормонозависимом распространенном раке молочной железы, при ангиомиолипоме почки, ассоциированной с ТС:
- У пациентов с нарушением функции печени легкой степени тяжести (класс А по классификации Чайлд-Пью) рекомендуемая доза составляет 7,5 мг в день.
- У пациентов с нарушением функции печени средней степени тяжести (класс В по классификации Чайлд-Пью) рекомендуемая доза составляет 5 мг в день; при плохой переносимости препарата возможно снижение дозы до 2,5 мг в день.
- У пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) препарат не рекомендован. В случаях, когда ожидаемая польза превышает потенциальный риск, возможен прием эверолимуса в максимальной дозе 2,5 мг в день. В случае изменения степени тяжести нарушения функции печени (по классификации Чайлд-Пью) необходимо провести коррекцию дозы препарата Николимус.
При субэпендимальных гигантоклеточных астроцитомах, ассоциированных с туберозным склерозом
Пациенты ≥18 лет
Нарушение функции печени легкой степени тяжести (класс А по классификации Чайлд-Пью): 75% от дозы, рассчитанной по площади поверхности тела (округленная до ближайшей дозировки).
Нарушения функции печени средней степени тяжести (класс В по классификации Чайлд-Пью): 50% от дозы, рассчитанной по площади поверхности тела (округленная до ближайшей дозировки).
Нарушение функции печени тяжелой степени (класс С по классификации Чайлд-Пью): применение препарата не рекомендовано. В случае, если ожидаемая польза превышает потенциальный риск, возможно применение препарата в дозе, не превышающей 25% от дозы, рассчитанной по площади поверхности тела.
Cmin эверолимуса в цельной крови следует определить приблизительно через 1-2 недели после начала лечения или после изменения функции печени (по классификации Чайлд-Пью). Следует корректировать дозу для достижения Cmin препарата в диапазоне от 5 до 15 нг/мл с учетом переносимости препарата. При изменении степени тяжести нарушения функции печени дозу препарата следует корректировать.
Пациенты <18 лет
Применение препарата Николимус у пациентов <18 лет с нарушениями функции печени не рекомендовано.
Терапевтический мониторинг концентрации эверолимуса у пациентов с СЭГА, ассоциированными с ТС
У пациентов с СЭГА, ассоциированными с ТС, следует контролировать Cmin эверолимуса в крови с помощью валидированных биоаналитических методов жидкостной хроматографии/масс-спектрометрии. Рекомендовано по возможности использовать один и тот же метод анализа и лабораторию для терапевтического контроля концентрации эверолимуса в крови на протяжении всего периода лечения.
Терапевтический мониторинг концентрации эверолимуса следует проводить в сроки через 1-2 недели после начала терапии, после любого изменения дозы или смены лекарственной формы препарата или добавления к терапии ингибиторов изофермента CYP3A4 или Р-ГП, или при появлении признаков нарушения функции печени. Концентрацию эверолимуса следует оценить приблизительно через 2 недели после добавления к терапии индукторов изофермента CYP3A4 или Р-ГП.
Дозу необходимо подбирать до достижения значения Cmin (5-15 нг/мл) с учетом переносимости терапии пациентом. Дозу можно увеличивать для достижения более высокой концентрации препарата в крови (в диапазоне терапевтической) и оптимального терапевтического эффекта с учетом переносимости препарата.
Побочное действие
Распространенный и/или метастатический почечно-клеточный рак, метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы
При применении препарата наиболее частыми НЛР (частота ≥1/10) являлись (по мере убывания частоты встречаемости): стоматит, кожная сыпь, повышенная утомляемость, диарея, инфекции, тошнота, уменьшение аппетита, анемия, изменение восприятия вкуса, пневмонит, периферические отеки, гипергликемия, астения, зуд, уменьшение массы тела, гиперхолестеринемия, носовое кровотечение, кашель, головная боль.
Наиболее частыми НЛР 3-4 степени тяжести (частота ≥1/100-<1/10) были: стоматит, анемия, гипергликемия, повышенная утомляемость, инфекции, пневмонит, диарея, астения, тромбоцитопения, нейтропения, одышка, лимфопения, протеинурия, кровотечение, гипофосфатемия, кожная сыпь, артериальная гипертензия, повышение активности аспартатаминотрансферазы (ACT), повышение активности аланинаминотрансферазы (АЛТ), пневмония и сахарный диабет.
Ниже представлены НЛР, возникавшие при применении эверолимуса (в дозе 10 мг в день) с указанием частоты их возникновения: очень часто (≥1/10), часто (≥ 1/100 и <1/10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000), включая отдельные сообщения. НЛР сгруппированы в соответствии с классификацией органов и систем органов MedDRA, в пределах каждой группы перечислены в порядке уменьшения частоты встречаемости.
Инфекционные и паразитарные заболевания: очень часто – инфекции (включая часто – пневмонию, инфекции мочевыводящих путей; нечасто – бронхит, опоясывающий лишай, сепсис, абсцесс, единичные случаи оппортунистических инфекций (например, аспергиллез, кандидоз, вирусный гепатит В), редко – миокардит вирусной этиологии).
Нарушения со стороны крови и лимфатической системы: очень часто – анемия; часто – тромбоцитопения, нейтропения, лейкопения, лимфопения; нечасто – панцитопения; редко – истинная эритроцитарная аплазия костного мозга.
Нарушения со стороны и.шунной системы: нечасто – реакции гиперчувствительности.
Нарушения со стороны обмена веществ и питания: очень часто – снижение аппетита, гипергликемия, гиперхолестеринемия; часто – гипертриглицеридемия, гипофосфатемия, сахарный диабет, гиперлипидемия, гипокалиемия, дегидратация, гипокальциемия.
Нарушения психики: часто – бессонница.
Нарушения со стороны нервной системы: очень часто – изменение восприятия вкуса, головная боль; нечасто – потеря вкусовой чувствительности.
Нарушения со стороны органа зрения: часто – отек век; нечасто – конъюнктивит.
Нарушения со стороны сердца: нечасто – хроническая сердечная недостаточность.
Нарушения со стороны сосудов: часто – артериальная гипертензия, кровотечения различной локализации; нечасто – «приливы», тромбоз глубоких вен.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: очень часто – пневмонит (включая часто: пневмонит, интерстициальную болезнь легких, инфильтрацию легких; редко: альвеолярные легочные кровотечение, легочную токсичность, альвеолит), носовое кровотечение, кашель; часто – одышка; нечасто – легочная эмболия, кровохарканье; редко – острый респираторный дистресс-синдром.
Нарушения со стороны желудочно-кишечного тракта: очень часто – стоматит (включая очень часто: стоматит; часто: афтозный стоматит, изъязвление слизистой оболочки языка и полости рта; нечасто: глоссит, глоссалгию), диарея, тошнота; часто – рвота, сухость слизистой оболочки полости рта, боль в ротовой полости, боль в животе, диспепсия, дисфагия.
Нарушения со стороны кожи и подкожных тканей: очень часто – кожная сыпь (включая, часто – сыпь; часто – эритематозная сыпь, эритема; нечасто – генерализованная сыпь, макуло-папулезная сыпь, макулезная сыпь), акне; часто – сухость кожи, акнеформный дерматит; нечасто – ангионевротический отек.
Нарушения со стороны скелетно-мышечной и соединительной ткани: часто – артралгия.
Нарушения со стороны почек и мочевыводящих путей: часто – протеинурия, почечная недостаточность; нечасто – учащенное мочеиспускание в дневное время суток, острая почечная недостаточность.
Нарушения со стороны половых органов и молочной железы: часто – нерегулярный менструальный цикл*; нечасто – аменорея. * – у пациенток в возрасте от 10 до 55 лет, получавших терапию препаратом во время клинических исследований.
Общие расстройства и нарушения в месте введения: очень часто – повышенная утомляемость, астения, периферические отеки; часто – лихорадка, воспаление слизистых оболочек; нечасто – некардиогенная боль в груди, медленное заживление ран.
Лабораторные и инструментальные показатели: очень часто – снижение массы тела.
Отклонения лабораторных и инструментальных показателей, отмечавшиеся с частотой ≥1/10 (градация «очень часто», НЛР перечислены по мере убывания частоты встречаемости):
— гематологические: снижение концентрации гемоглобина, лимфопения, лейкопения, громбоцитопения, нейтропения (или их сочетание – панцитопения);
— биохимические: повышение концентрации глюкозы крови натощак, холестерина, триглицеридов, повышение активности ACT, гипофосфатемия, повышение активности АЛТ, повышение концентрации креатинина, гипокалиемия, снижение концентрации альбумина.
Большинство отклонений лабораторных показателей были легкой и средней степени тяжести. Тяжелые (3-4 степени) отклонения включали:
— гематологические: очень часто – лимфопению, снижение концентрации гемоглобина; часто – нейтропению, тромбоцитопению, лейкопению;
— биохимические: очень часто – повышение концентрации глюкозы крови натощак; часто – гипофосфатемию, гипокалиемии), повышение активности ACT, АЛТ, а также повышение концентрации креатинина, общего холестерина, триглицеридов в сыворотке крови, снижение концентрации альбумина.
Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом, у пациентов в возрасте 3-х лет при невозможности выполнения хирургической резекции опухоли, ангиомиолипома почки, ассоциированная с туберозным склерозом, не требующая немедленного хирургического вмешательства
При применении препарата наиболее частыми НЛР ((частота ≥1/10), НЛР перечислены по мере убывания частоты встречаемости) являлись: стоматит, лихорадка, назофарингит, диарея, инфекции верхних дыхательных путей, рвота, кашель, кожная сыпь, головная боль, аменорея, угревая сыпь, пневмония, инфекции мочевыводящих путей, синусит, нерегулярный менструальный цикл, ухудшение аппетита, повышенная утомляемость, гиперхолестеринемия и артериальная гипертензия.
Наиболее частыми НЛР 3-4 степени тяжести (частота ≥1/100) явились: пневмония, стоматит, аменорея, нейтропения, лихорадка, нерегулярный менструальный цикл, гипофосфатемия, диарея и воспаление подкожной жировой клетчатки.
Ниже представлены НЛР, возникавшие при применении эверолимуса с указанием частоты их возникновения: очень часто (≥1/10), часто (≥1/100-<1/10), нечасто (≥1/1000-<1/100), редко (≥1/10000-<1/1000), очень редко (<1/10000), в том числе отдельные сообщения.
НЛР сгруппированы в соответствии с классификацией органов и систем органов MedDRA, в пределах каждой группы перечислены в порядке уменьшения частоты встречаемости.
Инфекционные и паразитарные заболевания: очень часто – назофарингит, инфекции верхних дыхательных путей, пневмония, синусит, инфекции мочевыводящих путей; часто – фарингит, средний отит, воспаление подкожной клетчатки, стрептококковый фарингит, гастроэнтерит вирусной этиологии, гингивит; нечасто – опоясывающий лишай, бронхит вирусной этиологии.
Нарушения со стороны крови и лимфатической системы: часто – анемия, нейтропения, лейкопения, тромбоцитопения, лимфопения.
Нарушения со стороны иммунной системы: часто – реакции гиперчувствительности.
Нарушения со стороны обмена веществ и питания: очень часто – гиперхолестеринемия, ухудшение аппетита; часто – гипертриглицеридемия, гиперлипидемия, гипофосфатемия, гипергликемия.
Нарушения психики: часто – бессонница, агрессивность, раздражительность.
Нарушения со стороны нервной системы: очень часто – головная боль; часто – изменение восприятия вкуса.
Нарушения со стороны сосудов: очень часто – артериальная гипертензия; часто – лимфедема.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: очень часто – кашель; часто – носовое кровотечение; нечасто – пневмонит.
Нарушения со стороны желудочно-кишечного тракта: очень часто – стоматит (включая очень часто – стоматит, изъязвление слизистой оболочки полости рта, афтозная язва; часто – изъязвление слизистой оболочки губ и языка; нечасто – глоссит, боль в деснах), диарея, рвота; часто – запор, тошнота, боль в животе, метеоризм, боль в ротовой полости, гастрит.
Нарушения со стороны кожи и подкожных тканей: очень часто – кожная сыпь (включая, часто – сыпь; часто – эритематозная сыпь, эритема; нечасто – генерализованная сыпь, эритема, макуло-папулезная сыпь, макулезная сыпь), акне; часто – сухость кожи, акнеформный дерматит; нечасто – ангионевротический отек.
Нарушения со стороны почек и мочевыводящих путей: часто – протеинурия.
Нарушения со стороны половых органов и молочной железы: очень часто – аменорея*, нерегулярный менструальный цикл*; часто – меноррагия, влагалищное кровотечение, киста яичника; нечасто – опсоменорея*.
* – у пациенток в возрасте от 10 до 55 лет, получавших терапию препаратом во время клинических исследований.
Общие расстройства и нарушения в месте введения: очень часто – лихорадка, повышенная утомляемость.
Лабораторные и инструментальные данные: часто – повышение активности лактатдегидрогеназы (ЛДГ), повышение концентрации лютеинизирующего гормона (ЛГ) в плазме крови; нечасто – повышение концентрации фолликулостимулирующего гормона (ФСГ) в крови.
Отклонения лабораторных и инструментальных показателей, отмечавшиеся с частотой ≥1/10 (по мере убывания частоты встречаемости)
Гематологические: увеличение частичного тромбопластинового времени, снижение абсолютного количества нейтрофилов, снижение концентрации гемоглобина, лейкопения, тромбоцитопения, лимфопения.
Биохимические: гиперхолестеринемия, гипертриглицеридемия, повышение активности ACT и АЛТ, гипофосфатемия, повышение активности щелочной фосфатазы (ЩФ), повышение концентрации глюкозы в плазме крови натощак.
Большинство из вышеуказанных НЛР были легкой (1-й) или средней (2-й) степени тяжести.
Отклонения тяжелой степени (3-4 степени) включали:
— гематологические: часто – снижение абсолютного количества нейтрофилов, увеличение частичного тромбопластинового времени, снижение концентрации гемоглобина; нечасто – лимфопения, лейкопения;
— биохимические: часто – гипофосфатемия, гипертриглицеридемия, повышение активности ЩФ, гиперхолестеринемия, повышение активности ACT и АЛТ; нечасто – повышение концентрации глюкозы крови натощак.
Описание отдельных НЛР по данным клинических исследований и при применении эверолимуса в клинической практике в пострегистрационном периоде
Отмечались случаи обострения вирусного гепатита В, включая случаи с летальным исходом. Обострение инфекций является ожидаемым явлением в периоды иммуносупрессии.
Отмечались случаи почечной недостаточности (в том числе с летальным исходом) и протеинурии. Рекомендуется контролировать функцию почек.
Отмечались случаи аменореи (включая вторичную аменорею).
Отмечались случаи развития пневмоцистной пневмонии (вызванной Pneumocystis jirovecii), некоторые с летальным исходом.
Отмечались случаи развития ангионевротического отека как при одновременном применении с ингибиторами ангиотензин-превращающего фермента (АПФ), так и при изолированном применении эверолимуса.
В пострегистрационном исследовании у пациенток в постменопаузе с гормон зависимым HER-раком молочной железы с момента начала терапии эверолимусом в дозе 10 мг/сутки в комбинации с эксеместаном (25 мг/сутки) с целью уменьшения частоты возникновения и степени тяжести стоматита местно применяли бесспиртовой раствор дексаметазона 0,5 мг/5 мл (10 мл раствора, полоскание полости рта в течение 2 минут 4 раза в сутки на протяжении 8 недель) с последующим приемом пищи не ранее чем через 1 час после полоскания. Частота возникновения стоматита ≥2 степени тяжести составила 2,4%, что ниже относительно ранее зарегистрированной частоты (27,4%) в клинических исследованиях у пациентов данной категории. Частота возникновения стоматита 1 степени составила 18,8%, при этом не зарегистрировано случаев стоматита 3 или 4 степени. Сводный профиль безопасности в данном исследовании был сравним с определенным ранее у пациентов с онкологическими заболеваниями и ТС, за исключением явлений кандидозного поражения слизистой полости рта, которые отмечались у 2,2% пациентов в данном исследовании по сравнению с 0,2% в ранее проведенном исследовании у пациентов данной популяции.
Пациенты в возрасте <18 лет
У пациентов данной категории основные характер, тип и частота НЛР, выявленных в клинических исследованиях, были схожими, за исключением инфекций, которые регистрировались с более высокой частотой и тяжестью у пациентов младше 6 лет. Результаты клинических исследований не выявили негативного влияния эверолимуса на рост и развитие в пубертатном периоде.
Пациенты в возрасте >65 лет
НЛР, развивавшиеся при применении эверолимуса у пациентов в возрасте 65 лет и старше, чаще требовали прекращения терапии. Наиболее часто такие явления включали: пневмонит (в т.ч. интерстициальную болезнь легких), стоматит, повышенную утомляемость и одышку.
Если отмечено ухудшение клинического течения любого из указанных в инструкции побочных эффектов или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка
О случаях передозировки препарата не сообщалось. В случае передозировки препарата Николимус необходимо обеспечить наблюдение за пациентом, а также начать соответствующую симптоматическую терапию. При однократном приеме препарата внутрь в дозах до 70 мг его переносимость была удовлетворительной.
Взаимодействие с другими лекарственными средствами
Эверолимус является субстратом изофермента CYP3A4, а также субстратом и умеренно активным ингибитором Р-ГП (Р-ГП-насоса), обеспечивающего вывод многих лекарственных соединений из клеток, в связи с чем вещества, которые взаимодействуют с изоферментом CYP3A4 и/или Р-ГП., могут влиять на всасывание и последующее выведение эверолимуса.
In vitro эверолимус проявляет свойства конкурентного ингибитора изофермента CYP3A4 и смешанного ингибитора изофермента CYP2D6.
Лекарственные средства (ЛС), которые могут изменять концентрацию эверолимуса в крови:
| ЛС | Изменение AUC и Сmax эверолимуса | Рекомендации по одновременному применению |
| Мощные ингибиторы СУРЗА4/Р-ГП | ||
| Кетоконазол | AUC повышалась в 15,3 раз Сmax повышалась в 4,1 раз |
Одновременное применение с препаратом Николимус не рекомендовано. |
| Итраконазол Позаконазол Вориконазол |
Одновременное применение не изучено, ожидается значительное повышение концентрации эверолимуса. | |
| Телитромицин Кларитромицин |
||
| Нефазодон | ||
| Ритонавир Атазанавир Саквинавир Дарунавир Индинавир Нелфинавир |
||
| Ингибиторы СУРЗА4/Р-ГП, с умеренной активностью | ||
| Эритромицин | AUC повышалась в 4,4 раз Сmax повышалась в 2,0 раза | Следует соблюдать осторожность, в случае если невозможно избежать совместного применения препарата Николимус и умеренных ингибиторов CYP3A4 или Р-ГП. Распространенный и/или метастатический почечноклеточный рак при неэффективности антиангиогенной терапии; распространенные и/или метастатические нейроэндокринные опухоли желудочно-кишечного тракта, легкого и поджелудочной железы, гормонозависимый распространенный рак молочной железы, ангиомиолипома почки, не требующая немедленного хирургического вмешательства, у пациентов с туберозным склерозом. Если пациентам показано одновременное применение препаратов, которые являются умеренными ингибиторами CYP3A4 или Р-ГП, доза препарата Николимус в большинстве случаев должна быть снижена до 5 мг или 2,5 мг в сутки. Однако точные клинические данные по корректировке дозы отсутствуют, рекомендуемая коррекция дозы может варьировать у отдельных групп пациентов, поэтому рекомендуется проведение тщательного лекарственного мониторинга с целью своевременного выявления возможных побочных эффектов. В случае прекращения одновременного применения умеренных ингибиторов CYP3A4 или Р-ГП, следует учитывать продолжительность «отмывочного» периода препаратов, который в среднем составляет от 2 до 3 дней, перед возобновлением применения препарата Николимус в дозе, применяемой исходно, до начала совместного применения препарата Николимус и умеренных ингибиторов CYP3A4 или Р-ГП. Субэпендимальные гигантоклеточные астроцитомы, ассоциированные с туберозным склерозом, у пациентов в возрасте старше 3-х лет при невозможности выполнения хирургической резекции опухоли Если пациентам показано одновременное применение препаратов, которые являются умеренным ингибиторами CYP3A4 или Р-ГП, доза препарата Николимус в большинстве случаев должна быть снижена на 50%. При возникновении побочных эффектов может потребоваться дополнительное снижение дозы. Следует определить Cmin эверолимуса в крови по меньшей мере через 1 неделю после начала одновременного применения умеренного ингибитора изофермента CYP3A4 или Р-ГП. При отмене одновременно применяемых ингибиторов изофермента CYP3A4 или Р-ГП дозу препарата Николимус следует вернуть к исходной после 2-3 дней (отмывочного» периода и, по меньшей мере, через 1 неделю определить Cmin эверолимуса в крови. |
| Иматиниб | AUC повышалась в 3,7 раз Сmax повышалась в 2,2 раза | |
| Верапамил | AUC повышалась в 3,5 раз Сmax повышалась в 2,3 раз | |
| Циклоспорин | AUC повышалась в 2,7 раз Сmax повышалась в 1,8 раз | |
| Флуконазол Дилтиазем |
Одновременное применение не изучено, ожидается увеличение концентрации эверолимуса. | |
| Дронедарон | Одновременное применение не изучено, ожидается повышение концентрации эверолимуса. | |
| Ампренавир Фосампренавир |
Одновременное применение не изучено, ожидается увеличение концентрации эверолимуса. | |
| Грейпфрут, грейпфрутовый сок, плоды карамболы (тропической звезды), горький апельсин и другие продукты, влияющие на активность цитохрома Р450 и Р-ГП. | Одновременное применение не изучено, ожидается увеличение концентрации эверолимуса. | Одновременного применения с препаратом Николимус следует избегать. |
| Мощные индукторы CYP3A4 | ||
| Рифампицин | AUC уменьшалась на 63% Сmax уменьшалась на 58% | Одновременного применения с препаратом Николимус следует избегать. При необходимости одновременного применения следует увеличить дозу препарата Николимус. |
| Глюкокортикостероиды (например, дексаметазон, преднизон, преднизолон) | Одновременное применение не изучено, ожидается уменьшение концентрации эверолимуса. | |
| Карбамазепин Фенобарбитал Фенитоин |
Одновременное применение не изучено, ожидается уменьшение концентрации эверолимуса. | |
| Эфавиренз Невирапин |
Одновременное применение не изучено, ожидается уменьшение концентрации эверолимуса. | |
| Зверобой продырявленный | Одновременное применение не изучено, ожидается значительное уменьшение концентрации эверолимуса. | Одновременное применение с препаратом Николимус не рекомендовано. |
Влияние эверолимуса на концентрацию в плазме ЛС, применяемых в качестве сопутствующей терапии
У здоровых добровольцев при одновременном применении эверолимуса с аторвастатином (субстрат изофермента CYP3A4) или правастатином (не является субстратом изофермента CYP3A4) клинически значимого фармакокинетического взаимодействия не отмечалось. При популяционном фармакокинетическом анализе не было выявлено также влияния симвастатина (субстрат изофермента CYP3A4) на клиренс эверолимуса.
In vitro эверолимус конкурентно ингибировал метаболизм субстрата изофермента CYP3A4 – циклоспорина и являлся смешанным ингибитором субстрата изофермента CYP2D6 декстрометорфана в равновесном состоянии. Средняя равновесная Сmax эверолимуса при приеме препарата внутрь в дозе 10 мг в день или 70 мг в неделю более чем в 12-36 раз ниже значений Ki эверолимуса по ингибирующему действию in vitro на изоферменты CYP3A4 и CYP2D6. В связи с вышесказанным влияние эверолимуса in vivo на метаболизм субстратов изоферментов CYP3A4 и CYP2D6 маловероятно.
Одновременное применение эверолимуса и мидазолама приводит к увеличению Сmax мидазолама на 25% и возрастанию AUC(o-inf) мидазолама на 30%, при этом метаболическое отношение AUC (1-гидроксимидазолам/ мидазолам) и период полувыведения мидазолама не изменяются. Это свидетельствует о том, что увеличенная экспозиция мидазолама является следствием эффектов эверолимуса в желудочно-кишечном тракте, когда оба препарата принимаются в одно и то же время. Поэтому эверолимус может влиять на биодоступность одновременно принимаемых внутрь ЛС, которые являются субстратами изофермента CYP3A4. Маловероятно, что эверолимус изменяет экспозицию других ЛС, которые являются субстратами CYP3A4, вводимых не внутрь, а другими путями, например, внутривенно, подкожно и трансдермально.
При одновременном применении с эверолимусом отмечено 10%-ое увеличение концентрации в плазме крови противоэпилептических лекарственных средств – карбрмазепина, клобазама и его метаболита, N-дезметилклобазама, перед приемом очередной дозы. Данное явление может быть клинически незначимым, однако, следует принять во внимание возможность коррекции дозы противоэпилептических ЛС с узким терапевтическим индексом, например, карбамазепина. При одновременном применении эверолимус не влиял на концентрацию в плазме крови противоэпилептических ЛС, являющихся субстратами изофермента CYP3A4 (клоназепама, диазепама, фелбамата и зонисамида), перед приемом очередной их дозы. Также не отмечено влияние эверолимуса на концентрацию в плазме крови других противоэпилептических ЛС, в т.ч. вальпроевой кислоты, топирамата, окскарбазепина, фенобарбитала, фенитонина и пиримидона, перед приемом очередной их дозы.
Одновременное применение эверолимуса и эксеместана приводит к увеличению Сmax и С2ч последнего соответственно на 45% и 71%. Тем не менее, соответствующие уровни эстрадиола в равновесном состоянии (4 недели) не отличались в двух группах терапии. У пациенток в постменопаузе с гормонозависимым распространенным раком молочной железы с положительными гормональными рецепторами, получавших соответствующую комбинацию, не наблюдалось увеличения частоты развития побочных эффектов.
Влияние данного увеличения концентрации экссместана на его эффективность и безопасность маловероятно.
Одновременое применение эверолимуса и октреотида пролонгированного действия приводит к увеличению Cmin октреотида, оказывающее незначительное влияние на клинический эффект эверолимуса у пациентов с метастазирующими нейроэндокринными опухолями.
Вакцинация
Иммунодепрессанты могут оказывать влияние на ответ при вакцинации; на фоне лечения препаратом Николимус вакцинация может быть менее эффективной. Следует избегать применения живых вакцин и тесного контакта с лицами, вакцинированными живыми вакцинами.
Особые указания
Лечение препаратом Николимус следует проводить только под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами или лечения пациентов с ТС.
Контрацепция
Во время терапии препаратом Николимус и минимум в течение 8 недель после ее окончания следует применять надежные методы контрацепции.
Неинфекционный пневмонит
Неинфекционный пневмонит является класс-специфичным побочным эффектом производных рапамицина. При применении эверолимуса также отмечались случаи развития неинфекционного пневмонита (включая интерстициальную болезнь легких). В ряде случаев наблюдались тяжелые формы заболевания (редко со смертельным исходом). Диагноз неинфекционного пневмонита следует предположить при развитии таких неспецифических проявлений со стороны органов дыхания, как гипоксия, выпот в плевральную полость, кашель или одышка, а также при исключении с помощью соответствующих диагностических исследований инфекционной, опухолевой и других причин таких проявлений. При проведении дифференциальной диагностики неинфекционного пневмонита следует исключать оппортунистические инфекции, например, пневмоцистную пневмонию.
Пациента следует проинструктировать о необходимости сообщать лечащему врачу о появлении любых новых или усилении имеющихся симптомов со стороны дыхательной системы. У пациентов, имеющих только рентгенологические признаки неинфекционного пневмонита (при отсутствии или при наличии минимальных клинически значимых симптомов), возможно продолжение лечения препаратом Николимус без изменения дозы препарата. В случае если симптомы пневмонита выражены умеренно, необходимо рассмотреть вопрос о временной приостановке терапии до улучшения состояния. Для купирования симптомов возможно применение глюкокортикостероидов. Лечение препаратом может быть возобновлено в дозе на 50% ниже исходной.
При развитии выраженных симптомов (степень 3 или 4) неинфекционного пневмонита терапию препаратом Николимус следует прекратить до снижения степени тяжести симптомов до 1 степени. В зависимости от клинических условий после излечения пневмонита терапия препаратом может быть возобновлена в дозе на 50% ниже исходной (см. «Способ применения и дозы»). При повторном развитии симптомов до 3 степени следует рассмотреть возможность прекращения терапии препаратом Николимус. При развитии неинфекционного пневмонита 4 степени терапию препаратом следует прекратить.
Также получено сообщение о развитии пневмонита при приеме эверолимуса в сниженной дозе.
У пациентов, получающих с целью лечения неинфекционного пневмонита глюкокортикостероидные препараты, следует рассмотреть возможность проведения профилактики развития пневмоцистной пневмонии.
Инфекции
Препарат Николимус обладает иммуносупрессивными свойствами и может способствовать развитию у пациентов бактериальных, грибковых, вирусных или протозойных инфекций, в особенности вызываемых условно патогенными микроорганизмами. У пациентов, принимавших эверолимус, были описаны местные и системные инфекции, включая пневмонию, другие бактериальные инфекции, грибковые инфекции, такие как аспергиллез или кандидоз, пневмоцистную пневмонию и вирусные инфекции, включая обострение вирусного гепатита В. Некоторые из этих инфекций были тяжелыми (с развитием сепсиса, дыхательной или печеночной недостаточности) и иногда приводили к летальному исходу. Пациента следует проинформировать о повышенном риске развития инфекций при применении препарата Николимус, быть внимательными к симптомам и признакам инфекций и при их появлении своевременно обращаться к врачу. У пациентов с инфекционными заболеваниями перед применением препарата Николимус следует провести надлежащее лечение. При подтверждении диагноза инфекционного поражения следует незамедлительно начать соответствующую терапию и рассмотреть вопрос о временном приостановлении или полной отмене терапии препаратом.
В случае развития инвазивной системной грибковой инфекции терапию препаратом Николимус следует отменить и провести соответствующую противогрибковую терапию.
У пациентов, получающих терапию эверолимусом, описаны случаи развития пневмоцистной пневмонии, некоторые с летальным исходом. Развитие пневмоцистной пневмонии может быть связано с одновременным применением глюкокортикостероидов или других иммунодепрессивных препаратов. В случае одновременного лечения глюкокортикостероидами или другими препаратами, угнетающими иммунную систему, следует рассмотреть возможность проведения профилактики развития пневмоцистной пневмонии.
Реакции гиперчувствительности
Реакции гиперчувствительности при применении эверолимуса включали (но не ограничивались) анафилактический шок, одышку, покраснение кожных покровов, боль в грудной клетке или ангионевротический отек (например, отек дыхательных путей или языка с/без нарушения функции дыхания).
Ангионевротический отек при одновременном применении с ингибиторами АПФ
У пациентов, получающих одновременное лечение ингибиторами АПФ, может быть повышен риск развития ангионевротического отека (например, отека дыхательных путей или языка с/без нарушения функции дыхания).
Стоматит
Стоматит, включая изъязвление слизистой оболочки полости рта, воспаление слизистой полости рта, является наиболее частой НЛР у пациентов, получающих эверолимус (см. раздел «Побочное действие»). Стоматит, как правило, развивается в первые 8 недель терапии. В случае возникновения стоматита рекомендуется применение местной терапии. Следует избегать применения средств, содержащих спирт, перекись водорода, йод, чабрец (тимьян), так как они могут усугубить состояние (см. раздел «Способ применения и дозы»). Не следует применять противогрибковые средства, если наличие грибковой инфекции не подтверждено.
В исследовании у пациенток в постменопаузе с раком молочной железы применение в качестве средства для полоскания полости рта глюкокортикостероидного раствора, не содержащего спирта, в течение первых 8 недель терапии эверолимусом в комбинации с эксеместаном позволило достигнуть клинически значимого снижения частоты и тяжести стоматита (см. раздел «Побочное действие»).
Почечная недостаточность
При применении эверолимуса были отмечены случаи развития почечной недостаточности (включая острую почечную недостаточность), некоторые с летальным исходом. Необходимо контролировать функцию почек во время терапии препаратом, особенно у пациентов с дополнительными факторами риска (см. раздел «Побочное действие»).
Лабораторные исследования и контроль
Функция почек
При применении эверолимуса были отмечены случаи повышения концентрации креатинина в сыворотке крови (обычно легкой степени) и протеинурии (см. раздел «Побочное действие»). До начала лечения препаратом Николимус и периодически во время терапии следует контролировать функцию почек, включая измерение концентрации мочевины в сыворотке крови, концентрации белка в моче или концентрации креатинина в сыворотке крови, проводить клинический анализ крови и определять концентрацию эверолимуса у пациентов с СЭГА.
Глюкоза крови
При применении эверолимуса были отмечены случаи гипергликемии (см. раздел «Побочное действие»). До начала лечения препаратом Николимус и периодически во время терапии следует контролировать концентрацию глюкозы в сыворотке крови натощак. Более частый контроль рекомендуется проводить у пациентов, одновременно получающих другие препараты, провоцирующие гипергликемию. Следует обеспечить адекватный контроль концентрации глюкозы крови до начала лечения препаратом Николимус.
Липиды крови
При применении эверолимуса были отмечены случаи дислипидемии (см. раздел «Побочное действие»). До начала лечения препаратом Николимус и периодически во время терапии следует контролировать концентрацию холестерина и триглицеридов в плазме крови. При отклонении данных показателей от нормы рекомендуется применять соответствующие средства терапии.
Гематологические нарушения
При применении эверолимуса были отмечены случаи снижения концентрации гемоглобина, количества лимфоцитов, тромбоцитов и нейтрофилов (см. раздел «Побочное действие»). Необходимо проводить развернутый анализ крови до начала терапии и периодически в течение всего курса лечения.
Нарушение функции печени
Концентрация эверолимуса была выше у пациентов с нарушением функции печени легкой (класс А по классификации Чайлд-Пью), средней (класс В по классификации Чайлд-Пью) и тяжелой (класс С по классификации Чайлд-Пью) степени (см. раздел «Фармакологические свойства»), У пациентов старше 18 лет с нарушениями функции печени тяжелой степени (класс С по классификации Чайлд-Пью) препарат не рекомендован за исключением случаев, когда ожидаемая польза превышает возможный риск. Препарат Николимус противопоказан пациентам с СЭГА, ассоциированными с ТС, в возрасте до 18 лет с нарушениями функции печени класса А, В, С по классификации Чайлд-Пью.
Вакцинация
Следует избегать применения живых вакцин и тесного контакта с лицами, вакцинированными живыми вакцинами (см. раздел «Взаимодействие с другими лекарственными средствами»). В случае применения препарата Николимус у пациентов младше 18 лет следует провести все рекомендованные местным календарем прививок противовирусные вакцинации.
Заживление ран
Нарушение процесса заживления ран является класс-эффектом производных рапамицина, включая эверолимус. Необходимо соблюдать осторожность при применении препарата Николимус в периоперационном периоде.
Влияние на способность управлять транспортными средствами и механизмами
Исследования влияния эверолимуса на способность управлять транспортными средствами и механизмами не проводились. Учитывая возможность развития некоторых побочных реакций на фоне приема препарата Николимус (усталость, головокружение, сонливость), пациентам следует соблюдать осторожность при управлении транспортными средствами и занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания.
Форма выпуска
Таблетки 2,5 мг, 5,0 мг, 10,0 мг.
По 10 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой печатной лакированной.
По 3 контурных ячейковых упаковки вместе с пакетиком силикагеля в пакет термосвариваемый из буфлена или фольги ламинированной. По 1 пакету термосвариваемому вместе с инструкцией по применению в пачку из картона для потребительской тары. Пачки помещают в групповую упаковку.
Условия хранения
Хранить в оригинальной упаковке производителя (контурные ячейковые упаковки, помещенные в пакет, в пачке) при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Срок годности
2 года.
После вскрытия пакета таблетки хранить при температуре не выше 25 °С в течение 1 месяца
Не применять по истечении срока годности.
Владелец регистрационного удостоверения/Организация, принимающая претензии потребителей
АО «Фармасинтез-Норд», Россия,
194356, Россия, г. Санкт-Петербург, дорога в Каменку, д. 74, пом. 1-Н
Производители
АО «Фармасинтез», Россия.
Юридический адрес:
664007, г. Иркутск, ул. Красногвардейская, д. 23, оф. 3;
Адрес производственной площадки:
г. Иркутск, ул. Р. Люксембург, д. 184. или
АО «Фармасинтез-Норд», Россия.
Юридический адрес:
194356, г. Санкт-Петербург, дорога в Каменку, д. 74, пом. 1-Н;
Адрес производственной площадки:
г. Санкт-Петербург, дорога в Каменку, д. 74, лит. А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Афинитор® (10 мг)
МНН: Эверолимус
Производитель: Новартис Фарма Штейн АГ
Анатомо-терапевтическо-химическая классификация: Everolimus
Номер регистрации в РК:
№ РК-ЛС-5№019539
Информация о регистрации в РК:
10.10.2017 — 10.10.2022
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
36 847.73 KZT
- Скачать инструкцию медикамента
Торговое название
Афинитор®
Международное непатентованное название
Эверолимус
Лекарственная форма
Таблетки 5 мг и 10 мг
Состав
Одна таблетка содержит
активное вещество — эверолимус 5 мг или 10 мг,
вспомогательные вещества: лактоза безводная, кросповидон, гидроксипропилметилцеллюлоза, лактозы моногидрат, магния стеарат, бутилгидрокситолуол (ВНТ).
Описание
Таблетки от белого до слегка желтоватого цвета, продолговатой формы, со скошенными краями, без риски, с гравировкой «NVR» на одной стороне и «5» (для дозировки 5 мг) или «UHE» (для дозировки 10 мг) на другой стороне.
Фармакотерапевтическая группа
Противоопухолевые препараты. Противоопухолевые препараты другие. Ингибиторы протеинкиназы. Эверолимус.
Код АТХ L01XE10
Фармакологические свойства
Фармакокинетика
Всасывание
При приеме препарата Афинитор® у пациентов с распространенными солидными опухолями концентрация эверолимуса достигает пикового значения спустя 1-2 часа после приема внутрь в дозах от 5 до 70 мг натощак или с небольшим количеством нежирной пищи.
Cmax изменяется пропорционально дозе в диапазоне от 5 до 10 мг при приеме препарата ежедневно. При приеме разовых доз эверолимуса 20 мг и выше возрастание Cmax происходит менее чем пропорционально дозе, однако значения площади под кривой «концентрация-время» (AUC) увеличиваются пропорционально дозе при приеме в диапазоне доз от 5 мг до 70 мг препарата.
Влияние пищи
У здоровых людей пища с высоким содержанием жира уменьшала систематическое воздействие 10 мг эверолимуса (по данным AUC) на 22%, а наивысшую концентрацию в плазме Cmax на 54%. Пища с низким содержание жиров снижала AUC на 32% и Cmax на 42%. Однако прием пищи не оказывал значимого влияния на время концентрации фазы после всасывания.
Распределение
Соотношение кровь/плазма для эверолимуса, зависящее от концентрации в диапазоне от 5 до 5000 нг/мл, составляет от 17% до 73%. Количество эверолимуса, находящегося в плазме, составляет примерно 20% от общей концентрации в крови, что наблюдается у больных раком пациентов, принимающих Афинитор® по 10 мг/сут. Связывание с белками плазмы составляет приблизительно 74% как у здоровых добровольцев, так и у пациентов с умеренными нарушениями функции печени.
В экспериментальных исследованиях на животных было показано, что после в/в введения проницаемость эверолимуса через гематоэнцефалический барьер (ГЭБ) зависит от дозы нелинейно, что предполагает насыщение насоса гематоэнцефалического барьера, обеспечивающего попадание препарата из крови в ткани мозга. Проникновение эверолимуса через ГЭБ продемонстрировано также у животных при введении препарата внутрь.
Метаболизм
Эверолимус является субстратом CYP3A4 и Р-гликопротеина (PgP). После перорального приема эверолимус является основным циркулирующим компонентом в крови человека. В крови человека были обнаружены шесть основных метаболитов эверолимуса, включая три моногидроксилированных метаболита, два гидроксилированных продукта с открытым кольцом и фосфатидилхолиновый конъюгат эверолимуса. Эти метаболиты были также обнаружены у животных при исследовании токсичности. Активность этих метаболитов была почти в 100 раз меньше активности эверолимуса. Таким образом, эверолимус играет главную роль в общей фармакологической активности.
Элиминация
Специальных исследований выведения препарата с участием онкологических пациентов не проводилось, однако имеются данные исследований с участием пациентов, перенесших трансплантацию. После однократного приема эверолимуса, меченого радиоактивным изотопом, вместе с циклоспорином 80% радиоактивности выводилось с фекалиями, а 5% — с мочой. В кале и моче исходное вещество обнаружено не было.
Средний элиминационный период полувыведения эверолимуса составляет примерно 30 часов.
Фармакокинетика равновесного состояния
После приема препарата Афинитор® пациентами с распространенными солидными опухолями равновесное значение AUC0-τ было пропорционально дозе в диапазоне дневных доз от 5 до 10 мг. Равновесное состояние достигалось в течение 2 недель. Значение Cmax является пропорциональным дозе между 5 и 10 мг. Значение tmax наблюдается через 1-2 часа после приема дозы. Значение AUC0-τ и минимальная концентрация перед приемом дозы значительно коррелировали при ежедневном приеме эверолимуса.
Особые группы пациентов
Нарушение функции печени
Среднее значение AUC эверолимуса у 8 человек с умеренным нарушением функции печени (класс В по Чайлд-Пью) вдвое превышало показатель, зафиксированный у 8 человек с нормальной функцией печени.
У 34 человек с различными нарушениями функции печени системное воздействие препарата (AUC(0-inf)) повышалось в 1.6, 3.3 и 3.6 раз при наличии незначительной (класс А по шкале Чайлд-Пью), умеренной (класс В по шкале Чайлд-Пью) и тяжелой (класс С по шкале Чайлд-Пью) степеней нарушения функции печени соответственно.
Нарушение функции почек
У пациентов с распространенными солидными опухолями существенного влияния клиренса креатинина (25-178 мл/мин) на значение CL/F эверолимуса обнаружено не было. Нарушение функции почек после трансплантации (диапазон клиренса креатинина 11-107 мл/мин) не влияло на фармакокинетику эверолимуса у пациентов, перенесших трансплантацию.
Пациенты пожилого возраста
При фармакокинетической оценке онкологических больных значительного влияния возраста (27-85 лет) на клиренс эверолимуса при пероральном приеме обнаружено не было.
Этническая принадлежность
Клиренс эверолимуса при пероральном приеме (CL/F) является сходным у больных раком среди пациентов-японцев и пациентов европеоидной расы с одинаковой функцией печени. Основываясь на анализе популяционной фармакокинетики, клиренс эверолимуса при пероральном приеме (CL/F) у пациентов негроидной расы в среднем на 20% выше, чем у пациентов европеоидной расы, перенесших трансплантацию.
Фармакодинамика
Механизм действия
Эверолимус является селективным ингибитором mTOR (мишени рапамицина у млекопитающих). mTOR представляет собой основную серин-треонинкиназу, активность которой повышается при развитии многих видов онкологических заболеваний человека.
Эверолимус связывается с внутриклеточным белком FKBP-12, образуя комплекс, подавляющий активность комплекса 1mTOR (mTORC1). Угнетение сигнального пути mTORC1 препятствует трансляции и синтезу белков путем снижения активности рибосомальной протеинкиназы S6 (S6K1) и эукариотического фактора инициации 4E-связующего белка (4EBP-1), регулирующих функцию белков, задействованных в клеточном цикле, ангиогенезе и гликолизе, что приводит в дальнейшем к подавлению роста опухоли и уменьшению экспрессии фактора роста эндотелия сосудов (VEGF), усиливающего процессы ангиогенеза опухоли. Эверолимус является сильнодействующим ингибитором роста и пролиферации опухолевых клеток, клеток эндотелия, фибробластов и гладкомышечных клеток кровеносных сосудов и снижает гликолиз в солидных опухолях in vitro и in vivo.
Показания к применению
-
гормональный рецептороположительный распространенный рак молочной железы в сочетании с ингибитором ароматазы, после предварительной гормональной терапии у женщин в постменопаузе
-
распространенные нейроэндокринные опухоли поджелудочной железы
-
распространенная почечно-клеточная карцинома
-
лечение пациентов с комплексом туберозного склероза (КТС) и почечной ангиомиолипомой, не требующим немедленного хирургического вмешательства
-
лечение пациентов с КТС и субэпендимальной гигантоклеточной астроцитомой (СЭГА), не требующей немедленного хирургического вмешательства
Способ применения и дозы
Лечение препаратом Афинитор® должно назначаться строго врачом, имеющим опыт применения противоопухолевой терапии и лечения пациентов с КТС.
Рекомендованная доза составляет 10 мг эверолимуса 1 раз в сутки. Терапию препаратом продолжают до тех пор, пока сохраняется клинический эффект, либо пока не разовьется неприемлемая токсичность.
В случае пропуска дозы не следует принимать дополнительную дозу, а принять обычную следующую назначенную дозу.
Препарат Афинитор® следует принимать внутрь один раз в сутки в одно и то же время ежедневно, независимо от приема пищи.
Таблетки проглатывают, запивая стаканом воды. Таблетки не следует разжевывать или измельчать. В случае если пациент не может проглотить таблетку, препарат необходимо полностью растворить в стакане с водой (около 30 мл), аккуратно помешивая до полного растворения таблеток (таблетки) (приблизительно 7 минут), непосредственно перед приемом препарата. Затем стакан следует ополоснуть тем же количеством воды и полностью выпить содержимое, чтобы убедиться в приеме полной дозы препарата.
Дозировка при гормональном рецептороположительном распространенном раке молочной железы, распространенных нейроэндокринных опухолях поджелудочной железы, раке почки, КТС с почечной ангиомиолипомой: рекомендуемая доза препарата Афинитор® составляет 10 мг, принимается один раз в день.
Дозировка при КТС с субэпендимальной гигантоклеточной астроцитомой (СЭГА):
Может потребоваться осторожное титрование дозы для того, чтобы добиться оптимального терапевтического эффекта. Переносимые эффективные дозы подбираются для пациентов индивидуально. Сопутствующее антиэпилептическое лечение может влиять на метаболизм эверолимуса и способствовать варьированию исходов у разных пациентов. Способ применения индивидуализирован на основе площади поверхности тела (ППТ, в м2) с помощью формулы Дюбуа, где вес (W) измеряется в килограммах, а рост (H) в сантиметрах:
ППТ = (W0.425 х H0.725) х 0,007184
Рекомендуемая начальная суточная доза препарата Афинитор® для лечения пациентов с КТС, у которых наблюдается СЭГА, составляет 4,5 мг/м2, округляется до ближайшей дозировки таблеток препарата Афинитор®. Более высокая начальная доза 7 мг/м2 рекомендуется пациентам в возрасте от 1 года до (не включительно) 3 лет, на основании фармакокинетического моделирования. Можно комбинировать различные дозировки таблеток для достижения желаемой дозы.
Минимальные концентрации эверолимуса в цельной крови необходимо оценивать как минимум через 1 неделю после начала лечения пациентов в возрасте < 3 лет и приблизительно через 2 недели после начала лечения пациентов в возрасте ≥ 3 лет. Дозу необходимо титровать так, чтобы получить минимальные концентрации от 5 до 15 нг/мл. Для достижения оптимальной эффективности дозу можно увеличивать с учетом переносимости так, чтобы получить более высокую минимальную концентрацию в пределах целевого диапазона.
Рекомендации по дозировке для педиатрических пациентов с СЭГА сопоставимы с дозами у взрослых пациентов группы с СЭГА, за исключением пациентов в возрасте от 1 года до (не включительно) 3 лет, и с дозами у пациентов с нарушением функции печени.
Объем СЭГА должен определяться примерно через 3 месяца после начала лечения препаратом Афинитор®, с последующей коррекцией дозы с учетом изменения объема СЭГА, соответствующего минимальной концентрации и переносимости.
После стабилизации дозы, мониторинг минимальной концентрации должен проводиться каждые 3-6 месяцев у пациентов с изменением площади поверхности тела, и каждые 6-12 месяцев у пациентов со стабильной площадью поверхности тела в течение всего срока лечения.
Продолжать лечение до достижения клинической пользы или до появления признаков неприемлемой токсичности.
Если доза пропущена, пациент не должен принимать дополнительную дозу, а принять назначенную обычную следующую дозу.
Корректировка дозы по причине нежелательных реакций
Управление тяжелыми или непереносимыми побочными реакциями может потребовать временного прерывания лечения (с или без снижения дозы) или прекращение терапии препаратом Афинитор®. При нежелательных реакциях степени 1 корректировка дозы обычно не требуется. Если требуется снижение дозы, предлагаемая доза должна быть приблизительно на 50% ниже (5 мг в день), чем ранее применявшаяся суточная доза. При снижении доз ниже наименьшей концентрации следует рассмотреть прием дозы через день.
Таблица 1
Корректировка дозы препарата Афинитор® и рекомендации по управлению нежелательными реакциями на лекарство
|
Нежелательная реакция на лекарство |
Тяжесть1 |
Корректировка дозы и рекомендации по управлению |
|
Неинфекционный пневмонит |
Степень 2 (наличие симптомов, не влияющих на повседневные жизненные активности) Степень 3 (наличие симптомов, влияющих на повседневные жизненные активности, требуется кислородная терапия) Степень 4 (наблюдаются симптомы, опасные для жизни, показана дополнительная вентиляция легких) |
Рассмотрите возможность прерывания терапии, исключите инфекцию и рассмотрите вариант лечения кортикостероидами, пока симптомы не улучшатся до Степени < 1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50% (5 мг). Прекратите прием, если не наступает улучшение симптоматики в течение 4 недель. Прервите прием препарата Афинитор®, пока симптомы не улучшатся до Степени<1. Рассмотреть возможность возобновления приема препарата Афинитор®, сократив ранее применяемую суточную дозу как минимум на 50 % (5 мг). Если симптомы Степени 3 не проходят, следует отменить данный препарат. Прекратите прием препарата Афинитор®. |
|
Стоматит |
Степень 2 (выраженные симптомы стоматита, но глотательная и жевательная функции сохранены, диета обычная) Степень 3 (выраженные симптомы стоматита, глотательная и жевательная функции нарушены) Степень 4 (симптомы, связанные с опасными для жизни последствиями) |
Временное прерывание приема до улучшения состояния до степени< 1. Восстановить прием препарата Афинитор® в той же дозе. Если возникает рецидив стоматита 2 степени, прервать прием препарата до улучшения состояния до степени< 1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50% . Временное прерывание приема до улучшения состояния до степени< 1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50% . Прекратите прием препарата Афинитор®. |
|
Другие не гематологические виды токсичности (исключая метаболические состояния) |
Степень 2 Степень 3 Степень 4 |
Если токсичность переносима, корректировка дозы не требуется. Если токсичность становится непереносимой, необходимо временное прерывание дозы до улучшения состояния до степени<1. Восстановите прием препарата Афинитор® в той же дозе. Если возникает рецидив токсичности 2 степени, прервите прием препарата Афинитор® до улучшения состояния до степени<1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. Временное прерывание дозы до улучшения состояния до степени<1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. Если возникает рецидив токсичности 3 степени, прием препарата Афинитор® следует прекратить. Прекратите прием препарата Афинитор® и принимайте соответствующую медикаментозную терапию. |
|
Метаболические события (например, гипергликемия, дислипидемия) |
Степень 2 Степень 3 Степень 4 |
Корректировка дозы не требуется. Временное прерывание дозы. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. Прекратите прием препарата Афинитор® |
|
Тромбоцитопения |
Степень 2 (<75, ≥ 50 x 109/л) Степень 3 и 4 (<50 x 109/л) |
Временное прерывание дозы до улучшения состояния до степени1. Восстановите прием препарата Афинитор® в той же дозе. Временное прерывание дозы до улучшения состояния до степени1. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. |
|
Нейтропения |
Степень 2 (≥1 x 109/л) Степень 3 (<1, ≥0,5 x 109/л) Степень 4 (<0,5 x 109/л) |
Корректировка дозы не требуется. Временное прерывание дозы до улучшения состояния до степени2 (≥1 x 109/л). Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. Временное прерывание дозы до улучшения состояния до степени2 (≥1 x 109/л). Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. |
|
Фебрильная нейтропения |
Степень 3 Степень 4 |
Временное прерывание дозы до улучшения состояния до степени2 (≥1,25 x 109/л) и отсутствие лихорадки. Возобновить прием препарата, сократив ранее применяемую суточную дозу как минимум на 50%. Прекратите прием препарата Афинитор®. |
Классификация по степени основана на общей терминологии, используемой в описании критериев нежелательных явлений Национального института рака, версия 3.0.
Терапевтический лекарственный мониторинг
Требуется с помощью валидированного анализа выполнять терапевтический лекарственный мониторинг концентраций эверолимуса в крови пациентов, получающих лечение при СЭГА. Минимальные концентрации должны оцениваться приблизительно через 2 недели после начальной дозы, после любого изменения дозы или лекарственной формы препарата, после начала или изменения сопутствующего применения индукторов или ингибиторов CYP3A4 (смотрите разделы «Лекарственные взаимодействия» и «Особые указания») или после любого изменения состояния функции печени (по шкале Чайлд-Пью). Для пациентов в возрасте <3 лет минимальные концентрации должны контролироваться как минимум через 1 неделю после начала лечения или после любого изменения дозы или лекарственной формы препарата.
Терапевтический лекарственный мониторинг концентраций эверолимуса в крови с валидированным анализом является вариантом выбора. Данный вариант рассматривается в отношении пациентов, получающих лечение при ангиомиолипоме почки, ассоциированной с КТС, после начала сопутствующего применения или изменения применения индукторов или ингибиторов CYP3A4 (см. разделы «Лекарственные взаимодействия» и «Особые указания») или после любого изменения состояния функции печени (по шкале Чайлд-Пью).
По возможности необходимо проводить одинаковый анализ в одной лаборатории для терапевтического лекарственного мониторинга в течение периода лечения.
Дозировка для особых групп населения:
Пациенты в возрасте ≤ 18 лет
-
Афинитор® не рекомендуется для лечения рака у детей и подростков в возрасте от 0 до 18 лет.
-
Афинитор® не рекомендуется для лечения детей и подростков в возрасте от 0 до 18 лет с КТС, у которых наблюдается почечная ангиомиолипома при отсутствии СЭГА.
-
Нет данных об исследованиях по применению препарата Афинитор® у детей в возрасте до 1 года с КТС с СЭГА
Результаты клинических исследований не показали воздействия препарата Афинитор® на рост и развитие в пубертатный период.
Пациенты пожилого возраста (≥65 лет)
Коррекция дозы не требуется.
Пациенты с нарушениями функции почек
Коррекция дозы не требуется.
Пациенты с нарушением функции печени
Гормональный рецептороположительный распространенный рак молочной железы, распространенные нейроэндокринные опухоли поджелудочной железы, распространенная почечно-клеточная карцинома и КТС с почечной ангиомиолипомой:
-
Незначительная печеночная недостаточность (класс А по шкале Чайлд-Пью) – рекомендуемая суточная доза составляет 7,5 мг.
-
Умеренная печеночная недостаточность (класс В по шкале Чайлд-Пью) – рекомендуемая суточная доза составляет 5 мг.
-
Тяжелая печеночная недостаточность (класс С по шкале Чайлд-Пью) – не рекомендуется. Если ожидаемая польза перевешивает риск, не следует превышать суточную дозу 2,5 мг.
-
Необходимо корректировать дозу, если класс печеночной недостаточности пациента (по шкале Чайлд-Пью) во время лечения изменяется.
КТС с СЭГА:
Пациенты в возрасте < 18 лет:
Препарат Афинитор® не рекомендуется пациентам в возрасте < 18 лет с СЭГА и нарушением функции печени.
Пациенты в возрасте ≥ 18 лет:
-
Легкое нарушение функции печени (класс А по шкале Чайлд-Пью) – 75% дозы, рассчитываемой на основе ППТ (округляется до ближайшей дозировки)
-
Умеренная печеночная недостаточность (класс В по шкале Чайлд-Пью) – 25% дозы, рассчитываемой на основе ППТ (округляется до ближайшей дозировки)
-
Тяжелая печеночная недостаточность (класс С по шкале Чайлд-Пью) – не рекомендуется
Концентрация эверолимуса в цельной крови должна оцениваться примерно через 2 недели после начала лечения или после любых изменений класса печеночной недостаточности (по шкале Чайлд-Пью).
Побочные действия
Обзор профиля безопасности
Профиль безопасности основан на совокупности данных по 2672 пациентам, проходившим лечение с применением препарата Афинитор® в ходе 10 клинических исследований, включавших 5 рандомизированных двойных слепых плацебо-контролируемых исследований III фазы и 5 открытых исследований I и II фазы, связанных с зарегистрированными показаниями.
По сводным данным, наиболее распространенными нежелательными реакциями (частота возникновения ≥ 1/10) были (в порядке снижения частоты): стоматит, кожная сыпь, повышенная утомляемость, диарея, инфекции, тошнота, снижение аппетита, анемия, дисгевзия, пневмонит, периферические отеки, гипергликемия, астения, зуд, снижение массы тела, гиперхолестеринемия, носовое кровотечение, кашель и головная боль.
Наиболее распространенными нежелательными явлениями 3–4 степени тяжести (частота возникновения ≥ 1/100 — < 1/10) были стоматит, анемия, гипергликемия, инфекции, повышенная утомляемость, диарея, пневмонит, астения, тромбоцитопения, нейтропения, одышка, протеинурия, лимфопения, кровотечения, гипофосфатемия, кожная сыпь, гипертензия, пневмония, повышение уровня аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и сахарный диабет.
Побочные действия по результатам онкологических исследований:
Очень часто (≥ 1/10)
-
инфекции a, *
-
анемия
-
снижение аппетита, гипергликемия, гиперхолестеринемия
-
дисгевзия, головная боль
-
пневмонит c, носовое кровотечение, кашель
-
стоматит d, диарея, тошнота
-
кожная сыпь, зуд
-
утомляемость, астения, периферический отек
-
снижение массы тела
Часто (от ≥ 1/100 до < 1/10)
-
тромбоцитопения, нейтропения, лейкопения, лимфопения
-
гипертриглицеридемия, гипофосфатемия, сахарный диабет, гиперлипидемия, гипокалиемия, обезвоживание, гипокальциемия
-
бессонница, отек век, кровотечение b, гипертензия
-
одышка
-
рвота, сухость во рту, боль в животе, боль во рту, воспаления слизистой оболочки, диспепсия, дисфагия
-
сухость кожи, ломкость ногтей, легкая форма алопеции, акне, эритема, онихоклазия, синдром ладонно-подошвенной эритродизестезии, шелушение кожи, повреждения кожи
-
артралгия
-
протеинурия*, почечная недостаточность*
-
нарушения менструального цикла e
-
лихорадка, увеличение уровня АСТ, АЛТ, креатинина в крови
Нечасто (от ≥ 1/1000 до < 1/100)
-
панцитопения
-
гиперчувствительность
-
потеря вкуса
-
конъюнктивит
-
застойная сердечная недостаточность
-
гиперемия, тромбоз глубоких вен
-
кровохарканье, эмболия легочной артерии
-
повышенное мочеиспускание в дневное время, острая почечная недостаточность*
-
аменореяe
-
некардиальная боль в грудной клетке, нарушение заживления ран
Редко (от ≥1/10 000 до <1/1000)
-
истинная красноклеточная аплазия
-
респираторный дистресс-синдром взрослых
-
ангионевротический отек
* Также см. подраздел «Описание отдельных нежелательных реакций».
a Включает все явления в рамках класса системы органов «Инфекции и инвазии», включая (часто) пневмонию, инфекции мочевыводящих путей, (нечасто) бронхит, опоясывающий герпес, сепсис, абсцесс и отдельные случаи оппортунистических инфекций [например, аспергиллез, кандидоз, пневмония, вызванная pneumocystis jirovecii (carinii) (пневмония PJP, PCP), гепатит B (также см. раздел «Особые указания»)] и (редко) вирусный миокардит.
b Включает эпизоды кровотечения разных локализаций, не перечисленные поименно.
c Включает (часто) пневмонит, интерстициальное заболевание легких, инфильтрацию легких и (редко) легочное альвеолярное кровоизлияние, легочную токсичность и альвеолит
d Включает (очень часто) стоматит, (часто) афтозный стоматит, образование язв на слизистой оболочке языка и ротовой полости и (нечасто) глоссодинию, глоссит.
e Частота указана на основании количества женщин в возрасте от 10 до 55 лет в сводных данных.
Описание отдельных нежелательных реакций
По результатам клинических исследований и спонтанно поступающих сообщений в пострегистрационном периоде, прием эверолимуса приводил к серьезным случаям реактивации вируса гепатита В, включая летальные случаи. Реактивация инфекции является ожидаемым явлением на протяжении периода иммуносупрессии.
По результатам клинических исследований и спонтанно поступающих сообщений в пострегистрационном периоде, прием эверолимуса был связан со случаями почечной недостаточности (включая летальные случаи) и протеинурии. Рекомендуется тщательно контролировать функцию почек (см. раздел «Особые указания»).
По результатам клинических исследований и спонтанно поступающих сообщений в пострегистрационном периоде, прием эверолимуса был связан со случаями аменореи (вторичная аменорея и другие нарушения менструального цикла).
По результатам клинических исследований и спонтанно поступающих сообщений в пострегистрационном периоде, прием эверолимуса был связан со случаями пневмонии, вызванной pneumocystis jirovecii (carinii) (пневмонии PJP, PCP), некоторые с летальным исходом (см. раздел «Особые указания»).
По результатам клинических исследований и спонтанно поступающих сообщений в пострегистрационном периоде, сообщалось о случаях ангионевротического отека при одновременном применении с ингибиторами АПФ или без такового (см. раздел «Особые указания»).
Пациенты пожилого возраста
В сводных данных по безопасности 37% пациентов, получавших Афинитор, были в возрасте ≥ 65 лет. Число пациентов, у которых появились нежелательные реакции, которые повлекли за собой прекращение приема препарата, было выше среди пациентов в возрасте ≥ 65 лет (20% по сравнению с 13%). Наиболее частыми нежелательными реакциями, повлекшими за собой отмену препарата, являлись пневмонит (включая интерстициальное заболевание легких), стоматит, повышенная утомляемость и одышка.
При комплексе туберозного склероза (КТС)
Краткий обзор профиля безопасности
Профиль безопасности препарата Афинитор® составлен на основе двух рандомизированных двойных слепых плацебо-контролируемых базовых исследований фазы III и исследования фазы II.
-
EXIST‑2 (CRAD001M2302) — рандомизированное двойное слепое контролируемое исследование фазы III по сравнению эверолимуса (n=79) с плацебо (n=39) у пациентов либо с КТС плюс ангиомиолипома почки (n=113), либо спорадический лимфангиолейомиоматоз плюс ангиомиолипома почки (n=5). Средняя продолжительность слепого этапа исследования составляла 48,1 недели (диапазон от 2 до 115) у пациентов, получающих препарат Афинитор®, и 45,0 недели (диапазон от 9 до 115) у тех, кто получал плацебо. Не наблюдалось различий между двумя группами в отношении процента пациентов, которые прекратили лечение по причине нежелательных лекарственных реакций (НЛР) (2,5% при эверолимусе по сравнению с 2,6% при плацебо). Суммарное воздействие препарата Афинитор® (112 пациентов, которые приняли по крайней мере одну дозу эверолимуса) со средней продолжительностью воздействия до 204,1 недели (диапазон от 2 до 278) было связано с коэффициентом прекращения лечения по причине НЛР 7,1 % (n=8/112).
-
EXIST‑1 (CRAD001M2301) — рандомизированное двойное слепое контролируемое исследование фазы III эверолимуса (n=78) по сравнению с плацебо (n=39) у пациентов с КТС, у которых имелась СЭГА, независимо от возраста. Средняя продолжительность слепого этапа исследования составляла 52,2 недели (диапазон от 24 до 89) у пациентов, получающих препарат Афинитор®, и 46,6 недели (диапазон от 14 до 88) у тех, кто получал плацебо. В течение фазы слепого этапа исследования никто из пациентов не прекратил применение исследуемого препарата по причине НЛР. Суммарное воздействие препарата Афинитор® (111 пациентов, которые приняли по крайней мере одну дозу эверолимуса) со средней продолжительностью воздействия до 204,9 недели (диапазон от 8,1 до 253,7) было связано с коэффициентом прекращения лечения по причине НЛР 7,2% (n=8/111).
-
CRAD001C2485 — проспективное открытое несравнительное исследование фазы II применения эверолимуса у пациентов с СЭГА (n=28). Средняя продолжительность воздействия составляла 67,8 месяца (диапазон от 4,7 до 83,2). Никто из пациентов не прекратил применение исследуемого препарата по причине НЛР.
Наиболее частыми нежелательными реакциями (частота возникновения ≥1/10 и, по предположению исследователя, связанная с лечением) в объединенных данных о безопасности являются (в порядке убывания): стоматит, инфекции верхних дыхательных путей, аменорея, гиперхолестеринемия, назофарингит, акне, нарушение менструального цикла, синусит, отит среднего уха и пневмония.
Наиболее частыми нежелательными реакциями степени 3‑4 (частота возникновения ≥1%) являлись стоматит, аменорея, пневмония, нейтропения, пирексия, вирусный гастроэнтерит и целлюлит. Степени соответствуют общей терминологии, используемой в описании критериев нежелательных явлений, версия 3.0.
Очень часто (≥ 1/10)
-
инфекции верхних дыхательных путей, назофарингит, синусит, отит среднего уха, пневмония a
-
гиперхолестеринемия
-
стоматит b
-
акне
-
аменорея d, нарушение менструального цикла d
Часто (от ≥ 1/100 до< 1/10)
-
инфекции мочевыводящих путей, фарингит, целлюлит, стрептококковый фарингит, вирусный гастроэнтерит, гингивит, опоясывающий герпес
-
нейтропения, анемия, лейкопения, лимфопения, тромбоцитопения
-
гиперлипидемия, снижение аппетита, гипертриглицеридемия, гипофосфатемия, гипергликемия
-
головная боль, дисгевзия
-
гипертензия, лимфостаз
-
кашель, носовое кровотечение, пневмонит
-
диарея, тошнота, рвота, боли в животе, боль во рту, метеоризм, запор, гастрит
-
сыпь c, угревой дерматит, сухость кожи, зуд, алопеция
-
протеинурия
-
влагалищные кровотечения, меноррагии, киста яичника, задержка менструаций d
-
усталость, лихорадка, раздражительность, агрессия
-
повышение уровня лактатдегидрогеназы крови, повышение уровня лютеинизирующего гормона крови, снижение массы тела
Нечасто (от ≥ 1/1000 до < 1/100)
-
вирусный бронхит
-
гиперчувствительность
-
бессонница
-
ангионевротический отек
-
рабдомиолиз
-
повышение уровня фолликулостимулирующего гормона крови
a Включает пневмонию, вызванную pneumocystis jirovecii (carinii) (PJP, PCP)
b Включает (очень часто) стоматит, язвы полости рта, афтозный стоматит и (нечасто) боль десен, глоссит, язвы на губах, язвы на языке
c Включает (часто) сыпь, эритематозную сыпь, эритему и (нечасто) макулезную сыпь, макулопапулезную сыпь, генерализованную сыпь
d Частота основана на взятом из объединенных сведений количестве данных женщин в возрасте от 10 до 55 лет, получающих лечение
Описание отдельных нежелательных реакций
В клинических исследованиях эверолимус был связан с серьезными случаями реактивации гепатита B, включая летальный исход. Реактивация инфекции является предполагаемой реакцией в периоды иммуносупрессии.
В клинических исследованиях и постмаркетинговых спонтанных сообщениях эверолимус был связан с явлениями почечной недостаточности (включая летальный исход), протеинурией и повышением креатинина сыворотки. Рекомендуется мониторинг функции почек (см. раздел «Особые указания»).
В клинических исследованиях эверолимус был связан с явлениями кровотечения. В редких случаях на фоне онкологии наблюдались летальные исходы (см. раздел «Особые указания»). При КТС никаких серьезных случаев почечного кровотечения не сообщалось.
В клинических исследованиях и постмаркетинговых спонтанных сообщениях эверолимус был связан со случаями пневмонии, вызванной pneumocystis jirovecii (carinii), (пневмония PJP, PCP), некоторыми с летальным исходом (см. раздел «Особые указания»).
Дополнительно, имеющими значение нежелательными реакциями, наблюдаемыми в онкологических клинических исследованиях и постмаркетинговых спонтанных сообщениях, были сердечная недостаточность, легочная эмболия, тромбоз глубоких вен, ухудшение заживления ран и гипергликемия.
В клинических исследованиях и постмаркетинговых спонтанных сообщениях при сопутствующем применении или без применения ингибиторов ангиотензинпревращающего фермента, сообщалось об ангионевротическом отеке (см. раздел «Особые указания»).
Дети и подростки
В базовом исследовании фазы II, 22 из 28 исследуемых пациентов с СЭГА были в возрасте до 18 лет, и в базовом исследовании фазы III 101 из 117 исследуемых пациентов с СЭГА были в возрасте до 18 лет. В обоих исследованиях частота возникновения, тип и тяжесть наблюдаемых нежелательных реакций у детей и подростков в основном соответствовали тем, что наблюдались у взрослых, за исключением инфекций, которые сообщались с большей частотой особенно у детей в возрасте до 3 лет.
Противопоказания
-
повышенная чувствительность к активному веществу, а также другим производным рапамицина или любому из вспомогательных веществ препарата
Лекарственные взаимодействия
Эверолимус является субстратом CYP3A4, а также субстратом и умеренным ингибитором PgP. Таким образом, абсорбция и последующая элиминация эверолимуса могут быть подвержены влиянию препаратов, которые воздействуют на CYP3A4 и/или PgP. In vitro эверолимус является конкурентным ингибитором CYP3A4 и смешанным ингибитором CYP2D6.
Установленные, в том числе теоретически, взаимодействия с селективными ингибиторами и индукторами CYP3A4 и PgP перечислены в Таблице 2.
Ингибиторы CYP3A4 и PgP, увеличивающие концентрацию эверолимуса
Субстанции, которые являются ингибиторами CYP3A4 или PgP, могут увеличивать концентрацию эверолимуса в крови за счет замедления метаболизма или выделения эверолимуса из клеток кишечника.
Индукторы CYP3A4 и PgP, снижающие концентрацию эверолимуса
Субстанции, которые являются индукторами CYP3A4 или PgP, могут снижать концентрацию эверолимуса в крови за счет замедления метаболизма или выделения эверолимуса из клеток кишечника.
Таблица 2. Влияние других активных веществ на эверолимус
|
Активное вещество по взаимодействию |
Взаимодействие. Изменение AUC/Cmax эверолимуса Соотношение среднегеометрических величин (наблюдаемый диапазон) |
Рекомендации относительно сопутствующего применения |
|
Сильные ингибиторы CYP3A4/PgP |
||
|
Кетоконазол |
AUC ↑ в 15,3 раза (диапазон 11,2‑22,5) Cmax ↑ в 4,1 раза (диапазон 2,6‑7,0) |
Сопутствующее лечение препаратом Афинитор® и сильными ингибиторами не рекомендуется. |
|
Итраконазол, позаконазол, вориконазол |
Не исследовалось. Предполагается значительное увеличение концентрации эверолимуса. |
|
|
Телитромицин, кларитромицин |
||
|
Нефазодон |
||
|
Ритонавир, атазанавир, саквинавир, дарунавир, индинавир, нелфинавир |
||
|
Умеренные ингибиторы CYP3A4/PgP |
||
|
Эритромицин |
AUC ↑ в 4,4 раза (диапазон 2,0–12,6). Cmax ↑ в 2,0 раза (диапазон 0,9–3,5). |
Проявлять осторожность, когда невозможно избежать сопутствующего применения умеренных ингибиторов CYP3A4 или ингибиторов PgP. Если пациент нуждается в одновременном применении умеренного ингибитора CYP3A4 или PgP, можно рассмотреть вопрос о снижении дозы до 5 мг или 2,5 мг в сутки. Однако клинические данные относительно такой коррекции дозы отсутствуют. Ввиду межсубъектной вариабельности, рекомендуемая коррекция дозы может оказаться непригодной для всех пациентов, поэтому рекомендовано внимательно следить за состоянием пациента, чтобы не пропустить возникновение побочных эффектов. При отмене умеренного ингибитора нужно учесть необходимость отмывочного периода продолжительностью не менее 2–3 дней (среднее время выведения для большинства наиболее часто применяемых умеренных ингибиторов) до возвращения дозы препарата Афинитор к той, которая применялась до начала одновременного применения. Для пациентов с ангиомиолипомой почки, ассоциированной с КТС: Если пациентам требуется сопутствующее применение умеренного ингибитора CYP3A4 или PgP, можно рассмотреть вопрос о снижении дозы до 5 мг или 2,5 мг в сутки. Однако клинические данные относительно такой коррекции дозы отсутствуют. Ввиду межсубъектной вариабельности, рекомендуемая коррекция дозы может оказаться непригодной для всех пациентов, поэтому рекомендовано внимательно следить за состоянием пациента, чтобы не пропустить возникновение побочных эффектов. При отмене умеренного ингибитора нужно учесть необходимость отмывочного периода продолжительностью не менее 2–3 дней (среднее время выведения для большинства наиболее часто применяемых умеренных ингибиторов) до возвращения дозы препарата Афинитор® к той, которая применялась до начала одновременного применения. Для пациентов с СЭГА, ассоциированной с КТС: Если пациентам требуется сопутствующее применение умеренного ингибитора CYP3A4 или PgP, необходимо уменьшить суточную дозу приблизительно на 50%. Может потребоваться дальнейшее снижение дозы, чтобы устранить нежелательные реакции (см. разделы «Способ применения и дозы», «Особые указания»). Минимальные концентрации эверолимуса должны оцениваться приблизительно через 2 недели после включения в лечение умеренного ингибитора CYP3A4 или PgP. Если прекращается применение умеренного ингибитора, рассмотреть возможность установления периода вымывания в течение как минимум 2-3 дней (среднее время выведения для большинства наиболее распространенных умеренных ингибиторов), прежде чем вернуть дозу препарата Афинитор® на уровень ранее применяемой дозы до начала сопутствующего применения. Минимальная концентрация эверолимуса должна оцениваться приблизительно через 2 недели после любого изменения дозы (см. разделы «Способ применения и дозы», «Особые указания». |
|
Иматиниб |
AUC ↑ в 3,7 раза. Cmax ↑ в 2,2 раза. |
|
|
Верапамил |
AUC ↑ в 3,5 раза (диапазон 2,2–6,3). Cmax ↑ в 2,3 раза (диапазон 1,3–3,8). |
|
|
Пероральный циклоспорин |
AUC ↑ в 2,7 раза (диапазон 1,5–4,7). Cmax ↑ в 1,8 раза (диапазон 1,3–2,6). |
|
|
Флуконазол |
Не исследовалось. Предполагается повышенное воздействие. |
|
|
Дилтиазем |
||
|
Дронедарон |
Не исследовалось. Предполагается повышенное воздействие. |
|
|
Ампренавир, фосампренавир |
Не исследовалось. Предполагается повышенное воздействие. |
|
|
Грейпфрутовый сок или другие продукты питания, воздействующие на CYP3A4/PgP |
Не исследовалось. Предполагается повышенное воздействие. |
Следует избегать такой комбинации. |
|
Сильные и умеренные индукторы CYP3A4 |
||
|
Рифампицин |
AUC ↓63% (диапазон 0–80%). Cmax ↓58% (диапазон 10–70%). |
Избегать одновременного применения с сильными индукторами CYP3A4. Для пациентов с ангиомиолипомой почки, ассоциированной с КТС: Если пациентам требуется сопутствующее применение сильного ингибитора CYP3A4, необходимо рассмотреть увеличение дозы препарата Афинитор® с 10 мг в сутки до 20 мг в сутки, используя шаг увеличения 5 мг или менее в День 4 и 8 после начала применения индуктора. Предполагается, что данная доза препарата Афинитор® скорректирует AUC до диапазона, наблюдаемого без индукторов. Тем не менее, клинические данные по данной корректировке дозы отсутствуют. Если лечение с применением индуктора прекращается, рассмотреть возможность установления периода вымывания в течение как минимум 3-5 дней (установленный период значительной деиндукции ферментов), прежде чем вернуть дозу препарата Афинитор® на уровень ранее применяемой дозы до начала сопутствующего применения (также смотрите «Терапевтический лекарственный мониторинг» в разделе «Способ применения и дозы»). Для пациентов с СЭГА, ассоциированной с КТС: Пациентам, получающим одновременно сильные индукторы CYP3A4, может потребоваться увеличенная доза препарата Афинитор®, чтобы достичь такого же воздействия, как и у пациентов, не принимающих сильные индукторы. Дозу необходимо титровать до получения минимальных концентраций в пределах от 5 до 15 нг/мл. Если концентрации ниже 5 нг/мл, суточную дозу можно увеличивать на 2,5 мг каждые 2 недели, контролируя минимальный уровень и оценивая переносимость перед увеличением дозы. Если применение сильного индуктора прекращается, рассмотреть возможность установления периода вымывания в течение как минимум 3-5 дней (установленный период значительной деиндукции ферментов), прежде чем вернуть дозу препарата Афинитор® на уровень ранее применяемой дозы до начала сопутствующего применения. Минимальные концентрации эверолимуса должны оцениваться приблизительно через 2 недели после любого изменения дозы (см. разделы «Способ применения и дозы», «Особые указания»). |
|
Дексаметазон |
Не исследовалось. Предполагается снижение воздействия. |
|
|
Антиэпилептические средства (например, карбамазепин, фенобарбитал, фенитоин) |
Не исследовалось. Предполагается снижение воздействия. |
|
|
Эфавиренз, невирапин |
Не исследовалось. Предполагается снижение воздействия. |
|
|
Зверобой (Hypericum perforatum) |
Не исследовалось. Предполагается значительное снижение воздействия. |
В течение лечения эверолимусом не должны использоваться препараты, содержащие зверобой. |
Препараты, концентрация в плазме которых может изменяться вследствие приема эверолимуса
На основании результатов in vitro установлено, что влияние ингибиторов PgP, CYP3A4 и CYP2D6 на системные концентрации, полученные после пероральных суточных доз 10 мг, маловероятно. Тем не менее, нельзя исключать ингибирование CYP3A4 и PgP в кишечнике. Исследование взаимодействия у здоровых добровольцев показало, что сопутствующее применение пероральной дозы мидазолама, чувствительным маркером субстрата CYP3A, с эверолимусом приводило к 25 % увеличению Cmax мидазолама и 30% увеличению AUC(0-∞) мидазолама. Подобный эффект, вероятно, обусловлен тем, что эверолимус ингибирует CYP3A4 в кишечнике. Следовательно, эверолимус может влиять на биодоступность применяемых одновременно с ним пероральных субстратов CYP3A4. Тем не менее, не предполагается клинически значимого эффекта на воздействие субстратов CYP3A4 при системном введении (см. раздел «Особые указания»).
Одновременное применение эверолимуса и Октреотид-депо увеличивало Cmin последнего с соотношением среднегеометрических величин (эверолимус/плацебо) 1,47. Невозможно установить клинически значимую эффективность ответа на применение эверолимуса у пациентов с распространенными нейроэндокринными опухолями.
Одновременное применение эверолимуса и эксеместана увеличивало Cmin и C2h эксеместана на 45% и 64% соответственно. Однако не было зафиксировано различий в соответствующих уровнях эстрадиола в равновесном состоянии (4 недели) в двух группах лечения. Не наблюдалось увеличения числа нежелательных явлений, связанных с приемом эксеместана среди пациентов с гормон-рецептор-положительным распространенным раком молочной железы, получавших данную комбинацию препаратов. Маловероятно, что повышение уровня эксеместана будет влиять на эффективность или безопасность.
Сопутствующее применение ингибиторов ангиотензинпревращающего фермента
Пациенты с сопутствующей терапией с применением ингибиторов ангиотензинпревращающего фермента (например, рамиприла) находятся в группе повышенного риска ангионевротического отека (см. раздел «Особые указания»).
Вакцинация
Может изменяться иммунный ответ на вакцинацию, и, следовательно, в течение лечения препаратом Афинитор® вакцинация может быть менее эффективной. Во время лечения препаратом Афинитор® следует избегать применения живых вакцин. Примеры живых вакцин: интраназальная гриппозная вакцина, вакцина против кори, паротита, краснухи, пероральная вакцина против полиомиелита, БЦЖ (бацилла Кальметта- Герена), вакцина против желтой лихорадки, ветряной оспы и тифозные вакцины TY21a.
Особые указания
Неинфекционная пневмония
Неинфекционная пневмония является характерным эффектом производных рапамицина, включая эверолимус. Неинфекционная пневмония (включая интерстициальное заболевание легких) очень часто описывалась у пациентов, принимающих эверолимус при распространенной почечно-клеточной карциноме (см. раздел «Побочные действия»). Некоторые случаи были тяжелыми, и в редких случаях наблюдался летальный исход. Диагноз неинфекционной пневмонии необходимо рассматривать у пациентов с наличием неспецифических респираторных признаков и симптомов, таких как гипоксия, плевральный выпот, кашель и одышка, и пациентов, у которых с помощью соответствующих исследований были исключены инфекционные, опухолевые и другие нелекарственные причины. При постановке дифференциального диагноза неспецифической пневмонии должны быть исключены оппортунистические инфекции, такие как пневмония, вызванная pneumocystis jirovecii (carinii) (пневмония PJP, PCP) (см. ниже «Инфекции»). Необходимо рекомендовать пациентам незамедлительно сообщать о любых новых респираторных симптомах или об их ухудшении.
Пациенты, у которых обнаруживаются рентгенологические изменения, с подозрением на неспецифическую пневмонию и пациенты, у которых имеется незначительное количество симптомов, или симптомы отсутствуют, могут продолжать терапию с применением препарата Афинитор® без корректировки доз. Если симптомы умеренные, необходимо рассмотреть вопрос прерывания терапии до снижения симптомов. Может быть показано применение кортикостероидов до устранения клинических симптомов. Допустимо возобновить применение препарата Афинитор®, сократив ранее применяемую суточную дозу как минимум на 50%.
Если симптомы неспецифической пневмонии тяжелые, следует прекратить терапию с применением препарата Афинитор®, и можно назначить применение кортикостероидов до устранения клинических симптомов. Применение препарата Афинитор® можно возобновить в суточной дозе, которая приблизительно на 50% менее ранее применяемой суточной дозы в зависимости от индивидуальной клинической картины.
Если лечение неинфекционной пневмонии требует применения кортикостероидов, то у таких пациентов может рассматриваться возможность проведения профилактики пневмонии, вызванной pneumocystis jirovecii (carinii) (пневмонии PJP, PCP).
Инфекции
Эверолимус обладает иммунодепрессивными свойствами и может способствовать заражению пациентов бактериальными, грибковыми, вирусными или протозойными инфекциями, включая инфекции с оппортунистическими патогенами (смотрите «Побочные действия»). У пациентов, применяющих эверолимус, описывались местные системные инфекции, включая пневмонию, другие бактериальные инфекции, инвазивные грибковые инфекции, такие как аспергиллез, кандидоз или пневмония, вызванная pneumocystis jirovecii (carinii) (пневмония PJP, PCP), и вирусные инфекции, включая реактивацию вируса гепатита B. Некоторые из указанных инфекций были тяжелыми (например, приводящими к сепсису, дыхательной или печеночной недостаточности), а в редких случаях — к летальному исходу.
Врачи и пациенты должны знать о повышенном риске инфекций при применении препарата Афинитор®. Для лечения уже существующих инфекций должна быть назначена соответствующая терапия, и такие инфекции должны полностью регрессировать до начала лечения препаратом Афинитор®. Во время приема препарата Афинитор® следует внимательно наблюдать за симптомами и признаками развития инфекций. При диагностировании инфекционного заболевания немедленно необходимо назначить адекватное лечение, а также рассмотреть возможность временного прекращения приема препарата Афинитор® или его полной отмены.
При диагностировании инвазивной системной грибковой инфекции Афинитор® немедленно отменяют, а пациенту назначают соответствующую противогрибковую терапию.
У пациентов, которые получали эверолимус, отмечались случаи пневмонии, вызванной pneumocystis jirovecii (carinii) (пневмония PJP, PCP), в том числе с летальным исходом. Пневмония PJP/PCP может быть связана с сопутствующим применением кортикостероидов или других иммунодепрессивных препаратов. В случае, когда требуется применение кортикостероидов или других иммунодепрессивных препаратов, необходимо рассмотреть профилактику пневмонии PJP/PCP.
Реакции гиперчувствительности
При применении эверолимуса наблюдались реакции гиперчувствительности, проявляющейся анафилактическими реакциями, одышкой, приливами крови к лицу, болью в груди или ангионевротическим отеком (например, отек дыхательных путей и языка с нарушением дыхания или без такового) и др. (см. раздел «Противопоказания»).
Сопутствующее применение ингибиторов ангиотензинпревращающего фермента
Риск ангионевротического отека (например, отек дыхательных путей или языка с дыхательной недостаточностью или без нее) у пациентов, принимающих сопутствующее лечение ингибиторами ангиотензинпревращающего фермента (например, рамиприлом), повышен (см. раздел «Лекарственные взаимодействия»).
Язвы ротовой полости
У пациентов, получающих лечение препаратом Афинитор®, наблюдались язвы полости рта, стоматит и мукозит слизистой оболочки полости рта (см. раздел «Побочные действия»). В данных случаях рекомендуется местное лечение, причем запрещено использовать средства для полоскания рта, содержащие алкоголь, перекись водорода, производные йода и тимьяна, поскольку они могут усугубить состояние. Не применять противогрибковые препараты за исключением случаев, когда выявляется грибковая инфекция (см. раздел «Лекарственные взаимодействия»).
Кровотечение
У пациентов, получающих лечение эверолимусом при онкологических состояниях, сообщалось о серьезных случаях кровотечения, в том числе с летальным исходом. О серьезных случаях почечного кровотечения при КТС состояниях не сообщалось.
Рекомендуется проявлять осторожность при назначении пациентам, принимающим препарат Афинитор® особенно в течение сопутствующего применения с активными веществами, как известно влияющими на тромбоцитарную функцию или способными повышать риск кровотечения, а также у пациентов с нарушениями свертываемости крови в анамнезе. В период лечения специалисты в области здравоохранения и пациенты должны уделять особое внимание случаям проявления признаков и симптомов кровотечения, особенно при наличии нескольких факторов риска кровотечения.
Почечная недостаточность
Случаи почечной недостаточности (включая острую почечную недостаточность), в том числе с летальным исходом, наблюдались у пациентов, получающих лечение препаратом Афинитор® (см. раздел «Побочные действия»). Необходимо проводить мониторинг функции почек особенно у пациентов, которые имеют дополнительные факторы риска, которые могут привести к нарушению функции почек.
Лабораторные анализы и мониторинг
Функция почек
Сообщалось о повышении креатинина в сыворотке, обычно легкой степени, и протеинурии у пациентов, получающих лечение препаратом Афинитор® (см. раздел «Побочные действия»). До начала лечения препаратом Афинитор® и периодически в дальнейшем рекомендуется проводить мониторинг функции почек, включая измерение азота мочевины крови, белка в моче и креатинина в сыворотке.
Глюкоза в крови
Сообщалось о развитии гипергликемии у пациентов, принимающих Афинитор® (см. раздел «Побочные действия»). До начала лечения препаратом Афинитор® и периодически в дальнейшем рекомендуется проводить мониторинг уровня глюкозы в сыворотке натощак. Осуществление более частого мониторинга рекомендуется в случае, когда Афинитор® применяется одновременно с другими лекарственными препаратами, которые могут вызывать гипергликемию. При возможности должен быть достигнут оптимальный гликемический контроль до начала приема препарата Афинитор®.
Липиды крови
При применении препарата Афинитор® у пациентов сообщалось о возникновении дислипидемии (включая гиперхолестеринемию и гипертриглицеридемию). До начала лечения препаратом Афинитор® и периодически в дальнейшем рекомендуется делать анализ холестерина и триглицеридов в крови, а также соответствующее медикаментозное лечение.
Гематологические показатели
У пациентов, применяющих препарат Афинитор®, сообщалось о пониженном уровне гемоглобина, лимфоцитов, нейтрофилов и тромбоцитов (см. раздел «Побочные действия»). До начала лечения препаратом Афинитор® и периодически в дальнейшем рекомендуется делать общий анализ крови.
Взаимодействия
Следует избегать сопутствующего применения с ингибиторами и индукторами CYP3A4 и/или эффлюксным насосом, обеспечивающим множественную лекарственную устойчивость P‑гликопротеина (PgP). Если невозможно избежать сопутствующего применения умеренного ингибитора или индуктора CYP3A4 и/или PgP, может потребоваться корректировка дозы препарата Афинитор® с учетом ожидаемого значения AUC (см. «Лекарственные взаимодействия»).
Сопутствующее лечение сильными ингибиторами CYP3A4 приводит к значительному повышению концентрации эверолимуса в крови (см. раздел «Лекарственные взаимодействия»). Имеющихся в настоящее время данных недостаточно для составления рекомендаций по дозированию в подобной ситуации. Следовательно, не рекомендуется применять препарат Афинитор® и сильными ингибиторами CYP3A4.
Необходимо проявлять осторожность в случае, когда Афинитор® применяется одновременно с пероральными субстратами CYP3A4 с узким терапевтическим индексом по причине возможного лекарственного взаимодействия. Если Афинитор® применяется с пероральными субстратами CYP3A4 с узким терапевтическим индексом (например, пимозид, терфенадин, астемизол, цизаприд, хинидин или производные алкалоидов спорыньи), необходимо внимательно следить за состоянием пациентов, чтобы не пропустить возникновения нежелательных эффектов, перечисленных в информации о препарате перорального субстрата CYP3A4 (см. раздел «Лекарственные взаимодействия»).
Нарушение функции печени
Для онкологических показаний:
Экспозиция эверолимуса повышалась у пациентов с незначительной (класс A по шкале Чайлд-Пью), умеренной (класс В по шкале Чайлд-Пью) и тяжелой (класс C по шкале Чайлд-Пью) печеночной недостаточностью (см. раздел «Фармакокинетика»).
Рекомендуется применять препарат Афинитор у пациентов с тяжелой печеночной недостаточностью (класс C по шкале Чайлд-Пью), только если ожидаемая польза перевешивает риск (см. разделы «Фармакокинетика» и «Способ применения и дозы»).
В настоящее время нет клинических данных по безопасности и эффективности, которые подтверждали бы рекомендации по коррекции дозы препарата при возникновении нежелательных реакций у пациентов с нарушением функции печени.
Применение препарата Афинитор® не рекомендуется пациентам:
-
с ангиомиолипомой почки, ассоциированной с КТС, и сопутствующим тяжелым нарушением функции печени (класс C по шкале Чайлд-Пью) за исключением случаев, когда потенциальная польза превосходит риск (см. разделы «Фармакокинетика» и «Способ применения и дозы»).
-
в возрасте ≥ 18 лет с СЭГА и сопутствующим тяжелым нарушением функции печени (класс C по шкале Чайлд-Пью) (см. разделы «Фармакокинетика» и «Способ применения и дозы»).
-
в возрасте < 18 лет с СЭГА и сопутствующим нарушением функции печени (класс A, B или C по шкале Чайлд-Пью) (см. разделы «Фармакокинетика» и «Способ применения и дозы»).
Вакцинация
В течение лечения препаратом Афинитор® следует избегать применения живых вакцин (см. раздел «Лекарственные взаимодействия»). Для пациентов детского возраста с СЭГА, которым не требуется неотложное лечение, рекомендуется до начала терапии завершить серию рекомендованных детских прививок живых вирусов в соответствии с местными руководствами по лечению.
Осложнения при заживлении ран
Ухудшение заживления ран характерно для такого класса препаратов, как производные рапамицина, включая препарат Афинитор®. Следовательно, необходимо проявлять осторожность при применении препарата Афинитор® в периоперационный период.
Лактоза
Данный лекарственный препарат не следует применять пациентам с редкими наследственными заболеваниями, такими как непереносимость галактозы, дефицит лактазы Лаппа или синдром мальабсорбции глюкозы и галактозы.
Женщины детородного возраста/контрацепция у мужчин и женщин
В течение применения эверолимуса и в период до 8 недель после окончания лечения женщины детородного возраста должны использовать высокоэффективный метод контрацепции (например, пероральный, инъекционный или гормональный метод контрацепции с применением импланта, не содержащего эстроген, контрацептивные средства на основе прогестерона, гистерэктомия, перевязка маточных труб, полное воздержание, барьерные методы, внутриматочная спираль [ВМС] и/или стерилизация женщины/мужчины).
Пациентам мужского пола не запрещается заводить детей.
Фертильность
Потенциал эверолимуса вызывать бесплодие у пациентов мужчин и женщин неизвестен, тем не менее, у пациенток наблюдались вторичная аменорея и связанный с препаратом дисбаланс лютеинизирующего гормона/фолликулостимулирующего гормона, касающийся доклинических наблюдений по репродуктивным системам мужчин и женщин). На основании данных доклинических исследований при лечении с применением эверолимуса может быть нарушена фертильность у мужчин и женщин.
Применение при беременности и в период лактации
Данные о применении эверолимуса у беременных женщин отсутствуют или ограничены. Исследования на животных продемонстрировали репродуктивную токсичность, включая эмбриотоксичность и фетотоксичность. Потенциальный риск для людей неизвестен.
Эверолимус не применяют во время беременности и у женщин детородного возраста, не использующих методы контрацепции.
Неизвестно, выделяется ли эверолимус в грудное молоко. Тем не менее, у крыс эверолимус и/или его метаболиты легко проникают в молоко. Таким образом, матерям, принимающим эверолимус, необходимо отказаться от грудного вскармливания.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Не изучались.
Передозировка
Сообщения о случаях передозировки у человека ограничены. Одноразовые дозы до 70 мг приводили к приемлемой переносимости. При передозировке следует использовать общие поддерживающие мероприятия.
Форма выпуска и упаковка
Таблетки 5 мг и 10 мг
По 10 таблеток помещают в контурную ячейковую упаковку из пленки полиамид/алюминий/поливинилхлоридной и фольги алюминиевой печатной лакированной.
По 3 контурных упаковки вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
Условия хранения
Хранить при температуре не выше 30oС.
Хранить в недоступном для детей месте.
Срок хранения
3 года
Препарат не следует применять после истечения срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
Новартис Фарма Штейн АГ
Шаффхаузерштрассе
Штейн, Швейцария
Владелец регистрационного удостоверения
Новартис Фарма АГ, Швейцария
Адрес организации, принимающей претензии от потребителя по качеству продукта (товара) и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства на территории Республики Казахстан
Филиал Новартис Фарма Сервисэз АГ в Казахстане
050051 г. Алматы, ул. Луганского, 96
тел.: (727) 258-24-47
факс: (727) 244-26-51
e-mail: drugsafety.cis@novartis.com
CDS (2015-PSB/GLC-0765-s) of 01.09.2015, SMPC of 26.05.2016
| 812662251477976965_ru.doc | 268.5 кб |
| 723778441477978123_kz.doc | 284.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
- Описание препарата Эверолимус алуфарма
- Состав препарата Эверолимус алуфарма
- Показания препарата Эверолимус алуфарма
- Условия хранения препарата Эверолимус алуфарма
- Срок годности препарата Эверолимус алуфарма
Код ATX:
Противоопухолевые препараты и иммуномодуляторы (L) > Противоопухолевые препараты (L01) > Другие противоопухолевые препараты (L01X) > Ингибиторы протеинкиназы (L01XE) > Everolimus (L01XE10)
Форма выпуска, состав и упаковка
таб. 5 мг: 30 шт.
Рег. №: 21/05/3142 от 14.05.2021 — Действующее
Таблетки белые или почти белые, овальные, двояковыпуклые, с гравировкой E9VS 5 на одной стороне.
Вспомогательные вещества: бутилгидрокситолуол, гипромеллоза 2910, лактозы моногидрат, лактоза безводная, кросповидон (тип A), магния стеарат.
5 шт. — упаковки ячейковые контурные (полиамид/алюминий/поливинилхлорид) (6) — пачки картонные.
таб. 10 мг: 30 шт.
Рег. №: 21/05/3142 от 14.05.2021 — Действующее
Таблетки белые или почти белые, овальные, двояковыпуклые, с гравировкой E9VS 10 на одной стороне.
Вспомогательные вещества: бутилгидрокситолуол, гипромеллоза 2910, лактозы моногидрат, лактоза безводная, кросповидон (тип A), магния стеарат.
5 шт. — упаковки ячейковые контурные (полиамид/алюминий/поливинилхлорид) (6) — пачки картонные.
Описание активных компонентов препарата ЭВЕРОЛИМУС АЛУФАРМА . Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата. Дата обновления: 29.11.2007 г.
Фармакологическое действие
Иммунодепрессант, ингибитор передачи пролиферативного сигнала. Иммуносупрессивное действие обусловлено ингибированием антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими интерлейкинами Т-клеток, например, интерлейкином-2 и интерлейкином-15. Эверолимус ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием этих факторов роста Т-клеток с соответствующими рецепторами. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
На молекулярном уровне эверолимус образует комплекс с цитоплазматическим белком FKBP-12. В присутствии эверолимуса происходит ингибирование фосфорилирования р70 S6 киназы, стимулируемой фактором роста. Поскольку фосфорилирование р70 S6 киназы находится под контролем FRAP (так называемого m-TOR ), эти данные позволяют предположить, что комплекс эверолимус-РКВР-12 связывается с FRAP. FRAP — это ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией; нарушение функции FRAP, таким образом, объясняет остановку клеточного цикла, вызываемую эверолимусом. Эверолимус имеет, таким образом, отличный от циклоспорина механизм действия. В доклинических моделях аллотрансплантации была показана более высокая эффективность комбинации эверолимуса с циклоспорином, чем при изолированном использовании каждого из них.
Помимо влияния на Т-клетки, эверолимус ингибирует стимулируемую факторами роста пролиферацию как гемопоэтических, так и негемопоэтических клеток (например, гладкомышечных клеток). Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, которая запускается при повреждении эндотелиальных клеток и приводит к образованию неоинтимы, играет ключевую роль в патогенезе хронического отторжения.
Эверолимус является активным ингибитором роста и пролиферации опухолевых клеток, эндотелиальных клеток, фибробластов и гладкомышечных клеток кровеносных сосудов.
У пациентов с распространенным и/или метастатическим почечно-клеточным раком, прогрессирующим после предшествующей терапии ингибиторами тирозиновых киназ и/или цитокинами, эверолимус достоверно снижал риск прогрессирования заболевания и смерти больных на 67%. При применении эверолимуса выживаемость больных без прогрессирования заболевания составила 4.9 месяцев. В течение 6 месяцев у 36% больных, получавших эверолимус, не отмечалось прогрессирования заболевания. Считается, что применение эверолимуса позволяет значительно улучшить качество жизни пациентов (оценивалось влияние симптомов заболевания на различные сферы жизни пациента).
Фармакокинетика
После приема внутрь Cmax достигается через 1-2 ч. У пациентов после пересадки концентрация эверолимуса в крови пропорциональна дозе в диапазоне доз от 0.25 мг до 15 мг.
Соотношение концентрации эверолимуса в крови и его концентрации в плазме находится в пределах от 17% до 73% и зависит от значений концентрации в диапазоне от 5 до 5000 нг/мл. У здоровых добровольцев и пациентов с умеренными нарушениями функции печени связывание с белками плазмы составляет приблизительно 74%. Vd в конечной фазе у пациентов после трансплантации почки, находящихся на поддерживающей терапии, составляет 342±107 л.
Эверолимус является субстратом CYP3A4 и Р-гликопротеина. Основными путями метаболизма, выявленными у человека, были моногидроксилирование и О-деалкилирование. Два основных метаболита образуются путем гидролиза циклического лактона. Ни один из них не имеет существенной иммуносупрессивной активности. В системном кровотоке находится в основном эверолимус.
После введения однократной дозы меченого радиоактивной меткой эверолимуса пациентам после трансплантации, получающим циклоспорин, большая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось с мочой. Неизмененное вещество не определялось ни в моче, ни в кале.
У пациентов с умеренно выраженными нарушениями функции печени (класс В по шкале Чайлд-Пью) AUC эверолимуса увеличивалась. Показатель AUC положительно коррелировал с концентрацией сывороточного билирубина и увеличением протромбинового времени и отрицательно коррелировал с концентрацией сывороточного альбумина. Если концентрация билирубина составляла > 34 мкмоль/л, протромбиновое время >1.3 INR (пролонгирование > 4 сек) и/или концентрация альбумина составляла < 35 г/л, то наблюдалась тенденция к увеличению показателя AUC у пациентов с умеренно выраженной печеночной недостаточностью. При тяжелой печеночной недостаточности (класс С по шкале Чайлд-Пью) изменения AUC не изучены, но, вероятно, они такие же или более выраженные, чем при умеренной печеночной недостаточности.
Клиренс эверолимуса повышался в линейной зависимости от возраста пациента (от 1 до 16 лет), площади поверхности тела (0.49-1.92 м2) и массы тела (11-77 кг). В равновесном состоянии клиренс составлял 10.2±3.0 л/ч/м2, T1/2 — 30±11 ч.
У реципиентов почки и сердца в течение 6 мес после трансплантации была выявлена связь между базальной концентрацией эверолимуса и частотой подтвержденного биопсией острого отторжения и тромбоцитопении.
| Трансплантация почки | |||||
| С0 (нг/мл) | ≤3.4 | 3.5-4.5 | 4.6-5.7 | 5.8-7.7 | 7.8-15 |
| Отсутствие отторжения | 68% | 81% | 86% | 81% | 91% |
| Тромбоцитопения (<100×109/л) | 10% | 9% | 7% | 14% | 17% |
| Трансплантация сердца | |||||
| С0 (нг/мл) | ≤3,5 | 3.6-5.3 | 5.4-7.3 | 7.4-10.2 | 10.3-21.8 |
| Отсутствие отторжения | 65% | 69% | 80% | 85% | 85% |
| Тромбоцитопения (<75×109/л) | 5% | 5% | 6% | 8% | 9% |
Показания к применению
Профилактика отторжения трансплантата почки и сердца у взрослых реципиентов с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию (циклоспорин и ГКС).
Распространенный и/или метастатический почечно-клеточный рак (при неэффективности антиангиогенной терапии).
Реклама
Режим дозирования
Принимают внутрь.
В качестве средства профилактики отторжения трансплантата рекомендуемая начальная доза для взрослых с почечными и сердечными трансплантатами составляет по 750 мкг 2 раза/сут. Применение следует начинать как можно скорее после трансплантации. Принимают в одно и то же время с циклоспорином в специальной лекарственной форме. Может потребоваться коррекция режима дозирования эверолимуса с учетом достигнутых концентраций в плазме крови, переносимости, индивидуального ответа на лечение, изменений сопутствующей медикаментозной терапии и клинической ситуации. Коррекцию режима дозирования можно проводить с интервалами 4-5 дней.
В качестве противоопухолевого средства применяют в дозе 10 мг 1 раз/сут ежедневно. Лечение проводят до тех пор, пока сохраняется клинический эффект. При развитии тяжелых и/или труднопереносимых побочных реакций следует снизить дозу до 5 мг/сут и/или временно прекратить терапию. При применении одновременно с умеренными ингибиторами CYP3A4 и ингибиторами Р-гликопротеина дозу эверолимуса следует уменьшить до 5 мг/сут. При развитии тяжелых и/или труднопереносимых побочных реакций у пациентов, получающих препарат одновременно с умеренными ингибиторами CYP3A4 и ингибиторами Р-гликопротеина, дозу эверолимуса следует уменьшить до 5 мг/сут через день. При одновременном применении эверолимуса с сильными индукторами CYP3A4 или индукторами Р-гликопротеина доза может быть повышена постепенно с 10 мг/сут до 20 мг/сут (величина пошагового увеличения дозы — 5 мг). При прекращении терапии сильными индукторами CYP3A4 или индукторами Р-гликопротеина эверолимус следует применять в дозе, которая применялась до начала лечения индукторами CYP3A4 или индукторами Р-гликопротеина.
У пациентов с нарушениями функции печени умеренной степени (класс В по классификации Чайлд-Пью) дозу следует уменьшить до 5 мг/сут.
Побочные действия
Со стороны системы кроветворения и лимфатической системы: очень часто — лейкопения; часто — тромбоцитопения, анемия, коагулопатия, тромботическая тромбоцитопеническая пурпура/гемолитический уремический синдром; иногда — гемолиз.
Со стороны эндокринной системы: иногда — гипогонадизм у мужчин (снижение уровня тестостерона, повышение уровня ЛГ).
Со стороны обмена веществ: очень часто — гиперхолестеринемия, гиперлипидемия; часто — гипертриглицеридемия.
Со стороны сердечно-сосудистой системы: часто — повышение АД, лимфоцеле, венозный тромбоз.
Со стороны дыхательной системы: часто — пневмония; иногда — пневмонит.
Со стороны пищеварительной системы: часто — боли в животе, диарея, тошнота, рвота; иногда — гепатит, нарушения функции печени, желтуха, повышение АЛТ, ACT , ГГТ.
Со стороны кожи и подкожной клетчатки: часто — ангионевротический отек, акне, осложнения со стороны хирургической раны; иногда — сыпь.
Со стороны костно-мышечной системы: иногда — миалгия.
Со стороны мочевыделительной системы: часто — инфекции мочевых путей; иногда — некроз почечных канальцев, пиелонефрит.
Прочие: часто — отек, боль, вирусные, бактериальные и грибковые инфекции, сепсис; иногда — раневая инфекция.
В контролируемых клинических исследованиях, в которых пациентов наблюдали не менее одного года, сообщалось о возникновении лимфом или лимфопролиферативного заболевания в 1.4% случаев при применении эверолимуса с другими иммунодепрессантами; злокачественные новообразования кожи (1.3%); другие типы малигнизации (1.2%).
Применение при беременности и кормлении грудью
Данные по применению при беременности отсутствуют. Не следует применять эверолимус при беременности за исключением тех случаев, когда ожидаемая польза для матери превышает потенциальный риск для плода.
Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения и в течение 8 недель после окончания терапии.
Неизвестно, выделяется ли эверолимус с грудным молоком у человека. При необходимости применения эверолимуса в период лактации следует решить вопрос о прекращении грудного вскармливания.
В экспериментальных исследованиях показано наличие токсического влияния на репродуктивность, включая эмбриотоксичность и фетотоксичность. Неизвестно, существует ли потенциальный риск для человека. Показано, что эверолимус и/или его метаболиты быстро проникали в молоко лактирующих крыс.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени умеренной степени (класс В по классификации Чайлд-Пью) дозу следует уменьшить до 5 мг/сут. Эверолимус не изучен у пациентов с тяжелой печеночной недостаточностью. Рекомендуется тщательно мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
Применение при нарушениях функции почек
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Особые указания
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Не рекомендуется одновременное применение с сильными ингибиторами CYP3А4 (например, кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (например, рифампицин, рифабутин), за исключением случаев, когда ожидаемая польза такой терапии превышает потенциальный риск. Рекомендуется контролировать концентрации эверолимуса в цельной крови при одновременном применении с индукторами или ингибиторами CYP3A4 и после их отмены.
Эверолимус не изучен у пациентов с тяжелой печеночной недостаточностью. Рекомендуется тщательно мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
В период лечения следует контролировать состояние пациентов для выявления кожных новообразований. Следует регулярно контролировать состояние пациентов для выявления кожных новообразований, рекомендовать сведение к минимуму воздействие ультрафиолетового излучения, солнечного света и использовать соответствующие солнцезащитные средства.
С осторожностью применять у пациентов с гиперлипидемией. В период лечения следует контролировать содержание в крови холестерина и триглицеридов. Следует оценивать соотношение риск/польза продолжения терапии эверолимусом у пациентов с тяжелой рефрактерной гиперлипидемией. Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития нежелательных реакций, вызванных применением указанных лекарственных средств.
Чрезмерная иммуносупрессия предрасполагает к развитию инфекций (в т.ч. оппортунистических). Имеются сообщения о развитии фатальных инфекций и сепсиса.
В течение 3 мес после трансплантации рекомендуется профилактика развития цитомегаловирусной инфекции, особенно у пациентов с повышенным риском ее развития.
Пациентам, получающим ингибиторы ГМГ-КоА-редуктазы, требуется клинический контроль с целью своевременного выявления рабдомиолиза.
В период лечения эверолимусом не следует применять живые вакцины.
Лекарственное взаимодействие
На абсорбцию и последующую элиминацию эверолимуса могут оказывать влияние препараты, взаимодействующие с CYP3A4 и/или Р-гликопротеином. Сочетанное применение эверолимуса с сильными ингибиторами или индукторами CYP3A4 не рекомендуется. Ингибиторы Р-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить концентрацию эверолимуса в сыворотке. In vitro эверолимус являлся конкурентным ингибитором CYP3A4 и CYP2D6, потенциально увеличивающим концентрации в плазме препаратов, выводящихся при участии этих ферментов.
Биодоступность эверолимуса значительно увеличивалась при одновременном применении циклоспорина (ингибитор CYP3A4/Р-гликопротеина).
При изучении лекарственного взаимодействия у здоровых добровольцев, получавших предшествующую терапию многократными дозами рифампицина (индуктор CYP3A4), при последующем применении эверолимуса в однократной дозе наблюдалось почти 3-кратное повышение клиренса эверолимуса и уменьшение Сmах на 58% и AUC — на 63% (данная комбинация не рекомендуется).
Умеренные ингибиторы CYP3А4 и Р-гликопротеина могут повышать концентрацию эверолимуса в крови, в т.ч. противогрибковые средства: флуконазол; антибиотики группы макролидов (эритромицин); блокаторы кальциевых каналов (верапамил, никардипин, дилтиазем); ингибиторы протеазы (нелфинавир, индинавир, ампренавир).
Индукторы CYP3А4 могут повышать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови, в т.ч. зверобой продырявленный, противосудорожные средства (карбамазепин, фенобарбитал, фенитоин); препараты для лечения ВИЧ (эфавиренз, невирапин).
Грейпфрут и грейпфрутовый сок влияют на активность изоферментов CYP и Р-гликопротеина, поэтому следует избегать употребления этих соков на фоне применения эверолимуса.
Поскольку иммунодепрессанты могут оказывать влияние на ответ при вакцинации, на фоне лечения эверолимусом вакцинация может быть менее эффективной.

Все аналоги
Аналоги препарата
АФИНИТОР (NOVARTIS PHARMA, AG, Швейцария)
СЕРТИКАН (NOVARTIS PHARMA, AG, Швейцария)
Аналоги КФУ
ЛОРБРЕНА (PFIZER H.C.P. CORPORATION, США)
СТИВАРГА® (BAYER, AG, Германия)
БОЗУЛИФ (PFIZER H.C.P. CORPORATION, США)
АЛУНБРИГтм (ARIAD PHARMACEUTICALS Inc, США)
МИТИКАЙД (NOVARTIS PHARMA SERVICES, AG, Швейцария)
АЛЕЦЕНЗА (F.Hoffmann-La Roche, Ltd., Швейцария)
ТАФИНЛАР (NOVARTIS PHARMA, AG, Швейцария)
ПАЛБОЦИКЛИБ (METIGRINS, SIA, Латвия)
ИБРАНСА (PFIZER H.C.P. CORPORATION, США)
МЕКИНИСТ (NOVARTIS PHARMA, AG, Швейцария)