Хлор на протяжении многих лет является эффективным дезинфекционным средством. Его применяли (и сейчас используют) для обеззараживания:
«Гипохлорит кальция [Ca(OCl)2] Твердый (65 или 68%)»
Но положительный эффект и тогда и сейчас во многом зависит от профессионализма тех, кто применяет гипохлорит кальция для дезинфекции и от того используют ли они инструкцию по применению гипохлорита кальция для дезинфекции.
Гипохлорита кальция
Что такое гипохлорит кальция
Порошок белого цвета, со слабым запахом хлорки – это и есть кальция гипохлорит нейтральный
При определении данного средства используют аббревиатуру КГН.
Содержание хлора в данном средстве не больше 60%, но не меньше 45%. Храниться оно должно строго в герметичной упаковке (именно так его хранят на предприятиях-производителей). Температура при хранении не должна превышать +30 градусов.
Из данного порошка готовят специальный раствор. Он мутный, чуть беловатого оттенка. Храниться может не более трех суток. На дне раствора остается осадок из нерастворимых кальционных солей.
Общее применение
Средство используют при обеззараживании:
Такое средство как гипохлорит кальция 45 применяется при обеззараживании питьевой воды и воды в плавательных бассейнах.
Для дезинфекции одежды данный раствор не применяют, она почти сразу приходит в негодность.
Если раствор попадет в глаза или на незащищенную кожу, может возникнуть покраснение и начаться жжение. Необходимо промыть глаза и кожу большим количеством чистой воды
При попадании в желудок раствор может вызвать воспаление ЖКТ. Это умеренно опасное средство. Лечение при попадании вещества в организм человека должен назначить врач.
Применение гипохлорита кальция должно строго контролироваться специалистами.
Как правильно приготовить раствор
Для дезинфекции КГН используют:
Не осветленный раствор изготовляют из 200 грамм порошка КГН и одного литра воды.
Светлый раствор готовят из не осветленного раствора.
- Не осветлённому раствору дают отстояться.
- Жидкость, которая образовалась над осадком, сливают (получается один литр раствора с концентрацией чистого хлора 10%).
- Жидкость разбавляют для получения светлого раствора (если нужен один литр раствора с хлором 0,5%, то 50 мл активированного раствора разводят в одном литре воды (10% разделить на 0,5%, 1000 мл разделить на 20); если нужна другая концентрация применяются простые математические методы подсчета).
Для получения активированного раствора в светлый раствор подсыпают соли аммония в пропорциях один к двум. Данного типа раствор изготовляют прямо перед применением.
В любом случае только специалисты имеют право изготавливать препараты и проводить их проверку.
Читайте также — Насколько эффективен карбид кальция против кротов
Применение разного типа растворов и порошка
Вопрос о том, где применяют раствор гипохлорита кальция важен. Здесь акценты расставлены очень точно.
Не осветленный раствор применяют для обработки:
Осветленный раствор используют при обеззараживании:
Активированный раствор используют при вспышках вирусных и инфекционных заболеваний (600 мл на квадратный метр).
Порошком обрабатывают выделения больных, остатки пищи, питьевую воду. Порошок используют в больших количествах или в пропорциях один к одному.
Правила работы со средством
Техника безопасности при работе должна обязательно соблюдаться.
Категорически запрещено работать со средством:
Кроме того:
Правила оказания помощи при отравлении КГН
В некоторых случаях возникает отравление КГЛ (если не соблюдается техника безопасности или случается авария на производстве). Симптомы отравления:
При появлении первых симптом необходимо:
Если вещество попало в желудок, то нужно вызвать рвоту, а потом выпить молока или воду с нашатырным спиртом (несколько капель на стакан).
При использовании КГН надо руководствоваться инструкцией, которая была специально издана для производителей средства и для тех, кто использует его для дезинфекции.
Наш специалист уточняет информацию, подбирает оптимальное решение Вашей проблемы и договаривается с Вами об удобном для Вас времени выезда мастера.
Полный осмотр помещения, обнаружение зон обитания грибка, грызунов или насекомых и уничтожение заражений. По окончанию обработки Вы получаете бесплатную консультацию, во избежание повторения заражения.
Мы следим за санитарно-техническим состоянием объекта в течение всего срока гарантии.
Источник
Хлор на протяжении многих лет является эффективным дезинфекционным средством. Его применяли (и сейчас используют) для обеззараживания:
«Гипохлорит кальция [Ca(OCl)2] Твердый (65 или 68%)»
- различных поверхностей;
- очищения колодцев;
- дезинфекции выгребных ям и септиков.
Но положительный эффект и тогда и сейчас во многом зависит от профессионализма тех, кто применяет гипохлорит кальция для дезинфекции и от того используют ли они инструкцию по применению гипохлорита кальция для дезинфекции.
Гипохлорита кальция
Содержание статьи
- Что такое гипохлорит кальция
- Общее применение
- Как правильно приготовить раствор
- Применение разного типа растворов и порошка
- Правила работы со средством
- Правила оказания помощи при отравлении КГН
Что такое гипохлорит кальция
Порошок белого цвета, со слабым запахом хлорки – это и есть кальция гипохлорит нейтральный
При определении данного средства используют аббревиатуру КГН.
Содержание хлора в данном средстве не больше 60%, но не меньше 45%. Храниться оно должно строго в герметичной упаковке (именно так его хранят на предприятиях-производителей). Температура при хранении не должна превышать +30 градусов.
Из данного порошка готовят специальный раствор. Он мутный, чуть беловатого оттенка. Храниться может не более трех суток. На дне раствора остается осадок из нерастворимых кальционных солей.
Общее применение
Средство используют при обеззараживании:
- скотомогильников (особенно, если есть подозрение на наличие очага инфекции);
- выгребных ям и септиков;
- почвы и асфальта;
- помещений, в которых долгое время находились больные холерой или туберкулезом (действует как бактерицидное средство);
- помещений общего пользования (больницы, школы, детские сады, лагеря, базы отдыха и пансионаты);
- уборных общего пользования;
- жилых индивидуальных помещений;
- предметов быта (кроме металлических предметов, которые могут подвергнуться коррозии);
- посуды (после обработки посуду необходимо тщательно промыть несколько раз).
Такое средство как гипохлорит кальция 45 применяется при обеззараживании питьевой воды и воды в плавательных бассейнах.
Для дезинфекции одежды данный раствор не применяют, она почти сразу приходит в негодность.
Если раствор попадет в глаза или на незащищенную кожу, может возникнуть покраснение и начаться жжение. Необходимо промыть глаза и кожу большим количеством чистой воды
При попадании в желудок раствор может вызвать воспаление ЖКТ. Это умеренно опасное средство. Лечение при попадании вещества в организм человека должен назначить врач.
Применение гипохлорита кальция должно строго контролироваться специалистами.
Как правильно приготовить раствор
Для дезинфекции КГН используют:
- в виде не осветленного раствора;
- в виде светлого раствора;
- активированного раствора;
- в виде порошка.
Не осветленный раствор изготовляют из 200 грамм порошка КГН и одного литра воды.
Светлый раствор готовят из не осветленного раствора.
- Не осветлённому раствору дают отстояться.
- Жидкость, которая образовалась над осадком, сливают (получается один литр раствора с концентрацией чистого хлора 10%).
- Жидкость разбавляют для получения светлого раствора (если нужен один литр раствора с хлором 0,5%, то 50 мл активированного раствора разводят в одном литре воды (10% разделить на 0,5%, 1000 мл разделить на 20); если нужна другая концентрация применяются простые математические методы подсчета).
Для получения активированного раствора в светлый раствор подсыпают соли аммония в пропорциях один к двум. Данного типа раствор изготовляют прямо перед применением.
В любом случае только специалисты имеют право изготавливать препараты и проводить их проверку.
Читайте также – Насколько эффективен карбид кальция против кротов
Применение разного типа растворов и порошка
Вопрос о том, где применяют раствор гипохлорита кальция важен. Здесь акценты расставлены очень точно.
Не осветленный раствор применяют для обработки:
- производственных помещений (600 мл. на квадратный метр);
- надворных построек (600 мл. на квадратный метр);
- мусорных ям (600 мл. на квадратный метр);
- инвентаря, которым убирается мусор.
Осветленный раствор используют при обеззараживании:
- жилых помещений (210 мл. на квадратный метр; после обработки помещение надо в обязательном порядке убрать и проветрить);
- мебели (можно распылять средство из расчета 210 мл на квадратный метр; можно использовать раствор для влажного протирания поверхностей из расчета 180 мл. на квадратный метр);
- посуды (один комплект посуды на два литра средства);
- детских игрушек (мелкие можно вымачивать в растворе, а крупные – орошать; после выдерживания игрушки необходимо отчистить с помощью большого количества воды).
Активированный раствор используют при вспышках вирусных и инфекционных заболеваний (600 мл на квадратный метр).
Порошком обрабатывают выделения больных, остатки пищи, питьевую воду. Порошок используют в больших количествах или в пропорциях один к одному.
Правила работы со средством
Техника безопасности при работе должна обязательно соблюдаться.
Категорически запрещено работать со средством:
- детям до 18 лет;
- беременным;
- лицам с общими противопоказаниями.
Кроме того:
- приготовление раствора необходимо проводить в помещениях с хорошей системой вентиляции или в специальных вытяжных шкафах;
- специалисты должны быть одеты в спецодежду и иметь защитные маски на лице. Если действовать строго по инструкции, то человек должен быть защищен респиратором РУ-60 с патроном марки А; защитными очками, резиновыми перчатками; защитными передниками;
- хранить порошок и раствор можно только в емкостях с плотными крышками, в помещениях, недоступным детям, хорошо вентилируемых и не влажных;
- все обработанные бытовые предметы и детские игрушки необходимо тщательно промывать до полного исчезновения запаха хлора;
- Остатки порошка запрещено просто выбрасывать в мусорник, его разводят водой и сливают в канализацию;
- после окончания работы со средством необходимо тщательно вымыть руки (но лучше принять душ).
Правила оказания помощи при отравлении КГН
В некоторых случаях возникает отравление КГЛ (если не соблюдается техника безопасности или случается авария на производстве). Симптомы отравления:
- резь и боль в глазах;
- першение в горле;
- першение в носу;
- кашель;
- покраснения или ожоги.
При появлении первых симптом необходимо:
- вывести пострадавшего человека на воздух;
- заставить его хорошо вымыть руки и лицо;
- заставить выпить щелочное питье (самый лучший вариант – молоко с растворенной в нем содой пищевой);
- остановить кашель;
- проверить ритм биения сердца и измерить давление;
- если появилось покраснение или ожог, его необходимо тщательно промыть, а потом обработать пораженный участок раствором соды;
- если КГН попало в глаза, необходимо промыть их проточной водой, закапать альбуцитом или новокаином (раствором), а потом обратиться к врачу.
Если вещество попало в желудок, то нужно вызвать рвоту, а потом выпить молока или воду с нашатырным спиртом (несколько капель на стакан).
При использовании КГН надо руководствоваться инструкцией, которая была специально издана для производителей средства и для тех, кто использует его для дезинфекции.
Наш специалист уточняет информацию, подбирает оптимальное решение Вашей проблемы и договаривается с Вами об удобном для Вас времени выезда мастера.
Полный осмотр помещения, обнаружение зон обитания грибка, грызунов или насекомых и уничтожение заражений. По окончанию обработки Вы получаете бесплатную консультацию, во избежание повторения заражения.
Мы следим за санитарно-техническим состоянием объекта в течение всего срока гарантии.
Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Брутто формула
-
Фармакологическая группа вещества Кальция хлорид
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Кальция хлорид
-
Противопоказания
-
Побочные действия вещества Кальция хлорид
-
Способ применения и дозы
-
Особые указания
-
Торговые названия с действующим веществом Кальция хлорид
Структурная формула
Русское название
Кальция хлорид
Английское название
Calcium chloride
Латинское название
Calcii chloridum (род. Calcii chloridi)
Брутто формула
CaCl2
Фармакологическая группа вещества Кальция хлорид
Нозологическая классификация
Список кодов МКБ-10
-
A16.2 Туберкулез легких без упоминания о бактериологическом или гистологическом подтверждении
-
E20 Гипопаратиреоз
-
E55.0 Рахит активный
-
E58 Алиментарная недостаточность кальция
-
E83.5 Нарушения обмена кальция
-
E83.5.1* Гипокальциемия
-
G83.8 Другие уточненные паралитические синдромы
-
I77.6 Артериит неуточненный
-
I78.8 Другие болезни капилляров
-
J18 Пневмония без уточнения возбудителя
-
J45 Астма
-
K71 Токсическое поражение печени
-
K75.8 Другие уточненные воспалительные болезни печени
-
K92.2 Желудочно-кишечное кровотечение неуточненное
-
L29 Зуд
-
L30.9 Дерматит неуточненный
-
L40 Псориаз
-
L50 Крапивница
-
M83.9 Остеомаляция у взрослых неуточненная
-
N05 Нефритический синдром неуточненный
-
N70 Сальпингит и оофорит
-
N71 Воспалительные болезни матки, кроме шейки матки
-
N93 Другие аномальные кровотечения из матки и влагалища
-
N95.1 Менопаузное и климактерическое состояние у женщин
-
O15 Эклампсия
-
O25 Недостаточность питания при беременности
-
O62.2 Другие виды слабости родовой деятельности
-
R04.0 Носовое кровотечение
-
R04.8 Кровотечение из других отделов дыхательных путей
-
R09.1 Плеврит
-
R25.2 Судорога и спазм
-
R29.0 Тетания
-
R58 Кровотечение, не классифицированное в других рубриках
-
R60.0 Локализованный отек
-
T56.0 Свинца и его соединений
-
T56.8 Других металлов
-
T65.8 Других уточненных веществ
-
T66 Неуточненные эффекты излучения
-
T78.3 Ангионевротический отек
-
T78.4 Аллергия неуточненная
-
T80.6 Другие сывороточные реакции
-
Z39.1 Помощь и обследование кормящей матери
Код CAS
10043-52-4
Фармакологическое действие
—
гемостатическое, дезинтоксикационное, противоаллергическое, противовоспалительное, снижающее проницаемость капилляров.
Характеристика
Бесцветные кристаллы без запаха, горько-соленого вкуса. Кальция хлорид очень легко растворим в воде (4:1) с сильным охлаждением раствора, легко растворим в этаноле. Очень гигроскопичен, на воздухе расплывается. Содержит 27% кальция. Молекулярная масса 110,98.
Фармакология
Восполняет дефицит ионов кальция, необходимых для передачи нервных импульсов, сокращения скелетных и гладких мышц, деятельности сердца, формирования костной ткани, свертывания крови. Кальций снижает проницаемость клеточных мембран и сосудистой стенки, предотвращает развитие воспалительных реакций, повышает сопротивляемость организма инфекциям и усиливает фагоцитоз. При в/в введении стимулирует симпатический отдел вегетативной нервной системы, увеличивает выделение надпочечниками адреналина, оказывает умеренное диуретическое действие.
Применение вещества Кальция хлорид
Гипокальциемия, повышенная потребность в кальции (беременность, кормление грудью, период усиленного роста организма), недостаточное поступление кальция с пищей, нарушение обмена кальция, в т.ч. в постменопаузном периоде, повышенное выведение кальция (хроническая диарея, вторичная гипокальциемия, в т.ч. на фоне длительного приема некоторых диуретиков, противосудорожных ЛС или глюкокортикоидов), кровотечения различной этиологии и локализации (легочные, желудочно-кишечные, носовые, маточные и др.), аллергические заболевания и реакции, в т.ч. сывороточная болезнь, крапивница, зуд, отек Квинке, бронхиальная астма, воспалительные и экссудативные процессы, в т.ч. пневмония, плеврит, аднексит, эндометрит, повышенная проницаемость сосудов (геморрагический васкулит, лучевая болезнь), дистрофические алиментарные отеки, гипопаратиреоз, гипокальциемия, спазмофилия, свинцовые колики, тетания, гиперкалиемическая форма пароксизмальной миоплегии, туберкулез легких, рахит и остеомаляция, гепатит (паренхиматозный, токсический), нефрит, эклампсия, отравление солями магния, щавелевой и фтористой кислотами, экзема, псориаз, слабость родовой деятельности.
Противопоказания
Гиперчувствительность, гиперкальциемия, атеросклероз, склонность к тромбозам.
Побочные действия вещества Кальция хлорид
При приеме внутрь — боль в эпигастрии, изжога, тошнота, рвота, гастрит. При в/в введении — ощущение жара, гиперемия лица, брадикардия; при быстром в/в введении — фибрилляция желудочков сердца; местные реакции при в/в введении — боль и гиперемия по ходу вены.
Способ применения и дозы
В/в, медленно (по 6 капель/мин) — перед введением 5–10 мл 10% раствора, разбавляют в 100–200 мл изотонического раствора натрия хлорида или 5% раствора декстрозы. Внутрь, после еды, в виде 5–10% раствора 2–3 раза в сутки: взрослым — 10–15 мл на прием, детям — 5–10 мл.
Особые указания
Нельзя вводить п/к и в/м — возможен некроз тканей (кальция хлорид, начиная с концентрации 5%, оказывает сильное раздражающее действие). При в/в введении кальция хлорида появляется ощущение жара сначала в полости рта, а затем по всему телу (этот эффект ранее использовали при определении скорости кровотока — регистрировали время между моментом введения в вену кальция хлорида и появлением ощущения жара).
Торговые названия с действующим веществом Кальция хлорид
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Кальция хлорид |
от 46.00 до 55.00 |
Кальция хлорид (Calcium chloride)
💊 Состав препарата Кальция хлорид
✅ Применение препарата Кальция хлорид
Описание активных компонентов препарата
Кальция хлорид
(Calcium chloride)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2022.11.10
Владелец регистрационного удостоверения:
Код ATX:
B05XA07
(Кальция хлорид)
Лекарственная форма
| Кальция хлорид |
Р-р д/в/в введения 1 г/10 мл: амп. 10 шт. рег. №: ЛС-000366 |
Форма выпуска, упаковка и состав
препарата Кальция хлорид
10 мл — ампулы (10) — пачки картонные.
Фармакологическое действие
Кальций — макроэлемент, участвующий в формировании костной ткани, процессе свертывания крови, необходим для поддержания стабильной сердечной деятельности, процессов передачи нервных импульсов. Улучшает сокращение мышц при мышечной дистрофии, миастении, уменьшает проницаемость сосудов, оказывает противоаллергическое действие. При в/в введении кальций вызывает возбуждение симпатической нервной системы и усиление выделения надпочечниками адреналина; оказывает умеренное диуретическое действие.
При взаимодействии раствора кальция хлорида с солями магния, щавелевой и фтористой кислотами образуются нерастворимые соединения, что позволяет применять раствор кальция хлорида в качестве антидота.
Фармакокинетика
В крови кальций находится в ионизированном и в связанном состоянии. В плазме около 45% кальция находится в комплексе с белками. Физиологической активностью обладает ионизированный кальций. Депонируется в костной ткани. Около 20% выводится почками, остальное количество (80%) — кишечником. 95% кальция, выводящегося путем гломерулярной фильтрации, подвергается резорбции в восходящем сегменте петли Генле, а также в проксимальных и дистальных почечных канальцах.
Показания активных веществ препарата
Кальция хлорид
Аллергические заболевания (крапивница, ангионевротический отек, аллергодерматозы, сывороточная болезнь), гипокальциемия (в т.ч. гипокальциемическая тетания, при гипопаратиреозе), свинцовая колика, гиперкалиемия, передозировка солями магния (в составе комплексной терапии).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Применяют внутрь, в/в струйно или капельно. Дозу, способ и схему применения, длительность терапии определяют индивидуально, в зависимости от показаний, клинической ситуации и возраста пациента.
Дозу для детей устанавливают из расчета на массу тела.
Побочное действие
Возможно: ощущение жара сначала в полости рта, а затем по всему телу, привкус мела во рту, периферическая вазодилатация, снижение АД, аритмия (в т.ч. брадикардия), тошнота, обморок. При попадании в подкожную клетчатку и в мышцу вызывает сильное раздражение и некроз окружающих тканей. При быстром в/в введении возможны фибрилляция желудочков сердца, сердечно-сосудистая недостаточность, вплоть до остановки сердца.
Местные реакции: раздражение по ходу вены; гиперемия кожи, боль, сыпь, кальцификация могут свидетельствовать об экстравазации, которая может приводить к некрозу окружающих тканей.
Противопоказания к применению
Повышенная чувствительность к кальция хлориду, гиперкальциемия, тяжелая хроническая почечная недостаточность, фибрилляция желудочков, мочекаменная болезнь, саркоидоз, выраженный атеросклероз, склонность к тромбообразованию, одновременный прием с сердечными гликозидами; беременность; период грудного вскармливания.
С осторожностью: хроническая почечная недостаточность легкой и средней степени тяжести, дегидратация, нарушение электролитного баланса (риск гиперкальциемии), заболевания сердца (риск аритмии), заболевания почек, «легочное» сердце, респираторный ацидоз, дыхательная недостаточность (риск токсических реакций вследствие окисления кальция), детский возраст.
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности и в период лактации (грудного вскармливания). При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания.
Применение при нарушениях функции почек
Противопоказано применение при тяжелой хронической почечной недостаточности. С осторожностью применять при хронической почечной недостаточности легкой и средней степени тяжести, заболеваниях почек.
Применение у детей
Кальция хлорид следует с осторожностью применять у детей.
Особые указания
Не вводить п/к и в/м. При попадании кальция хлорида под кожу или в мышечные ткани развивается сильное раздражение с образованием очагов некроза.
При возникновении боли или гиперемии в месте введения следует прекратить введение и исключить экстравазацию средства.
Лечение проводят под контролем концентрации кальция в крови.
При аллергических заболеваниях рекомендуется совместное применение кальция хлорида и антигистаминных препаратов.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения в связи с возможным развитием побочных эффектов необходимо соблюдать осторожность при вождении автотранспорта и занятиях другой деятельностью, требующей высокой концентрации внимания и скорости психомоторных реакций.
Лекарственное взаимодействие
При одновременном применении уменьшает действие блокаторов «медленных» кальциевых каналов; с другими кальций- и магнийсодержащими препаратами повышается риск гиперкальциемии или гипермагниемии соответственно, особенно у пациентов с хронической почечной недостаточностью; с хинидином — возможно замедление внутрижелудочковой проводимости и повышение токсичности хинидина.
Снижает эффективность недеполяризующих миорелаксантов. Может увеличивать продолжительность действия тубокурарина хлорида.
Фармацевтически несовместим с тетрациклинами, магния сульфатом, лекарственными препаратами, содержащими фосфаты, карбонаты или тартраты.
Кальция хлорид несовместим с солями свинца, серебра, одновалентной ртути вследствие образования нерастворимых хлоридов тяжелых металлов и с барбиталом натрия, т.к. при этом образуется малорастворимая кальциевая соль барбитала.
Во время лечения сердечными гликозидами парентеральное применение кальция хлорида не рекомендуется в связи с усилением кардиотоксического действия.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Д. А. Меркулов, к.х.н., зав. кафедрой фундаментальной и прикладной химии, ФГБОУ ВПО «Удмуртский государственный университет», г. Ижевск
Введение
Гипохлоритами называют соли хлорноватистой кислоты HClO. Наиболее распространенными из них являются гипохлорит натрия, гипохлорит кальция и гипохлорит калия. Гипохлориты широко применяются для обеззараживания питьевой воды, отбеливания, дегазации и дезинфекции. Гипохлориты являются одними из самых важных химических соединений.
Таблица 1. Наиболее распространенные гипохлориты.
| Систематическое наименование | Традиционное название | Хим. формула | CAS № | М, г/моль |
|---|---|---|---|---|
| Гипохлорит натрия | Хлорноватистокислый натрий, лабарракова вода (гипохлорит натрия в смеси с хлоридом натрия и гидроксидом натрия) | NaClO | 7681–52–9 | 74,44 |
| Гипохлорит калия | Хлорноватистокислый калий,
жавелевая вода (гипохлорит калия в смеси с гидрокарбонатом калия и хлоридом калия) |
KClO | 7778–66–7 | 90,55 |
| Гипохлорит кальция | Хлорноватистокислый кальций, хлорная известь (гипохлорит кальция в смеси с хлоридом кальция, оксихлоридом кальция и гидроксидом кальция) | Ca(ClO)2 | 7778–54–3 | 142,98 |
История открытия
В 1774 г. шведский химик Карл Вильгельм Шееле получил хлор (Cl2) в результате взаимодействия оксида марганца(IV) MnO2 и соляной кислоты (HCl). Позже, в 1785 г. французский химик Клод Луи Бертолле обнаружил, что водный раствор газообразного хлора («хлорная вода»), содержащий хлорноватистую и хлороводородную кислоты, может отбелить белье, и сообщил о своих выводах Французской академии наук.
Cl2 + H2O = HClO + HCl
Знания об отбеливающих свойствах хлора были незамедлительно использованы Джеймсом Уаттом на текстильной фабрике в Глазго. Несмотря на то, что отбеливание с использованием хлора был значительно эффективнее традиционных способов отбеливания солнечным светом, слабыми растворами кислот и щелочей, применение хлора ограничивалось его токсичностью и разрушающим действием на ткани. Для стабилизации раствора газообразного хлора в воде и безопасности его применения, в 1787 г. на Парижском предприятии Societe Javel хлор стали пропускать через водный раствор карбоната калия (поташа)
Cl2 + K2СO3 = 2KHCO3 + KClO + KCl.
Глава предприятия Леонард Альбан назвал новый продукт «Eau de Javel» («жавелевая вода»), и вскоре белильная жидкость стала популярной во Франции и Англии.
В 1820 г. француз Антуан Лабаррак усовершенствовал способ получения отбеливателя, заменив поташ на более дешевый гидроксид натрия (каустическую соду). Полученный раствор гипохлорита и хлорида натрия получил название «Eau de Labarraque» («лабарракова вода»).
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Широкое применение гипохлоритов для обеззараживания питьевой воды и дезинфекции стало возможным гораздо позже, в начале XX века, благодаря развитию промышленного производства хлора электролизом поваренной соли.
Физические свойства
Гипохлориты встречаются нам преимущественно в виде водных растворов, хотя некоторые из них можно выделить в твердом виде. Так, известен безводный гипохлорит натрия, который представляет собой неустойчивое бесцветное кристаллическое вещество. Из кристаллогидратов наиболее устойчивой формой является NaClO×5H2O. Это соединение представляет собой белые или бледно-зеленые ромбические кристаллы, расплывающиеся на воздухе. При нагревании пентагидрата гипохлорита натрия до температуры 24,4°С, он плавится. Кристаллогидрат NaClO×2,5H2O плавится при температуре 57,5°С. Моногидрат крайне неустойчив и разлагается выше 60°С, при более высоких температурах разложение протекает со взрывом.
Таблица 2. Плотности и температуры замерзания водных растворов гипохлорита натрия.
| Концентрация, % | 1 | 2 | 4 | 6 | 8 | 10 | 14 |
| Плотность, г/мл (18 °С) | 1,0053 | 1,0121 | 1025,8 | 1,0397 | 1,0538 | 1,0681 | 1,0977 |
| Концентрация, % | 18 | 22 | 26 | 30 | 34 | 38 | 40 |
| Плотность, г/мл (18 °С) | 1,1288 | 1,1614 | 1,1953 | 1,2307 | 1,2680 | 1,3085 | 1,3285 |
| Концентрация, % | 2 | 4 | 6 | 8 | 10 | 12 | 15,6 |
| tзам, °С | – 2,2 | – 4,4 | – 7,5 | – 10,0 | – 13,9 | – 19,4 | –29,7 |
В отличие от гипохлорита калия, известного только в растворах, гипохлорит кальция можно выделить в форме бесцветных кристаллов, устойчивых в сухой атмосфере без углекислого газа. Из водных растворов гипохлорит кальция можно выделить в виде кристаллогидратов Ca(ClO)2×2H2O, Ca(ClO)2×3H2O, Ca(ClO)2×4H2O.
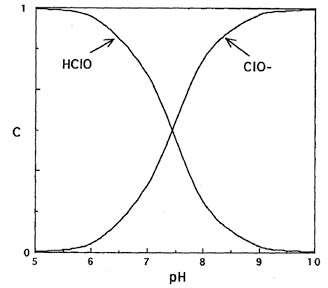
Кислотно-основное равновесие между хлорноватистой кислотой и гипохлорит-ионом описывается обратимой реакцией с константой равновесия Ka = 2,63×10–8 при 20°С.
HClO = H+ + ClO–.
Используя константу равновесия Ka, можно рассчитать мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от рН (рис.1).
Данные свидетельствуют, что при подкислении растворов гипохлоритов увеличивается доля неустойчивой хлорноватистой кислоты. При рН < 7,58 в растворе присутствует преимущественно хлорноватистая кислота, а при рН > 7,58 существуют преимущественно гипохлорит-ионы.
Рис. 1. Мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от кислотности среды.
Химические свойства
Гипохлориты являются неустойчивыми соединениями, легко разлагающимися с выделением кислорода. Разложение твердых гипохлоритов натрия и кальция можно представить уравнениями
2NaClO = 2NaCl + O2↑ и 2Сa(ClO)2 = СaCl2 + O2↑.
Процессы при комнатной температуре происходят медленно, а при нагревании могут протекать со взрывом. Параллельно реакциям, сопровождающимся образованием хлоридов и свободного кислорода, могут протекать реакции диспропорционирования
3NaClO = NaClO3 + 2NaCl и 3Сa(ClO)2 = Ca(ClO3)2 + 2СaCl2.
Разложение гипохлоритов в водных растворах зависит от кислотности раствора и его температуры. В сильнокислых средах при рН ≤ 3 хлорноватистая кислота при комнатной температуре разлагается до хлора и кислорода
4HClO = 2Cl2↑ + O2↑ + 2H2O.
Если при подкислении используется соляная кислота или в растворе присутствуют хлориды, образование кислорода не происходит
HClO + HCl = Cl2↑ + H2O.
Хлорноватистая кислота очень слабая, поэтому она может быть вытеснена из раствора ее солей действием углекислого газа
ClO– + CO2 + H2O = HCO3– + HClO.
В слабокислых и нейтральных средах при 3 < рН < 7,5 протекает следующая окислительно-восстановительная реакция
2HClO = 2HCl + O2↑.
В нейтральных и щелочных растворах имеет место конкурирующая реакция образования хлоридов и хлоратов
3ClO– = ClO3– + 2Cl–.
При комнатной температуре реакция диспропорционирования протекает медленно, но при температурах выше 70°С эта реакция становится преобладающей.
В щелочных средах при рН > 7,5 в растворах преобладают гипохлорит-ионы, разлагающиеся следующим образом:
2ClO– = 2Cl– + O2↑.
Стабилизация гипохлоритов в водных растворах. Соли хлорноватистой кислоты значительно устойчивее самой кислоты. С ростом рН уменьшается мольная доля хлорноватистой кислоты в растворе и тем самым повышается стабильность гипохлоритов (рис. 1). В области рН > 11 содержание хлорноватистой кислоты крайне низкое, однако, и при этой кислотности наблюдается медленное разложение соединений хлора(I). Протекающие реакции можно записать в виде:
2ClO– = ClO2– + Cl–, (1)
ClO2– + ClO– = ClO3– + Cl–, (2)
2ClO– = O2 + 2Cl–. (3)
Около 95% от общего количества гипохлорит-ионов разлагается в результате последовательных реакций (1) и (2), причем реакция (1) является самой медленной (лимитирующей) и определяет общую скорость процесса. Реакция (3) не является основной, но отвечает за выделение кислорода, количество которого может быть значительным.
В присутствии некоторых ионов металлов, например, меди, никеля, кобальта наблюдается каталитическое разложение гипохлорит-ионов. Ионы железа обладают слабым каталитическим действием и являются сокатализаторами в сочетании с другими ионами металлов. В простейшем случае, при содержании ионов меди(II) в растворе в концентрации 1мг/кг порядки гомогенной реакции по гипохлориту и по меди(II) равны единице.
Гетерогенный катализ металлами и их нерастворимыми соединениями, является сложным и плохо воспроизводимым. Из нерастворимых катализаторов наибольшее мешающее влияние оказывает никель и его оксиды, которые попадают в растворы гипохлоритов при их контакте с легированными никелевыми сталями, используемыми для изготовления трубопроводов и резервуаров.
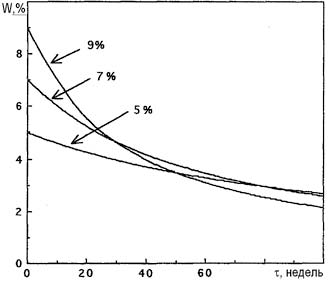
На константы скорости реакций (1)-(3) большое влияние оказывает ионная сила растворов. Высокие концентрации электролитов уменьшают константы скорости реакций и обеспечивают разумную стабильность при хранении растворов электролитов. Увеличение концентрации гипохлорит-ионов, напротив, уменьшает их стабильность в водных растворах. На рис. 2 показан феномен «кривой пересечения». Растворы гипохлорита натрия с концентрацией 9% и 5% при хранении разлагаются настолько, что через 50 недель показывают одинаковую концентрацию вещества, а через 100 недель первоначально более концентрированный раствор содержит гипохлорит-ионов меньше, чем разбавленный.
Рис. 2. Разложение гипохлорита натрия различных концентраций при 30°С.
Повышение температуры способствует ускорению процессов разложения гипохлоритов, поэтому целесообразно хранить растворы гипохлоритов в прохладном месте для обеспечения срока годности (рис. 3).
Рис. 3. Влияние температуры на разложение 5%-ного раствора NaClO.
Для стабилизации водных растворов гипохлоритов, а так же продуктов на их основе, каждый производитель применяет собственные методы, которые редко публикуются в виде статей. Однако известны некоторые запатентованные методы, которые, не претендуя на полноту, можно представить следующим списком:
- удаление хлорид-ионов, сопутствующих гипохлорит-ионам, методом кристаллизации;
- приготовление хлорноватистой кислоты, свободной от хлорид-ионов, методами электродиализа, дистилляции и жидкостной экстракции с последующей нейтрализацией щелочью;
- добавление многоатомных спиртов (например галактита, маннита, сорбита, инозита и пентаэритрита);
- добавление амидов;
- осаждение и фильтрация после добавления соединений щелочноземельных металлов;
- добавление перйодатов или перйодат-образующих соединений, способных образовывать комплексы с ионами металлов – катализаторов разложения гипохлоритов;
- добавление силикатов совместно с добавками или без добавок;
- добавление бромидов;
- добавление арилсульфаниламидов или их производных;
- увеличение светостойкости гипохлоритов путем добавления солей имидодисульфатов; солей церия и ЭДТА; феррицианидов; изоциануровой кислоты и цитрата натрия;
- добавление избытка хлорида железа с последующей фильтрацией;
- добавление гептоната натрия или боргептоната натрия;
- добавление 2-оксазолидинонов;
- добавление фосфата натрия;
- добавление бихромата калия;
- добавление солей кальция;
- добавление полидентатных гетероароматических соединений.
Направление окислительно-восстановительных процессов с участием гипохлорит-ионов и хлорноватистой кислоты обусловлены значениями стандартных электродных потенциалов полуреакций в водной среде:
в кислой среде
2HClO + 2H+ + 2e– = Cl2↑ + 2H2O, E° = 1,630 В,
HClO + H+ + 2e– = Cl– + H2O, E° = 1,500 В.
в нейтральной и щелочной среде
ClO– + H2O + 2e– = Cl– + 2OH–, E° = 0,890 В,
2ClO– + 2H2O + 2e– = Cl2↑ + OH–, E° = 0,421 В.
Таким образом, гипохлорит-ионы и хлорноватистая кислота обладают выраженными окислительными свойствами, причем их окисляющая способность в кислой среде значительно выше, чем в нейтральной и щелочной средах.
Дезинфицирующее действие
Гипохлориты являются одними из лучших антибактериальных средств. Они убивают микроорганизмы очень быстро даже при очень низких концентрациях.
Наивысшее бактерицидное действие гипохлоритов проявляется в нейтральной среде, когда концентрации хлорноватистой кислоты и гипохлорит-ионов приблизительно равны (рис. 1). Образующиеся при разложении гипохлоритов активные частицы (атомарный кислород и хлор) обладают высоким биоцидным действием. Они уничтожают микроорганизмы, взаимодействуя с биополимерами в их структуре, способными к окислению. Аналогичным образом, например, действуют клетки человека нейтрофилы, гепатоциты и др., которые синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциями.
Бактерицидная активность гипохлоритов настолько велика, что они способны привести к гибели дрожжеподобных грибов, вызывающих кандидоз, Candida albicans, в течение 30 секунд при действии 5,0 – 0,5%-го гипохлоритного раствора. Патогенный Enterococcus faecalis погибает через 30 секунд после обработки 5,25%-ым раствором и через 30 минут после обработки 0,5%-ым раствором. Грамотрицательные анаэробные бактерии, такие как Porphyromonas gingivalis, Porphyromonas endodontalis и Prevotella intermedia, погибают в течение 15 секунд после обработки 5,0 – 0,5%-м раствором гипохлорит-ионов.
Несмотря на высокую биоцидную активность гипохлоритов, некоторые потенциально опасные простейшие организмы, например, возбудители лямблиоза или криптоспоридиоза, к сожалению, устойчивы к его действию.
При помощи гипохлорит-ионов можно успешно обезвреживать различные токсины (табл. 3).
Таблица 3. Результаты инактивации токсинов при 30-минутной экспозиции различных концентраций гипохлорита натрия («+» – токсин инактивирован; «–» – токсин остался активен).
| Токсин | 2,5% NaClO + 0,25 н. NaOH | 2,5% NaClO | 1,0% NaClO | 0,1% NaClO |
|---|---|---|---|---|
| Т-2 токсин | + | – | – | – |
| Бреветоксин | + | + | – | – |
| Микроцистин | + | + | + | – |
| Тетродотоксин | + | + | + | – |
| Сакситоксин | + | + | + | + |
| Палитоксин | + | + | + | + |
| Рицин | + | + | + | + |
| Ботулотоксин | + | + | + | + |
Методы анализа
Качественными реакциями на гипохлорит-ион могут служить:
- окисление йодид-иона до йода в сильнокислой среде;
- выпадение коричневого осадка метагидроксида таллия(III) (TlO(OH)) при действии щелочного раствора соли таллия (I);
- цветная реакция с 4,4´-тетраметилдиаминодефенилметаном или N,N´-диокситрифенил метаном в присутствии бромата калия.
Наиболее распространенным методом количественного анализа гипохлорит-иона является титриметрический метод с использованием йодида калия. Для проведения испытания водный раствор или водную суспензию, содержащие гипохлорит-ион, смешивают с избытком раствора йодида калия в сернокислой среде. Выдерживают герметично закрытую смесь в течение 5 минут в темном месте. Выделившийся йод титруют стандартизированным раствором тиосульфата натрия. В качестве индикатора вблизи точки эквивалентности используют крахмальный раствор.
При количественном определении гипохлорит-иона косвенным йодометрическим методом результаты анализа пересчитывают на концентрацию «активного хлора» в ыделившегося при реакции
2H+ + ClO– + Cl– = Cl2↑ + H2O.
Альтернативным методом количественного определения гипохлорит-иона является потенциометрический анализ с использованием бром-ионселективного электрода. Концентрацию гипохлорит-иона находят методом добавок анализируемого раствора к стандартному раствору или методом уменьшения концентрации анализируемого раствора при его добавлении к стандартному раствору.
Способы получения наиболее важных товарных продуктов
Крупнотоннажными гипохлоритсодержащими продуктами являются гипохлорит натрия и гипохлорит кальция. Их глобальный объем производства превышает 1 млн тонн/год. При этом почти половина этого объема используется в быту, а другая половина в промышленности. Гипохлорит калия, являющийся исторически первым гипохлоритом, нашедшим промышленное применение, производится в ограниченном количестве.
Для промышленного производства гипохлорита натрия используются химический и электрохимический методы. При химическом методе производится хлорирование водных растворов гидроксида натрия. Суть химического превращения не изменилась со времен его открытия и применения Лабарраком
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Существуют две производственные схемы данного метода:
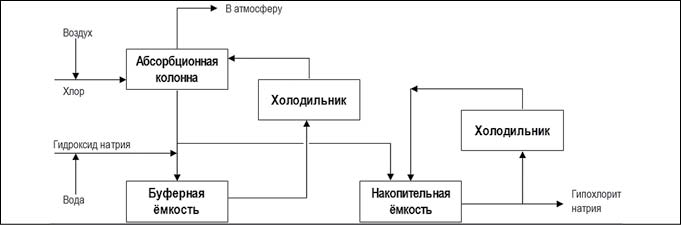
- основной процесс, в результате которого производится 16%-ный раствор гипохлорита натрия в смеси с хлоридом натрия и гидроксидом натрия (рис. 4).
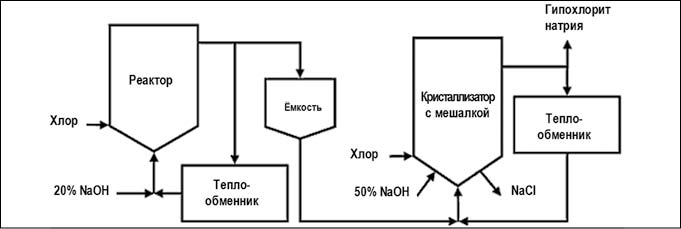
- низко-солевой или концентрированный процесс позволяет получить концентрированные растворы (25–40%) гипохлорита натрия с меньшим содержанием примесей. Его отличие от основного способа заключается в добавлении второй стадии хлорирования. Во второй реактор подается не гидроксид натрия, а раствор гипохлорита натрия из первого реактора, в результате происходит концентрирование готового продукта (рис. 5).
Рис. 4. Химический метод получения гипохлорита натрия основным процессом (рис. с сайта https://ru.wikipedia.org)
Рис. 5. Химический метод получения гипохлорита натрия концентрированным процессом (рис. с сайта https://ru.wikipedia.org)
При электрохимическом методе получения гипохлорита натрия водный раствор хлорида натрия подвергается электролизу в электролизере с открытыми электродными зонами (бездиафрагменный способ). Гидроксид натрия, образующийся на катоде, и хлор, выделяющийся на аноде, беспрепятственно смешиваются в ходе электрохимического процесса
NaCl + H2O = NaClO + H2↑(суммарная реакция).
Гипохлорит кальция производится в виде хлорной извести, представляющей собой смесь целевого продукта с хлоридом кальция и гидроксидом кальция. В качества сырья для получения хлорной извести используется порошкообразный гидроксид кальция (пушенка), содержащий менее 1% свободной влаги и разбавленный влажным воздухом хлор. Небольшая влажность исходных веществ обеспечивает начало реакции гидролиза хлора, сопровождающейся нейтрализацией образующихся кислот известью. Затем реакция продолжается за счет воды, выделяющейся из гидроксида кальция при хлорировании
2Сa(OH)2 + 2Cl2 = Сa(ClO)2 + СaCl2 + 2H2O (суммарно).
Хлорирование пушенки осуществляется в аппаратах непрерывного действия – механических полочных камерах Бакмана.
Таблица 4. Производители гипохлорита натрия в России.
| Название предприятия | Сайт предприятия |
|---|---|
| «Каустик» ЗАО, г. Стерлитамак | www.kaus.ru/ |
| «Каустик» ОАО, г. Волгоград | www.kaustik.ru/ |
| «Новомосковский хлор» ООО, г. Новомосковск | www.hlor.biz/ |
| «Сода-хлорат» ООО, г. Березняки | www.soda.perm.ru/ |
Характеристика товарных гипохлоритов, обращение, хранение и транспортировка
В Российской Федерации гипохлориты производятся в соответствии с ГОСТ 11086–76 «Гипохлорит натрия. Технические условия» и ГОСТ 1692–85 «Известь хлорная. Технические условия». Гипохлорит натрия по назначению и показателям выпускается двух марок «А» и «Б» (табл. 5).
Таблица 5. Физико-химические показатели и назначение гипохлорита натрия по ГОСТ 11086–76
| Наименование показателя |
Марка А |
Марка Б |
|---|---|---|
| Внешний вид |
Жидкость зеленовато-желтого цвета |
|
| Коэффициент светопропускания, % не менее |
20 |
20 |
| Массовая концентрация активного хлора, г/дм3, не менее |
190 |
170 |
| Массовая концентрация щелочи в пересчете на NaOH, г/дм3 |
10–20 |
40–60 |
| Массовая концентрация железа, г/дм3, не более |
0,02 |
0,06 |
| Область применения |
В химической промышленности для обеззараживания питьевой воды и воды плавательных бассейнов, для дезинфекции и отбелки |
В витаминной промышленности как окислитель и для отбеливания ткани |
Гипохлорит натрия должен храниться в специальных полиэтиленовых, стальных гуммированных или других, покрытых коррозионно-стойкими материалами ёмкостях, наполненных на 90% объёма и оборудованных воздушником для сброса образующегося при распаде кислорода. Емкости с гипохлоритом натрия хранят в защищённых от света закрытых складских неотапливаемых помещениях. Перевозка продукции осуществляется в соответствии с правилами транспортировки опасных грузов.
Хлорная известь в зависимости от способа получения выпускается двух марок «А» и «Б» и трех сортов для каждой марки (табл. 6).
Таблица 6. Физико-химические показатели и способ получения хлорной извести по ГОСТ 1692–85
|
Наименование показателя |
Марка А | Марка Б | ||||
| 1-й сорт | 2-й сорт | 3-й сорт | 1-й сорт | 2-й сорт | 3-й сорт | |
|
Внешний вид |
Порошок белого цвета или слабоокрашенный, с наличием комков |
|||||
|
Массовая концентрация активного хлора, %, не менее |
28 | 25 | 20 | 35 | 32 | 27 |
|
Коэффициент термостабильности, не менее |
0,90 | 0,90 | 0,80 | 0,75 | 0,70 | 0,60 |
|
Способ получения |
Хлорирование пушенки в кипящем слое | Хлорирование пушенки в аппаратах Бакмана |
Хлорную известь упаковывают в полиэтиленовые мешки и стальные барабаны, окрашенные со всех сторон химически стойкой краской. Хлорную известь хранят в закрытых складских неотапливаемых, затемненных и хорошо проветриваемых помещениях. Не допускается хранение с хлорной известью взрывчатых веществ, огнеопасных грузов и баллонов со сжатыми газами. Гарантийный срок хранения хлорной извести марки А 1-го и 2-го сортов – 3 года со дня изготовления, марки А 3-го сорта и марки Б – 1 год со дня изготовления. Перевозка продукции осуществляется в соответствии с правилами транспортировки опасных грузов.
Требования безопасности
Гипохлориты являются окислителями, вызывающими раздражение кожных покровов и слизистых оболочек. Гипохлориты при попадании на кожу могут вызвать ожоги, а при попадании в глаза – слепоту. При попадании гипохлоритов на кожные покровы необходимо обмывать их обильной струей воды в течение 10–15 мин. При попадании гипохлоритов в глаза следует немедленно промыть их обильным количеством воды и направить пострадавшего к врачу. Приём внутрь разбавленных растворов (3 – 6%) гипохлоритов приводит обычно только к раздражению пищевода и иногда ацидозу, в то время как концентрированные растворы способны вызвать довольно серьёзные повреждения, вплоть до перфорации желудочно-кишечного тракта. При работе с гипохлоритами следует иметь специальные средства защиты: защитные очки, резиновые сапоги, резиновые перчатки, фартук из прорезиненной ткани и противогаз, а также использовать специальную одежду.
Несмотря на свою высокую химическую активность, безопасность гипохлоритов для человека документально подтверждена исследованиями токсикологических центров Северной Америки и Европы. Результаты показывают, что гипохлориты не являются мутагенными, канцерогенными и тератогенными соединениями, а также кожными аллергенами. Международное агентство по изучению рака пришло к выводу, что питьевая вода, прошедшая обработку гипохлоритом натрия, не содержит человеческих канцеро- генов.
При нагревании выше 35°С растворы гипохлоритов разлагаются с образованием хлоратов и выделением кислорода. Слабощелочной раствор достаточно устойчив. Растворы гипохлоритов негорючи и невзрывоопасны. Однако в процессе высыхания гипохлориты могут вызвать загорание органических продуктов и горючих веществ. При взаимодействии гипохлоритов с кислотами выделяется токсичный хлор (раздражающий и удушающий эффект), поэтому не допускается смешение и совместное хранение данных веществ.
При работе с гипохлоритами производственные помещения должны быть оборудованы приточно-вытяжной вентиляцией. Оборудование должно быть герметичным. Негерметичные узлы должны быть снабжены местными вентиляционными отсосами.
Применение в средствах бытовой химии
Применение гипохлоритов в средствах бытовой химии обусловлено их окислительными и дезинфицирующими свойствами. Гипохлориты являются основными действующими веществами в химических отбеливателях, пятновыводителях, средствах для обеззараживания воды в бассейнах, в чистящих и моющих средствах с дезинфицирующим эффектом.
Отбеливатели
Мировое производство гипохлорита натрия оценивается в 5 миллионов тонн. Более половины всего производимого гипохлорита натрия используется в качестве отбеливателя и пятновыводителя для тканей. Гипохлорит натрия может быть использован для многих видов тканей, включая хлопок, полиэстер, нейлон, ацетат, лен, вискозу и другие. Он эффективен для удаления следов почвы и широкого спектра пятен, в том числе, от кофе, крови, травы, горчицы, ягодных и фруктовых соков и т.д.
Содержание гипохлорита натрия в отбеливателях и пятновыводителях для тканей обычно находится в диапазоне от 2,5 до 10%. В большинстве случаев эти средства выпускаются в жидкой форме в пластиковых бутылках или канистрах. Дополнительными компонентами отбеливателей являются поверхностно-активные вещества, модификаторы реологии, оптические отбеливатели, стабилизаторы разложения и др.
Преимуществами отбеливателей на основе гипохлоритов являются:
- быстрое и качественное отбеливание;
- использование отбеливателя без нагревания и даже в холодной воде;
- доступная цена;
- более удобная форма выпуска: не «пылят», в отличие от порошков и легко дозируются;
- многофункциональность, так как помимо отбеливания и удаления пятен подходят для дезинфекции различных поверхностей.
Недостатками отбеливателей на основе гипохлоритов являются:
- активное использование хлорсодержащих отбеливателей приводит к тому, что ткани быстрее изнашиваются и, как следствие, легко рвутся;
- невозможность отбеливания шёлковых, шерстяных и некоторых синтетических волокон из-за интенсивного разрушения;
- относительно короткий срок хранения;
- невозможность использования в автоматической стиральной машине, особенно в сочетании с современными порошками;
- сильный специфичный запах хлора.
Моющие и чистящие средства с дезинфицирующими свойствами
Гипохлориты используются во многих жидких и порошкообразных средствах:
- для автоматических посудомоечных машин;
- для ухода за ванными комнатами, душевыми и туалетами;
- для очистки кухонных плит;
- для мытья каменных и бетонных полов;
- для очистки коптилен и грилей;
- очистки канализационных сливов;
- для уборки поверхностей в кухнях и столовых и др.
Эффективность очистки средствами, содержащими гипохлорит-ионы, обусловлена их сильным окисляющим действием. При деструкции крупных молекул загрязнителей образуются низкомолекулярные продукты разложения, характеризующиеся высокой растворимостью, отсутствием окраски и запаха. Одновременно с очищающим действием, гипохлориты проявляют высокую дезинфицирующую способность. В целом эффективность гипохлоритов возрастает с увеличением концентрации и температуры раствора, а так же при понижении кислотности раствора.
Гипохлоритсодержащие средства с дезинфицирующими свойствами обладают следующими достоинствами:
- эффективны в отношении различных бактерий, грибов и вирусов;
- дезинфицирующая активность мало зависит от жесткости воды;
- при использовании не образуют побочных токсичных продуктов;
- выпускаются в жидкой, порошкообразной и гранулированной формах.
К недостаткам можно отнести:
- нестабильность и потерю активности с увеличением температуры и при взаимодействии с органическими веществами;
- снижение биологической активности с увеличением кислотности среды;
- коррозия нержавеющей стали и других металлов, что допускает лишь кратковременный контакт с поверхностями и оборудованием из металлов;
- потеря активности при хранении на свету;
- ограниченный перечень поверхностно-активных веществ, комплексообразователей, красителей, отдушек, способных быть устойчивыми в композиции моющего или чистящего средства, содержащего гипохлориты.
В заключение следует отметить, что рост производства и потребления гипохлоритов составляет более 2,5% ежегодно. Причем более половины всех произведенных гипохлоритов используется для бытовых целей, а менее половины для промышленных. Широкое использование гипохлоритов в средствах бытовой химии стало возможным благодаря их коммерческой доступности и высокой эффективности. Гипохлорит натрия является безусловным лидером среди других солей хлорноватистой кислоты, занимая 91% мирового рынка. Почти 9% остается за гипохлоритом кальция. Использование гипохлорита калия имеет историческое значение, однако, объемы его современного применения незна- чительные.
Источники
- Handbook of detergents. Part A: Properties/ Edited by Guy Broze. New York: Marsell Dekker, 1999. 809 p.
- Фурман Л. А. Хлорсодержащие окислительно-отбеливающие и дезинфицирующие вещества. М.: Химия, 1976. 88 с.
- Ушакова В.Н. Мойка и дезинфекция. Пищевая промышленность, торговля, общественное питание. – СПб.: Профессия, 2009. 288 с.
- ГОСТ 1692–85. Известь хлорная. Технические условия.
- ГОСТ 11086–76. Гипохлорит натрия. Технические условия.
- Лидин Р.А. и др. Константы неорганических веществ: справочник / Под ред. проф. Р.А. Лидина. М.: Дрофа, 2000. 480 с.
- Химическая энциклопедия/ Гл. ред. И.Л. Кнунянц. М.: Советская энциклопедия, 1992. Т. 3. 555 с.
- Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей/ Под ред. проф. Н.В. Лазарева и проф. И.Д. Гадаскиной. Л.: Химия, 1977. Т. 3. 608 с.
- https://ru.wikipedia.org/wiki/Гипохлорит_натрия
Гипохлорит кальция / общая информация
Соль кальция и хлорноватистой кислоты с формулой Сa(ClO)2, образует кристаллогидраты. Устойчив в сухой атмосфере без CO2.
Формула: Ca(ClO)2
Название ИЮПАК: Calcium hypochlorite
Молярная масса: 142,98 г/моль
Насыпная плотность: 0,9 г/см3
Температура плавления: 100°C
Растворимость: Вода
ТУ Гипохлорит кальция в каталоге продукции

Область применения
Гипохлорит кальция — широко распространенный реагент для нейтрализации стоков золотодобычи, обеззараживания и очистки воды и водопроводных сооружений, дезинфекции различных поверхностей, содержащий 65-70% активного хлора.
Нейтрализация цианидов в золотодобыче
Эффективное обеззараживание воды
Дезинфекция общественных зон
Отбеливание ткани и бумаги
Приоритеты
Проект соответствует приоритетам, обозначенным в ежегодном Послании Президента РФ Федеральному собранию от 4 декабря 2014 года.
- Улучшение инвестиционного климата;
- Социальное развитие и осуществление инвестиции в человеческий капитал;
- Поддержка высокотехнологичных секторов экономики;
- Сбалансированное региональное развитие.
Проект отвечает основным приоритетам, отраженным в Стратегии социально-экономического развития Чувашской Республики до 2020 года.
Импортозамещение
Проект включен в отраслевой план мероприятий по импортозамещению в отрасли химической промышленности Российской Федерации, утвержденный приказом № 646 Минпромторга России от 31 марта 2015 года.



Инвестиции
Проект включен в Перечень комплексных инвестиционных проектов по приоритетным направлениям гражданской промышленности в соответствии с постановлением Правительства РФ.



Экология
Цех по производству гранулированного гипохлорита кальция спроектирован как современное высокотехнологичное предприятие. В проекте заложен ряд технологических и технических решений, способствующих минимизации негативного воздействия на окружающую среду в рамках требований Российского экологического законодательства и международных стандартов.
При производстве гипохлорита кальция выбросы в атмосферу будут практически исключены за счет использования систем улавливания промышленных выбросов со всех технологических схем производства. Все побочные продукты предполагается перерабатывать для дальнейшего использования в производственном цикле цехов ПАО «Химпром» или для получения других товарных продуктов.



Производственный цикл
В производстве гипохлорита кальция используются не только основные сырьевые ресурсы, но и попутно получаемые полупродукты, которые снижают расход сырья и сводят к минимуму загрязнение окружающей среды.

Контакты управления реализации
Для получения дополнительной информации, а так же по вопросам приобретения и поставки гипохлорита кальция
Цена: 9 500,00 руб.
Гипохлорит кальция (кальция гипохлорит нейтральный) (CaCL2O2) — соль кальция и хлороноватистой кислоты, представляет собой порошкообразный продукт белого цвета слабоокрашенный с резким запахом хлора.
Хлор на протяжении многих лет является эффективным дезинфекционным средством. Его применяли (и сейчас используют) для обеззараживания:
- различных поверхностей;
- очищения колодцев;
- дезинфекции выгребных ям и септиков.
Но положительный эффект и тогда и сейчас во многом зависит от профессионализма тех, кто применяет гипохлорит кальция для дезинфекции и от того используют ли они инструкцию по применению гипохлорита кальция для дезинфекции.
Что такое гипохлорит кальция
Порошок белого цвета, со слабым запахом хлорки – это и есть кальция гипохлорит нейтральный. При определении данного средства используют аббревиатуру КГН.
Содержание хлора в данном средстве не больше 60%, но не меньше 45%. Храниться оно должно строго в герметичной упаковке (именно так его хранят на предприятиях-производителей). Температура при хранении не должна превышать +30 градусов.
Из данного порошка готовят специальный раствор. Он мутный, чуть беловатого оттенка. Храниться может не более трех суток. На дне раствора остается осадок из нерастворимых кальционных солей.
Общее применение
Средство используют при обеззараживании:
- скотомогильников (особенно, если есть подозрение на наличие очага инфекции);
- выгребных ям и септиков;
- почвы и асфальта;
- помещений, в которых долгое время находились больные холерой или туберкулезом (действует как бактерицидное средство);
- помещений общего пользования (больницы, школы, детские сады, лагеря, базы отдыха и пансионаты);
- уборных общего пользования;
- жилых индивидуальных помещений;
- предметов быта (кроме металлических предметов, которые могут подвергнуться коррозии);
- посуды (после обработки посуду необходимо тщательно промыть несколько раз).
Такое средство как гипохлорит кальция 45 применяется при обеззараживании питьевой воды и воды в плавательных бассейнах.
Для дезинфекции одежды данный раствор не применяют, она почти сразу приходит в негодность.
Если раствор попадет в глаза или на незащищенную кожу, может возникнуть покраснение и начаться жжение. Необходимо промыть глаза и кожу большим количеством чистой воды
При попадании в желудок раствор может вызвать воспаление ЖКТ. Это умеренно опасное средство. Лечение при попадании вещества в организм человека должен назначить врач.
Применение гипохлорита кальция должно строго контролироваться специалистами.
Как правильно приготовить раствор
Для дезинфекции КГН используют:
- в виде не осветленного раствора;
- в виде светлого раствора;
- активированного раствора;
- в виде порошка.
Не осветленный раствор изготовляют из 200 грамм порошка КГН и одного литра воды.
Светлый раствор готовят из не осветленного раствора.
- Не осветлённому раствору дают отстояться.
- Жидкость, которая образовалась над осадком, сливают (получается один литр раствора с концентрацией чистого хлора 10%).
- Жидкость разбавляют для получения светлого раствора (если нужен один литр раствора с хлором 0,5%, то 50 мл активированного раствора разводят в одном литре воды (10% разделить на 0,5%, 1000 мл разделить на 20); если нужна другая концентрация применяются простые математические методы подсчета).
Для получения активированного раствора в светлый раствор подсыпают соли аммония в пропорциях один к двум. Данного типа раствор изготовляют прямо перед применением.
Применение разного типа растворов и порошка
Вопрос о том, где применяют раствор гипохлорита кальция важен. Здесь акценты расставлены очень точно.
Не осветленный раствор применяют для обработки:
- производственных помещений (600 мл. на квадратный метр);
- надворных построек (600 мл. на квадратный метр);
- мусорных ям (600 мл. на квадратный метр);
- инвентаря, которым убирается мусор.
Осветленный раствор используют при обеззараживании:
- жилых помещений (210 мл. на квадратный метр; после обработки помещение надо в обязательном порядке убрать и проветрить);
- мебели (можно распылять средство из расчета 210 мл на квадратный метр; можно использовать раствор для влажного протирания поверхностей из расчета 180 мл. на квадратный метр);
- посуды (один комплект посуды на два литра средства);
- детских игрушек (мелкие можно вымачивать в растворе, а крупные — орошать; после выдерживания игрушки необходимо отчистить с помощью большого количества воды).
Активированный раствор используют при вспышках вирусных и инфекционных заболеваний (600 мл на квадратный метр).
Порошком обрабатывают выделения больных, остатки пищи, питьевую воду. Порошок используют в больших количествах или в пропорциях один к одному.
Правила работы со средством
Техника безопасности при работе должна обязательно соблюдаться.
Категорически запрещено работать со средством:
- детям до 18 лет;
- беременным;
- лицам с общими противопоказаниями.
Кроме того:
- приготовление раствора необходимо проводить в помещениях с хорошей системой вентиляции или в специальных вытяжных шкафах;
- специалисты должны быть одеты в спецодежду и иметь защитные маски на лице. Если действовать строго по инструкции, то человек должен быть защищен респиратором РУ-60 с патроном марки А; защитными очками, резиновыми перчатками; защитными передниками;
- хранить порошок и раствор можно только в емкостях с плотными крышками, в помещениях, недоступным детям, хорошо вентилируемых и не влажных;
- все обработанные бытовые предметы и детские игрушки необходимо тщательно промывать до полного исчезновения запаха хлора;
- Остатки порошка запрещено просто выбрасывать в мусорник, его разводят водой и сливают в канализацию;
- после окончания работы со средством необходимо тщательно вымыть руки (но лучше принять душ).
Характеристики
| Страна производитель | Китай |
| Вес | 50 |
| Внешний вид | Порошкообразный продукт белого цвета или слабоокрашенный |
| Массовая доля активного хлора, не менее, %* | 45 — 54 |
| Массовая доля воды, не более, % | 4 |
| Коэффициент стабильности, не менее | 0,8 |
| Гарантийный срок хранения продукта | 1 год со дня изготовления |