ИНФЛАРЕТ инструкция по применению
📜 Инструкция по применению ИНФЛАРЕТ
💊 Состав препарата ИНФЛАРЕТ
✅ Применение препарата ИНФЛАРЕТ
📅 Условия хранения ИНФЛАРЕТ
⏳ Срок годности ИНФЛАРЕТ
Описание лекарственного препарата ветеринарного назначения ИНФЛАРЕТ
Основано на официально утвержденной инструкции по применению
препарата ИНФЛАРЕТ для специалистов
и утверждено компанией-производителем для электронного издания справочника Видаль Ветеринар
2017 года
Дата обновления: 2016.10.07
Лекарственная форма
|
|
ИНФЛАРЕТ |
Раствор для инъекций рег. №4477-10-14 БПХ-Ф |
Форма выпуска, состав и упаковка
Раствор для инъекций в виде прозрачной жидкости от светло-желтого до желтого цвета, без механических включений.
Вспомогательные вещества, растворитель.
Расфасован по 100 мл в стеклянные флаконы.
Фармакологические (биологические) свойства и эффекты
Мелоксикам, входящий в состав препарата, относится к НПВС класса оксикамов (производное еноловой кислоты), обладает выраженным противовоспалительным, анальгезирующим и жаропонижающим действием.
Механизм действия заключается в избирательном ингибировании фермента ЦОГ и подавлении синтеза простагландинов (медиаторов воспаления). Мелоксикам ингибирует преимущественно ЦОГ-2, обеспечивая противовоспалительный и жаропонижающий эффект, и незначительно влияет на ЦОГ-1, сводя к минимуму развитие побочных эффектов, таких как кровотечения, образование язв и нарушение функции почек.
Препарат полностью абсорбируется после парентерального введения. Биодоступность при в/м введении близка к 100%. После в/м введения препарата максимальная концентрация мелоксикама создается в крови через 60-90 мин и удерживается на терапевтическом уровне до 24 ч. Препарат метаболизируется в печени. Выводится в равной мере с фекалиями и мочой, преимущественно в виде метаболитов. В неизменном виде с калом выводится меньше 5% величины суточной дозы, в моче в неизменном виде препарат обнаруживается только в следовых количествах. Средний период полувыведения составляет 20 ч.
Показания к применению препарата ИНФЛАРЕТ
В качестве противовоспалительного, обезболивающего и жаропонижающего средства в составе комплексной терапии при:
- акушерско-гинекологических заболеваниях (маститы, эндометриты, синдром мастит-метрит-агалактия);
- заболеваниях ЖКТ (диарея различной этиологии молодняка сельскохозяйственных животных);
- респираторных заболеваниях (пневмонии, бронхиты и другие);
- острых и хронических заболеваниях опорно-двигательного аппарата, которые сопровождаются сильной болью и воспалением (переломы, травматические артропатии, растяжение связок и сухожилий, остеоартриты, хронические дегенеративные заболевания суставов и другие).
Для снятия болевого синдрома различной этиологии у сельскохозяйственных животных.
Порядок применения
Препарат применяют однократно:
- крупному и мелкому рогатому скоту — п/к или в/м в дозе 2.5 мл на 100 кг массы животного (0.5 мг/кг мелоксикама);
- лошадям — в/м в дозе 3 мл на 100 кг массы животного (0.6 мг/кг мелоксикама);
- свиньям — в/м в область шеи в дозе 0.2 мл на 10 кг массы животного (0.4 мг/кг мелоксикама).
Объем введения не должен превышать 10 мл в одно место.
При необходимости введение препарата повторяют через 24 ч.
Побочные эффекты
Побочных явлений и осложнений при применении препарата в соответствии с инструкцией не наблюдается. При применении препарата у животных в месте введения возможно образование припухлости, которая постепенно проходит.
Противопоказания к применению препарата ИНФЛАРЕТ
Запрещается применение препарата:
- телятам, не достигшим недельного возраста;
- жеребятам, не достигшим 6-недельного возраста;
- жеребым или лактирующим кобылам;
- животным с нарушениями функции почек и печени;
- при повышенной чувствительности к мелоксикаму.
Особые указания и меры личной профилактики
Запрещается одновременное применение препарата с ГКС, другими НПВС, антикоагулянтами.
В случае возникновения аллергических реакций препарат отменяют и назначают антигистаминные препараты (Димедрол, Тавегил), препараты кальция (кальция глюконат, кальция хлорид) и вводят плазмозаменяющие растворы.
Убой животных на мясо разрешается через 5 суток после последнего введения. Мясо животных, вынужденно убитых до истечения указанного срока, может быть использовано для кормления пушных зверей.
Молоко можно использовать в пищу через 3 суток после применения препарата. До истечения указанного срока молоко после предварительного кипячения скармливают молодняку сельскохозяйственных животных.
Меры личной профилактики
При работе с препаратом следует соблюдать меры личной гигиены и правила техники безопасности.
Условия хранения ИНФЛАРЕТ
Препарат следует хранить в упаковке производителя, в сухом, защищенном от света месте при температуре от 5°С до 25°С.
Срок годности ИНФЛАРЕТ
Срок годности при соблюдении условий хранения — 2 года со дня изготовления; после первого вскрытия флакона — не более 28 суток.
Контакты для обращений
|
|
222823 Минская обл., Пуховичский р-н, г.п. Свислочь, Промышленный пер., 9 |
ИНФЛАРЕТ отзывы
Помогите другим с выбором, оставьте отзыв об ИНФЛАРЕТ
Оставить отзыв
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
- 8.07.2019
- 237 просмотров
Медикамент выпускает белорусское предприятие Белэкотехника. Активный компонент мелоксикам, зарегистрированный ВОЗ, применяется в медицине. Терапевтическая форма — раствор для инъекций.
Как работает лекарство
Препарат представляет прозрачный 2% раствор мелоксикама желтого цвета, расфасованный во флаконы объемом 100 мл.
Стоимость в июне 2019 г. составила 1680 руб.
Фармакологическое действие заключается в подавлении синтеза простагландинов — передатчиков воспаления. Концентрация мелоксикама достигает терапевтических значений через час после введения и удерживается сутки.
Инфларет назначают при перечисленных заболеваниях:
- Акушерско-гинекологических — эндометрит, мастит, синдром ММА.
- Алиментарных и респираторных — энтериты, бронхиты.
- Опорно-двигательного аппарата, сопровождающиеся болевыми симптомами — переломы, артриты.
Препарат вводят жвачным животным внутримышечно или подкожно, однократно, согласно схеме:
| Вид животного | Дозировка, мл/100 кг веса |
| Жвачные | 2,5 |
| Лошади | 3 |
| Свиньи | 2 |
При необходимости препарат вводят повторно через 24 часа. В одну точку прокалывают не более 10 мл. Инфларет не назначают жеребым и лактирующим лошадям. Срок ожидания по молоку — 3; по мясу — 5 суток.
Чем заменяют и как хранят
Аналоги Инфларета:
- Мексикам;
- Локсик;
- Мелоксидил.
Препарат хранят 2 года при температуре от 5 до 25 °С. После вскрытия флакона его содержимое необходимо выработать за 4 недели.
Автор: Кулешов Е. И. (ветеринар, доцент, кандидат сельскохозяйственных наук)
Белэкотехника
Редакция сайта категорически не рекомендует заниматься самостоятельным лечением животных! Информация о ветеринарных препаратах, опубликованная на сайте, предназначена для специалистов. Самостоятельное лечение животных, описанными препаратами, может нанести вред. Обязательно консультируйтесь с ветеринарными врачами в очной форме перед применением препаратов.
Название:
Артикул:
Текст:
Инфларет, 100 мл
- Описание
- Отзывы
Инфларет. Раствор для инъекций.
- Инструкция Инфларет (pdf, 2 Мб)
Препарат применяют в качестве противовоспалительного, обезболивающего и жаропонижающего средства в составе комплексной терапии при акушерско-гинекологических (маститы, эндометриты, синдром мастит-метрит-агалактия), желудочно-кишечных (диареи различной этиологии молодняка сельскохозяйственных животных), респираторных (пневмонии, бронхиты и др.) заболеваниях.
Препарат назначают при острых и хронических заболеваниях опорно-двигательного аппарата, которые сопровождаются сильной болью и воспалением (переломы, травматические артропатии, растягивание связок и сухожилий, остеоартриты, хронические дегенеративные заболевания суставов и другое), а также для снятия болевого синдрома различной этиологии у сельскохозяйственных животных.
| Состав | В 1 мл раствора для инъекций содержится: 20,0 мг мелоксикама |
| Применение |
Препарат применяют однократно: — крупному и мелкому рогатому скоту – подкожно или внутримышечно в дозе 2,5 см3 на 100 кг массы животного (0,5 мг/кг мелоксикама); — лошадям – внутримышечно в дозе 3,0 см3 на 100 кг массы животного (0,6 мг/кг мелоксикама); — свиньям – внутримышечно в область шеи в дозе 0,2 см3 на 10 кг массы животного (0,4 мг/кг мелоксикама). |
| Период ожидания |
Молоко — 5 суток Мясо — 15 суток |
| Форма выпуска | Стеклянные флаконы 100 мл |
| Срок годности | 2 года от даты изготовления при соблюдении условий хранения. После первого вскрытия флакона — не более 28 суток. |
| Условия хранения | Препарат хранят в упаковке предприятия-изготовителя по списку Б, в сухом, защищенном от света месте при температуре от плюс 5 °С до плюс 25 °С. |


Назад
Ветеринарный инструмент из Европы и Азии.
Заказывай у нас!
Получай свои скидки!

Cкидки и акции
распродажа каждую неделю
Онлайн поддержка
24/7 за неделю
Действующим веществом препарата АДЕНУРИК таблетки является фебуксостат, и он используется для лечения при подагре – заболевании, связанном с избыточным накоплением мочевой кислоты (уратов) в организме. У некоторых людей в крови содержится слишком много мочевой кислоты, в связи с чем она становится нерастворимой. Вследствие этого могут образоваться кристаллы уратов, откладывающиеся в суставах и почках. Данный процесс может сопровождаться внезапной сильной болью, покраснением, припухлостью и повышением температуры сустава (приступ подагры). При отсутствии лечения отдельные кристаллы формируют большие скопления (тофусы) в суставах и вокруг них. Эти тофусы могут разрушать сустав и кость.
Эффект препарата АДЕНУРИК основан на снижении уровня мочевой кислоты. На фоне приема препарата АДЕНУРИК концентрация мочевой кислоты остается достаточно низкой, что предотвращает образование кристаллов и со временем способствует уменьшению тяжести симптомов заболевания. Если концентрация мочевой кислоты остается низкой в течении длительного времени, то размер тофусов также может уменьшиться.
Препарат АДЕНУРИК таблетки 120 мг применяется также для лечения и профилактики при высокой концентрации мочевой кислоты в крови, которая может возникать в начале химиотерапии по поводу злокачественных заболеваний крови.
При проведении химиотерапии происходит разрушение опухолевых клеток, вызывая повышение концентрации мочевой кислоты в крови, если не проводилась профилактика образования мочевой кислоты.
Препарат АДЕНУРИК предназначен для применения у взрослых.
• При наличии аллергии на фебуксостат, или на другие компоненты препарата (перечисленные в разделе «Состав»).
Перед началом приема препарата АДЕНУРИК сообщите врачу, если:
• Вы страдаете (или страдали) сердечной недостаточностью или другими заболеваниями сердца.
• Вы страдаете (или страдали) заболеваниями почек и/или у Вас были тяжелые аллергические реакции на аллопуринол (медикамент, применяющийся для лечения подагры).
• Вы страдаете (или страдали) заболеваниями печени или у Вас имеют место отклонения показателей функции печени.
• Вы получали лечение в связи с повышением уровня мочевой кислоты при синдроме Леш-Нихана (редкое наследственное заболевание, для которого характерен высокий уровень мочевой кислоты в крови).
• Вы страдаете заболеваниями щитовидной железы.
В случае появления аллергических реакций на АДЕНУРИК, прекратите прием препарата (см. также раздел «Возможные побочные действия»). Возможными симптомами аллергических реакций являются:
— сыпь, включая тяжелые формы (такие, как пузыри, узлы, зудящая и эксфолиативная сыпь), кожный зуд,
— отек конечностей или лица,
— затрудненное дыхание,
— лихорадка и увеличение лимфоузлов,
— а также тяжелые угрожающие жизни аллергические состояния, сопровождающиеся остановкой сердца и кровообращения.
Лечащий врач может принять решение о бессрочной отмене терапии препаратом АДЕНУРИК.
Имеются редкие сообщения о возникновении кожной сыпи, потенциально опасной для жизни, после приема препарата АДЕНУРИК (синдром Стивенса-Джонсона), при котором на теле сначала появляются красноватые мишеневидные пятна или циркулярные очаги, часто с центральным пузырем. Также при этом могут развиться язвы в полости рта, глотке, в носу, на половых органах и конъюнктивит (покраснение и опухание глаз). Прогрессирование сыпи может происходить с распространением пузырей или отслоением кожи.
В случае развития синдрома Стивенса-Джонсона после приема фебуксостата, прием препарата АДЕНУРИК возобновлять нельзя. В случае развития сыпи или вышеперечисленных кожных симптомов, следует немедленно обратиться к врачу и сообщить ему о том, что Вы принимаете данный препарат.
Если в настоящее время у Вас наблюдается обострение подагры (внезапная сильная боль, покраснение, болезненность, припухлость и повышение температуры суставов), то следует дождаться его затихания, прежде чем начинать лечение препаратом АДЕНУРИК.
В некоторых случаях обострение подагры может иметь место в начале лечения препаратами, снижающими уровень мочевой кислоты. Такое обострение отмечается далеко не у всех пациентов, но в первые недели или месяцы лечения препаратом АДЕНУРИК у Вас могут появляться приступы подагры. Важно не прекращать лечение при появлении таких приступов, так как даже в этом случае АДЕНУРИК способствует уменьшению концентрации мочевой кислоты. Если Вы принимаете АДЕНУРИК ежедневно согласно назначениям врача, то со временем приступы подагры станут более редкими и будут менее болезненными.
При необходимости Ваш лечащий врач может назначить препараты, предотвращающие или облегчающие симптомы подагры (боль и припухлость суставов).
У пациентов с очень высоким уровнем уратов (например, у тех, кто получает химиотерапию по поводу злокачественных заболеваний), лечение препаратами, снижающими уровень мочевой кислоты, может приводить к накоплению ксантинов в мочевыводящих путях с возможным образованием камней, даже если это не наблюдалось у пациентов, принимавших АДЕНУРИК в связи с синдромом распада опухоли.
Ваш лечащий врач может назначить проведение анализа крови для оценки функции печени.
Дети и подростки
Детям младше 18 лет данный препарат принимать нельзя в связи с тем, что для данной группы пациентов его безопасность и эффективность не установлены.
АДЕНУРИК содержит лактозу
Таблетки препарата АДЕНУРИК содержат лактозу (вид сахара). Если у Вас была установлена непереносимость каких-либо видов сахара, перед применением данного препарата проконсультируйтесь со своим лечащим врачом.
Если Вы принимаете или до недавнего времени принимали какие-либо другие лекарственные средства, включая препараты, отпускаемые без рецепта, сообщите об этом лечащему врачу или работнику аптеки.
Особенно важно сообщить о препаратах, содержащих приведенные ниже вещества, которые могут взаимодействовать с препаратом АДЕНУРИК. В этом случае врач может принять необходимые меры:
• Меркаптопурин (используется для лечения злокачественных новообразований).
• Азатиоприн (используется для снижения иммунного ответа).
• Теофиллин (используется для лечения бронхиальной астмы).
Риск неблагоприятного воздействия на плод при лечении препаратом АДЕНУРИК не установлен. Во время беременности прием препарата АДЕНУРИК не рекомендуется. Также не известно, проникает ли АДЕНУРИК в грудное молоко. Препарат нельзя принимать во время кормления грудью или при подготовке к нему.
В случае, если Вы беременны или кормите грудью, или думаете, что беременны, или собираетесь забеременеть, обратитесь за советом к лечащему врачу или работнику аптеки перед тем, как принимать данный препарат.
Следует помнить, что во время лечения могут появляться ощущение оглушенности, сонливость, размытость зрения, чувство онемения или покалывания, при развитии которых рекомендуется воздержаться от управления транспортными средствами или от работы с механизмами.
Всегда принимайте АДЕНУРИК в соответствии с рекомендациями лечащего врача. При возникновении вопросов проконсультируйтесь с врачом или работником аптеки.
• Стандартная доза препарата составляет 1 таблетку 1 раз в сутки. На оборотной стороне блистерной упаковки отмечены дни недели, чтобы Вы могли контролировать регулярность приема препарата.
• АДЕНУРИК принимают внутрь до, во время или после еды.
Подагра
АДЕНУРИК выпускается в таблетках по 80 мг или 120 мг. Лечащий врач должен назначить препарат в наиболее подходящей Вам дозе.
Важно принимать АДЕНУРИК ежедневно, даже при отсутствии приступов подагры.
Профилактика и лечение при высоком уровне мочевой кислоты у пациентов, получающих химиотерапию по поводу злокачественного заболевания
АДЕНУРИК выпускается в таблетках по 120 мг.
Прием препарата АДЕНУРИК следует начинать за двое суток перед началом химиотерапии и продолжать в соответствии с указаниями лечащего врача. Обычно лечение является кратковременным.
Если Вы превысили рекомендованную дозу препарата АДЕНУРИК
Если Вы случайно приняли большую дозу препарата, необходимо немедленно проинформировать лечащего врача или обратиться в ближайшее отделение неотложной помощи.
Если Вы забыли принять АДЕНУРИК
Если Вы забыли вовремя принять АДЕНУРИК, примите его сразу же, как вспомните. Если же Вы вспомнили об этом незадолго до следующего приема препарата, пропустите забытый прием и примите препарат в обычное время. Не принимайте препарат в двойной дозе для компенсации пропущенного приема.
Если Вы прекратили принимать АДЕНУРИК
Не прекращайте прием препарата АДЕНУРИК без предварительной консультации с врачом, даже если Вы чувствуете себя значительно лучше. Прекращение лечения может сопровождаться повышением концентрации мочевой кислоты и усугублением симптомов заболевания за счет образования новых кристаллов уратов в суставах и вокруг них, и в почках.
Если у Вас появились дополнительные вопросы по поводу данного препарата, обратитесь к врачу или работнику аптеки.
Как и все лекарственные препараты, данный препарат может оказывать побочные действия, хотя они проявляются не у всех пациентов.
Необходимо прекратить прием данного препарата и немедленно обратиться к лечащему врачу или в ближайшее отделение неотложной помощи при появлении следующих редких побочных действий (отмечаются не более чем у 1 из 1 000 пациентов), так как могут последовать тяжелые аллергические реакции:
• анафилактические реакции, гиперчувствительность к препарату (см. также раздел «Предупреждения и меры предосторожности»);
• потенциально опасная для жизни кожная сыпь, характеризующаяся образованием пузырей и отслоением кожи и внутренних поверхностей полостей тела, например, полости рта и половых органов, болезненных язв в полости рта и/или в области половых органов, сопровождающиеся лихорадкой, болью в горле и слабостью (синдром Стивенса-Джонсона / токсикодермальный некролиз) или увеличением лимфоузлов, увеличением печени, гепатитом (вплоть до почечной недостаточности), увеличением количества лейкоцитов в крови (лекарственная реакция с эозинофилией и системными симптомами – DRESS).
• генерализованная кожная сыпь
Частые побочные действия (могут возникать не более чем у 1 из 10 пациентов):
• отклонение показателей функции печени;
• диарея;
• головная боль;
• сыпь (включая различные виды сыпи, см. ниже в разделах «Побочные действия, возникающие иногда/нечастые» и «Редкие побочные действия»);
• тошнота;
• усугубление симптоматики подагры;
• локальное опухание в связи с задержкой жидкости в тканях (отек).
Другие побочные действия, не указанные выше, перечислены ниже.
Побочные действия, возникающие иногда/нечастые (могут возникать не более чем у 1 из 100 пациентов):
• пониженный аппетит, изменение уровня сахара в крови (сахарный диабет), которое может проявляться сильной жаждой, повышением уровня жиров в крови, увеличением веса тела;
• утрата полового влечения;
• нарушения сна, сонливость;
• ощущение оглушенности, чувство онемения или покалывания, снижение или изменение чувствительности (гипестезия, гемипарез или парестезия), снижение вкусовой чувствительности, ухудшение обоняния (гипосмия);
• изменения на электрокардиограмме, аритмия или учащение сердцебиения, ощущение сердцебиения;
• приливы жара (например, покраснение лица или шеи), повышение артериального давления, кровотечение (кровоизлияния, имеющие место только у пациентов, проходящих курс химиотерапии по поводу заболеваний крови);
• кашель, одышка, боль или дискомфорт в грудной клетке, воспаление носовых ходов и/или глотки (инфекции верхних дыхательных путей), бронхит;
• сухость во рту, боль/дискомфорт в животе или метеоризм, изжога/несварение, запор, частый стул, рвота, ощущение дискомфорта в животе;
• зуд, крапивница, воспаление или изменение цвета кожи, мелкие красные или пурпурные пятна на коже, мелкие плоские красные пятна на коже, плоские участки покраснения на коже, покрытые мелкими сливающимися бугорками, сыпь, участки покраснения и пятна на коже, а также другие нарушения со стороны кожи;
• мышечные судороги, мышечная слабость, боль в мышцах или суставах, бурсит или артрит (воспаление суставов, обычно сопровождающееся болью, припухлостью и/или скованностью), боль в конечностях, боль в спине;
• появление крови в моче, учащенное мочеиспускание, изменения в анализе мочи (повышение уровня белка), нарушение функции почек;
• повышенная утомляемость, боль или дискомфорт в грудной клетке;
• камни в желчном пузыре и печеночных протоках (холелитиаз);
• повышение уровня тиреотропного гормона (ПТ);
• изменения в биохимическом анализе крови или в количестве клеток крови или тромбоцитов (нарушения в результатах анализа крови);
• камни в почках;
• нарушение эрекции.
Редкие побочные действия (отмечаются не более чем у 1 из 1000 пациентов):
• поражение мышц, состояние, которое в ряде случаев может стать тяжелым. Это может вызывать нарушения в работе мышц, особенно, если в это время у Вас плохое самочувствие или высокая температура, это может быть вызвано аномальной миопатией. Если у Вас возникли боли в мышцах, болезненность или слабость, немедленно обратитесь к врачу;
• тяжелый отек глубоких слоев кожи, особенно вокруг губ, глаз, половых органов, рук, стоп или языка, с возможным наличием затруднений дыхания;
• лихорадка в сочетании с кореподобной сыпью, увеличением лимфузлов, увеличением печени, гепатитом (вплоть до почечной недостаточности), увеличением количества лейкоцитов в крови (лейкоцитоз с эозинофилией или без нее);
• покраснение кожи (эритема), различные виды сыпи (например, зудящая, с белыми пятнами, с пузырями, с пузырями, содержащими гной, с отслоением кожи, кореподобная сыпь), генерализованная эритема, некроз, а также буллезное отслоение эпидермиса и слизистой оболочки, результатом которых является шелушение кожи и возможный сепсис (синдрома Стивенса-Джонсона/токсикодермальный некролиз);
• повышенная возбудимость;
• жажда;
• звон в ушах
• размытость зрения, изменение зрительного восприятия;
• выпадение волос;
• изъязвление слизистой ротовой полости;
• воспаление поджелудочной железы: частыми симптомами являются боль в животе, тошнота и рвота;
• повышенное потоотделение
• снижение веса, повышение аппетита, неконтролируемая потеря аппетита (анорексия);
• мышечная и/или суставная скованность;
• аномально низкое количество клеток крови (эритроцитов, лейкоцитов или тромбоцитов);
• позывы на немедленное мочеиспускание;
• изменение или снижение объема мочи в связи с воспалением почек (тубулоинтерстициальный нефрит);
• воспаление печени (гепатит);
• пожелтение кожных покровов (желтуха);
• поражение печени;
• повышение уровня креатинфосфокиназы в крови (индикатор повреждения мышц).
Сообщения о побочных действиях
При появлении каких-либо побочных действий обратитесь к своему врачу или работнику аптеки. Это касается также любых побочных действий, которые не описаны в данном листке- вкладыше. Сообщая о побочных действиях, Вы можете помочь собрать больше информации о безопасности данного лекарственного препарата.
• Хранить в недоступном для детей месте.
• Не использовать препарат после истечения срока годности, указанного на картонной упаковке и блистере после указания «Годен до» («ЕХР»). Срок годности относится к последнему дню указанного месяца.
• Для хранения данного лекарственного средства особых условий не требуется.
Не выбрасывайте никакие лекарственные препараты в канализацию или с бытовым мусором. По вопросам утилизации препаратов, которые Вы больше не используете, обращайтесь к работнику аптеки. Эти меры помогут защитить окружающую среду.
Действующим веществом препарата является фебуксостат.
В одной таблетке содержится 80 мг или 120 мг фебуксостата.
Прочие компоненты:
Ядро таблетки: лактозы моногидрат, целлюлоза микрокристаллическая, магния стеарат, гидроксипропилцеллюлоза, кроскармеллозы натриевая соль, кремния диоксид коллоидный гидратированный.
Пленочная оболочка: Opadry II желтый, 85F42129, в котором содержатся: спирт поливиниловый, титана диоксид (Е171), макрогол 3350, тальк, железа оксид желтый (Е172).
Описание:
Таблетки с дозировкой 80 мг: таблетки капсуловидной формы, покрытые пленочной оболочкой, от бледно-желтого до желтого цвета, с тиснением «80» на одной стороне.
Таблетки с дозировкой 120 мг: таблетки капсуловидной формы, покрытые пленочной оболочкой, от бледно-желтого до желтого цвета, с тиснением «120» на одной стороне.
В одной оригинальной упаковке содержится:
28 таблеток, покрытых пленочной оболочкой (2 прозрачных блистера Аклар/ПВХ/алюминий на
14 таблеток, покрытых пленочной оболочкой) вместе с листком-вкладышем;
56 таблеток, покрытых пленочной оболочкой (4 прозрачных блистера Аклар/ПВХ/алюминий на
14 таблеток, покрытых пленочной оболочкой) вместе с листком-вкладышем;
84 таблетки, покрытые пленочной оболочкой (6 прозрачных блистеров Аклар/ПВХ/алюминий на 14 таблеток, покрытых пленочной оболочкой) вместе с листком-вкладышем.
В продаже могут иметься упаковки не всех размеров.
По рецепту.
Информация о производителе/заявителе
Заявитель:
Менарини Интернэшнл Оперейшнз Люксембург С.А
1, Авеню де ла Гар, 1611 Люксембург
Люксембург
Производитель:
Патеон Франция
Бульвар де Шампаре, 40
38 300 Бургуин-Жалльё
Франция
или
Менарини — Фон Хейден ГмбХ
Лейпцигер Штрассе 7-13
01097 Дрезден
Германия
Уполномоченный представитель:
БЕРЛИН-ХЕМИ АГ
Глиникер Вег 125
12489 Берлин
Германия
Эфлейра — инструкция по применению
Синонимы, аналоги
Статьи
Внимательно прочтите эту инструкцию перед тем, как начать прием/использование лекарственного средства.
Сохраните инструкцию, она может потребоваться вновь.
Если у Вас возникли вопросы, обратитесь к врачу.
Это лекарственное средство назначено лично Вам, и его не следует передавать другим лицам, поскольку оно может причинить им вред даже при наличии тех же симптомов, что и у Вас.
Регистрационный номер:
ЛП-005439
Торговое наименование препарата:
Эфлейра®
Международное непатентованное наименование:
нетакимаб
Лекарственная форма:
раствор для подкожного введения
Состав:
1 мл раствора содержит:
Действующее вещество: нетакимаб – 60 мг;
Вспомогательные вещества: натрия ацетата тригидрат – 1,74 мг, трегалозы дигидрат – 80 мг, полоксамер 188 – 0,5 мг, уксусная кислота ледяная – до pH 5,0, вода для инъекций – до 1,0 мл.
Описание:
Прозрачный или слегка опалесцирующий от бесцветного до светло-желтого или светло-желтого с коричневатым оттенком цвета раствор.
Фармакотерапевтическая группа:
Интерлейкина ингибитор
Код АТХ:
L04AC
Фармакологические свойства
Фармакодинамика
Нетакимаб является рекомбинантным гуманизированным моноклональным антителом, в терапевтических концентрациях специфически связывающим интерлейкин-17А (ИЛ-17А), находящийся непосредственно в тканях или в крови и других биологических жидкостях. ИЛ-17А – провоспалительный цитокин, гиперпродукция которого преимущественно обусловлена активацией Th17-лимфоцитов. В рамках врожденного иммунитета ИЛ-17А выполняет защитную роль. При хронических иммуновоспалительных заболеваниях патологическая активация Th17-лимфоцитов и гиперпродукция ИЛ-17 стимулирует Т-клеточный ответ и усиленную продукцию других медиаторов воспаления: ИЛ-1, ИЛ-6, фактора некроза опухоли альфа (ФНО-α), факторов роста (Г-КСФ, ГМ-КСФ) и различных хемокинов.
Нетакимаб обладает высокой термодинамической константой специфического связывания с ИЛ-17А человека. По данным доклинических исследований специфическое связывание нетакимаба в нормальных тканях человека ограничено тканями легкого, тимуса, лимфатического узла, миндалин, что согласуется с данными об экспрессии ИЛ-17 клетками этих тканей.
Применение нетакимаба не сопровождается статистически значимым изменением уровня Т-лимфоцитов и не влияет на уровень и соотношение иммуноглобулинов классов А, G и М.
Специфическая противовоспалительная активность нетакимаба продемонстрирована в тестах in vitro и in vivo. Нетакимаб дозозависимо ингибирует ИЛ-17 и ФНОα-зависимую продукцию интерлейкина-6 на культуре клеток при IC50 40 pM. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (один раз в неделю в течение 4-х недель) подкожное введение нетакимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (суставной хрящ остается интактным, синовиальные оболочки — без признаков поражения и воспалительной реакции, пролиферации синовиоцитов не отмечено).
У больных псориазом использование нетакимаба сопровождается угасанием явлений воспаления и гиперкератоза в коже, достоверным снижением уровня С-реактивного белка и СОЭ. У пациентов с активным анкилозирующим спондилитом и псориатическим артритом на фоне применения нетакимаба отмечается уменьшение симптомов воспаления в позвоночнике, энтезисах и суставах, а также быстрое снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание/распределение
Изменение концентрации нетакимаба после его подкожного введения является дозозависимым (значения Сmax, Cmax-mult, AUC0-t находятся в прямой зависимости от дозы). Препарат характеризуется медленной фазой абсорбции с постепенным линейным нарастанием концентрации в сыворотке крови.
При однократном подкожном введении нетакимаба в дозе 120 мг пациентам с бляшечным псориазом препарат начинал обнаруживаться в сыворотке крови в течение 0,5 — 4 часов после введения; максимальная концентрация нетакимаба (Сmax) составляла 15,1 [7,7-19,3] мкг/мл, время ее достижения – 144 [72-168] ч, AUC0-168 – 1667,8 [932,2-2270,8] (мкг/мл)*ч.
При повторных введениях отмечено накопление препарата в сыворотке крови с ростом концентрации в 1,8-3,6 раза. Максимальная концентрация при многократном введении (Cmax-mult) составляла 33,0 [23,1-44,0] мкг/мл и достигалась (Tmax-mult) через 1680 [672-2016] часов.
Выведение
Характеристики выведения нетакимаба являются типичными для препаратов на основе моноклональных антител: показатели Kel, T½, MRT, Cl не зависят от дозы вводимого препарата, период полувыведения после однократного введения составляет около 16 суток.
Средний клиренс нетакимаба при однократном введении в дозе 120 мг пациентам с бляшечным псориазом составил 1,8 л/сутки.
Фармакокинетические параметры нетакимаба у пациентов с анкилозирующим спондилитом схожи с таковыми у пациентов с бляшечным псориазом.
Пациенты с почечной и печеночной недостаточностью: фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания к применению
- Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия.
- Лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
- Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию.
Противопоказания
- Гиперчувствительность к нетакимабу, а также к любому из вспомогательных веществ препарата.
- Клинически значимые инфекционные заболевания в острой фазе, включая туберкулез.
- Детский и подростковый возраст до 18 лет.
- Беременность, грудное вскармливание.
С осторожностью
Следует соблюдать осторожность при назначении нетакимаба пациентам с хроническими и рецидивирующими инфекциями или с анамнестическими указаниями на них, в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний, а также после недавно проведенной вакцинации живыми вакцинами.
В связи с ограниченными данными клинических исследований о применении нетакимаба у пациентов в возрасте старше 65 лет, следует соблюдать осторожность при назначении препарата пациентам указанной возрастной группы.
В связи с отсутствием сведений о применении нетакимаба у больных воспалительными заболеваниями кишечника, следует избегать его назначения пациентам с болезнью Крона или язвенным колитом.
Применение при беременности и в период грудного вскармливания
Применение при беременности
При применении нетакимаба у животных не выявлено отрицательного влияния на репродуктивную функцию, эмбриотоксичности или тератогенных эффектов.
Исследований влияния на плод у беременных женщин не проводилось. Препарат противопоказан к применению во время беременности.
Применение при грудном вскармливании
Нет данных о проникновении нетакимаба в грудное молоко. Учитывая, что иммуноглобулины класса G, к которым относится нетакимаб, при циркуляции в крови матери могут выделяться с грудным молоком, применение в период грудного вскармливания противопоказано. Во избежание негативного воздействия на ребенка следует прекратить либо грудное вскармливание, либо терапию, учитывая соотношение риска и пользы для матери и ребенка.
Влияние на фертильность
В исследованиях у животных не обнаружено негативного воздействия нетакимаба на фертильность. Данные о влиянии препарата на фертильность у людей отсутствуют.
Способ применения и дозы
Применение препарата Эфлейра® должно осуществляться под наблюдением врачей, имеющих опыт лечения заболеваний, при которых показан препарат Эфлейра®. После соответствующего обучения возможно самостоятельное введение препарата пациентом при условии динамического наблюдения со стороны лечащего врача. Препарат Эфлейра® может применяться как в стационарных, так и в амбулаторных условиях.
Препарат Эфлейра® вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл препарата с концентрацией 60 мг/мл.
Лечение бляшечного псориаза среднетяжелой и тяжелой степени у взрослых пациентов, когда показана системная терапия или фототерапия: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая вводится 1 раз в неделю на неделях 0, 1 и 2, затем 1 раз каждые 4 недели.
Лечение активного анкилозирующего спондилита при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом при недостаточном ответе на стандартную терапию: рекомендуемая доза 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) препарата каждая. Препарат вводится 1 раз в неделю на неделях 0, 1 и 2, затем каждые 2 недели до недели 10 включительно. Далее с недели 14 препарат вводится в дозе 120 мг в виде двух подкожных инъекций по 1 мл (60 мг) каждая 1 раз в 4 недели.
| Показание | Разовая доза | Индукция | Поддерживающая терапия |
| Бляшечный псориаз | 120 мг | 0, 1, 2 недели |
1 раз в 4 недели, начиная с недели 6 |
| Анкилозирующий спондилит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 |
| Псориатический артрит | 120 мг | 0, 1, 2 недели |
1 раз в 2 недели, начиная с недели 4 по неделю 10 включительно, далее 1 раз в 4 недели с недели 14 |
При пропуске очередного введения по любой причине инъекция препарата Эфлейра® должна быть произведена как можно быстрее. Дата следующего введения рассчитывается исходя из продолжительности задержки с введением препарата: если со времени пропуска введения прошло не более 3 дней, то следующую инъекцию препарата необходимо выполнить по текущему графику, если с момента пропуска введения прошло более 3 дней, то новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Эфлейра®.
Указания по применению
Подготовка к проведению подкожной инъекции
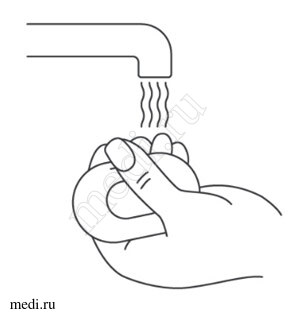

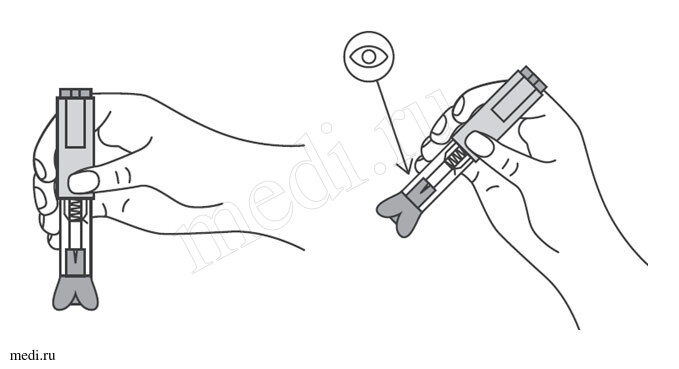
Препарат Эфлейра ® в автоинжекторе
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца/автоинжектора;
- истечения срока годности (годен до…), указанного на картонной пачке, а также на этикетке шприца/автоинжектора.
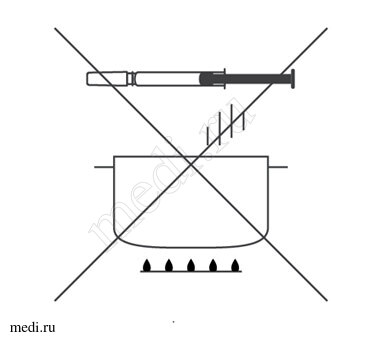
На данном этапе не следует снимать колпачок шприца/автоинжектора
1. Техника выполнения подкожной инъекции препарата Эфлейра® в преднаполненном шприце
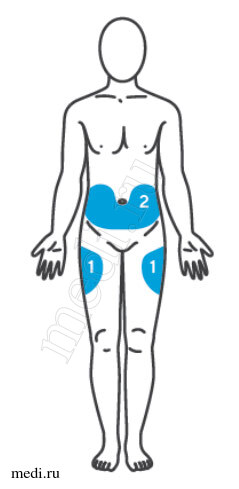
Выбор и подготовка места для инъекции


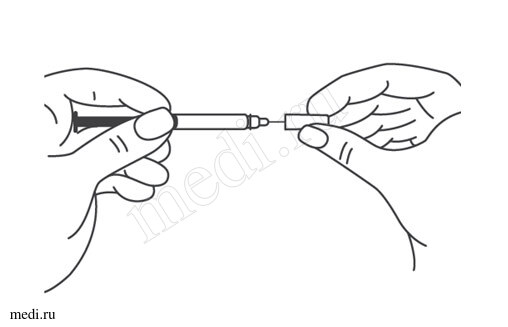

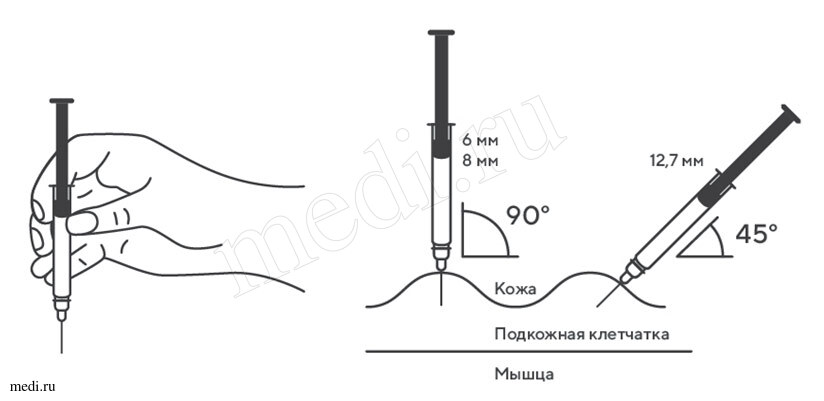
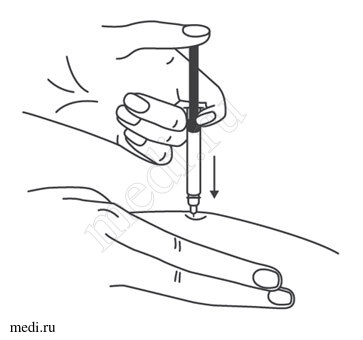
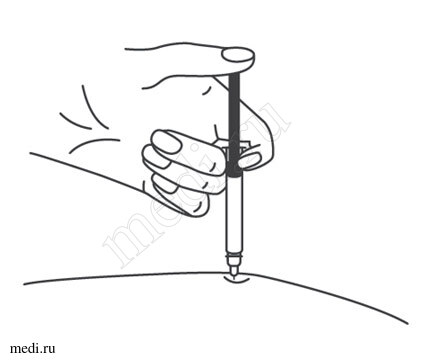
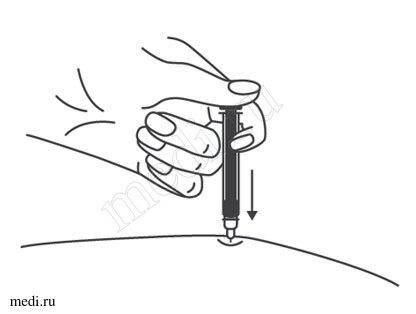
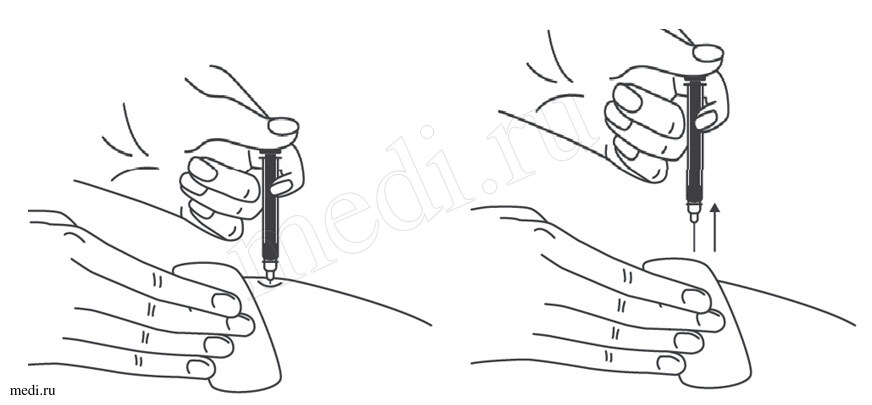
После инъекции шприц повторно не использовать
2. Техника выполнения подкожной инъекции препарата Эфлейра® в автоинжекторе
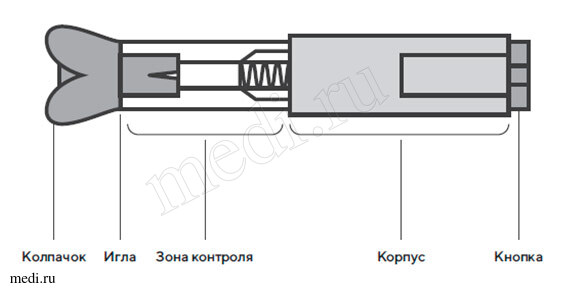
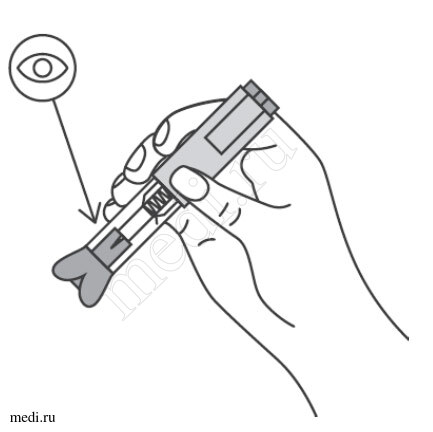



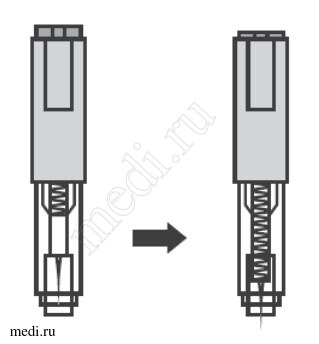
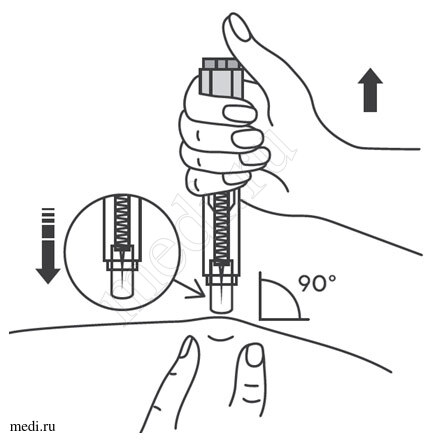
После инъекции автоинжектор повторно не использоватьУтилизация расходного материала

Побочное действие
В рамках проведенных клинических исследований у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом препарат Эфлейра® показал благоприятный профиль безопасности. Явлений дозолимитирующей токсичности не выявлено.
Большинство зарегистрированных нежелательных явлений (НЯ), связанных с применением препарата Эфлейра®, имели легкую или среднюю степень тяжести и не требовали прекращения терапии. Летальных исходов, связанных с терапией препаратом Эфлейра®, в ходе клинических исследований выявлено не было.
Наиболее частой нежелательной реакцией в проведенных клинических исследованиях была нейтропения, большинство случаев которой были легкой или средней степени тяжести, носили транзиторный характер и не требовали дополнительной терапии.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших нетакимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную связь с приемом препарата. Частота указана с учетом следующих критериев: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000), очень редко (<10000).
Инфекции и инвазии: часто – инфекции верхних дыхательных путей; нечасто – инфекция дыхательных путей, пневмония, назофарингит, фарингит, синусит, инфекция мочевыводящих путей, кандидоз пищевода, конъюнктивит вирусный, простой герпес, стафилококковое импетиго, фурункул, туберкулезная инфекция.
Нарушения со стороны печени и желчевыводящих путей: нечасто – гипербилирубинемия.
Желудочно-кишечные нарушения: нечасто – боль в животе, диарея.
Нарушения со стороны кожи и подкожной клетчатки: нечасто – экзема, дерматит, сыпь, зуд, крапивница.
Нарушения со стороны крови и лимфатической системы: часто – нейтропения, лейкопения, лимфоцитоз; нечасто – тромбоцитопения, лимфопения.
Нарушения со стороны иммунной системы: нечасто – гиперчувствительность.
Нарушения со стороны органа зрения: нечасто – эписклерит.
Нарушения со стороны нервной системы: нечасто – головная боль, головокружение, парестезия, поражение лицевого нерва.
Нарушения со стороны сердца: нечасто — синусовая брадикардия, блокада левой ножки пучка Гиса.
Нарушения со стороны сосудов: нечасто — гипертензия (в том числе изолированная систолическая/диастолическая гипертензия), гипертонический криз.
Общие нарушения и реакции в месте введения: нечасто — гриппоподобное заболевание*, местная реакция**.
Нарушения метаболизма и питания: нечасто – гипергликемия.
Нарушения со стороны почек и мочевыводящих путей: нечасто – протеинурия.
Лабораторные и инструментальные данные: часто – повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), положительный результат исследования на комплекс Mycobacterium tuberculosis; нечасто – повышение гамма-глутамилтрансферазы (ГГТ), повышение уровня холестерина в крови, увеличение веса.
Травмы, интоксикации и осложнения процедур: нечасто – головокружение во время процедуры (во время инъекции).
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): нечасто – инфицированный невус.
Нарушения со стороны репродуктивной системы и молочных желез: нечасто – фиброзно-кистозная болезнь молочных желез.
* «Гриппоподобное заболевание» характеризуется появлением ряда симптомов, сходных с выявляемыми при гриппе или простуде, включая, например, но не ограничиваясь: повышение температуры, озноб, ломоту в теле, недомогание, слабость, снижение аппетита, сухой кашель, которые имеют временную связь с проведением инъекции препарата.
** Местные реакции могут включать в себя любые неблагоприятные проявления, возникающие в месте инъекции.
Передозировка
Клинические данные о передозировке отсутствуют. Максимальная переносимая доза для человека не установлена. В клинических исследованиях явлений дозолимитирующей токсичности не зарегистрировано: при подкожном введении нетакимаба в максимальной дозе 3 мг/кг (195 – 355 мг для взрослого человека с весом 65 – 85 кг) патологических отклонений не было выявлено.
Специфический антидот отсутствует. Лечение симптоматическое.
Взаимодействие с другими лекарственными средствами
Сведений о наличии неблагоприятных лекарственных взаимодействий нетакимаба с другими лекарственными препаратами до настоящего времени не получено. Предполагается, что нетакимаб может усиливать иммуносупрессивное действие глюкокортикоидов, метотрексата, сульфасалазина, лефлуномида и других базисных противовоспалительных препаратов.
Смешивание препарата с другими лекарственными средствами, введение в виде инфузии строго запрещено.
Особые указания
Наличие таких потенциально тяжелых инфекций как ВИЧ, активный гепатит В и/или С, сифилис, туберкулез, относится к противопоказаниям для назначения нетакимаба. Применение нетакимаба у данной группы больных не изучено. Учитывая иммуносупрессивное действие нетакимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования. Необходимо проводить скрининг и оценивать соотношение риска и пользы терапии нетакимабом у этих пациентов.
Пациентам с активным туберкулезом терапия препаратом Эфлейра® противопоказана. Перед назначением препарата Эфлейра® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Эфлейра®.
При реактивации гепатита В терапия нетакимабом должна быть прекращена и назначена соответствующая противовирусная терапия.
Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии.
При использовании нетакимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований нетакимаба анафилактических реакций не зарегистрировано, нечасто отмечались реакции гиперчувствительности и крапивница. Однако при использовании других ингибиторов ИЛ17 крапивница и анафилактические реакции отмечались в редких и очень редких случаях. При возникновении анафилактических или других серьёзных аллергических реакций применение препарата Эфлейра® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения нетакимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходим более тщательный мониторинг за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований на данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Эфлейра® при лечении псориаза, псориатического артрита и анкилозирующего спондилита выработка связывающих антител к нетакимабу была зарегистрирована менее чем в 0,5 % случаев. Нейтрализующих антител выявлено не было. Полученные данные демонстрируют низкую иммуногенность нетакимаба у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Пациенты моложе 18 лет, дети
Исследование эффективности и безопасности препарата у детей и лиц моложе 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми вакцинами в ходе лечения препаратом Эфлейра®, так как клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми вакцинами до начала терапии препаратом Эфлейра®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям. Иммунизация инактивированными вакцинами во время терапии нетакимабом должна выполняться с осторожностью.
Влияние на способность управлять транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Эфлейра® на способность управлять транспортными средствами и работать с машинами и (или) механизмами.
Форма выпуска
Раствор для подкожного введения 60 мг/мл.
Преднаполненные шприцы
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса. Шприц с одной стороны имеет впаянную иглу для инъекций из нержавеющей стали, которая защищена жестким колпачком. С другой стороны шприц укупорен поршнем, шток которого изготовлен из полипропилена; на конце поршня имеется уплотнитель из бутилкучука, ламинированный фторполимером.
На каждый шприц наклеивают самоклеящуюся этикетку.
По 1 шприцу помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Автоинжектор
По 1,0 мл препарата в трехкомпонентные шприцы. Цилиндр каждого шприца изготовлен из бесцветного нейтрального стекла I гидролитического класса.
Шприц с препаратом встроен в пластиковый автоинжектор, состоящий из защитного колпачка, корпуса с прозрачной зоной контроля, верхнего корпуса и кнопки активации. Внутреннее устройство автоинжектора имеет цилиндр, защищающий иглу, и поршень, который через систему механического пуска соединен с кнопкой активации.
На каждый автоинжектор наклеивают самоклеящуюся этикетку.
По 1 автоинжектору помещают в контурную ячейковую упаковку из пленки ПВХ или ПЭТ.
По 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона. Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 шт.
Условия хранения
При температуре от 2 до 8°С в защищенном от света месте. Не замораживать!
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Производитель
ЗАО «БИОКАД», Россия, 143422, Московская обл., Красногорский р-н, с. Петрово-Дальнее.
Владелец регистрационного удостоверения
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Организация, принимающая претензии потребителей
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый р-н, пос. Стрельна, ул. Связи, д. 34, лит. А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Выбор описания
| Лек. форма | Дозировка |
|---|---|
|
таблетки, покрытые пленочной оболочкой |
50 мг 100 мг |
таблетки, покрытые пленочной оболочкой
Арпефлю (таблетки, покрытые пленочной оболочкой, 100 мг), инструкция по медицинскому применению РУ № ЛСР-005752/09
Дата последнего изменения: 06.05.2022
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
- A08.0 Ротавирусный энтерит
- B00.9 Герпетическая инфекция неуточненная
- B34.8 Другие вирусные инфекции неуточненной локализации
- D84.8 Другие уточненные иммунодефицитные нарушения
- D84.9 Иммунодефицит неуточненный
- J06 Острые инфекции верхних дыхательных путей множественной и неуточненной локализации
- J10 Грипп, вызванный идентифицированным вирусом гриппа
- J11 Грипп, вирус не идентифицирован
- J18.9 Пневмония неуточненная
- J22 Острая респираторная инфекция нижних дыхательных путей неуточненная
- J42 Хронический бронхит неуточненный
- J80 Синдром респираторного расстройства [дистресса] у взрослого
- T81.4 Инфекция, связанная с процедурой, не классифицированная в других рубриках
- Z29.1 Профилактическая иммунотерапия
Фармакологическая группа
Лекарственная форма
Таблетки,
покрытые пленочной оболочкой.
Состав
Одна
таблетка, покрытая пленочной оболочкой, содержит:
Действующее вещество:
Умифеновира
гидрохлорида моногидрат в пересчете на умифеновира гидрохлорид — 50 мг или
100 мг.
Вспомогательные вещества:
Повидон
(К 17) — 0,66 мг или 1,32 мг; целлюлоза микрокристаллическая —
29,5 мг или 59,0 мг; крахмал прежелатинизированный (крахмал — 1500) —
15,0 мг или 30,0 мг; магния стеарат — 1,5 мг или 3,0 мг;
кремния диоксид коллоидный безводный — 1,5 мг или 3,0 мг; лактоза
моногидрат — до получения таблетки без оболочки массой 150,0 мг
или 300,0 мг; оболочка опадрай II белый — 6,0 мг или
12,0 мг.
Состав оболочки:
спирт поливиниловый частично гидролизованный (40,000%), титана диоксид (25,000%),
макрогол 4000/ ПЭГ (20,200%), тальк (14,800%).
Описание лекарственной формы
Круглые
двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого
цвета.
Фармакокинетика
Быстро
абсорбируется и распределяется по органам и тканям. Максимальная концентрация
в плазме крови при приеме в дозе 50 мг достигается через 1,2 ч,
в дозе 100 мг — через 1,5 ч.
Метаболизируется в печени. Период полувыведения равен 17–21 ч. Около
40% выводится в неизмененном виде, в основном с желчью (38,9%) и в
незначительном количестве почками (0,12%). В течение первых суток выводится 90%
от введенной дозы.
Фармакодинамика
Противовирусное
средство. Специфически подавляет in vitro
вирусы гриппа A и B (Influenza
virus А, B), включая высокопатогенные подтипы A(H1N1)pdm09
и A(H5N1), а также другие вирусы —
возбудители острых респираторных вирусных инфекций (ОРВИ) (коронавирус (Coronavirus), ассоциированный с тяжелым
острым респираторным синдромом (ТОРС), риновирус (Rhinovirus), аденовирус (Adenovirus),
респираторно-синцитиальный вирус (Pneumovirus)
и вирус парагриппа (Paramyxovirus)).
По механизму противовирусного действия относится к ингибиторам слияния (фузии),
взаимодействует с гемагглютинином вируса и препятствует слиянию липидной
оболочки вируса и клеточных мембран. Оказывает умеренное иммуномодулирующее
действие, повышает устойчивость организма к вирусным инфекциям. Обладает
интерферон-индуцирующей активностью —
в исследовании на мышах индукция интерферонов отмечалась уже через 16 часов,
а высокие титры интерферонов сохранялись в крови до 48 часов после
введения. Стимулирует клеточные и гуморальные реакции иммунитета: повышает
число лимфоцитов в крови, в особенности T‑клеток (CD3),
повышает число T‑хелперов
(CD4),
не влияя на уровень T‑супрессоров
(CD8),
нормализует иммунорегуляторный индекс, стимулирует фагоцитарную функцию
макрофагов и повышает число естественных киллеров (NK‑клеток).
Терапевтическая
эффективность при вирусных инфекциях проявляется в уменьшении
продолжительности и тяжести течения болезни и ее основных симптомов, а также в снижении
частоты развития осложнений, связанных с вирусной инфекцией, и обострений хронических
бактериальных заболеваний.
При
лечении гриппа или ОРВИ у взрослых пациентов в клиническом исследовании
показано, что эффект умифеновира у взрослых пациентов наиболее выражен в остром
периоде заболевания и проявляется сокращением сроков разрешения симптомов
болезни, снижением тяжести проявлений заболевания и сокращением сроков
элиминации вируса.
Терапия
умифеновиром приводит к более высокой частоте купирования симптомов заболевания
на третьи сутки терапии по сравнению с плацебо: через 60 ч после начала
терапии разрешение всех симптомов лабораторно подтвержденного гриппа
более чем в 5 раз превышает аналогичный показатель в группе
плацебо.
Установлено
значимое влияние умифеновира на скорость элиминации вируса гриппа, что,
в частности, проявлялось уменьшением частоты выявления РНК вируса на 4‑е сутки.
Относится
к малотоксичным лекарственными средствами (ЛС) (LD50 >4 г/кг).
Не оказывает какого‑либо отрицательного воздействия на организм
человека при пероральном применении в рекомендуемых дозах.
Показания
Профилактика
и лечение у взрослых и детей: грипп A
и B,
другие ОРВИ.
Комплексная
терапия острых кишечных инфекций ротавирусной этиологии у детей старше
3 лет.
Комплексная
терапия хронического бронхита, пневмонии и рецидивирующей герпетической
инфекции.
Профилактика
послеоперационных инфекционных осложнений.
Противопоказания
Повышенная
чувствительность к умифеновиру или любому компоненту препарата, детский возраст
до 3 лет.
Первый триместр беременности. Грудное вскармливание.
Непереносимость
лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция.
С осторожностью
Второй
и третий триместры беременности.
Применение при беременности и кормлении грудью
В
исследованиях на животных не было выявлено вредных воздействий на течение
беременности, развитие эмбриона и плода, родовую деятельность и постнатальное
развитие.
Применение
умифеновира в первом триместре беременности противопоказано.
Во
втором и третьем триместре беременности умифеновир может применяться только для
лечения и профилактики гриппа и в том случае, если предполагаемая польза для
матери превышает потенциальный риск для плода. Соотношение польза/риск
определяется лечащим врачом. Неизвестно, проникает ли умифеновир в грудное
молоко у женщин в период лактации. При необходимости применения
препарата следует прекратить грудное вскармливание.
Способ применения и дозы
Внутрь,
до приема пищи.
Разовая
доза:
–
детям от 3 до 6
лет — 50 мг,
–
от 6 до 12 лет —
100 мг,
–
старше 12 лет и
взрослым — 200 мг (2 таблетки по 100 мг или 4 таблетки по 50 мг).
Неспецифическая профилактика в период эпидемии гриппа и
других ОРВИ у детей с 3 лет и взрослых:
В
разовой дозе 2 раза в неделю в течение 3 недель.
Неспецифическая профилактика при непосредственном контакте с
больными гриппом и другими ОРВИ:
В
разовой дозе 1 раз в день в течение 10–14 дней.
Лечение гриппа и других ОРВИ:
В
разовой дозе 4 раза в день (каждые 6 часов) в течение 5 дней.
Комплексная терапия острых кишечных инфекций ротавирусной
этиологии у детей с 3‑х лет:
В
разовой дозе 4 раза в сутки (каждые 6 часов) в течение 5 суток.
Комплексная терапия хронического бронхита, пневмонии, герпетической
инфекции у детей с 3 лет и взрослых:
В
разовой дозе 4 раза в день (каждые 6 часов) в течение 5 дней, затем разовую
дозу 1 раз в неделю в течение 4 недель.
Профилактика послеоперационных осложнений у детей с 3 лет и
взрослых:
В
разовой дозе за 2 дня до операции, затем на 2 и 5 день после операции.
Прием
препарата начинают с момента появления первых симптомов заболевания
гриппом и другими ОРВИ, желательно не позднее 3 суток от начала болезни.
Если
после применения препарата Арпефлю в течение трех суток при лечении гриппа
и других ОРВИ сохраняется выраженность симптомов заболевания, в том числе
высокая температура (38 °С и более), то необходимо обратиться к врачу
для оценки обоснованности приема препарата.
Применяйте
препарат только согласно тем показаниям, тому способу применения и
в тех дозах, которые указаны в инструкции.
При
лечении гриппа и ОРВИ возможна сопутствующая симптоматическая терапия, включая
прием жаропонижающих препаратов, муколитических и местных сосудосуживающих
средств.
Побочные действия
Препарат
Арпефлю относится к малотоксичным препаратам и обычно хорошо переносится.
Побочные
эффекты возникают редко, обычно слабо или умеренно выражены и носят преходящий
характер.
Частота
возникновения нежелательных лекарственных реакций определена
в соответствии с классификацией ВОЗ: очень часто (с частотой более
1/10), часто (с частотой не менее 1/100, но менее 1/10), нечасто
(с частотой не менее 1/1000, но менее 1/100), редко (с частотой
не менее 1/10000, но менее 1/1000), очень редко (с частотой менее
1/10000), частота неизвестна (не может быть установлена по имеющимся
данным).
Нарушения со стороны иммунной системы:
Редко — аллергические
реакции.
Если
любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили
любые другие побочные эффекты, не указанные в инструкции, сообщите об этом
врачу.
Взаимодействие
При
назначении с другими лекарственными средствами отрицательных эффектов отмечено
не было.
Специальные
клинические исследования, посвященные изучению взаимодействий препарата Арпефлю
с другими лекарственными средствами, не проводились.
Сведения
о наличии нежелательного взаимодействия с жаропонижающими,
муколитическими и местными сосудосуживающими лекарственными средствами в условиях
клинического исследования не были выявлены.
Передозировка
Особые указания
Необходимо
соблюдать рекомендованную в инструкции схему и длительность приема препарата.
В случае пропуска приема одной дозы препарата пропущенную дозу следует
принять как можно раньше и продолжить курс приема препарата по начатой схеме.
Если после применения препарата Арпефлю в течение трех суток при лечении гриппа
и других ОРВИ сохраняется выраженность симптомов заболевания, в том числе
высокая температура (38 °С и более), то необходимо обратиться к врачу
для оценки обоснованности приема препарата.
Влияние на способность управлять
транспортными средствами и механизмами
Не
проявляет центральной нейротропной активности и может применяться в медицинской
практике у лиц различных профессий, в т. ч.
требующих повышенного внимания и координации движений (водители транспорта,
операторы и т. д.).
Форма выпуска
Таблетки,
покрытые пленочной оболочкой, 50 мг, 100 мг.
По
10 или 20 таблеток в контурной ячейковой упаковке.
1,
2, 3 или 4 контурные ячейковые упаковки по 10 таблеток вместе с инструкцией
по применению помещают в пачку картонную.
1
контурную ячейковую упаковку по 20 таблеток с дозировкой 50 мг вместе
с инструкцией по применению помещают в пачку картонную.
Условия отпуска из аптек
Условия хранения
При
температуре не выше 25 °С.
В
недоступном для детей месте.
Срок годности
3
года.
Не
использовать по истечении срока годности.
Заказ в аптеках
Выбор региона:
| Название препарата | Цена за упак., руб. | Аптеки |
|---|---|---|
|
Арпефлю, таблетки, покрытые пленочной оболочкой, |
||
|
320.00 |
|
|
|
320.00 |
|
|
|
403.00 |
|
|
|
Арпефлю, таблетки, покрытые пленочной оболочкой, |
||
|
190.00 |
|
|
|
226.00 |
|
|
|
241.00 |
|
|
|
Арпефлю, таблетки, покрытые пленочной оболочкой, |
||
|
234.00 |
|
|
|
257.00 |
|
|
|
261.00 |
|
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Отзывы