Перед длительной поездкой, связанной со сменой,часовых поясов, пациент должен проконсультироваться со своим лечащим врачом, поскольку смена часового пояса означает, что пациент должен принимать пищу и вводить инсулин в другое время.
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете 1 типа, может привести к развитию гипергликемии или диабетического кетоацидоза. Как правило, первые симптомы гипергликемии появляются постепенно, в течение нескольких часов или дней. Симптомами гипергликемии являются чувство жажды, увеличение количества выделяемой мочи, тошнота, рвота, сонливость, покраснение и сухость кожи, сухость во рту, потеря аппетита, а также появление запаха ацетона в выдыхаемом воздухе. Без соответствующего лечения гипергликемия у пациентов с сахарным диабетом 1 типа может приводить к диабетическому кетоацидозу — состоянию, которое является потенциально летальным.
Пропуск приема пищи или незапланированная интенсивная физическая нагрузка могут привести к гипогликемии. Гипогликемия также может развиться, если введена слишком высокая по отношению к потребности пациента доза инсулина.
После компенсации углеводного обмена, например, при интенсифицированной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чем больные должны быть проинформированы. Обычные симптомы-предвестники могут исчезать при длительном течении сахарного диабета.
Сопутствующие заболевания, особенно инфекционные и сопровождающиеся лихорадкой, обычно повышают потребность организма в инсулине. Коррекция дозы может также потребоваться при наличии у пациента сопутствующих заболеваний почек, печени, нарушении функции надпочечников, гипофиза или щитовидной железы.
При переводе пациента на другие типы инсулина, ранние симптомы-предвестники гипогликемии могут изменяться или становиться менее выраженными, по сравнению с таковыми при использовании предыдущего типа инсулина.
Перевод пациента на новый тип инсулина или препарат инсулина другого производителя необходимо осуществлять под строгим медицинским контролем. При изменении концентрации, типа, производителя и вида (человеческий инсулин, аналог человеческого инсулина) препаратов инсулина и/или способа производства может потребоваться изменение дозы.
Сообщалось о случаях развития хронической сердечной недостаточности при лечении пациентов тиазолидиндионами в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития хронической сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии тиазолидиндионами и препаратами инсулина. При назначении такой комбинированной терапии необходимо проводить медицинские обследования пациентов на предмет выявления у них признаков и симптомов хронической сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности лечение тиазолидиндионами необходимо прекратить.
Влияние на способность к управлению транспортными средствами и механизмами
Способность пациентов к концентрации внимания и скорость реакции могут нарушаться во время гипогликемии, что может представлять опасность в тех ситуациях, когда эти способности особенно необходимы (например, при управлении транспортными средствами или работе с машинами и механизмами).
Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии при управлении транспортными средствами. Это особенно важно для пациентов с отсутствием или снижением выраженности симптомов-предвестников в развивающейся гипогликемии или страдающих частыми эпизодами гипогликемии. В этих случаях следует рассмотреть целесообразность управления транспортными средствами и выполнения подобных работ.
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-007449
Торговое наименование лекарственного средства:
РинФаст® Микс 30
Международное непатентованное наименование:
инсулин аспарт двухфазный
Лекарственная форма:
суспензия для подкожного введения
Состав:
В 1 мл препарата содержится:
действующее вещество*: инсулин аспарт 100 ЕД (эквивалентно 3,5 мг);
Препарат содержит 30% растворимого инсулина аспарт и 70% кристаллов инсулина аспарт протамина.
вспомогательные вещества: глицерол 16,00 мг, фенол 1,50 мг, метакрезол 1,72 мг, цинк 19,6 мкг (в виде цинка хлорида), натрия хлорид 0,877 мг, натрия гидрофосфата дигидрат 1,25 мг, протамина сульфат 0,32 мг, хлористоводородной кислоты 10% раствор и/или натрия гидроксида 10% раствор (до pH 7,1 – 7,5), вода для инъекций до 1,0 мл.
Описание:
суспензия белого цвета, которая при стоянии расслаивается, образуя белый осадок и прозрачную бесцветную или почти бесцветную надосадочную жидкость. Осадок легко ресуспендируется при осторожном встряхивании.
Фармакотерапевтическая группа лекарственного препарата:
гипогликемическое средство, комбинация аналогов инсулина средней продолжительности или длительного и короткого действия.
Код ATX:
A10AD05.
Фармакологические свойства
Фармакодинамика
Препарат РинФаст® Микс 30 представляет собой двухфазную суспензию, состоящую из смеси аналогов инсулина: растворимого инсулина аспарт (30% аналога инсулина короткого действия) и кристаллов инсулина аспарт протамина (70% аналога инсулина средней продолжительности действия). Действующим веществом препарата РинФаст® Микс 30 является инсулин аспарт, произведенный методом биотехнологии рекомбинантной ДНК с использованием штамма Escherichia coli.
Инсулин аспарт является эквипотенциальным растворимому человеческому инсулину на основании показателей молярности.
Снижение концентрации глюкозы в крови происходит за счет повышения ее внутриклеточного транспорта после связывания инсулина аспарт с инсулиновыми рецепторами мышечных и жировых тканей и одновременного торможения продукции глюкозы печенью.
После подкожного введения инсулина аспарт двухфазного 30 эффект развивается в течение 10-20 минут. Максимальный эффект наблюдается в пределах от 1 до 4 часов после инъекции. Продолжительность действия препарата достигает 24 часов.
В трехмесячном сравнительном клиническом исследовании с участием пациентов с сахарным диабетом 1 и 2 типа, которые получали инсулин аспарт двухфазный 30 и двухфазный человеческий инсулин 30 2 раза в сутки перед завтраком и ужином было показано, что инсулин аспарт двухфазный 30 сильнее снижает постпрандиальную концентрацию глюкозы крови (после завтрака и ужина).
Мета-анализ данных, полученных в ходе девяти клинических исследований с участием пациентов с сахарным диабетом 1 и 2 типа, показал, что инсулин аспарт двухфазный 30 при введении перед завтраком и ужином обеспечивает лучший контроль постпрандиальной концентрации глюкозы крови (среднее увеличение прандиальных концентраций глюкозы после завтрака, обеда и ужина), по сравнению с человеческим двухфазным инсулином 30. Хотя концентрация глюкозы натощак у пациентов, применяющих инсулин аспарт двухфазный 30, была выше, в целом инсулин аспарт двухфазный 30 оказывает такое же воздействие на концентрацию гликозилированного гемоглобина (HbA1с), как и двухфазный человеческий инсулин 30.
В клиническом исследовании с участием 341 пациента с сахарным диабетом 2 типа пациенты были рандомизированы в следующие группы лечения: только инсулином аспарт двухфазным 30; инсулином аспарт двухфазным 30 в комбинации с метформином; метформином в комбинации с производным сульфонилмочевины. Концентрация HbA1с после 16 недель лечения не отличалась у пациентов, получавших инсулин аспарт двухфазный 30 в комбинации с метформином, и у пациентов, получавших метформин в комбинации с производным сульфонилмочевины. В данном исследовании у 57% пациентов базальная концентрация HbA1с была выше 9%; у этих пациентов терапия инсулином аспарт двухфазным 30 в комбинации с метформином привела к более значительному снижению концентрации HbA1с, чем у пациентов, получавших метформин в комбинации с производным сульфонилмочевины.
В другом исследовании пациенты с сахарным диабетом 2 типа, у которых отсутствовал удовлетворительный контроль гликемии и которые принимали пероральные гипогликемические препараты, были рандомизированы в нижеследующие группы: получавшие инсулин аспарт двухфазный 30 2 раза в сутки (117 пациентов) и получавшие инсулин гларгин 1 раз в сутки (116 пациентов). По прошествии 28 недель применения препаратов среднее уменьшение концентрации HbA1с в группе инсулина аспарт двухфазный 30 составило 2,8% (начальное среднее значение равнялось 9,7%). У 66% и 42% пациентов, применявших инсулин аспарт двухфазный 30 в конце исследования значения HbA1с были ниже 7% и 6,5% соответственно. Среднее значение глюкозы плазмы натощак снизилось примерно на 7 ммоль/л (с 14,0 ммоль/л в начале исследования до 7,1 ммоль/л).
Результаты мета-анализа данных, полученных при проведении клинических исследований с участием пациентов с сахарным диабетом 2 типа, продемонстрировали снижение общего числа эпизодов ночной гипогликемии и тяжелой гипогликемии при применении инсулина аспарт двухфазный 30 по сравнению с двухфазным человеческим инсулином 30. При этом общий риск возникновения дневной гипогликемии у пациентов, получавших инсулин аспарт двухфазный 30, был выше.
Дети и подростки
Было проведено 16-недельное клиническое исследование, в котором сравнивалась концентрация глюкозы в крови после еды на фоне введения инсулина аспарт двухфазного 30 (до еды), человеческого инсулина/двухфазного человеческого инсулина 30 (до еды) и изофан-инсулина (вводимого перед сном). В исследовании участвовали 167 пациентов в возрасте от 10 до 18 лет. Средние значения HbA1с в обеих группах оставались близкими к начальным значениям на протяжении всего исследования. Также при применении инсулина аспарт двухфазного 30 или двухфазного человеческого инсулина 30 не наблюдалось различий в частоте возникновения гипогликемии.
Также было проведено двойное слепое перекрестное исследование в популяции пациентов в возрасте от 6 до 12 лет (всего 54 пациента, по 12 недель на каждый вид лечения). Частота возникновения гипогликемии и повышение концентрации глюкозы после приема пищи в группе пациентов, применявших инсулин аспарт двухфазный 30, были достоверно ниже по сравнению со значениями в группе пациентов, применявших двухфазный человеческий инсулин 30. Значения HbA1с в конце исследования в группе применения двухфазного человеческого инсулина 30 были значительно ниже, чем в группе пациентов, применявших инсулин аспарт двухфазный 30.
Пациенты пожилого возраста
Фармакодинамика инсулина аспарт двухфазного 30 у пациентов пожилого и старческого возраста не исследовалась. Однако в рандомизированном двойном слепом перекрестном исследовании, проведенном на 19 пациентах с сахарным диабетом 2 типа в возрасте 65-83 лет (средний возраст – 70 лет), сравнивали фармакодинамику и фармакокинетику инсулина аспарт и растворимого человеческого инсулина. Относительные различия значений показателей фармакодинамики (максимальной скорости инфузии глюкозы – GIRmax и площади под кривой скорости ее инфузии в течение 120 минут после введения препаратов инсулина – AUCGIR, 0-120 min) между инсулином аспарт и человеческим инсулином у пациентов пожилого возраста были схожи с таковыми у здоровых добровольцев и у более молодых пациентов с сахарным диабетом.
Фармакокинетика
В инсулине аспарт замещение аминокислоты пролин в положении В28 на аспарагиновую кислоту уменьшает тенденцию молекул к образованию гексамеров в растворимой фракции инсулина аспарт двухфазного 30, которая наблюдается в растворимом человеческом инсулине. В связи с этим инсулин аспарт (30%) абсорбируется из подкожной жировой клетчатки быстрее, чем растворимый инсулин, содержащийся в двухфазном человеческом инсулине. Остальные 70% приходятся на долю кристаллической формы протамин-инсулина аспарт, скорость всасывания которого такая же, как у человеческого НПХ инсулина.
Максимальная концентрация инсулина в сыворотке крови после введения инсулина аспарт двухфазного 30 на 50% выше, чем у двухфазного человеческого инсулина 30, а время ее достижения вдвое короче по сравнению с двухфазным человеческим инсулином 30.
У здоровых добровольцев после подкожного введения инсулина аспарт двухфазного 30 из расчета 0,20 ЕД/кг массы тела максимальная концентрация инсулина аспарт в сыворотке крови достигалась через 60 мин и составляла 140±32 пмоль/л. Длительность периода полувыведения (t1/2) инсулина аспарт двухфазного 30, которая отражает скорость всасывания связанной с протамином фракции, составляла 8-9 часов. Концентрация инсулина в сыворотке крови возвращалась к исходной через 15-18 ч после подкожного введения препарата. У пациентов с сахарным диабетом 2 типа максимальная концентрация достигалась через 95 минут после введения и оставалась выше исходной в течение не менее 14 часов.
Пациенты пожилого и старческого возраста
Изучение фармакокинетики инсулина аспарт двухфазного 30 у пациентов пожилого и старческого возраста не проводилось. Однако относительные различия значений показателей фармакокинетики между инсулином аспарт и человеческим растворимым инсулином у пациентов пожилого возраста с сахарным диабетом 2 типа (в возрасте 65-83 лет, средний возраст – 70 лет) были схожи с таковыми у здоровых добровольцев и у более молодых пациентов с сахарным диабетом. У пациентов пожилого возраста наблюдалось уменьшение скорости абсорбции, что приводило к замедлению tmax (82 минуты (межквартильный размах: 60-120 минут)), тогда как средняя максимальная концентрация Сmax была схожа с таковой, наблюдаемой у более молодых пациентов с сахарным диабетом 2 типа, и немного меньше, чем у пациентов с сахарным диабетом 1 типа.
Пациенты с нарушением функции почек и печени
Изучение фармакокинетики инсулина аспарт двухфазного 30 у пациентов с нарушением функции почек и печени не проводилось. Тем не менее, при увеличении дозы препарата у пациентов с различной степенью нарушения функции почек и печени не отмечено изменения фармакокинетики растворимого инсулина аспарт.
Дети и подростки
Фармакокинетические свойства инсулина аспарт двухфазного 30 у детей и подростков не изучались. Однако фармакокинетические и фармакодинамические свойства растворимого инсулина аспарт изучались у детей (от 6 до 12 лет) и подростков (от 13 до 17 лет) с сахарным диабетом 1 типа. У пациентов обеих возрастных групп инсулин аспарт характеризовался быстрой абсорбцией и значениями tmax, схожими с таковыми у взрослых. Однако значения Сmax в двух возрастных группах были различными, что указывает на важность индивидуального подбора дозы инсулина аспарт.
Доклинические данные по безопасности
В ходе доклинических исследований не было выявлено какой-либо опасности для людей, исходя из данных общепринятых исследований фармакологической безопасности, токсичности при повторном применении, генотоксичности и репродуктивной токсичности. В тестах in vitro, включавших в себя связывание с инсулиновыми и ИФР-1 рецепторами и влияние на рост клеток, было показано, что свойства инсулина аспарт аналогичны свойствам человеческого инсулина. Результаты исследований также показали, что диссоциация инсулина аспарт с инсулиновыми рецепторами эквивалентна таковой для человеческого инсулина.
Показания к применению
Сахарный диабет.
Противопоказания
- Гиперчувствительность к инсулину аспарт или любому из вспомогательных веществ препарата.
Не рекомендуется применять у детей до 6 лет, т.к. клинические исследования инсулина аспарт двухфазного 30 у них не проводились.
Применение во время беременности и в период грудного вскармливания
Клинический опыт применения инсулина аспарт двухфазного 30 при беременности ограничен.
Беременность
Исследования по применению инсулина аспарт двухфазного 30 у беременных женщин не проводились. Тем не менее, данные двух рандомизированных контролируемых клинических исследований (соответственно 157 и 14 беременных, получавших инсулин аспарт в базис-болюсном режиме терапии) не выявили никакого неблагоприятного воздействия инсулина аспарт на течение беременности или здоровье плода/новорожденного по сравнению с растворимым человеческим инсулином. Кроме того, в клиническом рандомизированном исследовании с участием 27 женщин с гестационным диабетом, получавших инсулин аспарт и растворимый человеческий инсулин (инсулин аспарт получали 14 женщин, человеческий инсулин – 13) были продемонстрированы сходные профили безопасности для обоих типов инсулина.
В период возможного наступления беременности и в течение всего ее срока необходимо вести тщательное наблюдение за состоянием пациенток с сахарным диабетом и контролировать концентрацию глюкозы в крови.
Потребность в инсулине, как правило, снижается в I триместре и постепенно повышается во II и III триместрах беременности. Вскоре после родов потребность в инсулине быстро возвращается к уровню, который был до беременности.
Период грудного вскармливания
В период грудного вскармливания инсулин аспарт двухфазный 30 может применяться без ограничений. Введение инсулина кормящей матери не представляет угрозы для ребенка. Однако может возникнуть необходимость коррекции дозы препарата РинФаст® Микс 30.
Способ применения и дозы
Препарат РинФаст® Микс 30 предназначен для подкожного введения. Нельзя вводить препарат РинФаст® Микс 30 внутривенно, так как это может привести к тяжелой гипогликемии. Следует также избегать внутримышечного введения препарата РинФаст® Микс 30. Нельзя использовать препарат РинФаст® Микс 30 для подкожных инсулиновых инфузий (ППИИ) в инсулиновых насосах.
Доза препарата РинФаст® Микс 30 определяется лечащим врачом индивидуально в каждом конкретном случае в соответствии с потребностями пациента. Для достижения оптимального уровня гликемии рекомендуется проводить контроль концентрации глюкозы в крови и коррекцию дозы препарата.
Пациентам с сахарным диабетом 2 типа препарат РинФаст® Микс 30 можно назначать как в виде монотерапии, так и в сочетании с пероральными гипогликемическими препаратами в тех случаях, когда содержание глюкозы в крови недостаточно регулируется только пероральными гипогликемическими препаратами.
Начало терапии
Для пациентов с сахарным диабетом 2 типа, которым впервые назначен инсулин, рекомендуемая начальная доза препарата РинФаст® Микс 30 составляет 6 ЕД перед завтраком и 6 ЕД перед ужином. Также допускается введение 12 ЕД препарата РинФаст® Микс 30 1 раз в сутки вечером (перед ужином).
Перевод пациента с других препаратов инсулина
При переводе пациента с двухфазного человеческого инсулина на препарат РинФаст® Микс 30 следует начинать с той же дозы и режима введения. Затем корректируют дозу в соответствии с индивидуальными потребностями пациента (см. приведенные ниже рекомендации по титрованию дозы препарата). Как и всегда при переводе пациента на новый тип инсулина необходим строгий медицинский контроль в период перевода пациента и в первые недели использования нового препарата.
Интенсификация терапии
Усилить терапию препаратом РинФаст® Микс 30 можно с помощью перехода с однократной суточной дозы на двухкратную. Рекомендуется после достижения дозы 30 ЕД препарата переходить на применение препарата РинФаст® Микс 30 2 раза в сутки, разделив дозу на две равные части – утреннюю и вечернюю (перед завтраком и ужином).
Переход на применение препарата РинФаст® Микс 30 3 раза в сутки возможен, если разделить утреннюю дозу на две равные части и вводить эти две части утром и в обед (трёхкратная суточная доза).
Коррекция дозы
Для корректировки дозы препарата РинФаст® Микс 30 используется наименьшее значение концентрации глюкозы в крови натощак, полученное в течение последних трех дней.
Для оценки адекватности предыдущей дозы используют значение концентрации глюкозы в крови перед следующим приемом пищи.
Коррекцию дозы можно проводить один раз в неделю до достижения целевого значения HbA1с.
Не следует увеличивать дозу препарата, если в этот период наблюдалась гипогликемия.
Коррекция дозы может быть необходима при усилении физической активности пациента, изменении его обычной диеты или наличии сопутствующего заболевания.
Для коррекции дозы препарата РинФаст® Микс 30 рекомендуется использовать приведенные ниже рекомендации по титрованию дозы:
| Концентрация глюкозы в крови перед приемом пищи | Корректировка дозы препарата РинФаст® Микс 30 | |
| <4,4 ммоль/л | <80 мг/дл | -2 ЕД |
| 4,4-6,1 ммоль/л | 80-110 мг/дл | 0 (не требуется) |
| 6,2-7,8 ммоль/л | 111-140 мг/дл | +2 ЕД |
| 7,9-10,0 ммоль/л | 141-180 мг/дл | +4 ЕД |
| >10,0 ммоль/л | >180 мг/дл | +6 ЕД |
Применение препарата РинФаст® Микс 30 в комбинации с агонистами рГПП-1 может приводить к снижению потребности в инсулине. У пациентов с сахарным диабетом 2 типа с HbA1с менее 8%, получающих препарат РинФаст® Микс 30, при добавлении агониста рГПП-1 рекомендуется снижение дозы препарата РинФаст® Микс 30 на 20% для уменьшения риска развития гипогликемии. У пациентов с HbA1с выше 8% при применении препарата РинФаст® Микс 30 в комбинации с агонистом рГПП-1 возможность снижения дозы препарата следует рассматривать индивидуально. Впоследствии дозу препарата также следует корректировать индивидуально.
Инструкция по применению и обращению
Препарат РинФаст® Микс 30 в картридже
а) Приготовление дозы
Во избежание возможной передачи инфекционного заболевания каждый картридж должен использоваться только одним пациентом, даже в случае замены иглы на устройстве введения.
Картриджи препарата РинФаст® Микс 30 следует применять только со следующими шприц-ручками:
- Пен-инъектор для введения инсулина ХумаПен ® Саввио («Эли Лилли энд Компани/ Eli Lilly and Company», США)
- Пен-инъектор для введения инсулина индивидуальный РинсаПен® I с принадлежностями («Ипсомед АГ/ Ypsomed AG», Швейцария)
- Пен-инъектор для введения инсулина индивидуальный РинсаПен® II с принадлежностями («Ипсомед АГ/ Ypsomed AG», Швейцария)
При проведении инъекций препарата РинФаст® 30 Микс при помощи перечисленных устройств необходимо внимательно соблюдать указания инструкций по использованию шприц-ручек, представленных их производителями.
Эти картриджи не должны применяться с другими многоразовыми шприц-ручками, так как точность дозирования подтверждена только при применении препарата с перечисленными выше шприц-ручками.
Перед применением препарата РинФаст® Микс 30:
- Проверьте этикетку, чтобы убедиться в использовании необходимого типа инсулина.
- Всегда проверяйте картридж, включая резиновый поршень. Перед применением следует убедиться, что картридж препарата РинФаст® Микс 30 не поврежден (например, что на нем нет трещин). Не используйте картридж препарата РинФаст® Микс 30, если он имеет какие-либо повреждения или если ширина видимой части резинового поршня больше ширины белой кодовой полоски. Если картридж поврежден, его необходимо вернуть производителю. Для получения более подробной информации необходимо обратиться к Инструкции по использованию инъекционной системы для введения инсулина.
- Продезинфицируйте резиновую мембрану ватным тампоном, смоченным медицинским антисептическим раствором.
Перед установкой нового картриджа препарата РинФаст® 30 Микс в шприц-ручку необходимо:
Перед проведением каждой следующей инъекции препарата РинФаст® 30 Микс необходимо:
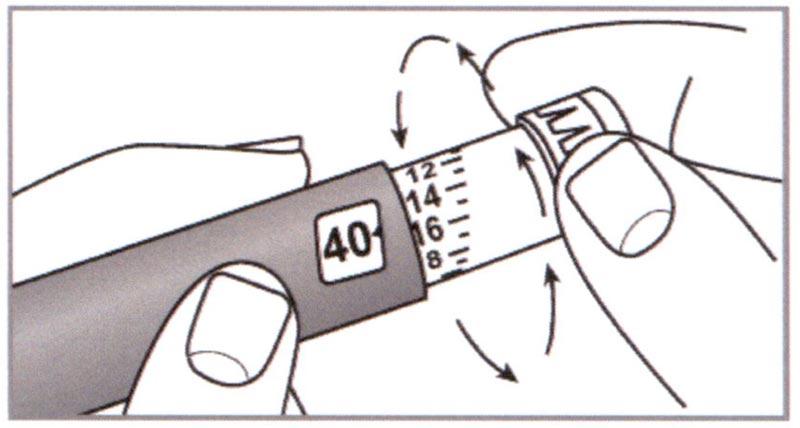
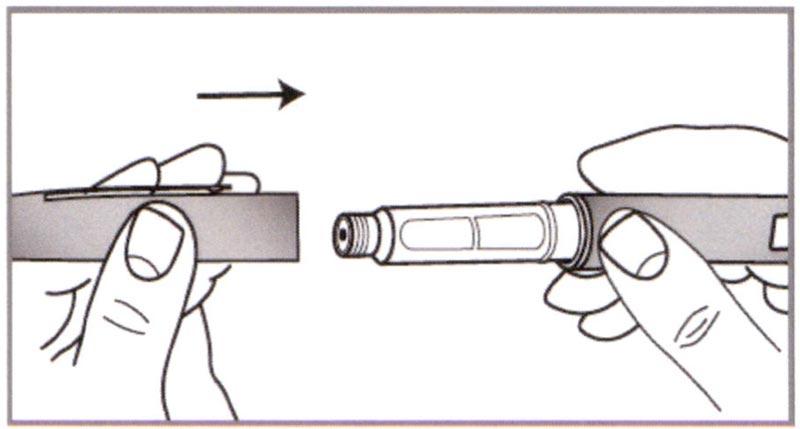
- Встряхнуть картридж не менее 10 раз между позициями а и b (см. Рисунок 2) до тех пор, пока содержимое картриджа не приобретет вид белой однородной мутной водянистой жидкости.
Не допускается применять картридж с препаратом, если после ресуспендирования содержимое не приобрело вид однородной белой мутной жидкости.
б) Введение инсулина
- Введите иглу под кожу. Используйте технику инъекции, рекомендованную Вашим врачом или медицинской сестрой и описанную в Инструкции по использованию инъекционной системы.
- После инъекции оставьте иглу под кожей не менее 6 секунд. Это обеспечит введение полной дозы инсулина.
- Удаляйте иглу после каждой инъекции. В противном случае, при перепаде температуры возможно вытекание жидкости из картриджа препарата РинФаст® Микс 30, что приведет к изменению концентрации инсулина.
Препарат РинФаст® Микс 30 в шприц-ручке для многократных инъекций Ринастра® II или Ринастра® III
Перед применением препарата РинФаст® Микс 30 в предзаполненной шприц-ручке Ринастра® II или Ринастра® III необходимо внимательно ознакомиться с инструкцией по использованию шприц-ручки, соблюдая требования и рекомендации по обращению с картриджем, присоединению иглы и технике инъекции инсулина, представленные в ней. Вводить инсулин при помощи одноразовой шприц-ручки допустимо только подкожно.
Во избежание возможной передачи инфекционного заболевания каждая шприц-ручка должна использоваться только одним пациентом, даже в случае замены иглы на устройстве введения.
Применение препарата в особых клинических группах пациентов
Как всегда при применении препаратов инсулина, у пациентов особых групп следует более тщательно контролировать концентрацию глюкозы в крови и корректировать дозу инсулина индивидуально.
Пациенты пожилого и старческого возраста:
Препарат РинФаст® Микс 30 может применяться у пациентов пожилого возраста, однако опыт его применения в комбинации с пероральными гипогликемическими препаратами у пациентов старше 75 лет ограничен.
Пациенты с недостаточностью функции почек и печени:
У пациентов с почечной или печеночной недостаточностью потребность в инсулине может быть снижена.
Дети до 18 лет:
Препарат РинФаст® Микс 30 может применяться для лечения детей и подростков в возрасте старше 10 лет в тех случаях, когда предпочтительно применение предварительно смешанного инсулина. Существуют ограниченные клинические данные для детей в возрасте 6-9 лет (см. раздел «Фармакодинамические свойства»).
Препарат РинФаст® Микс 30 следует вводить подкожно в область бедра или передней брюшной стенки. При желании препарат можно вводить в область плеча или ягодицы. Следует постоянно менять места инъекций в пределах анатомической области, чтобы уменьшить риск развития липодистрофии и амилоидоза кожи (см. разделы «Особые указания» и «Побочное действие»).
Как и при применении любых других препаратов инсулина, продолжительность действия препарата РинФаст® Микс 30 зависит от дозы, места введения, интенсивности кровотока, температуры и уровня физической активности.
По сравнению с двухфазным человеческим инсулином, препарат РинФаст® Микс 30 начинает действовать быстрее, поэтому его следует вводить непосредственно перед приемом пищи. При необходимости можно вводить препарат РинФаст® Микс 30 вскоре после приема пищи.
Побочное действие
Нежелательные реакции (HP), наблюдаемые у пациентов, применяющих препарат инсулин аспарт двухфазный 30, обусловлены, в основном, фармакологическим эффектом инсулина. Наиболее часто встречающимся нежелательным явлением при применении инсулина является гипогликемия. Частота возникновения HP на фоне применения препарата инсулин аспарт двухфазный 30 изменяется в зависимости от популяции пациентов, режима дозирования препарата и контроля гликемии.
На начальной стадии инсулинотерапии могут возникать нарушения рефракции, отеки и реакции в местах введения препарата (включающие боль, покраснение, крапивницу, воспаление, гематому, припухлость и зуд в месте инъекции). Эти симптомы обычно носят временный характер. Быстрое улучшение контроля гликемии может приводить к состоянию «острой болевой нейропатии», которая обычно является обратимой. Интенсификация инсулинотерапии с резким улучшением контроля углеводного обмена может привести к временному ухудшению проявлений диабетической ретинопатии, в то же время длительное улучшение контроля гликемии снижает риск прогрессирования диабетической ретинопатии.
Перечень HP представлен в таблице.
Все представленные ниже HP, основанные на данных, полученных в ходе клинических исследований, распределены по группам согласно частоте развития в соответствии с MedDRA и системами органов. Частота развития HP определена как: очень часто (≥1/10), часто (≥1/100 до <1/10), нечасто (≥1/1,000 до <1/100), редко (≥1/10,000 до <1/1,000), очень редко (<1/10,000) и неизвестно (невозможно оценить на основании имеющихся данных).
| Нарушения со стороны иммунной системы | Нечасто – крапивница, кожная сыпь, высыпания на коже |
| Очень редко – анафилактические реакции* | |
| Нарушения со стороны обмена веществ и питания | Очень часто – гипогликемия* |
| Нарушения со стороны нервной системы | Редко – периферическая нейропатия («острая болевая нейропатия») |
| Нарушения со стороны органа зрения | Нечасто – нарушения рефракции |
| Нечасто – диабетическая ретинопатия | |
| Нарушения со стороны кожи и подкожных тканей | Нечасто – липодистрофия* Неизвестно – амилоидоз кожи |
| Общие расстройства и нарушения в месте введения | Нечасто – реакции в местах введения |
| Нечасто – отеки |
*См. «Описание отдельных нежелательных реакций»
Описание отдельных нежелательных реакций:
Анафилактические реакции
Отмечены очень редкие случаи возникновения реакций генерализованной гиперчувствительности (в том числе генерализованная кожная сыпь, зуд, повышенное потоотделение, желудочно-кишечные расстройства, ангионевротический отек, затруднение дыхания, учащенное сердцебиение, снижение артериального давления), которые являются потенциально опасными для жизни.
Гипогликемия
Гипогликемия является наиболее частой HP. Она может развиться, если доза инсулина слишком высока по отношению к потребности в инсулине. Тяжелая гипогликемия может приводить к потере сознания и/или судорогам, временному или необратимому нарушению функции головного мозга вплоть до летального исхода. Симптомы гипогликемии, как правило, развиваются внезапно. Они могут включать «холодный пот», бледность кожных покровов, повышенную утомляемость, нервозность или тремор, чувство тревоги, необычную усталость или слабость, нарушение ориентации, снижение концентрации внимания, сонливость, выраженное чувство голода, нарушение зрения, головную боль, тошноту и учащенное сердцебиение.
Клинические исследования показали, что частота развития гипогликемии варьирует в зависимости от популяции пациентов, режима дозирования и контроля гликемии. В ходе клинических исследований не выявлено разницы в общей частоте наступления эпизодов гипогликемии между пациентами, получающими терапию инсулином аспарт, и пациентами, применяющими препараты человеческого инсулина.
Нарушения со стороны кожи и подкожных тканей
Липодистрофия (включая липогипертрофию, липоатрофию) и амилоидоз кожи могут возникать в месте инъекции и замедлять местное всасывание инсулина. Соблюдение правила смены места инъекции в пределах одной анатомической области может помочь уменьшить риск развития или предотвратить липодистрофию и амилоидоз кожи (см. раздел «Особые указания»).
Передозировка
Симптомы
Определенная доза, необходимая для передозировки инсулина, не установлена, однако гипогликемия может развиваться постепенно, если вводимые дозы значительно выше потребности пациента.
Лечение
- Легкую гипогликемию пациент может устранить сам, приняв внутрь глюкозу или сахаросодержащие продукты питания. Поэтому пациентам с сахарным диабетом рекомендуется постоянно носить с собой сахаросодержащие продукты.
- В случае тяжелой гипогликемии, когда пациент находится без сознания, следует ввести от 0,5 мг до 1 мг глюкагона внутримышечно или подкожно (может вводить обученный человек) либо внутривенно раствор глюкозы (декстрозы) (может вводить только медицинский работник). Также необходимо внутривенно ввести декстрозу в случае, если через 10-15 минут после введения глюкагона пациент не приходит в сознание. После восстановления сознания пациенту рекомендуется принять богатую углеводами пищу для профилактики рецидива гипогликемии.
Взаимодействие с другими лекарственными средствами
Имеется ряд лекарственных средств, которые влияют на потребность в инсулине.
Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, агонисты рГПП-1, ингибиторы моноаминооксидазы, ингибиторы ангиотензинпревращающего фермента, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромкриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, салицилаты.
Гипогликемическое действие инсулина ослабляют пероральные контрацептивы, глюкокортикостероиды, тиреоидные гормоны, тиазидные диуретики, гепарин, трициклические антидепрессанты, симпатомиметики, соматропин, даназол, клонидин, блокаторы «медленных» кальциевых каналов, диазоксид, морфин, фенитоин, никотин.
Бета-адреноблокаторы могут маскировать симптомы гипогликемии.
Октреотид/ланреотид может как повышать, так и снижать потребность организма в инсулине.
Алкоголь может как усиливать, так и ослаблять гипогликемический эффект инсулина.
Несовместимость
Поскольку исследования совместимости не проводились, препарат РинФаст® Микс 30 не должен смешиваться с другими препаратами.
Особые указания
Длительные поездки
Перед длительной поездкой, связанной со сменой часовых поясов, пациент должен проконсультироваться со своим лечащим врачом, поскольку смена часового пояса означает, что пациент должен принимать пищу и вводить инсулин в другое время.
Гипергликемия
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете 1 типа, может приводить к развитию гипергликемии или диабетического кетоацидоза. Как правило, первые симптомы гипергликемии появляются постепенно, в течение нескольких часов или дней. К этим симптомам относятся жажда, учащённое мочеиспускание, тошнота, рвота, сонливость, покраснение и сухость кожи, сухость во рту, потеря аппетита, а также запах ацетона в выдыхаемом воздухе. При сахарном диабете 1 типа без соответствующего лечения гипергликемия приводит к развитию диабетического кетоацидоза – состоянию, которое является потенциально летальным.
Гипогликемия
Пропуск приема пищи или незапланированная интенсивная физическая нагрузка у пациента могут привести к гипогликемии.
Гипогликемия может развиться, если введена слишком высокая по отношению к потребности пациента доза инсулина (см. разделы «Побочное действие» и «Передозировка»).
Препарат РинФаст® Микс 30 по сравнению с двухфазным человеческим инсулином
По сравнению с двухфазным человеческим инсулином препарат РинФаст® Микс 30 оказывает более выраженное гипогликемическое действие, вплоть до 6 часов после введения. В связи с этим, в отдельных случаях может потребоваться коррекция дозы инсулина и/или характера питания.
Интенсифицированная инсулинотерапия
После компенсации углеводного обмена, например, при более интенсивной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чём пациенты должны быть проинформированы. Обычные симптомы-предвестники могут исчезать при длительном течении сахарного диабета.
Строгий контроль концентрации глюкозы
Более строгий контроль гликемии у пациентов может увеличивать риск развития гипогликемии, поэтому увеличение дозы препарата РинФаст® Микс 30 необходимо осуществлять под строгим медицинским контролем, как указано в разделе «Способ применения и дозы».
Введение препарата РинФаст® Микс 30
Поскольку препарат РинФаст® Микс 30 следует применять в непосредственной связи с приёмом пищи, следует учитывать высокую скорость наступления эффекта препарата при лечении пациентов, имеющих сопутствующие заболевания или принимающих лекарственные средства, замедляющие всасывание пищи.
Сопутствующие заболевания
Сопутствующие заболевания, особенно инфекционные и сопровождающиеся лихорадкой, обычно повышают потребность организма в инсулине. Коррекция дозы препарата может также потребоваться при наличии у пациента сопутствующих заболеваний почек, печени, нарушении функции надпочечников, гипофиза или щитовидной железы.
Перевод с других препаратов инсулина
При переводе пациента на другие типы инсулина, ранние симптомы-предвестники гипогликемии могут становиться менее выраженными, по сравнению с наблюдавшимися при применении предыдущего типа инсулина.
Перевод пациента на новый тип инсулина или препарат инсулина другого производителя необходимо осуществлять под строгим медицинским контролем. При изменении концентрации, производителя, типа и вида (человеческий инсулин, аналог человеческого инсулина) препаратов инсулина и/или способа производства может потребоваться изменение дозы. Пациентам, переходящим с других препаратов инсулина на лечение препаратом РинФаст® Микс 30, может потребоваться увеличение частоты инъекций или изменение дозы по сравнению с дозами ранее применявшихся препаратов инсулина. При необходимости коррекции дозы, она может быть произведена уже при первом введении препарата или в течение первых недель или месяцев лечения (см. раздел «Способ применения и дозы»).
Реакции в месте введения
Как и при лечении другими препаратами инсулина, могут развиваться реакции в месте введения, что проявляется болью, покраснением, крапивницей, воспалением, гематомами, припухлостью и зудом. Регулярная смена места инъекции в одной и той же анатомической области уменьшает риск развития этих реакций. Реакции обычно разрешаются в течение нескольких дней – нескольких недель. В редких случаях реакции в месте введения требуют прекращения лечения препаратом РинФаст® Микс 30.
Нарушения со стороны кожи и подкожных тканей
Пациенты должны быть проинформированы о необходимости постоянно менять места инъекции в пределах одной анатомической области, чтобы снизить риск развития липодистрофии и амилоидоза кожи. Существует потенциальный риск изменения абсорбции инсулина и ухудшения гликемического контроля, если инъекция инсулина проводится в область липодистрофии или амилоидоза. Были получены сообщения о развитии гипогликемии при внезапном изменении места инъекции с пораженной области на инъекцию в нормальную ткань. После изменения места инъекции рекомендуется контроль концентрации глюкозы крови и, при необходимости, проведение коррекции дозы препарата.
Совместное применение с препаратами тиазолидиндиона
Сообщалось о случаях развития хронической сердечной недостаточности при лечении пациентов тиазолидиндионами в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития хронической сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии тиазолидиндионами и препаратами инсулина. При назначении такой комбинированной терапии необходимо проводить медицинские обследования пациентов на предмет выявления у них признаков и симптомов хронической сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности лечение тиазолидиндионами необходимо прекратить.
Предотвращение ошибочного введения препаратов инсулина
Следует проинструктировать пациента о необходимости перед каждой инъекцией проверять маркировку на этикетке во избежание случайного введения препаратов другого инсулина вместо препарата РинФаст® Микс 30.
Антитела к инсулину
При применении инсулина возможно образование антител. В редких случаях при образовании антител может потребоваться коррекция дозы инсулина для предотвращения случаев гипергликемии или гипогликемии.
Влияние на способность управлять транспортными средствами и механизмами
При гипогликемии способность пациентов к концентрации внимания и скорость реакции могут нарушаться, что представляет опасность в тех ситуациях, когда эти способности особенно необходимы (например, при управлении транспортными средствами или во время работы с механизмами).
Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии при управлении транспортными средствами или во время работы с механизмами. Это особенно важно для пациентов, у которых отсутствуют симптомы-предвестники гипогликемии или снижена выраженность их проявлений, а также для пациентов с частыми эпизодами гипогликемии. В этих случаях следует обсудить, насколько целесообразно управление транспортным средством или выполнение подобных работ.
Форма выпуска
Суспензия для подкожного введения, 100 ЕД/мл.
По 3 мл в бесцветные стеклянные картриджи нейтрального стекла (1-й гидролитический класс) производства SCHOTT Hungary Kft («ШОТТ Хан-гари Кфт») с плунжерами резиновыми из бромбутилового каучука по ISO 13926-2:2011 или производства «West Pharmaceutical Services» («Вест Фармасьютикал Сервис»), обкатанные колпачками комбинированными из алюминия с дисками резиновыми из бромбутилового каучука по ISO 13926-3:2012 или по ISO 11040-3:2012 или производства «West Pharmaceutical Services» («Вест Фармасьютикал Сервис»). В каждый картридж вложен шарик диаметром 2,50±0,05 мм из стекла 1-го гидролитического класса с полированной поверхностью, разрешенный к применению в фармацевтической промышленности. На каждый картридж наклеивают этикетку из пленки прозрачной полипропиленовой импортной, разрешенной к применению в РФ.
1) По 5 картриджей в контурную ячейковую упаковку из пленки поливинилхлоридной или пленки полиэтилентерефталатной или другой, разрешенной к применению в РФ, и фольги алюминиевой с нанесением маркировки типографским способом. По 1 контурной ячейковой упаковке с инструкцией по применению помещают в пачку из картона по ГОСТ 7933-89 или импортного, разрешенного к применению в РФ.
2) По одному картриджу предварительно устанавливают в пластиковую мультидозовую одноразовую шприц-ручку для многократных инъекций Ринастра® II (производитель Ипсомед АГ, Швейцария) или в шприц-ручку Ринастра® III (производитель Бектон Дикинсон энд Компани, США). На корпус каждой шприц-ручки наклеивают этикетку из пленки полипропиленовой импортной, разрешенной к применению в РФ. По 5 предварительно заполненных мультидозовых одноразовых шприц-ручек для многократных инъекций Ринастра® II или Ринастра® III с инструкцией по применению и инструкцией по использованию шприц-ручки помещают в пачку из картона по ГОСТ 7933-89 или импортного, разрешенного к применению в РФ.
Групповая упаковка и транспортная тара в соответствии с ГОСТ 17768-90.
Срок годности
До первого применения:
2 года.
После вскрытия:
4 недели.
Не применять по истечении срока годности, указанного на упаковке.
Условия хранения
Хранить в недоступном для детей месте.
До первого использования:
Хранить в холодильнике при температуре от 2 до 8 °С.
Не замораживать. Не размещать рядом с морозильной камерой.
Предохранять от воздействия избыточного тепла и света. Картриджи хранить в картонной упаковке для защиты от света.
После вскрытия:
Хранить при температуре не выше 30 °С вдали от источников тепла и солнечных лучей. Не замораживать.
Шприц-ручка, находящаяся в употреблении или переносимая в качестве запасной, не должна храниться в холодильнике.
Для защиты от света шприц-ручку хранить с надетым защитным колпачком.
Меры предосторожности при применении
Препарат РинФаст® Микс 30 и иглы предназначены только для индивидуального применения. Не допускается повторное заполнение картриджа или картриджа шприц-ручки.
Препарат РинФаст® Микс 30 нельзя применять, если после перемешивания он не становится однородно белым и мутным.
Следует подчеркнуть пациенту необходимость тщательного перемешивания суспензии препарата РинФаст® Микс 30 непосредственно перед применением.
Нельзя применять препарат РинФаст® Микс 30, если он был заморожен.
Пациенты должны быть предупреждены о необходимости выбрасывать иглу после каждой инъекции.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «ГЕРОФАРМ», Россия
191119, г. Санкт-Петербург, ул. Звенигородская, д. 9
Производитель
ООО «ГЕРОФАРМ», Россия
Адреса мест производства:
- Московская обл., г.о. Серпухов, р.п. Оболенск, тер. «Квартал А», стр. 5
- Московская обл., г.о. Серпухов, р.п. Оболенск, тер. «Квартал А», стр. 5, корп. 1
- Московская обл., городской округ Серпухов, рабочий поселок Оболенск, территория «Квартал А», стр. 4, корп. 82
Организация, принимающая претензии от потребителей
ООО «ГЕРОФАРМ»,
Россия, 191144, г. Санкт-Петербург, Дегтярный пер., д. 11, лит. Б
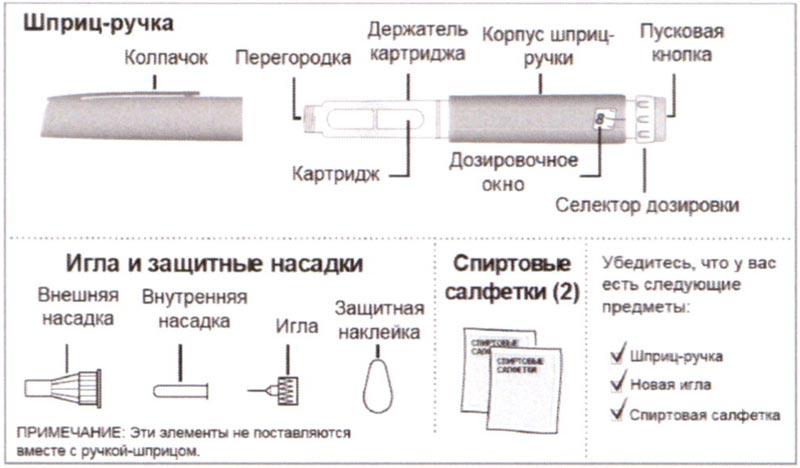
Инструкция для пациентов по использованию шприц-ручки для многократных инъекций Ринастра® II или Ринастра® III
Перед проведением инъекции необходимо вымыть руки водой с мылом и выбрать место для инъекции. Протереть кожу в месте инъекции спиртовой салфеткой только после того, как доза инсулина была установлена в шприц-ручке. Перед инъекцией дать высохнуть спирту в месте инъекции.
Сборка
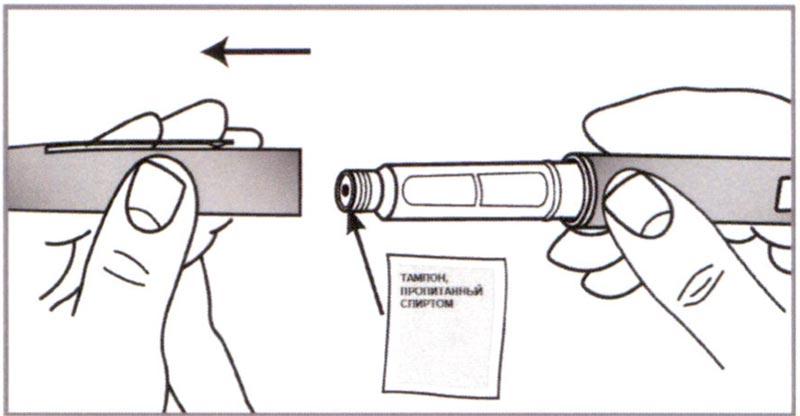
А) Удерживать шприц-ручку одной рукой и снять Колпачок, потянув за него другой рукой. Протереть резиновую мембрану (Перегородку) спиртовой салфеткой.
Примечание: Использование спиртовой салфетки помогает свести к минимуму риск инфицирования.
Б) Выбрать иглу из набора. Удалить Защитную наклейку с новой Иглы.
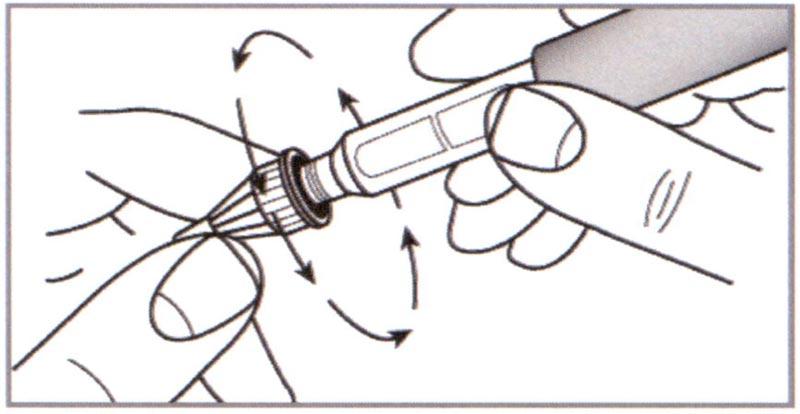
В) При помощи Внешней насадки установить иглу прямо на Держатель картриджа. Надежно закрутить.
⚠ Внимание: Всегда используйте новую иглу для шприц-ручки.
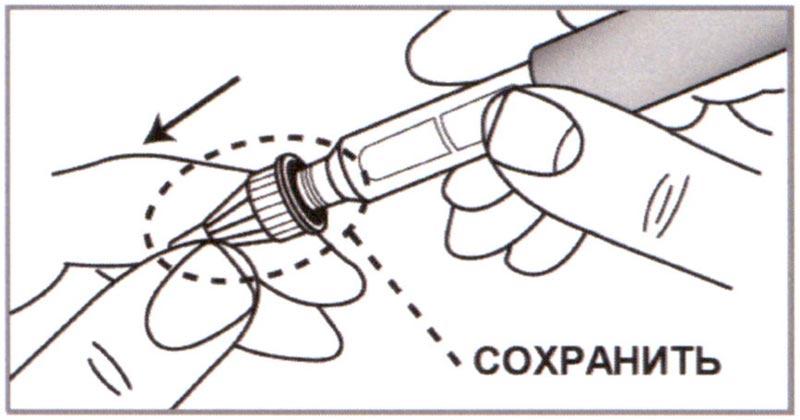
Г) Слегка потянув, снять Внешнюю насадку. Сохранить Внешнюю насадку для последующего удаления использованной Иглы.
Подготовка
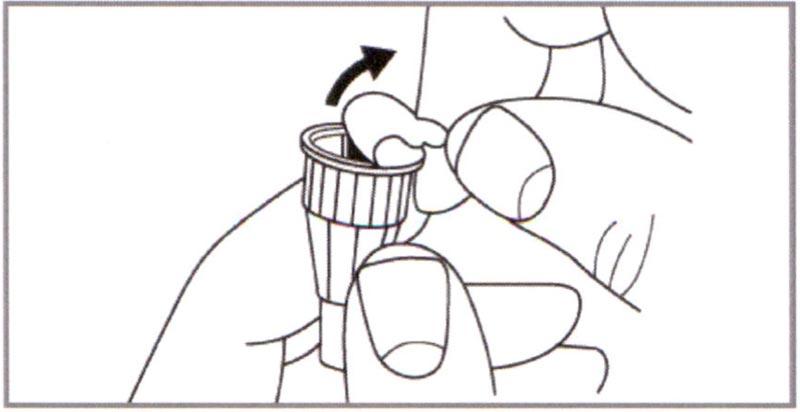
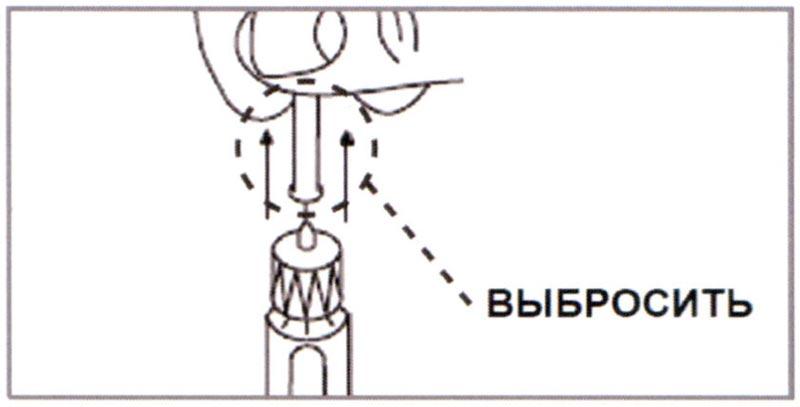
Д) Осторожно снять Внутреннюю насадку и выбросить. Удерживать Шприц-ручку иглой вверх. Слегка постучать пальцем по картриджу, чтобы помочь пузырькам воздуха подняться вверх. Могут оставаться маленькие пузырьки, но это допустимо.
Примечание: Игла становится видимой (обнажается) по мере удаления Внутренней насадки.
Проверка пригодности шприц-ручки перед инъекцией необходима для того, чтобы удалить воздух из иглы.
⚠ Внимание: Проверку пригодности шприц-ручки необходимо проводить перед каждой инъекцией.
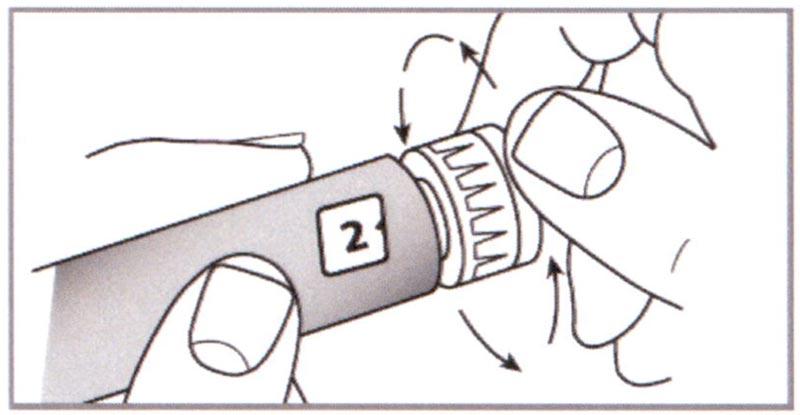
Е) Прокрутить Селектор дозировки и установить дозу на 2 единицы таким образом, чтобы цифра 2 совпала в Дозировочном окне с указателем. При наборе каждой единицы будет слышен щелчок.
Примечание: Если Селектор дозировки проскочил необходимую дозу, просто прокрутите его в обратном направлении для того, чтобы скорректировать дозу.
⚠ Внимание: Не нажимайте Пусковую кнопку во время установки дозы.
Ж) Удерживая Шприц-ручку с Иглой, направленной вверх, нажать Пусковую кнопку до упора. Селектор дозировки издаст щелчок, когда достигнет нуля.
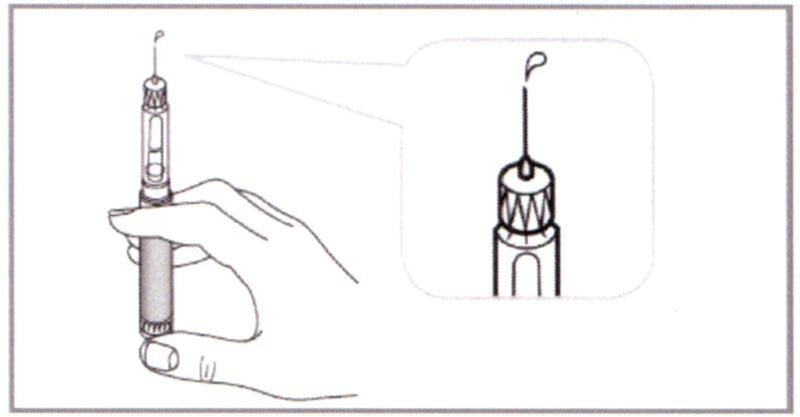
Проверьте, чтобы из Иглы вышла капля жидкости. Если этого не произошло, повторите шаги Е и Ж, но не более 6 раз. Если капля по-прежнему не вышла, снимите Иглу (см. шаг Л) и повторите свои действия, начиная с шага Б (с выбора новой иглы).
⚠ Внимание: Чтобы доза была полной, перед каждым введением дозы необходимо всегда проверять выход капли жидкости из иглы.
Небольшая «потеря» инсулина допускается
⚠ Внимание: Вы проверили Шприц-ручку с дозой, установленной на 2 единицы, чтобы удалить воздух из иглы? Если нет, вернитесь к пункту «Е».
Установка дозы
З) Прокручивайте Селектор дозировки до тех пор, пока необходимая доза не совпадет с указателем в Дозировочном окне.
Например, если Вам нужна доза 40 единиц, прокрутите Селектор дозировки до 40 (как показано на рисунке).
⚠ Внимание: Вы не сможете выбрать дозу, превышающую количество единиц, оставшихся в картридже. В случае если Селектор дозировки не прокручивается, это означает, что в Шприц-ручке отсутствует достаточное количество лекарственного средства. Выбросите Шприц-ручку или введите оставшиеся единицы дозы и используйте новую шприц-ручку, чтобы завершить введение необходимой дозы.
Введение дозы
И) Убедитесь, что вы набрали требуемую дозу.
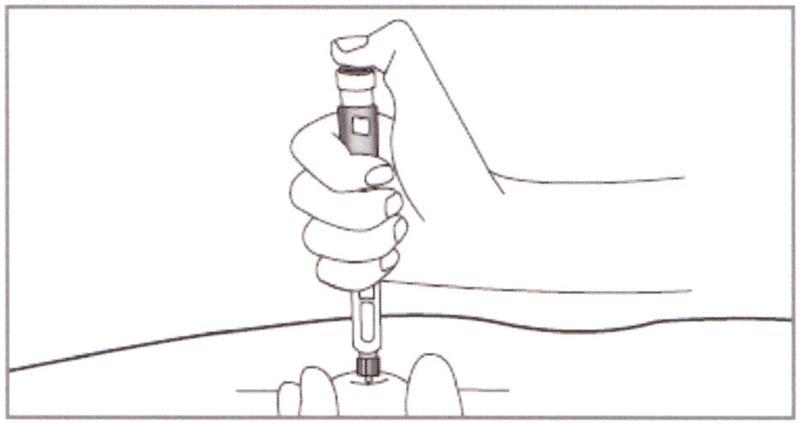
Протрите кожу спиртовой салфеткой в месте инъекции. Зажмите участок кожи в нужном месте и введите иглу под кожу одним непрерывным движением.
Чтобы избежать случайной травмы от укола иглой:
- ЗАЖИМАТЬ не менее 2,5 см кожи.
- НЕ ВВОДИТЬ иглу под углом в направлении к пальцам.
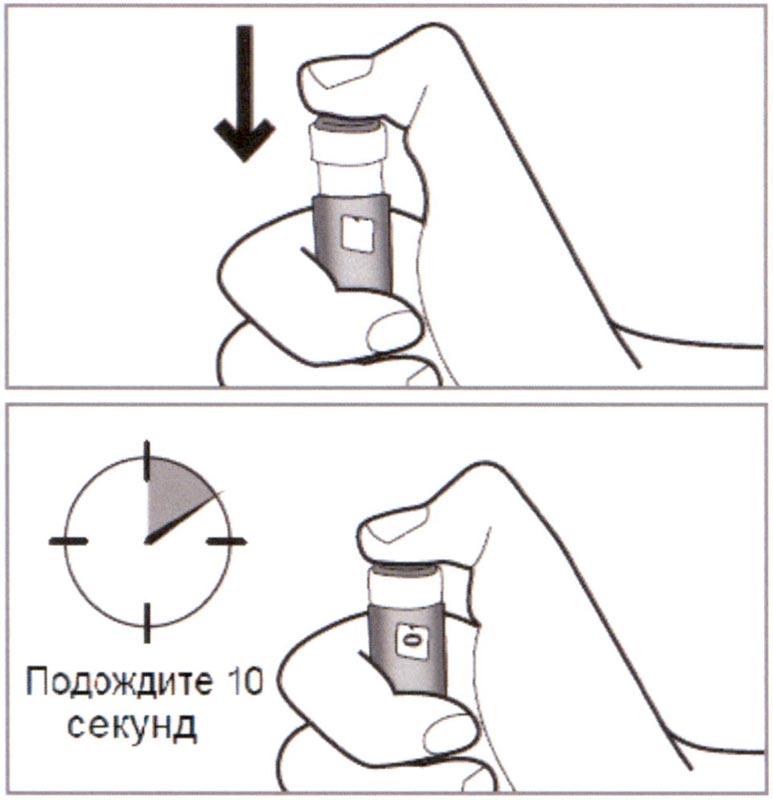
К) Нажать Пусковую кнопку, пока значение «0» не совпадет с указателем в Дозировочном окне. Удерживать кнопку нажатой, а Шприц-ручку на месте инъекции в течение 10 секунд после щелчка остановки.
⚠ Внимание: Невыполнение этих шагов может привести к введению неправильной дозы.
Если Вы не удерживаете Шприц-ручку в месте инъекции в течение полных 10 секунд, требуемая доза препарата может быть не получена.
Если инсулин продолжает вытекать из иглы после инъекции, при проведении последующих инъекций удерживайте иглу в коже дольше.
Утилизация иглы и хранение шприц-ручки
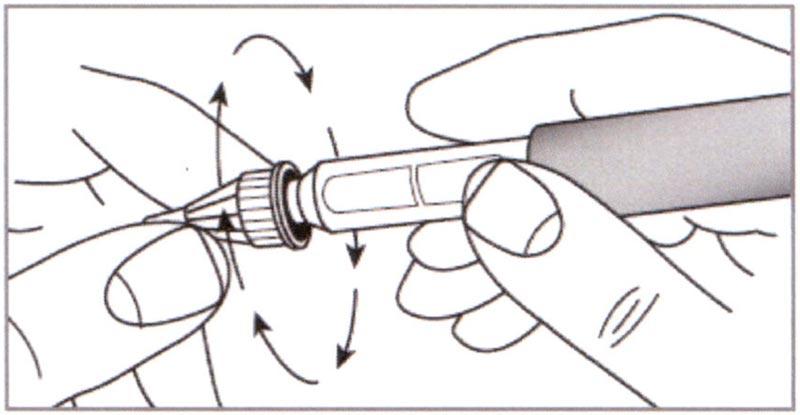
Л) Осторожно надеть Внешнюю насадку на иглу до упора. Открутить иглу и выбросить ее вместе с Внешней насадкой.
М) Надеть Колпачок Шприц-ручки и хранить Шприц-ручку до следующего использования.
Уход за Шприц-ручкой и утилизация
- Хранить Шприц-ручку вдали от попадания прямых солнечных лучей.
- Шприц-ручка предназначена для индивидуального использования и не может использоваться несколькими лицами.
- Не пытайтесь самостоятельно ремонтировать Шприц-ручку. Сообщите о возникновении проблемы в организацию, принимающую претензию, указанную в инструкции по медицинскому применению.
Пустая шприц-ручка не должна использоваться повторно и подлежит уничтожению.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Код ATX: A10AD05 (Insulin aspart)
Активное вещество: инсулин аспарт бифазный (insulin aspart — biphasic)
Rec.INN зарегистрированное ВОЗ
Лекарственная форма
| НовоМикс® 30 ФлексПен® |
Сусп. д/п/к введения 100 ЕД/1 мл: картридж в шприц-ручке 3 мл 5 шт. рег. №: П N015640/01 от 06.10.08 — Бессрочно |
Форма выпуска, упаковка и состав препарата НовоМикс® 30 ФлексПен®
Суспензия для п/к введения белого цвета, гомогенная (не содержащая комочков, в образце могут появляться хлопья); при стоянии расслаивается, образуя белый осадок и бесцветную или почти бесцветную надосадочную жидкость; при осторожном перемешивании должна образовываться однородная суспензия.
| 1 мл | |
| инсулин аспарт двухфазный | 100 ЕД* |
| инсулин аспарт растворимый | 30% |
| инсулин аспарт протамин кристаллический | 70% |
Вспомогательные вещества: глицерол — 16 мг, фенол — 1.5 мг, метакрезол — 1.72 мг, цинка хлорид — 19.6 мкг, натрия хлорид — 0.877 мг, натрия гидрофосфата дигидрат — 1.25 мг, протамина сульфат ~ 0.33 мг, натрия гидроксид ~ 2.2 мг, хлористоводородная кислота ~ 1.7 мг, вода д/и — до 1 мл.
3 мл (300 ЕД) — картриджи стеклянные (1) — шприц-ручки мультидозовые одноразовые для многократных инъекций (5) — пачки картонные.
* 1 ЕД соответствует 35 мкг (или 6 нмоль) безводного инсулина аспарт.
Клинико-фармакологическая группа: Комбинация аналогов человеческого инсулина средней продолжительности или длительного и короткого действия
Фармако-терапевтическая группа: Гипогликемическое средство — комбинация аналогов инсулинов короткой и средней продолжительности действия
Фармакологическое действие
Представляет собой двухфазную суспензию, состоящую из смеси аналогов инсулина: растворимого инсулина аспарт (30% аналога инсулина короткого действия) и кристаллов инсулина аспарт протамина (70% аналога инсулина средней продолжительности действия).
Снижение уровня глюкозы в крови происходит за счет повышения ее внутриклеточного транспорта после связывания инсулина аспарта бифазного с инсулиновыми рецепторами мышечных и жировых тканей и одновременного торможения продукции глюкозы печенью.
Показания активных веществ препарата НовоМикс® 30 ФлексПен®
Сахарный диабет.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Лечение препаратами инсулина следует проводить строго в соответствии с инструкцией по медицинскому применению конкретного лекарственного препарата.
Побочное действие
Со стороны иммунной системы: нечасто — крапивница, кожная сыпь, высыпания на коже; очень редко — анафилактические реакции.
Со стороны обмена веществ и питания: очень часто — гипогликемия.
Со стороны нервной системы: редко — периферическая невропатия (острая болевая нейропатия).
Со стороны органа зрения: нечасто — нарушения рефракции, диабетическая ретинопатия.
Со стороны кожи и подкожных тканей: нечасто — липодистрофия.
Общие реакции: нечасто — отеки.
Противопоказания к применению
Повышенная чувствительность к инсулину аспарт.
Не рекомендуется применять у детей до 6 лет.
Применение при беременности и кормлении грудью
Клинический опыт применения при беременности ограничен.
В период возможного наступления беременности и в течение всего ее срока необходимо вести тщательное наблюдение за состоянием пациенток с сахарным диабетом и контролировать концентрацию глюкозы в крови. Потребность в инсулине, как правило, снижается в I триместре и постепенно повышается во II и III триместрах беременности. Вскоре после родов потребность в инсулине быстро возвращается к уровню, который был до беременности.
В период кормления грудью можно применять без ограничений. Введение инсулина кормящей матери не представляет угрозы для ребенка. Однако может возникнуть необходимость в коррекции дозы.
Применение у детей
Не рекомендуется применять у детей до 6 лет, т.к. клинические исследования у них не проводились.
Можно применять для лечения детей и подростков в возрасте старше 10 лет в тех случаях, когда предпочтительно использование предварительно смешанного инсулина. Существуют ограниченные клинические данные для детей в возрасте 6-9 лет.
Применение у пожилых пациентов
Можно применять пациентов пожилого возраста, однако опыт его применения в комбинации с пероральными гипогликемическими препаратами у пациентов старше 75 лет ограничен.
Особые указания
Перед длительной поездкой, связанной со сменой,часовых поясов, пациент должен проконсультироваться со своим лечащим врачом, поскольку смена часового пояса означает, что пациент должен принимать пищу и вводить инсулин в другое время.
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете 1 типа, может привести к развитию гипергликемии или диабетического кетоацидоза. Как правило, первые симптомы гипергликемии появляются постепенно, в течение нескольких часов или дней. Симптомами гипергликемии являются чувство жажды, увеличение количества выделяемой мочи, тошнота, рвота, сонливость, покраснение и сухость кожи, сухость во рту, потеря аппетита, а также появление запаха ацетона в выдыхаемом воздухе. Без соответствующего лечения гипергликемия у пациентов с сахарным диабетом 1 типа может приводить к диабетическому кетоацидозу — состоянию, которое является потенциально летальным.
Пропуск приема пищи или незапланированная интенсивная физическая нагрузка могут привести к гипогликемии. Гипогликемия также может развиться, если введена слишком высокая по отношению к потребности пациента доза инсулина.
После компенсации углеводного обмена, например, при интенсифицированной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чем больные должны быть проинформированы. Обычные симптомы-предвестники могут исчезать при длительном течении сахарного диабета.
Сопутствующие заболевания, особенно инфекционные и сопровождающиеся лихорадкой, обычно повышают потребность организма в инсулине. Коррекция дозы может также потребоваться при наличии у пациента сопутствующих заболеваний почек, печени, нарушении функции надпочечников, гипофиза или щитовидной железы.
При переводе пациента на другие типы инсулина, ранние симптомы-предвестники гипогликемии могут изменяться или становиться менее выраженными, по сравнению с таковыми при использовании предыдущего типа инсулина.
Перевод пациента на новый тип инсулина или препарат инсулина другого производителя необходимо осуществлять под строгим медицинским контролем. При изменении концентрации, типа, производителя и вида (человеческий инсулин, аналог человеческого инсулина) препаратов инсулина и/или способа производства может потребоваться изменение дозы.
Сообщалось о случаях развития хронической сердечной недостаточности при лечении пациентов тиазолидиндионами в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития хронической сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии тиазолидиндионами и препаратами инсулина. При назначении такой комбинированной терапии необходимо проводить медицинские обследования пациентов на предмет выявления у них признаков и симптомов хронической сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности лечение тиазолидиндионами необходимо прекратить.
Влияние на способность к управлению транспортными средствами и механизмами
Способность пациентов к концентрации внимания и скорость реакции могут нарушаться во время гипогликемии, что может представлять опасность в тех ситуациях, когда эти способности особенно необходимы (например, при управлении транспортными средствами или работе с машинами и механизмами).
Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии при управлении транспортными средствами. Это особенно важно для пациентов с отсутствием или снижением выраженности симптомов-предвестнико в развивающейся гипогликемии или страдающих частыми эпизодами гипогликемии. В этих случаях следует рассмотреть целесообразность управления транспортными средствами и выполнения подобных работ.
Лекарственное взаимодействие
Имеется ряд лекарственных средств, которые влияют на потребность в инсулине. Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы МАО, ингибиторы АПФ, ингибиторы карбоангидразы, не селективные бета-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, салицилаты.
Гипогликемическое действие инсулина ослабляют пероральные контрацептивы, глюкокортикостероиды, тиреоидные гормоны, тиазидные диуретики, гепарин, трициклические антидепрессанты, симпатомиметики, соматропин, даназол, клонидин, блокаторы медленных кальциевых каналов, диазоксид, морфин, фенитоин, никотин.
Бета-адреноблокаторы могут маскировать симптомы гипогликемии.
Октреотид/ланреотид может как повышать, так и снижать потребность организма в инсулине.
Алкоголь может усиливать или уменьшать гипогликемический эффект инсулина.
НовоРапид®
МНН: Инсулин аспарт двухфазный
Производитель: Ново Нордиск А/С
Анатомо-терапевтическо-химическая классификация: Insulin aspart
Номер регистрации в РК:
№ РК-ЛС-5№021556
Информация о регистрации в РК:
06.08.2020 — 06.08.2030
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
8 807.04 KZT
- Скачать инструкцию медикамента
Торговое название
НовоРапид®
Международное непатентованное название
Инсулин аспарт
Лекарственная форма
Раствор для инъекций, 100 ЕД/мл
Состав
1 мл препарата содержит
активное вещество — инсулин аспарт 100 ЕД (3,5 мг);
вспомогательные вещества: глицерол, фенол, метакрезол, цинк, натрия хлорид, натрия гидрофосфата дигидрат, натрия гидроксид 2 М, кислота хлороводородная 2 М, вода для инъекций.
Один флакон содержит 10 мл раствора, эквивалентного 1000 ЕД.
Описание
Прозрачная бесцветная жидкость.
Фармакотерапевтическая группа
Средства для лечения сахарного диабета. Инсулины.
Инсулины и аналоги быстрого действия. Инсулин аспарт.
Код АТХ A10АВ05
Фармакологические свойства
Фармакокинетика
После подкожного введения инсулина аспарт время достижения максимальной концентрации (tmax) в плазме крови в среднем в 2 раза меньше, чем после введения растворимого человеческого инсулина. Максимальная концентрация в плазме крови (Сmax) в среднем составляет 492±256 пмоль/л и достигается через 40 минут после подкожного введения дозы 0,15 ЕД/кг массы тела пациентам с сахарным диабетом типа 1. Концентрация инсулина возвращается к исходному уровню через 4–6 часов после введения препарата. Скорость абсорбции несколько ниже у пациентов с диабетом типа 2, что приводит к более низкой максимальной концентрации (352±240 пмоль/л) и более позднему tmax (60 минут). Межиндивидуальная вариабельность по tmax существенно ниже при использовании инсулина аспарт, по сравнению с растворимым человеческим инсулином, тогда как указанная вариабельность в Сmax для инсулина аспарт больше.
Исследования фармакокинетики не проводились у пожилых пациентов и у пациентов с нарушением функции почек или печени.
Фармакокинетика у детей (6-12 лет) и подростков (13-17 лет) с сахарным диабетом типа 1. Абсорбция инсулина аспарт происходит быстро в обеих возрастных группах, с tmax, аналогичным таковому у взрослых. Однако, имеются отличия Cmax в двух возрастных группах, что подчеркивает важность индивидуальной дозировки препарата.
Пациенты пожилого возраста (≥65 лет)
НовоРапид® можно использовать у пациентов пожилого возраста.
У пациентов пожилого возраста следует более тщательно контролировать концентрацию глюкозы в крови и корректировать дозу инсулина аспрат индивидуально.
Пациенты с почечной и печеночной недостаточностью
У пациентов с почечной или печеночной недостаточностью может быть снижена потребность в инсулине.
У пациентов с нарушением функции почек или печени следует более тщательно контролировать уровень концентрации глюкозы в крови и корректировать дозу инсулина аспрат индивидуально.
Фармакодинамика
НовоРапид® — аналог человеческого инсулина короткого действия, произведенный методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, в котором аминокислота пролин в положении В28 замещена на аспарагиновую кислоту.
Взаимодействует со специфическим рецептором внешней цитоплазматической мембраны клеток и образует инсулин-рецепторный комплекс, стимулирующий внутриклеточные процессы, в т.ч. синтез ряда ключевых ферментов (гексокиназа, пируваткиназа, гликогенсинтетаза и др.). Снижение содержания глюкозы в крови обусловлено повышением ее внутриклеточного транспорта, усилением усвоения тканями, стимуляцией липогенеза, гликогеногенеза, снижением скорости продукции глюкозы печенью и др.
Замещение аминокислоты пролин в положении В28 на аспарагиновую кислоту в препарате НовоРапид® снижает тенденцию молекул к образованию гексамеров, которая наблюдается в растворе обычного инсулина. В связи с этим НовоРапид® гораздо быстрее всасывается из подкожно-жировой клетчатки и начинает действовать гораздо быстрее, чем растворимый человеческий инсулин. НовоРапид® сильнее снижает уровень глюкозы крови в первые 4 часа после приема пищи, чем растворимый человеческий инсулин. У пациентов с сахарным диабетом типа 1 выявляется более низкий постпрандиальный уровень глюкозы крови при введении препарата НовоРапид®, по сравнению с растворимым человеческим инсулином.
Продолжительность действия препарата НовоРапид® после подкожного введения короче, чем растворимого человеческого инсулина.
После подкожного введения действие препарата начинается в течение 10–20 минут после введения. Максимальный эффект наблюдается через 1–3 часа после инъекции. Продолжительность действия препарата составляет 3-5 часов.
Клинические исследования с участием пациентов с сахарным диабетом 1 типа продемонстрировали снижение риска ночной гипогликемии при использовании инсулина аспарт по сравнению с растворимым человеческим инсулином. Риск дневной гипогликемии достоверно не повышался.
Инсулин аспарт является эквипотенциальным растворимому человеческому инсулину на основании показателей молярности.
Взрослые Клинические исследования с участием пациентов с сахарным диабетом типа 1 демонстрируют более низкий постпрандиальный уровень глюкозы крови при введении препарата НовоРапид®, по сравнению с растворимым человеческим инсулином.
Дети и подростки Использование препарата НовоРапид® у детей показало схожие результаты длительного контроля глюкозы при сравнении с растворимым человеческим инсулином.
Клиническое исследование, с использованием растворимого человеческого инсулина до приема пищи и инсулина аспарт после приема пищи, было проведено у маленьких детей (26 пациентов в возрасте от 2 до 6 лет); а также ФК/ФД исследование с использованием однократной дозы было проведено у детей (6-12 лет) и подростков (13-17 лет). Фармакодинамический профиль инсулина аспарт у детей был схожим с таковым у взрослых пациентов.
Беременность: Клинические исследования сравнительной безопасности и эффективности инсулина аспарт и человеческого инсулина при лечении беременных женщин, страдающих сахарным диабетом типа 1 (322 обследованных беременных, из них инсулин аспарт: 157; человеческий инсулин: 165) не выявили никакого негативного воздействия инсулина аспарт на течение беременности или здоровье плода/новорожденного.
Дополнительные клинические исследования 27 женщин с гестационным диабетом, получающих инсулин аспарт и человеческий инсулин (инсулин аспарт получали 14 женщин, человеческий инсулин – 13) свидетельствуют о сопоставимости профилей безопасности наряду со значительным улучшением контроля уровня глюкозы после приема пищи при лечении инсулином аспарт.
Показания к применению
— лечение сахарного диабета у взрослых, подростков и детей от 2-х лет и старше
Способ применения и дозы
НовоРапид® предназначен для подкожного и внутривенного введения. НовоРапид® представляет собой быстродействующий аналог инсулина.
Благодаря более быстрому началу действия, НовоРапид® следует вводить, как правило, непосредственно перед приемом пищи, при необходимости можно вводить вскоре после приема пищи.
Доза препарата определяется врачом индивидуально в каждом конкретном случае, на основании уровня глюкозы в крови. Обычно НовоРапид® используют в сочетании с препаратами инсулина средней продолжительности или длительного действия, которые вводят как минимум 1 раз в сутки.
Индивидуальная суточная потребность в инсулине у взрослых и детей с 2-х лет составляет обычно от 0,5 до 1,0 ЕД/кг массы тела. При введении препарата перед едой, потребность в инсулине может обеспечиваться препаратом НовоРапид® на 50-70%, оставшаяся потребность в инсулине обеспечивается инсулином продленного действия. Температура вводимого инсулина должна соответствовать комнатной. НовоРапид® вводится подкожно в область передней брюшной стенки, бедра, плеча или ягодицы. Места инъекций в пределах одного и того же участка тела нужно регулярно менять для уменьшения риска развития липодистрофии. Как и при использовании любых других препаратов инсулина, продолжительность действия НовоРапид® зависит от дозы, места введения, интенсивности кровотока, температуры и уровня физической активности.
Подкожное введение в переднюю брюшную стенку обеспечивает более быстрое всасывание по сравнению с введением в другие места. Тем не менее, более быстрое начало действия по сравнению с растворимым человеческим инсулином сохраняется независимо от локализации места инъекции.
При необходимости, НовоРапид® может вводиться внутривенно, но только квалифицированным медицинским персоналом.
Для внутривенного введения используются инфузионные системы с препаратом НовоРапид® 100 ЕД/мл с концентрацией от 0,05 ЕД/мл до 1 ЕД/мл инсулина аспарт в 0,9% растворе хлорида натрия; 5% или 10% растворе декстрозы, содержащем 40 ммоль/л хлорида калия, с использованием полипропиленовых контейнеров для инфузий. Данные растворы стабильны при комнатной температуре в течение 24 часов. Во время инфузий инсулина необходимо постоянно контролировать уровень глюкозы крови.
Особые группы пациентов
Как и при использовании других инсулинов, у пожилых пациентов и пациентов с почечной или печеночной недостаточностью следует более тщательно контролировать концентрацию глюкозы в крови и корректировать дозу инсулина аспарт индивидуально.
Дети и подростки
Применять НовоРапид® вместо растворимого человеческого инсулина у детей предпочтительнее в том случае, когда необходимо быстрое начало действия препарата, например, когда ребенку трудно соблюдать необходимый интервал времени между инъекцией и приемом пищи.
Перевод с других препаратов инсулина
При переводе пациента с других препаратов инсулина на НовоРапид®, может потребоваться коррекция дозы НовоРапид®
и базального инсулина.
Инструкция для пациентов по использованию НовоРапид®
Перед использованием НовоРапид® Проверьте этикетку, чтобы убедиться, что выбран правильный тип инсулина.
-
Всегда проверяйте флакон, включая резиновый поршень. Не используйте, если он имеет видимые повреждения, или виден зазор между поршнем и белой полоской на флаконе. За дальнейшими указаниями обращайтесь к инструкции по использованию системы для введения инсулина.
-
Дезинфицируйте резиновую мембрану ватным тампоном, смоченным в медицинском спирте.
-
Всегда используйте новую иглу для каждой инъекции, чтобы предотвратить заражение.
Не используйте НовоРапид®, если
-
флакон или систему для введения инсулина роняли, или флакон поврежден или раздавлен, так как существует риск утечки инсулина;
-
условия хранения инсулина не соответствовали указанным, или препарат был заморожен;
-
инсулин перестал быть прозрачным и бесцветным.
НовоРапид® предназначен для подкожных инъекций или продолжительных инфузий в инсулиновой насосной системе (ППИИ). НовоРапид® также может применяться внутривенно под строгим контролем врача.
Следует всегда менять места инъекций, чтобы избежать образования липодистрофий. Лучшими местами для инъекций являются: передняя брюшная стенка, ягодицы, передняя поверхность бедра или плечо. Инсулин будет действовать быстрее, если он введен в область передней брюшной стенки. Места инфузий следует периодически менять.
НовоРапид® во флаконе используется с инсулиновыми шприцами с соответствующей шкалой в единицах действия.
Если одновременно используются препарат НовоРапид® и другой инсулин во флаконе или картридже Пенфилл®, необходимо использовать два отдельных инсулиновых шприца или две отдельные инъекционные системы для введения инсулина, по одной для каждого типа инсулина.
НовоРапид® флакон не подлежит повторному заполнению.
В качестве меры предосторожности всегда носите с собой запасную систему для введения инсулина на случай потери или повреждения Вашего НовоРапид®.
Как сделать инъекцию
-
Инсулин следует вводить под кожу. Используйте технику инъекции, рекомендованную Вашим врачом или медицинской сестрой, или следуйте инструкциям по введению инсулина, приведенным в руководстве к устройству для введения инсулина.
-
Удерживайте иглу под кожей не менее 6 секунд, чтобы быть уверенным, что вы ввели полную дозу препарата.
-
После каждой инъекции обязательно выбрасывайте иглу. В противном случае возможно вытекание жидкости, что может привести к неправильной дозировке инсулина.
Для использования в инсулиновой насосной системе для длительных инфузий
При использовании в насосной системе НовоРапид® никогда не следует смешивать с другими типами инсулина.
Следуйте инструкциям и рекомендациям врача по использованию НовоРапид® в насосной системе. Перед использованием НовоРапид® в насосной системе необходимо тщательно ознакомиться с полной инструкцией по использованию данной системы и информацией о любых действиях, которые следует предпринять в случае болезни, слишком высокого или слишком низкого содержания сахара в крови, или при неисправности системы для ППИИ.
-
Перед тем, как ввести иглу, вымойте руки и кожу в месте введения иглы с мылом, для того, чтобы избежать попадания какой-либо инфекции в месте инфузии.
-
При заполнении нового резервуара проверьте, не осталось ли больших пузырьков воздуха в шприце или трубке.
-
Замену инфузионного набора (трубки и катетера) необходимо производить в соответствии с руководством пользователя, прилагаемом к инфузионному набору.
Для обеспечения оптимальной компенсации нарушений углеводного обмена и своевременного выявления возможной неисправности инсулинового насоса, рекомендуется регулярно контролировать содержание глюкозы в крови.
Что делать, если инсулиновая насосная система не работает
В качестве меры предосторожности всегда носите с собой запасную систему для введения инсулина на случай потери или повреждения.
Меры предосторожности при использовании и утилизации
НовоРапид® следует использовать только с теми изделиями, которые совместимы с ним и обеспечивают его безопасное и эффективное функционирование.
НовоРапид® предназначен только для индивидуального использования.
НовоРапид® может использоваться в инсулиновых насосах. Трубки, внутренняя поверхность которых выполнена из полиэтилена или полиолефина, были проконтролированы и признаны пригодными для использования в насосах.
Растворы для инфузий в полипропиленовых контейнерах, приготовленные из НовоРапид® 100 ЕД/мл с концентрацией от 0,05 до 1,0 ЕД/мл инсулина аспарт в 0,9% растворе натрия хлорида, 5% растворе декстрозы или 10% растворе декстрозы, содержащем 40 ммоль/л калия хлорида, стабильны при комнатной температуре в течение 24 часов.
Несмотря на устойчивость в течение некоторого времени, определенное количество инсулина изначально абсорбируется материалом инфузионной системы.
Во время инфузии инсулина необходимо постоянно контролировать уровень глюкозы в крови.
НовоРапид® нельзя использовать, если он перестал быть прозрачным и бесцветным.
Неиспользованный препарат и прочие материалы следует утилизировать в соответствии с местными правилами.
Побочные действия
Побочные реакции, наблюдаемые у пациентов, использующих препарат НовоРапид®, являются в основном дозозависимыми и обусловлены фармакологическим эффектом инсулина.
Часто (>1/100, <1/10)
Наиболее частыми нежелательными эффектами во время лечения является гипогликемия. Частота развития гипогликемии зависит от популяции пациентов, дозы препарата и уровня гликемического контроля.
В начале лечения инсулином могут наблюдаться нарушения рефракции, отеки и реакции в местах введения (боль, покраснение, сыпь, воспаление, кровоподтеки, отек и зуд в месте инъекции). Эти реакции обычно носят переходящий характер. Быстрое улучшение контроля гликемии может быть связана с острой болевой нейропатией, которая обычно обратима. Интенсификация исулинотерапии с резким улучшением гликемического контроля может быть связана с временным ухудшением диабетической ретинопатии, в то время как долговременный улучшенный гликемический контроль снижает риск прогрессирования диабетической ретинопатии.
— гипогликемия (гипогликемия, как правило, является наиболее частым побочным эффектом; симптомы гипогликемии («холодный пот», бледность кожных покровов, повышенная утомляемость, нервозность или тремор, чувство тревоги, необычная усталость или слабость, нарушение ориентации, снижение концентрации внимания, сонливость, выраженное чувство голода, нарушение зрения, головная боль, тошнота, сердцебиение) развиваются
внезапно, тяжелая гипогликемия может приводить к потере сознания и/или судорогам, временному или необратимому нарушению функции головного мозга вплоть до летального исхода)
Редко (>1/1000, <1/100)
— липодистрофия (включая липогипертрофию, липоатрофию) может возникать в месте инъекции. Чередование мест введения в пределах одной области может уменьшить риск развития этих реакции.
— отеки (отеки могут возникать на начальной стадии инсулинотерапии. Эти симптомы обычно носят временный характер)
— аллергические реакции, крапивница, кожная сыпь (симптомы генерализованной гиперчувствительности: зуд, потливость, желудочно-кишечные расстройства, ангионевротический отек, затруднение дыхания, сердцебиение, снижение артериального давления, анафилактические реакции являются потенциально опасными для жизни)
— нарушения рефракции (нарушения рефракции могут возникать на начальной стадии инсулинотерапии, эти симптомы обычно являются временными)
— диабетическая ретинопатия (длительное улучшение контроля гликемии снижает риск прогрессирования диабетической ретинопатии, однако, интенсификация инсулинотерапии с резким улучшением контроля углеводного обмена может привести к временному ухудшению состояния диабетической ретинопатии)
— реакции в местах введения
покраснение, воспаление, кровоподтеки, припухлость и зуд в месте инъекций (могут развиваться во время лечения инсулином, реакции в местах введения могут наблюдаться чаще при лечении препаратом Левемир® Пенфилл®, нежели при введении человеческого инсулина; большинство реакций в местах введения незначительны и носят временный характер, т.е. исчезают при продолжении лечения в течение от нескольких дней до нескольких недель)
Очень редко (>1/10000, <1/1000)
— периферическая нейропатия (быстрое улучшение контроля гликемии может приводить к состоянию «острой болевой нейропатии», которая обычно является обратимой)
Противопоказания
— повышенная индивидуальная чувствительность к инсулину аспарт илилюбому из компонентов препарата
— гипогликемия
— детский возраст до 2 лет (клинические исследования на данной группе пациентов не проводились).
Лекарственные взаимодействия
Имеется ряд лекарственных средств, которые влияют на потребность в инсулине.
Гипогликемическое действие инсулина усиливают пероральные гипогликемические препараты, ингибиторы моноаминооксидазы, ингибиторы ангиотензинпревращающего фермента, ингибиторы карбоангидразы, неселективные бета-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, препараты, салицилаты.
Гипогликемическое действие инсулина ослабляют пероральные контрацептивы, глюкокортикостероиды, тиреоидные гормоны, тиазидные диуретики, гепарин, трициклические антидепрессанты, симпатомиметики, даназол, клонидин, блокаторы кальциевых каналов, диазоксид, морфин, фенитоин, никотин.
Бета-адреноблокаторы могут маскировать симптомы гипогликемии. Октреотид/ ланреотид могут как повышать, так и снижать потребность в инсулине.
Алкоголь может как усиливать, так и снижать гипогликемический эффект инсулина.
Одновременное применение препаратов группы тиазолидиндиона и препаратов инсулина
Сообщалось о случаях развития застойной сердечной недостаточности при лечении пациентов тиазолидиндионами в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития застойной сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии тиазолидиндионами и препаратами инсулина. При назначении такой комбинированной терапии необходимо проводить медицинские обследования пациентов на предмет выявления у них признаков и симптомов застойной сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности лечение тиазолидиндионами необходимо прекратить.
Несовместимость
Лекарственные средства, содержащие тиоловую или сульфитную группы, при добавлении к препарату НовоРапид® могут вызывать разрушение инсулина аспарт.
Препарат НовоРапид® не следует смешивать с другими лекарственными средствами. Исключение составляет инсулин НПХ (нейтральный протамин Хагедорна) и растворы для инфузий, описанные в разделе «Способ применения и дозы».
Особые указания
Гипогликемия развивается в случае, если введена слишком высокая доза инсулина относительно потребности организма в инсулине.
НовоРапид® нельзя вводить в случае гипогликемии или подозрения на гипогликемию. Следует принять решение о корректировке дозы после стабилизации уровня глюкозы в крови пациента.
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете типа 1, может привести к развитию гипергликемии или диабетического кетоацидоза.
Обычно симптомы-предвестники гипрегликемии развивааются постепенно в течение нескольких часов или дней. Симптомы включают жажду, увеличение частоты мочеиспускания, тошноту, рвоту, сонливость, покраснение и сухость кожи, сухость в полости рта, потерю аппетита, а также запах ацетона при дыхании. При диабете 1 типа, не пролеченные гипергликемические события в конечном итоге могут привести к диабетическому кетоацидозу, который является потенциально смертельным состоянием.
Недостаточная доза препарата или прекращение лечения, особенно при сахарном диабете типа 1, может привести к развитию гипергликемии или диабетического кетоацидоза с летальным исходом (непролеченные гипрегликемические события при диабете 1 типа). После компенсации углеводного обмена, например, при интенсифицированной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чем больные должны быть проинформированы. У пациентов с сахарным диабетом при оптимальном метаболическом контроле поздние осложнения диабета развиваются позже и прогрессируют медленнее. В связи с этим рекомендуется проводить мероприятия, направленные на оптимизацию метаболического контроля, включая мониторинг уровня глюкозы в крови.
НовоРапид® следует применять в непосредственной связи с приемом пищи. Следует учитывать высокую скорость наступления эффекта препарата при лечении пациентов, имеющих сопутствующие заболевания или принимающих лекарственные средства, замедляющие всасывание пищи. При наличии сопутствующих заболеваний, особенно инфекционной природы, потребность в инсулине, как правило, возрастает. Нарушение функции почек или печени может привести к снижению потребности в инсулине. Сопутствующие заболевания почек, печени или влияющие на функцию надпочечников, гипофиза или щитовидной железы могут потребовать изменение дозы инсулина.
Применять НовоРапид® вместо растворимого человеческого инсулина у детей следует только в том случае, когда необходимо быстрое начало действия препарата, например, когда ребенку трудно соблюдать необходимый интервал времени между инъекцией и приемом пищи.
При переводе пациента на другие типы инсулина, ранние симптомы-предвестники гипогликемии могут изменяться или становиться менее выраженными, по сравнению с таковыми при использовании предыдущего типа инсулина.
Перевод пациента на новый тип инсулина или препарат инсулина другого производителя необходимо осуществлять под строгим медицинским контролем. При изменении концентрации, типа, производителя и вида (человеческий инсулин, инсулин животного происхождения, аналог человеческого инсулина) препаратов инсулина и/или метода изготовления может потребоваться изменение дозы. Пациентам, переходящим на лечение НовоРапид®, может потребоваться увеличение частоты инъекций или изменение дозы по сравнению с дозами ранее применявшихся препаратов инсулина. При необходимости коррекции дозы, она может быть произведена уже при первом введении препарата или в течение первых недель или месяцев лечения. Кроме того, изменение дозы препарата может потребоваться при изменении диеты и при повышенных физических нагрузках. Физические упражнения, выполняемые сразу после приема пищи, могут увеличивать риск развития гипогликемии. Пропуск приема пищи или незапланированная физическая нагрузка могут привести к развитию гипогликемии.
Значительное улучшение состояния компенсации углеводного обмена может приводить к состоянию «острой болевой нейропатии», которая обычно является обратимой.
Длительное улучшение гликемического контроля снижает риск прогрессирования диабетической ретинопатии. Однако, интенсификация инсулинотерапии с резким улучшением гликемического контроля может сопровождаться временным ухудшением диабетической ретинопатии. НовоРапид содержит метакрезол, который в редких случаях может вызывать аллергические реакции.
Реакции в местах введения
Как и при введении других типов инсулина, могут возникать реакции в местах введения, включая боль, покраснение, зуд, сыпь, отек и воспаление. Непрерывное чередование мест введения в пределах определенной области помогает уменьшить или предупредить появление этих реакции. Обычно реакции исчезают в течение нескольких дней или недель. В редких случаях из-за реакций в местах введения может потребоваться прекращение введения НовоРапид®.
Комбинированное применение НовоРапид® с пиоглитазоном.
Сообщалось о случаях развития застойной сердечной недостаточности при лечении пациентов пиоглитазоном в комбинации с препаратами инсулина, особенно при наличии у таких пациентов факторов риска развития застойной сердечной недостаточности. Следует учитывать данный факт при назначении пациентам комбинированной терапии пиоглитазоном и НовоРапид®. При назначении такой комбинированной терапии необходимо проводить медицинское обследование пациентов на предмет выявления у них признаков и симптомов застойной сердечной недостаточности, увеличения массы тела и наличия отеков. В случае ухудшения у пациентов симптоматики сердечной недостаточности, лечение пиоглитазоном необходимо прекратить.
Инсулиновые антитела
Прием инсулина может привести к образованию инсулиновых антител. В редких случаях присутствие таких инсулиновых антител может потребовать корректировки инсулиновых доз для корректировки тенденции к гипер или гипогликемии.
Беременность и лактация
НовоРапид® (инсулин аспарт) можно назначать при беременности. Данные двух рандомизированных контролируемых клинических исследований (322 + 27 обследованных беременных) не выявили никакого неблагоприятного воздействия инсулина аспарт на течение беременности или здоровье плода/новорожденного по сравнению с человеческим инсулином (см. раздел «Фармакологические свойства»).
Рекомендуется тщательный контроль уровня глюкозы в крови и мониторинг беременных женщин, страдающих диабетом (диабет типа 1, диабет типа 2 или в гестационный диабет), в течение всей беременности и в период возможного наступления беременности. Потребность в инсулине, как правило, снижается в I триместре и постепенно повышается во II и III триместрах беременности. Вскоре после родов потребность в инсулине быстро возвращается к уровню, который был до беременности. Противопоказания к применению НовоРапид® во время кормления грудью отсутствуют. Инсулинотерапия кормящих матерей не представляет риска для здоровья ребенка. Однако может потребоваться корректировка дозы НовоРапид®.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами.
Способность пациентов к концентрации внимания и скорость реакции могут нарушаться во время гипогликемии и гипергликемии, что может представлять опасность в тех ситуациях, когда эти способности особенно необходимы (например, при управлении автомобилем или работе с машинами и механизмами). Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии и гипергликемии при вождении автомобиля и работе с механизмами. Это особенно важно для пациентов с отсутствием или снижением выраженности симптомов-предвестников развивающейся гипогликемии или страдающих частыми эпизодами гипогликемии. В этих случаях следует рассмотреть целесообразность выполнения подобных работ.
Передозировка
При передозировке возможно развитие гипогликемии.
Лечение:
— Легкую гипогликемию пациент может устранить сам, приняв внутрь глюкозу, сахар или богатые углеводами продукты питания. Поэтому, больным сахарным диабетом рекомендуется постоянно носить с собой сахар, сладости, печенье или напитки, содержащие сахар.
— В тяжелых случаях, при потере пациентом сознания, следует ввести глюкагон от 0,5 до 1 мг внутримышечно или подкожно (может вводить только медицинский работник). Также необходимо внутривенно ввести глюкозу в случае, если через 10-15 мин. после введения глюкагона пациент не приходит в сознание. После восстановления сознания пациенту рекомендуют принять пищу, богатую углеводами, для профилактики рецидива гипогликемии.
При развитии тяжелой гипогликемии требуется экстренная госпитализация пациента.
Форма выпуска и упаковка
Раствор для инъекций, 100 ЕД/мл.
По 10 мл препарата во флакон из стекла 1 гидролитического класса, укупоренный бромбутиловым/полиизопреновым резиновым диском, и обжатый защитным пластиковым колпачком.
На каждый флакон наклеивают этикетку самоклеящуюся.
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную пачку.
Условия хранения
Хранить при температуре от 2°С до 8°С (в холодильнике). Не замораживать.
Хранить флакон в картонной пачке для защиты от света.
После первого вскрытия: использовать в течение 4 недель при хранении при температуре не выше 30ºС. Не хранить в холодильнике.
Хранить в недоступном для детей месте!
Срок хранения
2.5 года
Не использовать после срока, указанного на этикетке флакона и упаковке.
Условия отпуска из аптек
По рецепту
Производитель
Ново Нордиск А/C
Ново Алле,
DK-2880 Багсваерд, Дания
Владелец регистрационного удостоверения
Ново Нордиск А/C, Дания
Упаковщик
Ново Нордиск А/C, Дания
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции
Представительство компании Ново Нордиск А/С в Республике Казахстан
Адрес: 050010, г. Алматы, Бизнес Центр «Кен Дала», проспект Достык, д. 38, Блок Б, Южная сторона, 8-ой этаж.
Номер телефона: +7 (727) 330 77 88
Номер факса: +7 (727) 261 08 04
Адрес электронной почты: roa-td@novonordisk.com
НовоРапид® — зарегистрированная торговая марка, принадлежащая компании Ново Нордиск А/С, Дания.
© 20XX
Ново Нордиск А/С
| 962897961477976426_ru.doc | 118 кб |
| 539199651477977625_kz.doc | 136.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Фармакологическая группа вещества Инсулин аспарт
-
Нозологическая классификация
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Инсулин аспарт
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Инсулин аспарт
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Торговые названия с действующим веществом Инсулин аспарт
Русское название
Инсулин аспарт
Английское название
Insulin aspart
Латинское название
Insulinum aspartum (род. Insulini asparti)
Фармакологическая группа вещества Инсулин аспарт
Нозологическая классификация
Фармакологическое действие
—
гипогликемическое.
Характеристика
Инсулин ультракороткого действия. Аналог человеческого инсулина, полученный методом рекомбинантной ДНК-технологии с использованием штамма Saccharomyces cerevisiae, в котором аминокислота пролин в положении B28 замещена на аспарагиновую кислоту. Молекулярная масса 5825,8.
Фармакология
Связывается с рецепторами к инсулину на мышечных и жировых клетках. Снижение уровня глюкозы в крови обусловлено усилением ее внутриклеточного транспорта, повышением утилизации тканями, снижением скорости продукции глюкозы в печени. Повышает интенсивность липогенеза и гликогеногенеза, синтеза белка. После п/к инъекции действие наступает в течение 10–20 мин, достигает максимума через 1–3 ч и продолжается 3–5 ч.
Быстро всасывается из подкожно-жировой клетчатки. Замещение аминокислоты пролин в положении B28 на аспарагиновую кислоту уменьшает тенденцию молекул к образованию гексамеров, что увеличивает скорость всасывания (по сравнению с обычным человеческим инсулином). После п/к введения Tmax составляет 40–50 мин, связывание с белками очень низкое (0–9%), T1/2 — 81 мин.
Канцерогенность, мутагенность, влияние на фертильность
Стандартных двухгодичных исследований оценки потенциальной канцерогенности инсулина аспарт не проведено. В одногодичных исследованиях онкогенности крысам Sprague-Dawley п/к вводили инсулин аспарт в дозах 10, 50 и 200 единиц/кг (примерно в 2, 8 и 32 раза выше дозы для человека при п/к введении). Полученные результаты показали, что при дозе 200 единиц/кг у самок частота опухолей молочной железы выше, по сравнению с контролем (эти наблюдения не отличаются значимо от полученных в случае применения обычного человеческого инсулина). Значимость полученных данных для человека неизвестна.
Не выявлено мутагенноcти инсулина аспарт в ряде генотоксических тестов (в т.ч. тест Эймса, тест генных мутаций на клетках мышиной лимфомы, тест на хромосомные аберрации на культуре клеток лимфоцитов человека), а также in vivo в микроядерном тесте у мышей и ex vivo в UDS-тесте (внепланового синтеза ДНК) на гепатоцитах крыс.
Не отмечалось нарушения фертильности у самцов и самок крыс при п/к дозах инсулина аспарт, примерно в 32 раза превышающих рекомендуемую дозу для п/к введения у человека.
Применение вещества Инсулин аспарт
Сахарный диабет.
Противопоказания
Гиперчувствительность, гипогликемия.
Ограничения к применению
Детский возраст до 6 лет (безопасность и эффективность применения не определены).
Применение при беременности и кормлении грудью
В исследованиях на животных показано, что при введении как инсулина аспарт, так и обычного человеческого инсулина в дозах, превышающих рекомендуемую дозу для п/к введения у человека примерно в 32 раза (крысы) и 3 раза (кролики), оба инсулина вызывали пред- и постимплантационные потери, а также висцеральные/скелетные аномалии.
Адекватных и строго контролируемых исследований у беременных женщин не проведено. Следует вести тщательное наблюдение и контролировать уровень глюкозы в крови в период возможного наступления беременности и в течение всего ее срока как у пациенток с сахарным диабетом, так и у женщин с гестационным диабетом в анамнезе. Потребность в инсулине, как правило, снижается в I триместре беременности и повышается во II–III триместах. Во время родов и непосредственно после них потребность в инсулине может резко снизиться.
Категория действия на плод по FDA — C.
Опыт клинического применения в период лактации ограничен. Следует применять с осторожностью (неизвестно, экскретируется ли инсулина аспарт в грудное молоко).
Побочные действия вещества Инсулин аспарт
Гипогликемия (слабость, «холодный» пот, бледность кожных покровов, сердцебиение, нервозность, тремор, чувство голода, парестезии в кистях рук, ногах, губах, языке, головная боль, сонливость, неуверенность движений, нарушение речи и зрения, депрессия), транзиторные отеки, транзиторное обратимое нарушение рефракции глаза, обострение диабетической ретинопатии, острая болевая нейропатия, генерализованные аллергические реакции; местные реакции: гиперемия, отек и зуд в месте инъекции, липодистрофия в месте инъекции.
Генерализованные жизнеугрожающие аллергические реакции, включая анафилаксию, могут проявляться при применении инсулинов, в т.ч. и инсулина аспарт, сыпью по всему телу с зудом, затруднением дыхания, артериальной гипотензией, тахикардией, повышенным потоотделением.
Взаимодействие
Фармацевтически несовместим с растворами других ЛС. Гипогликемическое действие усиливают пероральные гипогликемические ЛС, сульфаниламиды, ингибиторы МАО (в т.ч. фуразолидон, прокарбазин, селегилин), ингибиторы карбоангидразы, ингибиторы АПФ, анаболические стероиды (в т.ч. станозолол, оксандролон, метандростенолон), андрогены, бромокриптин, тетрациклины, дизопирамид, фибраты, флуоксетин, кетоконазол, мебендазол, теофиллин, циклофосфамид, фенфлурамин, пиридоксин, хинидин, хинин, хлорохинин, этанол и этанолсодержащие ЛС. Гипогликемическое действие ослабляют глюкокортикоиды, глюкагон, соматропин, тиреоидные гормоны, эстрогены, прогестогены (например пероральные контрацептивы), тиазидные диуретики, БКК, гепарин, сульфинпиразон, симпатомиметики (например эпинефрин, сальбутамол, тербуталин), изониазид, производные фенотиазина, даназол, трициклические антидепрессанты, диазоксид, морфин, никотин, фенитоин.
Бета-адреноблокаторы, клонидин, соли лития, резерпин, салицилаты, пентамидин — могут как усиливать, так и ослаблять гипогликемическое действие инсулина.
Передозировка
Симптомы: гипогликемия, гипогликемическая кома, судороги.
Лечение: легкую гипогликемию больной может устранить самостоятельно, приняв внутрь сахар или богатые легкоусвояемыми углеводами продукты питания. П/к, в/м или в/в вводят глюкагон или в/в гипертонический раствор декстрозы. При развитии гипогликемической комы в/в струйно вводят 20–40 мл (до 100 мл) 40% раствора декстрозы до тех пор, пока больной не выйдет из коматозного состояния. После восстановления сознания рекомендуется пероральный прием углеводов для профилактики рецидива гипогликемии.
Способ применения и дозы
П/к, в область брюшной стенки, бедра, плеча или ягодицы, непосредственно перед приемом пищи (прандиально) или сразу после еды (постпрандиально). Места инъекций в пределах одного и того же участка тела нужно регулярно менять. Дозу и режим введения определяют индивидуально. Индивидуальная потребность в инсулине обычно составляет 0,5–1 ЕД/кг/сут, из которых 2/3 приходится на прандиальный (перед приемом пищи) инсулин, 1/3 — на базальный (фоновый) инсулин.
В/в (при необходимости), с использованием инфузионных систем. В/в введение может проводиться только квалифицированным медицинским персоналом.
Меры предосторожности
Недостаточная доза или прерывание лечения (особенно при сахарном диабете типа 1) может привести к гипергликемии и диабетическому кетоацидозу. При наличии сопутствующих заболеваний, особенно инфекционной природы, потребность в инсулине, как правило, увеличивается, а при нарушении функции почек или печени — уменьшается. Перевод больного на новый тип или торговую марку инсулина нужно осуществлять под строгим медицинским контролем. При использовании инсулина аспарт может потребоваться большее число инъекций в сутки или изменение дозы по сравнению с таковыми при использовании обычных инсулинов. Возникновение потребности в коррекции дозы может произойти уже при первом введении или в первые несколько недель или месяцев после перевода. После компенсации углеводного обмена у больных могут измениться типичные для них симптомы-предвестники гипогликемии, о чем их следует проинформировать. Пропуск приема пищи или незапланированная физическая нагрузка могут привести к гипогликемии.
Интенсификация инсулинотерапии с резким улучшением гликемического контроля может сопровождаться временным ухудшением течения диабетической ретинопатии и развитием острой болевой нейропатии. Длительное улучшение гликемического контроля снижает риск диабетической ретинопатии и нейропатии.
В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятии другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (может развиться гипогликемия, особенно у пациентов со слабовыраженными или отсутствующими симптомами-предвестниками гипогликемии или ее частыми эпизодами).
Торговые названия с действующим веществом Инсулин аспарт
| Торговое название | Цена за упаковку, руб. |
|---|---|
| НовоРапид® ФлексПен® |
от 1510.00 до 1878.00 |
| Фиасп® |
от 1895.00 до 1895.00 |