Тебериф® (Teberif) инструкция по применению
📜 Инструкция по применению Тебериф®
💊 Состав препарата Тебериф®
✅ Применение препарата Тебериф®
📅 Условия хранения Тебериф®
⏳ Срок годности Тебериф®
Описание лекарственного препарата
Тебериф®
(Teberif)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2021 года.
Дата обновления: 2020.11.20
Владелец регистрационного удостоверения:
Контакты для обращений:
БИОКАД АО
(Россия)
Код ATX:
L03AB07
(Интерферон бета-1a)
Лекарственные формы
| Тебериф® |
Р-р д/п/к введения 22 мкг/0.5 мл: шприцы 3 или 12 шт. рег. №: ЛП-004137 |
|
|
Р-р д/п/к введения 44 мкг/0.5 мл: шприцы 3 или 12 шт. рег. №: ЛП-004137 |
Форма выпуска, упаковка и состав
препарата Тебериф®
Раствор для п/к введения в виде прозрачной и бесцветной жидкости.
Вспомогательные вещества: лизина гидрохлорид — 27.4 мг, полисорбат 20 — 0.05 мг, натрия ацетата тригидрат — 0.272 мг, уксусная кислота ледяная — до pH 4.2, вода д/и — до 1 мл.
0.5 мл — шприцы бесцветного стекла (1) — упаковки контурные ячейковые (3) — коробки картонные.
0.5 мл — шприцы бесцветного стекла (1) — упаковки контурные ячейковые (12) — коробки картонные.
Раствор для п/к введения в виде прозрачной и бесцветной жидкости.
Вспомогательные вещества: лизина гидрохлорид — 27.4 мг, полисорбат 20 — 0.05 мг, натрия ацетата тригидрат — 0.272 мг, уксусная кислота ледяная — до pH 4.2, вода д/и — до 1 мл.
0.5 мл — шприцы бесцветного стекла (1) — упаковки контурные ячейковые (3) — коробки картонные.
0.5 мл — шприцы бесцветного стекла (1) — упаковки контурные ячейковые (12) — коробки картонные.
Фармакологическое действие
Интерфероны относятся к группе эндогенных гликопротеинов, обладающих иммуномодулирующими, противовирусными и антипролиферативными свойствами. Белковая структура препарата Тебериф® (интерферон бета-1а человеческий рекомбинантный) представляет собой природную аминокислотную последовательность интерферона бета человека, полученную методом генной инженерии с использованием культуры клеток яичника китайского хомячка и, следовательно, является гликозилированным, как и природный, белком.
Независимо от способа введения, изменения фармакодинамического эффекта связывают с терапией препаратом Тебериф®. После однократной дозы внутриклеточная и сывороточная активность 2’,5’-олигоаденилат-синтетазы (2’,5’OAS) и сывороточная концентрация бета-2-микроглобулина и неоптерина повышаются в течение 24 ч и затем в течение 2 дней начинают снижаться. При п/к и в/м введении ответ на введение препарата Тебериф® полностью идентичен. После 4 последовательных п/к инъекций, повторяющихся каждые 48 ч, биологический ответ остается повышенным без признаков привыкания.
П/к введение интерферона бета-1а здоровым добровольцам и пациентам с рассеянным склерозом повышает уровень маркеров биологического ответа (активность 2′,5′-олигоаденилат-синтетазы, концентрация неоптерина и бета-2-микроглобулина в плазме). Время достижения Cmax после однократного п/к введения препарата Тебериф® составляет от 24 до 48 ч для неоптерина, бета-2-микроглобулина и 2’,5’OAS, 12 ч для MXI и 24 ч для олигоаденилат-синтетазы 1 (OAS1) и олигоаденилат-синтетазы 2 (OAS2). Подобные пики концентраций для большинства этих маркеров наблюдаются после первого и шестого введений.
Механизм действия препарата Тебериф® в организме больных рассеянным склерозом до конца не изучен. Показано, что препарат способствует ограничению повреждений ЦНС (демиелинизация), лежащих в основе заболевания.
Данные клинических исследований
Первый эпизод демиелинизации
В двухлетнем контролируемом клиническом исследовании интерферон бета-1а в рекомендуемой дозе продемонстрировал эффективность при лечении пациентов с первым эпизодом демиелинизации, предположительно в результате рассеянного склероза. У пациентов, включенных в исследование, отмечалось как минимум 2 асимптомных очага на Т2-взвешенных МРТ изображениях размером не менее 3 мм, причем хотя бы один из очагов был овальной формы, перивентрикулярным или инфратенториальным. Другие заболевания, которые могли лучше объяснить симптоматику пациента, чем диагноз рассеянного склероза, были исключены. Было установлено, что интерферон бета-1а 44 мкг при приеме 3 раза в неделю задерживал прогрессирование заболевания у пациентов с первым эпизодом демиелинизации. Снижение риска прогрессирования заболевания составило 52% по сравнению с плацебо. Данные эффективности интерферона бета-1а при приеме 44 мкг 3 раза в неделю приведены ниже.
Ремиттирующий рассеянный склероз
Безопасность и эффективность интерферона бета-1а были оценены у пациентов с ремиттирующим рассеянным склерозом при дозах в диапазоне 11-44 мкг (2-12 млн. ME), вводимых п/к 3 раза в неделю. Было показано, что в дозе 44 мкг интерферон бета-1а снижает частоту (30% в течение 2 лет) и тяжесть обострений у пациентов с двумя и более обострениями в течение последних 2 лет и с оценкой от 0 до 5 по расширенной шкале оценки степени инвалидизации (EDSS) перед началом лечения. Доля пациентов с подтвержденным прогрессированием инвалидизации уменьшилась с 39% (плацебо) до 30% и 27% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг соответственно). Через 4 года среднее снижение числа обострений составляло 22% и 29% у пациентов, получавших 22 мкг интерферона бета-1а и 44 мкг интерферона бета-1а соответственно, по сравнению с группой пациентов, получавших в течение 2 лет плацебо, а затем — интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг.
В трехгодичном исследовании у пациентов с вторично-прогрессирующим растерянным склерозом (3-6.5 баллов по шкале EDSS) с достоверным прогрессированием инвалидизации в течение предшествующих 2 лет и отсутствием обострений в течение предшествующих 8 нед., интерферон бета-1а не оказывал существенного влияния на инвалидизацию, однако частота обострений снизилась на 30%. При выделении двух групп пациентов (имевших или не имевших обострения заболевания за последние 2 года) в группе «без обострений» не было обнаружено влияния препарата на прогрессирование инвалидизации, тогда как в группе «с обострениями» доля пациентов с прогрессированием в конце исследования снизилась с 70% (плацебо) до 57% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг).
Первично-прогрессирующий рассеянный склероз
Действие препарата при первично-прогрессирующем рассеянном склерозе не изучалось.
Фармакокинетика
Всасывание и распределение
После в/в введения здоровым добровольцам концентрация интерферона бета-1a подвергается резкому экспоненциальному уменьшению, причем уровни препарата в сыворотке крови оказываются пропорциональными дозе.
После повторных п/к инъекций препарата Тебериф® в дозе 22 мкг и 44 мкг Cmax интерферона бета-1а наблюдаются через 8 ч, но значения сильно варьируют.
Метаболизм и выведение
Интерферон бета-1а подвергается метаболизму и выводится печенью и почками.
После повторных п/к инъекций препарата Тебериф® здоровым добровольцам основные фармакокинетические параметры (AUC и Cmax) возрастают пропорционально увеличению дозы от 22 мкг до 44 мкг. Т1/2 составляет от 50 до 60 ч, что коррелирует с процессом кумуляции, наблюдаемым после многократного введения.
Показания препарата
Тебериф®
- лечение пациентов с первым эпизодом демиелинизации, в основе которого лежит острый воспалительный процесс, если иные диагнозы были исключены, и если существует высокий риск развития клинически достоверного рассеянного склероза;
- лечение пациентов с ремиттирующим рассеянным склерозом, у которых заболевание характеризуется двумя или более обострениями за предшествующие два года.
Эффективность не была продемонстрирована у пациентов с вторично-прогрессирующим рассеянным склерозом в отсутствии обострений.
Режим дозирования
Препарат вводят п/к. Лечение следует начинать под контролем врача-специалиста, имеющего опыт лечения данного заболевания. Лечение препаратом Тебериф® с целью предотвращения развития тахифилаксии и снижения нежелательных реакций рекомендуется начинать с дозы 8.8 мкг и затем в течение 4 недель дозу увеличивать до рекомендуемой дозы согласно приведенной ниже схеме.
При назначении препарата Тебериф® в дозе 44 мкг, начиная с 5-й недели вводится 0.5 мл препарата в данной дозировке. Для уменьшения гриппоподобных симптомов, связанных с назначением препарата Тебериф® перед введением и в течение 24 ч после каждой инъекции, рекомендуется назначать жаропонижающее средство (антипиретик).
Первый эпизод демиелинизации
Доза интерферона бета-1а для пациентов с первым эпизодом демиелинизации составляет 44 мкг 3 раза в неделю п/к.
Ремиттирующий рассеянный склероз
Взрослым и подросткам старше 16 лет рекомендуемая доза препарата обычно составляет 44 мкг 3 раза в неделю. В дозе 22 мкг 3 раза в неделю препарат Тебериф® назначается тем пациентам, которые, по мнению лечащего врача, недостаточно хорошо переносят высокую дозу.
Безопасность и эффективность применения интерферона бета-1а для п/к применения у подростков в возрасте 12-16 лет до сих пор окончательно не установлена. Данные по безопасности, приведенные в разделе «Побочное действие», не дают возможности дать рекомендации по режиму дозирования для этой группы пациентов. Тем не менее, опубликованные данные позволяют предположить, что профиль безопасности интерферона бета-1а у подростков от 12 до 16 лет, получающих п/к инъекции препарата в дозе 22 мкг 3 раза в неделю, аналогичен таковому у взрослых.
Безопасность и эффективность интерферона бета-1а у детей в возрасте до 12 лет не установлена, имеются лишь ограниченные сведения, поэтому препарат Тебериф® не следует применять в этой возрастной группе.
Препарат следует применять в одно и то же время (желательно вечером), в определенные дни недели, с интервалом не менее 48 ч.
Препарат Тебериф® можно использовать только в том случае, если раствор препарата прозрачен или слегка опалесцирует и, если в нем не содержится посторонних частиц.
В настоящее время нет четких рекомендаций о том, как долго следует проводить лечение. Рекомендуется оценивать состояние пациентов, как минимум, каждые 2 года в течение первых 4 лет лечения препаратом Тебериф®, решение о более длительной терапии должно приниматься лечащим врачом индивидуально для каждого пациента.
Информация, которую необходимо довести до пациента
Чтобы применение препарата Тебериф® было эффективным и безопасным, следует:
- применять препарат Тебериф® только под наблюдением опытного врача;
- для предупреждения некроза необходимо внимательно прочитать инструкцию и следовать ее указаниям. При возникновении реакции в месте инъекции следует проконсультироваться с врачом;
- не следует менять дозы препарата без согласования с врачом;
- не следует прерывать лечение без согласования с врачом;
- необходимо предупредить врача, если имеется непереносимость каких-либо лекарственных препаратов;
- в ходе лечения необходимо сообщать врачу о любых нарушениях состояниях здоровья.
Самостоятельное п/к введение препарата
Поскольку препарат Тебериф® выпускается в виде предварительно заполненного шприца для п/к введения, пациент может безопасно его применять в домашних условиях, как самостоятельно, так и при помощи родственников и друзей. Если возможно, первая инъекция должна быть сделана под наблюдением квалифицированного медицинского работника.
Перед применением препарата Тебериф® необходимо внимательно прочитать следующую инструкцию:
- Выбрать удобное время проведения инъекции. Инъекции желательно делать вечером перед сном.
- Перед введением препарата тщательно вымыть руки водой с мылом.
- Взять одну контурную ячейковую упаковку с заполненным шприцем из картонной пачки, которая должна храниться в холодильнике, и выдержать ее при комнатной температуре в течение нескольких минут для того, чтобы температура препарата сравнялась с температурой окружающего воздуха.
В случае появления конденсата на поверхности шприца следует подождать еще несколько минут до тех пор, пока конденсат не испарится.
В случае невозможности хранения невскрытого шприца в холодильнике, допустимо однократное хранение в защищенном от света месте не более 30 суток при температуре не выше 25°С. Дату начала хранения при комнатной температуре следует отмечать на упаковке.
- Перед использованием следует осмотреть раствор в шприце. При наличии взвешенных частиц или изменении цвета раствора, или повреждении шприца препарат не следует применять. Если появилась пена, что бывает когда шприц встряхивают или сильно покачивают, следует подождать, пока осядет пена.
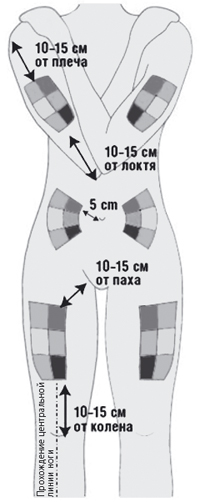
- Выбрать область тела для инъекции. Препарат Тебериф® вводится в подкожную жировую клетчатку (жировой слой между кожей и мышечной тканью), поэтому следует выбирать места с рыхлой клетчаткой вдали от мест растяжения кожи, нервов, суставов и сосудов (на рис. 1 и 2 указаны рекомендованные области для инъекций):
- бедра (передняя поверхность бедер кроме паха и колена);
- живот (кроме срединной линии и околопупочной области);
- наружная поверхность плеч;
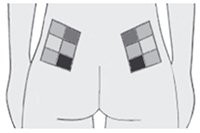
- ягодицы (верхний наружный квадрант).
Рис. 1. Схема расположения мест инъекций.
Рис. 2. Схема расположения мест инъекций в ягодичную область.
Не следует выбирать для инъекции болезненные точки, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками.
Каждый раз следует выбирать новое место для укола, так можно уменьшить неприятные ощущения и боль на участке кожи в месте инъекции. Внутри каждой инъекционной области есть много точек для укола. Следует постоянно менять точки инъекций внутри конкретной области.
- Подготовка к инъекции.
Взять подготовленный шприц в рабочую руку. Снять защитный колпачок с иглы.
- Количество раствора препарата Тебериф®, которое нужно ввести при проведении инъекции, зависит от рекомендованной врачом дозы. Не следует хранить излишки препарата, оставшиеся в шприце, для повторного использования.
В зависимости от дозы, которую прописал врач, может потребоваться удалить лишний объем раствора препарата из шприца. В случае такой необходимости следует медленно и аккуратно нажимать на поршень шприца для удаления лишнего количества раствора. Следует давить на поршень до тех пор, пока поршень не дойдет до необходимой метки на этикетке шприца.
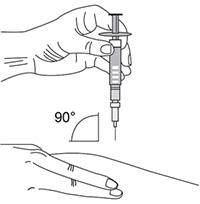
- Следует предварительно продезинфицировать участок кожи, куда будет введен препарат Тебериф®. Когда кожа обсохнет, слегка собрать кожу в складку большим и указательным пальцами (рис. 3).
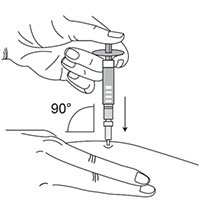
- Располагая шприц перпендикулярно месту инъекции, ввести иглу в кожу под углом 90° (рис. 4). Рекомендуемая глубина введения иглы составляет 6 мм от поверхности кожи. Глубина подбирается в зависимости от типа телосложения и толщины подкожной жировой клетчатки. Следует вводить препарат, равномерно нажимая на поршень шприца вниз до конца (до его полного опустошения).
Рис. 3.
Рис. 4.
- Удалить шприц с иглой движением вертикально вверх, сохраняя прежний угол наклона.
- К месту инъекции можно приложить сухой стерильный ватный шарик. При необходимости можно заклеить пластырем. Не рекомендуется растирать или массировать место инъекции после введения препарата.
- Использованные шприцы следует выбрасывать только в специально отведенное место, недоступное для детей.
- Если пациент забыл ввести препарат, необходимо сделать инъекцию немедленно, как только он вспомнит об этом. Следующую инъекцию производят через 48 ч. Не допускается вводить двойную дозу препарата.
Не следует прекращать применение препарата Тебериф® без консультации с врачом.
Что делать в случае передозировки препаратом Тебериф®
Ни одного случая передозировки до настоящего времени не описано. Однако в случае повышения дозы (увеличения одноразового объема и частоты приема в неделю) пациенту следует немедленно сообщить об этом врачу.
Коррекция режима дозирования
При превышении ВГН содержания АЛТ дозу препарата Тебериф® необходимо снизить и постепенно увеличивать после нормализации активности АЛТ.
Временное снижение дозы препарата может потребоваться также при значительной выраженности гриппоподобных симптомов.
Применение у особых групп пациентов
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, признаками заболевания печени, признаками злоупотребления алкоголем, уровнем АЛТ в 2.5 раза превышающим ВГН. Терапию следует прекратить при появлении желтухи или других симптомов нарушения функции печени.
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Побочное действие
Самые частые нежелательные реакции, наблюдающиеся при лечении интерфероном бета-1a, связаны с возникновением гриппоподобного синдрома. Гриппоподобные симптомы бывают особенно выраженными в начале лечения и ослабевают по частоте по мере продолжения лечения. Примерно у 70% пациентов, принимающих интерферон бета-1а, можно ожидать появления типичного гриппоподобного синдрома в первые 6 месяцев после начала лечения. Примерно у 30% пациентов возникают реакции в месте инъекции, преимущественно умеренное раздражение или эритема.
Асимптоматическое повышение лабораторных показателей печеночной функции и снижение количества лейкоцитов также являются частыми. Ниже представлены нежелательные реакции, которые наблюдались как в клинических исследованиях, так и в пострегистрационный период (помечены *) у пациентов с рассеянным склерозом.
Нежелательные реакции перечислены в соответствии с их частотой и системно-органным классом. Для обозначения частоты нежелательных реакций используется общепринятая классификация: очень часто (≥1/10 случаев), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000), очень редко (<1/10000), частота неизвестна (не может быть установлена на основании полученных данных).
Со стороны системы кроветворения: очень часто — нейтропения, лимфопения, лейкопения, тромбоцитопения, анемия; редко — тромботическая микроангиопатия, включающая тромботическую тромбоцитопеническую пурпуру/гемолитико-уремический синдром* (является класс-эффектом интерферонов; см. раздел «Особые указания»), панцитопения*.
Со стороны иммунной системы: редко — анафилактические реакции*.
Со стороны эндокринной системы: нечасто — нарушение функции щитовидной железы, наиболее часто проявляющееся в виде гипо- или гипертиреоза (см. раздел «Особые указания»).
Со стороны пищеварительной системы: часто — диарея, рвота, тошнота.
Со стороны печени и желчевыводящих путей: очень часто — бессимптомное повышение активности трансаминаз в крови; часто — значительное повышение активности трансаминаз в крови; нечасто — гепатит (с желтухой или без нее)*; редко — печеночная недостаточность*, аутоиммунный гепатит*.
Психические нарушения: часто — депрессия, бессонница; редко — суицидальные попытки (см. раздел «Особые указания»).
Со стороны нервной системы: очень часто — головная боль; нечасто — судороги* (см. раздел «Особые указания»); частота неизвестна — преходящие неврологические симптомы (гипестезия, мышечные спазмы, парестезия, затруднения при ходьбе, ригидность мышц), которые могут имитировать обострение рассеянного склероза*.
Со стороны органа зрения: нечасто — поражение сосудов сетчатки (т.е. ретинопатия, «ватные пятна» на сетчатке, обструкция артерии или вены сетчатки)*.
Со стороны сердечно-сосудистой системы: нечасто — тромбоэмболия*.
Со стороны дыхательной системы: нечасто — одышка*; частота неизвестна — артериальная легочная гипертензия (класс-эффект, см. ниже «Артериальная легочная гипертензия»).
Со стороны кожи и подкожных тканей: часто — зуд, сыпь, эритематозная сыпь, макуло-папулезная сыпь, алопеция*; нечасто — крапивница*; редко — отек Квинке*, многоформная эритема*, кожная реакция, напоминающая многоформную эритему*, синдром Стивенса-Джонсона*.
Со стороны костно-мышечной системы: часто — миалгия, артралгия; редко — лекарственная красная волчанка*.
Со стороны мочевыделительной системы: редко — нефротический синдром*, гломерулосклероз* (см. раздел «Особые указания»).
Общие расстройства и нарушения в месте введения: очень часто — воспаление в месте инъекции, реакции в месте инъекции (например, кровоподтек, припухлость в месте инъекции, отек, покраснение), гриппоподобные симптомы; часто — боль в месте введения, утомляемость, озноб, лихорадка; нечасто — некроз в месте инъекции, припухлость в месте инъекции, абсцесс в месте инъекции, инфицирование места инъекции*, усиление потоотделения*; редко — флегмона в месте инъекции*.
Дети
Отдельные клинические или фармакокинетические исследования для детей и подростков не проводились. Однако опубликованные данные по применению интерферона бета-1а у подростков в возрасте от 12 до 16 лет, получавших интерферон бета-1а в дозе 22 мкг 3 раза в неделю п/к, позволяют предположить, что профиль безопасности препарата Тебериф® в этой группе аналогичен таковому у взрослых пациентов.
Класс-эффекты
Применение интерферонов связано с потерей аппетита, головокружениями, беспокойством, аритмией, расширением кровеносных сосудов и учащенным сердцебиением, меноррагией и метроррагией.
В ходе лечения интерфероном бета может происходить усиленное образование антител.
Артериальная легочная гипертензия
На фоне применения препаратов интерферона бета регистрировались случаи артериальной легочной гипертензии. Данные случаи регистрировались на разных этапах лечения, в т.ч. через несколько лет после начала терапии интерфероном бета.
Пациенту необходимо информировать врача о любых перечисленных выше нежелательных реакциях, а также о тех, которые не указаны в данной инструкции. При сохранении нежелательных реакций в течение длительного времени или в случае развития тяжелых нежелательных реакций по усмотрению врача допускается временное снижение дозы препарата или прерывание лечения.
Противопоказания к применению
- повышенная чувствительность к природному или рекомбинантному интерферону бета, к другим компонентам препарата;
- инициация терапии во время беременности;
- тяжелые депрессивные нарушения и/или суицидальные идеи;
- возраст до 12 лет.
Применение при беременности и кормлении грудью
Женщины с детородным потенциалом
Женщины детородного возраста должны пользоваться эффективными средствами контрацепции. Учитывая потенциальную опасность для плода, пациентки, планирующие беременность или забеременевшие на фоне лечения, должны обязательно сообщить об этом лечащему врачу для решения об отмене препарата. Для пациенток с высокой частотой рецидивов перед началом лечения необходимо сопоставить риск возникновения тяжелого рецидива в случае прекращения приема препарата из-за наступления беременности с возможным повышением вероятности самопроизвольного аборта.
Беременность
Начинать лечение препаратом Тебериф® в период беременности противопоказано. Имеющиеся данные указывают на возможное повышение риска самопроизвольного аборта.
Период грудного вскармливания
Данные об экскреции препарата Тебериф® с грудным молоком отсутствуют. Учитывая вероятность развития серьезных побочных реакций у новорожденных, следует сделать выбор между отменой препарата Тебериф® и прекращением грудного вскармливания.
Применение при нарушениях функции печени
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, признаками заболевания печени, повышением активности АЛТ в 2.5 раза превышающим ВГН.
Применение при нарушениях функции почек
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью.
Применение у детей
Противопоказано применение препарата в возрасте до 12 лет.
Особые указания
Пациентов следует проинформировать относительно наиболее частых побочных действий, связанных с приемом интерферона бета, включая гриппоподобные симптомы (см. раздел «Побочное действие»), которые бывают особенно выраженными в начале лечения и уменьшаются по частоте и выраженности по мере продолжения лечения.
Тромботическая микроангиопатия (ТМА)
Имеется информация о случаях тромботической микроангиопатии, которые проявлялись в виде тромботической тромбоцитопенической пурпуры или гемолитико-уремического синдрома, включая случаи с летальным исходом. Такие случаи регистрировались в различные периоды времени, от нескольких недель до нескольких лет после начала лечения интерфероном бета-1а. Рекомендуется проводить мониторинг ранних симптомов, таких как тромбоцитопения, вновь возникающие случаи гипертензии, лихорадка, нарушения со стороны ЦНС (например, спутанное сознание, парез) и снижение почечной функции. Лабораторные данные при предположительном диагнозе ТМА включают снижение числа тромбоцитов, увеличение сывороточной активности ЛДГ, вызванное гемолизом, и обнаружение шизоцитов (фрагменты эритроцитов) в мазке крови. Если наблюдаются клинические признаки ТМА, рекомендуется провести определение содержания тромбоцитов, сывороточной ЛДГ, взять мазок крови и оценить почечную функцию. Если диагноз ТМА подтверждается, требуется немедленное лечение (может потребоваться переливание плазмы) и прекращение лечения интерфероном бета-1а.
Депрессия и суицидальные идеи
Препарат Тебериф® должен с осторожностью назначаться пациентам, находящимся или перенесшим депрессивные состояния. Депрессивные и суицидальные состояния с повышенной частотой наблюдаются в группе пациентов, страдающих рассеянным склерозом и принимающих интерферон.
Пациентов необходимо предупредить о том, что им следует немедленно сообщить о любых симптомах депрессии и/или появлении суицидальных идей лечащему врачу. Лечение больных, страдающих депрессией, препаратом Тебериф® должно проходить в условиях пристального контроля и предоставления им необходимой помощи. В ряде случаев может встать вопрос о прекращении лечения препаратом.
Судорожный синдром
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с эпилептическими припадками в анамнезе, особенно если течение этого заболевания не полностью контролируется противоэпилептическими препаратами.
Сердечно-сосудистые заболевания
На первых этапах лечения препаратом Тебериф® необходимо строгое наблюдение за пациентами, страдающими сердечно-сосудистыми заболеваниями, такими как стенокардия, застойная сердечная недостаточность и нарушения ритма. Это наблюдение должно быть направлено на своевременное выявление возможного ухудшения состояния. При заболеваниях сердца гриппоподобные симптомы, связанные с терапией интерфероном бета-1а, могут оказаться серьезной нагрузкой для больных.
Некроз в месте инъекций
Имеются единичные сообщения о некрозе в месте инъекций. Чтобы свести до минимума риск развития некроза, необходимо строгое соблюдение правил асептики при выполнении инъекции и смена места введения после каждой инъекции. Необходимо регулярно оценивать технику самостоятельного введения препарата пациентами, особенно при возникновении реакций в месте инъекций. Если отмечается повреждение кожи с отеком и выделением жидкости в месте инъекции, пациенту необходимо обратиться к врачу прежде, чем продолжать введение препарата. При множественных повреждениях кожи следует отменить препарат до их заживления. При единичном поражении возможно продолжение терапии препаратом Тебериф®, при условии, что поражение выражено умеренно.
Нарушение функции печени
В клинических испытаниях продемонстрировано бессимптомное повышение активности печеночных трансаминаз, особенно АЛТ, а у 1-3% пациентов содержание печеночных трансаминаз превышало ВГН более чем в 5 раз. При отсутствии клинической симптоматики необходимо контролировать активность АЛТ в плазме до начала применения интерферона бета-1а, в 1-й, 3-й и 6-й месяцы от его начала, а также периодически в ходе дальнейшего лечения. Необходимо снизить дозу препарата, если активность АЛТ превысит в 5 раз ВГН, и постепенно увеличивать дозу после ее нормализации. Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, с признаками заболевания печени, с признаками злоупотребления алкоголем, активностью АЛТ в 2.5 раза превышающей ВГН. Терапию препаратом Тебериф® необходимо прекратить при появлении желтухи или других клинических симптомов нарушения функции печени.
Тебериф®, как и другие интерфероны бета, потенциально может вызывать тяжелое поражение печени, в т.ч. острую печеночную недостаточность. Тяжелые нарушения функции печени главным образом возникают в первые 6 месяцев терапии. Механизм этих состояний неизвестен, специфические факторы риска не выявлены.
Нарушение функции почек и мочевыводящей системы
В ходе лечения интерфероном бета-1а и другими интерферонами бета могут иметь место случаи нефротического синдрома с различными нефропатиями, включая очаговый сегментарный гломерулосклероз (ОСГС), мембранопролиферативный гломерулонефрит и мембранную гломерулопатию. Случаи имели место как в процессе лечения, так и через несколько лет после его завершения. Рекомендуется проводить периодический мониторинг ранних признаков или симптомов (например, отеки, протеинурия или нарушение функции почек) особенно у пациентов с высоким риском возникновения заболеваний почек. Нефротический синдром требует немедленного лечения и прекращения приема препарата Тебериф®.
Нарушение лабораторных показателей
В дополнение к лабораторным анализам, которые всегда проводятся пациентам с рассеянным склерозом, рекомендуется в 1-й, 3-й и 6-й месяцы с момента начала терапии препаратом Тебериф®, а также периодически, при отсутствии клинической симптоматики, в ходе дальнейшего лечения определять общий клинический анализ крови с лейкоцитарной формулой, содержание тромбоцитов, а также проводить биохимическое исследование крови, включая функциональные пробы печени.
Заболевания щитовидной железы
У пациентов, получающих интерферон бета-1а, иногда могут развиваться или усугубляться имеющиеся патологические изменения щитовидной железы. Рекомендуется проводить исследование функции щитовидной железы непосредственно до начала лечения и, при выявлении нарушений, каждые 6-12 месяцев с момента его начала. Если до начала лечения функция щитовидной железы в норме, то периодические исследования ее функции не требуются, однако их проведение необходимо при появлении клинических признаков дисфункции щитовидной железы.
Выраженные нарушения функции почек и выраженная миелосупрессия
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Нейтрализующие антитела
У пациентов, получающих интерфероны бета, возможно образование нейтрализующих антител. Клинические данные позволяют предположить, что после 24-48 месяцев лечения интерфероном бета-1а в дозе 44 мкг примерно у 13-14% (24% для дозы 22 мкг) пациентов в сыворотке крови появляются нейтрализующие антитела на интерферон бета-1а. Присутствие антител связывают со снижением эффективности лечения, что подтверждается МРТ исследованием и клиническими показателями. Полная клиническая значимость выработки нейтрализующих антител еще недостаточно изучена.
Образование нейтрализующих антител связывают с реакцией на наличие различных форм интерферона бета. Если у пациента недостаточно хороший ответ на терапию препаратом Тебериф®, и это связано с устойчивым наличием нейтрализующих антител, врач должен оценить целесообразность продолжения терапии интерфероном. Использование различных методов для обнаружения антител в сыворотке и определения их характеристик ограничивает возможность сравнения иммуногенности различных препаратов.
Другие формы рассеянного склероза
По неамбулаторным пациентам, страдающим рассеянным склерозом, доступны лишь отдельные данные по безопасности и эффективности препарата. Использование интерферона бета-1а у пациентов с первичным прогрессирующим рассеянным склерозом до настоящего времени не изучалось, поэтому препарат не должен применяться при данном заболевании.
Влияние на способность к управлению транспортными средствами и механизмами
Побочные реакции со стороны ЦНС на проводимую терапию интерферонами (см. «Побочное действие») могут влиять на способность к управлению автомобилем и техникой.
Передозировка
При введении пациентом большей, чем предписано, дозы следует немедленно сообщить об этом лечащему врачу. При необходимости в случае передозировки пациента следует госпитализировать для дальнейшего наблюдения и проведения поддерживающей терапии.
Лекарственное взаимодействие
Специально спланированные клинические исследования по изучению взаимодействия интерферона бета-1а с другими лекарственными средствами не проводились. Однако известно, что в организме людей и животных интерфероны снижают активность цитохром-Р450-зависимых ферментов печени. Поэтому следует соблюдать осторожность при назначении препарата Тебериф® одновременно с лекарственными средствами, имеющими узкий терапевтический индекс, клиренс которых в значительной степени зависит от системы цитохрома Р450 печени, например, с противоэпилептическими средствами и некоторыми антидепрессантами.
Систематическое изучение взаимодействия интерферона бета-1а с кортикостероидами или АКТГ не проводилось. Данные клинических исследований указывают на возможность получения больными рассеянным склерозом интерферона бета-1а и кортикостероидов или АКТГ во время обострений заболевания.
Условия хранения препарата Тебериф®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°С. Не замораживать.
Срок годности препарата Тебериф®
Срок годности — 2 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
БИОКАД АО
(Россия)

|
|
198515 Санкт-Петербург, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Тебериф — инструкция по применению
Регистрационный номер
ЛП-004137
Торговое наименование препарата
Тебериф®
Международное непатентованное наименование
Интерферон бета-1a
Лекарственная форма
раствор для подкожного введения
Состав
1 мл раствора содержит:
действующее вещество — интерферона бета-1а рекомбинантного человеческого 44 мкг (12 млн ME) или 88 мкг (24 млн. ME)
вспомогательные вещества — лизина гидрохлорида 27,4 мг, полисорбата-20 0,05 мг, натрия ацетата тригидрата 0,272 мг, уксусной кислоты ледяной до pH 4,2, воды для инъекций до 1,0 мл.
Описание
Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Цитокин (Интерферон бета-1а)
Код АТХ
L03AB07
Фармакодинамика:
Интерфероны относятся к группе эндогенных гликопротеинов, обладающих иммуномодулирующими, противовирусными и антипролиферативными свойствами. Белковая структура препарата Тебериф® (интерферон бета-1а рекомбинантный человеческий) представляет собой природную аминокислотную последовательность интерферона бета человека, полученную методом генной инженерии с использованием культуры клеток яичника китайского хомячка и, следовательно, является гликозилированным, как и природный, белком.
Независимо от способа введения, изменения фармакодинамического эффекта связывают с терапией препаратом Тебериф®. После однократной дозы внутриклеточная и сывороточная активность 2’,5’-олигоаденилат-синтетазы (2’,5’OAS) и сывороточная концентрация бета-2-микроглобулина и неоптерина повышаются в течение 24 часов и затем в течение 2-х дней начинают снижаться. При подкожном и внутримышечном введении ответ на введение препарата Тебериф® полностью идентичен. После 4-х последовательных подкожных инъекций, повторяющихся каждые 48 часов, биологический ответ остается повышенным без признаков привыкания.
Подкожное введение интерферона бета-1а здоровым добровольцам и пациентам с рассеянным склерозом повышает уровень маркеров биологического ответа (активность 2’,5’-олигоаденилат-синтетазы, концентрация неоптерина и бета-2-микроглобулина в плазме). Время достижения максимальной концентрации после однократного подкожного введения препарата Тебериф® составляет от 24 до 48 часов для неоптерина, бета-2- микроглобулина и 2’,5’OAS, 12 часов для MXI и 24 часа для олигоаденилат-синтетазы 1 (OAS1) и олигоаденилат-синтетазы 2 (OAS2). Подобные пики концентраций для большинства этих маркеров наблюдаются после первого и шестого введений. Механизм действия препарата Тебериф® в организме больных рассеянным склерозом до конца не изучен. Показано, что препарат способствует ограничению повреждений центральной нервной системы (димеилинизация), лежащих в основе заболевания.
Данные клинических исследований
Первый эпизод демиелинизации
В двухлетнем контролируемом клиническом исследовании интерферон бета-1а в рекомендуемой дозировке продемонстрировал эффективность при лечении пациентов с первым эпизодом демиелинизации, предположительно в результате рассеянного склероза. У пациентов, включенных в исследование, отмечалось как минимум 2 асимптомных очага Т2 взвешенных МРТ изображениях размером не менее 3 мм, причем хотя бы один из очагов был овальной формы, перивентрикулярным или инфратенториальным. Другие заболевания, которые могли лучше объяснить симптоматику пациента, чем диагноз рассеянного склероза, были исключены. Было установлено, что интерферон бета-1а 44 мкг при приеме 3 раза в неделю задерживал прогрессирование заболевания у пациентов с первым эпизодом демиелинизации. Снижение риска прогрессирования заболевания составило 52% по сравнению с плацебо.
Ремиттирующий рассеянный склероз
Безопасность и эффективность интерферона бета-1а были оценены у пациентов с ремиттирующим рассеянным склерозом при дозах в диапазоне 11-44 мкг (2-12 млн. ME), вводимых подкожно три раза в неделю. Было показано, что в дозировке 44 мкг интерферон бета-1а снижает частоту (30% в течение 2 лет) и тяжесть обострений у пациентов с двумя и более обострениями в течение последних 2 лет и с оценкой от 0 до 5 по расширенной шкале оценки степени инвалидизации (EDSS) перед началом лечения. Доля пациентов с подтвержденным прогрессированием инвалидизации уменьшилась с 39% (плацебо) до 30% и 27% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг соответственно). Через 4 года среднее снижение числа обострений составляло 22% и 29% у пациентов, получавших 22 мкг интерферона бета-1а и 44 мкг интерферона бета-1а соответственно, по сравнению с группой пациентов, получавших в течение 2 лет плацебо, а затем — интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг.
В трехгодичном исследовании у пациентов с вторично-прогрессирующим рассеянным склерозом (3-6,5 баллов по шкале EDSS) с достоверным прогрессированием инвалидизации в течение предшествующих 2 лет и отсутствием обострений в течение предшествующих 8 нед., интерферон бета-1а не оказывал существенного влияния на инвалидизацию, однако частота обострений снизилась на 30 %. При выделении двух групп пациентов (имевших или не имевших обострения заболевания за последние 2 года) в группе «без обострений» не было обнаружено влияния препарата на прогрессирование инвалидизации, тогда как в группе «с обострениями» доля пациентов с прогрессированием в конце исследования снизилась с 70% (плацебо) до 57% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг).
Первично-прогрессирующий рассеянный склероз
Действие препарата при первично-прогрессирующем рассеянном склерозе не изучалось.
Фармакокинетика:
Всасывание:
После внутривенного введения здоровым добровольцам концентрация интерферона бета- la подвергается резкому экспоненциальному уменьшению, причем уровни препарата в сыворотке крови оказываются пропорциональными дозе.
Распределение:
После повторных подкожных инъекций препарата Тебериф® в дозе 22 мкг и 44 мкг максимальные концентрации интерферона бета-1а наблюдаются через 8 часов, но значения сильно варьируют.
Метаболизм:
Интерферон бета-1а подвергается метаболизму и выводится печенью и почками.
Выведение:
После повторных подкожных инъекций препарата Тебериф® здоровым добровольцам основные фармакокинетические параметры (площадь под фармакокинетической кривой (AUC) и максимальная концентрация (Сmах)) возрастают пропорционально увеличению дозы от 22 мкг до 44 мкг. Период полувыведения составляет от 50 до 60 часов, что коррелирует с процессом кумуляции, наблюдаемым после многократного введения.
Показания:
- Лечение пациентов с первым эпизодом демиелинизации, в основе которого лежит острый воспалительный процесс, если иные диагнозы были исключены, и если существует высокий риск развития клинически достоверного рассеянного склероза;
- Лечение пациентов с ремиттирующим рассеянным склерозом, у которых заболевание характеризуется двумя или более обострениями за предшествующие два года.
Эффективность не была продемонстрирована у пациентов с вторично-прогрессирующим рассеянным склерозом в отсутствии обострений.
Противопоказания:
- Повышенная чувствительность к природному или рекомбинантному интерферону бета, к другим компонентам препарата.
- Инициация терапии во время беременности.
- Тяжелые депрессивные нарушения и/или суицидальные идеи.
- Возраст до 12 лет.
Беременность и лактация:
Женщины с детородным потенциалом
Женщины детородного возраста должны пользоваться эффективными средствами контрацепции. Учитывая потенциальную опасность для плода, пациентки, планирующие беременность или забеременевшие на фоне лечения, должны обязательно сообщить об этом лечащему врачу для решения об отмене препарата. Для пациенток с высокой частотой рецидивов перед началом лечения необходимо сопоставить риск возникновения тяжелого рецидива в случае прекращения приема препарата из-за наступления беременности с возможным повышением вероятности самопроизвольного аборта.
Беременность
Начинать лечение препаратом Тебериф® в период беременности противопоказано. Имеющиеся данные указывают на возможное повышение риска самопроизвольного аборта.
Период грудного вскармливания
Данные об экскреции препарата Тебериф® в грудное молоко отсутствуют. Учитывая вероятность развития серьезных побочных реакций у новорожденных, следует сделать выбор между отменой препарата Тебериф® и прекращением грудного вскармливания.
Способ применения и дозы:
Препарат вводят подкожно. Лечение следует начинать под контролем врача-специалиста, имеющего опыт лечения данного заболевания. Лечение препаратом Тебериф® с целью предотвращения развития тахифилаксии и снижения нежелательных реакций рекомендуется начинать с дозы 8,8 мкг и затем в течение 4 недель дозу увеличивать до рекомендованной дозировки
При назначении препарата Тебериф® в дозе 44 мкг, начиная с 5-й недели вводится 0,5 мл препарата в данной дозировке. Для уменьшения гриппоподобных симптомов, связанных с назначением препарата Тебериф® перед введением и в течение 24 ч после каждой инъекции, рекомендуется назначать жаропонижающее средство (антипиретик).
Первый эпизод демиелинизации
Дозировка интерферона бета-1а для пациентов с первым эпизодом демиелинизации составляет 44 мкг 3 раза в неделю подкожно.
Ремиттирующий рассеянный склероз
Взрослым и подросткам старше 16 лет рекомендуемая доза препарата обычно составляет 44 мкг 3 раза в неделю. В дозе 22 мкг 3 раза в неделю препарат Тебериф® назначается тем пациентам, которые, по мнению лечащего врача, недостаточно хорошо переносят высокую дозу.
Безопасность и эффективность применения интерферона бета-1а для подкожного применения у подростков в возрасте 12-16 лет до сих пор окончательно не установлена. Данные по безопасности, приведенные в разделе «Побочное действие», не дают возможности дать рекомендации по режиму дозирования для этой группы пациентов. Тем не менее, опубликованные данные позволяют предположить, что профиль безопасности интерферона бета-1а у подростков от 12 до 16 лет, получающих подкожные инъекции препарата в дозе 22 мкг 3 раза в неделю, аналогичен таковому у взрослых. Безопасность и эффективность интерферона бета-1а у детей до 12 лет не установлена, имеются лишь ограниченные сведения, поэтому препарат Тебериф® не следует применять в этой возрастной группе. Препарат следует применять в одно и то же время (желательно вечером), в определенные дни недели, с интервалом не менее 48 ч. Препарат Тебериф® можно использовать только в том случае, если раствор препарата прозрачен или слегка опалесцирует и, если в нем не содержится посторонних частиц. В настоящее время нет четких рекомендаций о том, как долго следует проводить лечение. Рекомендуется оценивать состояние пациентов, как минимум, каждые два года в течение первых 4 лет лечения препаратом Тебериф®, решение о более длительной терапии должно приниматься лечащим врачом индивидуально для каждого пациента.
Врач должен довести следующую информацию до пациента:
Чтобы применение препарата Тебериф® было эффективным и безопасным, нужно:
- Применять препарат Тебериф® только под наблюдением опытного врача.
- Для предупреждения некроза внимательно прочтите инструкцию и следуйте ее указаниям. При возникновении реакции в месте инъекции проконсультируйтесь с врачом.
- Не менять дозы препарата без согласования с врачом.
- Не прерывать лечение без согласования с врачом.
- Предупредить врача, если у Вас имеется непереносимость каких-либо лекарственных препаратов.
- В ходе лечения сообщать врачу о любых нарушениях состояниях здоровья.
Поскольку препарат Тебериф® выпускается в виде предварительно заполненного шприца для подкожного введения, Вы можете безопасно его применять в домашних условиях, как самостоятельно, так и при помощи родственников и друзей. Если возможно, первая инъекция должна быть сделана под наблюдением квалифицированного медицинского работника.
Перед применением препарата Тебериф®, пожалуйста, внимательно прочтите следующую инструкцию:
1. Выберите удобное для Вас время проведения инъекции. Инъекции желательно делать вечером перед сном.
2. Перед введением препарата тщательно вымойте руки водой с мылом.
3. Возьмите одну контурную ячейковую упаковку с заполненным шприцем из картонной пачки, которая должна храниться в холодильнике, и выдержите ее при комнатной температуре в течение нескольких минут для того, чтобы температура препарата сравнялась с температурой окружающего воздуха. В случае появления конденсата на поверхности шприца подождите еще несколько минут до тех пор, пока конденсат не испарится. В случае невозможности хранения невскрытого шприца в холодильнике, допустимо однократное хранение в защищенном от света месте не более 30 суток при температуре не выше 25 °С. Дату начала хранения при комнатной температуре следует отмечать на упаковке.
4. Перед использованием следует осмотреть раствор в шприце. При наличии взвешенных частиц или изменении цвета раствора или повреждении шприца препарат не следует применять. Если появилась пена, что бывает, когда шприц встряхивают или сильно покачивают, подождите, пока осядет пена.
5. Выберите область тела для инъекции. Препарат Тебериф® вводится в подкожную жировую клетчатку (жировой слой между кожей и мышечной тканью), поэтому используйте места с рыхлой клетчаткой вдали от мест растяжения кожи, нервов, суставов и сосудов (на рис. 1 и 2. указаны рекомендованные области для инъекций):
- Бедра (передняя поверхность бедер кроме паха и колена);
- Живот (кроме срединной линии и околопупочной области);
- Наружная поверхность плеч;
- Ягодицы (верхний наружный квадрант).
Не следует использовать для инъекции болезненные точки, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками.
Каждый раз выбирайте новое место для укола, так Вы сможете уменьшить неприятные ощущения и боль на участке кожи в месте инъекции. Внутри каждой инъекционной области есть много точек для укола. Постоянно меняйте точки инъекций внутри конкретной области.
6. Подготовка к инъекции.
Возьмите подготовленный шприц в руку, которой Вы пишете. Снимите защитный колпачок с иглы.
7. Количество раствора препарата Тебериф®, которое нужно ввести при проведении инъекции, зависит от рекомендованной Вашим врачом дозы. Не храните остатки препарата, оставшиеся в шприце, для повторного использования.
В зависимости от дозы, которую прописал Ваш врач, Вам может потребоваться удалить лишний объем раствора препарата из шприца. В случае такой необходимости медленно и аккуратно нажимайте на поршень шприца для удаления лишнего количества раствора. Давите на поршень до тех пор, пока поршень не дойдет до необходимой метки на этикетке шприца.
8. Предварительно продезинфицируйте участок кожи, куда будет введен препарат Тебериф®. Когда кожа обсохнет, слегка соберите кожу в складку большим и указательным пальцами (рис.3).
9. Располагая шприц перпендикулярно месту инъекции, введите иглу в кожу под углом 90° (рис. 4). Рекомендуемая глубина введения иглы составляет 6 мм от поверхности кожи. Глубина подбирается в зависимости от типа телосложения и толщины подкожной жировой клетчатки. Вводите препарат, равномерно нажимая на поршень шприца вниз до конца (до его полного опустошения).
10. Удалите шприц с иглой движением вертикально вверх, сохраняя прежний угол наклона.
11. К месту инъекции можно приложить сухой стерильный ватный шарик. При необходимости можно заклеить пластырем. Не рекомендуется растирать или массировать место инъекции после введения препарата.
12. Использованные шприцы выбрасывайте только в специально отведенное место, недоступное для детей.
13. Если Вы забыли ввести препарат, сделайте инъекцию немедленно, как только вспомнили об этом. Следующую инъекцию производят через 48 ч. Не допускается вводить двойную дозу препарата.
Не прекращайте применение препарата Тебериф® без консультации с врачом.
Что делать в случае передозировки препаратом Тебериф®
Ни одного случая передозировки до настоящего времени не описано. Однако в случае повышения дозы (увеличения одноразового объема и частоты приема в неделю) немедленно сообщите врачу.
Что делать, если Вы пропустили дозу
Если Вы пропустили дозу, продолжайте инъекции, начиная со следующей по графику. Не вводите двойную дозу.
Коррекция режима дозирования
При повышении верхней границы нормы содержания АЛТ дозу препарата Тебериф® необходимо снизить и постепенно увеличивать после нормализации уровня АЛТ. Временное снижение дозы препарата может потребоваться также при значительной выраженности гриппоподобных симптомов.
Применение у особых групп пациентов
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, с признаками заболевания печени, с признаками злоупотребления алкоголем, уровнем АЛТ в 2,5 раза превышающим верхнюю границу нормы. Терапию следует прекратить при появлении желтухи или других симптомов нарушения функции печени.
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Побочные эффекты:
Самые частые нежелательные реакции, наблюдающиеся при лечении интерфероном бета- la, связаны с возникновением гриппоподобного синдрома. Гриппоподобные симптомы бывают особенно выраженными в начале лечения и ослабевают по частоте по мере продолжения лечения. Примерно у 70 % пациентов, принимающих интерферон бета-1а, можно ожидать появления типичного гриппоподобного синдрома в первые шесть месяцев после начала лечения. Примерно у 30 % пациентов возникают реакции в месте инъекции, преимущественно умеренное раздражение или эритема.
Асимптоматическое повышение лабораторных показателей печеночной функции и снижение количества лейкоцитов также являются частыми. Ниже представлены нежелательные реакции, которые наблюдались как в клинических исследованиях, так и в пострегистрационный период (помечены *) у пациентов с рассеянным склерозом. Нежелательные реакции перечислены в соответствии с их частотой и системно-органным классом. Для обозначения частоты нежелательных реакций используется общепринятая классификация: очень часто (≥ 1/10 случаев), часто (≥ 1/100, <1/10), нечасто (≥ 1/1,000, < 1/100), редко (≥ 1/10,000, < 1/1,000), очень редко (< 1/10,000), частота неизвестна (не может быть установлена на основании полученных данных)
Нарушения со стороны крови и лимфатической системы:
Очень часто: нейтропения, лимфопения, лейкопения, тромбоцитопения, анемия.
Редко: тромботическая микроангиопатия, включающая тромботическую тромбоцитопеническую пурпуру/гемолитико-уремический синдром* (является класс-эффектом интерферонов; см. раздел «Особые указания»), панцитопения*.
Нарушения со стороны иммунной системы:
Редко: анафилактические реакции*.
Нарушения со стороны эндокринной системы:
Нечасто: нарушение функции щитовидной железы, наиболее часто проявляющееся в виде гипо- или гипертиреоза (см. раздел «Особые указания»).
Нарушения со стороны печени и желчевыводящих путей:
Очень часто: бессимптомное повышение активности трансаминаз в крови.
Часто: значительное повышение активности трансаминаз в крови.
Нечасто: гепатит (с желтухой или без нее)*.
Редко: печеночная недостаточность*, аутоиммунный гепатит*.
Психические нарушения:
Часто: депрессия, бессонница.
Редко: суицидальные попытки (см. раздел «Особые указания»).
Нарушения со стороны нервной системы:
Очень часто: головная боль.
Нечасто: судороги* (см. раздел «Особые указания»).
Частота неизвестна: преходящие неврологические симптомы (гипестезия, мышечные спазмы, парестезия, затруднения при ходьбе, ригидность мышц), которые могут имитировать обострение рассеянного склероза*.
Нарушения со стороны органа зрения:
Нечасто: поражение сосудов сетчатки (т.е. ретинопатия, «ватные пятна» на сетчатке, обструкция артерии или вены сетчатки)*.
Нарушения со стороны сосудистой системы:
Нечасто: тромбоэмболия*.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: Нечасто: одышка*.
Частота неизвестна: артериальная легочная гипертензия (класс-эффект, см. ниже «Артериальная легочная гипертензия»)
Нарушения со стороны желудочно-кишечного тракта:
Часто: диарея, рвота, тошнота.
Нарушения со стороны кожи и подкожных тканей:
Часто: зуд, сыпь, эритематозная сыпь, макулопапулезная сыпь, алопеция*.
Нечасто: крапивница*.
Редко: отек Квинке*, мультиформная эритема*, кожная реакция, напоминающая мультиформную эритему*, синдром Стивенса-Джонсона*.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
Часто: миалгия, артралгия.
Редко: лекарственная красная волчанка*.
Нарушения со стороны почек и мочевыделительной системы:
Редко: нефротический синдром*, гломерулосклероз* (см. раздел «Особые указания»).
Общие расстройства и нарушения в месте введения:
Очень часто: воспаление в месте инъекции, реакции в месте инъекции, например, кровоподтек, припухлость в месте инъекции, отек, покраснение), гриппоподобные симптомы.
Часто: боль в месте введения, утомляемость, озноб, лихорадка.
Нечасто: некроз в месте инъекции, припухлость в месте инъекции, абсцесс в месте инъекции, инфицирование места инъекции*, усиление потоотделения*.
Редко: флегмона в месте инъекции*.
Дети
Отдельные клинические или фармакокинетические исследования для детей и подростков не проводились. Однако опубликованные данные по применению интерферона бета-1а у подростков от 12 до 16 лет, получавших интерферон бета-1а в дозе 22 мкг 3 раза в неделю подкожно, позволяют предположить, что профиль безопасности препарата Тебериф® в этой группе аналогичен таковому у взрослых пациентов.
Класс-эффекты
Применение интерферонов связано с потерей аппетита, головокружениями, беспокойством, аритмией, расширением кровеносных сосудов и учащенным сердцебиением, меноррагией и метроррагией.
В ходе лечения интерфероном бета может происходить усиленное образование антител.
Артериальная легочная гипертензия
На фоне применения препаратов интерферона бета регистрировались случаи артериальной легочной гипертензии. Данные случаи регистрировались на разных этапах лечения, в том числе через несколько лет после начала терапии интерфероном бета.
Необходимо информировать врача о любых перечисленных выше нежелательных реакциях, а также о тех, которые не указаны в данной инструкции. При сохранении нежелательных реакций в течение длительного времени или в случае развития тяжелых нежелательных реакций по усмотрению врача допускается временное снижение дозы препарата или прерывание лечения.
Не следует прекращать лечение или изменять дозу без указания лечащего врача.
Передозировка:
При введении пациентом большей чем предписана дозы следует немедленно сообщить об этом лечащему врачу. При необходимости в случае передозировки пациента следует госпитализировать для дальнейшего наблюдения и проведения поддерживающей терапии.
Взаимодействие:
Специально спланированные клинические исследования по изучению взаимодействия интерферона бета-1а с другими лекарственными средствами не проводились. Однако известно, что в организме людей и животных интерфероны снижают активность цитохром-Р450-зависимых ферментов печени. Поэтому следует соблюдать осторожность при назначении препарата Тебериф® одновременно с лекарственными средствами, имеющими узкий терапевтический индекс, клиренс которых в значительной степени зависит от цитохромовой Р450 системы печени, например, с противоэпилептическими средствами и некоторыми антидепрессантами.
Систематическое изучение взаимодействия интерферона бета-1а с кортикостероидами или адренокортикотропным гормоном (АКТГ) не проводилось. Данные клинических исследований указывают на возможность получения больными рассеянным склерозом интерферона бета-1а и кортикостероидов или АКТГ во время обострений заболевания.
Особые указания:
Пациентов следует проинформировать относительно наиболее частых побочных действий, связанных с приемом интерферона бега, включая гриппоподобные симптомы (см. раздел «Побочное действие»), которые бывают особенно выраженными в начале лечения и уменьшаются по частоте и выраженности по мере продолжения лечения.
Тромботическая микроангиопатия (ТМА)
Имеется информация о случаях тромботической микроангиопатии, которые проявлялись в виде тромботической тромбоцитопенической пурпуры или гемолитико-уремического синдрома, включая случаи с летальным исходом. Такие случаи регистрировались в различные периоды времени, от нескольких недель до нескольких лет после начала лечения интерфероном бета-1а. Рекомендуется проводить мониторинг ранних симптомов, таких как тромбоцитопения, вновь возникающие случаи гипертензии, лихорадка, нарушения со стороны центральной нервной системы (например, спутанное сознание, парез) и снижение почечной функции. Лабораторные данные при предположительном диагнозе ТМА включают снижение числа тромбоцитов, увеличение сывороточной активности лактатдегидрогеназы (ЛДГ), вызванное гемолизом и шизоцитами (фрагменты эритроцитов) в мазке крови. Если наблюдаются клинические признаки ТМА, рекомендуется провести определение содержания тромбоцитов; сывороточной ЛДГ, взять мазок крови и оценить почечную функцию. Если диагноз ТМА подтверждается, требуется немедленное лечение (может потребоваться переливание плазмы) и прекращение лечения интерфероном бета-1а.
Депрессии и суицидальные идеи
Препарат Тебериф® должен с осторожностью назначаться пациентам, находящимся или перенесшим депрессивные состояния. Депрессивные и суицидальные состояния с повышенной частотой наблюдаются в группе пациентов, страдающих рассеянным склерозом и принимающих интерферон.
Пациентов необходимо предупредить о том, что им следует немедленно сообщить о любых симптомах депрессии и/или появлении суицидальных идей лечащему врачу. Лечение больных, страдающих депрессией, препаратом Тебериф® должно проходить в условиях пристального контроля и предоставления им необходимой помощи. В ряде случаев может встать вопрос о прекращении лечения препаратом.
Судорожный синдром
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с эпилептическими припадками в анамнезе, особенно если течение этого заболевания не полностью контролируется противоэпилептическими препаратами.
Сердечно-сосудистые заболевания
На первых этапах лечения препаратом Тебериф® необходимо строгое наблюдение за пациентами, страдающими сердечно-сосудистыми заболеваниями, такими как стенокардия, застойная сердечная недостаточность и нарушения ритма. Это наблюдение должно быть направлено на своевременное выявление возможного ухудшения состояния. При заболеваниях сердца гриппоподобные симптомы, связанные с терапией интерфероном бета-1а, могут оказаться серьезной нагрузкой для больных.
Некроз в месте инъекций
Имеются единичные сообщения о некрозе в месте инъекций. Чтобы свести до минимума риск развития некроза необходимо строгое соблюдение правил асептики при выполнении инъекции и смена места введения после каждой инъекции. Необходимо регулярно оценивать технику самостоятельного введения препарата пациентами, особенно при возникновении реакций в месте инъекций. Если отмечается повреждение кожи с отеком и выделением жидкости в месте инъекции, необходимо обратиться к врачу прежде, чем продолжать введение препарата. При множественных повреждениях кожи следует отменить препарат до их заживления. При единичном поражении возможно продолжение терапии препаратом Тебериф®, при условии, что поражение выражено умеренно.
Нарушения функции печени
В клинических испытаниях продемонстрировано бессимптомное повышение активности печеночных трансаминаз, особенно аланинаминотрансферазы (АЛТ), а у 1-3% пациентов содержание печеночных трансаминаз превышало верхние пределы нормы (ВПН) более чем в 5 раз. При отсутствии клинической симптоматики необходимо контролировать активность АЛТ в плазме до начала применения интерферона бета-1а, в 1-й, 3-й и 6-й месяцы от его начала, а также периодически в ходе дальнейшего лечения. Необходимо снизить дозу препарата, если активность АЛТ превысит в 5 раз верхнюю границу нормы, и постепенно увеличивать дозу после ее нормализации. Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, с признаками заболевания печени, с признаками злоупотребления алкоголем, активностью АЛТ в 2,5 раза превышающей верхнюю границу нормы. Терапию препаратом Тебериф® необходимо прекратить при появлении желтухи или других клинических симптомов нарушения функции печени.
Тебериф®, как и другие интерфероны бета, потенциально может вызывать тяжелое поражение печени, в том числе, острую печеночную недостаточность. Тяжелые нарушения функции печени главным образом возникают в первые 6 месяцев терапии. Механизм этих состояний неизвестен, специфические факторы риска не выявлены.
Нарушение функции почек и мочевыводящей системы
Нефротический синдром
В ходе лечения интерфероном бета-1а и другими интерферонами бета могут иметь место случаи нефротического синдрома с различными нефропатиями, включая очаговый сегментарный гломерулосклероз (ОСГС), мембранопролиферативный гломерулонефрит и мембранную гломерулопатию. Случаи имели место как в процессе лечения, так и через несколько лет после его завершения. Рекомендуется проводить периодический мониторинг ранних признаков или симптомов (например, отеки, протеинурия или нарушение функции почек) особенно у пациентов с высоким риском возникновения заболеваний почек. Нефротический синдром требует немедленного лечения и прекращения приема препарата Тебериф®.
Нарушение лабораторных показателей
В дополнение к лабораторным анализам, которые всегда проводятся пациентам с рассеянным склерозом, рекомендуется в 1-й, 3-й и 6-й месяцы с момента начала терапии препаратом Тебериф®, а также, периодически, при отсутствии клинической симптоматики, в ходе дальнейшего лечения определять общий клинический анализ крови с лейкоцитарной формулой, содержание тромбоцитов, а также проводить биохимическое исследование крови, включая функциональные пробы печени.
Заболевания щитовидной железы
У пациентов, получающих интерферон бета-1а, иногда могут развиваться или усугубляться имеющиеся патологические изменения щитовидной железы. Рекомендуется проводить исследование функции щитовидной железы непосредственно до начала лечения и, при выявлении нарушений, каждые 6-12 мес. с момента его начала. Если до начала лечения функция щитовидной железы в норме, то периодические исследования ее функции не требуются, однако их проведение необходимо при появлении клинических признаков дисфункции щитовидной железы.
Выраженные нарушения функции почек и печени и выраженная миелосупрессия
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Нейтрализующие антитела
У пациентов, получающих интерфероны бета, возможно образование нейтрализующих антител. Клинические данные позволяют предположить, что после 24-48 месяцев лечения интерфероном бета-1а 44 мкг примерно у 13-14% (24% для 22 мкг) пациентов в сыворотке крови появляются нейтрализующие антитела на интерферон бета-1а. Присутствие антител связывают со снижением эффективности лечения, что подтверждается МРТ исследованием и клиническими показателями. Полная клиническая значимость выработки нейтрализующих антител еще недостаточно изучена.
Образование нейтрализующих антител связывают с реакцией на наличие различных форм интерферона бета. Если у пациента недостаточно хороший ответ на терапию препаратом Тебериф®, и это связано с устойчивым наличием нейтрализующих антител, врач должен оценить целесообразность продолжения терапии интерфероном. Использование различных методов для обнаружения антител в сыворотке и определения их характеристик ограничивает возможность сравнения иммуногенности различных препаратов.
Другие формы рассеянного склероза
По неамбулаторным пациентам, страдающим рассеянным склерозом, доступны лишь отдельные данные по безопасности и эффективности препарата. Использование интерферона бета-1а у пациентов с первичным прогрессирующим рассеянным склерозом до настоящего времени не изучалось, поэтому препарат не должен применяться при данном заболевании.
Меры предосторожности при применении
Не требует особых мер предосторожности при использовании.
Влияние на способность управлять транспортными средствами и механизмами:
Побочные реакции со стороны центральной нервной системы на проводимую терапию интерферонами (см. «Возможные побочные действия при применении») могут влиять на способность к управлению автомобилем и техникой.
Форма выпуска/дозировка:
Раствор для подкожного введения 22 мкг/ 0,5 мл, 44 мкг/0,5 мл.
Упаковка:
По 0,5 мл в шприцы из бесцветного стекла I гидролитического класса. По 1 шприцу в контурную ячейковую упаковку. По 3 или 12 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению помещают в пачку из картона. Пачка со шприцами дополнительно комплектуется спиртовыми салфетками в количестве 3 или 12 шт.
Условия хранения:
Хранить при температуре от 2 до 8 °С в защищенном от света месте.
Не замораживать.
Хранить в недоступном для детей месте.
Срок годности:
2 года. Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Тебериф — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-004137
Торговое наименование препарата
Тебериф®
Международное непатентованное наименование
Интерферон бета-1a
Лекарственная форма
раствор для подкожного введения
Состав
1 мл раствора содержит:
действующее вещество — интерферона бета-1а рекомбинантного человеческого 44 мкг (12 млн ME) или 88 мкг (24 млн. ME)
вспомогательные вещества — лизина гидрохлорида 27,4 мг, полисорбата-20 0,05 мг, натрия ацетата тригидрата 0,272 мг, уксусной кислоты ледяной до pH 4,2, воды для инъекций до 1,0 мл.
Описание
Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Цитокин (Интерферон бета-1а)
Код АТХ
L03AB07
Фармакодинамика:
Интерфероны относятся к группе эндогенных гликопротеинов, обладающих иммуномодулирующими, противовирусными и антипролиферативными свойствами. Белковая структура препарата Тебериф® (интерферон бета-1а рекомбинантный человеческий) представляет собой природную аминокислотную последовательность интерферона бета человека, полученную методом генной инженерии с использованием культуры клеток яичника китайского хомячка и, следовательно, является гликозилированным, как и природный, белком.
Независимо от способа введения, изменения фармакодинамического эффекта связывают с терапией препаратом Тебериф®. После однократной дозы внутриклеточная и сывороточная активность 2’,5’-олигоаденилат-синтетазы (2’,5’OAS) и сывороточная концентрация бета-2-микроглобулина и неоптерина повышаются в течение 24 часов и затем в течение 2-х дней начинают снижаться. При подкожном и внутримышечном введении ответ на введение препарата Тебериф® полностью идентичен. После 4-х последовательных подкожных инъекций, повторяющихся каждые 48 часов, биологический ответ остается повышенным без признаков привыкания.
Подкожное введение интерферона бета-1а здоровым добровольцам и пациентам с рассеянным склерозом повышает уровень маркеров биологического ответа (активность 2’,5’-олигоаденилат-синтетазы, концентрация неоптерина и бета-2-микроглобулина в плазме). Время достижения максимальной концентрации после однократного подкожного введения препарата Тебериф® составляет от 24 до 48 часов для неоптерина, бета-2- микроглобулина и 2’,5’OAS, 12 часов для MXI и 24 часа для олигоаденилат-синтетазы 1 (OAS1) и олигоаденилат-синтетазы 2 (OAS2). Подобные пики концентраций для большинства этих маркеров наблюдаются после первого и шестого введений. Механизм действия препарата Тебериф® в организме больных рассеянным склерозом до конца не изучен. Показано, что препарат способствует ограничению повреждений центральной нервной системы (димеилинизация), лежащих в основе заболевания.
Данные клинических исследований
Первый эпизод демиелинизации
В двухлетнем контролируемом клиническом исследовании интерферон бета-1а в рекомендуемой дозировке продемонстрировал эффективность при лечении пациентов с первым эпизодом демиелинизации, предположительно в результате рассеянного склероза. У пациентов, включенных в исследование, отмечалось как минимум 2 асимптомных очага Т2 взвешенных МРТ изображениях размером не менее 3 мм, причем хотя бы один из очагов был овальной формы, перивентрикулярным или инфратенториальным. Другие заболевания, которые могли лучше объяснить симптоматику пациента, чем диагноз рассеянного склероза, были исключены. Было установлено, что интерферон бета-1а 44 мкг при приеме 3 раза в неделю задерживал прогрессирование заболевания у пациентов с первым эпизодом демиелинизации. Снижение риска прогрессирования заболевания составило 52% по сравнению с плацебо. Данные эффективности интерферона бета-1а при приеме 44 мкг 3 раза в неделю приведены ниже:
|
Параметры |
Терапия |
Сравнение терапии интерферон бета-1а 44 мкг и плацебо |
|||
|
Плацебо (n=171) |
Интерферон бета-1а 44 мкг, 3 р/нед. (n=171) |
Снижение риска |
Пропор. Относит. Риск Кокса (95% Сl) |
Р-значение |
|
|
Переход в рассеянный склероз по критерию МакДональда (2005) |
|||||
|
Кол-во случаев |
144 |
106 |
51% |
0,49 (0,38; 0,64) |
<0,001 |
|
Оценка КМ |
85,8% |
62,5% |
|||
|
Переход в клинический достоверный рассеянный склероз |
|||||
|
Кол-во случаев |
60 |
33 |
52% |
0,48 (0,31; 0,73) |
<0,001 |
|
Оценка КМ |
37,5% |
20,6% |
|||
|
Среднее по CUA (комбинированные уникальные активные очаги) на 1 пациента во время обследования в ходе двойного слепого периода |
|||||
|
Минимальная погрешность |
2,58 (0,30) |
0,50 (0,06) |
81% |
0,19 (0,14; 0,26) |
<0,001 |
Ремиттирующий рассеянный склероз
Безопасность и эффективность интерферона бета-1а были оценены у пациентов с ремиттирующим рассеянным склерозом при дозах в диапазоне 11-44 мкг (2-12 млн. ME), вводимых подкожно три раза в неделю. Было показано, что в дозировке 44 мкг интерферон бета-1а снижает частоту (30% в течение 2 лет) и тяжесть обострений у пациентов с двумя и более обострениями в течение последних 2 лет и с оценкой от 0 до 5 по расширенной шкале оценки степени инвалидизации (EDSS) перед началом лечения. Доля пациентов с подтвержденным прогрессированием инвалидизации уменьшилась с 39% (плацебо) до 30% и 27% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг соответственно). Через 4 года среднее снижение числа обострений составляло 22% и 29% у пациентов, получавших 22 мкг интерферона бета-1а и 44 мкг интерферона бета-1а соответственно, по сравнению с группой пациентов, получавших в течение 2 лет плацебо, а затем — интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг.
В трехгодичном исследовании у пациентов с вторично-прогрессирующим рассеянным склерозом (3-6,5 баллов по шкале EDSS) с достоверным прогрессированием инвалидизации в течение предшествующих 2 лет и отсутствием обострений в течение предшествующих 8 нед., интерферон бета-1а не оказывал существенного влияния на инвалидизацию, однако частота обострений снизилась на 30 %. При выделении двух групп пациентов (имевших или не имевших обострения заболевания за последние 2 года) в группе «без обострений» не было обнаружено влияния препарата на прогрессирование инвалидизации, тогда как в группе «с обострениями» доля пациентов с прогрессированием в конце исследования снизилась с 70% (плацебо) до 57% (интерферон бета-1а 22 мкг и интерферон бета-1а 44 мкг).
Первично-прогрессирующий рассеянный склероз
Действие препарата при первично-прогрессирующем рассеянном склерозе не изучалось.
Фармакокинетика:
Всасывание:
После внутривенного введения здоровым добровольцам концентрация интерферона бета- la подвергается резкому экспоненциальному уменьшению, причем уровни препарата в сыворотке крови оказываются пропорциональными дозе.
Распределение:
После повторных подкожных инъекций препарата Тебериф® в дозе 22 мкг и 44 мкг максимальные концентрации интерферона бета-1а наблюдаются через 8 часов, но значения сильно варьируют.
Метаболизм:
Интерферон бета-1а подвергается метаболизму и выводится печенью и почками.
Выведение:
После повторных подкожных инъекций препарата Тебериф® здоровым добровольцам основные фармакокинетические параметры (площадь под фармакокинетической кривой (AUC) и максимальная концентрация (Сmах)) возрастают пропорционально увеличению дозы от 22 мкг до 44 мкг. Период полувыведения составляет от 50 до 60 часов, что коррелирует с процессом кумуляции, наблюдаемым после многократного введения.
Показания:
— Лечение пациентов с первым эпизодом демиелинизации, в основе которого лежит острый воспалительный процесс, если иные диагнозы были исключены, и если существует высокий риск развития клинически достоверного рассеянного склероза;
— Лечение пациентов с ремиттирующим рассеянным склерозом, у которых заболевание характеризуется двумя или более обострениями за предшествующие два года.
Эффективность не была продемонстрирована у пациентов с вторично-прогрессирующим рассеянным склерозом в отсутствии обострений.
Противопоказания:
— Повышенная чувствительность к природному или рекомбинантному интерферону бета, к другим компонентам препарата.
— Инициация терапии во время беременности.
— Тяжелые депрессивные нарушения и/или суицидальные идеи.
— Возраст до 12 лет.
Беременность и лактация:
Женщины с детородным потенциалом
Женщины детородного возраста должны пользоваться эффективными средствами контрацепции. Учитывая потенциальную опасность для плода, пациентки, планирующие беременность или забеременевшие на фоне лечения, должны обязательно сообщить об этом лечащему врачу для решения об отмене препарата. Для пациенток с высокой частотой рецидивов перед началом лечения необходимо сопоставить риск возникновения тяжелого рецидива в случае прекращения приема препарата из-за наступления беременности с возможным повышением вероятности самопроизвольного аборта.
Беременность
Начинать лечение препаратом Тебериф® в период беременности противопоказано. Имеющиеся данные указывают на возможное повышение риска самопроизвольного аборта.
Период грудного вскармливания
Данные об экскреции препарата Тебериф® в грудное молоко отсутствуют. Учитывая вероятность развития серьезных побочных реакций у новорожденных, следует сделать выбор между отменой препарата Тебериф® и прекращением грудного вскармливания.
Способ применения и дозы:
Препарат вводят подкожно. Лечение следует начинать под контролем врача-специалиста, имеющего опыт лечения данного заболевания. Лечение препаратом Тебериф® с целью предотвращения развития тахифилаксии и снижения нежелательных реакций рекомендуется начинать с дозы 8,8 мкг и затем в течение 4 недель дозу увеличивать до рекомендованной дозировки согласно приведенной ниже схеме:
|
Сроки введения |
Рекомендованное титрование (% конечной дозировки) |
Титрование дозы препарата Тебериф® 44 мкг 3 раза в неделю |
|
Недели 1 и 2 |
20% |
8,8 мкг 3 р/нед. |
|
Недели 3 и 4 |
50% |
22 мкг 3 р/нед. |
|
Неделя 5 и далее |
100% |
44 мкг 3 р/нед. |
При назначении препарата Тебериф® в дозе 44 мкг, начиная с 5-й недели вводится 0,5 мл препарата в данной дозировке. Для уменьшения гриппоподобных симптомов, связанных с назначением препарата Тебериф® перед введением и в течение 24 ч после каждой инъекции, рекомендуется назначать жаропонижающее средство (антипиретик).
Первый эпизод демиелинизации
Дозировка интерферона бета-1а для пациентов с первым эпизодом демиелинизации составляет 44 мкг 3 раза в неделю подкожно.
Ремиттирующий рассеянный склероз
Взрослым и подросткам старше 16 лет рекомендуемая доза препарата обычно составляет 44 мкг 3 раза в неделю. В дозе 22 мкг 3 раза в неделю препарат Тебериф® назначается тем пациентам, которые, по мнению лечащего врача, недостаточно хорошо переносят высокую дозу.
Безопасность и эффективность применения интерферона бета-1а для подкожного применения у подростков в возрасте 12-16 лет до сих пор окончательно не установлена. Данные по безопасности, приведенные в разделе «Побочное действие», не дают возможности дать рекомендации по режиму дозирования для этой группы пациентов. Тем не менее, опубликованные данные позволяют предположить, что профиль безопасности интерферона бета-1а у подростков от 12 до 16 лет, получающих подкожные инъекции препарата в дозе 22 мкг 3 раза в неделю, аналогичен таковому у взрослых. Безопасность и эффективность интерферона бета-1а у детей до 12 лет не установлена, имеются лишь ограниченные сведения, поэтому препарат Тебериф® не следует применять в этой возрастной группе. Препарат следует применять в одно и то же время (желательно вечером), в определенные дни недели, с интервалом не менее 48 ч. Препарат Тебериф® можно использовать только в том случае, если раствор препарата прозрачен или слегка опалесцирует и, если в нем не содержится посторонних частиц. В настоящее время нет четких рекомендаций о том, как долго следует проводить лечение. Рекомендуется оценивать состояние пациентов, как минимум, каждые два года в течение первых 4 лет лечения препаратом Тебериф®, решение о более длительной терапии должно приниматься лечащим врачом индивидуально для каждого пациента.
Врач должен довести следующую информацию до пациента:
Чтобы применение препарата Тебериф® было эффективным и безопасным, нужно:
— Применять препарат Тебериф® только под наблюдением опытного врача.
— Для предупреждения некроза внимательно прочтите инструкцию и следуйте ее указаниям. При возникновении реакции в месте инъекции проконсультируйтесь с врачом.
— Не менять дозы препарата без согласования с врачом.
— Не прерывать лечение без согласования с врачом.
— Предупредить врача, если у Вас имеется непереносимость каких-либо лекарственных препаратов.
— В ходе лечения сообщать врачу о любых нарушениях состояниях здоровья. Самостоятельное подкожное введение
Поскольку препарат Тебериф® выпускается в виде предварительно заполненного шприца для подкожного введения, Вы можете безопасно его применять в домашних условиях, как самостоятельно, так и при помощи родственников и друзей. Если возможно, первая инъекция должна быть сделана под наблюдением квалифицированного медицинского работника.
Перед применением препарата Тебериф®, пожалуйста, внимательно прочтите следующую инструкцию:
1. Выберите удобное для Вас время проведения инъекции. Инъекции желательно делать вечером перед сном.
2. Перед введением препарата тщательно вымойте руки водой с мылом.
3. Возьмите одну контурную ячейковую упаковку с заполненным шприцем из картонной пачки, которая должна храниться в холодильнике, и выдержите ее при комнатной температуре в течение нескольких минут для того, чтобы температура препарата сравнялась с температурой окружающего воздуха. В случае появления конденсата на поверхности шприца подождите еще несколько минут до тех пор, пока конденсат не испарится. В случае невозможности хранения невскрытого шприца в холодильнике, допустимо однократное хранение в защищенном от света месте не более 30 суток при температуре не выше 25 °С. Дату начала хранения при комнатной температуре следует отмечать на упаковке.
4. Перед использованием следует осмотреть раствор в шприце. При наличии взвешенных частиц или изменении цвета раствора или повреждении шприца препарат не следует применять. Если появилась пена, что бывает, когда шприц встряхивают или сильно покачивают, подождите, пока осядет пена.
5. Выберите область тела для инъекции. Препарат Тебериф® вводится в подкожную жировую клетчатку (жировой слой между кожей и мышечной тканью), поэтому используйте места с рыхлой клетчаткой вдали от мест растяжения кожи, нервов, суставов и сосудов (на рис. 1 и 2. указаны рекомендованные области для инъекций):
— Бедра (передняя поверхность бедер кроме паха и колена);
— Живот (кроме срединной линии и околопупочной области);
— Наружная поверхность плеч;
— Ягодицы (верхний наружный квадрант).
Не следует использовать для инъекции болезненные точки, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками.
Каждый раз выбирайте новое место для укола, так Вы сможете уменьшить неприятные ощущения и боль на участке кожи в месте инъекции. Внутри каждой инъекционной области есть много точек для укола. Постоянно меняйте точки инъекций внутри конкретной области.
6. Подготовка к инъекции.
Возьмите подготовленный шприц в руку, которой Вы пишете. Снимите защитный колпачок с иглы.
7. Количество раствора препарата Тебериф®, которое нужно ввести при проведении инъекции, зависит от рекомендованной Вашим врачом дозы. Не храните остатки препарата, оставшиеся в шприце, для повторного использования.
В зависимости от дозы, которую прописал Ваш врач, Вам может потребоваться удалить лишний объем раствора препарата из шприца. В случае такой необходимости медленно и аккуратно нажимайте на поршень шприца для удаления лишнего количества раствора. Давите на поршень до тех пор, пока поршень не дойдет до необходимой метки на этикетке шприца.
8. Предварительно продезинфицируйте участок кожи, куда будет введен препарат Тебериф®. Когда кожа обсохнет, слегка соберите кожу в складку большим и указательным пальцами (рис.3).
9. Располагая шприц перпендикулярно месту инъекции, введите иглу в кожу под углом 90° (рис. 4). Рекомендуемая глубина введения иглы составляет 6 мм от поверхности кожи. Глубина подбирается в зависимости от типа телосложения и толщины подкожной жировой клетчатки. Вводите препарат, равномерно нажимая на поршень шприца вниз до конца (до его полного опустошения).
10. Удалите шприц с иглой движением вертикально вверх, сохраняя прежний угол наклона.
11. К месту инъекции можно приложить сухой стерильный ватный шарик. При необходимости можно заклеить пластырем. Не рекомендуется растирать или массировать место инъекции после введения препарата.
12. Использованные шприцы выбрасывайте только в специально отведенное место, недоступное для детей.
13. Если Вы забыли ввести препарат, сделайте инъекцию немедленно, как только вспомнили об этом. Следующую инъекцию производят через 48 ч. Не допускается вводить двойную дозу препарата.
Не прекращайте применение препарата Тебериф® без консультации с врачом.
Что делать в случае передозировки препаратом Тебериф®
Ни одного случая передозировки до настоящего времени не описано. Однако в случае повышения дозы (увеличения одноразового объема и частоты приема в неделю) немедленно сообщите врачу.
Что делать, если Вы пропустили дозу
Если Вы пропустили дозу, продолжайте инъекции, начиная со следующей по графику. Не вводите двойную дозу.
Коррекция режима дозирования
При повышении верхней границы нормы содержания АЛТ дозу препарата Тебериф® необходимо снизить и постепенно увеличивать после нормализации уровня АЛТ. Временное снижение дозы препарата может потребоваться также при значительной выраженности гриппоподобных симптомов.
Применение у особых групп пациентов
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, с признаками заболевания печени, с признаками злоупотребления алкоголем, уровнем АЛТ в 2,5 раза превышающим верхнюю границу нормы. Терапию следует прекратить при появлении желтухи или других симптомов нарушения функции печени.
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Побочные эффекты:
Самые частые нежелательные реакции, наблюдающиеся при лечении интерфероном бета- la, связаны с возникновением гриппоподобного синдрома. Гриппоподобные симптомы бывают особенно выраженными в начале лечения и ослабевают по частоте по мере продолжения лечения. Примерно у 70 % пациентов, принимающих интерферон бета-1а, можно ожидать появления типичного гриппоподобного синдрома в первые шесть месяцев после начала лечения. Примерно у 30 % пациентов возникают реакции в месте инъекции, преимущественно умеренное раздражение или эритема.
Асимптоматическое повышение лабораторных показателей печеночной функции и снижение количества лейкоцитов также являются частыми. Ниже представлены нежелательные реакции, которые наблюдались как в клинических исследованиях, так и в пострегистрационный период (помечены *) у пациентов с рассеянным склерозом. Нежелательные реакции перечислены в соответствии с их частотой и системно-органным классом. Для обозначения частоты нежелательных реакций используется общепринятая классификация: очень часто (≥ 1/10 случаев), часто (≥ 1/100, <1/10), нечасто (≥ 1/1,000, < 1/100), редко (≥ 1/10,000, < 1/1,000), очень редко (< 1/10,000), частота неизвестна (не может быть установлена на основании полученных данных)
Нарушения со стороны крови и лимфатической системы:
Очень часто: нейтропения, лимфопения, лейкопения, тромбоцитопения, анемия.
Редко: тромботическая микроангиопатия, включающая тромботическую тромбоцитопеническую пурпуру/гемолитико-уремический синдром* (является класс-эффектом интерферонов; см. раздел «Особые указания»), панцитопения*.
Нарушения со стороны иммунной системы:
Редко: анафилактические реакции*.
Нарушения со стороны эндокринной системы:
Нечасто: нарушение функции щитовидной железы, наиболее часто проявляющееся в виде гипо- или гипертиреоза (см. раздел «Особые указания»).
Нарушения со стороны печени и желчевыводящих путей:
Очень часто: бессимптомное повышение активности трансаминаз в крови.
Часто: значительное повышение активности трансаминаз в крови.
Нечасто: гепатит (с желтухой или без нее)*.
Редко: печеночная недостаточность*, аутоиммунный гепатит*.
Психические нарушения:
Часто: депрессия, бессонница.
Редко: суицидальные попытки (см. раздел «Особые указания»).
Нарушения со стороны нервной системы:
Очень часто: головная боль.
Нечасто: судороги* (см. раздел «Особые указания»).
Частота неизвестна: преходящие неврологические симптомы (гипестезия, мышечные спазмы, парестезия, затруднения при ходьбе, ригидность мышц), которые могут имитировать обострение рассеянного склероза*.
Нарушения со стороны органа зрения:
Нечасто: поражение сосудов сетчатки (т.е. ретинопатия, «ватные пятна» на сетчатке, обструкция артерии или вены сетчатки)*.
Нарушения со стороны сосудистой системы:
Нечасто: тромбоэмболия*.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: Нечасто: одышка*.
Частота неизвестна: артериальная легочная гипертензия (класс-эффект, см. ниже «Артериальная легочная гипертензия»)
Нарушения со стороны желудочно-кишечного тракта:
Часто: диарея, рвота, тошнота.
Нарушения со стороны кожи и подкожных тканей:
Часто: зуд, сыпь, эритематозная сыпь, макулопапулезная сыпь, алопеция*.
Нечасто: крапивница*.
Редко: отек Квинке*, мультиформная эритема*, кожная реакция, напоминающая мультиформную эритему*, синдром Стивенса-Джонсона*.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
Часто: миалгия, артралгия.
Редко: лекарственная красная волчанка*.
Нарушения со стороны почек и мочевыделительной системы:
Редко: нефротический синдром*, гломерулосклероз* (см. раздел «Особые указания»).
Общие расстройства и нарушения в месте введения:
Очень часто: воспаление в месте инъекции, реакции в месте инъекции, например, кровоподтек, припухлость в месте инъекции, отек, покраснение), гриппоподобные симптомы.
Часто: боль в месте введения, утомляемость, озноб, лихорадка.
Нечасто: некроз в месте инъекции, припухлость в месте инъекции, абсцесс в месте инъекции, инфицирование места инъекции*, усиление потоотделения*.
Редко: флегмона в месте инъекции*.
Дети
Отдельные клинические или фармакокинетические исследования для детей и подростков не проводились. Однако опубликованные данные по применению интерферона бета-1а у подростков от 12 до 16 лет, получавших интерферон бета-1а в дозе 22 мкг 3 раза в неделю подкожно, позволяют предположить, что профиль безопасности препарата Тебериф® в этой группе аналогичен таковому у взрослых пациентов.
Класс-эффекты
Применение интерферонов связано с потерей аппетита, головокружениями, беспокойством, аритмией, расширением кровеносных сосудов и учащенным сердцебиением, меноррагией и метроррагией.
В ходе лечения интерфероном бета может происходить усиленное образование антител.
Артериальная легочная гипертензия
На фоне применения препаратов интерферона бета регистрировались случаи артериальной легочной гипертензии. Данные случаи регистрировались на разных этапах лечения, в том числе через несколько лет после начала терапии интерфероном бета.
Необходимо информировать врача о любых перечисленных выше нежелательных реакциях, а также о тех, которые не указаны в данной инструкции. При сохранении нежелательных реакций в течение длительного времени или в случае развития тяжелых нежелательных реакций по усмотрению врача допускается временное снижение дозы препарата или прерывание лечения.
Не следует прекращать лечение или изменять дозу без указания лечащего врача.
Передозировка:
При введении пациентом большей чем предписана дозы следует немедленно сообщить об этом лечащему врачу. При необходимости в случае передозировки пациента следует госпитализировать для дальнейшего наблюдения и проведения поддерживающей терапии.
Взаимодействие:
Специально спланированные клинические исследования по изучению взаимодействия интерферона бета-1а с другими лекарственными средствами не проводились. Однако известно, что в организме людей и животных интерфероны снижают активность цитохром-Р450-зависимых ферментов печени. Поэтому следует соблюдать осторожность при назначении препарата Тебериф® одновременно с лекарственными средствами, имеющими узкий терапевтический индекс, клиренс которых в значительной степени зависит от цитохромовой Р450 системы печени, например, с противоэпилептическими средствами и некоторыми антидепрессантами.
Систематическое изучение взаимодействия интерферона бета-1а с кортикостероидами или адренокортикотропным гормоном (АКТГ) не проводилось. Данные клинических исследований указывают на возможность получения больными рассеянным склерозом интерферона бета-1а и кортикостероидов или АКТГ во время обострений заболевания.
Особые указания:
Пациентов следует проинформировать относительно наиболее частых побочных действий, связанных с приемом интерферона бега, включая гриппоподобные симптомы (см. раздел «Побочное действие»), которые бывают особенно выраженными в начале лечения и уменьшаются по частоте и выраженности по мере продолжения лечения.
Тромботическая микроангиопатия (ТМА)
Имеется информация о случаях тромботической микроангиопатии, которые проявлялись в виде тромботической тромбоцитопенической пурпуры или гемолитико-уремического синдрома, включая случаи с летальным исходом. Такие случаи регистрировались в различные периоды времени, от нескольких недель до нескольких лет после начала лечения интерфероном бета-1а. Рекомендуется проводить мониторинг ранних симптомов, таких как тромбоцитопения, вновь возникающие случаи гипертензии, лихорадка, нарушения со стороны центральной нервной системы (например, спутанное сознание, парез) и снижение почечной функции. Лабораторные данные при предположительном диагнозе ТМА включают снижение числа тромбоцитов, увеличение сывороточной активности лактатдегидрогеназы (ЛДГ), вызванное гемолизом и шизоцитами (фрагменты эритроцитов) в мазке крови. Если наблюдаются клинические признаки ТМА, рекомендуется провести определение содержания тромбоцитов; сывороточной ЛДГ, взять мазок крови и оценить почечную функцию. Если диагноз ТМА подтверждается, требуется немедленное лечение (может потребоваться переливание плазмы) и прекращение лечения интерфероном бета-1а.
Депрессии и суицидальные идеи
Препарат Тебериф® должен с осторожностью назначаться пациентам, находящимся или перенесшим депрессивные состояния. Депрессивные и суицидальные состояния с повышенной частотой наблюдаются в группе пациентов, страдающих рассеянным склерозом и принимающих интерферон.
Пациентов необходимо предупредить о том, что им следует немедленно сообщить о любых симптомах депрессии и/или появлении суицидальных идей лечащему врачу. Лечение больных, страдающих депрессией, препаратом Тебериф® должно проходить в условиях пристального контроля и предоставления им необходимой помощи. В ряде случаев может встать вопрос о прекращении лечения препаратом.
Судорожный синдром
Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с эпилептическими припадками в анамнезе, особенно если течение этого заболевания не полностью контролируется противоэпилептическими препаратами.
Сердечно-сосудистые заболевания
На первых этапах лечения препаратом Тебериф® необходимо строгое наблюдение за пациентами, страдающими сердечно-сосудистыми заболеваниями, такими как стенокардия, застойная сердечная недостаточность и нарушения ритма. Это наблюдение должно быть направлено на своевременное выявление возможного ухудшения состояния. При заболеваниях сердца гриппоподобные симптомы, связанные с терапией интерфероном бета-1а, могут оказаться серьезной нагрузкой для больных.
Некроз в месте инъекций
Имеются единичные сообщения о некрозе в месте инъекций. Чтобы свести до минимума риск развития некроза необходимо строгое соблюдение правил асептики при выполнении инъекции и смена места введения после каждой инъекции. Необходимо регулярно оценивать технику самостоятельного введения препарата пациентами, особенно при возникновении реакций в месте инъекций. Если отмечается повреждение кожи с отеком и выделением жидкости в месте инъекции, необходимо обратиться к врачу прежде, чем продолжать введение препарата. При множественных повреждениях кожи следует отменить препарат до их заживления. При единичном поражении возможно продолжение терапии препаратом Тебериф®, при условии, что поражение выражено умеренно.
Нарушения функции печени
В клинических испытаниях продемонстрировано бессимптомное повышение активности печеночных трансаминаз, особенно аланинаминотрансферазы (АЛТ), а у 1-3% пациентов содержание печеночных трансаминаз превышало верхние пределы нормы (ВПН) более чем в 5 раз. При отсутствии клинической симптоматики необходимо контролировать активность АЛТ в плазме до начала применения интерферона бета-1а, в 1-й, 3-й и 6-й месяцы от его начала, а также периодически в ходе дальнейшего лечения. Необходимо снизить дозу препарата, если активность АЛТ превысит в 5 раз верхнюю границу нормы, и постепенно увеличивать дозу после ее нормализации. Необходимо соблюдать осторожность при назначении препарата Тебериф® пациентам с выраженной печеночной недостаточностью в анамнезе, с признаками заболевания печени, с признаками злоупотребления алкоголем, активностью АЛТ в 2,5 раза превышающей верхнюю границу нормы. Терапию препаратом Тебериф® необходимо прекратить при появлении желтухи или других клинических симптомов нарушения функции печени.
Тебериф®, как и другие интерфероны бета, потенциально может вызывать тяжелое поражение печени, в том числе, острую печеночную недостаточность. Тяжелые нарушения функции печени главным образом возникают в первые 6 месяцев терапии. Механизм этих состояний неизвестен, специфические факторы риска не выявлены.
Нарушение функции почек и мочевыводящей системы
Нефротический синдром
В ходе лечения интерфероном бета-1а и другими интерферонами бета могут иметь место случаи нефротического синдрома с различными нефропатиями, включая очаговый сегментарный гломерулосклероз (ОСГС), мембранопролиферативный гломерулонефрит и мембранную гломерулопатию. Случаи имели место как в процессе лечения, так и через несколько лет после его завершения. Рекомендуется проводить периодический мониторинг ранних признаков или симптомов (например, отеки, протеинурия или нарушение функции почек) особенно у пациентов с высоким риском возникновения заболеваний почек. Нефротический синдром требует немедленного лечения и прекращения приема препарата Тебериф®.
Нарушение лабораторных показателей
В дополнение к лабораторным анализам, которые всегда проводятся пациентам с рассеянным склерозом, рекомендуется в 1-й, 3-й и 6-й месяцы с момента начала терапии препаратом Тебериф®, а также, периодически, при отсутствии клинической симптоматики, в ходе дальнейшего лечения определять общий клинический анализ крови с лейкоцитарной формулой, содержание тромбоцитов, а также проводить биохимическое исследование крови, включая функциональные пробы печени.
Заболевания щитовидной железы
У пациентов, получающих интерферон бета-1а, иногда могут развиваться или усугубляться имеющиеся патологические изменения щитовидной железы. Рекомендуется проводить исследование функции щитовидной железы непосредственно до начала лечения и, при выявлении нарушений, каждые 6-12 мес. с момента его начала. Если до начала лечения функция щитовидной железы в норме, то периодические исследования ее функции не требуются, однако их проведение необходимо при появлении клинических признаков дисфункции щитовидной железы.
Выраженные нарушения функции почек и печени и выраженная миелосупрессия
Следует соблюдать осторожность при назначении препарата пациентам с выраженной почечной недостаточностью и миелосупрессией.
Нейтрализующие антитела
У пациентов, получающих интерфероны бета, возможно образование нейтрализующих антител. Клинические данные позволяют предположить, что после 24-48 месяцев лечения интерфероном бета-1а 44 мкг примерно у 13-14% (24% для 22 мкг) пациентов в сыворотке крови появляются нейтрализующие антитела на интерферон бета-1а. Присутствие антител связывают со снижением эффективности лечения, что подтверждается МРТ исследованием и клиническими показателями. Полная клиническая значимость выработки нейтрализующих антител еще недостаточно изучена.
Образование нейтрализующих антител связывают с реакцией на наличие различных форм интерферона бета. Если у пациента недостаточно хороший ответ на терапию препаратом Тебериф®, и это связано с устойчивым наличием нейтрализующих антител, врач должен оценить целесообразность продолжения терапии интерфероном. Использование различных методов для обнаружения антител в сыворотке и определения их характеристик ограничивает возможность сравнения иммуногенности различных препаратов.
Другие формы рассеянного склероза
По неамбулаторным пациентам, страдающим рассеянным склерозом, доступны лишь отдельные данные по безопасности и эффективности препарата. Использование интерферона бета-1а у пациентов с первичным прогрессирующим рассеянным склерозом до настоящего времени не изучалось, поэтому препарат не должен применяться при данном заболевании.
Меры предосторожности при применении
Не требует особых мер предосторожности при использовании.
Влияние на способность управлять транспортными средствами и механизмами:
Побочные реакции со стороны центральной нервной системы на проводимую терапию интерферонами (см. «Возможные побочные действия при применении») могут влиять на способность к управлению автомобилем и техникой.
Форма выпуска/дозировка:
Раствор для подкожного введения 22 мкг/ 0,5 мл, 44 мкг/0,5 мл.
Упаковка:
По 0,5 мл в шприцы из бесцветного стекла I гидролитического класса. По 1 шприцу в контурную ячейковую упаковку. По 3 или 12 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению помещают в пачку из картона. Пачка со шприцами дополнительно комплектуется спиртовыми салфетками в количестве 3 или 12 шт.
Условия хранения:
Хранить при температуре от 2 до 8 °С в защищенном от света месте.
Не замораживать.
Хранить в недоступном для детей месте.
Срок годности:
2 года. Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
Закрытое акционерное общество «БИОКАД» (ЗАО «БИОКАД»), 143422, Московская обл., Красногорский район, с. Петрово-Дальнее, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ЗАО «БИОКАД»
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Interferon beta-1a
Фармакологическое действие
Интерферон бета-1a (IFN-β1a) — представляет собой природную аминокислотную последовательность интерферона β человека, полученную методами генной инженерии с использованием культуры клеток яичника китайского хомячка. Обладает иммуномодулирующими, противовирусными и антипролиферативными свойствами. Механизм действия препарата интерферона бета-1а у больных рассеянным склерозом до конца не изучен. Показано, что препарат способствует ограничению повреждений центральной нервной системы, лежащих в основе заболевания, снижает частоту и тяжесть обострений у больных с ремиттирующей формой рассеянного склероза.
Фармакокинетика
При подкожном введении концентрация интерферона бета-1a в сыворотке крови определяются в течение 12–24 часов после инъекции. После однократной инъекции дозы 60 мкг максимальная концентрация, определяемая иммунологическими методами, составляет 6–10 ME/мл через 3 часа после введения. При 4-кратном подкожном введении одной и той же дозы каждые 48 часов происходит умеренное аккумулирование препарата. После однократного введения внутриклеточная и сывороточная активность 2-5A синтетазы и сывороточные концентрации β2-микроглобулина и неоптерина (маркёры биологического ответа) повышаются в течение 24 часа, а затем снижаются в течение 2 дней. Интерферон бета-1a метаболизируется и выводится печенью и почками.
Показания
Рецидивирующий рассеянный склероз (при наличии не менее 2 рецидивов неврологической дисфункции в течение 3 лет и отсутствии признаков непрерывного прогрессирования заболевания между рецидивами).
Противопоказания
- Повышенная чувствительность к эндогенному или рекомбинантному интерферону бета, сывороточному альбумину человека;
- тяжёлая депрессия и/или суицидальные идеи;
- эпилепсия в случае отсутствия эффекта от применения соответствующей терапии;
- беременность;
- лактация;
- возраст до 16 лет.
С осторожностью
- Депрессивные состояния (и суицидальные идеи);
- стенокардия;
- нарушения ритма;
- застойная сердечная недостаточность.
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — C.
Адекватных и строго контролируемых исследований по безопасности применения интерферона бета-1a при беременности не проведено.
В период лечения интерфероном бета-1a женщины репродуктивного возраста должны пользоваться надёжными методами контрацепции.
В случае наступления беременности, отсутствия менструации или при подозрении на возможную беременность пациентка должна сообщить об этом своему лечащему врачу.
Применение интерферона бета-1a во время беременности не рекомендуется, за исключением случаев отсутствия альтернатив, по назначению врача и, если потенциальная польза для матери превышает возможный риск для плода.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения интерферона бета-1a в период грудного вскармливания не проведено.
Не известно, выводится ли интерферон бета-1a с грудным молоком.
Рекомендуется прекратить кормление грудью в случае применения препарата.
Способ применения и дозы
Режим дозирования индивидуальный, в зависимости от показаний, схемы терапии, способа введения, переносимости препарата и лекарственной формы.
Подкожно.
Рекомендуемая доза — по 22–44 мкг 3 раза в неделю в одно и то же время (желательно вечером), в определённые дни недели, с интервалом не менее 48 часов.
При первом применении рекомендуется вводить в течение первых 2 недель в разовой дозе 8,8 мкг, в течение 3-й и 4-й недели — 22 мкг, начиная с 5-й недели и далее — 44 мкг.
Побочные действия
Гриппоподобные симптомы
Приблизительно у 40 % пациентов в течение первых 6 месяцев на фоне терапии интерфероном бета-1a может наблюдаться типичный для интерферонов гриппоподобный синдром (головная боль, лихорадка, озноб, мышечные и суставные боли, тошнота
Со стороны пищеварительной системы
Редко — диарея, потеря аппетита, рвота, поражение печени.
Со стороны центральной нервной системы
Редко — нарушение сна, головокружение, нервозность; в единичных случаях — депрессия, суицидальные идеи, деперсонализация, а также судорожные припадки.
Со стороны сердечно-сосудистой системы
Редко — периферическая вазодилатация, сердцебиение; в единичных случаях — нарушения сердечного ритма.
Со стороны лабораторных показателей
Возможно отклонение от нормы лабораторных показателей, проявляющиеся лейкопенией, лимфопенией, тромбоцитопенией, повышением активности аланинаминотрансферазы (AЛT), γ-глутамилтрансферазы и щелочной фосфатазы. Эти изменения обычно бывают незначительными и обратимыми. Могут наблюдаться симптомы нарушений со стороны печени, такие как потеря аппетита, тошнота, рвота, желтуха.
Реакции со стороны эндокринной системы
Интерфероны могут оказывать влияние на функцию щитовидной железы, как в сторону повышения, так и угнетения. Эти изменения могут быть незаметны для пациента, но врач может назначить дополнительное обследование.
Депрессия
У больных рассеянным склерозом возможно развитие депрессии.
Местные реакции
Покраснение, припухлость, побледнение кожи, болезненность (обычно незначительно выражены и имеют обратимый характер); в единичных случаях в месте инъекции может наблюдаться некроз, который обычно проходит самостоятельно.
Прочие
Редко — кожная сыпь, крапивница.
Передозировка
Случаи передозировки препарата не выявлены.
Взаимодействие
В организме людей и животных интерфероны снижают активность цитохром P450-зависимых ферментов печени. Поэтому следует соблюдать осторожность при назначении интерферона бета-1a одновременно с лекарственными средствами, имеющими узкий терапевтический индекс, клиренс которых в значительной степени зависит от цитохрома P450, например, с противоэпилептическими средствами и некоторыми антидепрессантами.
Систематическое изучение взаимодействия интерферона бета-1a с глюкокортикостероидами или адренокортикотропным гормоном (АКТГ) не проводилось.
Данные клинических исследований указывают на возможность получения больными рассеянным склерозом интерферона бета-1a и глюкокортикостероидов или АКТГ во время обострений заболевания.
Меры предосторожности
На первых этапах лечения необходимо строгое наблюдение за пациентами со стенокардией, застойной сердечной недостаточностью, аритмией. При заболеваниях сердца развитие гриппоподобного синдрома, связанного с терапией интерфероном бета-1a, может способствовать ухудшению состояния больных.
С осторожностью и под строгим контролем врача следует назначать препарат пациентам с тяжёлой почечной и печёночной недостаточностью, а также с выраженной миелосупрессией.
С осторожностью применять у пациентов с депрессией. Больных необходимо предупредить о том, что им следует немедленно сообщить врачу о любых симптомах депрессии и/или появлении суицидальных идей. Лечение больных с депрессией следует проводить под строгим контролем врача и в случае необходимости назначать соответствующую терапию. В ряде случаев может потребоваться прекращение лечения интерфероном бета-1a.
Следует с осторожностью применять у пациентов с указанием в анамнезе на судороги. При возникновении во время лечения судорог у больных, ранее не страдавших такими нарушениями, необходимо отменить интерферон бета-1a, установить их этиологию и назначить противосудорожную терапию прежде, чем возобновить лечение интерфероном бета-1a.
Больного следует предупредить о том, что при интенсивных или стойких проявлениях любого из гриппоподобных симптомов следует сообщить об этом врачу.
В случае выраженных побочных реакций или сохранения их в течение длительного времени по усмотрению врача допускается временное снижение дозы или прерывание лечения.
Пациенту не следует самостоятельно прекращать лечение или изменять дозу.
В дополнение к лабораторным исследованиям, которые всегда проводятся пациентам с рассеянным склерозом, в период лечения интерфероном бета-1a рекомендуется определять полную и лейкоцитарную формулу крови, содержание тромбоцитов, а также проводить биохимическое исследование крови, включая функциональные пробы печени.
Влияние на способность к вождению автотранспорта и управлению механизмами
Следует соблюдать осторожность при вождении автомобиля и занятиях другими потенциально опасными видами деятельности, требующими повышенного внимания и быстроты психомоторных реакций.
Классификация
-
АТХ
L03AB07
-
Фармакологические группы
-
Код МКБ 10
-
Категория при беременности по FDA
C
(риск не исключается)
Информация о действующем веществе Интерферон бета-1a предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Интерферон бета-1a, содержатся в инструкции производителя, прилагаемой к упаковке.
Состав
Активное вещество — интерферон бета-1а.
Вспомогательные компоненты: альбумин человеческий, маннитол, натрия хлорид, двухосновной натрия фосфат, вода стерильная.
Форма выпуска
Раствор прозрачный желтоватого цвета, свободный от примесей для п/к введения в шприце в пластиковом контейнере в картонной пачке №3.
Фармакологическое действие
Иммуномодулирующее, антипролиферативное.
Фармакодинамика и фармакокинетика
Фармакодинамика
Препарат относится к интерферонам I типа, обладает противовирусным, иммуномодулирующим и антипролиферативным эффектом.
Интерферон бета вырабатывается в организме различными видами клеток (макрофаги, фибробласты). Интерферон бета гликолизируется с интерфероном бета-1а, и они имеют единый комплексный углеводородный фрагмент. Механизм действия препарата базируется на его связывании с рецепторами клеток макроорганизма и последующим запуском каскада сложных межклеточных взаимодействий, способствующих интерферон-обусловленной экспрессии различных генных продуктов, в том числе, комплекс гистосовместимости I класса, белок 2’/5′-олигоаденилатсинтетаза, Мх, неоптерин и бета2-микроглобулин. После введения 1 дозы концентрация в сыворотке крови этих соединений остается повышенной на протяжении 4-7 дней.
Фармакокинетика
Концентрация действующего вещества препарата в сыворотке крови после введения достигается через 5 – 15 часов. Генфаксон имеет невысокую биологическую доступность (порядка 40%). Препарат выводится через почки. Период полувыведения — около 10 часов.
Показания к применению
Применяется в комплексном лечении рассеянного рецидивирующего склероза при наличии в анамнезе 2 и более рецидивов неврологической дисфункции на протяжении 3 лет и отсутствии между рецидивами признаков прогрессирования заболевания.
Противопоказания
Высокая чувствительность к препарату, беременность и период лактации, депрессия в выраженной форме, суицидальные мысли, возраст до 12 лет, эпилепсия.
Принимать с осторожностью при наличии в анамнезе нарушений ритма сердца, стенокардии, сердечной недостаточности в стадии декомпенсации, депрессии, судорог, заболеваний щитовидной железы, заболеваний почек/печени с выраженными нарушениями функции.
Побочные действия
Тошнота, озноб, лихорадка, головная боль, суставные и мышечные боли, рвота, диарея, потеря аппетита, нервозность, головокружение, нарушение сна, суицидальные мысли, деперсонализация, депрессия, судорожные припадки, сердцебиение, покраснение/побледнение кожи, припухлость в месте введения препарата, крапивница, кожная сыпь, лимфоцитопения, тромбоцитопения, лейкопения, повышение уровня ГГТ, АЛТ.
Генфаксон, инструкция по применению (Способ и дозировка)
Препарат вводится подкожно из расчета 44 мкг 3 раза в неделю при его хорошей переносимости, при плохой переносимости дозировка уменьшается до 22 мкг. Инъекции желательно выполнять в определенные дни недели в одно и то же время с перерывом не менее 2-х суток.
При первичном назначении рекомендуется на протяжении первых 2 недель вводить в дозировке 8,8 мкг, на протяжении 3-4 недели 22 мкг, а с пятой недели вводить всю дозу — 44 мкг. Пациентам с лейкопенией и заболеваниями печени дозировку уменьшают на 20-50%.
Передозировка
Достоверных данных о клинически выраженной симптоматики при приеме препарата в высоких дозах нет.
Взаимодействие
Вводить интерферон бета-1a совместно с ЛС, метаболизм которых происходит при участии изоферментов системы цитохрома Р450 указанных ферментов, в том числе с некоторыми антидепрессантами и противосудорожными препаратами следует крайне осторожно.
Условия продажи
Рецептурная продажа.
Условия хранения
Не замораживать, хранить при температуре 2-8 °C. Транспортировать при температуре до 25 °C в оригинальной упаковке.
Срок годности
2 года.
Аналоги
Совпадения по коду АТХ 4-го уровня:
К препаратам с аналогичным фармакологическим действием относятся: Альтевир, Герпферон, Ингарон, Альфарона, Интерфераль, Лайфферон, Диаферон, Инфибета, Ронбетал и другие.
Отзывы о Генфаксоне
Отзывы о препарате диаметрально противоположные, от резко отрицательных до крайне восторженных. Это обусловлено тем, что на некоторых пациентов препарат действует очень эффективно, вызывая минимум побочных действий, а у других пациентов эффект практически отсутствует. Поэтому препарат следует подбирать с учетом реакций пациента. Однако, если при первом назначении Генфаксона эффект отсутствует, не стоит категорически от него отказываться и считать неподходящим вам.
Это может быть связано с тем, что Генфаксон из разных партий может оказаться эффективным для вас. Так как активное вещество Генфаксона синтезируется живыми клетками, то технологически невозможно создавать всегда идентичные условия. Поэтому разные партии препарата одного производителя, производимые по одной технологии имеют различия.
Некоторые пациенты интересуются, какой из препаратов Генфаксон или Рефиб более эффективен. Ребиф является препаратом синонимом, который выпускается в форме раствора и имеет аналогичное терапевтическое действие.
Цена Генфаксона, где купить
Средняя цена Генфаксона с дозировкой 12000000 МЕ варьирует в пределах 7500 – 11000 рублей за упаковку, препарат с дозировкой 6000000 МЕ — 5500 – 6500 рублей за упаковку. Купить Генфаксон можно в большинстве аптек Москвы и других городах.
В интернете можно встреть объявления о продаже Генфаксона по ценам значительно ниже рыночных. Покупать препарат «с рук» не рекомендуется, поскольку неизвестны условия его хранения.
-
По рецепту
Внешний вид товара может отличаться
Ребиф раствор для подкожного введения 44 мкг/0,5 мл 12 млн.ЕД шприц 3 шт.
Товара нет в наличии.
🏥 Купить Ребиф раствор для подкожного введения 44 мкг/0,5 мл 12 млн.ЕД шприц 3 шт. в наших аптеках в Москве
💊 Ребиф раствор для подкожного введения 44 мкг/0,5 мл 12 млн.ЕД шприц 3 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки
- Форма выпуска:раствор
- Дозировка:44 мкг/0,5 мл
Перейти к формам выпуска
Это термолабильный препарат — перевозится в специальном контейнере, для сохранения оптимальной температуры.
Учтите это при самовывозе.
Доставка и самовывоз только по Москве
все
товары Ребиф,
2 шт.
🏥 Купить Ребиф раствор для подкожного введения 44 мкг/0,5 мл 12 млн.ЕД шприц 3 шт. в наших аптеках в Москве
💊 Ребиф раствор для подкожного введения 44 мкг/0,5 мл 12 млн.ЕД шприц 3 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки