|
1 |
Кожа |
56 |
Скуловая кость, дуга (а) |
|
|
2 |
Жировая клетчатка |
57 Верхняя челюсть, твердое небо (а) |
||
|
3 |
Артефакты |
58 |
Нижняя челюсть, головка сус- |
|
|
4 |
Воздух/газ |
59 |
тавного отростка (а) |
|
|
5 |
Фасция, перегородка, соедини- |
Носовая перегородка, носовая |
||
|
тельная ткань |
кость (а) |
|||
|
6 |
Лимфоузел (ЛУ) |
60 |
Клиновидная кость |
|
|
7 |
Опухоль, метастаз |
61 |
Слуховые косточки: молоточек |
|
|
8 |
Выпот, кровоизлияние |
62 |
(а), наковальня (b), стремя (с) |
|
|
9 |
Костные трабекулы |
Ячейки сосцевидного отростка |
||
|
10 |
Грудиноключичнососцевидная |
63 |
Слуховой проход, внутренний |
|
|
11 |
мышца |
64 |
(а) и наружный (b) |
|
|
Грудиноподъязычная / грудино- |
Каротидный канал |
|||
|
12 |
щитовидная мышца |
65 |
Канал лицевого нерва |
|
|
Лестничная мышца |
66 |
Барабанная полость, барабан- |
||
|
13 |
Дельтовидная мышца |
67 |
ная перепонка (а) |
|
|
14 |
Широчайшая мышца спины |
Слуховая труба, глоточное |
||
|
15 |
Большая круглая мышца |
68 |
углубление (устье) |
|
|
16 |
Малая круглая мышца |
Улитка |
||
|
17 |
Мышца, поднимающая лопатку |
69 |
Преддверие |
|
|
18 |
Подлопаточная мышца |
70 |
Полукружные каналы: латераль- |
|
|
19 |
Надостная мышца |
71 |
ный (а), передний (b), задний (с) |
|
|
20 |
Подостная мышца |
Шилососцевидное отверстие |
||
|
21 |
Ромбовидная мышца |
72 |
(а), шиловидный отросток (b) |
|
|
22 |
Мышца, выпрямляющая |
Лицевой нерв |
||
|
23 |
позвоночник |
73 |
Клиновидная пазуха |
|
|
Трапециевидная мышца |
74 |
Ячейки решетчатой кости |
||
|
24 |
Передняя зубчатая мышца |
75 |
Верхнечелюстная пазуха |
|
|
25 |
Ременная мышца |
76 |
Лобная пазуха |
|
|
26 Длинная мышца шеи / головы |
77 |
Полость носа |
||
|
27 Длиннейшая мышца шеи / головы |
78 |
Зрительный канал / нерв |
||
|
28 |
Полуостистая мышца головы |
79 |
Крылонебная ямка |
|
|
29 |
Полуостистая мышца шеи |
80 |
Большое затылочное отверстие |
|
|
30 |
Многораздельная мышца |
81 Трахея: бифуркация (а), бронхи (b) |
||
|
31 |
Двубрюшная мышца |
82 |
Пищевод |
|
|
32 Прямая / косая мышца головы |
83 |
Щитовидная железа |
||
|
33 |
Подбородочно-язычная мышца |
84 |
Легкое |
|
|
34 |
Подбородочно-подъязычная |
85 |
Общая сонная артерия, внут- |
|
|
35 |
мышца |
86 |
ренняя (а), наружная (b) |
|
|
Мышцы-сжиматели глотки: |
Яремная вена, внутренняя (а), |
|||
|
нижняя (а), медиальная (b) |
87 |
наружная (b), передняя (с) |
||
|
36 Латеральная (а) и медиальная |
Верхняя щитовидная артерия |
|||
|
37 |
(b) крыловидные мышцы |
88 |
Позвоночная артерия |
|
|
Мышца, поднимающая небо |
89 Ветви лицевой / угла глаза арте- |
|||
|
38 |
Мышца, напрягающая небо |
90 |
рии / вены |
|
|
39 |
Небноглоточная мышца |
Базилярная артерия |
||
|
40 |
Щитовидноподъязычная мышца |
91 Мозговые артерии: передняя (а), |
||
|
41 |
Шилоподъязычная мышца |
92 |
средняя (b), задняя (с) |
|
|
42 |
Жевательная мышца |
Соединительные артерии: пере- |
||
|
43 |
Височная мышца |
93 |
дняя (а), средняя (b) |
|
|
44 |
Щечная мышца |
Артерии мозолистого тела |
||
|
45 |
Круговая мышца рта |
94 |
Артерии островка |
|
|
46 |
Мышца, поднимающая веко / |
95 |
Мозжечковые артерии: верхняя |
|
|
47 |
круговая мышца глаза |
96 |
(а), передненижняя (b) |
|
|
Мышцы глазного яблока: верх- |
Поверхностные височные сосуды |
|||
|
няя прямая (а), нижняя прямая |
97 |
Артерия языка |
||
|
(b), внутренняя прямая (с), на- |
98 |
Восходящая глоточная артерия |
||
|
ружная прямая (d), верхняя ко- |
99 |
Позадичелюстная вена |
||
|
48 |
сая (е), нижняя косая (f) |
100 |
Большая вена мозга (Галена) |
|
|
Подкожная мышца шеи, мышца |
101 Сагиттальный синус, верхний |
|||
|
49 |
смеха |
(а), затылочный (b) |
||
|
Мышца, поднимающая верхнюю |
102 Поперечный синус, прямой |
|||
|
50 |
губу, мышца угла носа |
103 |
синус (а) |
|
|
Тела позвонков: атлант (а), зуб |
Сигмовидный синус |
|||
|
осевого позвонка (b), остистый |
104 |
Мозжечок |
||
|
отросток (с), межпозвоночный |
105 Червь мозжечка |
|||
|
сустав (d), межпозвоночный |
106 |
Средний мозг |
||
|
диск (е), поперечный или ребер- |
107 |
Мост, продолговатый мозг |
||
|
51 |
ный отросток (f) |
108 |
Ножки мозжечка |
|
|
Ребро |
109 |
Ножки мозга |
||
|
52 |
Ключица |
110 |
Височная доля |
|
|
53 Лопатка: акромион (а), ость ло- |
111 |
Лобная доля |
||
|
патки (b), клювовидный отросток |
112 Затылочная доля, полосы коры (а) |
|||
|
54 |
(с), суставная ямка (d) |
113 |
Теменная доля |
|
|
Позвоночный |
канал (внутри |
114 |
Сосцевидные тела |
|
|
55 |
спинной мозг) |
черепа: лобная |
115 |
Ангулярная извилина |
|
Кости свода |
116 |
Мозолистое тело |
||
|
кость (а), височная кость (b), те- |
117 |
Хвостатое ядро |
||
|
менная кость (с), затылочная |
118 |
Скорлупа |
||
|
кость (d) |
119 |
Бледный шар |
120Таламус
121Внутренняя капсула
122Наружная капсула
123Сосудистое сплетение
124Глазничная щель
125Островок
126Поясная извилина
127Латеральная (Сильвиева) борозда
128Центральная борозда, прецентральная (а)
129Прецентральная доля (а), постцентральная (b)
130Серп мозга
131Намет мозжечка
132Спинномозговая жидкость (ликвор)
133Боковые желудочки, прозрачная перегородка (а)
134Третий желудочек
135Четвертый желудочек
136Водопровод среднего мозга 137 Базальная цистерна
138Мост / мостомозжечковая цистерна
139Окружающая цистерна
140Цистерна мозолистого тела
141Межжелудочковое отверстие, Монро
142Обонятельная луковица / нерв
143Лучистый венец
144Зрительный тракт
145Зрительный перекрест
146Гипофиз, гипофизарный
147Воронка
148Шишковидное тело
149Свод черепа
150Глазное яблоко, хрусталик (а)
151Слезная железа
152Слезный проток
153Околоушная железа
154Подчелюстная железа
155Язык, подъязычная железа
156Миндалины
157Кольцо Вальдейра
158Зуб
159Подъязычная кость
160Мыщелки затылочной кости
161Крыловидный отросток
162Петушиный гребень
163Турецкое седло
164Наружный затылочный выступ
165Внутренний затылочный выступ
166Носовая раковина
167Перстневидный хрящ
168Черпаловидный хрящ
169Щитовидный хрящ
170Надгортанник
171Черпаловидно-надгортанная складка
172Грушевидная ямка
173Преддверие гортани
174Преддверие рта
175Язычок, мягкое небо
176Глотка
177Голосовые связки
178Голосовая щель
179Выйная связка
180Инфаркт, отек
181Абсцесс, размягчение
182Катетер, дренажная трубка, зонд
183Глубокие сосуды шеи
184Спинальный нерв
185Шейное сплетение
186Ветви тройничного нерва
187Черпаловидно-надгортанная складка
188Перелом
В 1886 году, на следующий год после открытия Вильгельмом Рентгеном «икс-лучей», знаменитый изобретатель Томас Эдисон публично заявил, что намерен получить первый рентгеновский снимок «живого мозга». Однако уже через несколько недель работы великому ученому пришлось признать свою неудачу — ему так и не удалось создать технологию, позволяющую рентгеновским лучам «заглянуть внутрь» плотной структуры костей черепа, сохранив данные о мягкой ткани мозга. Такой возможности человечеству пришлось подождать до конца следующего века, пока в 1972 году не был предложен метод компьютерной томографии.
Сегодня компьютерная томография считается сравнительно простым, доступным и повсеместно используемым диагностическим методом.
Принцип получения изображений
Компьютерная томография базируется на рентгеновском излучении и его детектировании. Это особый вид электромагнитного излучения, которое способно проходить через непрозрачные для обычного света среды. Нужно помнить, что это излучение:
- ослабляется в среде (тканях) тем больше, чем плотнее среда, сквозь которую они прошли;
- имеет непрямой ионизирующий эффект, то есть отрыв электронов от атомов вещества, через которое проходит рентген-излучение, что и обуславливает лучевую нагрузку на пациента при исследовании;
Итак, у нас есть излучатель (рентген-трубка) и детекторы. Наша задача — получить визуальное отображение аксиальных «срезов» тела пациента. Как нам нужно направить луч?
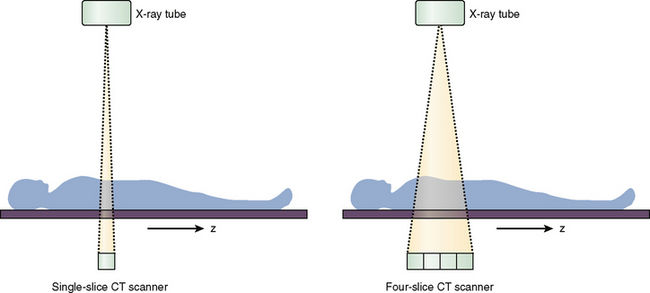
Линию, по которой проходит рентген-излучение от излучателя к детектору, как правило называют осью х, линию, которая проходит, проще говоря, от «право» к «лево» для пациента — осью у, а линию «верх-низ» пациента, то есть толщину среза — осью z.
Рисунок 1 | Направление рентгеновского луча в компьютерном томографе.
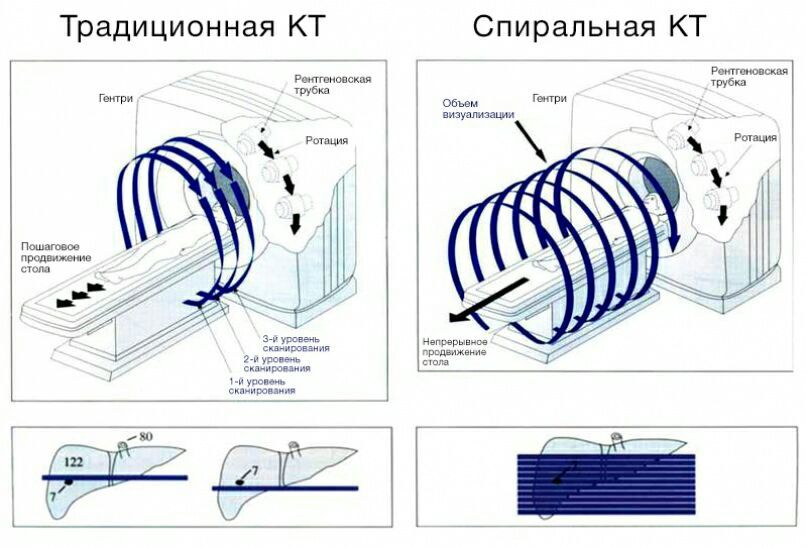
В современном компьютерном томографе рентгеновская трубка совершает спиральное вращение вокруг тела пациента в аксиальной плоскости, постоянно генерируя излучение. Если точнее, трубка вращается по кругу, и одновременно с этим непрерывно смещается вперед или назад стол с пациентом.
В традиционных пошаговых томографах происходит цикл «вращение — шаг стола — вращение».
Рисунок 2 | Принцип работы спирального и пошагового томографов. Основным недостатком пошаговых томографов является то, что при небольшом размере образования и разной глубине вдоха пациента образование может быть «пропущено».
При этом пучок излучения сформирован в виде тонкого веера — широкий по оси у, узкий по оси z. Проходя сквозь тело пациента, рентгеновское излучение ослабляется соответственно плотности ткани, через которую оно прошло, затем попадает на детекторы и регистрируется.
Детекторы в современных КТ-аппаратах расположены в несколько рядов, причем наружный ряд шире, чем внутренний. Это позволяет многократно регистрировать излучение от каждого среза, получая более точные данные и сокращая время исследования. В наиболее распространенных на сегодня типах томографов может быть от 4 или 16 до 320 рядов детекторов, как в представленном фирмой Toshiba в 2007 году AQUILION ONE. Когда Вы слышите термин «16-срезовый КТ», имеется ввиду именно количество рядов детекторов. Детекторы могут быть расположены дугой напротив излучателя и вращаться одновременно с трубкой (томографы 3-го поколения), а могут быть неподвижными и занимать всю окружность, в то время как вращается только рентгеновская трубка (4-е поколение томографов).
А дальше начинается именно то, за что Аллан Кормак и Годфри Хаунсфилд получили Нобелевскую премию в 1979 году: на основе имеющихся данных о том:
- какое количество излучения покинуло рентгеновскую трубку;
- какое количество излучения зарегистрировалось детекторами;
- и где находилась трубка и детекторы в каждый момент времени происходит реконструкция и построение изображений с помощью итеративных алгоритмов.
Для реконструкции используются данные от каждого луча, который проходил через выбранное поле обзора от трубки до детектора. Коэффициент ослабления для каждой точки изображения рассчитывают с помощью усреднения значений ослабления для всех лучей, пересекающих эту точку. Полученные таким образом данные называют исходными, или «сырыми». Эти необработанные данные уже представляют изображения срезов, отображенные в оттенках серой шкалы, однако нуждаются в дальнейшей обработке.
Шкала Хаунсфилда
Во время реконструкции изображения каждому пикселю приписывается числовое значение, выраженное в единицах ослабления, или единицах Хаунсфилда, которое определяется тем, насколько ослабляется луч, проходя через данный воксель (единицу объема) — проще говоря, эта шкала показывает примерную плотность вещества.
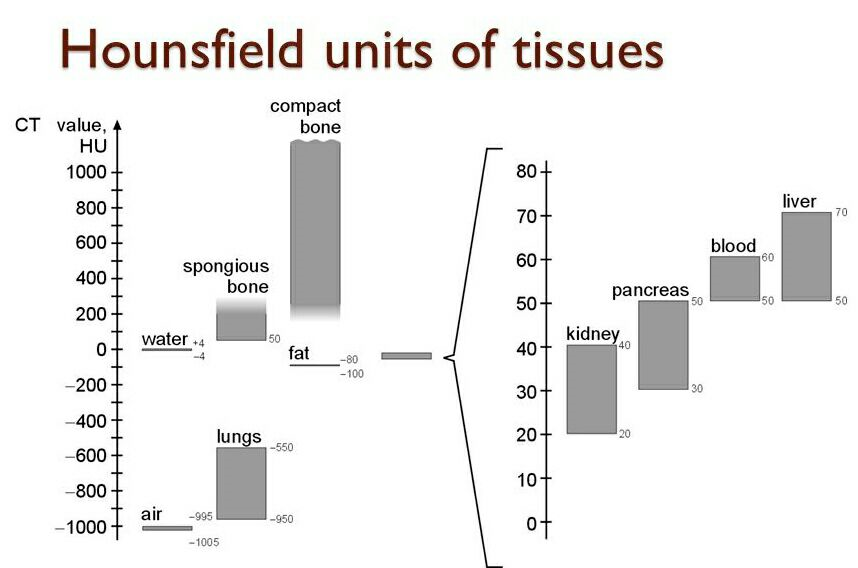
Само изображение среза, каким мы увидим его на экране, получается благодаря тому, что каждый пиксель будет отображен каким-то оттенком серого в зависимости от плотности вокселя и настроек окна. Шкала Хаунсфилда начинается со значения –1000 HU (hounsfield unit) для воздуха, значение 0 HU задано для воды, жир занимает значения от –120 до –90 HU, нормальная ткань печени — 60–70 HU, кровь — 50–60, костная ткань — 250 и выше. Верхний предел шкалы колеблется от +1000 до более чем +3000 для разных томографов. Программы-просмотрщики КТ-изображений всегда имеют возможность вычислить среднюю плотность выделенной области, ведь отличить разницу в 10–15 HU «на глаз» трудно, но разница эта может быть значима, например, для диагностики жирового гепатоза, степени накопления новообразованием контраста и т. д.
Рисунок 3 | Шкала Хаунсфилд.
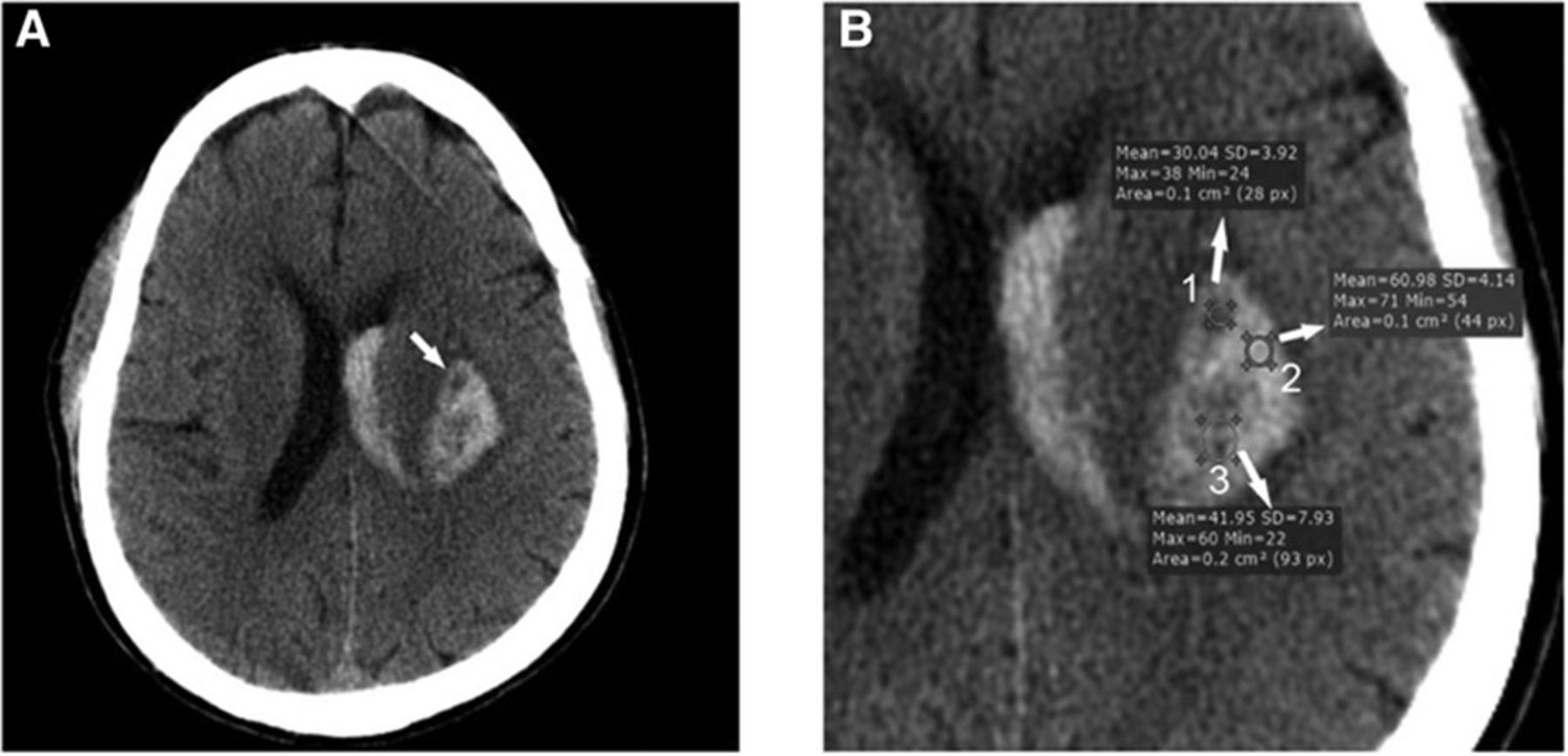
Рисунок 4 | Измерение плотности внутримозговой гематомы: область под номером 2 имеет типичную для крови плотность 60 HU. Область сниженной плотности под номером 1 представляет собой проявление симптома «черной дыры», область под номером 3 представлена как пример неправильного проведения денситометрии (выделенная область интереса гетерогенна, поэтому полученные показатели усреднены).
Функция «окон»
Для визуальной оценки КТ-изображений важны настройки окна. Дело в том, что человеческий глаз не способен различить несколько тысяч оттенков серого, и, чтобы различить близкие по значению плотности, но все же разные структуры, изображение рассматривают в определенном окне. Например, ширина костного окна — 2000 HU, уровень — 500 HU. Это значит, что структуры плотностью 500 HU отобразятся на экране в виде средне-серого цвета, значениям 500 HU до –500 HU будут присвоены оттенки от средне- до очень темно-серого, а структуры плотностью ниже –500 будут отображены слишком темными, чтобы четко их дифференцировать. Структуры плотность выше 1500 HU будут, соответственно, слишком светлыми.
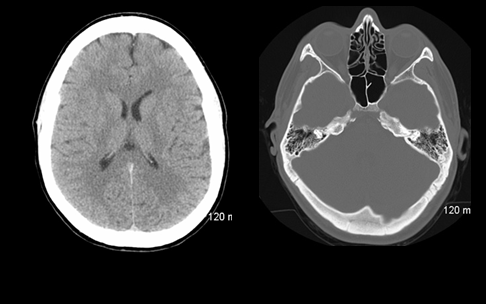
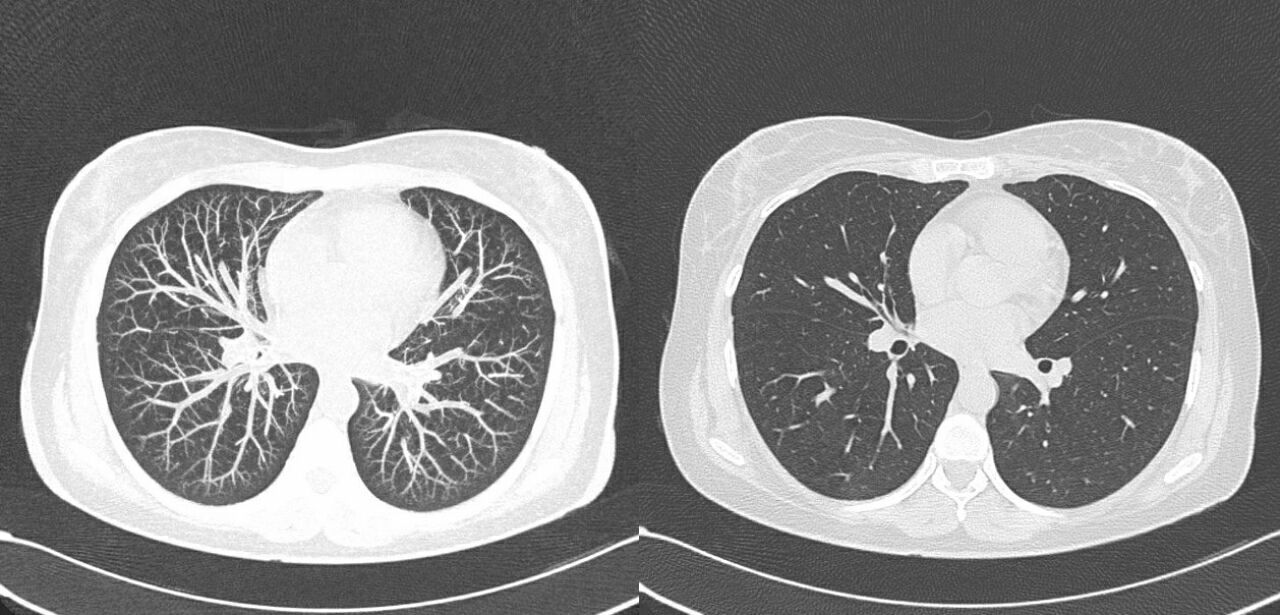
Рисунок 5 | КТ-сканы мозга в «мозговом» (слева) и «костном» (справа) окнах.
Обработка данных
Но вернемся к полученным в результате первичной алгебраической обработки данным. Если перевести «сырые» данные в изображения, то они получатся нерезкими и с размытыми контурами, поэтому для дальнейшей обработки применяют математическую фильтрацию с усилением контуров (конволюцию).
Кернель, или ядро конволюции заложено в протоколе исследования и обработки данных, однако радиолог может менять его по своему усмотрению, задав более «жесткий» или «мягкий» кернель. Например, для сред с высоким естественным контрастом (ткань легкого, костные структуры) применяют жесткий кернель, для органов брюшной полости (низкий естественный контраст) — мягкий. Есть возможность применить разный кернель конволюции к одному и тому же массиву сырых данных, например, после сканирования головы пациента с подозрением на черепно-мозговую травму создать одну серию изображений с жестким кернелем для четкой визуализации костей черепа, а вторую — с мягким кернелем, на ней будут хорошо визуализированы ткани мозга и мозговых оболочек. Каждая серия анализируется радиологом отдельно.
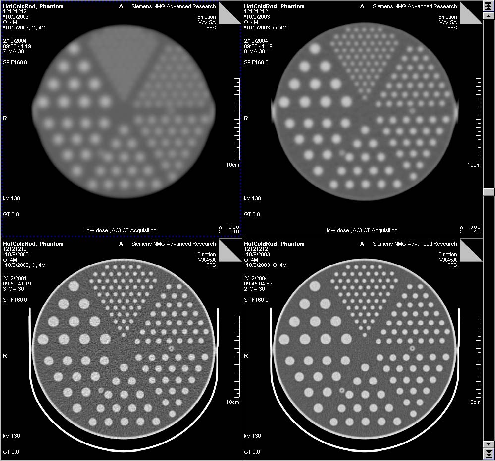
Рисунок 6 | КТ-сканы «фантома» (объекта с внутренней структурой разных плотностей, который используется для проверки и калибровки томографа) с разным кернелем конволюции и силой тока: слева вверху — «мягкий» кернель AC05s, справа вверху — AC10s, внизу слева — стандартный кернель B40s с низкой силой тока 30 mAs, внизу справа — стандартные кернель и сила тока 140 mAs.
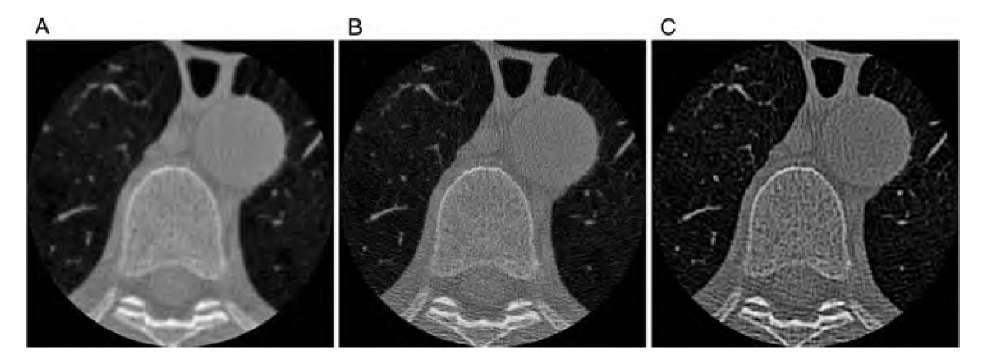
Рисунок 7 | КТ-сканы грудного отдела позвоночника с применением «стандартного» (А), «костного» (В) и «легочного» (С) кернеля конволюции.
Еще один важный параметр реконструкции изображения — толщина среза. Его минимальное значение определено параметрами сканирования (проще говоря, толщиной луча). Тонкие срезы используются там, где нужно визуализировать множество мелких контрастных структур — например, при томографии височной кости. Однако чем тоньше срезы, тем больше время сканирования и лучевая нагрузка на пациента.
Для дальнейшей удобной работы с полученными после первичной обработки исходными данными в КТ применяют инструменты постпроцессинга. Наиболее частые — это мультипланарная реконструкция (MPR), позволяющая из аксиальных сканов построить коронарные и саггитальные изображения.
Проекция максимальной интенсивности (MIP) строится таким образом: для каждой координаты XY представлен только пиксель с наивысшим номером Хаунсфилда вдоль оси z, так что в одном двумерном изображении наблюдаются все самые плотные структуры в данном объеме. MIP используют для визуализации костных структур или контрастированных сосудов.
Рисунок 8 | Аксиальный КТ-скан (слева), корональная (вверху) и саггитальная (внизу) мультипланарные реконструкции.
Рисунок 9 | Использование MIP для просмотра ангиографии сосудов легких.
Другой метод — 3D-рендеринг, позволяющий восстановить из исходных данных, подходящих по определенный критерий (чаще всего это также структуры наивысшей плотности — кости и кровь, содержащая контрастное вещество) трехмерную модель. Работая на станции, радиолог может рассматривать модель со всех сторон и «отрезать» лишние фрагменты изображений. Одним из видов 3D рендеринга является виртуальная эндоскопия — технология, позволяющая вывести в трехмерном изображении полый орган (чаще всего проводят виртуальные колоноскопию и бронхоскопию). Это исследование не заменяет реальной скопической процедуры, но может предоставить дополнительные данные или помочь в планировании реальной процедуры.
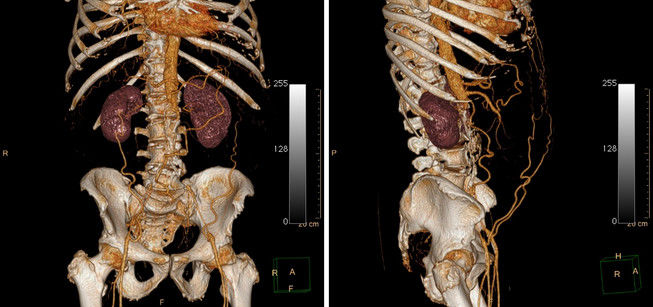
Рисунок 10 | 3D-реконструкция КТ органов брюшной полости и малого таза.
4D-рендеринг широко используется в основном для КТ-исследования сердца. Для этой технологии необходим томограф с возможностью синхронизировать сканирование и сердечный ритм пациента; используются томографы 4-го поколения либо мультисрезовые томографы с количеством детекторов от 64 и выше. Сканирование проводится в разные фазы сердечного цикла, затем из полученных изображений строится последовательность 3D-моделей, по очереди соединенных в «фильм», позволяющий отследить изменения во время сердечного цикла.
Использование контрастных веществ
Для большинства исследований в КТ используют контрастные вещества (КВ) — вещества, содержащие йод и повышающие значения плотности среды, в которой находятся. В настоящее время выделяют ионные и неионные, мономерные и димерные йодсодержащие рентгеноконтрастные средства. Ионные КВ имеют повышенную осмолярность и в настоящее время не рекомендованы для парентерального контрастирования из-за высокой частоты побочных эффектов. Ионные КС могут быть использованы для перорального контрастирования, сиалографии (контрастирования слюнных желез) и т.д.
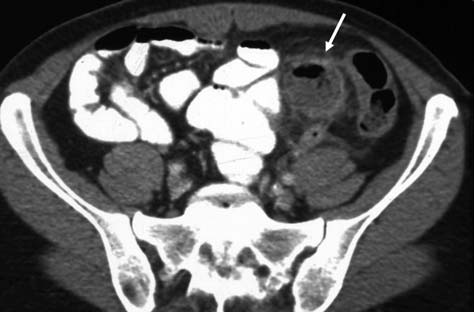
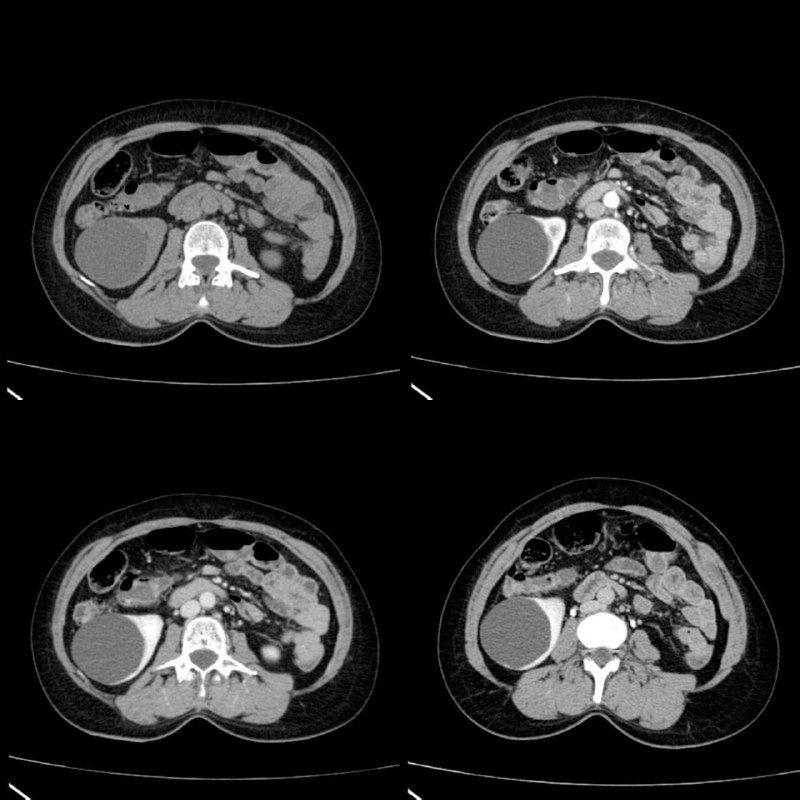
Рисунок 11 | КТ-сканы органов брюшной полости с пероральным контрастированием кишечника (стрелкой показан дивертикул стенки кишечника).
Существуют различные методики КТ-исследования с помощью контрастного препарата.
«Классическая» многофазная КТ предполагает введение сравнительно большого (обычно от 70 до 120 мл) контрастного средства со скоростью 3–4 мл/с. За этим следует несколько сканирований нужной области в определенные моменты времени — фазы. Например, исследование печени при подозрении на новообразование чаще выполняется в нативную (бесконтрастную), артериальную (контрастное вещество преимущественно в артериях, 15–40 с от начала введения), портовенозную (КВ в системе портальной вены и печеночных венах, 55–60 с) и отсроченную, или паренхиматозную (несколько минут после введения КВ) фазы. Полученные изображения позволяют не только оценить анатомию сосудов органа, но и дифференцировать найденные образования по характеру накопления КВ.
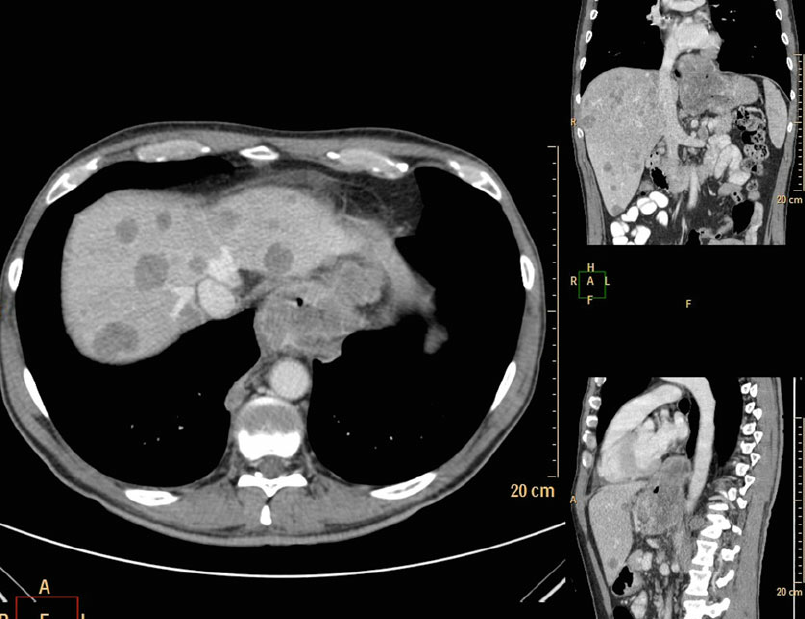
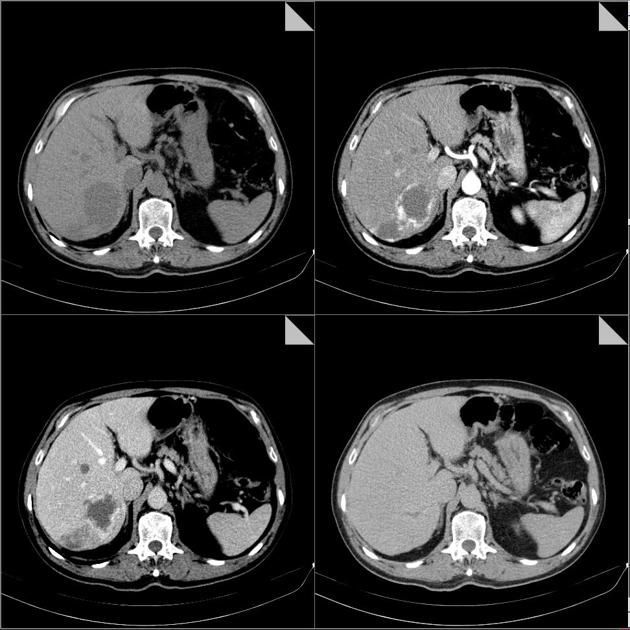
Рисунок 12 | Трехфазная контрастная КТ пациента с гигантской гемангиомой печени: нативная (бесконтрастная) фаза вверху слева; вверху справа — артериальная фаза; внизу слева — портовенозная фаза; внизу справа — отсроченная (5 мин).
Образование активно накапливает контраст и в артериальную фазу «светится» интенсивнее остальной паренхимы, а в венозную и отсроченную фазы контраст «вымывается» и образование выглядит менее плотным или таким же по плотности, как и остальная паренхима? Вероятно, это гиперваскулярная опухоль или метастаз. Не накапливает контраст (или накапливает в пределах 10 HU) и выглядит гиподенсным во всех фазах? Скорее всего, это киста.
Рисунок 13 | Трехфазная контрастная КТ пациента с простой кистой почки: нативная фаза — вверху слева; вверху справа — кортикальная почечная фаза; внизу слева — паренхиматозная фаза; внизу справа — экскреторная.
Учитывая накопление КВ в определенных фазах, характер этого накопления, а также размеры, расположение и структуру образования, рентгенолог делает предположение о характере образования. Внутривенное контрастирование используется также для проведения КТ-ангиографии.
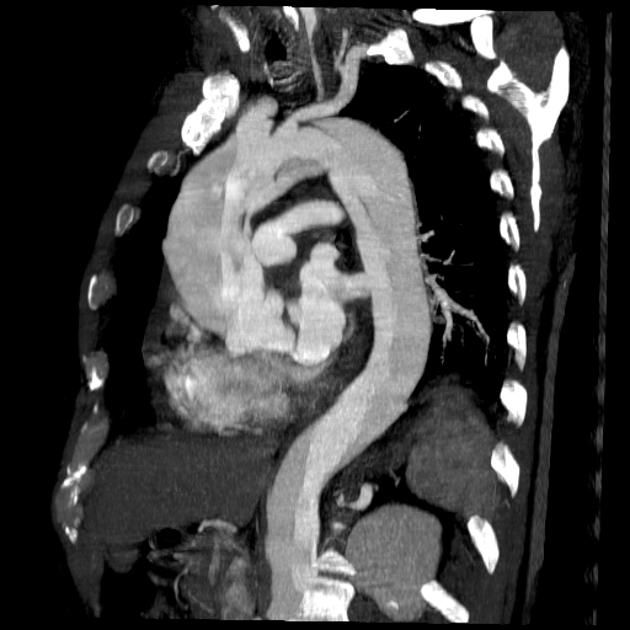
Рисунок 14 | КТ-аортография у пациента с диссекцией аорты.
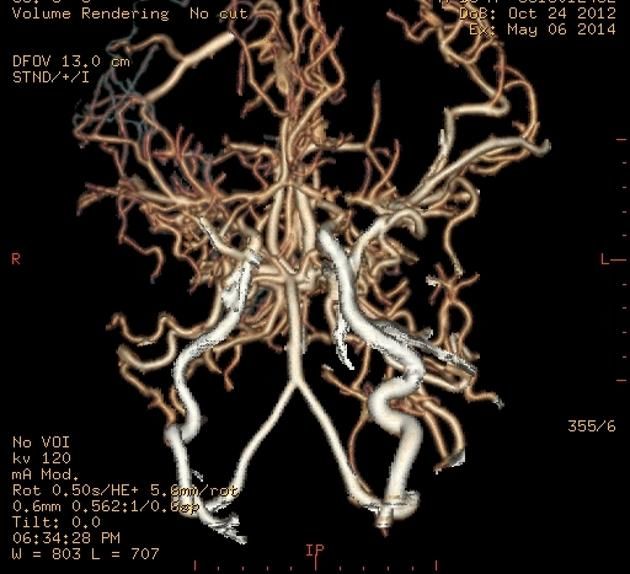
Рисунок 15 | КТ-ангиография артерий головного мозга у пациента с болезнью МояМоя (3D-реконструкция).
Перфузионная КТ используется чаще всего для диагностики нарушений мозгового кровообращения и нарушений перфузии миокарда, а также для оценки раннего ответа на химиотерапию. Эта методика позволяет отграничить зону некроза от пенумбры — зоны обратимой ишемии. Перфузионная КТ может быть выполнена на любом мультиспиральном компьютерном томографе, однако, чем больше он имеет детекторов, тем большую зону можно охватить при сканировании. Начальным этапом выполнения перфузионной КТ является нативное сканирование для исключения геморрагии, а также для выявления иной патологии головного мозга. Перфузионная КТ выполняется после внутривенного болюсного введения 40–50 мл контрастного препарата и 2030 мл физиологического раствора со скоростью 5 мл/с. После внутривенного болюсного введения контрастного препарата выполняются многократные сканирования на одном или нескольких уровнях, следующие друг за другом с минимальными промежутками времени или при непрерывной работе рентгеновской трубки. Общая длительность перфузионного исследования составляет около 1 минуты. Для получения графика контрастного усиления (зависимость плотности в единицах Хаунсфилда от времени) для каждого воксела в зоне интереса необходимо зарегистрировать множественные фазы и находить зоны, где скорость кровотока и времени транзита контрастного препарата не соответствуют объему кровотока, что и будет показателем обратимой ишемии.
Правила чтения томограмм
Можно выделить несколько основных факторов, затрудняющих чтение томограммы:
- бывает сложно «узнать» анатомические структуры, рассматривая их на аксиальных срезах;
- затруднять чтение могут также артефакты (чаще встречаются артефакты от движения и от присутствия металлических объектов);
- эффекты частного объема.
О последних поговорим подробнее.
Один срез на экране представляет собой плоскостное изображение, построенное из пикселей. Однако нужно помнить, что одному пикселю на экране соответствует трехмерный воксель в реальной жизни и толщина этого вокселя соответствует толщине среза.
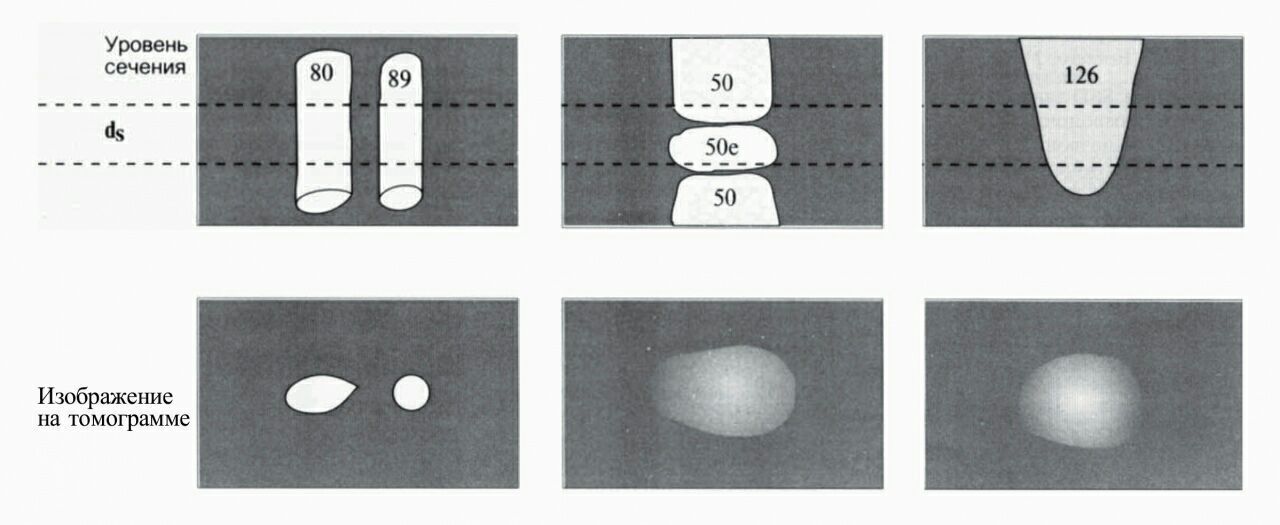
Допустим, в срез попала структура, которая на всей толщине среза имеет приблизительно одинаковую ширину, например, сосуд. В данном случае проблем не возникает, и структура будет иметь на сканах четкие контуры.
Но что, если срез пришелся на край позвонка? В воксель попала часть позвонка и часть межпозвоночного диска. Они имеют разную плотность и немного разные размеры. Полученные от вокселей данные суммировались, и в результате на скане появляется структура с нечеткими контурами, плотность которой представляется средней между плотностью позвонка и диска.
Еще один пример: округлой формы образование или лимфоузел. При сканировании в срез попадает часть лимфоузла, остальное — окружающая жировая клетчатка. На скане мы увидим нечеткую округлую структуру, а если захотим измерить ее плотность, значения будут средними между реальной плотностью узла и плотностью жира.
Если структура имеет коническую форму и сужается «в срезе», она также будет иметь нечеткие контуры. Примером может служить размытость контуров почки в области полюсов на томограммах. Такая же размытость появится, если, например, сосуд «делает поворот» в срезе.
Рисунок 16 | Эффеты частного объема.
Исходя из сказанного, можно дать несколько советов врачу или студенту, который осмелился открыть диск с КТ-исследованием пациента (или сесть за рабочую станцию радиолога) и проанализировать его самостоятельно:
- Пользуйтесь атласами посрезовой и специальными атласами КТ- и МРТ-анатомии наряду с обычными анатомическими атласами;
- Не анализируйте только аксиальные срезы: откройте в просмотрщике несколько окон и прослеживайте интересующую Вас структуру на аксиальных, сагиттальных и корональных срезах одновременно;
- Внимательно проанализируйте изображения, используя разные настройки окна, чтобы хорошо изучить структуры разной плотности; вы увидели образование легкого в «легочном» окне? Изучив его, перейдите в «костное» окно, чтобы выявить возможные метастазы в костные структуры;
- Также внимательно изучите исследование в разных фазах контрастирования; некоторые образования могут иметь схожую с окружающей тканью плотность на бесконтрастных сканах и выделяться только после введения контраста;
- Узнайте, проводилось ли пациенту контрастное исследование до проведенного КТ? Возможно, он проходил рентгеноскопию с применением сульфата бария, и увиденные вами ярко светящиеся области в просвете кишечника — это остатки бариевой взвеси; пациенту проводилось КТ с внутривенным контрастированием накануне? Контрастное вещество может оставаться в мочевыводящих путях (время его выведения зависит от используемого препарата и функции почек), а в случае экстравазации контрастного средства — в мягких тканях пациента;
- Держите в памяти тот факт, что больной во время исследования лежит на спине. Поэтому, например, жидкость в плевральной полости не собирается в плевральных синусах, а «растекается» по нижней стенке плевральной полости;
- Будьте внимательны, проводя денситометрию: помните, что в срез может попадать не только интересующая Вас структура, особенно, если эта структура небольших размеров из-за эффектов частного объема. Всегда измеряйте плотность в нескольких разных областях органа; проводите денситометрию только на бесконтрастных сканах (или сравнивайте показатели денситометрии на при нативном и контрастном исследовании; в этом случае следите, чтобы показатели были взяты из одной области). Интерпретировать результаты денситометрии также следует с осторожностью: жидкость высокой плотности в плевральной полости может быть кровью, транссудатом, гноем, смесью крови и экссудата и т. д; повышение плотности ткани печени — следствием цирротических изменений, диффузной формы злокачественного образования, а может быть и следствием нарушения обмена веществ, например, в виде отложений меди при болезни Вильсона-Коновалова.
А потому — главное правило: оценивайте изменения комплексно. Отмечайте не только изменение плотности, но и форму, объем, структуру органа; положение, форму, распространенность, контуры и структуру найденного образования и паттерн контрастного накопления. Сопоставляйте обнаруженные изменения с данными анамнеза и лабораторных исследований пациента. И помните, что любой метод имеет ограничения.
Источники:
- Прокоп, Матиас. «Михаэль Галански.» Спиральная многослойная компьютерная томография. 2-е издание.
- Перевод с английского. Москва.«МЕДпресс-информ 2 (2009). Хофер, Матиас. «Компьютерная томография.» Базовое руководство 2 (2008).
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Neuromuscular dysfunction of the bladder (NMDB) – multifaceted dis-ease whose main manifestations is a violation of accumulation and/or evacuation bladder function requires careful diagnosis and long-term comprehensive treat-ment, which is not always quite effective. Particularly noteworthy refractory 380 NMDB in children. The most common causes of dysfunction mainly consider congenital malformations (myelodysplasia, extrophy/epispadias etc.). In the US myelodysplasia occurs with a frequency of 1 in 1000 births and in 95% of cases accompanied NMDB [11]. While 30% of children with disorders of voiding in case myelodysplasia to primary surgery had urodynamic disorders and other complications associated with spinal cord defect [8]. The big problem is the condition in those countries where the law prohibits abortion even in the case of antenatal diagnosed anomalies of the spine and spinal cord (e.g., Poland). Each year in the United States for treatment NMDB spent 26.3 billion dollars, indicat-ing that the huge economic importance of this disease [14]. These aspects of the disease, the lack of standardized whole complex (ex-cept conservative therapy) treatments determine the relevance of the search for additional methods of complex treatment NMDB. Increasingly conduct research activities on urinary incontinence, more common takes neurourology. Searching methods treatment of this disease, which would enable to achieve long-term normalization of voiding that contrib-utes to the physiological and social adaptation patient [5, 10]. The study protocol NMDB children should consist of ultrasound of the kidneys and SM voiding cystography and urodynamic research. Some authors suggest benefits performance uroflowmetry at home that makes it possible to get the best results of the study [6]. If a combination of neurogenic dysfunction of recurrent urinary tract infection should conduct DMSA to determine the degree of kidney damage. Great importance is attached neuroimaging methods of diag-nosis of pelvic floor (CT and MRI). So, determined that only 37.2% of children with myelodysplasia have re-nal disease, and 78% of those who observed pathology of the upper urinary ways had bladder-ureteral reflux (mostly high degree) [4, 7, 9, 12]. Given the nature NMDB, it should be noted that in 37% of cases – a lack of sphincter apparatus of urine bladder and deficit its capacity, 22% – only lack of sphincter apparatus, 11% – high pressure in bladder background spastic con-traction sphincter, 4% – detrusor overactivity in 26% of patients causes urinary incontinence were mixed. Revealed that 69.4% of patients with urinary inconti-nence myelodysplasia [2, 7]. Other authors emphasize that urodynamic studies indicate that 62% of patients with myelodysplasia with detrusor contraction and discoordination sphincter, and in some cases sufficient to apply permanent cath-eterization and anticholinergic drugs. In 45% of patients observed violations locking properties sphincter [5]. Violations urine bladder innervations leads to severe hypoxic changes its walls that worsens impact of drug use means for correcting the pathology uro-dynamics [5, 9]. Results of treatment of patients with NMDB indicate the need for an inte-grated approach to problem-solving treatment of severe urinary incontinence in children. The most important aspect NMDB treatment – is prevention of kidney 381 damage. The effectiveness of neurosurgical treatment of urinary incontinence during myelodysplasia achieved only in 28.6% of cases [3, 9]. Only 22.1% for patients with myelodysplasia social adaptation rather complex conservative treatment, patients need rest various surgical correction (not only urological but neurosurgical) [9]. Others authors [1, 5] argue that the positive effect conservative therapy can achieve in 72% of patients, but this pos-itive effect is regarded as an adequate preoperative preparation. Some authors emphasize that in the absence effect of conservative therapy NMDB children with myelodysplasia for 18 months there is a need in the surgical treatment of defects [7]. By the choice of surgical treatment should be approached strictly individual-ly, taking into account the type of incontinence, a condition wall NMDB and cen-tral nervous system treatments which were applied in individual patients [13]. Thus, for successful treatment NMDB, particularly in myelodysplasia re-quired hard work urologist, and it is very useful collaboration with neurosur-geon. Only when patients and/or their relatives aware of the need, importance and complexity of surgical treatment NMDB then can be a satisfactory outcome. References: 1. Борисова С.А. Оптимизация лечения нейрогенной дисфункции мочевого пузыря у детей: Автореф. дис. …к. мед. н.– М., 2006. 2. Бурханов В.В. Хирургическая коррекция нижних мочевыводящих путей при недержании мочи у детей: Автореф. дис.…к. мед. н. – СПб, 2009. 3. Бурханов В.В., Осипов И.Б., Лебедев Д.А. Вестник Санкт-петербургского университета. Сер. 11. – Прил. К. – 2008. – Вып. 1.– С. 184-195. 4. Гаджиев Т.В. Урофлоуметрический мониторинг в диагностике нарушений мочеиспускания у детей с хирургическими заболеваниями нижних моче-вых путей: Автореф. …к. мед. н.– М., 2006. 5. Гусева Н.Б. Коррекция нарушений функции мочевого пузыря в консерва-тивном и оперативном лечении детей с недержанием мочи при миелодис-плазии: Автореф. дис. …д. мед. н. – М., 2007. 6. Данилов В.В., Вольных И.Ю. Уродинамические исследования в отборе больных и оценке результатов операции TVT у женщин с недержанием мочи // Pacific Medical Journal. – 2004. – N 1.– Р. 65 –69. 7. Еликбаева Г.М. Система диагностики и дифференцированного хирургиче-ского лечения миелодисплазии у детей: Автореф. дис. …д. мед. н.– СПб, 2009. 8. Николаев С.Н., Меновщикова Л.Б., Шмыров О.С. и др. Принципы хирур-гического лечения детей с миелодисплазией и недержанием мочи в ран-нем возрасте // Детская хирургия. – 2005. – № 4. – С. 4–8. 9. Осипов И.Б., Хачатрян В.А., Сарычев С.А. и др. Диагностика и лечение миелодисплазии у детей с урологическими осложнениями // Педиатрия жэне бала хирургиясы. – 2008. – № 1. – С. 14–17. 382 10. Шмыров О.С. Реконструкция сфинктерного аппарата нижних мочевыво-дящих путей у детей с недержанием мочи при миелодисплазии: Автореф. дис. …к. мед. н.– М., 2007. 11. Bauer S.B. Neurogenic bladder dysfunction // Pediatric Clin. North. Am.– 1987.– Vol. 34.– P. 1121–1132. 12. Joao Luiz Pippi Salle Bladder Neck Reconstruction for the Treatment of Refrac-tory Urinary Incontinence in Children // http://ww2.ttmed.com/sinsecc.cfm?Http://ww2.ttmed.com/arg_sida/texto_art_long.cfm?ID_dis=212&ID_Cou=20&ID_Art=1633&comecover=Y&ID_dis=212&ID_cou=20. 13. Schulte–Baukloh H., Michael T., Schobert J. et al. Efficacy of botulinum–a tox-in in children with detrusor hyperreflexia due to myelomeningocele: prelimi-nary results // Urology.– 2002.– Vol. 59 (3).– Vol. 325–327. 14. Wagner T.H., Hu T.W. Economic course of urinary incontinence in 1995 // Urology.– 1998.– Vol. 51.– P. 355.
Компьютерная томография в диагностике пневмоний : атлас : руководство для врачей / под ред. : Г. Е. Труфанова, А. С. Грищенкова. – Москва : ГЭОТАР-Медиа, 2021. – 304 с : ил. (Шифр 616.24-002 К 63)
28.12.2021
Атлас посвящен использованию рентгеновской компьютерной томографии в диагностике различных инфекционных заболеваний легких.
В настоящее время общепризнана ведущая роль этого метода лучевой диагностики не только при первичном обследовании пациентов с подозрением на данные заболевания, но и в процессе лечения и динамического наблюдения в качестве метода контроля. Представлены изображения и комментарии к ним, которые могут использоваться врачами-рентгенологами при написании заключений.
В отдельной главе рассмотрены конкретные клинические примеры компьютерной томографии в диагностике пневмоний, вызванных новой коронавирусной инфекцией COVID-19. Подчеркивается ведущая роль этого метода исследования в определении степени изменений и вероятности наличия данного типа вирусной пневмонии. Проиллюстрированы возможности компьютерной томографии в динамическом наблюдении при благоприятном или неблагоприятном течении патологического процесса, а также в выявлении различных осложнений.
Книга предназначена специалистам по лучевой диагностике, в большей степени врачам-рентгенологам отделений компьютерной томографии. Может быть рекомендована врачам смежных специальностей, занимающимся диагностикой и лечением пациентов, заболевших пневмонией, а также быть полезна специалистам, проходящим подготовку в системе непрерывного медицинского образования и обучающимся в аспирантуре или ординатуре.