Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Брутто формула
-
Фармакологическая группа вещества Ниволумаб
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Ниволумаб
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Ниволумаб
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Ниволумаб
Русское название
Ниволумаб
Английское название
Nivolumab
Латинское название
Nivolumabum (род. Nivolumabi)
Брутто формула
C6362H9862N1712O1995S42
Фармакологическая группа вещества Ниволумаб
Нозологическая классификация
Код CAS
946414-94-4
Фармакологическое действие
—
противоопухолевое.
Характеристика
Человеческое моноклональное антитело — IgG4 с приблизительной молекулярной массой 146 кДа.
Фармакология
Фармакодинамика
Блокирует взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами (PD-L1 и PD-L2).
PD-1-рецептор является негативным регулятором активности Т-клеток. Связывание PD-1 с лигандами PD-L1 и PD-L2, которые способны экспрессироваться клетками опухолей или иными клетками микроокружения опухолей, приводит к ингибированию пролиферации Т-клеток и секреции цитокинов. Ниволумаб потенцирует иммунный ответ посредством блокады связывания PD-1 с лигандами PD-L1 и PD-L2. В исследованиях на мышиных моделях блокирование активности PD-1 приводило к уменьшению роста опухоли.
Фармакокинетика
Фармакокинетика ниволумаба линейна в диапазоне доз от 0,1 до 10 мг/кг.
В популяционном фармакокинетическом анализе установлено, что средний системный клиренс ниволумаба составляет 9,5 мл/ч (коэффициент вариабельности 49,7%); средний Vss — 8 л (коэффициент вариабельности 30,4%); средний T1/2 — 26,7 дня (коэффициент вариабельности 101%). Cmax, Cmin и средняя концентрации ниволумаба в плазме после введения в течение 2 нед в дозе 3 мг/кг составляла 57; 116 и 75,3 мкг/мл соответственно.
Метаболизм ниволумаба не описан, однако ввиду идентичности структуры ниволумаба и человеческого моноклонального антитела IgG4 предполагаемый путь метаболизма соответствует метаболизму эндогенного Ig — распад на аминокислоты в каталитическом пути обмена белка.
Особые группы пациентов
Популяционный фармакокинетический анализ показал отсутствие зависимости клиренса ниволумаба от возраста пациента, пола, расы, типа опухоли, размера опухоли и наличия нарушений функции печени. Хотя в исследованиях и наблюдалась слабая зависимость клиренса от показаний ЭКГ, уровня гломерулярной фильтрации, количества сывороточного альбумина и массы тела (от 34 до 162 кг), эта связь была признана клинически незначимой.
Нарушение функции почек
Фармакокинетические свойства ниволумаба были изучены у пациентов с легкой (Cl креатинина от 60 до <90 мл/мин/1,73 м2), средней (от 30 до <60 мл/мин/1,73 м2), тяжелой (<30 мл/мин и >15 мл/мин/1,73 м2) степенью почечной недостаточности в сравнении с пацентами с нормальной функцией почек (Cl креатинина >90 мл/мин/1,73 м2). Не наблюдались клинически значимые различия в клиренсе ниволумаба у пациентов с легкой и средней почечной недостаточностью и пациентов с нормальной функцией почек. Клиренс ниволумаба у пациентов с тяжелой почечной недостаточностью недостаточно изучен.
Нарушение функции печени
Фармакокинетические свойства были изучены у пациентов с легкой степенью печеночной недостаточности (повышение общего билирубина в 1–1,5 раза выше ВГН или ACT выше ВГН, классификация национального института рака) и пациентов с нормальной функцией печени (общий билирубин и ACT в пределах нормы). Различий в клиренсе ниволумаба между вышеуказанными группами пациентов не обнаружено. Фармакокинетика ниволумаба не изучалась у пациентов со средней степенью печеночной недостаточности (повышение общего билирубина в 1,5–3×ВГН и ACT выше ВГН) и тяжелой степенью печеночной недостаточности (повышение общего билирубина более 3×ВГН и ACT выше ВГН).
Применение вещества Ниволумаб
Монотерапия у взрослых — неоперабельная или метастатическая меланома; местнораспространенный или метастатический немелкоклеточный рак легкого после предшествующей химиотерапии; распространенный почечноклеточный рак после предшествующей системной терапии.
Противопоказания
Гиперчувствительность; беременность и кормление грудью; возраст до 18 лет (данные по эффективности и безопасности отсутствуют).
Ограничения к применению
Тяжелые аутоиммунные заболевания в активной стадии, при которых дальнейшая активация иммунной системы может представлять потенциальную угрозу жизни; нарушение функции печени средней и тяжелой степени; нарушение функции почек тяжелой степени.
Опыт применения ниволумаба в терапии меланомы с положительной BRAF-мутацией у пациентов, ранее не получавших лечение, ограничен.
Пациенты с сопутствующими метастазами в головной мозг, активным аутоиммунным заболеванием или заболеваниями, требующими терапии системными иммунодепрессантами, были исключены из основного клинического исследования почечноклеточного рака. В случае отсутствия данных ниволумаб следует применять с осторожностью у данных групп пациентов после тщательной оценки соотношения польза-риск, основанной на индивидуальных показателях.
Отдельные группы пациентов
В клинических исследованиях не принимали участие следующие группы пациентов:
— пациенты с показателями исходного функционального статуса >2, неизлеченными метастазами головного мозга, аутоиммунными заболеваниями и пациенты, получавшие системные иммунодепрессанты до начала проведения исследования;
— пациенты с симптоматическими интерстициальными заболеваниями легких и меланомой глаза были исключены из проведения клинических исследований немелкоклеточного рака легкого и меланомы;
— пациенты с 4-й степенью тяжести нежелательных реакций, связанных с ранее проводимой анти-CTLA-4-терапией в анамнезе.
Ввиду отсутствия данных, ниволумаб должен применяться с осторожностью у данных групп пациентов после проведения оценки соотношения риск-польза, основанной на индивидуальных показателях.
Применение при беременности и кормлении грудью
Исследований применения ниволумаба у беременных женщин не проводилось. Исследования на животных показали репродуктивную токсичность ниволумаба. IgG4 может проникать через ГПБ, поэтому вероятно воздействие препарата на плод. Применение ниволумаба при беременности противопоказано. Во время лечения и на период как минимум 5 мес после последнего введения ниволумаба женщинам детородного возраста рекомендуется применение контрацепции.
Исследований касательно проникновения ниволумаба в грудное молоко женщин в период лактации не проводилось. Согласно общим сведениям, попадание антител в грудное молоко возможно, поэтому нельзя исключить риск для новорожденного при применении ниволумаба в период грудного вскармливания. Ввиду потенциальной опасности развития серьезных побочных реакций у ребенка применение ниволумаба при кормлении грудью противопоказано.
Побочные действия вещества Ниволумаб
При применении ниволумаба чаще всего отмечались иммуноопосредованные побочные реакции. Большинство таких побочных реакций, включая тяжелые, купировались при помощи соответствующей терапии или путем отмены терапии.
В клинических исследованиях с применением ниволумаба в качестве монотерапии в дозе 3 мг/кг по типам опухолей наиболее частыми (≥10%) нежелательными реакциями были утомляемость (34%), сыпь (19%), зуд (14%), диарея (13%), тошнота (13%) и снижение аппетита (10%). В большинстве случаев побочные реакции были выражены от легкой до средней степени (степень 1 и 2).
Ниже приведены побочные реакции, отмечавшиеся у пациентов, получавщих терапию ниволумабом. Побочные реакции представлены по частоте их регистрации: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000).
Инфекции и инвазии: часто — инфекция верхних дыхательных путей; нечасто — бронхит, пневмония; редко — энцефалит.
Новообразования доброкачественные, злокачественные и неустановленной природы (в т.ч. кисты и полипы): редко — гистиоцитарный некротический лимфаденит (лимфаденит Кикучи).
Со стороны крови и лимфатической системы: нечасто — эозинофилия.
Со стороны иммунной системы: часто — инфузионные реакции1; нечасто — анафилактические реакции1, гиперчувствительность1.
Со стороны эндокринной системы: часто — гипергликемия, гипотиреоз, гипертиреоз; нечасто — недостаточность функции надпочечников, гипопитуитаризм, гипофизит, тиреоидит, диабетический кетоацидоз, сахарный диабет.
Со стороны обмена веществ и питания: очень часто — снижение аппетита; нечасто — дегидратация, метаболический ацидоз.
Со стороны нервной системы: часто — периферическая нейропатия, головная боль, головокружение; нечасто — полинейропатия; редко — синдром Гийена-Барре, демиелинизация, миастенический синдром, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов).
Со стороны органа зрения: часто — нечеткость зрения, сухость глаз; нечасто — увеит.
Со стороны ССС: часто — повышение АД; нечасто — тахикардия, васкулит; редко — аритмия (включая желудочковую), мерцательная аритмия.
Со стороны дыхательной системы: часто — пневмонит1, одышка, кашель; нечасто — плеврит; редко — инфильтрация легких.
Со стороны ЖКТ: очень часто — диарея, тошнота; часто — колит, стоматит, рвота, боль в животе, запор, сухость во рту; нечасто — панкреатит; редко — гастрит, язва двенадцатиперстной кишки.
Со стороны печени и желчных путей: нечасто — гепатит1, гипербилирубинемия; редко — холестаз.
Со стороны кожи и подкожной клетчатки: очень часто — сыпь2, зуд; часто — витилиго, сухость кожи, эритема, алопеция; нечасто — многоформная эритема, псориаз, розацеа, крапивница; редко — токсический эпидермальный некролиз3.
Со стороны опорно-двигательного аппарата: часто — костно-мышечная боль4, артралгия; нечасто — ревматическая полимиалгия.
Со стороны почек и мочевыводящих путей: нечасто — тубулоинтерстициальный нефрит, почечная недостаточность1,3.
Общие нарушения и реакции на введение: очень часто — повышенная утомляемость; часто — повышение температуры тела, отеки (включая периферические); нечасто — боль в груди.
Со стороны лабораторных показателей: очень часто — снижение массы тела; часто — повышение активности трансаминаз, липазы, амилазы и ЩФ, повышение уровня креатинина, лимфопения, лейкопения, тромбоцитопения, анемия, гипонатриемия; нечасто — повышение концентрации общего билирубина, гиперкальциемия, гипокальциемия, гиперкалиемия. гипокалиемия, гипомагнезиемия, нейтропения, снижение абсолютного числа нейтрофилов, гипернатриемия; редко — гипермагнезиемия.
1Включая жизнеугрожающие побочные реакции.
2Включая пятнисто-папулезную, эритемную, зудящую, везикулезную, макулезную, кореподобную, папулезную, пустулезную, папуло-сквамозную, генерализованную сыпь, дерматит, акнеформный дерматит, аллергический дерматит, атопический дерматит, буллезный дерматит, эксфолиативный дерматит, псориазоформный дерматит, медикаментозную сыпь.
3Включая побочные реакции с летальным исходом.
4Включая боль в спине, костную боль, мышечно-скелетную боль в груди, костно-мышечный дискомфорт, миалгию, боль в шее и конечностях, спинальную боль.
Иммуногенность. Ниволумаб, как и другие моноклональные антитела, обладает иммуногенностыо.
У 11% пациентов, получавших терапию ниволумабом, наблюдалось образование антител к ниволумабу. Нейтрализация антител определилась у двух пациентов (0,6%). Однако зависимость наличия антител в плазме крови и изменений фармакокинетических параметров, выраженности клинического эффекта и развития побочных эффектов не выявлена.
Взаимодействие
Фармакокинетическое взаимодействие
Ниволумаб представляет собой человеческое моноклональное антитело. Ввиду того, что антитела не подвергаются метаболизму при участии изоферментов цитохрома Р450 и других изоферментов, ингибирование или индукция этих ферментов при совместном применении с другими ЛС не оказывают влияние на фармакокинетику ниволумаба.
Другие формы взаимодействия
Системная иммуносупрессия. В связи с возможностью фармакодинамического взаимодействия следует избегать применения системных ГКС и других иммунодепрессантов перед назначением терапии ниволумабом. После начала терапии ниволумабом ГКС и другие иммунодепрессанты могут применяться для коррекции иммуноопосредованных побочных реакций, вызванных воздействием ниволумаба на иммунную систему. Применение системных ГКС после начала лечения ниволумабом не снижает его эффективность.
Передозировка
Случаев передозировки выявлено не было.
Лечение: при передозировке лечение должно заключаться в симптоматической лекарственной терапии в соответствии с возникающими побочными реакциями при тщательном наблюдении за пациентом.
Способ применения и дозы
В/в, в виде инфузии, каждые 2 нед.
Меры предосторожности
Ниволумаб может вызывать тяжелые, в т.ч. с летальным исходом, побочные реакции, вызванные влиянием на иммунную систему и обусловленные специфическим механизмом его действия. Пациенты должны находиться под непрерывным контролем (как минимум 5 мес после введения последней дозы), т.к. нежелательные реакции, обусловленные воздействием ниволумаба, могут развиться в любой момент во время применения или после отмены терапии. При подозрении на развитие иммуноопосредованной нежелательной реакции должна быть проведена адекватная оценка для подтверждения или исключения иной этиологии. Основываясь на тяжести нежелательной реакции, применение ниволумаба должно быть прекращено с возобновлением или без назначения ГКС.
В случае проведения иммуносупрессивной терапии ГКС, предназначенной для устранения нежелательных реакций, после улучшения состояния снижение дозы ГКС проводят медленно, в течение по меньшей мере 1 мес. Быстрое снижение дозы может привести к ухудшению тяжести или рецидиву нежелательных реакций. Иммуносупрессивная терапия ЛС, отличными от ГКС, назначается в случае наступления ухудшения или отсутствия улучшения при применении ГКС.
Применение ниволумаба следует прекратить во время получения пациентом иммуносупрессивной дозы ГКС или проведения иммуносупрессивной терапии.
Ниволумаб должен быть отменен при любых рецидивирующих иммуноопосредованных нежелательных реакциях от средней до тяжелой степени и отменен без возобновления при тяжелом иммуноопосредованном пневмоните и иммуноопосредованном гепатите, а также жизнеугрожающих иммуноопосредованных нежелательных реакциях.
Применение ниволумаба у пациентов с быстрым прогрессированием меланомы
Врачи должны обсудить эффект отсроченного действия ниволумаба до начала проведения лечения у пациентов с быстро прогрессирующим заболеванием.
Иммуноопосредованный пневмонит
При терапии ниволумабом были отмечены случаи тяжелого пневмонита или интерстициального заболевания легких, включая случаи с летальным исходом. Пациенты должны наблюдаться на наличие признаков и симптомов пневмонита, таких как рентгенографические изменения (например затемнение по типу матового стекла, очаги воспаления), одышка и гипоксия. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3-й или 4-й степени тяжести пневмонита применение ниволумаба следует отменить без возобновления и начать прием ГКС в дозе, эквивалентной 2–4 мг/кг/день метилпреднизолона.
При 2-й степени тяжести (симптоматическая) пневмонита применение ниволумаба следует приостановить и начать прием ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на прием ГКС, дозу ГКС следует увеличить до эквивалентной 2–4 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованный колит
При терапии ниволумабом были отмечены случаи тяжелой диареи или колита. Пациенты должны наблюдаться на наличие признаков диареи и дополнительных симптомов колита, таких как боль в животе, слизь или кровь в стуле. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 4-й степени тяжести диареи или колита применение ниволумаба следует отменить окончательно и начать прием ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 3-й степени тяжести диареи или колита применение ниволумаба следует приостановить и начать прием ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на прием ГКС, применение ниволумаба должно быть отменено без возобновления.
При 2-й степени тяжести диареи или колита применение ниволумаба следует приостановить. Персистирующую диарею или колит следует устранять при помощи введения ГКС в дозе, эквивалентной 0,5–1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на прием ГКС, дозу ГКС следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованный гепатит
При терапии ниволумабом были отмечены случаи тяжелого гепатита. Пациенты должны наблюдаться на наличие признаков и симптомов гепатита, таких как повышение уровня трансаминаз и общего билирубина. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3-й или 4-й степени тяжести повышения уровня трансаминаз и общего билирубина применение ниволумаба следует отменить без возобновления и начать прием ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 2-й степени тяжести повышения уровня трансаминаз и общего билирубина применение ниволумаба следует приостановить. Персистирующий подъем уровня этих лабораторных показателей должен быть устранен при помощи введения ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на прием ГКС, дозу ГКС следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованные нефрит и почечная дисфункция
При терапии ниволумабом были отмечены случаи тяжелого нефрита или почечной дисфункции, поэтому пациенты должны наблюдаться на наличие их признаков и симптомов. У большинства пациентов отмечено бессимптомное повышение уровня сывороточного креатинина. Должна быть исключена этиология, связанная с заболеванием.
При 4-й степени тяжести повышения уровня сывороточного креатинина применение ниволумаба следует отменить окончательно и начать прием ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 2-й или 3-й степени тяжести повышения уровня сывороточного креатинина применение ниволумаба следует приостановить и начать прием ГКС в дозе, эквивалентной 0,5–1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на прием ГКС, дозу ГКС следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованная эндокринопатия
При терапии ниволумабом были отмечены случаи тяжелой эндокринопатии, включая гипотиреоз, гипертиреоз, недостаточность коры надпочечников, гипофизит, сахарный диабет и диабетический кетоацидоз.
Пациенты должны наблюдаться на наличие признаков и симптомов эндокринопатии и изменения функции щитовидной железы (в начале лечения, периодически во время лечения и основываясь на клинической оценке). У пациентов может отмечаться усталость, головная боль, изменение психического состояния, боль в животе, необычный ритм работы кишечника и гипотония или неспецифические симптомы, которые могут иметь сходство с другими состояниями, такими как метастазы в головной мозг или сопутствующие заболевания. Если иная этиология не выявлена, признаки и симптомы эндокринопатии должны считаться иммуноопосредованными.
При симптоматическом гипотиреозе применение ниволумаба следует приостановить и в случае необходимости провести заместительную терапию гормонами щитовидной железы. При симптоматическом гипертиреозе применение ниволумаба следует приостановить и в случае необходимости провести терапию антитиреоидными ЛС. В случае острого тиреоидита должны назначаться ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. Необходимо продолжать наблюдение за функцией щитовидной железы для контроля адекватности проводимой заместительной гормональной терапии гормонами щитовидной железы.
При симптоматической недостаточности коры надпочечников 2-й степени применение ниволумаба следует приостановить и в случае необходимости провести физиологическое замещение ГКС. При симптоматической недостаточности коры надпочечников 3–4-й степени применение ниволумаба следует отменить окончательно и в случае необходимости провести физиологическое замещение ГКС. Необходимо продолжать наблюдение за функцией надпочечников и уровнем гормонов для контроля адекватности проводимой заместительной терапии ГКС. При симптоматическом гипофизите 2–3-й степени применение ниволумаба следует приостановить и провести в случае необходимости гормонозаместительную терапию. В случае острого гипофизита назначают ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы ГКС. При симптоматическом гипофизите 4-й степени терапия ниволумабом должна быть отменена окончательно. Необходимо продолжать наблюдение за функцией гипофиза и уровнем гормонов для контроля адекватности проводимой гормонозаместительной терапии.
При симптоматическом диабете применение ниволумаба следует приостановить и провести в случае необходимости заместительную терапию инсулином. Необходимо контролировать уровень сахара в крови для контроля адекватности проводимой заместительной терапии инсулином.
Иммуноопосредованная сыпь
При терапии ниволумабом были отмечены случаи тяжелой формы сыпи (включая редкие случаи летального токсического эпидермального некролиза), которые могут иметь иммуноопосредованную природу. Применение ниволумаба следует прекратить при сыпи 3-й степени тяжести и отменить без восстановления при 4-й степени тяжести. При сыпи тяжелой степени назначается лечение ГКС в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
Ниволумаб следует назначать с осторожностью пациентам, у которых ранее отмечались тяжелые или жизнеугрожающие нежелательные кожные реакции при лечении иными иммуностимулирующими противоопухолевыми средствами.
Другие иммуноопосредованные нежелательные реакции
Следующие иммуноопосредованные нежелательные реакции были отмечены у менее 1% пациентов, получавших лечение ниволумабом во время проведения клинических исследований при любом дозировании и типе опухоли: панкреатит, увеит, демиелинизация, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов), синдром Гийена-Барре, гипопитуитаризм, миастенический синдром и энцефалит.
При подозрении на иммуноопосредованные нежелательные реакции должна быть проведена адекватная оценка для подтверждения этиологии или исключения иных причин их появления. Исходя из тяжести нежелательной реакции, применение ниволумаба следует прекратить и начать терапию ГКС. При наступлении улучшения прием ниволумаба может быть продолжен после медленного снижения дозы ГКС. Ниволумаб должен быть отменен без возобновления при проявлении любых рецидивирующих тяжелых и любых жизнеугрожающих иммуноопосредованных нежелательных реакций.
Инфузионные реакции
Во время клинических исследований отмечались случаи тяжелых инфузионных реакций. В случае развития тяжелых инфузионных реакций введение ниволумаба должно быть прекращено с назначением соответствующей лекарственной терапии. Пациенты с легкой или умеренной инфузионной реакцией могут продолжать терапию ниволумабом под непрерывным наблюдением и с проведением премедикации в соответствии с действующими стандартами профилактики инфузионных реакций.
Влияние на способность управлять транспортными средствами и работать с механизмами. Ввиду возможного появления нежелательных реакций, таких как утомляемость, пациентам следует воздерживаться от управления транспортом и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций в период лечения ниволумабом, до установления факта, что данные побочные реакции у них отсутствуют.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2016.
Торговые названия с действующим веществом Ниволумаб
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Опдиво® |
от 40927.00 до 67000.00 |
Инфекционные заболевания: часто — инфекция верхних дыхательных путей; нечасто — бронхит, пневмония; энцефалит.
Доброкачественные, злокачественные и неуточненные новообразования (включая полипы и кисты): редко — гистиоцитарный некротический лимфаденит (лимфаденит Кикучи).
Со стороны системы кроветворения: нечасто — эозинофилия.
Со стороны иммунной системы: нечасто — инфузионные реакции, анафилактические реакции, реакции гиперчувствительности.
Со стороны эндокринной системы: часто — гипергликемия, гипотиреоз, гипертиреоз; нечасто — недостаточность функции надпочечников, гипопитуитаризм, гипофизит, тиреоидит, диабетический кетоацидоз, сахарный диабет.
Со стороны обмена веществ: часто — снижение аппетита; нечасто — дегидратация, метаболический ацидоз.
Со стороны нервной системы: часто — периферическая нейропатия, головная боль, головокружение; нечасто — полиневропатия; редко — синдром Гийена-Барре, демиелинизация, миастенический синдром, аутоиммунная невропатия (включая парез лицевого и отводящего нервов).
Со стороны органа зрения: часто — нечеткость зрения, сухость глаз; нечасто — увеит.
Со стороны сердечно-сосудистой системы: часто — повышение АД; нечасто — тахикардия, васкулит; редко — аритмия (включая желудочковую аритмию), мерцательная аритмия.
Со стороны дыхательной системы: часто — пневмонит, одышка, кашель; нечасто — плеврит; редко — инфильтрация легких.
Со стороны пищеварительной системы: очень часто — диарея, тошнота; часто — колит, стоматит, рвота, боль в животе, запор, сухость во рту; нечасто — панкреатит; редко — гастрит, язва двенадцатиперстной кишки.
Со стороны печени и желчевыводящих путей: нечасто — гепатит, гипербилирубинемия; редко — холестаз.
Со стороны кожи и подкожных тканей: очень часто — сыпь (в т.ч. пятнисто-папулезная сыпь, эритемная сыпь, зудящая сыпь, везикулезная сыпь, макулезная сыпь, кореподобная сыпь, папулезная сыпь, пустулезная сыпь, папулосквамозная сыпь, везикулезная сыпь, генерализованная сыпь, дерматит, акнеиформный дерматит, аллергический дерматит, атопический дерматит, буллезный дерматит, эксфолиативный дерматит, псориазиформный дерматит, медикаментозная сыпь), зуд; часто — витилиго, сухость кожи, эритема, алопеция; нечасто — многоформная эритема, псориаз, розацеа, крапивница; редко — токсический эпидермальный некролиз.
Со стороны костно-мышечной системы: часто — костно-мышечная боль (в т.ч. боль в спине, боль в костях, мышечно-скелетная боль в груди, костно-мышечный дискомфорт, миалгия, боль в шее, боль в конечностях, спинальная боль), артралгия; нечасто — ревматическая полимиалгия.
Со стороны мочевыводящей системы: нечасто — тубулоинтерстициальный нефрит, почечная недостаточность.
Общие реакции: очень часто — утомляемость; часто — повышение температуры тела, отеки (включая периферические отеки); нечасто — боль в груди.
Со стороны лабораторных показателей: очень часто — снижение массы тела; часто — повышение активности трансаминаз, повышение активности липазы, повышение активности амилазы, повышение активности ЩФ, повышение креатинина, лимфопения, лейкопения, тромбоцитопения, анемия, гипонатриемия; нечасто — повышение концентрации общего билирубина, гиперкальциемия, гипокальциемия, гиперкалиемия, гипокалиемия, гипомагниемия, нейтропения, снижение абсолютного числа нейтрофилов, гипернатриемия; редко — гипермагнезиемия.

Иммунотерапия препаратом Ниволумаб
Обновлено: 28 апреля 2022
27479
Как действует ниволумаб при раке? О клиническом применении препарата Опдиво, его преимуществах и побочных эффектах рассказывает онколог-химиотерапевт высшей категории Круглова Марина Сергеевна
- arrow_forward
Как действует Ниволумаб? - arrow_forward
Преимущества терапии ниволумабом - arrow_forward
Побочные эффекты ниволумаба
Ниволумаб — противоопухолевый препарат из группы ингибиторов контрольных точек и фактический стимулятор иммунитета. Опдиво — это торговое название, присвоенное компанией-производителем моноклональному человеческому антителу ниволумаб. Антитело представляет собой чистейший и абсолютно однородный по свойствам белок.
Как действует Ниволумаб?
Принцип действия Ниволумаба на опухоль диаметрально отличается от всех прочих иммунологических противоопухолевых препаратов. Доставшиеся нам из прошлого века и до настоящего времени используемые в онкологии цитокины — интерферон-альфа и интерлейкин-2 — синтезированные человеком продукты жизнедеятельности лимфоцитов, доставляемые в организм уже в готовом виде.
Ниволумаб также радикально отличается от механизма действия цитостатиков, суть которых уничтожить опухолевую клетку (цитотоксический эффект) или остановить ее пролиферативную активность (цитостатический эффект).
В конечном итоге Опдиво вынуждает лимфоциты вырабатывать цитокины, но не прямым способом, а помогая лимфоциту выйти из оцепенения, в которое его ввергает злокачественный процесс.
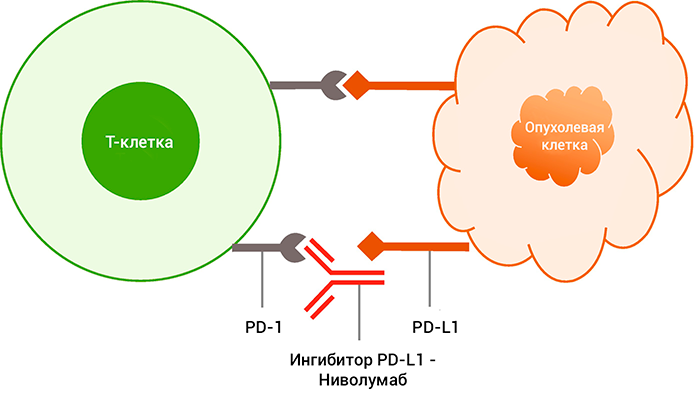
Ниволумаб блокирует взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами (PD-L1 и PD-L2).
PD-1-рецептор является негативным регулятором активности Т-клеток. Связывание PD-1 с лигандами PD-L1 и PD-L2, которые способны экспрессироваться клетками опухолей или иными клетками микроокружения опухолей, приводит к ингибированию пролиферации Т-клеток и секреции цитокинов. Ниволумаб потенцирует иммунный ответ посредством блокады связывания PD-1 с лигандами PD-L1 и PD-L2.
Выражаясь простыми словами, взаимодействие ниволумаба с лимфоцитом осуществляет через специальный рецептор на поверхностной мембране. Занятый им рецептор не может связаться с продуцируемыми опухолевыми клетками и их окружением — лигандами.
Лиганды специально синтезируются для обмана лимфоцита, чтобы он не замечал развитие злокачественного процесса. Связывание лигандов со специальным рецептором PD-1 на поверхности лимфоцита приводит к нарушению его работы и воспроизводства. В результате получается, что опухолевые клетки не замечаются «больным» лимфоцитом и могут спокойно воспроизводить себе подобных.
С помощью ниволумаба лимфоцит «прозревает» и вырабатывает смертельные для раковой клетки цитокины. Если интерферон и интерлейкин вводятся в огромных дозах, то активированный опдиво лимфоцит вырабатывает их без превышения своих функциональных возможностей.
О существовании рецептора можно узнать по присутствию специфического белка PD-1, который имеется у 10–15% больных.
Применение Ниволумаба
Ниволумаб при раке доказал свою эффективность в многочисленных клинических исследованиях по всему миру и сегодня зарегистрирован в России для лечения девяти нозологий:
- 1-я линия терапии почечно-клеточного рака;
- 2-я линия терапии почечно-клеточного рака;
- Метастатическая меланома;
- Адъювантная терапия меланомы;
- Опухоли головы и шеи;
- Мелкоклеточный рак легкого;
- Немелкоклеточный рак легкого;
- Рак желудка или пищеводно-желудочного перехода;
- Рак мочевого пузыря;
- Гепатоцеллюлярный рак;
- Колоректальный рак;
- Лимфома Ходжкина.
Преимущества терапии ниволумабом
Преимущество иммунотерапии состоит в том, что при показаниях, ее можно использовать у ослабленных, возрастных пациентов, с выраженной сопутствующей патологией ввиду меньшей токсичности и более легкой переносимостью.
То есть иммунотерапия дает новые возможности пациентам, которым химиотерапия противопоказана по состоянию здоровья.
Еще одним достоинством иммунотерапии является длительность ответа на лечение. Если по результатам контрольных обследований на иммунотерапии возникает регресс опухоли, то зачастую этот ответ может быть очень длительным.
Как проводится лечение Ниволумабом?
Препарат вводится в виде внутривенной инфузии в течение 30 или 60 минут согласно инструкции. Терапия ниволумабом должна продолжаться до прогрессирования или развития непереносимой токсичности.

Возможность назначать препарат одним из трех одобренных способов введения позволяет врачу подобрать оптимальный режим для каждого конкретного пациента:
- 3 мг/кг каждые 2 недели в течение 60 или 30 минут;
- 240 мг каждые 2 недели в течение 60 или 30 минут;
- 480 мг каждые 4 недели в течение 60 или 30 минут.
Отличие иммунотерапии от химиотерапии заключается в отсутствии специальной пре- и постмедикации. Пациент не нуждается в антиэметогенной терапии, глюкокортикостероидах, антигистаминных, гастропротективных препаратах. Не требуется принимать их для профилактики и между курсами иммунотерапии.
Побочные эффекты ниволумаба
Вторая сторона медали современной иммунотерапии – это побочные эффекты, осложнения, а также иммуноопосредованные нежелательные явления.
Токсичность на фоне иммунотерапии имеет другой профиль, нежели стандартная химиотерапия. Побочные действия ниволумаба связаны с аутоиммунными реакциями на фоне «гиперактивного» иммунитета. Они обусловлены избыточной активацией иммунной системы с аутоиммунным поражением нормальных тканей различных органов и систем.
Осложнения на терапии ниволумабом могут появиться уже в течение 1 недели или только через 54 недели от начала терапии, симптомы могут усиливаться в любой момент времени и приводить к фатальным последствиям.
Наиболее частыми побочными эффектами ниволумаба по результатам клинических исследований являются утомляемость (34%), сыпь (19%), зуд (14%), диарея (13%), тошнота (13%) и снижение аппетита (10%), а также – повышение температуры или озноб с лихорадочным состоянием. В большинстве случаев побочные реакции выражаются от легкой до средней степени тяжести.
Все побочные реакции, включая тяжелые, купируются или при помощи симптоматической терапии, или путем отмены иммунотерапии.
Что делать, если на лечении ниволумабом развились нежелательные явления?
Для того, чтобы устранить побочные эффекты иммунотерапии, необходимо не только знать весь анамнез и сопутствующие заболевания конкретного пациента, но и понимать природу и механизм иммуноопосредованной токсичности.
Крайне важно, чтобы лечение ниволумабом осуществлял онколог, который не только имеет опыт проведения иммунотерапии, но и умеет распознавать ее нежелательные явления на ранней стадии. Своевременное выявление осложнений позволит не только их купировать, но и не прерывать противоопухолевое лечение.
Например, когда мы проводим иммунотерапию в клинике, мы осуществляем тщательный мониторинг показателей систем организма, строго по графикам. Также мы информируем и обучаем пациентов, как оперативно выявить и вовремя среагировать на нежелательные явления, так как своевременная диагностика и надлежащая медикаментозная терапия может улучшить результаты и при этом не окажет негативного влияния на активность иммунного препарата.
Мы накопили большой клинический опыт применения ниволумаба и разработали собственные восстановительные программы и этапы действий для успешного устранения побочных эффектов иммунотерапии. Наш подход – сделать лечение не только эффективным, но и максимально комфортным для вас.
Запишитесь на прием к онкологу по телефону +7 (812) 952-83-73, и мы примем вас в день обращения.
Отзывы
Леонова О.П.
21 августа 2020
Хочу выразить благодарность сотрудникам клиники De Vita и особенно врачу-химиотерапевту Кругловой Марине Сергеевне за квалифицированную помощь, человечное отношение, высокий профессионализм. В тяжелые моменты онкологического лечения необходимы грамотные и своевременные консультации, психологическая помощь и поддержка. Все это было сделано в вашей клинике.
Спасибо вам за ваш опыт, профессионализм, грамотность и человеческое отношение. С уважением,
…
Читать полностью
семья Ивановых
20 августа 2020
Благодаря грамотному лечению, профессионализму и внимательному отношению врача с большой буквы Ирины Александровны, я вернулась к жизни! Спасибо Вам большое, что в самое сложное время для нашей семьи Вы были с нами! Отдельное спасибо хирургу Сергею Александровичу и всему медицинскому персоналу! С уважением, семья Ивановых. Желаем здоровья, долголетия и многомонетия!
…
Читать полностью
Замулина И.В.
7 августа 2020
Благодарю за чуткость, профессионализм, доброе отношение в клинике Де Вита. Очень серьезное лечение прошла легко и без побочных эффектов. Отдельное спасибо за профессионализм Анне Игоревне Буйняковой! С благодарностью,
…
Читать полностью
Вот и закончился мой 12-недельный курс химиотерапии в клинике De Vita.
Все это время сотрудники клиники помогали мне пройти лечение без осложнений и максимально комфортно .
Хочу поблагодарить:
— руководство за безупречную организацию работы и замечательно подобранных сотрудников;
— моего лечащего врача Круглову Марину Сергеевну за профессионализм, внимание и доброе отношение благодаря которому я поверила в лечение и смогла его выдержать;
— замечательных медсестер за золотые руки и сердечность, особенно Анастасию;
— улыбчивых и внимательных менеджеров, которые встречали и провожали меня каждый раз.
Желаю всем работникам крепкого здоровья, хорошего настроения и терпения в нелегком труде.
…
Читать полностью
Елена Викторовна
17 июля 2020
Хочу сказать большое спасибо всем сотрудникам клиники De VIta, это замечательные, внимательные, знающие свое дело люди. Отдельное спасибо моему лечащему врачу Буйняковой А.И. за ее помощь, поддержку и внимание. Доктора знаю уже больше 10 лет и очень ей благодарна за маму, которую она подняла на ноги. Судьба меня свела опять с Анной Игоревной, я очень рада, что эта замечательная женщина, мой лечащий врач. Она не просто профессионал своего дела, а красивая, чуткая женщина. И я от всего сердца хочу поблагодарить ее за все усилия и помощь в лечении. Так же огромное спасибо девочкам мед.сестрам и администраторам за четкую, слаженную работу. Всем сотрудникам клиники желаю успехов, процветания и конечно здоровья.
…
Читать полностью
Григорьева Л.Е.
26 июня 2020
Сегодня 26 июня 2020 года — моя последняя капельница!!! Позади долгий непростой путь длиной в 6 месяцев. И все это время я чувствовала огромную поддержку и внимание своего доктора Буйняковой Анны Игоревны.
Уважаемая, дорогая Анна Игоревна! Огромное Вам спасибо и низкий поклон за Вашу отзывчивость, Ваш профессионализм, чуткость, внимательность, ответственность, за позитивный настрой! Хочется поблагодарить медсестру Людмилу за ее «волшебные руки», внимательность, ответственное отношение к больным. Спасибо девушкам администраторам Яне и Марии, Вале за доброжелательность и внимание, четкую слаженную работу, а также психологу А.А. Ястребовой за моральную поддержку. Желаю всем сотрудникам ДеВита успехов, процветания, здоровья!
…
Читать полностью
семья Чаусовых
21 июня 2020
Наша семья выражает благодарность Уваровой Светлане Николаевне, Кругловой Марине Сергеевне и всему персоналу онкологического центра за отзывчивость, доброжелательность, высокий профессионализм. Поздравляем Вас с Днем Медицинского работника! Пусть всё сделанное Вами добро возвращается к Вам многократно в виде здоровья и долголетия!!
…
Читать полностью
Спасибо всей команде De Vita за работу и отношение. Особенно благодарю Андрея Сергеевича за профессионализм и поддержку! Спокойствие и уверенность врача передаётся пациенту, мне это очень помогло. В такой трудной ситуации сходишь с ума, здесь я получила помощь! А также все ответы на свои вопросы, заботу, хорошее лечение и только позитивный заряд. Спасибо!
…
Читать полностью
Поздравляю клинику с днём рождения и хочу сердечно поблагодарить химиотерапевта Анну Игоревну Буйнякову за высокий профессионализм, за помощь и поддержку в непростой «химический» период. Ни один вопрос не остался без ответа, Анна Игоревна практически провела меня за руку через всю химию. Спасибо Вам огромное за это!
Также благодарю и хочу отметить медсестру Людмилу, ее отличную работу и душевность. Очень хорошее и приятное впечатление от всех, с кем пришлось разговаривать и встречаться в клинике. Хорошие и комфортные условия для лечения такого коварного заболевания. Вы даёте уверенность в победе! Низкий поклон вам!
Татьяна, Великий Новгород.
…
Читать полностью
Юдина Наталия Андреевна
15 мая 2020
Всех сотрудников De Vita хочу поблагодарить за внимательное и чуткое отношение к запросам и потребностям клиентов. Отдельная огромная-преогромная благодарность лечащему врачу Буйняковой Анне Игоревне за профессионализм, отзывчивость, внимательность, за веру в возможности пациента, за готовность прийти на помощь а любое время суток. Здоровья Вам, успехов, всех благ.! Спасибо Вам большое.
С уважением,
…
Читать полностью
Ниволумаб
Nivolumab
Фармакологическое действие
Ниволумаб — человеческое моноклональное антитело, которое блокирует взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами (PD-L1 и PD-L2). Ниволумаб представляет собой иммуноглобулин G4 (IgG4), его приблизительная молекулярная масса составляет 146 кДа.
PD-1 рецептор является негативным регулятором активности T-клеток. Связывание PD-1 с лигандами PD-L1 и PD-L2, которые способны экспрессироваться клетками опухолей или иными клетками микроокружения опухолей, приводит к ингибированию пролиферации Т-клеток и секреции цитокинов. Ниволумаб потенцирует иммунный ответ посредством блокады связывания PD-1 с лигандами PD-L1 и PD-L2. В исследованиях на мышиных моделях блокирование активности PD-1 приводило к уменьшению роста опухоли.
Фармакокинетика
Фармакокинетика ниволумаба линейна в диапазоне доз от 0,1 до 10 мг/кг.
В популяционном фармакокинетическом анализе установлено, что средний системный клиренс ниволумаба составляет 9,5 мл/ч (коэффициент вариабельности 49,7 %); средний объём распределения в равновесном состоянии (Vss— 8 л (коэффициент вариабельности 30,4 %); средний период полувыведения (T½) — 26,7 дня (коэффициент вариабельности 101 %). Максимальная и минимальная плазменные концентрации (Cmax, Cmin) и средняя концентрации ниволумаба в плазме после введения в течение 2 недель в дозе 3 мг/кг составляла 57; 116 и 75,3 мкг/мл соответственно.
Метаболизм ниволумаба не описан, однако ввиду идентичности структуры ниволумаба и человеческого моноклонального антитела IgG4 предполагаемый путь метаболизма соответствует метаболизму эндогенного Ig — распад на аминокислоты в каталитическом пути обмена белка.
Особые группы пациентов
Популяционный фармакокинетический анализ показал отсутствие зависимости клиренса ниволумаба от возраста пациента, пола, расы, типа опухоли, размера опухоли и наличия нарушений функции печени. Хотя в исследованиях и наблюдалась слабая зависимость клиренса от показаний ЭКГ, уровня гломерулярной фильтрации, количества сывороточного альбумина и массы тела (от 34 до 162 кг), эта связь была признана клинически незначимой.
Нарушение функции почек
Фармакокинетические свойства ниволумаба были изучены у пациентов с лёгкой (клиренс креатинина от 60 до <90 мл/мин/1,73 м2), средней (от 30 до <60 мл/мин/1,73 м2), тяжёлой (<30 мл/мин и >15 мл/мин/1,73 м2) степенью почечной недостаточности в сравнении с пацентами с нормальной функцией почек (клиренс креатинина >90 мл/мин/1,73 м2). Не наблюдались клинически значимые различия в клиренсе ниволумаба у пациентов с лёгкой и средней почечной недостаточностью и пациентов с нормальной функцией почек. Клиренс ниволумаба у пациентов с тяжёлой почечной недостаточностью недостаточно изучен.
Нарушение функции печени
Фармакокинетические свойства были изучены у пациентов с лёгкой степенью печёночной недостаточности (повышение общего билирубина в 1–1,5 раза выше верхней границы нормы (ВГН) или аспартатаминотрансферазы (ACT) выше ВГН, классификация национального института рака) и пациентов с нормальной функцией печени (общий билирубин и ACT в пределах нормы). Различий в клиренсе ниволумаба между вышеуказанными группами пациентов не обнаружено. Фармакокинетика ниволумаба не изучалась у пациентов со средней степенью печёночной недостаточности (повышение общего билирубина в 1,5–3 × ВГН и ACT выше ВГН) и тяжёлой степенью печёночной недостаточности (повышение общего билирубина более 3 × ВГН и ACT выше ВГН).
Показания
- Монотерапия у взрослых — неоперабельная или метастатическая меланома;
- местнораспространённый или метастатический немелкоклеточный рак лёгкого после предшествующей химиотерапии;
- распространённый почечноклеточный рак после предшествующей системной терапии.
Противопоказания
- Повышенная чувствительность к ниволумабу;
- беременность;
- лактация (кормление грудью);
- возраст до 18 лет (данные по эффективности и безопасности отсутствуют).
С осторожностью
Тяжёлые аутоиммунные заболевания в активной стадии, при которых дальнейшая активация иммунной системы может представлять потенциальную угрозу жизни; нарушение функции печени средней и тяжёлой степени; нарушение функции почек тяжёлой степени.
Опыт применения ниволумаба в терапии меланомы с положительной BRAF-мутацией у пациентов, ранее не получавших лечение, ограничен.
Пациенты с сопутствующими метастазами в головной мозг, активным аутоиммунным заболеванием или заболеваниями, требующими терапии системными иммунодепрессантами, были исключены из основного клинического исследования почечноклеточного рака. В случае отсутствия данных ниволумаб следует применять с осторожностью у данных групп пациентов после тщательной оценки соотношения польза-риск, основанной на индивидуальных показателях.
Отдельные группы пациентов
В клинических исследованиях не принимали участие следующие группы пациентов:
- пациенты с показателями исходного функционального статуса >2, неизлеченными метастазами головного мозга, аутоиммунными заболеваниями и пациенты, получавшие системные иммунодепрессанты до начала проведения исследования;
- пациенты с симптоматическими интерстициальными заболеваниями лёгких и меланомой глаза были исключены из проведения клинических исследований немелкоклеточного рака лёгкого и меланомы;
- пациенты с 4-й степенью тяжести нежелательных реакций, связанных с ранее проводимой анти-CTLA-4-терапией в анамнезе.
Ввиду отсутствия данных, ниволумаб должен применяться с осторожностью у данных групп пациентов после проведения оценки соотношения риск-польза, основанной на индивидуальных показателях.
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — D.
Адекватных и строго контролируемых исследований по безопасности применения ниволумаба при беременности не проведено. Исследования на животных показали репродуктивную токсичность ниволумаба. IgG4 может проникать через плацентарный барьер, поэтому вероятно воздействие препарата на плод. Применение ниволумаба при беременности противопоказано.
В период лечения ниволумабом пациенты репродуктивного возраста должны пользоваться надёжными методами контрацепции. В случае наступления беременности, отсутствия менструации или при подозрении на возможную беременность пациентка должна сообщить об этом своему лечащему врачу.
Во время лечения и на период как минимум 5 месяцев после последнего введения ниволумаба женщинам детородного возраста рекомендуется применение контрацепции.
Применение в период грудного вскармливания
Исследований касательно проникновения ниволумаба в грудное молоко женщин в период лактации не проводилось. Согласно общим сведениям, попадание антител в грудное молоко возможно, поэтому нельзя исключить риск для новорождённого при применении ниволумаба в период грудного вскармливания. Ввиду потенциальной опасности развития серьёзных побочных реакций у ребёнка применение ниволумаба при кормлении грудью противопоказано.
Способ применения и дозы
Режим дозирования индивидуальный, в зависимости от схемы терапии и лекарственной формы. Препарат должен вводиться под руководством врача, имеющего опыт лечения онкологических заболеваний.
Побочные действия
При применении ниволумаба чаще всего отмечались иммуноопосредованные побочные реакции. Большинство таких побочных реакций, включая тяжёлые, купировались при помощи соответствующей терапии или путём отмены терапии.
В клинических исследованиях с применением ниволумаба в качестве монотерапии в дозе 3 мг/кг по типам опухолей наиболее частыми (≥10 %) нежелательными реакциями были утомляемость (34 %), сыпь (19 %), зуд (14 %), диарея (13 %), тошнота (13 %) и снижение аппетита (10 %). В большинстве случаев побочные реакции были выражены от лёгкой до средней степени (степень 1 и 2).
Ниже приведены побочные реакции, отмечавшиеся у пациентов, получавших терапию ниволумабом. Побочные реакции представлены по частоте их регистрации: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1 000, <1/100); редко (≥1/10 000, <1/1 000); очень редко (<1/10 000).
Инфекции и инвазии
Часто — инфекция верхних дыхательных путей; нечасто — бронхит, пневмония; редко — энцефалит.
Новообразования доброкачественные, злокачественные и неустановленной природы (в том числе кисты и полипы)
Редко — гистиоцитарный некротический лимфаденит (лимфаденит Кикучи).
Со стороны крови и лимфатической системы
Нечасто — эозинофилия.
Со стороны иммунной системы
Часто — инфузионные реакции1; нечасто — анафилактические реакции1, гиперчувствительность1.
Со стороны эндокринной системы
Часто — гипергликемия, гипотиреоз, гипертиреоз; нечасто — недостаточность функции надпочечников, гипопитуитаризм, гипофизит, тиреоидит, диабетический кетоацидоз, сахарный диабет.
Со стороны обмена веществ и питания
Очень часто — снижение аппетита; нечасто — дегидратация, метаболический ацидоз.
Со стороны нервной системы
Часто — периферическая нейропатия, головная боль, головокружение; нечасто — полинейропатия; редко — синдром Гийена-Барре, демиелинизация, миастенический синдром, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов).
Со стороны органа зрения
Часто — нечёткость зрения, сухость глаз; нечасто — увеит.
Со стороны сердечно-сосудистой системы
Часто — повышение артериального давления; нечасто — тахикардия, васкулит; редко — аритмия (включая желудочковую), мерцательная аритмия.
Со стороны дыхательной системы
Часто — пневмонит1, одышка, кашель; нечасто — плеврит; редко — инфильтрация лёгких.
Со стороны желудочно-кишечного тракта
Очень часто — диарея, тошнота; часто — колит, стоматит, рвота, боль в животе, запор, сухость во рту; нечасто — панкреатит; редко — гастрит, язва двенадцатиперстной кишки.
Со стороны печени и желчных путей
Нечасто — гепатит1, гипербилирубинемия; редко — холестаз.
Со стороны кожи и подкожной клетчатки
Очень часто — сыпь2, зуд; часто — витилиго, сухость кожи, эритема, алопеция; нечасто — многоформная эритема, псориаз, розацеа, крапивница; редко — токсический эпидермальный некролиз3.
Со стороны опорно-двигательного аппарата
Часто — костно-мышечная боль4, артралгия; нечасто — ревматическая полимиалгия.
Со стороны почек и мочевыводящих путей
Нечасто — тубулоинтерстициальный нефрит, почечная недостаточность1, 3.
Общие нарушения и реакции на введение
Очень часто — повышенная утомляемость; часто — повышение температуры тела, отёки (включая периферические); нечасто — боль в груди.
Со стороны лабораторных показателей
Очень часто — снижение массы тела; часто — повышение активности трансаминаз, липазы, амилазы и щелочной фосфатазы (ЩФ), повышение уровня креатинина, лимфопения, лейкопения, тромбоцитопения, анемия, гипонатриемия; нечасто — повышение концентрации общего билирубина, гиперкальциемия, гипокальциемия, гиперкалиемия. гипокалиемия, гипомагнезиемия, нейтропения, снижение абсолютного числа нейтрофилов, гипернатриемия; редко — гипермагнезиемия.
1Включая жизнеугрожающие побочные реакции.
2Включая пятнисто-папулезную, эритемную, зудящую, везикулёзную, макулёзную, кореподобную, папулёзную, пустулёзную, папуло-сквамозную, генерализованную сыпь, дерматит, акнеформный дерматит, аллергический дерматит, атопический дерматит, буллезный дерматит, эксфолиативный дерматит, псориазоформный дерматит, медикаментозную сыпь.
3Включая побочные реакции с летальным исходом.
4Включая боль в спине, костную боль, мышечно-скелетную боль в груди, костно-мышечный дискомфорт, миалгию, боль в шее и конечностях, спинальную боль.
Иммуногенность
Ниволумаб, как и другие моноклональные антитела, обладает иммуногенностыо.
У 11 % пациентов, получавших терапию ниволумабом, наблюдалось образование антител к ниволумабу. Нейтрализация антител определилась у двух пациентов (0,6 %). Однако зависимость наличия антител в плазме крови и изменений фармакокинетических параметров, выраженности клинического эффекта и развития побочных эффектов не выявлена.
Передозировка
Случаев передозировки выявлено не было.
Лечение
При передозировке лечение должно заключаться в симптоматической лекарственной терапии в соответствии с возникающими побочными реакциями при тщательном наблюдении за пациентом.
Взаимодействие
Фармакокинетическое взаимодействие
Ниволумаб представляет собой человеческое моноклональное антитело. Ввиду того, что антитела не подвергаются метаболизму при участии изоферментов цитохрома P450 и других изоферментов, ингибирование или индукция этих ферментов при совместном применении с другими препаратами не оказывают влияние на фармакокинетику ниволумаба.
Другие формы взаимодействия
Системная иммуносупрессия
В связи с возможностью фармакодинамического взаимодействия следует избегать применения системных глюкокортикостероидов и других иммунодепрессантов перед назначением терапии ниволумабом. После начала терапии ниволумабом глюкокортикостероиды и другие иммунодепрессанты могут применяться для коррекции иммуноопосредованных побочных реакций, вызванных воздействием ниволумаба на иммунную систему. Применение системных глюкокортикостероидов после начала лечения ниволумабом не снижает его эффективность.
Особые указания
Ниволумаб может вызывать тяжёлые, в том числе с летальным исходом, побочные реакции, вызванные влиянием на иммунную систему и обусловленные специфическим механизмом его действия. Пациенты должны находиться под непрерывным контролем (как минимум 5 месяцев после введения последней дозы), так как нежелательные реакции, обусловленные воздействием ниволумаба, могут развиться в любой момент во время применения или после отмены терапии. При подозрении на развитие иммуноопосредованной нежелательной реакции должна быть проведена адекватная оценка для подтверждения или исключения иной этиологии. Основываясь на тяжести нежелательной реакции, применение ниволумаба должно быть прекращено с возобновлением или без назначения глюкокортикостероидов.
В случае проведения иммуносупрессивной терапии глюкокортикостероидами, предназначенной для устранения нежелательных реакций, после улучшения состояния снижение дозы глюкокортикостероидов проводят медленно, в течение по меньшей мере 1 месяца. Быстрое снижение дозы может привести к ухудшению тяжести или рецидиву нежелательных реакций. Иммуносупрессивная терапия препаратами, отличными от глюкокортикостероидов, назначается в случае наступления ухудшения или отсутствия улучшения при применении глюкокортикостероидов.
Применение ниволумаба следует прекратить во время получения пациентом иммуносупрессивной дозы глюкокортикостероидов или проведения иммуносупрессивной терапии.
Ниволумаб должен быть отменён при любых рецидивирующих иммуноопосредованных нежелательных реакциях от средней до тяжёлой степени и отменён без возобновления при тяжёлом иммуноопосредованном пневмоните и иммуноопосредованном гепатите, а также жизнеугрожающих иммуноопосредованных нежелательных реакциях.
Применение ниволумаба у пациентов с быстрым прогрессированием меланомы
Врачи должны обсудить эффект отсроченного действия ниволумаба до начала проведения лечения у пациентов с быстро прогрессирующим заболеванием.
Иммуноопосредованный пневмонит
При терапии ниволумабом были отмечены случаи тяжёлого пневмонита или интерстициального заболевания лёгких, включая случаи с летальным исходом. Пациенты должны наблюдаться на наличие признаков и симптомов пневмонита, таких как рентгенографические изменения (например, затемнение по типу матового стекла, очаги воспаления), одышка и гипоксия. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3-й или 4-й степени тяжести пневмонита применение ниволумаба следует отменить без возобновления и начать приём глюкокортикостероидов в дозе, эквивалентной 2–4 мг/кг/день метилпреднизолона.
При 2-й степени тяжести (симптоматическая) пневмонита применение ниволумаба следует приостановить и начать приём глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на приём глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 2–4 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованный колит
При терапии ниволумабом были отмечены случаи тяжёлой диареи или колита. Пациенты должны наблюдаться на наличие признаков диареи и дополнительных симптомов колита, таких как боль в животе, слизь или кровь в стуле. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 4-й степени тяжести диареи или колита применение ниволумаба следует отменить окончательно и начать приём глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 3-й степени тяжести диареи или колита применение ниволумаба следует приостановить и начать приём глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на приём глюкокортикостероидов, применение ниволумаба должно быть отменено без возобновления.
При 2-й степени тяжести диареи или колита применение ниволумаба следует приостановить. Персистирующую диарею или колит следует устранять при помощи введения глюкокортикостероидов в дозе, эквивалентной 0,5–1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на приём глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованный гепатит
При терапии ниволумабом были отмечены случаи тяжёлого гепатита. Пациенты должны наблюдаться на наличие признаков и симптомов гепатита, таких как повышение уровня трансаминаз и общего билирубина. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3-й или 4-й степени тяжести повышения уровня трансаминаз и общего билирубина применение ниволумаба следует отменить без возобновления и начать приём глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 2-й степени тяжести повышения уровня трансаминаз и общего билирубина применение ниволумаба следует приостановить. Персистирующий подъём уровня этих лабораторных показателей должен быть устранён при помощи введения глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на приём глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованные нефрит и почечная дисфункция
При терапии ниволумабом были отмечены случаи тяжёлого нефрита или почечной дисфункции, поэтому пациенты должны наблюдаться на наличие их признаков и симптомов. У большинства пациентов отмечено бессимптомное повышение уровня сывороточного креатинина. Должна быть исключена этиология, связанная с заболеванием.
При 4-й степени тяжести повышения уровня сывороточного креатинина применение ниволумаба следует отменить окончательно и начать приём глюкокортикостероидов в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
При 2-й или 3-й степени тяжести повышения уровня сывороточного креатинина применение ниволумаба следует приостановить и начать приём глюкокортикостероидов в дозе, эквивалентной 0,5–1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются несмотря на приём глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1–2 мг/кг/день метилпреднизолона, и применение ниволумаба должно быть отменено без возобновления.
Иммуноопосредованная эндокринопатия
При терапии ниволумабом были отмечены случаи тяжёлой эндокринопатии, включая гипотиреоз, гипертиреоз, недостаточность коры надпочечников, гипофизит, сахарный диабет и диабетический кетоацидоз.
Пациенты должны наблюдаться на наличие признаков и симптомов эндокринопатии и изменения функции щитовидной железы (в начале лечения, периодически во время лечения и основываясь на клинической оценке). У пациентов может отмечаться усталость, головная боль, изменение психического состояния, боль в животе, необычный ритм работы кишечника и гипотония или неспецифические симптомы, которые могут иметь сходство с другими состояниями, такими как метастазы в головной мозг или сопутствующие заболевания. Если иная этиология не выявлена, признаки и симптомы эндокринопатии должны считаться иммуноопосредованными.
При симптоматическом гипотиреозе применение ниволумаба следует приостановить и в случае необходимости провести заместительную терапию гормонами щитовидной железы. При симптоматическом гипертиреозе применение ниволумаба следует приостановить и в случае необходимости провести терапию антитиреоидными средствами. В случае острого тиреоидита должны назначаться глюкокортикостероиды в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. Необходимо продолжать наблюдение за функцией щитовидной железы для контроля адекватности проводимой заместительной гормональной терапии гормонами щитовидной железы.
При симптоматической недостаточности коры надпочечников 2-й степени применение ниволумаба следует приостановить и в случае необходимости провести физиологическое замещение глюкокортикостероидов. При симптоматической недостаточности коры надпочечников 3–4-й степени применение ниволумаба следует отменить окончательно и в случае необходимости провести физиологическое замещение глюкокортикостероидов. Необходимо продолжать наблюдение за функцией надпочечников и уровнем гормонов для контроля адекватности проводимой заместительной терапии глюкокортикостероидами. При симптоматическом гипофизите 2–3-й степени применение ниволумаба следует приостановить и провести в случае необходимости гормонозаместительную терапию. В случае острого гипофизита назначают глюкокортикостероиды в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. При симптоматическом гипофизите 4-й степени терапия ниволумабом должна быть отменена окончательно. Необходимо продолжать наблюдение за функцией гипофиза и уровнем гормонов для контроля адекватности проводимой гормонозаместительной терапии.
При симптоматическом диабете применение ниволумаба следует приостановить и провести в случае необходимости заместительную терапию инсулином. Необходимо контролировать уровень сахара в крови для контроля адекватности проводимой заместительной терапии инсулином.
Иммуноопосредованная сыпь
При терапии ниволумабом были отмечены случаи тяжёлой формы сыпи (включая редкие случаи летального токсического эпидермального некролиза), которые могут иметь иммуноопосредованную природу. Применение ниволумаба следует прекратить при сыпи 3-й степени тяжести и отменить без восстановления при 4-й степени тяжести. При сыпи тяжёлой степени назначается лечение глюкокортикостероидами в дозе, эквивалентной 1–2 мг/кг/день метилпреднизолона.
Ниволумаб следует назначать с осторожностью пациентам, у которых ранее отмечались тяжёлые или жизнеугрожающие нежелательные кожные реакции при лечении иными иммуностимулирующими противоопухолевыми средствами.
Другие иммуноопосредованные нежелательные реакции
Следующие иммуноопосредованные нежелательные реакции были отмечены у менее 1% пациентов, получавших лечение ниволумабом во время проведения клинических исследований при любом дозировании и типе опухоли: панкреатит, увеит, демиелинизация, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов), синдром Гийена-Барре, гипопитуитаризм, миастенический синдром и энцефалит.
При подозрении на иммуноопосредованные нежелательные реакции должна быть проведена адекватная оценка для подтверждения этиологии или исключения иных причин их появления. Исходя из тяжести нежелательной реакции, применение ниволумаба следует прекратить и начать терапию глюкокортикостероидами. При наступлении улучшения приём ниволумаба может быть продолжен после медленного снижения дозы глюкокортикостероидов. Ниволумаб должен быть отменён без возобновления при проявлении любых рецидивирующих тяжёлых и любых жизнеугрожающих иммуноопосредованных нежелательных реакций.
Инфузионные реакции
Во время клинических исследований отмечались случаи тяжёлых инфузионных реакций. В случае развития тяжёлых инфузионных реакций введение ниволумаба должно быть прекращено с назначением соответствующей лекарственной терапии. Пациенты с лёгкой или умеренной инфузионной реакцией могут продолжать терапию ниволумабом под непрерывным наблюдением и с проведением премедикации в соответствии с действующими стандартами профилактики инфузионных реакций.
Влияние на способность к вождению автотранспорта и управлению механизмами
Ввиду возможного появления нежелательных реакций, таких как утомляемость, пациентам следует воздерживаться от управления транспортом и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций в период лечения ниволумабом, до установления факта, что данные побочные реакции у них отсутствуют.
Классификация
-
АТХ
L01XC17, L01FF01
-
Фармакологическая группа
-
Коды МКБ 10
-
Категория при беременности по FDA
D
(риск доказан)
Информация о действующем веществе Ниволумаб предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Ниволумаб, содержатся в инструкции производителя, прилагаемой к упаковке.

Fab fragment of nivolumab (blue) binding the extracellular domain of PD-1 (purple). From PDB entry 5ggr. |
|
| Monoclonal antibody | |
|---|---|
| Type | Whole antibody |
| Source | Human |
| Target | PD-1 |
| Clinical data | |
| Trade names | Opdivo |
| Other names | ONO-4538, BMS-936558, MDX1106 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a614056 |
| License data |
|
| Pregnancy category |
|
| Routes of administration |
Intravenous (IV) |
| Drug class | Immunotherapy[2] |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Identifiers | |
| CAS Number |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEMBL |
|
| Chemical and physical data | |
| Formula | C6362H9862N1712O1995S42 |
| Molar mass | 143599.39 g·mol−1 |
Nivolumab, sold under the brand name Opdivo, is a medication used to treat a number of types of cancer.[7] This includes melanoma, lung cancer, malignant pleural mesothelioma, renal cell carcinoma, Hodgkin lymphoma, head and neck cancer, urothelial carcinoma, colon cancer, esophageal squamous cell carcinoma, liver cancer, gastric cancer, and esophageal or gastroesophageal junction (GEJ) cancer.[5][6][7][8][9] It is used by slow injection into a vein.[5][6][7]
The most common side effects include fatigue, rash, musculoskeletal pain, pruritus, diarrhea, nausea, asthenia, cough, dyspnea, constipation, decreased appetite, back pain, arthralgia, upper respiratory tract infection, pyrexia, headache, abdominal pain, and vomiting.[9] Use during pregnancy may harm the baby and use when breastfeeding is not recommended.[7][1] Nivolumab is a human IgG4 monoclonal antibody that blocks PD-1.[7] It is a type of immunotherapy and works as a checkpoint inhibitor, blocking a signal that prevents activation of T cells from attacking the cancer.[7][2] The most common side effects when used in combination with chemotherapy include peripheral neuropathy (damage to the nerves outside of the brain and spinal cord), nausea, fatigue, diarrhea, vomiting, decreased appetite, abdominal pain, constipation and musculoskeletal pain.[8]
Nivolumab was approved for medical use in the United States in 2014.[7][5] It is on the World Health Organization’s List of Essential Medicines.[10] It is made using Chinese hamster ovary cells.[11] Nivolumab is the second FDA-approved systemic therapy for mesothelioma[12] and is the first FDA-approved immunotherapy for the first-line treatment of gastric cancer.[8]
Medical uses[edit]
In the U.S., nivolumab is indicated to treat:
- Unresectable or Metastatic Melanoma[5]
- Adjuvant Treatment of Melanoma[5]
- Metastatic Non-Small Cell Lung Cancer[5]
- Malignant Pleural Mesothelioma[5]
- Advanced Renal Cell Carcinoma[5]
- Classical Hodgkin Lymphoma[5]
- Squamous Cell Carcinoma of the Head and Neck[5]
- Urothelial Carcinoma[5]
- Microsatellite Instability-High or Mismatch Repair Deficient Metastatic Colorectal Cancer[5]
- Hepatocellular Carcinoma[5]
- Esophageal Cancer[5]
- Gastric Cancer, Gastroesophageal Junction Cancer, and Esophageal Adenocarcinoma[5]
Nivolumab is used as a first-line treatment for inoperable or metastatic melanoma in combination with ipilimumab if the cancer does not have a mutation in BRAF,[5] and as a second-line treatment for inoperable or metastatic melanoma following treatment of ipilimumab and, if the cancer has a BRAF mutation, a BRAF inhibitor.[5][13] It is also used to treat metastatic squamous non-small cell lung cancer with progression with or after platinum-based drugs and for treatment of small cell lung cancer[5][14] It also used as a second-line treatment for renal cell carcinoma after anti-angiogenic treatment has failed.[5]
Nivolumab is used for primary or metastatic urothelial carcinoma, the most common form of bladder cancer. It can be prescribed for locally advanced or metastatic form of the condition that experience disease progression during or following platinum-containing chemotherapy or have progression within 12 months of neoadjuvant or adjuvant treatment with platinum-containing chemotherapy.[15]
Nivolumab is indicated for the adjuvant treatment of people with melanoma with involvement of lymph nodes or in people with metastatic disease who have undergone complete resection.[5][16]
The combination of nivolumab with ipilimumab is used for the first-line treatment of adults with malignant pleural mesothelioma (MPM) that cannot be removed by surgery.[5][12]
In April 2021, the U.S. Food and Drug Administration (FDA) approved nivolumab, in combination with certain types of chemotherapy, for the initial treatment of people with advanced or metastatic gastric cancer, gastroesophageal junction cancer and esophageal adenocarcinoma.[8]
In May 2021, the U.S. FDA approved nivolumab for people with completely resected esophageal or gastroesophageal junction (GEJ) cancer with residual pathologic disease who have received neoadjuvant chemoradiotherapy.[9]
In August 2021, the U.S. FDA approved nivolumab for the adjuvant treatment of people with urothelial carcinoma (UC) who are at high risk of recurrence after undergoing radical resection.[17]
In May 2022, the U.S. FDA expanded the indication to include the first-line treatment of patients with advanced or metastatic esophageal squamous cell carcinoma (ESCC).[18]
Side effects[edit]
The drug label contains warnings with regard to increased risks of severe immune-mediated inflammation of the lungs, the colon, the liver, the kidneys (with accompanying kidney dysfunction), as well as immune-mediated hypothyroidism and hyperthyroidism.[5] Hypothyroidism may affect 8.5% and hyperthyroidism 3.7%.[19] Autoimmune diabetes similar to diabetes mellitus type 1 may occur in approximately 2% of people treated with nivolumab.[19]
In trials for melanoma, the following side effects occurred in more than 10% of subjects and more frequently than with chemotherapy alone: rash and itchy skin, cough, upper respiratory tract infections, and peripheral edema. Other clinically important side effects with less than 10% frequency were ventricular arrhythmia, inflammation of parts of the eye (iridocyclitis), infusion-related reactions, dizziness, peripheral and sensory neuropathy, peeling skin, erythema multiforme, vitiligo, and psoriasis.[5]
In trials for lung cancer, the following side effects occurred in more than 10% of subjects and more frequently than with chemotherapy alone: fatigue, weakness, edema, fever, chest pain, generalized pain, shortness of breath, cough, muscle and joint pain, decreased appetite, abdominal pain, nausea and vomiting, constipation, weight loss, rash, and itchy skin.[5]
Levels of electrolytes and blood cells counts were also disrupted.[5]
Pregnancy and breastfeeding[edit]
Use during pregnancy may harm the baby; it is not known if nivolumab is secreted in breast milk but use during breastfeeding is not recommended.[5][1][7]
Pharmacokinetics[edit]
Based on data from 909 patients, the terminal half-life of nivolumab is 26.7 days and steady-state concentrations were reached by 12 weeks when administered at 3 mg/kg every 2 weeks.[5]: 29 Age, gender, race, baseline LDH, PD-L1 expression, tumor type, tumor size, renal impairment, and mild hepatic impairment do not affect clearance of the drug.[5]: 30
Mechanism of action[edit]
T cells protect the body from cancer by killing certain cancer cells. But cancer cells evolve proteins to protect themselves from T cells. Nivolumab blocks those protective proteins. Thus, the T cells can kill the cancer cells.[20][21] This is an example of immune checkpoint blockade.[20][21]
PD-1 is a protein on the surface of activated T cells. If another molecule, called programmed cell death 1 ligand 1 or programmed cell death 1 ligand 2 (PD-L1 or PD-L2), binds to PD-1, the T cell becomes inactive. This is one way that the body regulates the immune system, to avoid an overreaction.[21] Many cancer cells make PD-L1, which inhibits T cells from attacking the tumor. Nivolumab blocks PD-L1 from binding to PD-1, allowing the T cell to work.[20][21] PD-L1 is expressed on 40–50% of melanomas and has limited expression otherwise in most visceral organs with the exception of respiratory epithelium and placental tissue.[13]
Physical properties[edit]
Nivolumab is a fully human monoclonal immunoglobulin G4 antibody to PD-1.[13] The gamma 1 heavy chain is 91.8% unmodified human design while the kappa light chain is 98.9%.[22]
History[edit]
Nivolumab was generated under intellectual property of Ono Pharmaceutical regarding PD-1 and under a research collaboration entered in 2005 between Ono and Medarex.[citation needed]
Through the research collaboration with Ono, it was invented by Dr. Changyu Wang and his team of scientists at Medarex using its transgenic mice with a humanized immune system; the discovery and in vitro characterization of the antibody, originally called MDX-1106/ONO-4538, was published (much later) in 2014.[23] Under the agreement between the companies in 2005, Medarex held an exclusive right of nivolumab in North America, and Ono retained the right in all other countries except North America.
Bristol-Myers Squibb acquired Medarex in 2009, for $2.4B, largely on the strength of its checkpoint inhibitor program.[24][25]
Promising clinical trial results made public in 2012, caused excitement among industry analysts and in the mainstream media; PD-1 was being avidly pursued as a biological target at that time, with companies including Merck with pembrolizumab (Keytruda), Roche (via its subsidiary Genentech) with atezolizumab, GlaxoSmithKline in collaboration with the Maryland biotech company Amplimmune; and Teva in collaboration with the Israeli biotech company CureTech competing.[26][27]
Ono received approval from Japanese regulatory authorities to use nivolumab to treat unresectable melanoma in July 2014, which was the first regulatory approval of a PD-1 inhibitor anywhere in the world.[28]
Merck received its first FDA approval for its PD-1 inhibitor, pembrolizumab (Keytruda), in September 2014.[29]
Nivolumab received FDA approval for the treatment of melanoma in December 2014.[13][30] In April 2015, the Committee for Medicinal Products for Human Use of the European Medicines Agency recommended approval of Nivolumab for metastatic melanoma as a monotherapy.[31]
In March 2015, the U.S. FDA approved it for the treatment of squamous cell lung cancer.[32]
On 19 June 2015, the European Medicines Agency (EMA) granted a marketing authorization valid throughout the European Union.[6]
In November 2015, the FDA approved nivolumab as a second-line treatment for renal cell carcinoma after having granted the application breakthrough therapy designation, fast track designation, and priority review status.[33]
In May 2016, the FDA approved nivolumab for the treatment of patients with classical Hodgkin lymphoma (cHL) who have relapsed or progressed after autologous hematopoietic stem cell transplantation (auto-HSCT) and post-transplantation brentuximab vedotin.[34]
On 20 December 2017, the FDA granted approval to nivolumab for adjuvant treatment of melanoma with involvement of lymph nodes or for metastatic disease with complete resection.[35]
On 16 April 2018, the FDA granted approval to nivolumab in combination with ipilimumab for the first-line treatment of intermediate and poor risk advanced renal cell carcinoma patients.[36]
On 15 June 2018, China’s Drug Administration approved nivolumab, the country’s first immuno-oncology and the first PD-1 therapy.[37]
In October 2020, the U.S. Food and Drug Administration (FDA) approved the combination of nivolumab with ipilimumab for the first-line treatment of adults with malignant pleural mesothelioma (MPM) that cannot be removed by surgery.[12]
In April 2021, the FDA approved nivolumab, in combination with certain types of chemotherapy, for the initial treatment of people with advanced or metastatic gastric cancer, gastroesophageal junction cancer and esophageal adenocarcinoma.[8]
Research[edit]
Nivolumab, and other PD-1 inhibitors, appear to be effective in people with brain metastases[38] and for cancer in people with autoimmune diseases.[39]
Hodgkin’s lymphoma[edit]
In Hodgkin’s lymphoma, Reed–Sternberg cells harbor amplification of chromosome 9p24.1, which encodes PD-L1 and PD-L2 and leads to their constitutive expression. In a small clinical study published in 2015, nivolumab elicited an objective response rate of 87% in a cohort of 20 patients.[26]
The evidence is very uncertain about the effect of Nivolumab for patients with a Hodgkin’s lymphoma on the overall survival, the quality of life, the survival without a progression, the response rate (=complete disappear) and grade 3 or 4 serious adverse events.[40]
Biomarkers[edit]
Amplification of chromosome 9p24 may serve as a predictive biomarker in Hodgkin’s lymphoma.[26]
Each company pursuing mAbs against PD-1 as drugs developed assays to measure PD-L1 levels as a potential biomarker using their drugs as the analyte-specific reagent in the assay. BMS partnered with Dako on a nivolumab-based assay. However, as of 2015 the complexity of the immune response had hindered efforts to identify people who would be likely to respond well to PD-1 inhibitors;[26] in particular PD-L1 levels appear to be dynamic and modulated by several factors, and efforts to correlate PD-L1 levels before or during treatment with treatment response or duration of response had failed to reveal any useful correlations as of 2015.[13]
Lung cancer[edit]
In 2016, BMS announced the results of a clinical trial in which nivolumab failed to achieve its endpoint and was no better than traditional chemotherapy at treating newly diagnosed lung cancer.[41] BMS went on to attempt to win approval for a combination therapy against lung cancer which included nivolumab and BMS’s older drug ipilimumab. The application was withdrawn in early 2019 following disappointing clinical trial data.[42]
Infusion times of 60 minutes and 30 minutes appear to have similar pharmacokinetics (absorption, distribution, metabolism, and elimination) of the treatment.[43]
Nivolumab is indicated for the treatment of people with metastatic squamous non small cell lung cancer (NSCLC) with progression on or after platinum-based chemotherapy.[5] CHECKMATE-227 [44] tested the combination of nivolumab and ipilimumab in patients with stage IV or recurrent NSCLC without previous treatment.[45] Patients with a PD-L1 expression level of 1% or more were randomized in a 1:1:1 ratio to receive nivolumab plus ipilimumab, nivolumab alone, or chemotherapy.[45][44] The chemotherapy used was cisplatin or carboplatin, combined with Gemcitabine for patient with squamous cell NSCLC, or pemetrexed for patients with nonsquamous disease.[44][45] The overall survival was 17.1, 15.7 and 14.9 months, respectively.[45][44] The patients who had a PD-L1 expression level of less than 1% were randomly assigned in a 1:1:1 ratio to receive nivolumab plus ipilimumab, nivolumab plus chemotherapy, or chemotherapy.[45] The OS was 17.2, 15.2 and 12.2 months, respectively[44]
Melanoma[edit]
PD-L1 is expressed in 40-50% of melanomas.[46] Phase I and II clinical trials have shown nivolumab as a promising and durable treatment option in melanoma as a single agent and in combination with ipilimumab.[13] Phase III trials are ongoing.[47]
In October 2022, the results of a Phase 3 trial, CheckMate -76K, showed that Opdivo reduced the risk of death by 58% as an adjuvant therapy in patients with completely resected stage two melanoma, the most serious type of skin cancer.[47][48]
Urothelial carcinoma[edit]
In February 2023, BMS reported that the three-year follow-up results from its phase 3 (CheckMate-274) trial of nivolumab showed significant sustained clinical benefits with nivolumab for the adjuvant treatment of patients with muscle-invasive urothelial carcinoma at a high risk of recurrence after radical resection.[49][50]
See also[edit]
- Nivolumab/relatlimab
References[edit]
- ^ a b c «Nivolumab (Opdivo) Use During Pregnancy». Drugs.com. 4 November 2019. Retrieved 11 March 2020.
- ^ a b «Nivolumab (Opdivo)». Cancer Research UK. Retrieved 15 December 2019.
- ^ «Prescription medicines: registration of new chemical entities in Australia, 2016». Therapeutic Goods Administration (TGA). 21 June 2022. Retrieved 10 April 2023.
- ^ «Opdivo 10 mg/mL concentrate for solution for infusion — Summary of Product Characteristics (SmPC)». (emc). 24 August 2020. Retrieved 2 October 2020.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad «Opdivo- nivolumab injection». DailyMed. 17 December 2019. Retrieved 11 March 2020.
- ^ a b c d «Opdivo EPAR». European Medicines Agency (EMA). 30 January 2020. Retrieved 11 March 2020.
- ^ a b c d e f g h «Nivolumab Monograph for Professionals». Drugs.com. Retrieved 14 November 2019.
- ^ a b c d e «FDA Approves First Immunotherapy for Initial Treatment of Gastric Cancer». U.S. Food and Drug Administration (FDA) (Press release). 16 April 2021. Retrieved 16 April 2021.
This article incorporates text from this source, which is in the public domain.
- ^ a b c «FDA approves nivolumab for resected esophageal or GEJ cancer». U.S. Food and Drug Administration. 20 May 2021. Retrieved 20 May 2021.
This article incorporates text from this source, which is in the public domain.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Rajan A, Kim C, Heery CR, Guha U, Gulley JL (September 2016). «Nivolumab, anti-programmed death-1 (PD-1) monoclonal antibody immunotherapy: Role in advanced cancers». Human Vaccines & Immunotherapeutics. 12 (9): 2219–31. doi:10.1080/21645515.2016.1175694. PMC 5027703. PMID 27135835.
- ^ a b c «FDA Approves Drug Combination for Treating Mesothelioma». U.S. Food and Drug Administration (FDA) (Press release). 2 October 2020. Retrieved 2 October 2020.
This article incorporates text from this source, which is in the public domain.
- ^ a b c d e f Johnson DB, Peng C, Sosman JA (March 2015). «Nivolumab in melanoma: latest evidence and clinical potential». Therapeutic Advances in Medical Oncology. 7 (2): 97–106. doi:10.1177/1758834014567469. PMC 4346215. PMID 25755682.
- ^ Sundar R, Cho BC, Brahmer JR, Soo RA (March 2015). «Nivolumab in NSCLC: latest evidence and clinical potential». Therapeutic Advances in Medical Oncology. 7 (2): 85–96. doi:10.1177/1758834014567470. PMC 4346216. PMID 25755681.
- ^ Bushey, R. Gains FDA Approval for Common Bladder Cancer. Drug Discovery & Development, Fri, 02/03/2017.
- ^ «FDA grants regular approval to nivolumab for adjuvant treatment of melanoma». U.S. Food and Drug Administration (FDA). 20 December 2017. Retrieved 2 October 2020.
This article incorporates text from this source, which is in the public domain.
- ^ «FDA approves nivolumab for adjuvant treatment of urothelial carcinoma». U.S. Food and Drug Administration (FDA). 20 August 2021. Retrieved 20 August 2021.
This article incorporates text from this source, which is in the public domain.
- ^ «FDA approves Opdivo». U.S. Food and Drug Administration (FDA). 31 May 2022. Retrieved 31 May 2022.
- ^ a b de Filette J, Andreescu CE, Cools F, Bravenboer B, Velkeniers B (March 2019). «A Systematic Review and Meta-Analysis of Endocrine-Related Adverse Events Associated with Immune Checkpoint Inhibitors». Hormone and Metabolic Research. 51 (3): 145–156. doi:10.1055/a-0843-3366. PMID 30861560.
- ^ a b c Pardoll DM (March 2012). «The blockade of immune checkpoints in cancer immunotherapy». Nature Reviews. Cancer. 12 (4): 252–64. doi:10.1038/nrc3239. PMC 4856023. PMID 22437870.
- ^ a b c d Syn NL, Teng MW, Mok TS, Soo RA (December 2017). «De-novo and acquired resistance to immune checkpoint targeting». The Lancet. Oncology. 18 (12): e731–e741. doi:10.1016/s1470-2045(17)30607-1. PMID 29208439.
- ^ WHO Drug Information, Vol. 26, No. 2, 2012. Proposed INN List 107
- ^ Wang C, Thudium KB, Han M, Wang XT, Huang H, Feingersh D, et al. (September 2014). «In vitro characterization of the anti-PD-1 antibody nivolumab, BMS-936558, and in vivo toxicology in non-human primates». Cancer Immunology Research. 2 (9): 846–56. doi:10.1158/2326-6066.CIR-14-0040. PMID 24872026.
- ^ Allison M (September 2009). «Bristol-Myers Squibb swallows last of antibody pioneers». Nature Biotechnology. 27 (9): 781–3. doi:10.1038/nbt0909-781. PMID 19741612. S2CID 205270797.
- ^ John Carroll for FierceBiotech 23 Jul 2009 Bristol-Myers to buy Medarex for $2.1B
- ^ a b c d Sharma P, Allison JP (April 2015). «The future of immune checkpoint therapy». Science. 348 (6230): 56–61. Bibcode:2015Sci…348…56S. doi:10.1126/science.aaa8172. PMID 25838373. S2CID 4608450.
- ^ A Pollack (June 2012). «Drug helps immune system fight cancer». New York Times.
- ^ John Carroll for FierceBiotech 7 Jul 2014 Anti-PD-1 cancer star nivolumab wins world’s first regulatory approval
- ^ «FDA approves Keytruda for advanced melanoma» (Press release). U.S. Food and Drug Administration (FDA). 4 September 2014. Archived from the original on 25 December 2015. Retrieved 24 December 2015.
- ^ «FDA approves Opdivo for advanced melanoma» (Press release). U.S. Food and Drug Administration (FDA). 22 December 2014. Archived from the original on 13 February 2017. Retrieved 16 December 2019.
- ^ «New treatment for advanced melanoma». European Medicines Agency (EMA) (Press release). 24 April 2015. Retrieved 11 March 2020.
- ^ «FDA expands approved use of Opdivo to treat lung cancer» (Press release). U.S. Food and Drug Administration (FDA). Archived from the original on 5 March 2015. Retrieved 4 March 2015.
- ^ «FDA approves Opdivo to treat advanced form of kidney cancer». U.S. Food and Drug Administration (FDA) (Press release). 23 November 2015. Archived from the original on 25 January 2018. Retrieved 2 October 2020.
- ^ «Nivolumab (Opdivo) for Hodgkin Lymphoma». U.S. Food and Drug Administration (FDA). 17 May 2016.
- ^ «FDA grants regular approval to nivolumab for adjuvant treatment of melanoma». U.S. Food and Drug Administration (FDA). 21 December 2017. Retrieved 12 April 2018.
- ^ «FDA approves nivolumab plus ipilimumab combination for intermediate or poor-risk advanced renal cell carcinoma». U.S. Food and Drug Administration (FDA). Retrieved 20 April 2018.
- ^ «Bristol-Myers’ Opdivo ushers in a new era as the first I-O therapy approved in China | FiercePharma». www.fiercepharma.com. 15 June 2018. Retrieved 19 June 2018.
- ^ Caponnetto S, Draghi A, Borch TH, Nuti M, Cortesi E, Svane IM, Donia M (May 2018). «Cancer immunotherapy in patients with brain metastases». Cancer Immunology, Immunotherapy. 67 (5): 703–711. doi:10.1007/s00262-018-2146-8. hdl:11573/1298742. PMID 29520474. S2CID 3782427.
- ^ Donia M, Pedersen M, Svane IM (April 2017). «Cancer immunotherapy in patients with preexisting autoimmune disorders». Seminars in Immunopathology. 39 (3): 333–337. doi:10.1007/s00281-016-0595-8. PMID 27730287. S2CID 3387103.
- ^ Goldkuhle, Marius; Dimaki, Maria; Gartlehner, Gerald; Monsef, Ina; Dahm, Philipp; Glossmann, Jan-Peter; Engert, Andreas; von Tresckow, Bastian; Skoetz, Nicole (12 July 2018). Cochrane Haematological Malignancies Group (ed.). «Nivolumab for adults with Hodgkin’s lymphoma (a rapid review using the software RobotReviewer)». Cochrane Database of Systematic Reviews. 2018 (7): CD012556. doi:10.1002/14651858.CD012556.pub2. PMC 6513229. PMID 30001476.
- ^ Loftus P, Rockoff JD, Steele A (5 August 2016). «Bristol Myers: Opdivo Failed to Meet Endpoint in Key Lung-Cancer Study». Wall Street Journal. ISSN 0099-9660. Retrieved 21 August 2016.
- ^ Erman M (24 January 2019). «Bristol-Myers has Opdivo lung cancer setback as sales beat estimates». Reuters. Retrieved 24 January 2019.
- ^ Waterhouse D, Horn L, Reynolds C, Spigel D, Chandler J, Mekhail T, Mohamed M, Creelan B, Blankstein KB, Nikolinakos P, McCleod MJ, Li A, Oukessou A, Agrawal S, Aanur N (April 2018). «Safety profile of nivolumab administered as 30-min infusion: analysis of data from CheckMate 153». Cancer Chemotherapy and Pharmacology. 81 (4): 679–686. doi:10.1007/s00280-018-3527-6. PMID 29442139. S2CID 3906670.
- ^ a b c d e Hellmann, Matthew D.; Paz-Ares, Luis; Caro, Reyes Bernabe; Zurawski, Bogdan; Kim, Sang-We; Costa, Enric Carcereny; Park, Keunchil; Alexandru, Aurelia; Lupinacci, Lorena; Jimenez, Emmanuel de la Mora; Sakai, Hiroshi (28 September 2019). «Nivolumab plus Ipilimumab in Advanced Non–Small-Cell Lung Cancer». New England Journal of Medicine. 381 (21): 2020–2031. doi:10.1056/NEJMoa1910231. PMID 31562796.
- ^ a b c d e Nasser, Nicola J.; Gorenberg, Miguel; Agbarya, Abed (November 2020). «First line Immunotherapy for Non-Small Cell Lung Cancer». Pharmaceuticals. 13 (11): 373. doi:10.3390/ph13110373. PMC 7695295. PMID 33171686.
- ^ Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, et al. (August 2002). «Tumor-associated B7-H1 promotes T-cell apoptosis: a potential mechanism of immune evasion». Nature Medicine. 8 (8): 793–800. doi:10.1038/nm730. PMID 12091876. S2CID 27694471.
- ^ a b «CA209-76K». EU Clinical Trials Register. Retrieved 20 October 2022.
- ^ «Bristol Myers Squibb Announces Adjuvant Treatment with Opdivo (nivolumab) Demonstrated Statistically Significant and Clinically Meaningful Improvement in Recurrence-Free Survival (RFS) in Patients with Stage IIB/C Melanoma in the CheckMate -76K Trial». news.bms.com. Retrieved 20 October 2022.
- ^ Bristol-Myers Squibb (9 January 2023). «A Phase 3 Randomized, Double-blind, Multi-center Study of Adjuvant Nivolumab Versus Placebo in Subjects With High Risk Invasive Urothelial Carcinoma (CheckMate 274: CHECKpoint Pathway and nivoluMAb Clinical Trial Evaluation 274)». Ono Pharmaceutical Co. Ltd.
- ^ «BMS reports positive three-year results for Opdivo to treat bladder cancer». PMLive. 21 February 2023. Retrieved 22 February 2023.
External links[edit]
- «Nivolumab». Drug Information Portal. U.S. National Library of Medicine.
- «Nivolumab». NCI Drug Dictionary. National Cancer Institute.
- «Nivolumab». National Cancer Institute. 7 January 2015.
- Clinical trial number NCT01721746 for «A Study to Compare BMS-936558 to the Physician’s Choice of Either Dacarbazine or Carboplatin and Paclitaxel in Advanced Melanoma Patients That Have Progressed Following Anti-CTLA-4 Therapy (CheckMate 037)» at ClinicalTrials.gov
- Clinical trial number NCT01721772 for «Study of Nivolumab (BMS-936558) Compared With Dacarbazine in Untreated, Unresectable, or Metastatic Melanoma (CheckMate 066)» at ClinicalTrials.gov
- Clinical trial number NCT01844505 for «Phase 3 Study of Nivolumab or Nivolumab Plus Ipilimumab Versus Ipilimumab Alone in Previously Untreated Advanced Melanoma (CheckMate 067)» at ClinicalTrials.gov
- Clinical trial number NCT02388906 for «Efficacy Study of Nivolumab Compared to Ipilimumab in Prevention of Recurrence of Melanoma After Complete Resection of Stage IIIb/c or Stage IV Melanoma (CheckMate 238)» at ClinicalTrials.gov
- Clinical trial number NCT02477826 for «An Investigational Immuno-therapy Trial of Nivolumab, or Nivolumab Plus Ipilimumab, or Nivolumab Plus Platinum-doublet Chemotherapy, Compared to Platinum Doublet Chemotherapy in Patients With Stage IV Non-Small Cell Lung Cancer (NSCLC) (CheckMate 227)» at ClinicalTrials.gov
- Clinical trial number NCT03215706 for «A Study of Nivolumab and Ipilimumab Combined With Chemotherapy Compared to Chemotherapy Alone in First Line NSCLC (CheckMate 9LA)» at ClinicalTrials.gov
- Clinical trial number NCT01642004 for «Study of BMS-936558 (Nivolumab) Compared to Docetaxel in Previously Treated Advanced or Metastatic Squamous Cell Non-small Cell Lung Cancer (NSCLC) (CheckMate 017)» at ClinicalTrials.gov
- Clinical trial number NCT01673867 for «Study of BMS-936558 (Nivolumab) Compared to Docetaxel in Previously Treated Metastatic Non-squamous NSCLC (CheckMate057)» at ClinicalTrials.gov
- Clinical trial number NCT02899299 for «Study of Nivolumab Combined With Ipilimumab Versus Pemetrexed and Cisplatin or Carboplatin as First Line Therapy in Unresectable Pleural Mesothelioma Patients (CheckMate743)» at ClinicalTrials.gov
- Clinical trial number NCT02231749 for «Nivolumab Combined With Ipilimumab Versus Sunitinib in Previously Untreated Advanced or Metastatic Renal Cell Carcinoma (CheckMate 214)» at ClinicalTrials.gov
- Clinical trial number NCT03141177 for «A Study of Nivolumab Combined With Cabozantinib Compared to Sunitinib in Previously Untreated Advanced or Metastatic Renal Cell Carcinoma (CheckMate 9ER)» at ClinicalTrials.gov
- Clinical trial number NCT01668784 for «Study of Nivolumab (BMS-936558) vs. Everolimus in Pre-Treated Advanced or Metastatic Clear-cell Renal Cell Carcinoma (CheckMate 025)» at ClinicalTrials.gov
- Clinical trial number NCT02181738 for «Study of Nivolumab in Patients With Classical Hodgkin’s Lymphoma (Registrational) (CheckMate 205)» at ClinicalTrials.gov
- Clinical trial number NCT01592370 for «An Investigational Immuno-Therapy Study to Determine the Safety and Effectiveness of Nivolumab and Daratumumab in Patients With Multiple Myeloma» at ClinicalTrials.gov
- Clinical trial number NCT02105636 for «Trial of Nivolumab vs Therapy of Investigator’s Choice in Recurrent or Metastatic Head and Neck Carcinoma (CheckMate 141)» at ClinicalTrials.gov
- Clinical trial number NCT02387996 for «A Study of Nivolumab in Participants With Metastatic or Unresectable Bladder Cancer» at ClinicalTrials.gov
- Clinical trial number NCT02060188 for «An Investigational Immuno-therapy Study of Nivolumab, and Nivolumab in Combination With Other Anti-cancer Drugs, in Colon Cancer That Has Come Back or Has Spread (CheckMate142)» at ClinicalTrials.gov
- Clinical trial number NCT01658878 for «An Immuno-therapy Study to Evaluate the Effectiveness, Safety and Tolerability of Nivolumab or Nivolumab in Combination With Other Agents in Patients With Advanced Liver Cancer (CheckMate040)» at ClinicalTrials.gov
- Clinical trial number NCT02743494 for «An Investigational Immuno-therapy Study of Nivolumab or Placebo in Participants With Resected Esophageal or Gastroesophageal Junction Cancer (CheckMate 577)» at ClinicalTrials.gov
- Clinical trial number NCT02569242 for «Study of Nivolumab in Unresectable Advanced or Recurrent Esophageal Cancer» at ClinicalTrials.gov
- Clinical trial number NCT02872116 for «Efficacy Study of Nivolumab Plus Ipilimumab or Nivolumab Plus Chemotherapy Against Chemotherapy in Stomach Cancer or Stomach/Esophagus Junction Cancer (CheckMate649)» at ClinicalTrials.gov
- Clinical trial number NCT02632409 for «An Investigational Immuno-therapy Study of Nivolumab, Compared to Placebo, in Patients With Bladder or Upper Urinary Tract Cancer, Following Surgery to Remove the Cancer (CheckMate 274)» at ClinicalTrials.gov