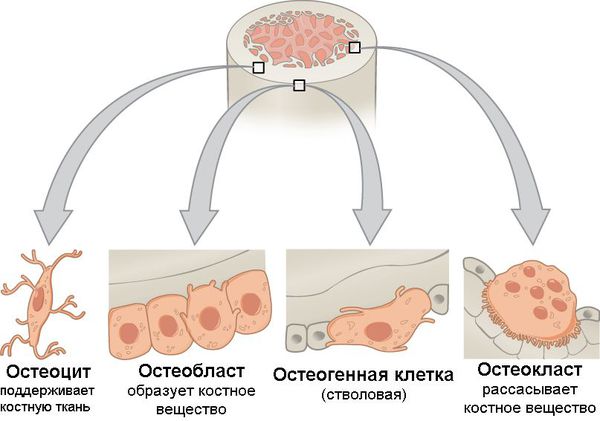
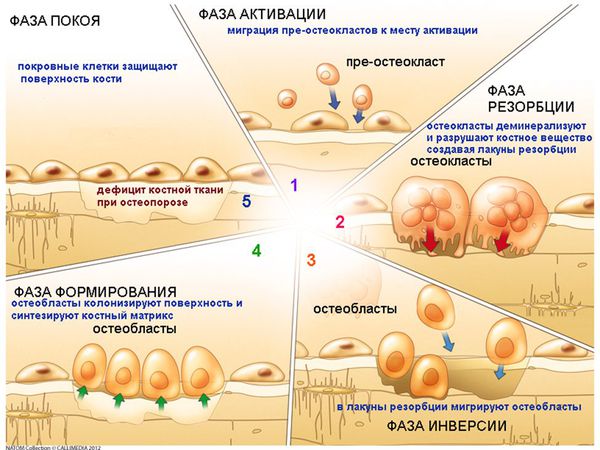
Остеопороз
Версия: Клинические рекомендации РФ 2021 (Россия)
Категории МКБ:
Другие остеопорозы (M81.8), Постменопаузный остеопороз (M81.0)
Разделы медицины:
Ревматология
Общая информация
Краткое описание
Общественная организация «Российская ассоциация эндокринологов»
Общественная организация «Российская ассоциация по остеопорозу»
Общероссийская Общественная Организация «Ассоциация ревматологов России»
Общероссийская Общественная Организация «Ассоциация травматологов-ортопедов России»
Межрегиональная общественная организация «Ассоциация гинекологов-эндокринологов»
Общероссийская Общественная Организация «Российская ассоциация геронтологов и гериатров»
Клинические рекомендации
Остеопороз
Возрастная группа: взрослые
Определение заболевания или состояния (группы заболеваний или состояний)
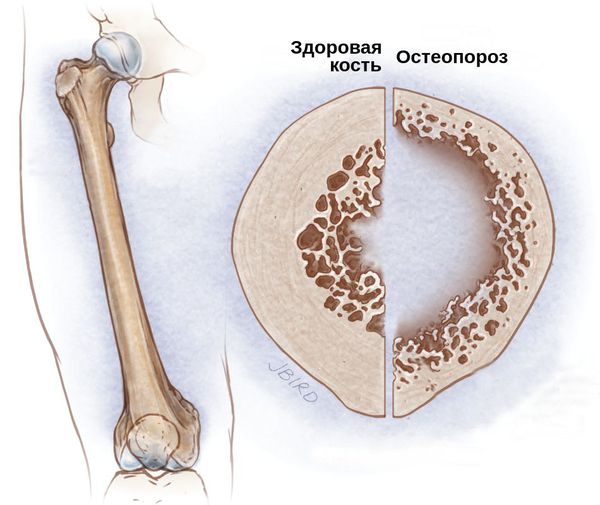
Остеопороз – метаболическое заболевание скелета, характеризующееся снижением костной массы, нарушением микроархитектоники костной ткани и, как следствие, переломами при минимальной травме [6, 7].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
M81.0 — Постменопаузный остеопороз.
M81.8 – Другие остеопорозы.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Первичный остеопороз развивается как самостоятельное заболевание без выявленной другой причины снижения прочности скелета, занимает 95% в структуре остеопороза у женщин в постменопаузе (постменопаузальный остеопороз) и 80% в структуре остеопороза у мужчин старше 50 лет [1-3, 16]. К первичному остеопорозу также относится идиопатический остеопороз, который развивается у женщин до менопаузы, мужчин до 50 лет и ювенильный остеопороз, который диагностируется у детей (до 18 лет). Идиопатические и ювенильные формы первичного остеопороза крайне редки.
Вторичный остеопороз развивается вследствие различных заболеваний или состояний, а также приема лекарственных средств, то есть имеется конкретная причина, приводящая к остеопорозу (Таблица 1). В структуре остеопороза вторичный остеопороз занимает 5% у женщин и 20% у мужчин [16].
Таблица 1. Состояния, заболевания и препараты, способные приводить к развитию вторичного остеопороза [1,2,16]
*Несовершенный остеогенез, гиперпаратиреоз, гипофосфатазия относятся к метаболическим заболеваниям с преимущественным поражением скелета и поэтому они могут рассматриваться как самостоятельные заболевания.
Возможно развитие смешанного характера остеопороза. Например, при приеме глюкокортикоидов у женщин в постменопаузе вследствие серьезного соматического заболевания, которое само по себе может приводить к развитию вторичного остеопороза. В данном случае очень сложно выделить первопричину снижения прочности костей скелета.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Остеопороз является полиэтиологическим заболеванием, развитие которого зависит от генетической предрасположенности, образа жизни, физической активности, эндокринологического статуса, наличия сопутствующих заболеваний, приема лекарственных препаратов, старения человека и индивидуальной продолжительности жизни [1-3]. Набор массы костной ткани происходит в детском и подростковом возрасте, достигая максимума к 20-30 годам. После достижения пика до 35-40 лет костная масса остается практически неизменной, после чего начинает постепенно уменьшаться. У женщин темпы снижения МПК значительно выше, чем у мужчин, что обусловлено дефицитом эстрогенов в период пери- и постменопаузы.
Костная ткань находится в состоянии постоянного изменения. Одновременно происходят два противоположных процесса: костеобразование и костная резорбция, от баланса которых зависит МПК, качество и прочность кости. В условиях дефицита эстрогенов данный баланс смещается в сторону потери костной массы. Однако дефицит эстрогенов не является единственной причиной потери МПК, как считали раньше. Ремоделирование костной ткани зависит от состояния фосфорно-кальциевого обмена, паратиреоидного гормона, витамина D, гормона роста, кальцитонина, тиреодных гормонов, глюкокортикоидов, старения и ассоциированного с ним секреторного фенотипа и т.д. В целом, все эффекты на состояние метаболизма костной ткани реализуются через основные регуляторные системы остеобластогенеза (канонический wnt-сигнальный путь) и остеокластогенеза (RANKL/RANK/OPG). Изменения экспрессии молекул-регуляторов остеобластогенеза и остеокластогенеза с возрастом и вследствие негативного влияния других факторов приводят к снижению прочности кости, что может проявляться нарушением внутренней микроархитектоники, снижением костной массы, МПК и, как следствие, переломами при минимальной травме [2]. Так, патологические переломы на фоне остеопороза могут возникнуть при падении с высоты собственного роста, неловком движении, кашле, чихании и вообще без видимого травматического вмешательства.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
В России среди лиц в возрасте 50 лет и старше остеопороз выявляется у 34% женщин и 27% мужчин, а частота остеопении составляет 43% и 44%, соответственно. Частота остеопороза увеличивается с возрастом [8]. В целом, остеопорозом страдают около 14 млн. человек и еще 20 млн. людей имеют снижение МПК, соответствующее остеопении [9]. Аналогичные показатели распространенности остеопороза у женщин отмечены среди белого населения Северной Америки и ряда стран Западной Европы [2, 3].
Социальная значимость остеопороза определяется его последствиями – переломами тел позвонков и костей периферического скелета, приводя к большим материальным затратам в области здравоохранения и обусловливающими высокий уровень нетрудоспособности, включая инвалидность и смертность.
Наиболее типичными переломами вследствие остеопороза считаются переломы проксимального отдела бедренной кости, лучевой кости и переломы тел позвонков, но также распространены переломы других крупных костей скелета (таза, ребер, грудины, голени, плечевой кости и т.д.) [10]. Одномоментное эпидемиологическое исследование среди городского населения России показало, что 24% женщин и 13% мужчин в возрасте 50 лет и старше ранее уже имели, по крайней мере, один патологический перелом, при этом наиболее распространены переломы тел позвонков [11]. Распространенность патологических переломов тел позвонков составляет около 10% у мужчин и 12,7% у женщин [9]. Частота переломов шейки бедренной кости, по данным эпидемиологического исследования, проведенного в 16 городах России (общая численность населения в возрасте 50 лет и старше составила 1 749 274 человек) в 1992-1997гг, составила 100,9/100 000 населения, при этом достоверно чаще эти переломы зафиксированы среди женщин (115,5/100000) по сравнению с мужчинами (77,0/100000), р <0,0001 [8]. Частота переломов была наиболее низкой у лиц обоего пола в возрасте 50-54 года и увеличивалась плавно до возраста 65 лет, а затем был отмечен ее экспоненциальный рост, особенно выраженный у женщин. За пятилетний период регистрации переломов отмечалось увеличение частоты переломов бедренной кости как у женщин, так и мужчин [8]. Аналогичное исследование было проведено через 11 лет (2008-2009гг.) в четырех городах России. Оно показало, что частота переломов проксимального отдела бедренной кости уже составляет 239 случаев на 100 000 населения (276 и 175 случаев у женщин и мужчин, соответственно). При этом у мужчин в возрасте 50-64 года она была в 2 раза выше, чем у женщин, а в возрасте 75 лет и старше эта тенденция была диаметрально противоположной [11].
Показатели смертности в течение первого года после перелома бедренной кости составляют от 12 до 40%, причем данный показатель выше у мужчин [10]. Особенно высока летальность в течение первых 6 месяцев после перелома, которая на 5-20% выше по сравнению с этим показателем у лиц того же возраста без переломов, а в некоторых городах России летальность в 8 раз превышала общегородские показатели смертности у лиц того же возраста [12]. У пациентов, перенесших патологические переломы, достоверно снижается качество жизни, которое лишь частично восстанавливается в среднем через 12-24 месяца в зависимости от локализации перелома [12]. Так, среди лиц, выживших после перелома бедренной кости, каждый третий утрачивает способность к самообслуживанию и нуждается в длительном постоянном уходе. Восстановление качества жизни у выживших пациентов, перенесших перелом проксимального отдела бедренной кости, происходит в среднем через 2 года и зависит от того, было ли проведено оперативное лечение.
Перелом дистального отдела предплечья – один из наиболее распространенных переломов при падении с высоты собственного роста. По данным эпидемиологического исследования в России частота его составляла 426/100000 населения, превышая частоту перелома бедренной кости в 3-7 раз у мужчин и 4-8 раз у женщин и достоверно превалируя у женщин.
При этом за пятилетний период отмечалось достоверное увеличение частоты переломов любой локализации, особенно у пациентов, которые уже перенесли перелом [8].
Усредненная стоимость 1 года лечения остеопороза, осложненного переломом, составляла 61151 рублей, при этом наиболее дорогостоящим является лечение пациентов с переломом проксимального отдела бедренной кости, а наименее затратным – при переломе дистального отдела предплечья [13]. С учетом эпидемиологических данных о частоте патологических переломов пересчет на население России в возрасте 50 лет и старше показал, что только прямые медицинские затраты на лечение патологических переломов пяти основных локализаций за один год могут достигать около 25 млрд. рублей, при этом затраты на лечение пациентов с переломами тел позвонков, которые в популяции встречаются примерно у 10% населения в возрасте 50 лет и старше, почти в два раза превышают стоимость лечения пациентов с переломом бедренной кости в масштабах страны [13].
Сравнительное исследование социальных и экономических последствий перелома шейки бедренной кости и инфаркта миокарда [14] показало, что при одинаковых затратах на лечение этих двух заболеваний пациенты с переломом имеют существенно более низкое качество жизни, обусловленное, в первую очередь, отсутствием оперативного лечения или плохой реабилитацией, и, как следствие – хроническим болевым синдромом и двигательными нарушениями.
С учетом прогнозируемого роста продолжительности жизни в России в ближайшие годы будет наблюдаться рост случаев патологических переломов. Так, например, к 2035 году у мужчин число случаев перелома проксимального отдела бедренной кости вырастет на 36%, у женщин – на 43% [15].
Таким образом, высокая и постоянно растущая распространенность остеопороза, значительная стоимость лечения как самого заболевания, так и его прямых осложнений – переломов, развитие болевого синдрома, деформаций и потери трудоспособности и способности к самообслуживанию, определяют важность данной проблемы для здравоохранения Российской Федерации.
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Остеопороз до развития патологического перелома не имеет клинических проявлений. В отличие от остеопороза, патологический перелом в остром периоде часто имеет яркую клиническую картину. Перелом сопряжен с болью, нарушением функции, и диагностируется рентгенологически врачом-травматологом, который в зависимости от характера предшествующей травмы может заподозрить остеопороз.
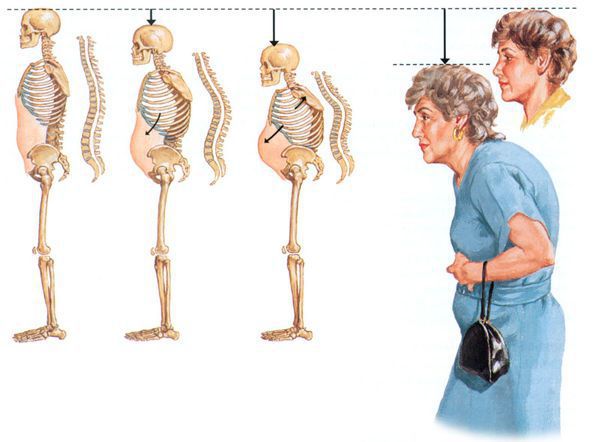
Отдельного внимания заслуживают клинические проявления патологических переломов тел позвонков, которые длительно могут оставаться не диагностированными. Компрессионные переломы тел позвонков сопровождаются болью или чувством усталости в спине, снижением роста, а также в случае развития множественных компрессионных деформаций целым рядом клинических проявлений, представленных на Рисунке 1.
Рисунок 1. Клинические проявления множественных компрессионных деформаций тел позвонков
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза остеопороз:
1. Наличие патологических переломов крупных костей скелета (бедренной кости, тел(а) позвонков(а), множественных переломов) в анамнезе или, выявленных при обследовании, независимо от результатов рентгеноденситометрии или FRAX (при условии исключения других заболеваний скелета).
2. Наличие высокой индивидуальной 10-летней вероятности основных патологических переломов (результат оценки FRAX соответствует Российскому порогу вмешательства и/или превышает его) независимо от показателя рентгеноденситометрии.
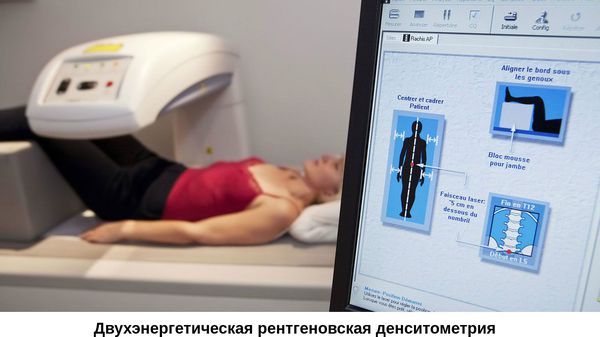
3. Снижение МПК на 2,5 и более стандартных отклонений (SD) по Т-критерию в шейке бедренной кости и/или в целом в проксимальном отделе бедренной кости и/или в поясничных позвонках (L1-L4, L2-L4), измеренной двухэнергетической рентгеноденситометрией (DXA), у женщин в постменопаузе и мужчин старше 50 лет.
Жалобы и анамнез
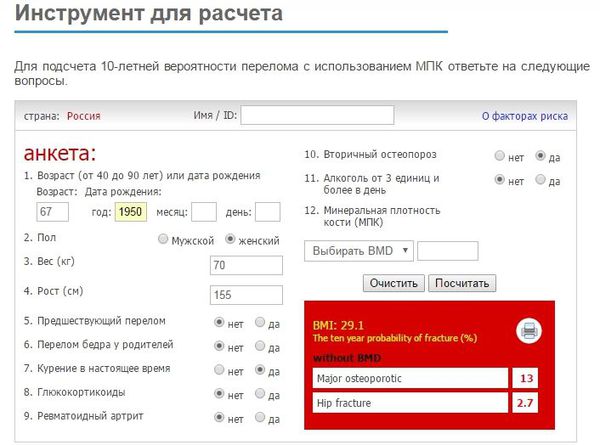
До развития патологического перелома остеопороз не имеет клинических проявлений. В связи с этим, на этапе сбора жалоб и анамнеза, в первую очередь, необходимо оценить индивидуальную 10-летнюю вероятность патологического перелома с использованием алгоритма FRAX (fracture risk assessment tool).
- Скрининг для выявления групп с высокой вероятностью переломов рекомендован с использованием алгоритма FRAX среди всех женщин в постменопаузе и мужчин старше 50 лет [15, 17-24].
Уровень убедительности рекомендации А (уровень достоверности доказательств 1)
Комментарии: Ввиду высокой распространенности остеопороза и патологических переломов в старших возрастных группах [1-3], тяжелых инвалидизирующих последствиях патологических переломов, высокими затратами на лечение перелома и последующую реабилитацию [9-13] оправдано проводить скрининг для выявления пациентов с высоким риском переломов среди всего населения старше 50 лет. Для подтверждения эффективности алгоритма FRAX в качестве инструмента скрининга было проведено рандомизированное контролируемое исследование с включением когорты 11580 женщин в постменопаузе, проживающих самостоятельно. Пациенты были рандомизированы на тех пациентов, среди кого проводился скрининг с использованием алгоритма FRAX (n=6233) и в группе высокого риска назначалась терапии и тех, кто традиционно наблюдался у своего лечащего врача (n=6250). Наблюдение за включенными когортами в течение 5 лет покзало, что активный скрининг с применением алгоритма FRAX позволяет сократить частоту переломов бедра на 28% (ОР 0,72-0,89) p=0,0002 по сравнению с традиционным наблюдением [17].
Факторы риска для основных патологических переломов и для перелома бедренной кости, включенные в алгоритм FRAX, были выявлены по результатам 12 проспективных когортных исследований во многих географических регионах с использованием первичных баз данных [6,25], что определяет высокую степень доказательности применения алгоритма. Наблюдение составило приблизительно 250 000 пациентов-лет среди 60 000 мужчин и женщин, в ходе которых было зарегистрировано более 5000 переломов [25]. Каждый включенный в алгоритм FRAX фактор риска повышает вероятность переломов независимо от МПК, но может быть совмещен с измерением МПК у индивидуального пациента [3,6,25]. Ключевые факторы риска патологических переломов, доказавшие свой независимый вклад, сведены в Приложении Г1.
В настоящее время, нет рандомизированного исследования использования инструмента скрининга у мужчин. Однако риск переломов, как и лечение остеопороза у мужчин определяется также, как и у женщин, на основании исследований, подтверждающих эффективность по суррогатному критерию. Валидизация алгоритма FRAX у мужчин осуществлялась в частности в проспективном исследовании СaMos [21]. Средняя предсказанная вероятность переломов с включением МПК у мужчин для основных патологических переломов не отличалась значимо от полученной в ходе исследования (предсказанная 5.4%, полученная 6.4% (95% ДИ 5.2-7.5%). Схожие результаты были получены в большом Канадском исследовании в провинции Манитоба [22], в Великобритании [19] и Норвегии [20]. Таким образом, алгоритм FRAX откалиброванный на основании национальных исследований переломов бедра предсказывает риск сопоставимый с частотой переломов при учете различных групп риска. При калибровании алгоритма FRAX учитываются данные перелома бедра у мужчин и женщин, а также частота летальных исходов в стране, поэтому любая страна при калибровке алгоритма включает мужчин и женщин.
В ходе опроса с использованием алгоритма FRAX наряду с другими факторами риска врач уточняет наличие перелома в анамнезе. При положительном ответе на этот вопрос необходимо уточнить локализацию перелома и характер травмы [6].
- При наличии патологических переломов крупных костей скелета (бедренной кости, тел(а) позвонков(а), множественных переломов) в анамнезе рекомендовано устанавливать диагноз остеопороза и назначать лечение независимо от результатов рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости или FRAX (при условии исключения других заболеваний скелета) [2,3,6,26-37].
Уровень убедительности рекомендации B (уровень достоверности доказательств 2)
Комментарии: Патологический перелом является ключевым осложнением остеопороза, который объединяет снижение костной массы и нарушение микроархитектоники, в то время как рентгеновская денситометрия отражает только снижение МПК и является одним из факторов риска переломов. Независимо от МПК, возраста и других клинических факторов риска, рентгенологически подтвержденные переломы тел позвонков (даже если они совершенно бессимптомны), переломы бедренной кости и других крупных костей скелета являются признаком изменения структуры и снижения прочности кости, и значимым предиктором новых переломов тел позвонков и других костей скелета [3,9,26-28], поэтому наличие перелома при минимальной травме достаточно для установления диагноза «остеопороз» и назначения лечения в международных клинических рекомендациях по остеопорозу [2,3,6]. Назначение препаратов для лечения остеопороза во многих исследованиях было основано на данных о снижении МПК. Многие исследования, в том числе мета-анализы, показали, что противопереломная эффективность у лиц с предшествующими переломами не зависит от исходной МПК [29-34]. Однако необходимым условием установки диагноза «остеопороз» является исключение других метаболических заболеваний скелета [2].
Физикальное обследование
- Всем пациентам (женщины в постменопаузе и мужчины старше 50 лет) рекомендуется проводить физикальное обследование, включающее измерение роста, оценку формы грудной клетки и осанки, наличия складок кожи на задней поверхности спины для выявления клинических признаков компрессионных переломов тел позвонков [1-3].
Уровень убедительности рекомендации C (уровень достоверности доказательств 5)
Комментарии: При фиксации результатов роста необходимо уточнить максимальный рост в молодом возрасте (25 лет) и/или при последнем предыдущем измерении роста. При снижении роста на 2 см и более за 1-3 года или на 4 см и более за жизнь необходимо заподозрить компрессионный(ые) перелом(ы) тела позвонка.
Наличие складок кожи на спине и боках (симптом «лишней кожи»), уменьшение расстояния между реберными дугами и гребнями подвздошных костей меньше ширины 2 пальцев являются физикальными признаками компрессионных переломов тел позвонков. Эти физикальные признаки не отличаются у мужчин и женщин
При измерении роста следует обратить внимание на невозможность полностью распрямиться, появление расстояния от стены до затылка, что является симптомом компрессионных переломов тел позвонков.
Характерная кифотическая деформация грудной клетки, относительное увеличение живота в объеме («выпячивание» передней брюшной стенки), относительное удлинение конечностей и укорочение грудной клетки представлены на рисунке 1 и являются симптомами множественных компрессионных деформаций тел позвонков.
Кроме того, при физикальном обследовании следует обращать внимание на наличие симптомов заболеваний, приводящих к вторичному остеопорозу (Табл. 1), которые достаточно специфичны для каждой патологии.
Лабораторные диагностические исследования
- Исследование уровня биохимических параметров крови: исследование уровня общего кальция в крови, исследование уровня креатинина в крови (с подсчетом скорости клубочковой фильтрации (СКФ)), исследование уровня неорганического фосфора в крови, определение активности щелочной фосфатазы в крови, исследование уровня глюкозы в крови рекомендуется проводить всем пациентам с впервые установленным диагнозом остеопороз, а также при неэффективности ранее назначенной терапии с целью дифференциальной диагностики с другими причинами повышенной хрупкости скелета [38-43].
Уровень убедительности рекомендации С (уровень достоверности доказательств 4)
Комментарии: Результаты лабораторного исследования позволяют установить другую причину повышенной хрупкости скелета и уточнить противопоказания к назначению той или иной терапии (например, гипокальциемия является противопоказанием к назначению БФ и деносумаба**, гиперкальциемия и повышение щелочной фосфатазы являются противопоказанием для назначения терипаратида** и т.д.). Когортные исследования показывают, что до 15-30% пациентов могут иметь другие заболевания, приводящие к остеопорозу или усугубляющие его течение [40-42]. Лабораторные исследования следует повторять при неэффективности терапии ввиду возможности развития сочетанных заболеваний или дефицита витамина D, как причины недостаточного ответа на лечение [2,43].
Общие и более специфические лабораторные методы для дифференциальной диагностики остеопороза и других метаболических заболеваний скелета сведены в Приложении А3.2. [1-3,16]. Например, выявление синдрома гиперкальциемии предполагает целый ряд обследований для уточнения причины этого состояния. Наиболее часто диагностируется гиперпаратиреоз, но синдром гиперкальциемии может наблюдаться и при тиреотоксикозе, множественной миеломе, болезни Педжета, метастатическом поражении скелета и т.д.
- Общий (клинический) анализ крови рекомендуется проводить всем пациентам с впервые установленным диагнозом остеопороз, а также при неэффективности ранее назначенной терапии с целью дифференциальной диагностики с другими причинами повышенной хрупкости скелета [38-42].
Уровень убедительности рекомендации С (уровень достоверности доказательств 4)
Комментарии: При первичном остеопорозе общий (клинический) анализ крови не имеет специфических изменений. Выявление анемии и повышенного СОЭ позволяет заподозрить другие заболевания, приводящие к снижению прочности скелета или причину вторичного остеопороза (Табл. 1 и Приложение А3.2).
- Рекомендуется определение С-концевого телопептида в крови, и/или исследование уровня N-терминального пропептида проколлагена 1-го типа (P1NP) в крови (маркера резорбции при назначении антирезорбтивной терапии и костеобразования при назначении анаболической терапии, соответственно) пациентам, получающим лечение остеопороза самостоятельно, исходно и через 3 месяца от начала терапии с целью ранней оценки эффективности лечения и приверженности к терапии. Достаточно оценивать один маркер, но в одной и той же лаборатории [44-51].
Уровень убедительности рекомендации А (уровень достоверности доказательств 2)
Комментарии: Костное ремоделирование происходит в течение всей жизни человека с целью адаптации костной ткани, репарации повреждений, а также для поддержания минерального гомеостаза. Основные биохимические маркеры костного ремоделирования, которые наиболее оправдано определять в клинической практике, сведены в Таблице 2.
Таблица 2. Биохимические маркеры костного ремоделирования
Примечание: * N-терминальный пропептид проколлагена 1 типа и С-концевой телопептид коллагена 1 типа считаются наиболее стабильными, с хорошей воспроизводимостью и рекомендуются для определения большинству пациентов [48-50].
До 50% случаев неэффективности терапии обусловлено недостаточной приверженностью пациентов, что включает в себя не только отказ от приема препарата, но и не соблюдение режима и правил приема таблетированных бифосфонатов (БФ) или ежедневных инъекций терипаратида**. Снижение маркеров костной резорбции у пациентов, получающих БФ, коррелировало с прибавкой МПК и в ряде случае независимо определяло снижение риска переломов [52-56]. Также повышение P1NP в ответ на терапию терипаратидом** является предиктором прироста МПК [57]. Исследование маркеров в ходе терапии позволяет отследить приверженности к лечению. Мета-анализ 171063 пациентов, которые наблюдались в течение 1-2,5 лет показал 46% снижение риска переломов у пациентов с хорошей комплаентностью по сравнению с теми, кто не в полной мере выполнял рекомендацию врача [58]. Оправдано исследовать уровень маркеров костного ремоделирования исходно и затем через 3 месяца терапии, ожидая как минимум 30% изменение [59]. Неадекватный ответ маркеров костного ремоделирования является ранним сигналом о необходимости дополнительного обучения или смены терапии. В условиях отсутствия возможности проведения рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости маркеры костного ремоделирования могут служить суррогатным критерием эффективности терапии. Ввиду биологической вариабильности оптимально исследовать маркеры костного ремоделирования в одно и тоже время на одинаковом анализаторе, используя наборы одного и того же производителя [60]. Необходимо отметить, что маркеры костного ремоделирования, в том числе костеобразования, повышаются после перелома и их повышение может сохраняться до 6 месяцев, при этом может не наблюдаться их дальнейшего повышения при терапии анаболическим агентом.
- Определение С-концевого телопептида коллагена в крови и/или исследование уровня N-терминального пропептида проколлагена 1-го типа (P1NP) в крови в верхней четверти референсного интервала рекомендуется оценивать как дополнительный фактор риска для инициации терапии остеопороза у женщин в постменопаузе с остеопенией [50, 61-66].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 2)
Комментарии: Имеются убедительные доказательства, что высокие показатели маркеров костного ремоделирования предсказывают более быструю потерю костной ткани [61-64, 67], хотя не существует точки вмешательства для индивидуального пациента. Фармакоэкономическое исследование с применением модели Маркова показало, что лечение алендроновой кислотой** у женщин с остеопенией с уровнем маркеров костного ремоделирования в верхней четверти референтного интервала экономически эффективно [66]. Некоторые специалисты считают обоснованным использовать маркеры для мониторинга состояния пациента после отмены терапии. Хотя наблюдение пациентов после отмены алендроновой кислоты**, ризедроновой кислоты и золедроновой кислоты** не выявило зависимости между повышением маркеров ремоделирования и повышением риска переломов [68-70], мониторинг маркеров костного ремоделирования после отмены терапии дает представление о присутствии терапевтического агента в костной ткани, механизме его действия. Необходимо отметить, что ни одно из исследований отмены препарата не обладало достаточной статистической мощностью, чтобы выявить связь между повышением маркеров костного ремоделирования и риском переломов.
- Не рекомендуется использовать маркеры костного ремоделирования для прогнозирования риска переломов у индивидуального пациента, а также выбора типа терапии (антирезорбтивной или анаболической) [71-73].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: На сегодняшний день, не существует отработанной точки вмешательства для одного лабораторного набора и/или одного маркера костного ремоделирования для определения риска перелома у женщин в постменопаузе, хотя известно, что уровень маркеров костного ремоделирования повышается в постменопаузе, и это отражает потерю костной массы [61-65]. По результатам исследований не было выявлено зависимости между уровнем маркеров костного ремоделирования исходно и степенью эффективности алендроновой кислоты** для предупреждения переломов или прибавки МПК [71]. Близкий результат был получен в исследовании ризедроновой кислоты [72]. Эффективность препаратов не определяется исходным уровнем маркеров. Например, при глюкокортикоидном остеопорозе (ГКО), несмотря на снижение маркеров костеобразования, лечение БФ является эффективным для предупреждения переломов; при постменопаузальном остеопорозе, особенно после перелома, уровень маркеров может быть повышен, тем не менее терипаратид** эффективен для предупреждения новых переломов. Таким образом, маркеры костного метаболизма являются только дополнительным фактором риска при принятии решения о терапии и не могут влиять на выбор терапии по механизму действия. Практическим специалистам не рекомендуется устанавливать первичный диагноз остеопороза на основании любых лабораторных исследований [2,3]. Первичный остеопороз диагностируется только на основании патологического перелома, снижения МПК или совокупности факторов риска [2,3,6]. На основании лабораторных обследований исключаются другие метаболические заболевания скелета, приводящие к симптомокомплексу повышенной хрупкости скелета и потери МПК, то есть лабораторные исследования проводятся с целью дифференциального диагноза. При нормальных результатах первых тестов, более детальное исследование, как правило, не требуется, и повторный диагностический поиск проводится в случае появления новых симптомов или неэффективности лечения.
Инструментальные диагностические исследования
Наличие единственного перелома тела позвонка повышает риск последующих переломов позвонков в 3-5 раз, а риск переломов бедренной кости и другой локализации в 2-3 раза [29]. Выявление компрессионного перелома тела позвонка является показанием к медикаментозному лечению остеопороза с целью уменьшения риска последующих переломов [74].
- Рекомендовано проведение стандартной рентгенографии позвоночника грудного и поясничного отделов (Th4-L5) в боковой проекции для выявления компрессионных переломов тел позвонков у следующих категорий пациентов:
— с болевым синдромом в спине [75];
— пациентам с длительно некомпенсированным сахарным диабетом (СД) 2 типа или на инсулинотерапии [76];
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 3)
— снижением роста на 4 см в течение жизни или на 2 см при регулярном медицинском контроле [77];
— принимающим глюкокортикоиды [78];
— c диагностированными переломами другой локализации [29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 4)
Комментарии: Компрессионные переломы тел позвонков могут протекать без выраженного болевого синдрома. Кроме того, клинические проявления перелома неспецифичны и могут быть расценены как другая причина боли в спине. Вместе с тем, до 20% пациентов, испытавших патологический перелом тела позвонка, перенесут второй перелом уже в течение следующего года [71, 72]. Поэтому необходимо активное выявление компрессионных переломов тел позвонков с направлением на исследование пациентов, у которых вероятность наличия перелома высока. Клинические симптомы компрессионных переломов тел позвонков описаны в разделе физикального обследования. Применение глюкокортикоидов более 3-х месяцев и длительно некомпенсированный СД 2 типа являются наиболее значимыми факторами риска развития компрессионных переломов тел позвонков [37, 76, 79], поэтому пациенты с вышеуказанными состояниями должны быть активно обследованы. После проведения первого исследования, динамический контроль необходимо проводить лишь в случаях документально подтвержденного проспективного снижения роста или при возникновении/возобновлении боли в спине или изменения осанки [37, 80-83]. Повторное рентгенологическое исследование позвоночника также рекомендовано у пациентов при принятии решения об отмене медикаментозного лечения остеопороза, так как у пациентов со свежими переломами тел позвонков прекращение приема препаратов нежелательно.
Изменённые позвонки часто чередуются с малоизменёнными или неизменёнными позвонками (симптом «клавиш») или располагаются среди тел позвонков с близкими по значению линейными размерами их передних краёв (симптом «выравнивания») [1, 84]. При первичном остеопорозе никогда не наблюдается деструктивных изменений, внутрикостных уплотнений, прерывов контуров или увеличения в объёме тел позвонков, выраженных сужений межпозвонковых дисков. В отдельных случаях, при однократном обследовании нельзя точно дать оценку той или иной деформации, что требует динамического наблюдения за пациентом или более детального исследования области перелома с помощью компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) [85, 86]. В качестве альтернативы рентгенологическому исследованию исходно может быть выполнена компьютерная томография или магнитно-резонансная томография позвоночника Th4-L5.
Применение рентгенологических методов визуализации позвоночника
Оценка состояния позвонков проводится с использованием рентгенографии грудного и поясничного отделов позвоночника в боковой проекции или с применением рентгеновской морфометрии в рамках рутинной рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости [83, 87]. Для выполнения рентгенографии применяется стандартное рентгенологическое оборудование. Получение боковых рентгенограмм грудного (Th4–Th12) и поясничного (L1–L5) отделов позвоночника требует соблюдения ряда правил [84,88]:
— положение пациента на левом боку;
— обязательное выпрямление сколиотического искривления позвоночника специальными поролоновыми валиками так, чтобы линия, проведённая по остистым отросткам, шла параллельно столу;
— использование при рентгенографии грудного отдела позвоночника специального режима дыхания; снимок поясничного отдела делается при задержке дыхания;
— желательно использование рентгеновских кассет со специальными выравнивающими экранами для рентгенографии позвоночника.
Методы оценки переломов тел позвонков.
Компрессионный перелом тела позвонка – это снижение высоты тела позвонка (компрессионная деформация) в переднем, среднем или заднем отделах на 20% и более по сравнению с другими отделами этого же позвонка [83].
Классификация переломов 0, 1, 2 и 3 степени схематически показаны в Приложении А3.3.
Практическим специалистам не рекомендуется устанавливать диагноз остеопороза на основании косвенных признаков повышенной прозрачности костей скелета на стандартных рентгенограммах у пациентов без компрессионных переломов тел позвонков. В ряде случаев, в заключении рентгенолога указаны признаки остеопороза при рентгенографии различных участков скелета. Основной рентгенологический симптом остеопороза – повышение рентгенопрозрачности костной ткани неспецифичен и в значительной степени зависит от технических условий съёмки и качества проявления рентгенограмм [1]. При отсутствии характерных компрессионных деформаций тел позвонков (компрессионных переломов) установление диагноза остеопороз на основании данных рентгенографии неправомочно [1]. КТ, МРТ и сцинтиграфия скелета могут рассматриваться в качестве дополнительных методов дифференциальной диагностики [85, 89-92].
- Рекомендовано устанавливать диагноз остеопороза и назначать лечение пациентам (женщинам в постменопаузе и мужчинам старше 50 лет) c высокой индивидуальной 10-летней вероятностью основных патологических переломов (результат оценки FRAX соответствует российскому порогу вмешательства (Рисунок 2) и/или превышает «высокую вероятность переломов» (Таблица 3)) независимо от показателя рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости [15, 17, 18, 93-95].
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 3)
Комментарии: Если в ходе оценки жалоб, анамнеза, физикального обследования и рентгенографии позвоночника патологические переломы не выявлены, решение о необходимости назначения терапии остеопороза принимается на основании 10-летней вероятности развития патологического перелома [3].
В результате расчета FRAX врач получает индивидуальную 10-летнюю вероятность перелома бедренной кости (%) и основных патологических переломов (%). Термин основные патологические переломы, в данном случае, объединяет клинически значимые переломы тел позвонков (то есть переломы, которые сопровождаются болью), переломы бедренной, плечевой и лучевой костей [3,6,16, 96].
При расчете индивидуальной 10-летней вероятности перелома, алгоритм FRAX учитывает вероятность летального исхода от других причин [6]. Вероятность патологического перелома и смертность заметно различается в разных регионах мира [97], поэтому алгоритм FRAX откалиброван для тех стран, где эпидемиология патологических переломов бедренной кости и уровень смертности известны [98-101].
Построенная на основании российских данных точка вмешательства [15], нижний порог вмешательства и верхний порог вмешательства сведены в Таблице 3.
Таблица 3. Точка вмешательства FRAX по 10-летней вероятности (в процентах) основных патологических переломов эквивалентных вероятности переломов у женщин с патологическим переломом в анамнезе без других факторов риска (ИМТ = 24 кг/м2), без данных по МПК [15]
Примечания:
1 Точка терапевтического вмешательства – значение индивидуальной 10-летней вероятности основных патологических переломов, при котором пациенту соответствующего возраста на основании совокупности факторов риска показано начинать терапию остеопороза. (Рентгеноденситометрия поясничного отдела позвоночника и проксимального отдела бедренной кости может быть проведена только для динамической оценки эффективности лечения.)
2 Низкая вероятность переломов – значение индивидуальной 10-летней вероятности основных патологических переломов, при котором (и при более низких значениях) пациенту соответствующего возраста на основании совокупности факторов риска не показано проведение рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости, и пациент не нуждается в лечении остеопороза.
3Высокая вероятность переломов – значение индивидуальной 10-летней вероятности основных патологических переломов, при котором (и при более высоких значениях) пациенту соответствующего возраста на основании совокупности факторов риска не показано проведение рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости, и пациент однозначно нуждается в лечении остеопороза.
Точка вмешательства была предложена Российской ассоциацией по остеопорозу (РАОП) на основании статистических данных, полученных из травматологических клиник в городе Ярославле и городе Первоуральске [15, 102], которая затем была доработана с предложением нижней и верхней границ точки вмешательства (Рисунок 2). Необходимо отметить, что как эпидемиологические исследования, положенные в основу разработки FRAX, так и данные проспективной когорты, на которой российская точка вмешательства оценивалась [103], не обладают достаточной статистической мощностью, соответствующей таковой в Великобритании или в европейских странах с эпидемиологическими исследованиями на уровне страны [3]. В этой связи, лицам, у которых было рекомендовано исследование рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости по результатам FRAX (оранжевая зона) и был выявлен остеопороз по критериям ВОЗ (Т-критерий ≤ -2,5) должно быть рекомендовано лечение остеопороза без переоценки FRAX. Точка вмешательства одинаково определяет необходимость терапии как для женщин, так и для мужчин.
Рисунок 2. Точка вмешательства FRAX, предложенная для российской популяции по данным исследований в Ярославле и Первоуральске (ИМТ 24кг/м2) без данных по МПК.
Ограничения FRAX.
Необходимо учитывать, что FRAX не показан для использования у молодых людей и детей. Инструмент FRAX не был валидизирован у пациентов, ранее получавших или получающих на момент обращения фармакотерапию по поводу остеопороза. Однако пациенты, прекратившие прием препаратов 2 и более года назад, могут считаться нелечеными [104]. FRAX может быть рассчитан с включением МПК /Т-критерия в шейке бедренной кости, и не учитывает МПК поясничного отдела позвоночника. ВОЗ определила, что для многих вторичных причин остеопороза риск переломов был обусловлен, прежде всего, влиянием основного заболевания на МПК [25]. По этой причине при включении МПК в шейке бедра в онлайн-расчет FRAX отмеченные значения «вторичные причины остеопороза» автоматически инактивируются. Алгоритм оценки 10-летней вероятности переломов имеет ограничения, требующее клинического суждения врача. Так, при наличии у пациента множественных переломов риск последующих переломов будет занижен инструментом FRAX. Таким пациентам лечение остеопороза назначается независимо от показателя FRAX. FRAX не учитывает дозу глюкокортикоидов, количество сигарет и количество алкоголя, а также не учитывает влияние СД 2 типа на риск переломов.
- Рекомендуется увеличить индивидуальную 10-летнюю вероятность основных патологических переломов (FRAX) на 15% у пациентов, принимающих глюкокортикоиды в течение 3-х месяцев и более в дозе 7,5 мг/сут и более в перерасчете на преднизолон** с целью коррекции вероятности перелома [6, 105-107].
Уровень убедительности рекомендации С (уровень достоверности доказательств 4)
Комментарий: Перерасчет индивидуальной 10-летней вероятности переломов в зависимости от дозы глюкокортикоидов сведен в Таблице 4 [3].
Таблица 4. Средний перерасчет 10-летней вероятности перелома бедренной кости и основных патологических переломов у женщин в постменопаузе и у мужчин в зависимости от дозы глюкокортикоидов [3]

- При проведении оценки индивидуальной 10-летней вероятности FRAX у лиц с сахарным диабетом 2 типа рекомендуется провести коррекцию полученного результата, добавив дополнительный риск, ассоциированный с ревматоидным артритом (поставить «да» для данного фактора риска) или ввести результаты исследования трабекулярного костного индекса (ТКИ) [108-110].
Уровень убедительности рекомендации С (уровень достоверности доказательств 4)
Комментарий: На основании ректроспективного исследования в провинции Манитоба и позиции рабочей группы по СД международного фонда остеопороза были предложены поправки для применения FRAX: при наличии у пациентов СД 2 типа рекомендуется отметить «да» для ревматоидного артрита, а также ввести значение ТКИ, который лучше, чем МПК отражает снижение качества костной ткани при СД [108, 109]. Рассматривались и другие возможности улучшения чувствительности FRAX для выявления популяции высокого риска переломов среди пациентов с СД 2 типа, в частности уменьшение Т-критерия в шейке бедренной кости на 0,5 стандартных отклонения при введении показателя рентгеноденситометрии и увеличение возраста пациента на 10 лет. Однако было принято решение, в первую очередь, использовать введение дополнительного риска сопоставимого с ревматоидным артритом или суррогатного маркера качества кости [110].
- Проведение двухэнергетической рентгеноденситометрии (DXA) поясничного отдела позвоночника и проксимального отдела бедренной кости рекомендовано лицам с индивидуальной 10-летней вероятностью основных патологических переломов (FRAX) в интервале между низкой и высокой вероятностью переломов (Табл.3 или оранжевая зона Рисунок 2) для диагностики остеопороза [111-117].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Рентгеноденситометрия проксимального отдела бедренной кости и поясничного отдела позвоночника может быть использована для следующих целей:
1. Для установки или подтверждения диагноза остеопороза, согласно рекомендациям ВОЗ 1994 года (Таблица 5);
Таблица 5. Диагностика остеопороза на основании снижения МПК согласно критериям ВОЗ [6] для женщин в постменопаузе и мужчин старше 50 лет

*В настоящее время к тяжелому остеопорозу относится остеопороз с патологическим переломом бедра, тела позвонка или множественными переломами независимо от снижения МПК.
2. прогнозирования/расчета риска переломов в зависимости от степени снижения МПК;
3. наблюдения за динамикой состояния пациентов на фоне терапии или без лечения.
Скрининг всех женщин, находящихся в периоде постменопаузы, с использованием рентгеноденситометрии поясничного отдела позвоночника и проксимального отдела бедренной кости экономически нецелесообразен, поскольку в 2-10 раз превышает стоимость лечения всех патологических переломов, поэтому единственной разумной стратегией является селективный скрининг в группах риска [81]. Ранее существовал широкий спектр показаний для проведения рентгеновской денситометрии аксиального скелета. Однако, в настоящее время, ключевые факторы риска переломов сведены в алгоритм FRAX и могут быть оценены через ресурс доступный в Интернете. Ввиду отсутствия достаточного количества денситометров в РФ рентгеноденситометрию поясничного отдела позвоночника и проксимального отдела бедренной кости рекомендуется проводить лицам со средней индивидуальной вероятностью перелома (оранжевая зона FRAX Рисунок 2), то есть, когда назначение лечения сомнительно. Использование значений МПК в сочетании с клиническими факторами риска улучшает прогнозирование переломов бедренной кости и патологических переломов в целом как у женщин, так и у мужчин. [92] Данная последовательность применения алгоритма FRAX и проведения рентгеноденситометрии была валидизирована [25, 111, 113, 118], а стратегия терапевтического вмешательства продемонстрировала экономическую эффективность. [119, 120]
- Проведение двухэнергетической рентгеноденситометрии (DXA) поясничного отдела позвоночника и проксимального отдела бедренной кости рекомендовано для оценки эффективности проводимой терапии, а также динамики состояния МПК у пациентов с ранее установленным остеопорозом и перерывом в лечении с временным интервалом не менее 12 месяцев от первого исследования [111, 121, 122].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Согласно всем проведенным исследованиям, рентгеновская денситометрия является наиболее точным методом мониторинга терапии, доказавшим связь изменений на фоне терапии со снижением риска переломов при применении зарегистрированных препаратов для лечения остеопороза, поэтому этот метод используется для динамического контроля, но не чаще 1 раза в 12 месяцев [123].
- Рекомендовано устанавливать диагноз остеопороз и назначать терапию при снижении МПК на 2,5 и более стандартных отклонения по Т-критерию в шейке бедренной кости и/или в целом в проксимальном отделе бедренной кости и/или в поясничных позвонках (L1-L4, L2-L4), измеренной двухэнергетической рентгеноденситометрией (DXA) у женщин в постменопаузе и мужчин старше 50 лет [1-3,6, 104, 124-132].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Основными показателями минерализации костной ткани при обследовании методом DXA являются [123, 132-134]:
— Костный минеральный компонент (bone mineral content, BMC) — показывает количество минерализованной ткани (г) при сканировании костей, обычно определяется длиной сканирующего пути (г/cм);
— МПК (или bone mineral density, BMD) — оценивается количество минерализованной костной ткани в сканируемой площади — (г/cм2).
В современной клинической практике индивидуальная МПК сравнивается с референсной базой данных. Из-за разницы в методах измерения МПК в зависимости от различий в диагностическом оборудовании, наиболее приемлемым методом оценки МПК является использование Т- и Z- критериев [124].
— Т-критерий представляет собой стандартное отклонение выше или ниже среднего показателя от пика костной массы молодых женщин в возрасте 20–29 лет. Рекомендуемый референсный интервал получен из базы данных третьего исследования национального здоровья и питания (NHANES III). Хотя существуют отдельные нормативные базы для мужчин и женщин, рекомендуется использовать единую базу данных для лиц обоих полов (NHANES III), так как при одном и том же Т-критерии риск переломов не отличается. Т-критерий, как упоминалось выше, используется для женщин в постменопаузе и мужчин старше 50 лет. Классификация ВОЗ по денситометрической диагностике остеопороза, предложенная в 1994 году, не пересмотрена до настоящего времени [125], последние изменения и дополнения были внесены в 2013 году [127] (Таблица 5).
— Z-критерий представляет собой стандартное отклонение выше или ниже среднего показателя МПК у здоровых мужчин и женщин аналогичного возраста.
У женщин до менопаузы, мужчин моложе 50 лет и детей диагностическая классификация по Т-критерию не может быть применима. В этих группах диагностика остеопороза не должна проводиться лишь на основании денситометрических критериев. Международное общество по клинической денситометрии (ISCD) рекомендует вместо T-критерия использовать скорректированные по этническому и расовому признаку Z-критерий, при значениях которого -2,0 и ниже следует давать определение «низкая МПК для хронологического возраста» или «ниже ожидаемых по возрасту значений», а выше -2,0 – «в пределах ожидаемых по возрасту значений» [132, 134].
Показатели денситометрии служили критерием включения в подавляющее большинство клинических исследований эффективности препаратов для лечения остеопороза, и именно в этих популяциях продемонстрирована противопереломная эффективность терапии на фоне улучшения МПК, поэтому при выявленном снижении МПК, соответствующему остеопорозу, оправдано рекомендовать существующую терапию.
- Результат трабекулярного костного индекса (ТКИ), или trabecular bone score (TBS), полученный в ходе стандартной рентгеноденситометрии поясничного отдела позвоночника, рекомендуется использовать для одномоментного включения в алгоритм FRAX у пациентов, проходящих скрининг по поводу остеопороза с целью повышения чувствительности метода выявления пациентов с повышенным риском переломов [135].
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 2)
Комментарии: По результатам мета-анализа, ТКИ показал независимый вклад в предсказание риска переломов и, на сегодняшний день, этот показатель введен в алгоритм FRAX для повышения чувствительности метода [109]. ТКИ – тканевой показатель, оценивающий пиксельные отклонения по шкале градаций серого на денситометрических изображениях поясничного отдела позвоночника, другими словами – непрямой показатель трабекулярной микроархитектоники [136]. Отдельной точки вмешательства в отличие от DXA для этого показателя не существует. Однако введение параметра позволяет улучшить чувствительность FRAX и учитывает недостающие данные МПК поясничного отдела позвоночника. Для женщин в постменопаузе была также разработана градация ТКИ по степени нарушения микроархитектоники: деградированная микроархитектоника ТКИ ≤ 1,23; частично деградированная микроархитектоника> 1,23, но <1,31 и нормальная микроархитектоника ≥ 1,31 [135-137]. Однако данная классификация используется в исследовательских целях и пока не может служить основанием для лечения.
Практическим специалистам не следует устанавливать диагноз остеопороза на основании данных ультразвуковой денситометрии, измерения МПК не аксиального скелета (например, МПК пяточной кости, лучевой кости и т.д.), а также использовать нестандартные, неодобренные производителем денситометров способы укладки пациентов (например, денситометрия лежа на боку) и другие локализации исследования МПК, измеренные при рентгеноденситометрии (например, треугольник Варда). Эти методы исследования не были валидизированы подобно стандартной двухэнергетической рентгенденситометрии и никогда не служили основанием для включения в исследование. Кроме того, вариабельность ультразвуковых методов исследования достаточно высока [137].
Все расчеты и градации риска переломов построены на относительных показателях: стандартных отклонениях от рефренсной базы данных молодых здоровых женщин (пика костной массы). Референсные данные были получены для определенных зон скелета с применением установленной укладки [104, 124, 133-135]. Эти нормы не являются референсными для других зон скелета и других укладок.
Иные диагностические исследования
В Таблице 6 приведены иные диагностические техники, которые точны и высоко воспроизводимы [137]. Трехмерное измерение МПК, производимое при количественной КТ, определяет количество минерализованной костной ткани на объем кости (г/см3). Вместе с тем, T-критерии, получаемые при применении этих технологий, не могут быть достоверно использованы в целях диагностической классификации, так как они не эквивалентны T-критериям, полученным при DXA.
Таблица 6. Дополнительные остеоденситометрические технологии [129]
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Препараты для лечения остеопороза можно условно разделить на антирезорбтивную терапию (БФ, деносумаб**), преимущественно подавляющие костную резорбцию, действуя на остеокласт и анаболические (терипаратид**), которые преимущественно усиливают костеобразование [10]. Ввиду сопряженности костного обмена, как правило, при уменьшении костного разрушения снижается и костеобразование, а при увеличении костеобразования постепенно увеличивается костная резорбция. Клиническая эффективность медикаментозной терапии остеопороза оценивается по снижению количества переломов и косвенно по ряду суррогатных критериев, таких как, изменение МПК или маркеров костного ремоделирования. Основные эффекты препаратов для лечения остеопороза, разделенные по популяциям с различным риском патологического перелома сведены в Приложении А3.1.
- БФ рекомендованы для предупреждения патологических переломов и повышения МПК у пациентов с постменопаузальным остеопорозом (алендроновая кислота**, ризедроновая кислота, ибандроновая кислота, золедроновая кислота**), остеопорозом у мужчин (алендроновая кислота**, ризедроновая кислота, золедроновая кислота**), глюкокортикоидным остеопорозом (ГКО) (алендроновая кислота**, ризедроновая кислота, золедроновая кислота**) [138-151].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Детальные результаты регистрационных исследований сведены в Приложении А3.1. Алендроновая кислота** снижает частоту переломов позвонков и бедренной кости в течение 3-х лет лечения у пациентов с предшествующим переломом позвонков или у пациентов с остеопорозом (Т-критерий ≤ -2,5) в области бедренной кости [138, 139]. Алендроновая кислота** также повышает МПК при остеопорозе у мужчин и ГКО у женщин и мужчин. [140, 141]. Похожие результаты и спектр показаний у ризедроновой кислоты [142-144], однако, следует отметить, что у неоригинальных препаратов, доступных в РФ, может отсутствовать показание ГКО согласно официальной инструкции. Ибандроновая кислота снижает частоту развития переломов тел позвонков в течение 3-х лет, но не влияет на снижение риска внепозвоночных переломов при первичном анализе данных исследования BONE [145]. Другие дозы ибандроновой кислоты (150 мг 1 раз в месяц и 3 мг 1 раз в 3 месяца внутривенно) подтвердили свою сходную эффективность [146, 147]. Эффективность ибандроновой кислоты для предупреждения внепозвоночных переломов была показана по данным мета-анализа [148]. Ибандроновая кислота 150 мг 1 раз в месяц исследовалась при ГКО (n = 140; Т-критерий > -2,0) [152] и у мужчин (n=132; Т критерий ≤ -2,0 в шейке бедренной кости) [153] и была эффективна для повышения МПК и снижения маркеров костного ремоделирования. Однако официально эти показания не зарегистрированы и назначение ибандроновой кислоты при ГКО и остеопорозе у мужчин не прописано в инструкции. Золедроновая кислота** снижает частоту переломов тел позвонков (со значительным снижением риска уже за 1 год лечения), переломов бедренной кости и внепозвоночных переломов в течение 3-х лет у пациентов с предшествующим переломом тела позвонка или снижением МПК в области бедренной кости, соответствующее остеопорозу [149]. Препарат продемонстрировал противопереломную эффективность для лечения остеопороза у мужчин [150], а также для повышения МПК при ГКО [151].
- Золедроновую кислоту** в дозе 5 мг 1 раз в год дополнительно рекомендуется назначать после хирургического лечения по поводу патологического перелома проксимального отдела бедренной кости (минимум через две недели после операции) для предупреждения новых переломов и улучшения выживаемости пациентов [152].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Инфузии золедроновой кислоты** через минимум две недели после хирургического вмешательства по поводу перелома бедренной кости у мужчин и женщин в течение 3–х лет, продемонстрировали лучшую выживаемость и снижение риска новых переломов по сравнению с теми, кто получил плацебо [152].
- Золедроновая кислота** в дозе 5 мг 1 раз в 24 месяца рекомендуется для предупреждения потери МПК у женщин в постменопаузе с остеопенией и 1 раз в 18 месяцев для предупреждения переломов в группе женщин старше 65 лет [153, 154].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарий: Золедроновая кислота** продемонстрировала эффективность для повышения МПК у женщин с остеопенией, назначенная в режиме 1 инфузии 5 мг на 2 года терапии [153]. Кроме того, в результате 6-летнего двойного слепого исследования с участием 2000 женщин старше 65 лет с остеопенией в бедренной кости (Total Hip и Neck Т-критерий от -1,0 SD до -2,5 SD) было показано снижение риска переломов тел позвонков (отношение рисков 0,63 ;95% ДИ 0,50 до 0,79; P <0,001) и внепозвоночных переломов (отношение рисков 0,66; P = 0,001) у пациенток, получавших золедроновую кислоту** 5 мг внутривенно капельно 1 раз в 18 месяцев по сравнению с приемом плацебо [154].
- Деносумаб** 60 мг 1 раз в 6 месяцев рекомендован для предупреждения патологических переломов и повышения МПК у женщин с постменопаузальным остеопорозом, у мужчин с повышенным риском переломов, при глюкокортикоидном остеопорозе, а также для предупреждения потери МПК и переломов при отсутствии костных метастазов у женщин, получающих терапию ингибиторами ароматазы по поводу рака молочной железы, и у мужчин с раком предстательной железы, получающим гормон-депривационную терапию [155-164].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: Эффективность деносумаба** по данным РКИ суммирована в Приложении А3.1 (снижение риска переломов тел позвонков на 68%, бедренной кости на 40% и внепозвоночных переломов на 20% по сравнению с плацебо) [155]. В ходе исследования была обнаружена дополнительная польза препарата для предупреждения падений: 175 (4,5%) в группе лечения по сравнению с 219 (5,7%) в группе плацебо p=0,02 и видимо, как следствие, уменьшение случаев ушибов 1 — в группе лечения (<1%) по сравнению с 11 (0,3%) в группе плацебо. Повышение МПК, сходное с полученным у женщин, наблюдалось у мужчин со сниженной костной массой (+8% в L1-L4 и +3,4% в шейке бедренной кости за 2 года лечения) [156,157]. Исследование по эффективности деносумаба** по сравнению с ризедроновой кислотой у лиц с ГКО включало 795 мужчин и женщин в возрасте ≥18 лет, получавших ≥7,5 мг преднизолона**. Все включенные пациенты моложе 50 лет уже имели патологический перелом в анамнезе, среди лиц старше 50 лет были пациенты со снижением МПК ≤-2,0 по Т-критерию или перелом независимо от МПК. Пациенты были рандомизированы для получения инъекций деносумаба** 60 мг 1 раз в 6 месяцев или ризедроновой кислоты 5 мг ежедневно. По результатам лечения в течение 24 месяцев деносумаб** превосходил ризедроновую кислоту в отношении увеличения МПК поясничного отдела позвоночника и МПК бедренной кости во всех измеренных зонах (за 24-месяца поясничный отдел позвоночника: деносумаб** +6,2% против ризедроновой кислоты + 1,7%, р <0,001; Total Hip: деносумаб** + 3,1% против ризедроновой кислоты 0,0%, р <0,001) [158].
Деносумаб** позволял предупредить новые переломы тел позвонков у женщин, получающих терапию по поводу гормонально-зависимого рака молочной железы без метастатического поражения скелета [159]. Кроме того, деносумаб** был эффективен для предупреждения переломов у мужчин, получающих андроген-депривационную терапию по поводу рака предстательной железы в течение 36 месяцев без метастатического поражения костей скелета (ОР 0,38 (95%ДИ 0,19-0,78) [160].
- Деносумаб** 60 мг 1 раз в 6 месяцев дополнительно рекомендуется назначать пациентам с остеопорозом с большей потерей МПК в кортикальной кости (шейке бедренной кости, лучевой кости), пациентам с компрометированной функцией почек, а также пациентам, у которых лечение БФ было неэффективно или не удалось достичь желаемой прибавки МПК [165-173].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Распределение деносумаба** в костной ткани в отличие от БФ не зависит от активности костного ремоделирования в момент введения препарата, что позволяет добиться сопоставимой концентрации деносумаба** в трабекулярной и кортикальной кости и постоянного присутствия препарата в любой зоне кровоснабжения костной ткани [167, 174, 175]. Кроме того, клиренс деносумаба**, как белковой молекулы, не зависит от функции почек [174, 175]. Деносумаб** был более эффективен для прироста МПК при прямом сравнении со всеми БФ [166-168] и эффективно повышал МПК будучи назначенный как после БФ [169], так и после терипаратида** [170].
- Терипаратид** в дозе 20 мкг 1 раз в сутки рекомендован для предупреждения патологических переломов и прибавки МПК у женщин в постменопаузе с компрессионными переломами тел позвонков, для лечения остеопороза у мужчин; для лечения ГКО [30, 176-179].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Клиническая эффективность терипаратида** в дозе 20 мкг 1 раз в сутки была доказана у женщин в постменопаузе с патологическими переломами тел позвонков в анамнезе независимо от исходного снижения МПК, предшествующих переломов и возраста (Приложение A3) [30, 31, 176], у мужчин со снижением МПК [177], в том числе вследствие гипогонадизма и у пациентов с ГКО [178]. Увеличение МПК и изменения костного обмена у мужчин (437 пациентов 30-85 лет средний Т-критерий в шейке бедренной кости -2,7 SD) соответствовали увеличению МПК и изменениям маркёров костного метаболизма у женщин, что позволяет предположить аналогичное влияние терипаратида** на снижение риска переломов у мужчин [177]. Наиболее серьезное исследование эффективности терипаратида** для лечения ГКО было проведено с участием 428 женщин и мужчин в возрасте от 22 до 89 лет [178]. Пациенты были рандомизированы на тех, кто принимал терипаратид** в дозе 20 мкг (n=214) и алендроновую кислоту** 70 мг (n=214). Лечение терипаратидом** в течение 18 месяцев оказалось более эффективным для предупреждения переломов тел позвонков по сравнению с алендроновой кислотой** (0,6% новых переломов позвонков в группе терипаратида** по сравнению с 6,1% в группе алендроновой кислоты** p=0,004). Лучший прирост МПК был зарегистрирован на фоне применения терипаратида** по сравнению с алендроновой кислотой** (+7,2% терипаратид** vs +3,4% алендроновая кислота** в позвонках p<0,001; +3,8% терипаратид** vs +2,4 % алендроновая кислота** p=0,005 в целом в бедренной кости) [178]. Применение терипаратида** при ГКО было пролонгировано на 3 года, что продемонстрировало хорошую эффективность и безопасность при более длительном использовании [179].
- Терипаратид** в дозе 20 мкг 1 раз в сутки рекомендуется использовать в качестве первой линии терапии у пациентов с остеопорозом с двумя и более компрессионными переломами тел позвонков, а также при неэффективности предшествующей терапии [179-185].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Терипаратид** был более эффективен для предупреждения переломов тел позвонков по сравнению с ризедроновой кислотой в рандомизированном контролируемом исследовании у женщин в постменопаузе с двумя компрессионными переломами тел позвонков в анамнезе [182]. Через 24 месяца лечения новые переломы позвонков произошли у 28 (5,4%) из 680 пациентов в группе терипаратида** и у 64 (12,0%) из 680 пациентов в группе ризедроновой кислоты (соотношение риска 0 44, 95% ДИ 0,29-0,68; р <0,0001). Клинические переломы произошли у 30 (4,8%) из 680 пациентов в группе терипаратида** по сравнению с 61 (9,8%) из 680 в группе ризедроновой кислоты (отношение рисков 0,48, 95% ДИ 0,32-0,74; р = 0,0009) [183]. Терипаратид** также был более эффективен по сравнению с алендроновой кислотой** для предупреждения переломов тел позвонков у лиц с ГКО [178]. Ранее была показана лучшая эффективность терипаратида для прибавки МПК и для снижения болевого синдрома в спине по сравнению с другими БФ [183-185].
В мировой практике терипаратид** считается экономически оправданным использовать преимущественно у лиц с тяжелым остеопорозом (у пациентов с уже имеющимися переломами тел позвонков, независимо от степени снижения МПК), при неэффективности или непереносимости другой терапии остеопороза, а также лицам с высоким риском переломов и непереносимостью альтернативной терапии [2,3]. В Российской Федерации терипаратид** введен в список ЖВНЛП и ОНЛС и назначается по врачебной комиссии как дорогостоящее лечение на 24 месяца.
- Не рекомендуется использовать стронция ранелат** в рутинной практике для лечения остеопороза ввиду высокого риска сердечно-сосудистых осложнений и тромбоэмболии [186-189].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: В 2007, 2013-2014 гг. Европейским Медицинским Агентством в связи с появлением новой информации о нежелательных явлениях были введены ограничения на применение стронция ранелата** [186-188]. Этот препарат не рекомендован пациентам с ишемической болезнью сердца (ИБС), цереброваскулярной болезнью, патологией периферических артерий, плохо контролируемой гипертензией и должен быть отменен при развитии сердечно-сосудистой патологии, что обусловлено повышением риска нежелательных явлений со стороны сердечно-сосудистой системы, в частности повышения риска инфаркта миокарда на 60% (ОР 1,6 95% ДИ 1,07-2,38)). Стронция ранелат** противопоказан у пациентов с тромбозами и тромбоэмболиями, в том числе в анамнезе, а также у пациентов с факторами риска тромбообразования: постоянной или временной иммобилизацией; не рекомендуется применение стронция ранелата** у пациентов старше 80 лет, так как в этой возрастной группе риск тромбозов и тромбоэмболий значительно возрастает.
Кроме того, редкие, но тяжелые кожные реакции гиперчувствительности, в некоторых случаях с летальным исходом, были связаны с применением стронция ранелата** [188].
Согласно официальной позиции регуляторных органов, решение о назначении стронция ранелата** может быть принято только у пациентов с тяжелым остеопорозом, когда ни один другой препарат для лечения остеопороза не подходит с учетом всех указанных выше ограничений. Если принято решение о назначении стронция ранелата** необходимо мониторировать риск развития сердечно-сосудистой патологии в течение всего времени лечения и отменять препарат в случае появления симптомов сердечно-сосудистых заболеваний, кожных реакций и вероятности развития тромбоза [186-189].
Продолжительность лечения остеопороза. Последовательная и комбинированная терапия остеопороза
- Пациентам с остеопорозом без патологических переломов при достижении клинического эффекта терапии (МПК до -2,0 SD по Т-критерию в шейке бедренной кости и отсутствием новых переломов) рекомендовано на 1-2 года прекратить терапию БФ с последующим динамическим наблюдением [190-192].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 2)
Комментарии: Снижение МПК до -2.5 SD по Т-критерию является традиционным основанием для начала терапии остеопороза, и этот показатель сохраняется для возобновления терапии БФ или начала альтернативной терапии. Терапия может быть возобновлена при появлении нового принципиального фактора риска [190]. По последним данным в ходе систематического анализа было показано, что уже через 1-2 года после отмены БФ частота переломов начинает возрастать [193], поэтому перерыв в лечении рассматривается с большей осторожностью особенно в популяции пациентов с высоким риском переломов, у пациентов с уже имеющимися переломами в анамнезе. Если лечение остеопороза было начато в связи со снижением МПК в поясничных позвонках без снижения МПК в бедре оправданно добиваться сопоставимого Т-критерия (-2,0 SD и лучше) в поясничных позвонках.
- Пациентам с переломами тел позвонков, бедренной кости или множественными переломами в анамнезе рекомендуется продолжать непрерывное длительное лечение остеопороза [46, 192-197].
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 3)
Комментарии: Средняя продолжительность непрерывного лечения остеопороза с целью предупреждения переломов и повышения МПК таблетированными БФ составляет 5 лет, внутривенными БФ — 3 года [190]. Максимальный период применения БФ в условиях клинических исследований составляет 10 лет (алендроновая кислота**) [46]. Средние и максимальные периоды лечения БФ были определены на основании систематического анализа доказательных данных американского общество исследований костей и минералов (American Society for Bone and Mineral Research) [190]. При применении деносумаба** [194] стойкий ежегодный прирост МПК сохраняется в течение 10 лет во всех отделах скелета, что дает преимущество перед БФ, на фоне которых прирост МПК в шейке бедренной кости наблюдается в течение первых 2-3 лет [46, 191, 192].
- Пациентам с остеопорозом без переломов в анамнезе рекомендуется лечение деносумабом** до достижения МПК -2,0 SD по Т-критерию и выше в шейке бедренной кости, а также поясничных позвонках; во всех случаях отмены деносумаба** необходим перевод на терапию БФ [174, 175, 195-203].
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 3)
Комментарии: Стойкий ежегодный прирост МПК сохраняется в течение 10 лет применения деносумаба** [194] во всех отделах скелета, что дает преимущество перед БФ, на фоне которых прирост МПК в шейке бедренной кости наблюдается в течение первых 2-3 лет [46, 192].
При отмене деносумаба** через 1-3 года лечения маркёры костного обмена и МПК возвращаются к исходному состоянию через 12 месяцев, а при возобновлении лечения прибавка МПК и подавление маркёров костного ремоделирования восстанавливаются вновь [195, 196]. Данные о повышении риска переломов после отмены деносумаба** противоречивы. С одной стороны, при наблюдении пациентов в течение двух лет после отмены деносумаба** не наблюдалось повышения количества переломов по сравнению с группой ранее леченных плацебо [196]. C другой стороны, были описаны клинические случаи спонтанных переломов тел позвонков, гиперкальциемии после отмены деносумаба** [199, 200, 204]. Есть основания полагать, что назначения БФ после длительного применения деносумаба** позволяет нивелировать нежелательные эффекты отмены [197,198]. Было проведено несколько систематических анализов и опубликованы позиции ведущих международных обществ, признавших обратимость терапевтического эффекта деносумаба**, который в отличие от БФ не накапливается в костной ткани [197, 198]. Так как остеопороз является хроническим заболеванием, пациенты нуждаются в непрерывном лечении деносумабом** или в переводе на альтернативную терапию в случае принятия решения о необходимости прекратить лечение этим препаратом.
Таким образом, ввиду лучшей эффективности деносумаба** для прибавки МПК по сравнению с БФ у лиц с тяжелым остеопорозом, с уже имеющимися переломами оправдано длительное лечение деносумабом** до 10 лет [194], что является эффективным и безопасным. Если решение о начале терапии остеопороза было принято только на основании снижения МПК, то по достижению терапевтического эффекта (Т-критерий -2,0 SD и более) ввиду отсутствия значительного снижения риска переломов при последующем лечении возможен перевод на терапию БФ. При этом таблетированные БФ могут быть рекомендованы сразу через 6 месяцев после последней инъекции деносумаба**, а введение золедроновой кислоты** оправдано примерно через 8 месяцев после последней инъекции деносумаба** [196].
- После окончания лечения терипаратидом** рекомендуется перевод на антирезорбтивную терапию деносумабом** для дальнейшего прироста МПК или БФ для сохранения терапевтического эффекта [205-207].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Максимально разрешенная продолжительность лечения остеопороза терипаратидом** составляет 24 месяца. После окончания терапии терипаратидом** обязательно назначение антирезорбтивной терапии, так как терипаратид** не накапливается в костной ткани и его эффекты обратимы [1-3]. Комбинированную терапию терипаратидом** и деносумабом** можно рассматривать при тяжелом остеопорозе и значительной потере МПК, поскольку единственным препаратом с антирезорбтивным действием, показавшим более выраженную прибавку МПК в комбинации с терипаратидом** по сравнению с терипаратидом** в монотерапии, был деносумаб** [205]. В рандомизированном исследовании назначения деносумаба** или БФ после терипаратида** было показано более выраженное повышение МПК на фоне назначения деносумаба** по сравнению с БФ** [206], поэтому для лиц с недостаточным приростом МПК оправдано дальнейшее лечение деносумабом** до достижения терапевтического эффекта и уже затем перевод пациента на БФ. Назначение терипаратида** после деносумаба** сопряжено с потерей МПК, данные по переломам неизвестны [205], поэтому при неэффективности деносумаба** будет более оправдано добавить к лечению терипаратид, а не производить замену деносумаба** на терипаратид**.
- При неэффективности проводимой терапии остеопороза: развитии 2 и более патологических переломов за время лечения; потере МПК на 4% в бедренной кости и 5% в позвонках за два последовательных измерения; изменении маркеров костного обмена на фоне лечения менее, чем на 30%, в сочетании с потерей МПК рекомендуется переоценка приверженности пациента к лечению, исключение вторичных причин остеопороза и других метаболических заболеваний скелета и смена терапии остеопороза [208].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: Согласно разработанному консенсусу смена терапии производится в случае неэффективности предшествующего лечения: от таблетированных к парентеральным БФ и анаболической терапии [208]. Вместе с тем, терапия остеопороза может назначаться в любой последовательности (за исключением замены деносумаба** на терипартид**) на усмотрение врача и с учетом пожеланий пациента по режиму дозирования. Как ранее было рекомендовано, у пациентов с впервые диагностированным тяжелым остеопорозом наиболее предпочтительно начинать лечение с анаболической терапии и затем переходить на антирезорбтивную [182-185].
Выбор таблетированных или парентеральных форм антирезорбтивной терапии как при первом назначении препарата, так и после анаболической терапии решается индивидуально [1-3]. Нет оснований начинать лечение остеопороза именно с таблетированных форм, но преимущественное назначение парентеральных препаратов рекомендуется пациентам с патологией верхних отделов желудочно-кишечного тракта. Деносумаб** может иметь дополнительное преимущество в качестве первой линии терапии при потере МПК в кортикальной кости и снижении функции почек. В случае исключения вторичных причин остеопороза, тяжелого дефицита витамина D, низкой приверженности пациента к лечению, оправдан перевод пациента с таблетированных БФ на парентеральные и/или с антирезорбтивной терапии на анаболическую терапию терипаратидом** [208]. В редких случаях крайне низкой МПК, тяжелого течения остеопороза возможна комбинация терипаратида** и деносумаба** по решению врачебной комиссии.
- Все препараты для лечения остеопороза рекомендуется назначать в сочетании с препаратами кальция и колекальциферола** [138-147, 149-152, 155-158, 176-182].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: Все препараты для терапии остеопороза должны назначаться в сочетании с препаратами кальция (500-1000 мг в сутки) и колекальциферола** (минимум 800 МЕ в сутки), так как доказанная эффективность по результатам РКИ была продемонстрирована именно в такой комбинации [138-147, 149-152, 155-158, 176-182]. Имеются небольшие исследования, доказывающие, что вместо нативного витамина D (колекальциферола**) в комбинации с БФ можно использовать альфакальцидол** в дозе 1 мкг, и это позволяет добиться положительного эффекта даже при предшествующей потере до 3% МПК при терапии в сочетании с колекальциферолом** [209].
Данные по эффективности препаратов для лечения остеопороза, полученные на основании регистрационных исследований детально изложены в приложении А3.1 [143, 147, 155, 210, 211]. Показания, противопоказания и потенциальные нежелательные явления задокументированы в инструкциях к препаратам. Риски редких нежелательных явлений (атипичные переломы, остеонекроз челюсти) на фоне антирезорбтивной терапии значительно уступают потенциальной пользе на фоне лечения у пациентов с повышенным риском переломов [211].
Хирургическое лечение
- Всем пациентам с патологическим переломом проксимального отдела бедренной кости рекомендуется госпитализация и хирургическое лечение у врача-травматолога-ортопеда в течение 48 часов с последующей активизацией пациента для повышения выживаемости [213-216].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: Единственной возможностью для пожилого пациента вернуться к прежнему уровню активности после перелома проксимального отдела бедренной кости является его оперативное лечение [213, 214]. Выбор метода хирургического лечения изложен в клинических рекомендациях и методических рекомендациях ассоциации травматологов-ортопедов [215].
Для оказания полноценной специализированной помощи данной группе пациентов необходимо руководствоваться следующими принципами [213].
1. Все пациенты с переломом проксимального отдела бедренной кости должны быть госпитализированы в специализированное отделение не позднее 4 часов с момента поступления в стационар;
2. Все пациенты с переломом шейки бедренной кости должны быть оперированы в течение 48 часов; с чрезвертельным переломом бедренной кости – в течение 72 часов;
3. Все пациенты с переломом проксимального отдела бедренной кости должны получать соответствующий уход для профилактики образования пролежней;
4. Все пациенты с переломом бедренной кости на фоне остеопороза должны быть осмотрены врачом-терапевтом при поступлении;
5. Всем пациентам с патологическим переломом бедренной кости должна в последующем быть назначена специфическая терапия остеопороза;
6. Всем пациентам с переломом бедренной кости на фоне остеопороза должны быть рекомендованы мероприятия по профилактике падений.
Все операции у данной категории пациентов должны проводиться в срочном порядке по жизненным показаниям, что должно быть отражено в предоперационном эпикризе [213, 214].
Противопоказаниями к проведению срочного хирургического лечения (остеосинтеза перелома или артропластики) являются [216, 217]:
1. Острый инфаркт миокарда или острое нарушение мозгового кровообращения;
2. Пневмония с необходимостью перевода пациента на ИВЛ;
3. Острое хирургическое заболевание, требующее немедленного хирургического лечения;
4. СД с декомпенсацией углеводного обмена (требуется срочный перевод на инсулинотерапию или контроль инсулинотерапии медперсоналом для подготовки к хирургическому лечению);
5. Кома любой этиологии;
6. Хроническая или острая гнойная инфекция в зоне предполагаемого разреза;
7. Терминальная стадия заболевания, приведшая к невозможности передвигаться пациенту еще до перелома;
8. Выраженные когнитивные нарушения или психическое заболевание пациента, приведшее к невозможности передвигаться до наступления перелома.
Все остальные сопутствующие заболевания в стадии декомпенсации могут расцениваться как противопоказания только в том случае, если их невозможно перевести в стадию субкомпенсации в течение 24-48 часов интенсивной терапии.
Отказ от операции в обязательном порядке должен быть оформлен консилиумом в составе врача-травматолога, врача-анестезиолога-реаниматолога и врача-терапевта. В случае однозначного отказа от операции пациента целесообразно перевести в соматическое отделение для лечения заболевания, по поводу которого было решение консилиума.
Организация оказания медицинской помощи
Остеопороз является системным хроническим заболеванием, поэтому, как правило, ведение таких пациентов осуществляется в амбулаторном порядке. Однако в некоторых случаях показана плановая госпитализация для проведения дифференциальной диагностики остеопороза и подбора терапии при тяжелом течении заболевания с множественными переломами, развитии новых патологических переломов на фоне проводимой терапии, а также при наличии костной патологии у пациентов молодого возраста.
Показания для плановой госпитализации в медицинскую организацию:
1) Наличие двух и более компрессионных переломов тел позвонков;
2) Наличие одного и более компрессионных переломов тел позвонков в сочетании внепозвоночными патологическими переломами в анамнезе;
3) Наличие патологического перелома у пациентов молодого возраста (менее 50 лет).
Показания к выписке пациента из медицинской организации:
1) Установления типа остеопороза: первичный или вторичный;
2) Оценка состояния фосфорно-кальциевого обмена, МПК и исключение других переломов;
4) Выбор тактики лечения пациента.
Одним из осложнений остеопороза является патологический перелом бедренной кости, который требует экстренной госпитализации и хирургического лечения у врача-травматолога-ортопеда в течение 48 часов с последующей активизацией пациента.
Показания для экстренной госпитализации в медицинскую организацию:
1) Патологический перелом бедренной кости.
Показания к выписке пациента из медицинской организации:
1) Проведение хирургического лечения перелома бедренной кости;
2) Активизация пациента в пределах палаты с опорой на «ходунки».
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Наибольшее влияние на течение и исход остеопороза, профилактику переломов оказывает приверженность пациента медикаментозной терапии. Лекарственные препараты для лечения остеопороза снижают риск развития переломов только при их регулярном приеме в сочетании с добавками препаратов кальция и препаратов витамина D и его аналогов. Продолжительность и последовательность терапии, преемственность между врачами хирургического и терапевтического профилей изложены в разделе «Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения».
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- После хирургического лечения перелома рекомендована ранняя активизация пациентов (желательно уже на 1-2 сутки после операции) и лечение остеопороза или другого заболевания скелета, приведшего к перелому для предупреждения новых переломов и улучшения прогноза реабилитации [213, 214, 216].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: После оперативного лечения перелома проксимального отдела бедренной кости перевод пациента из отделения ОРИТ должен осуществляться на 1-2 сутки. Оперативное пособие должно быть выполнено так, чтобы пожилой пациент смог с первых шагов нагружать оперированную ногу в полном объеме, опираясь на дополнительную опору («ходунки») [213, 214]. В послеоперационном периоде необходим тот же самый командный подход, как и в предоперационном периоде [217]. Важная роль в этой команде принадлежит специалисту по лечебной физкультуре (специалисту по физической и реабилитационной медицине), от активности которого во многом зависит успех всего предыдущего лечения. Оптимальным считается выписка пациента в реабилитационный центр на 5-7 день после операции и активизации пациента при помощи дополнительных средств опоры. При отсутствии такой возможности правильным будет выписать пожилого пациента после снятия послеоперационных швов на 12-14 день после операции. Основным критерием для выписки может считаться активизация пациента в пределах палаты с опорой на «ходунки» [217].
Обязательным в программе лечения пожилых пациентов с патологическими переломами проксимального отдела бедренной кости является профилактика повторных переломов и оценка риска падений. Профилактика повторных переломов заключается в лечении заболевания, наиболее часто остеопороза, сопровождающего патологические переломы у пожилых пациентов. Выбор препарата для лечения остеопороза после патологического перелома осуществляется индивидуально среди зарегистрированных препаратов. Назначение антирезорбтивной терапии (БФ, деносумаб**) не влияет на длительность сращения перелома [218]. В экспериментальных исследованиях отмечено, что назначение терипаратида** ведет к значительному улучшению формирования костной мозоли и положительно влияет на сращение перелома, но эти данные не были официально подтверждены у человека [218]. Все препараты назначаются в комбинации с препаратами кальция и колекальциферола**. Кроме того, необходимо уделить внимание факторам риска падений и устранить потенциально модифицируемые факторы риска падений. Факторы риска падения сведены в Таблице 7 [219].
Таблица 7. Факторы риска падений [219]
В работе с пожилым пациентом необходимо влиять на модифицируемые факторы риска, такие как коррекция сниженной остроты зрения, уменьшение потребления лекарственных препаратов, которые снижают концентрацию внимания и негативно влияют на равновесие, а также повышение безопасности домашней обстановки (устранение скользких полов, препятствий, недостаточного освещения, неудобных/отсутствующих поручней) [218].
- Пациентам с болевым синдромом в спине на фоне клинического компрессионного перелома позвонка, болях, возникающих при осевой нагрузке, и при нарушении статики позвоночника рекомендовано применение ортезов для уменьшения болевого синдрома [219-225].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 1)
Комментарии: Ортезы улучшают качество жизни, осанку и предотвращают увеличение угла кифоза [220, 221]. Ношение ортезов или корректоров осанки рекомендуется в постоянном или прерывистом режиме с обязательным освобождением от них в ночное время [222]. При множественных переломах возможно использование торако-люмбальных ортезов [223]. По индивидуальным показаниям, возможно, ношение корсетов-гиперэкстензоров [224, 225]. Однако следует понимать, что ортезы не являются методом лечения остеопороза, и в первую очередь необходимы для уменьшения болевого синдрома и более быстрой активизации пациента. Не следует рекомендовать ортез, если это не приносит облегчения боли пациенту и увеличения двигательной активности [221, 222]. Длительное ношение корсетов может привести к мышечной дистрофии, поэтому использование корсетов дольше 8-12 недель нежелательно [223-225]. При стабильном компрессионном переломе позвонка рекомендованы легкие конструкции, в менее тяжелых случаях – более эластичные ортезы, которые минимизируют риск развития слабости мышц спины [224].
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Профилактика остеопороза включает мероприятия, направленные на максимальный набор пика костной массы у детей и молодых людей, поддержание костной массы и предупреждение падений у здоровых людей старшей возрастной группы и профилактику падений и переломов у лиц с диагностированным переломом в анамнезе и с остеопорозом.
Физические нагрузки
- Физические упражнения с осевыми нагрузками (ходьба, бег, танцы, подвижные игры) рекомендованы для оптимального набора пика костной массы в юности и поддержания МПК у здоровых пожилых людей [226, 227].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 2)
Комментарии: Механическая нагрузка стимулирует анаболические процессы, характеризуемые повышением активности остеобластов и снижением костной резорбции остеокластами [228]. При наборе пика костной массы оправданы осевые нагрузки, в то время как в пожилом возрасте предпочтительно использовать охранительный режим, избегать значительных осевых нагрузок, чтобы избежать патологических переломов тел позвонков
Недостаток физической активности, а также избыточная физическая нагрузка в подростковом возрасте приводят к более низкому набору пиковой костной массы [226]. Дети и молодые люди, ведущие активный образ жизни, имеющие более высокие показатели мышечной силы, достигают более высокого пика костной массы [226, 227].
- Умеренные силовые тренировки (пилатес, тай-чи, плавание и т.д.) рекомендуются для укрепления мышечного корсета, улучшения координации у пожилых пациентов с переломом в анамнезе или с диагностированным остеопорозом [229].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 2)
Комментарии: Исследования с участием женщин c ранним наступлением менопаузы показали, что силовые тренировки приводили к небольшим, но значимым изменениям МПК [227]. Мета-анализ 16 исследований и 699 испытуемых показал улучшение на 2% МПК в поясничном отделе позвоночника в группе, где осуществлялись силовые упражнения, по сравнению с группой без значимой физической активности [230, 231].
Таким образом, в постменопаузе благоприятное влияние упражнений на МПК значительно меньше, чем у молодых, но физические нагрузки улучшают другие важные показатели, такие как равновесие и мышечная сила, что в конечном итоге благоприятно для уменьшения риска падений и снижения риска переломов. [232-234].
Иммобилизация является важной причиной потери костной массы. При обездвиженности пациенты могут потерять больше костной массы в неделю, чем за год при обычной физической активности [235].
Пациентам с патологическими переломами тел позвонков следует избегать сгибаний туловища вперед и вбок, поднятия тяжелого веса, а также выполнения упражнений, оказывающих силовое воздействие на позвонки (например, бег, прыжки, езда на лошади). У пациентов пожилого возраста с тяжелым кифозом, дискомфортом в спине, и нестабильностью походки, план физической реабилитации должен фокусироваться на упражнениях без дополнительного отягощения, укрепления мышечного корсета спины и тренировки равновесия. Важным также может быть использование ортопедических приспособлений (ортезы, трости, ходунки), что способно уменьшить дискомфорт, предотвратить падения и переломы и повысить качество жизни [234]. Наиболее оптимальным являются занятия под контролем опытного специалиста по лечебной физкультуре.
C целью профилактики падений, улучшения координации и укрепления мышц можно включать силовые тренировки и другие упражнения с сопротивлением, такие как йога, пилатес, тай-чи, плавание. Физиотерапия, например, электромиостимуляция, также может являться важным компонентом реабилитации после перелома. [232]. Эти же мероприятия целесообразно рассматривать для лиц с установленным остеопорозом, высоким риском перелома, однако без перелома в анамнезе.
Витамин D и кальций
Витамин D важен для абсорбции кальция в кишечнике и для минерализации костной ткани. Основным источником витамина D в организме является его синтез в коже под действием ультрафиолетового облучения. Получение данного витамина из пищи в необходимом объеме затруднительно ввиду ограниченного числа продуктов, которые его содержат в значимом количестве [236, 237].
При этом исследования показывают, что особенности образа жизни с ограничением пребывания на солнце и использование активной защиты от его излучения (солнцезащитные крема), являются одной из важных причин высокой мировой распространенности дефицита витамина D у населения. Подробно вопросы, касающиеся витамина D, изложены в соответствующих клинических рекомендациях [237].
-
Лечение дефицита витамина D рекомендуется препаратом колекальциферола** при установленном его дефиците (Табл.
и назначается курсом в лечебных дозах с последующим переводом на профилактическую терапию (Табл. 9) [237-244].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2).
Комментарии: Длительно существующие низкие уровни витамина D могут приводить к субоптимальной абсорбции кальция в кишечнике, в результате чего развивается вторичный гиперпаратиреоз с повышением мобилизации кальция из костей, снижением МПК и развитием остеопороза в ряде случаев в сочетании с остеомаляцией. Витамин D поддерживает формирование и обменные процессы в мышечной ткани, особенно на уровне быстрых мышечных волокон, что обуславливает предрасположенность к падениям лиц с дефицитом этого витамина [245-247]. Концентрация 25(ОН)D в сыворотке крови является лучшим индикатором для мониторинга статуса витамина D ввиду того, что это основная форма витамина D в циркуляции, имеет длительное время полужизни порядка 2-3 недель, отражает как поступление витамина D с пищей, приемом колекальциферола** и эргокальциферола, так и синтезированного в коже под воздействием ультрафиолетового облучения [246, 248].
Таблица 8. Интерпретация концентраций 25(OH)D, принятая Российской ассоциацией эндокринологов [245]
В связи с меньшей метаболической деградацией колекальциферола** (D3) он общепризнан препаратом выбора при коррекции низких уровней витамина D [245].
Таблица 9. Схемы лечения дефицита и недостаточности витамина D [245]
Дозы для поддержания уровня 25(ОН)D более 30 нг/мл, у лиц с ранее диагностированными низкими уровнями витамина D, как правило, выше профилактических и составляют не менее 1500-2000 МЕ колекальциферола** в сутки [245].
- Пациентам рекомендуется достаточное потребление кальция с продуктами питания (Табл. 10) или прием препаратов кальция при его недостаточном содержании в пищевом рационе [245, 249-251].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1).
Комментарии: Витамин D способен активировать абсорбцию кальция в кишечнике и минерализацию скелета только при наличии адекватного поступления самого кальция. Назначение антирезорбтивной терапии может резко повысить потребность в кальции, необходимом для восстановления костной ткани, поэтому очень важно для профилактики/лечения патологии скелета наряду с предварительной коррекцией уровня витамина D обеспечить адекватное поступление кальция с пищей [250].
При проведении рентгеноденситометрии в отчете рассчитывается показатель BMC, который отражает содержание кальция в костной ткани. Недостаточное поступление кальция может способствовать нарушению минерализации. Содержание кальция в продуктах питания сведено в Приложении А3.4.
Нормы потребления кальция для различных возрастных групп сведены в Таблице 10.
Таблица 10. Возрастные нормы потребления кальция [243]
Для здорового населения нормы потребления кальция учитывают все источники: кальций с пищей и с добавками/препаратами кальция.
Кальций, обладая слабым антирезорбтивным действием, потенцирует эффект основных препаратов для лечения остеопороза, предотвращает гипокальциемию и рекомендуется при любых терапевтических режимах и схемах [251].
В некоторых странах проводится обогащение часто используемых продуктов кальцием (круп, соков, хлеба). В России подобная практика не распространена. Достаточным суточным потреблением кальция с продуктами питание считается присутствие в рационе не менее трех порций молочных продуктов в день. К одной порции можно отнести 30г сыра, 100г творога, 150г йогурта, 200 мл молока [249]. Использование пищевых добавок кальция рекомендуется в случаях, когда невозможно достичь необходимого потребления кальция с пищевыми продуктами.
В мета-анализе 17 исследований, продолжавшихся до трех лет, более 50 000 пациентов получали монотерапию препаратами кальция или в сочетании с колекальциферолом**. В результате изолированного приема кальция было отмечено снижение риска переломов разных локализаций, включая позвонки, бедренную кость и предплечье, на 12% (ОР-0,88,95%ДИ, 0,83-0,95). Добавление колекальциферола** не приводило к существенному снижению риска переломов: на фоне приема кальция риск снижался на 10%, в комбинации с колекальциферолом** – на 13%. Примечательно, что в исследованиях с хорошим комплаенсом (>80%) отмечалось наибольшее снижение риска переломов, достигающее 24% [232]. Другой объединенный анализ 68 500 пациентов, получавших только колекальциферола**, не показал снижения риска переломов. Но комбинация препаратов кальция с колекальциферолом** снижала риск переломов на 12% (p=0,025) всех переломов и переломов бедренной кости – на 26% (p=0,005) [239].
- Активные метаболиты витамина D (альфакальцидол**, кальцитриол**) рекомендованы в группах пациентов с относительными или абсолютными показаниями для их назначения (Табл. 11), а также могут быть рекомендованы у пожилых пациентов с высоким риском падений как монотерапия или в комбинации с антирезорбтивной терапией для улучшения МПК [252].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: Абсолютные и относительные показания для назначения активных метаболитов витамина D сведены в Таблице 12.
ТАБЛИЦА 11. Абсолютные и относительные показания для назначения активных метаболитов витамина D [252]
Активные метаболиты витамина D и их аналоги продемонстрировали большую эффективность по сравнению с колекальциферолом** для снижения риска падений, особенно у пациентов со сниженной СКФ [252]. Вместе с тем, при установленном дефиците 25(OH)D, компенсация дефицита нативного витамина D является обязательным этапом лечения и проводится, в том числе, пациентам с терминальной стадией почечной недостаточности [253], и диабетической нефропатией [254]. Необходимо помнить, что активные метаболиты витамина D и их аналоги не определяются в значимых количествах при исследовании концентрации витамина D в сыворотке крови ввиду их структурных отличий от колекальциферола**, а также их быстрой деградации. Поэтому для контроля эффективности назначаемых доз активных метаболитов витамина D и их аналогов необходимо использовать концентрацию общего и/или ионизированного кальция, паратгормона в крови. Кроме того, эти препараты ввиду потенциальной возможности развития гиперкальциемии/гиперкальциурии могут назначаться только под врачебным контролем уровней кальция в крови и в ряде случаев в моче (при нормальной скорости клубочковой фильтрации). С осторожностью также следует назначать активные метаболиты витамина D и их аналоги одновременно с препаратами нативного витамина D, содержащими дозу колекальциферола** выше профилактической (более 800-1000 МЕ в сутки) [245].
Менопаузальная гормональная терапия (МГТ)
МГТ одобрена для профилактики постменопаузального остеопороза, облегчения вазомоторных симптомов и вульвовагинальной атрофии, ассоциированных с менопаузой [255]. Женщины, у которых не было гистерэктомии, нуждаются в МГТ, содержащей прогестагены для протекции эндометрия.
- МГТ рекомендована для профилактики остеопороза у женщин в возрасте до 60 лет с длительностью постменопаузы до 10 лет. Рекомендуется использовать наименьшие эффективные дозы МГТ: по мере увеличения возраста женщины снижать дозу препарата и проводить ежегодную оценку соотношения польза/риск в каждом конкретном случае [255-258].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2).
Комментарии: Доказательства профилактики переломов при назначении МГТ ограничены данными по пероральному применению стандартных доз конъюгированных эквинных эстрогенов (КЭЭ) и медроксипрогестерона**. В исследовании ‘The Woman’s Health Initiative (WHI)» выявили, что применение МГТ в течение пяти лет снижает риск развития переломов тел позвонков и переломов бедренной кости на 34%, а внепозвоночных переломов на 23% [255].
Хотя МГТ предотвращает переломы в любом возрасте после наступления менопаузы, важен возраст начала МГТ. В возрасте 50-60 лет, или в течение 10 лет после наступления менопаузы, преимущества МГТ с наибольшей вероятностью превосходят какой-либо риск, МГТ может рассматриваться в качестве терапии первой линии. Не следует начинать МГТ в возрасте после 60 лет. Однако отсутствуют обязательные ограничения продолжительности применения МГТ при условии, что она соответствует целям лечения [255, 257].
Имеются фактические данные о предотвращении потери МПК при пероральном (КЭЭ) и трансдермальном применении доз, которые ниже стандартных [258].
Нежелательные явления, ассоциированные с применением МГТ
Глобальное исследование МГТ (WHI) продемонстрировало повышение риска ИБС, инсульта, инвазивного рака молочной железы, ТЭЛА и тромбоза глубоких вен нижних конечностей в течение 5-ти лет лечения стандартными дозами КЭЭ и медроксипрогестерона** [256]. Однако последующий ре-анализ этих данных не подтвердил увеличения риска ИБС у женщин в возрасте до 60 лет, начавших лечение в первые 10 лет постменопаузы, в то время как повышенные риски рака молочной железы, инсульта и тромбоэмболии сохранялись, однако не были столь драматичными. Абсолютный риск инсульта, рака молочной железы у женщин моложе 60 лет был низким. В подгруппе женщин после гистерэктомии, получавших монотерапию КЭЭ в дозе 0,625 мг в сутки в возрасте до 60 лет c длительностью менопаузы до 10 лет в WHI, было отмечено снижение риска рака молочной железы (РМЖ), ИБС и общей смертности в течение 7 лет лечения [256]. Мета-анализ и данные наблюдательных исследований свидетельствуют о меньшем риске тромбоэмболии и ишемического инсульта при использовании трансдермальной МГТ [258].
Служба профилактики повторных переломов
- С целью своевременного назначения терапии остеопороза и обеспечения длительного наблюдения за пациентами 50 лет и старше с патологическими переломами для снижения риска повторных переломов рекомендуется создавать Службы профилактики повторных переломов (СППП). [35, 36, 259-266]
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: После возникновения низкоэнергетического перелома риск последующих увеличивается в 2-3 раза [267, 268]. Около 50% переломов проксимального отдела бедра происходит у лиц, получивших ранее перелом из-за остеопороза [268, 269]. При этом антиостеопоротическое лечение в рутинной практике назначается менее чем у 20% пациентов [264, 270]. В случае наблюдения таких пациентов в рамках СППП в проведенных исследованиях было показано снижение числа повторных переломов до 40% [35, 36, 259], а также снижение летальности [259, 260] и высокая экономическая эффективность [261, 262].
Для организации эффективно работающей СППП нужно учитывать следующие аспекты: 1) Клиническая и экономическая эффективность была показана только при наличии в штате СППП выделенного координатора-медсестры, обеспечивающего маршрутизацию пациентов с переломами [263]. 2) Необходимо организовать систему систематического и активного выявления всех пациентов 50 лет и старше с новыми низкоэнергетическими переломами. 3) Должно быть организовано обследование пациента (или направление на это обследование в другие медицинские учреждения) для оценки риска повторных переломов с целью выявления пациентов с высоким риском. Для этого рекомендуется использовать оценку 10-летнего абсолютного риска переломов FRAX и/или остеоденситометрию. Также требуется обеспечить обследование для поиска вторичных причин остеопороза и для оценки риска падений. Так как риск получения повторного перелома наибольший в первые месяцы после случившегося перелома, обследование рекомендуется проводиться в первые 3 месяца. 4) Обучение пациентов проводится для повышения приверженности к лечению и снижения риска падений. 5) После проведения оценок должны быть применяться медикаментозные и немедикаментозные мероприятия, включая меры по снижению риска падений. 6) Следует обеспечить длительное наблюдение за пациентом в СППП или направление для этого к врачам первичного звена или врачам-специалистам. 7) Данные обо всех пациентах, выявленных в СППП, должны поступать в базу данных. Для оптимизации оказания помощи необходимо обеспечить качество работы СППП, что включает в себя сбор данных и контроль.
Информация
Источники и литература
-
Клинические рекомендации Российской ассоциации эндокринологов
- 1. Мельниченко Г.А., Белая Ж.Е., Рожинская Л.Я., Торопцова Н.В., Алексеева Л.И., Бирюкова Е.В., Гребенникова Т.А., Дзеранова Л.К., Древаль А.В., Загородний Н.В., Ильин А.В., Крюкова И.В., Лесняк О.М, Мамедова Е.О., Никитинская О.А., Пигарова Е.А., Родионова С.С., Скрипникова И.А., Тарбаева Н.В., Фарба Л.Я., Цориев Т.Т., Чернова Т.О., Юренева С.В., Якушевская О.В., Дедов И.И.. Федеральные клинические рекомендации по диагностике, лечению и профилактике остеопороза. Проблемы Эндокринологии, 2017, Том 63, № 6, стр. 392-426
2. Camacho PM, Petak SM, Binkley N, Clarke BL, Harris ST, Hurley DL, Kleerekoper M, Lewiecki EM, Miller PD, Narula HS, Pessah-Pollack R, Tangpricha V,Wimalawansa SJ, Watts NB: American association of clinical endocrinologists and American college of endocrinology clinical practice guidelines for the diagnosis and treatment of postmenopausal osteoporosis -2016. Endocr Pract. 2016 Sep 2;22(Suppl 4):1-42.
3. Kanis JA, Cooper C, Rizzoli R, Reginster JY; Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis (ESCEO) and the Committees of Scientific Advisors and National Societies of the International Osteoporosis Foundation (IOF).European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int. 2019 Jan;30(1):3-44. doi: 10.1007/s00198-018-4704-5
4. Raman-Wilms L. Book Review: Guidelines for Preclinical Evaluation and Clinical Trials in Osteoporosis. Annals of Pharmacotherapy. 1999;33(12):1377-1378. doi:10.1177/106002809903301207.
5. American Association of Orthopedic Surgeon Position Statement, 1159, December 2009
6. Kanis JA, on behalf of the WHO Scientific Group. Assessment of osteoporosis at the primary health-care level. Technical Report. WHO Collaboraiting Centre, University of Sheffield, UK, 2008
7. Consensus development conference: diagnosis, prophylaxis, and treatment of osteoporosis. Am J Med. 1993 Jun;94(6):646-50. DOI: 10.1016/0002-9343(93)90218-e
8. Михайлов Е.Е., Беневоленская Л.И. Руководство по остеопорозу. М.: БИНОМ. Лаборатория знаний; 2003.
9. Лесняк О.М., Ершова О.Б. Аудит состояния проблемы остеопороза в странах Восточной Европы и Центральной Азии 2010. Naturaprint; 2011
10. Дедов И.И., Мельниченко Г.А., Белая Ж.Е., Рожинская Л.Я.: «Остеопороз – от редкого симптома эндокринных болезней до безмолвной эпидемии 20-21 века» Ж. Проблемы Эндокринологии, 2011, том 57, стр. 35-45
11. Ершова О.Б., Белова К.Ю., Белов М.В., Ганерт О.А., Гладкова Е.Н., Ходырев В.Н., Лесняк О.М., Давтян В.Г., Пилюкова Р.И., Романова М.А., Синицина О.С Эпидемиология переломов проксимального отдела бедренной кости у городского населения Российской Федерации: результаты многоцентрового исследования. Форум остеопороза, 23-25 сентября, 2012; Санкт-Петербург. Материалы научно-практической конференции «Остеопороз – важнейшая мультидисциплинарная проблема здравоохранения XXI века»; 23–27.
12. Меньшикова Л.В., Храмцова Н.А., Ершова О.Б. Ближайшие и отдаленные исходы переломов проксимального отдела бедра у лиц пожилого возраста и их медико-социальные последствия (по данным многоцентрового исследования). Остеопороз и остеопатии. 2002;1:8-11.
13. Добровольская О.В., Торопцова Н.В., Лесняк О.М. Экономические аспекты осложненного остеопороза: стоимость лечения в течение первого года после перелома. Современная ревматология. 2016;. т. 10. № 3. с. 29-34.
14. Бахтиярова С.А., Бортник С.Б., Лесняк О.М., Кузнецова Н.Л. Сравнительная оценка социальных последствий перелома проксимального отдела бедра и инфаркта миокарда у пациентов старшего возраста. Остеопороз и остеопатии. 2003; Приложение. Научная программа и тезисы Росс. Конгресса по остеопорозу, Москва, 20-22 октября 2003 г.- С.45
15. Lesnyak O, Ershova O, Belova K et al. Epidemiology of fracture in the Russian Federation and the development of a FRAX model. Arch Osteoporos. 2012;7(1-2):67-73. doi:10.1007/s11657-012-0082-3.
16. Cosman F, de Beur S, LeBoff M, de Beur SJ, Tanner B Clinician’s Guide to Prevention and Treatment of Osteoporosis. National Osteoporosis Foundation. 1150 17th St., NW, Suite 850, Washington, DC 20036, Release Date: April 1, 2014
17. Shepstone L, Lenaghan E, Cooper C, et al. SCOOP Study Team. Screening in the community to reduce fractures in older women (SCOOP): a randomised controlled trial. Lancet. 2018 Feb 24;391(10122):741-747. doi: 10.1016/S0140-6736(17)32640-5.
18. Turner DA, Khioe RFS, Shepstone L, et al. SCOOP Study Team. The Cost-Effectiveness of Screening in the Community to Reduce Osteoporotic Fractures in Older Women in the UK: Economic Evaluation of the SCOOP Study. J Bone Miner Res. 2018 May;33(5):845-851. doi: 10.1002/jbmr.3381.
19. Hippisley-Cox J, Coupland C (2009) Predicting risk of osteoporotic fracture in men and women in England and Wales: prospective derivation and validation of QFractures Scores. Br Med J 339: b4229
20. Hoff M, Meyer HE, Skurtveit S et al (2017) Validation of FRAX and the impact of self-reported falls among elderly in a general population: the HUNT study, Norway. Osteoporos Int 28:2935–2944
21. Fraser L-A, Langsetmo L, Berger C et al (2011) Fracture prediction and calibration of a Canadian FRAX® tool: a population-based report from CaMos. Osteoporos Int 22:829–837
22. Leslie WD, Lix LM, Johansson H et al (2010) Manitoba bone density program. Independent clinical validation of a Canadian FRAX((R)) tool: fracture prediction and model calibration. J Bone Miner Res 25:2350–2358
23. Jiang X, Gruner M, Trémollieres F, Pluskiewicz W, Sornay-Rendu E, Adamczyk P, Schnatz PF. Diagnostic accuracy of FRAX in predicting the 10-year risk of osteoporotic fractures using the USA treatment thresholds: A systematic review and meta-analysis. Bone. 2017 Jun;99:20-25. doi: 10.1016/j.bone.2017.02.008.
24. Marques A, Ferreira RJ, Santos E, Loza E, Carmona L, da Silva JA. The accuracy of osteoporotic fracture risk prediction tools: a systematic review and meta-analysis. Ann Rheum Dis. 2015 Nov;74(11):1958-67. doi: 10.1136/annrheumdis-2015-207907
25. Kanis J, Johnell O, Oden A, Johansson H, McCloskey E. FRAX™ and the assessment of fracture probability in men and women from the UK. Osteoporosis International. 2008;19(4):385-397. doi:10.1007/s00198-007-0543-5
26. Lindsay R, Silverman SL, Cooper C, Hanley DA, Barton I, Broy SB, et al. Risk of new vertebral fracture in the year following a fracture. JAMA. 2001;285:320-323
27. Gehlbach S, Saag KG, Adachi JD, Hooven FH, Flahive J, Boonen S, et al. Previous fractures at multiple sites increase the risk for subsequent fractures: the Global Longitudinal Study of Osteoporosis in Women. J Bone Miner Res. 2012;27:645-653,
28. Edwards BJ, Bunta AD, Simonelli C, Bolander M, Fitzpatrick LA. Prior fractures are common in patients with subsequent hip fractures. Clin Orthop Relat Res. 2007;461:226-230
29. Ross P. Pre-Existing Fractures and Bone Mass Predict Vertebral Fracture Incidence in Women. Annals of Internal Medicine. 1991;114(11):919. doi:10.7326/0003-4819-114-11-919.
30. Gallagher J, Genant H, Crans G, Vargas S, Krege J. Teriparatide Reduces the Fracture Risk Associated with Increasing Number and Severity of Osteoporotic Fractures. The Journal of Clinical Endocrinology & Metabolism. 2005;90(3):1583-1587. doi:10.1210/jc.2004-082631. Marcus R, Wang O, Satterwhite J, Mitlak B. The Skeletal Response to Teriparatide Is Largely Independent of Age, Initial Bone Mineral Density, and Prevalent Vertebral Fractures in Postmenopausal Women With Osteoporosis. J Bone Miner Res. 2003;18(1):18-23. doi:10.1359/jbmr.2003.18.1.18.
32. Kanis JA, Barton I, Johnell O. Risedronate decreases fracture risk in patients selected solely on the basis of prior vertebral fracture. Osteoporos Int 2005; 16: 475–82,
33. Johnell O, Kanis JA, Black DM, et al. Association between baseline risk factors and vertebral fracture risk in the Multiple Outcomes of Raloxifene Evaluation (MORE) study. J Bone Miner Res 2004; 19: 64–72,
34. Kanis JA, Jonsson B, Oden A, McCloskey EV. A metaanalysis of the effect of strontium ranelate on the risk of vertebral and non-vertebral fracture in postmenopausal osteoporosis and the interaction with FRAX. Osteoporos Int 2011; 22: 2347–55.
35. Kanis J.A., Johnell O., De Laet C., et al. A meta-analysis of previous fracture and subsequent fracture risk. Bone 2004; 35(2): 375-82.
36. Klotzbuecher C.M., Ross P.D., Landsman P.B., et al. Patients with prior fractures have an increased risk of future fractures: a summary of the literature and statistical synthesis. J Bone Mineral Research 2000; 15(4): 721-39.
37. Schousboe J, Ensrud K, Nyman J, Kane R, Melton L. Potential cost-effective use of spine radiographs to detect vertebral deformity and select osteopenic post-menopausal women for amino-bisphosphonate therapy. Osteoporosis International. 2005;16(12):1883-1893. doi:10.1007/s00198-005-1956-7
38. Gallagher JC, Sai AJ. Bone: Is screening for secondary causes of osteoporosis worthwhile? Nat Rev Endocrinol. 2010;6:360-362
39. Barzel US. Recommended testing in patients with low bone density. J Clin Endocrinol Metab. 2003;88:1404- 1405
40. Tannenbaum C, Clark J, Schwartzman K, Wallenstein S, Lapinski R, Meier D, et al. Yield of laboratory testing to identify secondary contributors to osteoporosis in otherwise healthy women. J Clin Endocrinol Metab. 2002;87: 4431-4437
41. Cerdá Gabaroi, D. et al. search for hidden secondary causes in postmenopausal women with osteoporosis. Menopause 17, 135–139 (2010)
42. Deutschmann, H. A. et al. search for occult secondary osteoporosis: impact of identified possible risk factors on bone mineral density. J. Intern. Med. 252, 389–397 (2002)
43. Priemel, M. et al. Bone mineralization defects and vitamin D deficiency: histomorphometric analysis of iliac crest bone biopsies and circulating 25-hydroxyvitamin D in 675 patients. J. Bone Miner. Res. 25, 305–312 (2009)
44. Eastell R, Barton I, Hannon RA, Chines A, Garnero P, Delmas PD. Relationship of early changes in bone resorption to the reduction in fracture risk with risedronate. J Bone Miner Res. 2003;18:1051-1056
45. Hochberg M.C., Greenspan S., Wasnich R.D. et al. Changes in bone density and turnover explain the reductions in incidence of nonvertebral fractures that occur during treatment with antiresorptive agents. J. Clin. Endocrinol. Metabol. 2002;87(4):1586–1592. doi: 10.1210/ jcem.87.4.8415
46. Bone H.G., Hosking D., Devogelaer J.P. et al. Ten years’ experience with alendronate for osteoporosis in postmenopausal women. New Engl. J. Med. 2004;350(12):1189–99. doi: 10.1056/NEJMoa030897.
47. Black D.M., Schwartz A.V., Ensrud K.E. et al. Effects of continuing or stopping alendronate after 5 years of treatment: the Fracture Intervention Trial Long-term Extension (FLEX): a randomized tri- al. J. Am. Med. Association. 2006;296(24):2927–38. doi: 10.1001/ jama.296.24.2927
48. Delmas PD, Eastell R, Garnero P, Seibel MJ, Stepan J (2000) The use of biochemical markers of bone turnover in osteoporosis. Committee of Scientific Advisors of the International Osteoporosis Foundation. Osteoporos Int 11(Suppl 6):S2–1749. Vasikaran S, Eastell R, Bruyère O, Foldes AJ, Garnero P, Griesmacher A, McClung M, Morris HA, Silverman S, Trenti T, Wahl DA, Cooper C, Kanis JA (2011) Markers of bone turnover for the prediction of fracture risk and monitoring of osteoporosis treatment: a need for international reference standards. Osteoporos Int 22:391–420
50. Johansson H, Odén A, Kanis JA, McCloskey EV, Morris HA, Cooper C, Vasikaran S (2014) A meta-analysis of reference markers of bone turnover for prediction of fracture. Calcif Tissue Int 94:560–567
51. Bauer DC, Black DM, Bouxsein ML, Lui LY, Cauley JA, de Papp AE, Grauer A, Khosla S, McCulloch CE, Eastell R; Foundation for the National Institutes of Health (FNIH) Bone Quality Project. Treatment-Related Changes in Bone Turnover and Fracture Risk Reduction in Clinical Trials of Anti-Resorptive Drugs: A Meta-Regression. J Bone Miner Res. 2018 Apr;33(4):634-642. doi: 10.1002/jbmr.3355. Epub 2018 Jan 10.
52. Ravn P, Hosking D, Thompson D et al. Monitoring of Alendronate Treatment and Prediction of Effect on Bone Mass by Biochemical Markers in the Early Postmenopausal Intervention Cohort Study1. The Journal of Clinical Endocrinology & Metabolism. 1999;84(7):2363-2368. doi:10.1210/jcem.84.7.5847.
53. Fink E, Cormier C, Steinmetz P, Kindermans C, Le Bouc Y, Souberbielle J. Differences in the Capacity of Several Biochemical Bone Markers to Assess High Bone Turnover in Early Menopause and Response to Alendronate Therapy. Osteoporosis International. 2000;11(4):295-303. doi:10.1007/pl00004183.
54. Bauer D, Black D, Garnero P et al. Change in Bone Turnover and Hip, Non-Spine, and Vertebral Fracture in Alendronate-Treated Women: The Fracture Intervention Trial. J Bone Miner Res. 2004;19(8):1250-1258. doi:10.1359/jbmr.040512.
55. Delmas P, Recker R, Chesnut C et al. Daily and intermittent oral ibandronate normalize bone turnover and provide significant reduction in vertebral fracture risk: results from the BONE study. Osteoporosis International. 2004;15(10). doi:10.1007/s00198-004-1602-9.
56. Reginster J, Gieschke R. Clinical Utility of a Pharmacostatistical Model for Ibandronate in Postmenopausal Osteoporosis. CDM. 2006;7(7):827-836. doi:10.2174/138920006778520624.
57. Krege J, Lane N, Harris J, Miller P. PINP as a biological response marker during teriparatide treatment for osteoporosis. Osteoporosis International. 2014;25(9):2159-2171. doi:10.1007/s00198-014-2646-0.
58. Imaz I, Zegarra P, González-Enríquez J, Rubio B, Alcazar R, Amate J. Poor bisphosphonate adherence for treatment of osteoporosis increases fracture risk: systematic review and meta-analysis. Osteoporosis International. 2009;21(11):1943-1951. doi:10.1007/s00198-009-1134-4.
59. Bergmann P, Body J, Boonen S et al. Evidence-based guidelines for the use of biochemical markers of bone turnover in the selection and monitoring of bisphosphonate treatment in osteoporosis: a consensus document of the Belgian Bone Club. International Journal of Clinical Practice. 2009;63(1):19-26. doi:10.1111/j.1742-1241.2008.01911.x.
60. Burch J, Rice S, Yang H et al. Systematic review of the use of bone turnover markers for monitoring the response to osteoporosis treatment: the secondary prevention of fractures, and primary prevention of fractures in high-risk groups. Health Technology Assessment. 2014;18(11). doi:10.3310/hta18110.
61. Dresner-Pollak R, Parker R, Poku M, Thompson J, Seibel M, Greenspan S. Biochemical Markers of Bone Turnover Reflect Femoral Bone Loss in Elderly Women. Calcified Tissue International. 1996;59(5):328-333. doi:10.1007/s002239900135.
62. Ross PKnowlton W. Rapid Bone Loss Is Associated with Increased Levels of Biochemical Markers. J Bone Miner Res. 1998;13(2):297-302. doi:10.1359/jbmr.1998.13.2.297.
63. Hansen MA, Overgaard K, Riis BJ et al. Role of peak bone mass and bone loss in postmenopausal osteoporosis: 12 year study. BMJ 1991; 303: 961–4
- 1. Мельниченко Г.А., Белая Ж.Е., Рожинская Л.Я., Торопцова Н.В., Алексеева Л.И., Бирюкова Е.В., Гребенникова Т.А., Дзеранова Л.К., Древаль А.В., Загородний Н.В., Ильин А.В., Крюкова И.В., Лесняк О.М, Мамедова Е.О., Никитинская О.А., Пигарова Е.А., Родионова С.С., Скрипникова И.А., Тарбаева Н.В., Фарба Л.Я., Цориев Т.Т., Чернова Т.О., Юренева С.В., Якушевская О.В., Дедов И.И.. Федеральные клинические рекомендации по диагностике, лечению и профилактике остеопороза. Проблемы Эндокринологии, 2017, Том 63, № 6, стр. 392-426
Информация
Список сокращений
БФ – бифосфонат
ВОЗ – Всемирная организация здравоохранения
ГКО — глюкокортикоидный остеопороз
ГнРГ — гонадотропин-рилизинг гормон
ДИ – доверительный интервал
ИБС – ишемическая болезнь сердца
ККТ — количественная компьютерная томография
КТ — компьютерная томография
КЭЭ — конъюгированные эквинные эстрогены
МГТ — менопаузальная гормональная терапия
МПК — минеральная плотность кости
МРТ — магнитно-резонансная томография
ОР – относительный риск
ОРИТ – отделение реанимации и интенсивной терапии
ПТГ — паратиреоидный гормон
РКИ – рандомизированное клиническое исследование
СД – сахарный диабет
СКФ – скорость клубочковой фильтрации
СОЭ – скорость оседания эритроцитов
СППП — служба профилактики повторных переломов
ТКИ (TBS) — трабекулярный костный индекс (trabecular bone score)
ТЭЛА – тромбоэмболия легочной артерии
BMC – костный минеральный компонент
BUA — широкополосное ослабление ультразвука
CTX — С-концевой телопептид коллагена 1 типа
DXA — двухэнергетическая рентгеновская абсорбциометрия
FRAX – алгоритм оценки индивидуальной 10-летней вероятности переломов
ISCD — международное общество по клинической денситометрии
P1NP – N-терминальный пропептид проколлагена 1-го типа
QUS — количественная ультразвуковая денситометрия
RANKL — рецептор лиганда ядерного фактора капа-бета
SD – стандартное отклонение
SOS — скорость ультразвука
SPEP — электрофорез белков в сыворотке крови
UPEP — электрофорез белков
WHI — The Woman’s Health Initiative (наименование исследования)
** — препарат введен в список жизненно-важных средств
Термины и определения
Вторичный остеопороз – это остеопороз, который развивается вследствие серьезной сопутствующей соматической патологии (в том числе, эндокринных заболеваний) или приема лекарственных средств [1-3].
Минимальная травма — падение с высоты собственного роста на ту же поверхность или еще меньшая травма [4, 5].
Патологический или низкотравматический (низкоэнергетический), или остеопоротический перелом — перелом, произошедший при минимальной травме, в подавляющем большинстве случаев вследствие остеопороза. Термин патологический перелом также используется для описания перелома вследствие заболевания, а не травматического воздействия, например, перелом у пациентов с метастатическим поражением скелета, перелом вследствие болезни Педжета и т.д. Перелом вследствие остеопороза можно отнести к патологическому перелому, и этот термин используется в МКБ 10 и 11 пересмотров, поэтому далее для унификации будет использоваться термин «патологический перелом» [6].
Первичный остеопороз – это остеопороз, который развивается как самостоятельное заболевание [1,2].
Тяжелый остеопороз – это остеопороз с уже имеющимся в анамнезе патологическим переломом: тела позвонка(ов), переломом бедренной кости или множественными переломами независимо от степени снижения минеральной плотности кости (МПК) по данным рентгеноденситометрии.
Остеопороз, осложненный патологическим переломом, — это остеопороз, осложненный патологическим переломом любой локализации, исключая переломы фаланг пальцев и костей черепа, которые не являются следствием остеопороза [3].
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Белая Ж.Е., д.м.н., заведующая отделением нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; член общественной организации «Российская ассоциация эндокринологов», член общественной организации «Российская ассоциация по остеопорозу»
Белова К.Ю. д.м.н., заведующая областным лечебно-диагностическим центром остеопороза и остеоартроза ГАУЗ ЯО «Клиническая больница скорой медицинской помощи им. Н. В. Соловьева»; доцент кафедры терапии имени профессора Е.Н. Дормидонтова Ярославского государственного медицинского университета, член общества пациентов с остеопорозом «Остеорус», член президиума общественной организации «Российская ассоциация по остеопорозу», член общероссийской общественной организации «Ассоциация ревматологов России».
Бирюкова Е.В., д.м.н., профессор кафедры эндокринологии и диабетологии лечебного факультета ФГБОУ ВО «МГМСУ им. А.И. Евдокимова» Минздрава России; член общественной организации «Российская ассоциация эндокринологов»
Дедов И.И., д.м.н., академик РАН, президент ФГБУ «НМИЦ эндокринологии» Минздрава России, президент общественной организации «Российская ассоциация эндокринологов», главный внештатный специалист-эксперт эндокринолог Министерства здравоохранения России
Дзеранова Л.К., д.м.н., главный научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; член общественной организации «Российская ассоциация эндокринологов»
Драпкина О.М., д.м.н., профессор, член-корреспондент РАН, директор ФГБУ «Национальный медицинский исследовательский центр профилактической медицины» Минздрава России, президент Российского общества профилактики неинфекционных заболеваний, президент Национального общества усовершенствования врачей им. С.П. Боткина, президент Ассоциации врачей общей практики (семейных врачей) России, президент Национальной ассоциации биобанков
Древаль АВ, д.м.н. профессор, доктор медицинских наук, заведующий кафедрой клинической эндокринологии ФУВ МОНИКИ, руководитель отделения терапевтической эндокринологии Московского областного научно-исследовательского клинического института (МОНИКИ) им.М.Ф.Владимирского, главный эндокринолог Московской области
Дубовицкая Т.А., к.м.н., старший научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом профессиональной ассоциации
Дудинская Е.Н., к.м.н., заведующая лаборатории возрастных метаболических и эндокринных нарушений обособленного структурного подразделения — Российский геронтологический научно-клинический центр федерального государственного автономного образовательного учреждения высшего образования «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации; член общественной организации «Российская ассоциация эндокринологов», член общественной организации «Российская ассоциация по остеопорозу»
Ершова О.Б., д.м.н., профессор кафедры терапии имени профессора Е.Н. Дормидонтова Ярославского государственного медицинского университета; руководитель общества пациентов с остеопорозом «Остеорус», вице-президент общественной организации «Российская ассоциация по остеопорозу», член общероссийской общественной организации «Ассоциация ревматологов России».
Загородний Н.В., д.м.н, профессор, член-корр. РАН, и.о. директора ФГБУ «НМИЦ ТО им. Н.Н. Приорова» Минздрава России, Москва; член общероссийской общественной организации «Ассоциация травматологов-ортопедов России»
Илюхина О.Б., главный внештатный эндокринолог Оренбургской области, заведующая отделением эндокринологии ГАУЗ Оренбургская областная клиническая больница №2, Оренбург; член общественной организации «Российская ассоциация эндокринологов»
Kanis JA, международный консультант, профессор, директор Центра метаболических заболеваний костей Университета Шеффилд, Великобритания, профессор Католического университета Австралии (Мельбурн), почетный президент Международного фонда остеопороза (президент IOF с 2008 по 2017 год), член его научного комитета IOF, председатель рабочей группы IOF по эпидемиологии и качеству жизни.
Крюкова И.В., к.м.н., доцент кафедры эндокринологии ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва; не является членом профессиональной ассоциации
Лесняк О.М., д.м.н., президент Российской Ассоциации по остеопорозу, профессор кафедры семейной медицины ГБОУ ВПО «Северо-Западный государственный медицинский университет имени И.И.Мечникова» Минздрава России, Санкт-Петербург; президент общественной организации «Российская ассоциация по остеопорозу»; член общероссийской общественной организации «Ассоциация ревматологов России»
Мамедова Е.О., к.м.н., старший научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом профессиональной ассоциации
Марченкова Л.А., к.м.н., ведущий научный сотрудник, заведующая отделением реабилитации пациентов с соматическими заболеваниями, заведующая отделом соматической реабилитации, репродуктивного здоровья и активного долголетия ФГБУ «НМИЦ РК» Минздрава РФ, член президиума общественной организации «Российская ассоциация по остеопорозу», член общественной организации «Российская ассоциация эндокринологов»
Мельниченко Г.А., д.м.н., академик РАН, директор Института клинической эндокринологии ФГБУ «НМИЦ эндокринологии» Минздрава России, председатель Московской ассоциации эндокринологов, вице-президент общественной организации «Российская ассоциация эндокринологов»
Никанкина Л.В., к.м.н., и.о. заведующей Клинико-диагностической лабораторией ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом профессиональной ассоциации
Никитинская О.А., к.м.н., старший научный сотрудник лаборатории остеопороза отдела метаболических заболеваний костей и суставов ФГБНУ НИИ Ревматологии им. В.А. Насоновой, Москва; генеральный секретарь общественной организации «Российская ассоциация по остеопорозу»; член общероссийской общественной организации «Ассоциация ревматологов России»
Петряйкин А.В, к.м.н., доцент, старший научный сотрудник ГБУЗ города Москвы «Научно-практический клинический центр диагностики и телемедицинских технологий Департамента здравоохранения города Москвы», член «Российского общества рентгенологов и радиологов»
Пигарова Е.А., к.м.н., ведущий научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; член общественной организации «Российская ассоциация эндокринологов»
Родионова С.С., д.м.н., профессор, руководитель научно-клинического центра остеопороза ФГБУ «НМИЦ ТО им. Н.Н. Приорова» Минздрава России, Москва; член президиума общественной организации «Российская ассоциация по остеопорозу»
Рожинская Л.Я., д.м.н., профессор, главный научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; член президиума общественной организации «Российская ассоциация по остеопорозу», член общественной организации «Российская ассоциация эндокринологов»
Скрипникова И.А., д.м.н, руководитель отдела профилактики остеопороза ФГБУ «Национальный медицинский исследовательский центр профилактической медицины» Минздрава России, Москва; член президиума общественной организации «Российская ассоциация по остеопорозу»
Тарбаева Н.В., к.м.н., врач-рентгенолог отдела лучевой диагностики ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом профессиональной ассоциации
Ткачева О.Н., д.м.н., профессор, директор обособленного структурного подразделения — Российский геронтологический научно клинический центр федерального государственного автономного образовательного учреждения высшего образования «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Министерства здравоохранения Российской Федерации, главный внештатный гериатр Минздрава России; президент общероссийской общественной организации «Российская ассоциация геронтологов и гериатров»
Торопцова Н.В., д.м.н., заведующая лабораторией остеопороза отдела метаболических заболеваний костей и суставов ФГБНУ НИИ Ревматологии им. В.А. Насоновой, Москва; член президиума общественной организации «Российская ассоциация по остеопорозу», член общероссийской общественной организации «Ассоциация ревматологов России»
Фарба Л.Я., врач-травматолог-ортопед ГБУЗ «Городская клиническая больница № 13 Департамента здравоохранения города Москвы», Москва; заместитель председателя член общероссийской общественной организации «Ассоциация травматологов-ортопедов России»
Цориев Т.Т., научный сотрудник отделения нейроэндокринологии и остеопатий ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом
профессиональной ассоциации
Чернова Т.О., к.м.н., ведущий научный сотрудник отдела лучевой диагностики ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва; не является членом профессиональной ассоциации
Юренева С.В., д.м.н., ведущий научный сотрудник отделения гинекологической эндокринологии ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, Москва; член президиума общественной организации «Российская ассоциация по остеопорозу»; член общественной организации «Российская ассоциация по менопаузе»
Якушевская О.В., к.м.н., научный сотрудник отделения гинекологической эндокринологии ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, Москва; член
общественной организации «Российская ассоциация по менопаузе»
Конфликт интересов: авторы, эксперты и рецензенты не имели конфликта интересов при разработке данных клинических рекомендаций.
Приложение А2. Методология разработки клинических рекомендаций
Клинические рекомендации по оказанию медицинской помощи пациентам с остеопорозом составлены в соответствии с требованиями о разработке клинических рекомендаций медицинскими профессиональными некоммерческими организациями, часть 2 статьи 76 Федерального закона от 21.11.2011г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», приказом Министерства здравоохранения Российской Федерации №103н от 28.02.2019г. «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации». Клинические рекомендации основаны на доказательном клиническом опыте, описывающем действия врача, по диагностике, дифференциальной диагностике, лечению, реабилитации и профилактике остеопороза у женщин в постменопаузе и у мужчин старше 50 лет.
Целевая аудитория данных клинических рекомендаций:
1. Врачи-эндокринологи;
2. Врачи-ревматологи;
3. Врачи-травматологи-ортопеды;
4. Врачи-терапевты;
5. Врачи общей практики (семейные врачи);
6. Врачи-нефрологи;
7. Врачи-акушеры-гинекологи;
8. Врачи-неврологи;
9. Врачи других специальностей, занимающихся диагностикой и ведением пациентов с остеопорозом.
Медицинским работникам следует придерживаться данных рекомендаций в процессе принятия клинических решений. В то же время, рекомендации не заменяют личную ответственность медицинских работников при принятии клинических решений с учетом индивидуальных особенностей пациентов и их пожеланий. Настоящие рекомендации учитывают накопленный российский и международный опыт ведения пациентов с остеопорозом и базируются на клинических рекомендациях, опубликованных Российской Ассоциацией Остеопороза [1] 2010, клинических рекомендациях Американской Ассоциации клинических эндокринологов 2016 [2], Европейских клинических рекомендациях по диагностике и лечению остеопороза у женщин в менопаузе, международного фонда остеопороза IOF 2013 [3] и Клинических рекомендациях национального фонда остеопороза США, 2014 [16].
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами. Экспертов просили прокомментировать, в том числе, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций. Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался и вносимые в результате этого изменения регистрировались в рекомендациях.
Проект клинических рекомендаций был представлен на обсуждение широкому кругу специалистов в рамках Bone Health Tеle Echo 27 ноября 2018 года и Всероссийского конгресса эндокринологов 25 мая 2019 года.
Таким образом, проект клинических рекомендаций обсуждался среди специалистов профессорско-преподавательского состава, организаторов здравоохранения в области эндокринологии и практических врачей, занимающихся проблемами остеопороза.
Шкалы оценки уровней достоверности доказательств (УДД) для методов диагностики, профилактики, лечения и реабилитации (диагностических, профилактических, лечебных, реабилитационных вмешательств) и шкала оценки уровне убедительности рекомендаций (УРР) для методов профилактики, диагностики, лечения и реабилитации (диагностических, профилактических, лечебных, реабилитационных вмешательств) представлены в Приложении А2-1, А2-2 и А2-3, соответственно.
Приложение А2-1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Приложение А2-2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Приложение А2-3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
Приложение А3.1 Характеристика лекарственных препаратов для лечения остеопороза
Примечания: L1-L4 – поясничный отдел позвоночника, Neck – шейка бедренной кости
* – кроме случаев, оговоренных/указанных в столбце 1
1 — Историческая справка, в превоначальных регистрационных исследованиях использовались алендроновая кислота в дозе 5 -10 мг для ежедневного применения, ризендроновая кислота 5 мг для ежедневного применения, ибандроновая кислота 2,5 мг для ежедневного применения и ибандроновая кислота 20 мг внутривенно через день по 12 доз каждые 3 месяца
2 – 4,2-летнее исследование
3 – МПК скорректирована по популяции NHANES, для препаратов входит в список ЖНВЛП
4 – 20-месячное исследование
Бифосфонаты (БФ)
Механизм действия
БФ представляют собой аналоги неорганических пирофосфатов, в которых атом кислорода заменён на атом углерода, что делает молекулу более стабильной. Химическая связь P-C-P не разлагается энзиматически, вследствие чего в организме человека не образуется промежуточных метаболитов, молекула выводится неизмененной почками, поэтому важно учитывать скорость клубочковой фильтрации. При костной резорбции остеокласт захватывает БФ, наиболее вероятно, вместе с кальцием и костным матриксом [272]. Нитроген-содержащий БФ связывается с ферментом фарнезилпирофосфат-синтазой, что блокирует синтез фарнезилдифосфата, необходимого для образования гераннил-геранил-дифосфата. Вследствие этого останавливается модификация сигнальных белков важных для нормальной функции остеокласта. Таким образом, ухудшается работа остеокласта, уменьшается резорбтивная поверхность, что в дальнейшем может приводить к апоптозу [273].
Алендроновая кислота**
Показания к применению: постменопаузальный остеопороз, остеопороз у мужчин, ГКО.
Противопоказания к применению: стриктура пищевода, ахалазия, неспособность больного стоять или сидеть прямо по крайней мере 30 мин после приема препарата, гипокальциемия, повышенная чувствительность к алендроновой кислоте.
Режим назначения: Препарат выпускается в таблетках по 70 мг. Принимается перорально 1 раз в 7 дней перорально. Алендроновая кислота** должна быть принята утром натощак за 30 мин до еды, их необходимо запивать стаканом простой воды. После приема таблетки важно сохранять вертикальное положение тела в течение 30-40 минут для предупреждения гастроэзофагеального рефлюкса, нельзя принимать пищу или жидкость, кроме простой воды.
Ибандроновая кислота
Показания к применению: постменопаузальный остеопороз.
Противопоказания к применению. Для всех лекарственных форм: повышенная чувствительность к ибандроновой кислоте или другим компонентам препарата; гипокальциемия. Для раствора для в/в введения: беременность; период кормления грудью, тяжелое нарушение функции почек (креатинин сыворотки крови >200 мкмоль/л (2,3 мг/дл) или клиренс креатинина <30 мл/мин). С осторожностью (для таблеток) — тяжелое нарушение функции почек (клиренс креатинина <30 мл/ мин).
Режим назначения: Препарат выпускается в таблетках по 150 мг и растворах для инъекции 3 мг в 3 мл. Таблетированную ибандроноваю кислоту следует принимать с частотой 1 раз в месяц, утром натощак, запивая стаканом простой воды. После приема препарата необходимо сохранять вертикальное положение тела и воздержаться от приема пищи и других лекарственных препаратов в течение 60 мин. Ибандроновая кислота в форме 3 мг в 3 мл шприце вводится внутривенно в течение 15-30 секунд с частотой 1 раза в 3 месяца.
Ризедроновая кислота
Показания к применению: постменопаузальный остеопороз, остеопороз у мужчин, ГКО.
Противопоказания к применению: стриктура пищевода, ахалазия, неспособность больного стоять или сидеть прямо по крайней мере 30 мин после приема препарата, гипокальциемия, повышенная чувствительность к ризедроновой кислоте.
Режим назначения: Препарат выпускается в таблетках по 35 мг. Принимается перорально 1 раз в 7 дней перорально. Ризедроновая кислота должна быть принята утром натощак за 30 мин до еды, их необходимо запивать стаканом простой воды. После приема таблетки важно сохранять вертикальное положение тела в течение 30-40 минут для предупреждения гастроэзофагеального рефлюкса, нельзя принимать пищу или жидкость, кроме простой воды.
Золедроновая кислота**
Показания к применению: постменопаузальный остеопороз, остеопороз у мужчин, ГКО, профилактика постменопаузального остеопороза (у пациенток с остеопенией), профилактика новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости.
Противопоказания к применению: повышенная чувствительность к золедроновой кислоте, другим БФ и другим компонентам препарата, беременность, период лактации, детский и подростковый возраст до 18 лет, тяжелые нарушения минерального обмена, включая гипокальциемию; тяжелые нарушения функции почек (клиренс креатинина <30 мл/мин).
Режим назначения: Препарат выпускается во флаконах 5мг/100 мл. Вводится внутривенно с помощью клапанной инфузионной системы, обеспечивающей постоянную скорость инфузии, в течение не менее 15 мин. Для лечения остеопороза частота введения – 1 раз в год, для профилактики – 1 раз в 2 года.
Нежелательные явления со стороны желудочного тракта (трудности при глотании, эзофагит и гастрит) встречаются при применении пероральных препаратов из группы БФ, внутривенные БФ не оказывают влияния на желудочно-кишечный тракт. Все БФ выводятся в неизмененном виде почками и противопоказаны пациентам с СКФ ниже 30-35 мл/мин. Для выявления пациентов группы риска необходимо контролировать уровень креатинина крови до начала лечения [274]. Для внутривенных БФ характерна гриппоподобная реакция (возможно развитие реакции и при приеме таблетированных препаратов, но реже) в ответ на введение препарата. Так, по данным клинического исследования гриппоподобная реакция (повышение температуры тела, артралгии, миалгии, слабость и т.д.) наблюдалась в 32% случаев после первого введения золедроновой кислоты**, в 7% после второй инфузии и в 2% после третьего введения. Данные симптомы, как правило, исчезают спустя 3 дня после введения БФ [274]. Прием нестероидных противовоспалительных средств (ибупрофена, парацетамола) облегчает симптомы гриппоподобной реакции.
На фоне длительного применения БФ для лечения остеопороза были зарегистрированы случаи остеонекроза челюсти. Данное осложнение более распространено при лечении онкологических заболеваний, при введении высоких доз БФ. Риск развития остеонекроза челюсти при лечении остеопороза увеличивается, если продолжительность терапии БФ составляет более пяти лет [275]. К редким осложнениям при длительном лечении БФ (более пяти лет) относятся патологические атипичные переломы бедренной кости. Часто таким переломам предшествует боль в области бедра и паха, которая может быть двусторонней. При подозрении на атипичный перелом бедренной кости необходимо выполнить рентгенографическое исследование обеих бедренных костей, при необходимости МРТ [190]. В некоторых случаях при атипичном переломе бедренной кости требуется хирургическое вмешательство, но чаще придерживаются консервативной тактики. При возникновении таких переломов необходимо прекратить лечение БФ.
Моноклональное антитело к лиганду рецептора ядерного фактора каппа-бета (RANKL) — деносумаб**.
Деносумаб** – человеческое антитело к RANKL [155, 156]. Препарат вмешивается в механизм привлечения активного остеокласта действуя по аналогии с остеопротегерином, который в естественных условиях, блокируя RANKL, препятствует его взаимодействию с рецептором ядерного фактора каппа-бета (RANK) и, таким образом, уменьшает привлечение зрелых остеокластов.
В отличие от БФ — деносумаб** уменьшает образование остеокластов, а не нарушает функцию зрелых клеток. Кроме того, будучи биологическим препаратом деносумаб** не накапливается в костной ткани и не оказывает отсроченного влияния с полным обратным развитием эффекта после отмены лечения [157].
Показания к применению:
— постменопаузальный остеопороз;
— остеопороз у мужчин;
— ГКО;
— предупреждение потери костной массы и переломов при отсутствии костных метастазов у женщин, получающих терапию ингибиторами ароматазы по поводу рака молочной железы и у мужчин с раком предстательной железы, получающим гормон-депривационную терапию [153-158].
Безопасность применения деносумаба**
По результатам трёхлетнего исследования с участием 7868 человек препарат продемонстрировал хороший профиль безопасности. Статистически значимо чаще у пациентов, получавших деносумаб**, наблюдалась экзема (118 чел. — 3% по сравнению с 65 чел. – 1,7% в группе плацебо), метеоризм (84 чел. – 2,2% по сравнению с 53 чел. 1,4% плацебо), воспаление подкожной жировой клетчатки (в том числе рожистое воспаление) 12 человек (0,3%) по сравнению 1 человеком (<0,1%) в группе плацебо [155]. Деносумаб** может способствовать развитию гипокальцемии, поэтому важно компенсировать дефицит витамина D до начала лечения и обеспечить достаточное поступление кальция.
Остеонекроз нижней челюсти на фоне терапии деносумабом** развивается крайне редко и встречается при лечении пациентов, страдающих онкологическими заболеваниями с метастатическим поражением скелета (при более высоких дозах препарата). Атипичные переломы бедренной кости редко ассоциированы с применением деносумаба**.
Польза от лечения деносумабом** значимо превосходит риски редких нежелательных эффектов.
Противопоказания и ограничения терапии деносумабом**
Гипокальциемия, повышенная чувствительность к препарату. Беременность или кормление грудью.
Режим назначения деносумаба**
Для лечения остеопороза деносумаб** вводится подкожно в дозе 60 мг каждые 6 месяцев. Препарат выпускается в шприце с предварительно набранной дозой.
Терипаратид**
Терипаратид** (генноинженерный фрагмента молекулы паратгормона (1-34 ПТГ)) относится к анаболической терапии остеопороза. Под анаболическим эффектом, в данном случае, понимается преимущественное действие на остеобласт, повышение продолжительности жизни костеобразующих клеток, уменьшение их апоптоза, увеличение дифференцировки мезенхимальной стволовой клетки по направлению к остеобласту (через Wnt сигнал), и, таким образом, усиление костеобразования в каждом цикле костного ремоделирования, а также активации моделирования в отдельных участках скелета, что доказано у человека по результатам костных биопсий [276, 277].
Режим назначения
Подкожные инъекции в дозе 20 мкг 1 раз в сутки, ежедневно. Терипаратид** выпускается в стеклянном картридже, который укреплён в одноразовую ручку, рассчитанную для введения 28 доз. Хранить препарат необходимо в холодильнике, однако в течение несколько часов (до 36 часов), возможно, пребывание при комнатной температуре.
Показания к применению:
— постменопаузальный остеопороз;
— остеопороз у мужчин;
— ГКО.
Нежелательные явления
Наиболее частые нежелательные явления (менее 10% испытуемых) были головокружение и судороги в ногах [176, 278]. Умеренная транзиторная гиперкальциемия (менее 2,8ммоль/л) была зарегистрирована у 2% группы контроля после иньекции, 11% — у пациентов, получавших 20 мкг терипаратида** [176]. Увеличение уровня кальция обычно наблюдалось через 4-6 часов после инъекции и полностью нормализовалось через 24 часа.
Увеличение кальциурии отличалось недостоверно от группы контроля и не ассоциировалось с увеличением риска мочекаменной болезни. Антитела к терипаратиду** были обнаружены у 3-8% женщин, но со временем их содержание уменьшилось, и они не оказали никакого эффекта на МПК или уровень кальция.
Применение терипаратида** у пациентов с умеренным снижением скорости клубочковой фильтрации (30-49 мл/мин) приводило к увеличению мочевой кислоты в сыворотке крови, но это не сочеталось с увеличением риска подагры, артралгией или камнеобразования в почках [279].
Противопоказания и ограничения
Гиперкальциемия, первичный гиперпаратиреоз, болезнь Педжета, необъяснимое повышение щелочной фосфатазы, остеогенная саркома, незакрытые зоны роста, облучение скелета в анамнезе, беременность или кормление грудью, злокачественные новообразования костной ткани или метастатическое поражение кости, аллергическая реакция к терипаратиду или компонентам растворителя.
Стронция ранелат** 2 г в саше для приема ежедневно в ходе клинических исследований демонстрировал умеренную противопереломную эффективность (Приложение A3.1). Снижение риска переломов бедренной кости наблюдалось только в субпопуляции пациентов старше 74 лет с остеопорозом в шейке бедренной кости.
«Двойной», или слабый анаболический эффект на костную ткань при применении стронция ранелата** [212] не подтвердился в дальнейших исследованиях [280]. Уплотнение и утяжеление кости за счет содержания стронция в кристаллической решетке гидроксиапатита было предложено в качестве объяснения механизма действия препарата [280, 281].
Приложение A3.2 Возможности лабораторных методов исследования для исключения вторичных причин остеопороза и других метаболических заболеваний скелета.
Приложение А3.3 Метод оценки компрессионных деформаций тел позвонков [83, 84]
Приложение А 3.4 Содержание кальция в молочных продуктах на 100 г [249]
Приложение Б. Алгоритмы действий врача
Приложение В. Информация для пациента
Остеопороз – это заболевание, при котором кости становятся хрупкими и могут легко ломаться. В норме кость имеет пористое строение, при остеопорозе уменьшается костная масса и нарушается структура кости
Кто болеет Остеопорозом?
Согласно данным международного общества остеопороза, каждая третья, а в странах с высокой продолжительностью жизни каждая вторая женщина старше 50 лет имеет перелом, связанный с остеопорозом. Поэтому 80% среди пациентов с остеопорозом – это женщины в постменопаузе (после прекращения менструаций).
Болеют остеопорозом и мужчины старшей возрастной группы (после 50 лет), а также пациенты любого возраста и пола, страдающие некоторыми эндокринными, ревматическими заболеваниями, тяжёлыми поражениями кишечника (болезнь Крона, неспецифический язвенный колит), пациенты после пересадок внутренних органов, люди с ограниченной подвижностью, вследствие любых причин, а также пациенты, длительно принимающие некоторые медикаменты (противосудорожные препараты, глюкокортикоидные гормоны, средства снижающие кислотность желудка и т.д.)
Чем опасен Остеопороз?
У пациентов с остеопорозом переломы происходят при минимальной травме (падение с высоты собственного роста, чихании, кашле, подъёме тяжестей и т.д.) или даже без травматического воздействия.
Самые опасные переломы, связанные с высокой смертностью – это переломы бедренной кости. Если такой перелом случился, необходимо хирургическое лечение.
Кроме того, остеопороз становится причиной патологических переломов рук (лучевой, плечевой костей), костей голени, таза, ключицы, рёбер при падении с высоты собственного роста.
Самые частые патологические переломы – это переломы тел позвонков. Перелом тела позвонка может сопровождаться болью в спине. Наличие одного перелома значительно увеличивают вероятность последующих переломов позвонков. Множественные переломы тел позвонков приводят к изменению осанки, снижению роста на 4-5 см и более.
Как заподозрить Остеопороз?
Некоторые называют остеопороз «безмолвной эпидемией». Пациента с остеопорозом без переломов обычно ничего не беспокоит. Вместе с тем, существуют факторы риска переломов, которые позволяют сориентироваться пациенту и врачу. Даже пациенту под силу оценить свою индивидуальную 10-летнюю вероятность основных переломов (FRAX).
Как диагностировать Остеопороз?
Для врача важно знать были ли у Вас переломы, развившиеся при минимальной травме в возрасте после 45 лет. Иногда наличие такого перелома достаточно, чтобы диагностировать остеопороз.
Для ранней диагностики остеопороза (когда переломов ещё нет) наиболее точный метод – двухэнергетческая рентгеноденситометрия поясничного отдела позвоночника и проксимального отдела бедренной кости. Это безболезненный и безопасный метод для оценки минеральной плотности кости. Плотность костной ткани измеряется в поясничных позвонках, бедренной кости и иногда при необходимости в лучевой кости. Этого достаточно, чтобы сориентироваться о состоянии всего скелета. Уровень лучевой нагрузки при проведении исследования в 10 раз меньше, чем при стандартной рентгенографии лёгких. До проведения исследования желательно избегать использования контрастных препаратов. Вас попросят снять все металлические предметы с тех зон, где будут проводить исследование (нижняя треть туловища, бёдра, предплечье). Ультразвуковые приборы (исследование костной плотности по пяточной кости, фаланге пальца и т.д.) являются методом скрининга, а не постановки диагноза.
Для определения причины остеопороза, выбора оптимального препарата для лечения и динамического наблюдения врачу могут потребоваться анализы крови, мочи, а также боковая рентгенография грудного и поясничного отделов позвоночника, иногда компьютерная томография позвоночника или магниторезонансное исследование.
Существуют ли методы лечения остеопороза?
На сегодняшний день, медикаментозное лечение остеопороза позволяет значительно уменьшить риск переломов и повысить костную плотность. Первые результаты лечения можно увидеть через 1 год, если ориентироваться на прибавку минеральной плотности кости по данным рентгеноденситометрии. Минимальная продолжительность непрерывного лечения остеопороза в большинстве случаев составляет 3 года. Однако у некоторых пациентов непрерывное лечение продолжается до 5 и более лет. Иногда врач может прекратить лечение и затем вновь возобновить терапию. Вместе с тем, выполнение рекомендаций специалиста позволяет предупредить переломы, сохранить осанку и, таким образом, значительно улучшить качество жизни. Новые препараты обладают высокой эффективностью в сочетании с всё более редким и удобным приёмом. Появление препаратов-копий позволяет сделать лечение остеопороза всё более доступным.
Внимание! Препараты отличаются по эффективности, показаниям, противопоказаниям и их применение требует наблюдения врача.
Можно ли предупредить остеопороз?
Заботиться о здоровье костей нужно с детского возраста. Особенно важно вести здоровый образ жизни в период набора пика костной массы (до 25-30 лет). Чем больше наш «пик костной массы», тем позже снижение костной массы достигнет того «порога», за которым стоит перелом.
Для профилактики остеопороза рекомендуется:
1. Потреблять достаточное количество кальция и витамина D в течение всей жизни
Источники кальция в пище:
• 100 г нежирных молочных продуктов (молоко, кефир, йогурт, мороженное, творог) содержат 100-120 мг кальция;
• 100 г твёрдого сыра могут содержать до 1000 мг кальция;
• кальций также содержится в шпинате, брокколи, рыбных консервах с костями и продуктах, обогащённых кальцием (апельсиновый сок, каши – если указано, что продукт обогащён кальцием).
Витамин D играет важную роль для усвоения кальция и здоровья костей и мышц. У молодых людей витамин D синтезируется в коже под воздействием ультрафиолетовых лучей. Достаточно гулять 15-30 минут с открытым лицом и кистями, чтобы получить адекватный уровень витамина D. Однако, у пожилых людей возможности кожи синтезировать витамин D снижаются.
2. В течение всей жизни заниматься любительским спортом:
Физические упражнения, которые выполняются на ногах (ходьба, бег, теннис, танцы, занятия на тренажёрах) благоприятны для лучшего набора пика костной массы и улучшения качества кости у молодых людей. Эти упражнения менее эффективны у женщин в постменопаузе для увеличения костной массы. Вместе с тем, упражнения, направленные на увеличение мышечной массы и улучшение равновесия благоприятны для предупреждения падений.
Истощающие физические нагрузки, напротив, могут приводить к преждевременной потере минеральной плотности кости.
3. Избегать вредных привычек (курение, злоупотребление алкоголем):
Курение негативно влияет на кости. Курящие женщины имеют более низкий уровень эстрогенов, раньше вступают в климакс. Курение влечёт худшее усвоение кальция из продуктов питания. Люди, которые выкуривают пачку сигарет ежедневно обычно имеют на 5-10% меньше костной массы к 50 годам, по сравнению с некурящими.
Злоупотребление алкоголем (более 2-3 установленных единиц алкоголя ежедневно, регулярно — соответствует стандартному бокалу пива (285 мл), одной стандартной порции крепкого спиртного (30 мл), бокалу вина средних размеров (120 мл) или одной порции аперитива (60 мл)) приводит к снижению костной плотности даже у молодых мужчин и женщин. Алкоголизм увеличивает риск переломов из-за потери костной массы, недостатка питательных веществ и увеличению частоты падений.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Оценка риска перелома по шкале FRAX [3]
Название на русском языке: ФРАКС – Инструмент оценки риска перелома
Оригинальное название (если есть): FRAX ®
Источник (официальный сайт разработчиков, публикация с валидацией):
https://www.sheffield.ac.uk/FRAX/tool.aspx?lang=rs
Тип: шкала оценки
Назначение: оценка риска перелома
Содержание: Для подсчета 10-летней вероятности перелома с использованием минеральной плотности кости ответьте на следующие вопросы.
Ключ (интерпретация): Результат оценки риска перелома в оранжевой зоне: рекомендовано проведение двухэнергетической рентгеноденситометрии (DXA) поясничного отдела позвоночника и проксимального отдела бедренной кости. При выявлении остеопороза (Т-критерий ≤ -2,5) показано назначение антиостеопоротической терапии без повторной оценки риска перелома.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Отрывок из книги «Руководство по натуральной медицине» — Пиццорно Дж. Е., Мюррей М. Т. Купить книгу
Клиническая картина
• Обычно протекает бессимптомно до появления сильной боли в спине.
• Распространен у женщин в постменопаузе и мужчин старше 70 лет или принимающих ингибиторы ароматазы и глюкокортикоиды.
• Отсутствие травматических переломов бедра и позвонка.
• Уменьшение роста.
• Определяется как Т-критерий на уровне —2,5 или ниже минеральной плотности кости (МПК) у молодого здорового взрослого.
Общие положения
• Остеопороз (ОП) является наиболее распространенным заболеванием костей у людей и представляет серьезную угрозу для здоровья женщин в постменопаузальном периоде. Особенности включают: низкую костную массу, ухудшение микроархитектуры костной ткани, хрупкость костей, снижение прочности костей и повышенный риск переломов.
• Каждый год в США происходит приблизительно 1,5 млн переломов вследствие остеопороза (ОП), из которых 250 тыс. переломов бедра.
• После остеопоротического перелома бедра риск смерти женщины удваивается; риск смерти мужчины увеличивается втрое.
• -2096 пациентов, перенесших остеопоротический перелом шейки бедра, умирают в последующие 6 мес, 50 % выживших не смогут ходить без посторонней помощи, а 25% нуждаются в длительном домашнем уходе.
Хотя по прогнозам афроамериканцы являются этнической группой с наименьшим риском ОР, заболевание встречается у 53 % афроамериканских женщин и 24% афроамериканских мужчин. Это означает, что более чем у половины всех афроамериканских женщин и у четверти всех афроамериканских мужчин развивается остеопения или остеопороз.
• У белой расы риск низкой костной массы и ОП еще выше; в настоящее время прогнозируется развитие заболевания у 77% женщин и у 4396 мужчин.
• Латиноамериканцы, однако, страдают в наибольшей степени: 86% латиноамериканских женщин и 53% латиноамериканских мужчин теряют столько костной ткани, что риск переломов остеопороза значительно возрастает.
• С 2015 до 2025 г. у латиноамериканцев ожидается увеличение частоты переломов вследствие остеопороза на 175%. Более 50 % патологических переломов отмечается у женщин с остеопенией, к тому же эта группа женщин, перенесших патологический перелом, подвержена такому же риску переломов, что и женщины с ОП.
• Переломы позвонков грудного и (или) поясничного отдела вызывают боль, уменьшение роста и выраженный кифоз или деформацию грудного отдела позвоночника с ограничением объема движений, изменением походки, ограничением функции легких и проблем, связанных с пищеварением. Перелом позвоночника предполагает увеличение риска последующих переломов позвоночника как минимум в 5-7 раз.
• Депрессия, тревожность, низкая самооценка и потеря зубов тоже являются следствием остеопороза.
Патофизиология
• Ремоделирование кости — это процесс резорбции (разрушения) костной ткани и ее формирования. При резорбции кости остеокласты вызывают ферментативное растворение минералов и белков. Остеобласты образуют белковый матрикс коллагена для реминерализации и формирования кости. Ремоделирование кости обычно представляет собой равновесие между ее резорбцией и формированием. Дисбаланс между удалением и замещением приводит к потере костной ткани и риску перелома.
• Костная масса быстро увеличивается в детском возрасте; это увеличение ярко выражено в позднем подростковом периоде, но продолжается и после 20 лет. У женщин процесс формирования костной ткани завершается к 17 годам. Пик костной массы приходится на 28 лет, после чего происходит ее медленная потеря со скоростью 0,4 % в год, главным образом в области шейки бедренной кости. После менопаузы потеря костной ткани ускоряется на 2 % каждый год в первые 5—10 лет. Этот процесс продолжается у женщин старше 70 лет с гораздо меньшей скоростью.
Факторы риска остеопороза
• Генетические факторы: уровень пика костной ткани определяется генетическими факторами. Переломы в анамнезе у родственников первой степени родства повышает риск переломов. Молодые дочери женщин с ОП переломами и родственники первой степени родства с ОП обладают субнормальной костной массой. Чернокожие женщины обладают большей костной массой по сравнению с белыми женщинами. На сегодняшний день доступно геномное исследование, позволяющее определить предрасположенность к дефекту рецепторов витамина D (VDR). Женщины с дефектом VDR требуют значительно большего уровня витамина D, предпочтительнее в виде D3. Новый ключевой генетический фактор: полиморфизм сайтов VDR, часть которых может обладать повышенной потребностью в витамине D.
• Дефицит витамина D: роль витамина D в поддержании нормального состояния костной ткани недооценивается. Плотность кости напрямую связана с 25-гидроксихолекальциферолом [25(ОН)D3] и обратно пропорциональна переломам всех типов.
• Дефицит витамина К; остеокальцин, который вводит кальций (Са) в кость, и матриксный белок Gla, который предотвращает отложение кальция в артериях, являются витамин-К-зависимыми белками.
• Образ жизни: образ жизни, гормональные факторы, Са, прием витаминов D и К2 физические упражнения, возраст менархе, регулярность менструального цикла, а также употребление алкоголя и табака оказывают большее влияние, чем генетические факторы, которые составляют всего 30 % риска развития ОП. Требования в период достижения пика костной массы: сбалансированная диета, адекватные калории, постоянный прием белка и Са на протяжении всей жизни. Са, Mg, витамин К2 и витамин D3 имеют критически важное значение для пожилых женщин. Потребности в Са с возрастом меняются: после 65 лет организм женщины усваивает на 50 % меньше Са, чем в молодости. Активность ферментов почек, продуцирующих активный витамин D, снижается.
• Пищевой белок: высокое потребление животного, а не растительного белка связано с повышенным риском перелома костей предплечья. Красное мясо является источником кислоты, вызывая высвобождение солей из кости для создания кислотного баланса и поддержания кислотнощелочного гомеостаза. Диета, богатая фруктами, овощами и растительными белками, является щелочной диетой.
• Курение: сигареты содержат большое количество кадмия и никотина, которые вызывают потерю костной ткани. Курящие женщины теряют костную ткань быстрее, обладают более низкой костной массой и характеризуются более высокой частотой переломов. У курильщиц менопауза наступает на 2 года раньше. Курение повышает печеночный клиренс эстрогенов.
• Алкоголь: употребление 200 мл алкоголя в день (злоупотребление) повышает риск падений и перелома бедренной кости. Умеренный прием алкоголя снижает риск перелома бедренной кости у пожилых женщин; алкоголь в небольших дозах замедляет резорбцию кости, повышая уровень эстрадиола и экскрецию серотонина.
• Отсутствие физической активности: лица с высокой активностью обладают большей костной массой; длительное пребывание в постели или прикованность к инвалидной коляске вызывает стремительную потерю кости. Упражнения снижают риск ОП за счет стимуляции остеобластов.
Гормональные факторы остеопороза
• Менопауза: все женщины утрачивают костную ткань, однако ускоренная потеря происходит в первые 5 лет менопаузы. Снижение уровня эстрогена уменьшает скорость резорбции кости. Чем раньше это происходит до наступления среднего возраста менопаузы (51 год), тем быстрее кости утрачивают защитный эффект эндогенного эстрогена. Преждевременная менопауза (до 40 лет), позднее менархе в подростковом возрасте, периоды аменореи из-за низкого уровня эстрогена в репродуктивном возрасте (например, гипоталамическая аменорея) или частые менструации повышают риск развития остеопороза. Костная масса позвоночника у женщин, пропустивших до половины ожидаемых менструальных периодов, на 120/0 меньше; у женщин, пропустивших более половины периодов, костная масса на 31 % меньше костной массы здоровых женщин из контрольной группы.
• Концентрация Са в крови строго поддерживается в узких границах. Снижение запускает повышенную секрецию паратгормона (ПТГ) и снижает секрецию кальцитонина щитовидной и паращитовидными железами. Избыток Са запускает сниженную секрецию ПТГ и повышает секрецию кальцитонина.
• ПТГ повышает содержание Са в сыворотке, увеличивая катаболизм остеокластов в кости, снижает экскрецию Са почками, повышает всасывание Са в кишечнике и повышает преобразование в почках 25-(OH)D3 дополнительные факторы
Чем больше факторов риска, тем выше потенциальное снижение костной массы и риск переломов. Факторы риска сами по себе не включают адекватную оценку низкой костной массы, но помогают при клинической оценке рисков для разработки оптимальной стратегии профилактики. Риск для каждой женщины — это наиболее важный параметр здоровья костей в будущем. Заболевания и лекарственные препараты могут нарушать нормальный метаболизм кости.
• Вторичные причины потери костной ткани:
— лекарственные препараты: ингибиторы ароматазы, цитотоксические препараты, избыточная терапия гормонами щитовидной железы, агонисты гонадотропин-релизинг фактора или его аналоги, некоторые антиконвульсанты при длительном приеме (например, фенитоин), применение глюкокортикоидов более З мес;
— генетические нарушения: гемохроматоз, гипофосфатазия, несовершенный остеогенез, талассемия, нарушения баланса Са, экскреция Са с мочой; — эндокринопатии: избыток кортизола, синдром Кушинга, гипертиреоз, недостаточность гонад, первичный гиперпаратиреоз, гиперкальциурия, дефицит витамина D, заболевания желчного пузыря, СД(1), гипоталамическая аменорея, преждевременная недостаточность яичников;
— заболевания ЖКТ: первичный билиарный цирроз, мальабсорбция, гипохлоргидрия, непереносимость лактозы, целиакия, болезнь Крона, тотальная гастрэктомия, шунтирование желудка;
— другие заболевания: анкилозирующий спондилоартрит, хроническая почечная недостаточность, лимфома и лейкоз, множественная миелома, нервная анорексия, булимия, ревматоидный артрит.
Диагностические принципы остеопороза
• Обследование всех женщин в постменопаузальном периоде на факторы риска — анамнез, физикальное обследование, диагностические тесты. Цели обследования: выявить женщин с риском ОП или переломов, диагностировать ОП и (или) определить тяжесть ОП, исключить все вторичные причины потери костной ткани, определить факторы риска падений и травм.
• Диагностика рисков переломов ВОЗ по шкале оценки рисков переломов FRAX: анамнез пациента (личный анамнез переломов после 40 лет, анамнез переломов шейки бедра у родителей, курение, злоупотребление алкоголем, прием глюкокортикоидов, ревматоидный артрит или другие вторичные причины ОП), тест на плотность кости и калькулятор рисков FRAX являются инструментами для определения риска переломов. Необходимо использовать калькулятор FRAX для ПМ женщин с низкой плотностью костной ткани, но без ОП. Он определяет вероятность развития ОП в ближайшие 10 лет и вероятность перелома шейки бедра. Калькулятор риска FRAX доступен в онлайн-версии.
• для выявления факторов риска акцентируйте внимание на анамнезе и физикальном обследовании. Физические признаки ОП: уменьшение роста более чем на 3,8 см (необходимо измерять рост ежегодно). Выраженный кифоз в грудном отделе позвоночника, кариес, потеря зубов, рецессии десен, боль в пояснице.
• Рентгенологическое исследование МПК: исследование МПК — наилучший метод диагностики ОП. Золотым стандартом диагностики является ДЭРА. К другим методам относятся: КТ, УЗИ пяточной кости, рентгенография; ни одно из этих исследований не является идеальным с точки зрения диагностики и последующего наблюдения.
• Необходимо регистрировать массу тела, чтобы выявить женщин с низким ИМТ и, следовательно, с повышенным риском низкой МПК. Расспросите и обследуйте пациента на предмет острой или хронической боли в пояснице, признаках болезненности при перкуссии и исследовании плотности кости. Оцените риск падений, который повышается с приемом лекарств, влияющих на равновесие и координацию; мышечную слабость, нарушение зрения, падения, обмороки, потери сознания в анамнезе, трудность при стоянии или ходьбе, артрит/или нейропатия нижних конечностей.
Тест на минеральную плотность кости
• Тест МПК — это оптимальный метод подтверждения диагноза ОП. Существует несколько методик измерения МПК, но золотым стандартом остается ДЭРА.
• ДЭРА дает меньшее облучение, чем рентгенография или КТ. Этот метод может измерять плотность бедренной кости и позвоночника. Предпочтительное место измерения для исследования МПК — бедренная кость, особенно у пациентов старше 60 лет, поскольку измерения в области позвонков ненадежны из-за внекостной оссификации. Исследования позвоночника могут быть полезны у женщин в постменопаузальном периоде, у которых потери костной ткани выше из-за низкого уровня эстрогена. Периферические локализации ДЭРА дают точный, не менее полезный результат. Они могут не коррелировать с риском переломов и показателями МПК, полученными при исследованиях бедренной кости и позвоночника.
• Рекомендации Североамериканского общества менопаузы (NAMS) по показаниям к исследованию ДЭРА:
— женщины в постменопаузальном периоде с вторичными причинами потери костной ткани (например, лечение стероидами, гиперпаратиреоз);
— рентгенологические признаки остеопении;
— все женщины в возрасте 65 лет и старше;
— женщины в постменопаузальном периоде (возраст 50 лет и старше) с дополнительными факторами риска [перелом после менопаузы, вес ниже 56 кг, перелом бедренной кости в анамнезе, курение, ревматоидный артрит, употребление более 2 единиц алкоголя в день (одна единица = 354 мл пива, 118 мл вина или 30 мл крепкого алкогольного напитка)];
— женщины в постменопаузальном периоде (независимо от возраста) с патологическими переломами после менопаузы, низким весом тела, переломом позвоночника или бедренной кости в семейном анамнезе.
• Отчет о результатах теста на МПК: стандартное отклонение Z-балла или Т-балла. Z-балл основан на стандартном отклонении от среднего значения МПК у женщин той же возрастной группы. Т-балл основан на среднем значении пика МПК у здоровых молодых женщин. Критерии ВОЗ для диагностики ОП определяются с помощью Т-баллов.
Лабораторные исследования метаболизма кости
• Биохимические маркеры обмена костной ткани:
— анализ мочи на выявление продуктов распада костной ткани (перекрестносвязанный N-телопептид коллагена 1-го типа или деоксипиридин);
— оценка обмена кости связана с потерей костной ткани; не предназначена для диагностики ОП или мониторинга потери костной ткани;
— использование ДЭРА для измерения МПК; анализ мочи на определение резорбции костной ткани, чтобы измерить скорость обмена;
— уменьшение маркеров распада в моче за 2-летний период расширило число методов измерения МПК, но значение маркеров в клинической практике еще не подтверждено.
• Дополнительные исследования вторичных причин потери МПК: Са, суточный Са в моче, ПТГ, тиреостимулирующий гормон, свободный тироксин, альбумин сыворотки, щелочная фосфатаза сыворотки, СОЭ, общий анализ крови и уровень витамина D. Непрямые тесты на определение абсорбции Ca. уровень желудочной кислотности и витамина 1).
Терапевтические принципы остеопороза
Цели лечения и предотвращения остеопороза:
• сохранение адекватной костной массы;
• сохранение прочности костей;
• предотвращение хрупкости костей;
• предотвращение разрушения микроархитектоники костной ткани;
• предотвращение или уменьшение риска переломов.
Вероятно, можно было бы в значительной степени предотвратить остеопороз, однако в настоящее время нет соответствующих фармакологических препаратов. Число пролеченных больных на одного излеченного для предотвращения одного перелома бедренной кости у женщин в возрасте от 55 до 64 лет составляет 4406 для бифосфонатов (БФ). В случае деносумаба необходимо лечить 334 женщины в течение З лет, чтобы предотвратить один перелом бедренной кости. Невзирая на эти факты, руководство Североамериканского общества менопаузы (NAMS) рекомендует фармакотерапию в следующих случаях:
• все женщины в постменопаузальном периоде с предшествующим ОП или переломом бедренной кости либо позвоночника;
• все женщины, у которых значения МПК в поясничном отделе позвоночника, шейке бедра или всего тазобедренного сустава составляют —2,5 и ниже;
• все женщины в постменопаузальном периоде, Т-балл которых составляет от —1,0 до -2,5, а также с 10-летним риском, основанным на калькуляторе результатов FRAX для основных переломов ОП (позвоночник, тазобедренный сустав, плечо или запястье) и равным как минимум 20 % для перелома шейки бедра и как минимум 3 % — при высоком риске.
Фармакотерапия: многочисленные препараты для лечения ОП [например, БФ, селективные модуляторы эстрогеновых рецепторов (СМЭР), ралоксифен, ПТГ, эстрогены и киьцитонин]. Эти препараты, за исключением эстрогена, изучались на предмет влияния на переломы только у пациентов с клиническим диагнозом ОП или диагнозом ОП, поставленным на основании МПК. Абсолютное снижение риска переломов было самым значительным у женщин с высоким риском переломов.
Лекарственная терапия
• ГЗТ: эстроген-заместительная терапия (ЭЗТ) и ГЗТ снижают скорость обмена и резорбции костной ткани. ЭЗТ может снижать скорость резорбции у женщин в период пременопаузы. ЭЗТ и ГЗТ снижают риск на 54%. ЭЗТ и ГЗТ более эффективны для снижения риска переломов, если их прием начинают в первые 5 лет менопаузы. Если принимать эти препараты более 10 лет, они дают еще большее снижение риска — 75 % для переломов запястья и 73% для переломов шейки бедра. Системные пероральные или трансдермальные эстрогены и эстроген-прогестерон в стандартных дозах повышают МПК во всех отделах у женщин в постменопаузальном периоде. Средняя разница МПК после 2 лет лечения составляет 6,8% для пояснично-крестцового отдела и 4,1 % — для шейки бедра. Дневная доза 0,625 мг конъюгированных конских эстрогенов с прогестероном или без него (медроксипрогестерона ацетат или пероральный микронизированный прогестерон), принимаемая в течение З лет, может повысить МПК позвоночника на 3,5-5,096, МПК тазобедренного сустава — на 1,7 %. ГЗТ может снизить риск перелома шейки бедра (34%), перелома позвоночника (3496) и переломов других костей (24%). Даже дозы ниже стандартных доз эстрогена могут увеличить МПК позвоночника и шейки бедра на 1-396 (например, при их систематическом поступлении через вагинальное кольцо). Стандартные дозы эстрогена или эстроген-прогестерона могут снизить риск переломов у женщин в постменопаузальном периоде на 27%. Несмотря на эти исследования, препараты, содержащие только эстроген или эстроген-прогестерон, разрешены только для профилактики, а не для лечения постменопаузального ОП, поскольку возрастает риск рака молочной железы, тромбов, инсультов, несмертельных инфарктов миокарда, желчнокаменной болезни, болезненности молочных желез, маточных кровотечений и головных болей. Необходим индивидуальный подход к лечению с определением соотношения риск/польза. ГЗТ и ЭЗТ лучше всего действуют в первые 5-10 лет после менопаузы. Оптимальная и максимальная длительность применения еще не установлены. ЭЗТ и ГЗТ не рассматриваются как первичное длительное лечение, за исключением женщин, не переносящих БФ, или женщин, у которых симптоматика не поддается лечению другими препаратами.
• БФ: ингибируют остеокласты, уменьшая резорбцию костной ткани. Необходимо повышать МПК позвоночника и тазобедренного сустава у женщин в постменопаузальном периоде независимо от их возраста. Несмотря на мнение о том, что БФ снижают риск переломов позвоночника у женщин с ОП на 40-70%, а частоту переломов шейки бедра и других переломов — на 50%, эти показатели ненадежны, как было показано выше при описании NNT. Большинство БФ в США (алендронат, ибандронат и ризендронат) предназначены только для перорального ежедневного или периодического приема. Золендроновая кислота назначается внутривенно (в/в). Ответ в форме МПК дает сходные результаты при еженедельном пероральном введении алендроната и ризендроната, ежемесячном пероральном введении ибандроната и ризендроната и внутривенном введении ибандроната раз в З мес. Применяйте БФ с осторожностью, взвешивая потенциальную пользу и серьезный риск. Неразрешенные вопросы, связанные с БФ, касаются качества кости; у некоторых пациентов возможно увеличение частоты переломов в отдаленном периоде и потенциальное чрезмерное подавление обмена костной ткани в отдаленном периоде, что приводит к ломкости костей. Проблемные случаи: нетипичные, плохо заживающие переломы; атипичные переломы бедренной кости. Реакция врачей на эти жалобы: перерыв в приеме препарата, частота и длительность которого в настоящее время изучается. Другие проблемы, связанные с БФ: ОП нижней челюсти (остеонекроз нижней челюсти) у пациентов, принимающих высокие дозы БФ внутривенно, и пациентов, получающих лучевую терапию при раке головы и шеи. Характеристики остеонекроза нижней челюсти: длительное (более 6—8 мес) заживание повреждений ротовой полости после операций или удаления зубов. Его частота при внутривенном введении БФ у пациентов без облучения шеи — 12%. Частота случаев, связанных с ротовой полостью, — 0,03-0,06 %. Тем не менее операции в ротовой полости повышают заболеваемость в 7 раз. Спорным остается вопрос, нужно ли прекращать прием БФ перед удалением зубов. Многие практические врачи приостанавливают прием БФ до заживления ран в ротовой полости. Редкие долговременные осложнения приема БО. остеопоротические переломы тела бедренной кости, которые проявляются в виде болей в области бедренной кости в продромальном периоде и могут быть двусторонними. Использование БФ в настоящее время ограничено максимум до 5 лет, для возможности ремоделирования кости. Тщательно наблюдайте за МПК, чтобы убедиться в стабильно минимальной потере костной ткани после прекращения приема БФ. Применение БФ в течение 5 лет может обеспечить такую же длительную защиту, как и при лечении БФ, длящемся более 5 лет. Побочные эффекты пероральных БФ: нарушения со стороны верхних отделов ЖКТ (например, дисфагия, эзофагит, язвы пищевода и желудка). Меры предосторожности: гипокальциемия и нарушения со стороны почек, редкие преходящие гриппоподобные состояния при больших пероральных и внутривенных дозах. Тщательно соблюдайте инструкции по применению. Основная польза: снижение боли
и страданий, улучшающее качество жизни; спасение жизней (переломы головки бедренной кости). Используйте инструмент FRAX для определения риска переломов при низком МПК, но еще не развившемся ОП. Используйте БФ только по показаниям, при правильном лечении и мониторинге нежелательных явлений, а также нарушении ремоделирования кости и только тогда, когда натуральные методы не дают положительных результатов.
• СМЭР: нестероидные агонисты и (или) антагонисты эстрогена.
Ралоксифен (60 мг ежедневно) разрешен для профилактики и лечения ОП и является единственным СМЭР, разрешенным в настоящее время для лечения ОП. Ралоксифен может значительно улучшить показатель МПК на 1,6-2,696 для поясничного отдела и на 1,2—2,1 % — для шейки бедра.
• ПТГ: анаболик, который назначают в виде ежедневных подкожных инъекций, стимулирующих формирование остеобластов и повышающих плотность трабекул кости у женщин с ОП. Терипаратид (Форстео) разрешен для лечения ОП у женщин в постменопаузальном периоде. В дозе 20 мкг на инъекцию ежедневно терипаратид повышал ПМК поясничного отдела позвоночника на 8,6% и ПМК шейки бедра — на 3,5% по сравнению с плацебо. Он также снижал частоту новых переломов позвоночника на 65% и других костей — на 5396. К сожалению, даже хроническое интермиттирующее повышение ПТГ на фоне стандартной дозы терипаратида (20 мкг в день), как оказалось, вызывает ряд нежелательных побочных эффектов: тошноту, судороги в ногах и головокружения, кальциемию, гиперкальциурию и гиперурицемию с гипермагниемией. Кроме того, в связи с развитием остеогенной саркомы (крайне агрессивного рака кости) практически у половины животных в исследованиях на крысах терипаратид идет с «черной рамкой» FDA, предупреждающей о его потенциальных долгосрочных побочных эффектах. К тому же хроническое повышение ПТГ вызывает снижение когнитивных функций.
• Кальцитонин: разрешен для лечения, но не для профилактики постменопаузального ОП; доступен в виде назального спрея и подкожных инъекций. Интраназальный спрей в дозе 200 МЕ ежедневно в течение 5 лет у женщин в постменопаузальном периоде с ОП снижал риск новых переломов позвоночника на 33 % по сравнению с плацебо. Эффекта в отношении тазобедренного сустава и невертебральных переломов не наблюдалось. Кальцитонин в виде спрея может также уменьшать боль в костях, связанную с компрессионными переломами позвоночника.
• Исследуются новые методы лечения: некоторые из них в настоящее время еще недоступны в США [например, тиболон и пероральный ранелат стронция (Protelos)]. Деносумаб (Пролиа), человеческое моноклональное антитело к активатору лиганда к рецептору RANk (ядерного фактора каппа В), разрешен к применению и показан для лечения женщин в постменопаузальном периоде, подверженных высокому риску ОП переломов, или женщин с непереносимостью либо неэффективностью других методов лечения. Препараты, находящиеся в стадии разработки: СМЭР и полноразмерный ПТГ.
Факторы, связанные с образом жизни
Подход, основанный только на образе жизни, неэффективен для предотвращения потери ПМК и переломов, однако он дает основу для натуральных методов лечения, направленных на профилактику и лечение ОП. Курение ускоряет потерю костной ткани и снижает костную массу. У курящих женщин менопауза наступает на 2 года раньше, чем у некурящих. У курящих женщин, находящихся в постменопаузальном периоде, выше частота переломов. У курильщиц может быть повышен риск переломов шейки бедра, особенно среди женщин старше 60 лет. Курение в анамнезе увеличивает риск будущих переломов независимо от МПК. Умеренное употребление алкоголя связано с повышением МПК у женщин в постменопаузальном периоде, однако употребление более семи единиц алкоголя в неделю влечет за собой повышенный риск падений. Употребление более двух единиц алкоголя в день повышает риск ОП переломов (одна единица = 350 мл пива, 118 мл вина или 30 мл крепкого спиртного напитка).
• Физические упражнения: физическая активность — главный определяющий фактор плотности кости. Один час умеренной нагрузки З раза в неделю предотвращает потерю костной ткани и повышает костную массу у женщин в постменопаузальном периоде. И поднятие тяжестей, и силовые тренировки положительно влияют на развитие кости, ее функцию и поддержание нормального состояния. Женщины, практикующие физические упражнения, могут повысить ПМК позвоночника на 2%. У женщин с постоперационной менопаузой, принимающих эстроген, подключение силовых тренировок улучшает МПК. Определенные упражнения не обязательно могут повышать МПК, однако они могут снизить риск переломов вследствие падений. Упражнения, направленные на укрепление мышц и улучшение равновесия, уменьшают риск падений и связанных с этим травм на 75% у женщин в возрасте 75 лет и старше. Неподвижность удваивает скорость выведения Са с мочой и калом, приводя к отрицательному балансу Са. Наиболее эффективный способ укрепления костей — это физическая активность. Простые силовые упражнения: ходьба или тай-чи. Простые укрепляющие упражнения: гантели или эспандеры. Проконсультируйтесь со специалистами, которые посоветуют эффективные упражнения, безопасные виды физических упражнений и упражнения, которых следует избегать.
Пищевые факторы
К диетическим факторам, которые могут быть предполагаемой причиной ОП, относятся следующие.
• Низкое содержание Са, витамина Кт Mg, высокий уровень употребления фосфора.
• Диета с высоким содержанием белка.
• Окисляющая диета.
• Высокий уровень потребления соли (половина ацидоза, спровоцированного диетой — большая часть которого нейтрализуется за счет изъятия Са из костей, — вызвана избыточным употреблением соли, что отрицательно влияет на выделение кислоты почками).
• Дефицит микроэлементов.
• Вегетарианская диета (лакто-вегетарианская и веганская): более
низкий риск ОП. Костная масса вегетарианцев не отличается от всеядных пациентов в 30, 40 и 50 лет, но отличается в более позднем возрасте. Снижение случаев ОП у вегетарианцев вызвано снижением потери костной ткани в более позднем возрасте. Диета с высоким содержанием белка и фосфатов повышает экскрецию Са с мочой. Повышение суточного потребления белка с 47 до 142 г удваивает выделение Са с мочой. Противоположная точка зрения: диета с высоким содержанием белка повышает экскрецию Са с мочой и выработку кислоты, вызывая отрицательный баланс Са только в случае неадекватного суточного приема. Лучше повышать потребление Са в совокупности с фруктами и овощами для создания ощелачивающего эффекта, чем уменьшать поступление белка. Разумный компромисс: старайтесь обеспечить потребление как минимум 20 г белка в день, особенно у лиц старше 80 лет, но не превышая 60 г. Ключевым фактором в данном случае является системное рН-влияние пищевых продуктов. Пищевой ацидоз, типичный при употреблении пищи с высоким содержанием белка и соли, заставляет организм нормализовать РН за счет буферизации Са, изъятого из костей. Введение добавок Са может предотвратить избыточную потерю костной ткани, однако они могут усилить образование кальцинатов в почках у пациентов с предрасположенностью к этому. Возможная стратегия, помогающая снизить риск образования камней в почках, — использование цитрата Са.
• Соляная кислота: Са должен подвергаться ионизации со стороны желудочной кислоты, чтобы произошло его всасывание. Слабая ионизация Са — главная проблема карбоната Са. Снижение кислотности желудочного сока происходит у 40% женщин в постменопаузальном периоде, однако эффект повышения РН достигается только в случае, когда слабо растворимые соли Са, такие как Са карбонат, принимаются утром натощак. Голодающие пациенты с недостаточной кислотностью желудочного сока усваивают только 4% принятого внутрь Са в виде карбоната, в то время как нормальная кислотность желудочного сока обеспечивает всасывание 2296. Предпочтительные предварительно ионизированные формы Са: цитрат, лактат или глюконат. В случае сниженной кислотности 45% Са всасывается при приеме формы цитрата. Однако если Са принимается с пищей, наблюдается небольшое отличие в его абсорбции даже у пожилых пациентов с атрофическим гастритом или пациентов, принимающих антагонисты Нгрецепторов.
• Сахар: после употребления рафинированного сахара экскреция Са с мочой увеличивается. Среднестатистический американец употребляет 125 г сахарозы, 50 г кукурузного сиропа и других простых сахаров, стакан газированного напитка с фосфатами и высокую дозу белка ежедневно.
• Безалкогольные напитки: содержат много фосфатов, но не кальция. Потребление на одного человека в США: 450 мл/сут. Безалкогольные напитки — главный фактор риска нарушения кальцификации растущих костей у детей. Уровень Са в крови обратно пропорционален числу бутылок безалкогольных напитков, выпитых за неделю.
• Зеленые листовые овощи: употребление в пищу зеленых листовых овощей (например, шпината, листовой капусты, петрушки, салата) предотвращают развитие ОП. Это богатые источники широкого спектра витаминов и минералов, входящих в состав здоровых костей (Са, витамин Кр бор).
• Изофлавоноиды сои: данные о потенциальной способности белков сои или ее изофлавоноидов изменять метаболизм и резорбцию костной ткани противоречивы и недостаточно подтверждены. Соевые бобы содержат фитоэстрогены (генистеин, даидзеин и глицитеин), по молекулярной структуре аналогичные 17+-эстрадиолу. Связывание изофлавоноидов с эстрогенными рецепторами происходит преимущественно с эстрогенными [3-рецепторами, указывая на то, что изофлавоноиды действуют как селективные модуляторы эстрогенных рецепторов. Даидзеин обладает молекулярным сходством с препаратом иприфлавон, который используется в Европе для лечения ОП. Иприфлавон — это БАД, используемая в США. МПК является золотым стандартом в области параметров, определяющих риск нетравматических переломов и обмена костной ткани, и является независимым прогностическим фактором. Соя может сыграть определенную роль в замедлении костного обмена и повышении МПК у женщин благодаря ее эстрогенному эффекту на костную ткань. Различные варианты дозы, длительности приема и рецептуры препаратов на основе сои, а также различные выборки пациентов — возможные причины противоречивых результатов относительно влияния изофлавоноидов на обмен костной ткани и КМП. Однако важным фактором является и способ всасывания изофлавоноидов в кишечнике. Существенный эффект на пептиды в моче наблюдается у азиатских женщин, отсутствующий, однако, у женщин европеоидной расы. Возможно, это происходит из-за превращения даидзеина в его активный метаболит эквол под воздействием кишечной флоры и в связи с тем, что только 1/3 белых женщин способна метаболизировать изофлавоноиды в эквол, в то время как такая способность есть у половины азиатских женщин. Изофлавоноиды сои могут также оказывать больший эффект у женщин в постменопаузальном периоде, чем у женщин в периодах пре- или перименопаузы. Недооцененное влияние со стороны соевых продуктов может быть связано с количеством Са в некоторых из них или в диетах, содержащих соевые продукты. Рациональный клинический совет: необходимо увеличить содержание соевых продуктов в качестве профилактики ОП у женщин в пре-, пери- и постменопаузе. Всем женщинам с высоким риском ОП необходимо назначать добавки сои, чтобы суточная доза изофлавоноидов составляла 90 мг ежедневно.
Биологически активные добавки
Кость нуждается в постоянном поступлении многих питательных веществ. дефицит любого из них отрицательно влияет на здоровье костей. Помимо витамина К и бора кости необходимы следующие:
• Кальций: адекватное потребление кальция необходимо очень молодым женщинам и пожилым людям. Тем не менее кальций лишь незначительно эффективен в замедлении потери МПК у женщин в перименопаузе и в ранней менопаузе. БАДЫ могут улучшить эффективность фармацевтических агентов, предназначенных для лечения потери костной массы. Более высокое потребление кальция и добавки (от 500 до 2000 мг/сут) не связаны с более низкой частотой переломов бедра. Кальций в дозе 1000 мг + 400 МЕ витамина D в день снижает переломы бедра на 29% по сравнению с плацебо. У женщин в постменопаузальном периоде добавки кальция снижают потерю костной массы на 5096 в непозвоночных частях скелета. Действие наиболее выражено у женщин, у которых исходное потребление кальция было низким, у пожилых женщин и у женщин с установленным ОП. Потеря позвоночной кости была уменьшена при приеме от 1000 до 2000 мг кальция в день в течение года. Кальций в рационе необходим на протяжении всей жизни женщины; потребность возрастает с возрастом из-за меньшей абсорбции и конверсии кальция почками. Однако только добавление кальция не предотвращает ускоренную потерю костной массы, происходящую вскоре после менопаузы. Спустя 10 лет после менопаузы добавка кальция снова помогает уменьшить возрастную потерю костной массы. Адекватное поступление кальция имеет большое значение, но существует риск передозировки. Кальций является лишь одним из многих факторов питания и образа жизни, которые влияют на здоровье костей.
• Витамин D: поддерживает баланс кальция, усиливая всасывание в кишечнике. Повышенная абсорбция кальция снижает опосредованную ПТГ резорбцию кости. В США основными источниками витамина D являются обогащенные молочные продукты. Потребление снижается с возрастом. Дозы витамина D должны быть достаточными для повышения уровня в сыворотке до эффективного диапазона. Тем не менее у пожилых женщин в постменопаузальном периоде даже неадекватная доза от 700 до 800 МЕ в день связана со сниженным риском переломов бедра и других непозвоночных костей. Витамин D в сочетании с добавками кальция снижает уровень потери костной массы, особенно у пожилых женщин.
Витамин D также улучшает мышечную силу и равновесие, тем самым снижая риск падения.
• Магний: может быть так же важен для профилактики и лечения ОП, как и добавка кальция. Женщины с ОП имеют более низкий уровень магния в костной ткани, чем женщины без ОП. Дефицит магния у человека связан с пониженным уровнем наиболее активного витамина D в сыворотке также наблюдаемым при ОП. Механизм: либо фермент, ответственный за превращение в зависит от магния, либо магний опосредует секрецию ПТГ и кальцитонина. Прием в дозе от 250 до 750 мг (в виде гидроксида магния) в течение года несколько улучшал МПК. Магний является кофактором щелочной фосфатазы, участвует в минерализации костей. У женщин с ОП часто встречается низкий уровень магния, а его дефицит связан с аномальными кристаллами минералов кости. У некоторых женщин со сниженной МПК частота переломов не повышается, возможно, из-за того, что их минеральные кристаллы кости имеют высокое качество, отчасти из-за высокого содержания магния в тканях. У женщин в постменопаузальном периоде добавление магния в дозе от 250 до 750 мг в день в течение 6 мес с последующим приемом 250 мг в день в течение 6—18 мес без добавления кальция увеличило МПК.
• Стронций: нерадиоактивный элемент почвы, физически и химически похожий на углерод. Ранелат стронция специально используется для терапии ОП в клинических испытаниях, но недоступен в США. Стронций в больших дозах стимулирует формирование костей и уменьшает их резорбцию. Данные клинических испытаний непоследовательны. Клиническое исследование: среди женщин в постменопаузальном периоде с переломами позвонков в анамнезе частота новых деформаций позвоночника была самой низкой (38,896) при самой низкой дозе стронция. Хлорид стронция является наиболее распространенной формой в США, но он не был исследован. Из-за потенциальных побочных эффектов более высоких доз, включая рахит, дефекты минерализации костей и нарушение метаболизма витамина D, целесообразно использовать низкие дозы, пока не будут проведены дополнительные исследования.
• Цинк: необходим для образования остеобластов и остеокластов. цинк усиливает биохимическое действие витамина D и поддерживает синтез костных белков. Дефицит цинка обнаруживается в сыворотке и кости пожилых людей с ОП.
• Медь: дефицит вызывает аномальное развитие костей у растущих детей и способствует ОП. Добавка меди ингибирует резорбцию кости: З мг в день в течение 2 лет значительно снижали потерю костной массы у женщин в постменопаузальном периоде.
• Марганец: дефицит марганца является скрытым, но важным фактором при ОП. Он вызывает снижение отложения кальция в кости и стимулирует выработку мукополисахаридов, обеспечивая основу для кальцификации.
• Цинк, медь и марганец: эта комбинация с кальцием может быть более эффективной, чем один кальций, для предотвращения потери костной массы у женщин в постменопаузальном периоде.
• Бор: добавки снижают экскрецию кальция и магния с мочой и повышают уровень 17-(3-эстрадиола и тестостерона в сыворотке у женщин в постменопаузальном периоде. Добавки бора помогут предотвратить потерю костной массы.
• Кремний: во время роста костей и ранней кальцификации кремний поддерживает связи между коллагеном и протеогликанами. Бедные кремнием рационы вызывают аномальное развитие черепа и задержку роста у животных; добавки кремния позволяют частично предотвратить потерю трабекулярной кости.
• Фолиевая кислота и витамин В12; высокий уровень гомоцистеина может способствовать потере костной массы. Гомоцистеин, продукт расщепления метионина, стимулирует развитие ОП, если он не выводится из организма. Женщины с высоким гомоцистеином имеют в 2 раза более высокий риск непозвоночных переломов, вызванных ОП, чем женщины с низким гомоцистеином. Тем не менее нет никакой связи между уровнем гомоцистеина и МПК шейного или поясничного отдела. Это говорит о том, что риск пе реломов является результатом ухудшенного состояния кости. Фолат способствует реметилированию гомоцистеина до метионина. Его добавление женщинам в постменопаузальном периоде снижает уровень гомоцистеина. В12 также снижает уровень гомоцистеина. Исследуемая дозировка: 5 мг фолата + 1500 мкг В12 в течение 2 лет снижали частоту переломов бедра на 78 0/0 по сравнению с плацебо.
• Витамин В6: также помогает контролировать уровень гомоцистеина. У людей с гомоцистинурией добавка В6 нормализует повышенный уровень гомоцистеина. Дефицит Вб может замедлить заживления перелома, нарушить рост хряща, вызвать образование дефектной кости и усилить ОП. Вб может влиять на выработку прогестерона и оказывать синергетический эффект на чувствительную к эстрогену ткань. Дефицит Вб распространен даже среди здоровых людей.
• Витамин С: способствует образованию и сшиванию некоторых структурных белков в кости. Дефицит аскорбата может вызвать ОП. Цинга, вызванная дефицитом витамина С, также связана с аномалиями костей.
• Витамины К1 и К2 (менахинон): противовоспалительное действие К1 помогает предотвратить чрезмерную активацию остеокластов. К2 требуется для активации 2 белков, необходимых для регуляции кальция: остеокальцина, который приносит ионы кальция к костной ткани, что способствует образованию кристаллов кальция, и матричного белка Gla, который предотвращает отложение кальция в сосудистой сети. Витамин К2 необходим для формирования, ремоделирования и восстановления костей, потому что остеокальцин является зависимым от витамина К белком. Низкое потребление витамина К увеличивает риск переломов шейки бедра у женщин. Формы витамина К: витамин К1 (филлохинон), МК-4 (форма витамина К) и МК-7 (форма витамина К2 с более длинной цепью). Низкое потребление витамина К связано с повышенной потерей костной массы у пожилых людей. Метаанализ рандомизированных контролируемых исследований добавок К1 или МК-4 в высокой дозе 45 мг/сут (15 мг каждые 6—8 ч) в течение более 6 мес показал снижение потери костной массы. Рекомендуемое потребление: от 90 до 120 мкг в день, однако оптимальная защитная доза и форма витамина К не установлены. В большинстве исследований МК-4 использовался в дозах, в 400 раз превышающих рекомендации для К1, и в них принимали участие исключительно японские женщины в постменопаузальном периоде, что исказило результаты в пользу японской диеты и генетики. МК-7 содержится в натто (самая высокая концентрация в ферментированных соевых бобах) и сыре, а в более низких концентрациях — в мясе и молочных продуктах. Небольшие количества могут вырабатываться полезными для здоровья кишечными бактериями из поступающего с пищей витамина Кр если запасы К1 в организме превышают потребности в выработке факторов свертывания крови. МК-7 является более мощной и биодоступной формой с гораздо более длительным периодом полувыведения, чем МК-4. В качестве ежедневной добавки (0,22 ммоль в день) МК-7 более эффективен в отношении карбоксилирования остеокальцина, чем МК-4. МК-7 показывает более длительное время удержания и более высокий уровень в сыворотке при длительном приеме. Менахиноны с более длинной цепью (МК-7) являются более гидрофобными, увеличивая период полувыведения. У японских женщин в постменопаузальном периоде потребление натго имеет обратную связь с частотой переломов бедра. Вероятной причиной противоречивых клинических результатов является эффект, затрудняющий интерпретацию статуса витамина D. На результаты влияет его дефицит.
• Иприфлавон: полусинтетический изофлавоноид, аналогичный изофлавоноидам сои и одобренный в Японии, Венгрии и Италии для лечения и профилактики ОП. Он продемонстрировал впечатляющие результаты в клинических исследованиях. Иприфлавон (200 мг З раза в день) увеличил измерения МПК на 2 и 5,896 через 6 и 12 мес у женщин с ОП. Иприфлавон (600 мг в день) вызывал увеличение МПК на 696 через 12 мес, в то время как МПК в контрольной группе снизился на 0,3 0/0. Встречающиеся в природе изофлавоноиды, такие как генистеин и даидзеин, содержащиеся в сое, могут обеспечивать аналогичные преимущества. Учитывая преимущества соевых изофлавоноидов против рака молочной железы, рекомендуется употребление соевых продуктов. Механизм действия: усиление действия кальцитонина (см. ранее) на метаболизм кальция. Иприфлавон не оказывает эстрогеноподобного действия. Самое последнее и обширное исследование не показало положительных результатов. Иприфлавон может не играть важную роль в лечении ОП. Он может быть более подходящим для женщин с остеопенией или для профилактики, но не для лечения ОП. Частота снижения количества лимфоцитов и отсутствия эффекта требует тщательного взвешивания риска и пользы. Иприфлавон может быть рекомендован для терапии женщин, у которых другие методы лечения ОП недопустимы, не переносятся или противопоказаны. Необходим мониторинг МПК, чтобы подтвердить пользу; следует контролировать уровень лимфоцитов для выявления побочных эффектов.
Фитотерапия
• Зеленый чай (Camellia sinensis): потребление зеленого чая может защитить от ОП. Зеленый чай богат полифенолами и является основным источником витамина К1. Дозировка: от З до 5 чашек в день, обеспечивающая 250 мг полифенолов (катехинов) ежедневно, или экстракт зеленого чая, обеспечивающий такое же количество полифенолов. Полифенолы зеленого чая нарушали резорбцию кости и стимулировали активность остеобластов в лабораторных экспериментах.
Протокол лечения
Наиболее эффективным подходом к ОП является профилактика. Необходимо оптимизировать пиковую массу кости в молодые годы и минимизировать последующую ее потерю в пожилом возрасте. Чтобы максимизировать пиковую массу кости (даже с наследственными и другими немодифицируемыми факторами риска), необходимы правильный образ жизни, полноценное питание и упражнения с умеренным весом в детстве и подростковом возрасте. Также необходимо исключить курение и чрезмерное потребление алкоголя. Улучшение образа жизни и добавки могут снизить риск у многих женщин, но не у всех. для женщин с уже установленным диагнозом факторы питания и образа жизни служат дополнением к традиционным методам лечения. Основные задачи: предотвратить потерю костной массы и снизить риск переломов. В случаях фактического ОП (в сравнении с остеопенией) необходимо использовать следующие рекомендации в сочетании с соответствующим традиционным лечением, включая отпускаемые по рецепту лекарства:
• упражнения: поднятие тяжестей 4 раза в неделю, а также силовые тренировки и (или) тренировки со свободными весами 2 раза в неделю;
• привычки:
— употребление менее 7 единиц алкоголя в неделю;
— исключение курения, в том числе пассивного;
— меры по предотвращению падений;
рацион: сбалансированная диета с акцентом на достаточное количеств белка; ежедневное употребление соевых изофлавонов, зеленых листовых овощей; достаточное количество кальция, магния, витаминов D и Следует избегать факторов, которые способствуют выведению кальция из организма (например, соль, сахар, избыток белка и безалкогольные напитки).
Биологически активные добавки
• ВМК.
• Основные БАДы:
— кальций: 1000—1200 мг в день;
— магний: 350—500 мг в день;
— витамин В3: от 2000 до 5000 МЕ/сут (измеряют уровень в крови и корректируют дозу соответственно);
— витамин В : 25—50 мг в день;
— фолат, оптимально 5-МТГФ: 800 мкг в день;
— витамин Вт; 800 мкг в день;
— витамин К2 (МК-7): 100 мкг в день;
— рыбий жир: 1000 мг ЭПК и ДГК в день;
— изофлавоноиды сои: 90 мг в день или иприфлавон: 600 мг в день; — стронций: от 170 до 680 мг 1 раз в день (см. описание выше).
Фитотерапевтические средства
• Зеленый чай: от З до 5 чашек в день или экстракт зеленого чая, содержащий от 250 до 300 мг полифенолов (катехинов) в день.
Отрывок из книги «Руководство по натуральной медицине» — Пиццорно Дж. Е., Мюррей М. Т. Купить книгу
Купить книгу «Руководство по натуральной медицине» — Пиццорно Дж. Е., Мюррей М. Т.
В книге рассмотрены актуальные вопросы применения немедикаментозных средств в лечении различных заболеваний. В основу изложения материала положен нозологический принцип, раскрывающий современный взгляд на клиническую картину, этиологию и патогенез различных заболеваний. В отличие от большинства медицинских справочников и руководств, в этом издании представлены основы лечебного питания, которые демонстрируют эффективность и механизмы лечебного действия пищевых и биологически активных веществ. Особое внимание уделено применению в лечебном питании специализированных пищевых продуктов, в частности биологически активных добавок к пище. Освещены механизмы их действия, а также использование в лечении (диетотерапии) сердечно-сосудистых заболеваний, сахарного диабета, ожирения, болезней костно-суставной системы, заболеваний желудочно-кишечного тракта, кожи и других патологий. Наряду с питанием значительное место отведено фитотерапии, физиотерапии, лечебной физкультуре, психологическим методам воздействия. В конце каждого раздела, посвященного определенному заболеванию, приведен краткий протокол лечения немедикаментозными средствами.
Содержание книги «Руководство по натуральной медицине» — Джозеф Е. Пиццорно, Майкл Т.
Алкогольная зависимость
Артериальная гипертензия
Астма
Атеросклероз
Атопический дерматит (экзема)
Афтозный стоматит (афтозные язвы/афтоид/язвенный стоматит)
Аффективные расстройства
Бактериальный синусит
Бесплодие, женское
Бесплодие, мужское
Бессонница
Болезни пародонта
Болезнь Альцгеймера
Болезнь Паркинсона
Бронхит и пневмония
Вагиниты
Варикозное расширение вен
Вирусный гепатит
ВИЧ/СПИД: принципы и методы природной медицины
Воспалительные заболевания кишечника
Воспалительные заболевания органов малого таза
Выпадение волос у женщин
Герпетиформный дерматит
Гипертиреоз
Гипогликемия
Гипотиреоз
Глаукома: острая (закрытоугольная) и хроническая (открытоугольная)
Глютенчувствительная целиакия
Дисплазия шейки матки
Доброкачественная гиперплазия предстательной железы
Желчнокаменная болезнь
Застойная сердечная недостаточность
Здоровье беременных и первичная профилактика болезней у взрослых
Инфекционная диарея
Камни в почках
Кистевой туннельный синдром
Крапивница
Красный плоский лишай
Лейкоплакия
Макулярная дегенерация
Менопауза
Меноррагия
Мигрень
Миома матки
Многоформная эритема
Нарушение пищеварения
Обыкновенные и конглобатные угри
Ожирение
Остеоартроз
Остеопороз
Отит среднего уха
Подагра
Порфирии
Предменструальный синдром
Проктологические заболевания
Простой герпес
Протозойная инфекция кишечника и системные заболевания
Псориаз
Рак: комплексная немедикаментозная поддержка
Рассеянный склероз
Ревматоидный артрит
Розацеа
Сахарный диабет
Себорейный дерматит
Сенильная (возрастная) катаракта
Синдром гипервентиляции / Дисфункциональное дыхание
Синдром дефицита внимания с гиперактивностью
Синдром раздраженного кишечника
Синдром фибромиалгии
Синдром хронической усталости
Стенокардия
Стрептококковый фарингит
Трихомониаз
Фиброзно-кистозная мастопатия
Хронический кандидоз
Цистит
Эндометриоз
Эпилепсия
Язвенная болезнь
Посмотреть примеры страниц из книги «Руководство по натуральной медицине» — Пиццорно Дж. Е., Мюррей М. Т. Купить книгу
Остеопороз. Руководство для врачей
Коллектив авторов, под редакцией проф. О.М. Лесняк
Издательство ГЭОТАР-Медиа, 2016 год
Твердый переплет, 464 страницы, ч/б илл., офсетная бумага
ISBN 978-5-9704-3986-9
Описание:
В руководстве на основе анализа современной литературы и большого клинического опыта представлено современное состояние проблемы диагностики и лечения остеопороза. Многие вопросы, вошедшие в книгу, такие как комбинированная терапия, вторичная профилактика переломов, трабекулярный костный индекс и ряд других, ранее не получили достаточного освещения в отечественной литературе. Авторы руководства — ведущие российские и зарубежные специалисты из различных областей клинической медицины, эксперты в области остеопороза.
Издание предназначено ревматологам, эндокринологам, гинекологам, ортопедам-травматологам, терапевтам, врачам общей практики, специалистам по инструментальной диагностике и другим врачам, в чьей практике встречаются больные с остеопорозом. Оно также будет полезно клиническим ординаторам и студентам медицинских вузов.
Дополнительно:
Оглавление, пример страниц
Дата публикации 9 апреля 2019Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Остеопороз — это хроническое заболевание костей скелета, которое связано с нарушением обмена веществ, проявляется прогрессирующим снижением плотности и нарушением структуры костной ткани и приводит к переломами при минимальной травме (например, при падении с высоты собственного роста).[2][3]
Данное заболевание является настолько актуальным, что Всемирная Организация Здравоохранения назвала остеопороз четвёртой причиной заболеваемости и смертности от хронических неинфекционных заболеваний.[2]
В России каждая третья женщина и каждый пятый мужчина в возрасте 50 лет и старше больны остеопорозом, что составляет 14 миллионов человек.
Переломы при остеопорозе
Остеопороз является «безмолвной эпидемией»: о своём недуге знают менее 1% больных. В результате в нашей стране каждую минуту происходит семь переломов позвонков, а каждые пять минут — один перелом шейки бедра, которые связаны с остеопорозом.[1]
Из-за чего кости становятся хрупкими
В зависимости от причин выделяют первичный и вторичный остеопороз.[4][5]
Первичный остеопороз возникает в 85% случаев. Его разделяют на четыре типа.
| Тип | Характеристики |
|---|---|
| Постменопаузальный | ⠀• возникает у женщин с эстрогенной недостаточностью; ⠀• характеризуется фазой ускоренной утраты костной массы, ⠀⠀прежде всего из трабекулярной кости; ⠀• характерны переломы костей дистального предплечья ⠀⠀и тел звонков |
| Сенильный (старческий) |
⠀• возникает у женщин и мужчин в связи с потерей костной массы ⠀⠀с возрастом; ⠀• появляются переломы кортикальной и трабекулярной кости; ⠀• характерны переломы костей дистального предплечья, ⠀⠀тел позвонков и шейки бедра |
| Ювенильный | ⠀• возникает у детей или молодых людей обоих полов ⠀⠀с нормальной функцией половых желёз; ⠀• начинается в 8-14 лет; ⠀• характерна резкая боль и/или перелом после травмы |
| Идиопатический (возникающий самостоятельно) |
⠀• причины развития неизвестны |
Вторичный остеопороз встречается реже — в 15% случаев. Можно выделить девять причин его возникновения:
- Генетические нарушения:
- почечная гиперкальциурия — одна из важнейших вторичных причин остеопороза;
- болезнь Гоше;
- муковисцидоз;
- несовершенный остеогенез («хрустальные кости»);
- гликогеновая болезнь (накопление гликогена);
- синдром Марфана;
- синдром Элерса — Данлоса («гиперэластичность кожи»);
- гомоцистинурия (нарушенный обмен метионина);
- порфирия (серьёзное нарушение пигментного обмена).
- Состояния, сопровождающиеся гипогонадизмом (нарушением функции половых желёз):
- нервная анорексия и булимия;
- спортивная аменорея (нарушение менструации, связанное с интенсивными тренировками);
- нечувствительность к андрогенам;
- гиперпролактинемия;
- овариэктомия (удаление яичников);
- пангипопитуитаризм (нехватка соматотропного гормона в связи с недостаточностью аденогипофиза);
- преждевременная менопауза (до 40 лет);
- синдром Тернера (аномалия половых хромосом);
- синдром Клайнфельтера (нарушение полового созревания мальчиков, связанное с появлением лишней Х хромосомы).
- Эндокринные расстройства:
- болезнь Иценко — Кушинга;
- сахарный диабет 1 и 2 типа;
- тиреотоксикоз;
- гипогонадизм;
- акромегалия (увеличение количества гормона роста);
- надпочечниковая недостаточность;
- дефицит эстрогена;
- беременность;
- пролактинома (доброкачественная опухоль гипофиза).
- Дефицитные состояния:
- дефицит кальция, магния, белка, витамина D;
- хирургическое лечение ожирения;
- целиакия (непереносимость глютена);
- гастрэктомия (удаление желудка);
- мальабсорбция (недостаточное всасывание питательных веществ в тонком кишечнике);
- мальнутриция (нехватка энергии и белков, получаемых во время приёма пищи);
- парентеральное питание (внутривенное введение питательных веществ);
- первичный билиарный цирроз.
- Нарушения питания:
- избыток витамина А;
- переизбыток соли в рационе.
- Хроническое воспалительные заболевания:
- воспалительные патологии кишечника (болезнь Крона, язвенный колит);
- анкилозирующий спондилоартрит (болезнь Бехтерева);
- ревматоидный артрит;
- системная красная волчанка.
- Заболевания крови:
- гемохроматоз (нарушенный обмен железа);
- гемофилия (нарушение свёртываемости крови)
- лейкоз (рак, поражающий кровь и костный мозг);
- лимфома (рак белых кровяных клеток);
- множественная миелома (опухоль, состоящая из изменённых плазматических клеток крови);
- серповидноклеточная анемия (наследственная болезнь крови);
- системный мастоцитоз (избыток тучных клеток);
- талассемия (нарушение выработки гемоглобина);
- метастатическая болезнь.
- Приём лекарственных средств:
- противосудорожные препараты;
- антипсихотические препараты;
- антиретровирусные препараты;
- ингибиторы ароматазы;
- химиотерапевтические препараты;
- фуросемид;
- преднизон (более 5 мг в день на протяжении трёх месяцев и дольше);
- гепарин (длительно);
- гормональная или эндокринная терапия: агонисты гонадотропин-рилизинг-гормона (GnRH), аналоги лютеинизирующего рилизинг-гормона (LHRH), депомедроксипрогестерон, избыточные дозы тироксина;
- литий;
- антидепрессанты (СИОЗС);
- антациды, содержащие алюминий («Альмагель»);
- ингибиторы протонной помпы (омепразол, лансопрозол).
- Другие состояния:
- алкоголизм;
- амилоидоз (внеклеточное отложение белка);
- хронический метаболический ацидоз (увеличение кислотности);
- хроническая сердечная недостаточность;
- депрессия;
- хроническая обструктивная болезнь лёгких, эмфизема (избыточное скопление воздуха в лёгких);
- хроническая болезнь почек, терминальная стадия хронической почечной недостаточности;
- хроническая патология печени;
- ВИЧ, СПИД;
- иммобилизация (неподвижность, фиксация части тела);
- рассеянный склероз;
- трансплантация органов;
- саркоидоз;
- невесомость.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы остеопороза
Заболевание на начальных этапах не сопровождается какими-либо проявлениями, поэтому чаще всего пациент с этим заболеванием обращается к врачу только после перелома при минимальной травме, который и становится первым признаком остеопороза.
Типичными местами переломов при остеопорозе являются:
- позвонки — 46%;
- шейка бедра — 20%;
- плечо и предплечье — 15%;
- остальные локализации — 19%.
Другие симптомы остеопороза проявляются, как правило, уже после множественных компрессионных переломов в телах позвонков. Они включают в себя следующие проявления:
- снижение роста;
- выступающий вперёд живот;
- рефлюксная болезнь (боли за грудиной, изжога);
- раннее насыщение при еде;
- снижение веса;
- ограничение движений;
- боли в спине и тазобедренных суставах;
- увеличение расстояния от стены до затылка, перерастяжение шеи, согбенность;
- соприкосновение рёбер с тазом.
Скелет человека при остеопорозе:
Кроме того, необходимо обращать внимание на наличие симптомов заболеваний, приводящих ко вторичному остеопорозу, которые достаточно специфичны для каждого состояния.[8]
Факторы риска
В связи с поздним появлением признаков остеопороза, важно учитывать и выявлять факторы риска заболевания.[4][5] Они бывают изменяемыми и неизменяемыми.
| Неизменяемые | Изменяемые |
|---|---|
| ⠀• женский пол; ⠀• переломы в возрасте > 50 лет; ⠀• возраст > 65 лет; ⠀• переломы шейки бедра ⠀⠀у близких родственников; ⠀⠀(матери, отца, сестры/брата) ⠀⠀в возрасте от 50 лет; ⠀• некоторые хронические заболевания; ⠀• ранняя (в том числе и хирургическая) ⠀⠀менопауза; ⠀• приём препаратов глюкокортикоидов ⠀⠀(преднизолона) более трёх месяцев; ⠀• длительный постельный режим ⠀⠀(дольше двух месяцев) |
⠀• недостаточное потребление кальция; ⠀• дефицит витамина D; ⠀• низкая физическая активность; ⠀• склонность к падениям ⠀⠀(головокружение, плохое зрение); ⠀• низкий вес — индекс массы тела ⠀⠀менее 20 кг/м2 и/или масса тела ⠀⠀менее 57 кг; ⠀• курение; ⠀• злоупотребление алкоголем |
Патогенез остеопороза
В течение нашей жизни кость непрерывно претерпевает изменения (ремоделирование) в ответ на микротравмы. Они происходят в различных местах скелета и включают в себя процесс рассасывания кости (резорбцию) и последующего образования костной ткани.[6]
В организме взрослого человека существует два типа костной ткани:
- плотный кортикальный — внешняя часть костных структур;
- губчатый (трабекулярный) — внутренний, основной слой костных структур.
Они отличаются по своей архитектуре, но сходны по молекулярному составу: оба типа костей состоят из клеток и внеклеточного костного вещества (матрикса). Матрикс представлен минералами (в основном, солями кальция) и неминеральными компонентами (20% коллагена и 8% воды).
Механические свойства кости зависят от состава и архитектуры внеклеточного вещества. Сила кости определяется белком коллагеном (эластичность, прочность при сгибании и скручивании) и минеральными составляющими (прочность при сжатии). Чем больше концентрация кальция, тем больше устойчивость кости к сжатию.
В костной ткани содержится четыре вида клеток:
- остеоциты;
- остеобласты;
- остеогенные клетки;
- остеокласты.
Остеокласты отвечают за резорбцию кости, то есть за ее разрушение, в то время как остеобласты отвечают за формирование костной ткани. Оба эти вида клеток связаны друг с другом в процессе ремоделирования костной ткани.
Остеобласты не только образуют костную ткань и отвечают за её минерализацию, но и контролируют резорбцию костной ткани, проводимую остеокластами.
Остеоциты — это клетки, которые являются конечной формой дифференцировки остеобластов и занимаются минерализацией костной ткани после завершения ремоделирования кости.
При остеопорозе взаимосвязь между остеокластами и остеобластами нарушается, и утрачивается способность непрерывного восстановления трабекулярной кости в ответ на продолжающиеся микротравмы. В итоге остеокласты рассасывают кость в течение недель, в то время как остеобластам требуются месяцы для производства новой костной ткани. Таким образом, любое состояние, которое повышает скорость ремоделирования костей, вызывает потерю костной массы.
Пик костной массы приходится на третью декаду жизни человека. С возрастом её показатель постепенно снижается. Поэтому неспособность накопления оптимальной костной массы в молодости является основным фактором, способствующим появлению остеопороза. Вот почему у некоторых женщин в постменопаузе обнаруживается небольшое снижение плотности костной ткани, а у других — остеопороз.
Также для накопления костной массы важны питание и физическая активность в процессе роста и развития. Однако основную роль играют генетические факторы, так как именно от них зависит, какими будут возможные значения максимальной костной массы и силы у каждого конкретного человека.[7]
Классификация и стадии развития остеопороза
Помимо классификации остеопороза по причинному фактору для сбора статистической информации используется также классификация МКБ-10 (Международная классификация болезней).[9] Согласно ей, выделяют постменопаузальный остеопороз с патологическим переломом (M80.0) и без него (M81.0), а также остеопороз при эндокринных нарушениях (M82.1).
Постменопаузальный остеопороз различают по причинам, вызвавшим его:
- остеопороз, возникший после удаления яичников (M80.1, M81.1);
- остеопороз, вызванный обездвиженностью (M80.2, M81.2);
- остеопороз, спровоцированный нарушением всасывания в кишечнике (M80.3) и оперативным вмешательством (M81.3);
- лекарственный остеопороз (M80.4, M81.4);
- идиопатический остеопороз (M80.5, M81.5);
- другой остеопороз с патологическим переломом (M80.8) и без него (M81.8);
- неуточнённый остеопороз с патологическим переломом (M80.9) и без (M81.9).
Помимо прочего возможно развитие остеопороза смешанного характера, к примеру, у женщины в постменопаузе на фоне длительного приёма глюкокортикоидов по поводу лечения серьёзного заболевания, которое само по себе может привести к возникновению вторичного остеопороза.
Остеопороз может быть равномерным и очаговым (его ещё называют локализованным, или пятнистым). Второй тип остеопороза чаще встречается не как самостоятельное заболевание, а как последствие иммобилизации, после травм или хирургических вмешательств.
Частота остеопоротических переломов по локализации:
- позвонки – 46 %;
- шейка бедренной кости – 20 %;
- плечо и предплечье – 15 %;
- остальные локализации – 19 %.
Степени остеопороза
Стадии изменения плотности костной ткани:
- Норма — при исследовании минеральной плотности костной ткани с помощью двухэнергетической рентгеновской денситометрии (DXA) Т-критерий выше −1,0 SD.
- Остеопения — это начальное снижение плотности костной ткани (T-критерий между −1,0 и −2,5 SD). Остеопения не всегда переходит в остеопороз, однако при её выявлении рекомендовано предпринять меры, направленные на снижение риска развития остеопороза и связанных с ним переломов.
- Остеопороз (Т-критерий равен или ниже −2,5 SD).
В некоторых источниках встречается классификация остеопороза по поражению суставов, например остеопороз коленного или тазобедренного сустава. Врачи такую классификацию не используют, к тому же остеопороз поражает не суставы, а кости.
Осложнения остеопороза
Осложнения остеопороза связаны, прежде всего, с последствиями переломов.
Компрессионные переломы позвонков часто возникают при минимальном напряжении, например, при кашле, подъёме или сгибании. Чаще всего страдают позвонки среднего и нижнего грудного и верхнего поясничного отделов позвоночника. У многих пациентов перелом позвонка может возникать постепенно и не сопровождаться симптомами.
Переломы бедра являются наиболее травматичными, чаще всего происходят в шейке бедра и в межвертельной области. Такие переломы обычно возникают при падениях на бок. Осложнениями переломов бедра могут стать внутрибольничные инфекции и тромбоэмболия лёгочной артерии.[10]
Все переломы могут повлечь за собой дальнейшие осложнения, включая хроническую боль от компрессионных переломов позвоночника и увеличение заболеваемости и смертности. Пациенты с множественными переломами страдают от сильных болей, которые приводят к ограничению возможностей и низкому качеству жизни. Они также подвержены риску осложнений, связанных с обездвиженностью после перелома: тромбоз глубоких вен и пролежни.
У пациентов с множественными переломами позвонков, которые приводят к тяжёлой деформации грудной клетки, развивается хроническое нарушение функции дыхания.
У пациентов с остеопорозом костей развиваются деформации позвоночника и «вдовий горб», что приводит к снижению роста на 3-5 см. В сочетании с хронической болью и снижением функциональных возможностей это может вызвать снижение самооценки и стать причиной депрессии.[1][11]
Диагностика остеопороза
При диагностике необходимо обратить внимание на несколько моментов:
- Остеопороз может развиваться у людей с отсутствием или немногочисленными факторами риска этого заболевания.
- Важно выявлять остеопороз до появления симптомов, то есть до развития его осложнений.
- Даже если перед нами женщина в постменопаузе или пожилой пациент, требуется исключить причины вторичного остеопороза.
В связи с этим скрининг населения, входящего в группы риска развития остеопороза, играет очень большую роль.
Собственно говоря, опрос пациента для выяснения его жалоб, истории заболевания и жизни, а также клинический осмотр необходимы именно для того, чтобы определить риски переломов в будущем и исключить другие заболевания, которые могли привести к остеопорозу.[5]
В настоящее время для оценки 10-летней вероятности появления переломов при минимальной травме рекомендован инструмент FRAX. Он представлен в виде бесплатного ресурса в интернете, и любой врач может сразу же на приёме оценить риски осложнений остеопороза у своего пациента.[12] В особенности данный скрининг рекомендуется проходить всем женщинам в постменопаузе и мужчинам старше 50 лет.[4]
Как проверить наличие остеопороза
Обследование пациента должно включать в себя следующие методы диагностики:[4][12]
- Измерение роста и массы тела с расчётом индекса массы тела.
- Клинический осмотр для выявления заболеваний, которые могут привести к развитию остеопороза, а также признаков компрессионных переломов позвонков.
- Инструментальная диагностика:
- рентгенография грудного и поясничного отделов позвоночника (Th4 — L5) — проводится в левой боковой проекции с целью обнаружения компрессионных переломов тел позвонков.
- двухэнергетическая рентгеновская абсорбциометрия (DXA или DEXA, предпочтительнее использование термина DXA) — низкодозовая рентгенография костей скелета для измерения минеральной плотности костной ткани. Используется как для диагностики остеопороза, так и для контроля лечения.
- Лабораторная диагностика — рекомендуется всем пациентам с остеопорозом, которые установлен впервые, а также в случае неэффективного лечения, проводимого ранее.
- Консультации различных специалистов.[5]
Как проверить, есть ли остеопороз с помощью денситометрии
Методика двухэнергетической рентгеновской денситометрии сочетает высокую чувствительность, специфичность и точность со сверхмалой дозой облучения.
Проведение денситометрии показано:
- женщинам старше 65 лет;
- женщинам до 65 лет при наступлении менопаузы;
- женщинам, имеющим факторы риска — остеопороз в семейном анамнезе, низкий индекс массы тела, употребление табака и/или приём препаратов с высоким риском потери костной ткани (например, глюкокортикоидов);
- пациенты, у которых по данным предыдущих исследований зарегистрирована пониженная плотность костной ткани или случайно обнаружены бессимптомные компрессионные переломы позвоночника;
- пациенты с риском вторичного остеопороза [18].
Направление на денситометрию выписывает лечащий врач. Процедура безболезненная и занимает 15-20 минут. Для получения чёткого изображения пациент во время исследования должен сохранять неподвижность.
Лабораторная диагностика предполагает различные исследования. К базовым относятся:
- клинический анализ крови;
- биохимический анализ крови — общий белок, мочевина, креатинин, подсчет СКФ, печёночные пробы (билирубин, АЛТ, АСТ, ГГТП, щелочная фосфатаза), кальций, фосфор, магний;
- ТТГ (тиреотропный гормон);
- 25-гидроксивитамин D .
Дополнительные исследования направлены на выявление вторичного остеопороза. Они проводятся при наличии характерных симптомов и у отдельных групп пациентов по назначению врача и включают в себя определение следующих показателей:
- кальций суточной мочи ;
- паратиреоидный гормон;
- тестостерон и гонадотропины;
- свободный кортизол в моче;
- СРБ, ревматоидный фактор;
- электрофорез белков в сыворотке крови;
- биопсия костного мозга;
- антитела к тканевой трансглутаминазе;
- гомоцистеин;
- пролактин;
- гистамин в моче и т. д.
Биохимические маркеры костного обмена определяют исходно и спустя три месяца от начала лечения. Для этого достаточно оценить один из двух маркеров, но только одним и тем же лабораторным набором:
- маркеры костеобразования (костноспецифическая щелочная фосфатаза, остеокальцин, N-концевой проколлаген 1 типа);
- маркеры костной резорбции (пиридин и дезоксипиридинолин, C- и N-концевые телопептиды коллагена 1 типа).
Пациент с подозрением на остеопороз, а также с установленным диагнозом и получающий лечение находится под наблюдением врача терапевта и должен быть консультирован ревматологом и/или эндокринологом. Эти специалисты помогут провести необходимые лабораторные и инструментальные исследования, чтобы исключить причины вторичного остеопороза.
Пациенты с неконтролируемой болью, которые не отвечают на стандартную терапию, должны быть консультированы специалистом по лечению боли. В случае вопроса о необходимости коррекции после переломов может понадобиться консультация хирурга или ортопеда.
Таким образом, диагноз остеопороза ставится только на основании низкотравматического перелома, снижения минеральной плотности костной ткани или совокупности факторов риска (инструмент FRAX), а лабораторные исследования служат для исключения других заболеваний скелета, приводящих к вторичному остеопорозу.
Лечение остеопороза
Цели лечения:[4][12]
- предотвращение или снижение количества переломов;
- повышение плотности костной ткани;
- улучшение показателей маркеров костного ремоделирования.
В первую очередь для профилактики переломов при остеопорозе требуется соблюдать меры коррекции образа жизни:[12][13]
- увеличение массы и выполнение упражнений для укрепления мышц и улучшения равновесия;
- обеспечение оптимального потребления кальция и витамина D в качестве дополнения к активной терапии.
Медикаментозное лечение
Лекарственная терапия остеопороза назначается женщинам в постменопаузе и мужчинам в старше 50 лет в следующих случаях:[4]
- перелом бедра или позвонка;
- результаты обследования DXA — Т-критерий равен или меньше –2,5 SD для шейки бедра или позвонков после исключения причин вторичного остеопороза;
- низкая костная масса (T-критерий между –1,0 и –2,5 SD для шейки бедра или позвоночника) и 10-летняя вероятность по шкале FRAX 3% или более для перелома бедра или 20% и более для крупного остеопоротического перелома).
Федеральные клинические рекомендации по диагностике, лечению и профилактике остеопороза предусматривают применение:[4]
- антирезорбтивных препаратов — направлены на подавление костной резорбции, действуя на остеокласты (бисфосфонаты, деносумаб);
- анаболических препаратов — направлены на усиление костеобразования (терипаратид).
БИСФОСФОНАТЫ
Эти препараты нарушают работу остеокластов, препятствуя разрушению кости. Накапливаясь в костной ткани, они оказывают отсроченное влияние с сохранением эффекта в течение месяцев после отмены лечения.
Нежелательные явления. При применении бисфосфонатов внутрь возможны неблагоприятные явления со стороны ЖКТ — трудности при глотании, эзофагит и гастрит. При внутривенном введении бисфосфонатов может возникнуть гриппоподобная реакция — повышение температуры тела, боли в суставах и мышцах, слабость и т. д. Выраженность таких симптомов значительно уменьшается после повторных внутривенных введений, а их полное исчезновение наступает через 2-3 дня. Облегчить течение гриппоподобной реакции можно с помощью нестероидных противовоспалительных средств. В редких случаях на фоне длительного применения бисфосфонатов (более пяти лет) возникали случаи остеонекроза челюсти.
Противопоказания и ограничения:
- гипокальциемия;
- тяжёлые нарушения функции почек (клиренс креатинина менее 35 мл/мин);
- нарушение минерального обмена (дефицит витамина D, остеомаляция, гипофосфатазия, гипофосфатемия);
- грудное вскармливание;
- дети и подростки до 18 лет.
Приём бисфосфонатов внутрь противопоказан при заболеваниях пищевода, нарушающих его проходимость, неспособности человека находиться в вертикальном положении в течение 30 минут. Эти препараты с осторожностью используются при заболеваниях ЖКТ в фазе обострения.
Применение. Все препараты бисфосфонатов в форме таблеток (алендронат, ризендронат, ибандронат) принимаются утром натощак за 30 минут до еды. Таблетка запивается стаканом воды, после чего необходимо находиться в вертикальном положении около 30-40 минут, не принимая пищу или жидкость, кроме воды.
Препараты для внутривенного введения применяют раз в три месяца (ибандронат) или раз в год (золедронат).
ДЕНОСУМАБ
Этот препарат разработан для блокирования процесса привлечения активных остеокластов. В отличие от бисфосфонатов, деносумаб снижает выработку остеокластов, но при этом функция зрелых клеток не нарушается. Препарат не накапливается в костной ткани, его действие прекращается после лечения. Он безопасен при нарушении функции почек.
Деносумаб выпускается в виде шприц-ручки, вводится подкожно раз в шесть месяцев.
Возможные нежелательные явления:
- кожные реакции;
- вздутие;
- гипокальциемия.
Противопоказания:
- гипокальциемия;
- повышенная чувствительность к препарату;
- беременность или лактация.
ТЕРИПАРАТИД
Данный препарат оказывает преимущественное действие на остеобласты, повышая продолжительность их жизни. Таким образом он усиливает костеобразование и активирует моделирование в отдельных участках скелета. Рекомендован для использования пациентами с тяжёлой формой остеопороза и при неэффективности лечения другими препаратами.
Терипаратид применяется подкожно по 20 мг один раз в сутки ежедневно, хранится в холодильнике.
Нежелательные явления: головокружение, судороги в ногах.
Противопоказания:
- гиперкальциемия;
- гиперпаратиреоз;
- остеогенная саркома;
- незакрытые зоны роста;
- облучение скелета в анамнезе;
- беременность или лактация;
- злокачественное образование костной ткани или метастазы в кости;
- аллергическая реакция к препарату.
КАЛЬЦИЙ И ВИТАМИН D
Все препараты, направленные на борьбу с остеопорозом, принимать в сочетании с препаратами кальция (500-1000 мг/сут) и витамина D (800-1000 МЕ/сут), так как эффективность такой комбинации подтверждена клинически.
Кроме того, проводится лечение потенциально устранимых причин вторичного остеопороза в случае их обнаружения.
АНАЛЬГЕТИКИ
Еще одна цель лечения пациентов с остеопоротическим переломом — контроль боли, которая бывает весьма выраженной при компрессионных переломах позвонков и серьёзно нарушает качество жизни. В таком случае назначаются обезболивающие препараты, которые принимаются внутрь в виде таблеток или капсул по мере необходимости или на регулярной основе. Также для обезболивания применяют физиотерапию и чрескожную электронейростимуляцию.[5]
Иные способы лечения
Хороший эффект в лечении остеопороза даёт механическая поддержка позвоночника и, в некоторых случаях, ортезы для грудного отдела позвоночника (ортопедические корсеты). Они выполняют опорную функцию, снимая часть осевой нагрузки с грудного и поясничного отделов позвоночника, и ограничивают движения в позвоночнике. Рекомендуется надевать ортез, если пациент намеревается ходить или стоять более часа, но при этом важно ограничивать время ношения, поскольку длительная иммобилизация способствует деминерализации костей.
Хирургическое лечение применяется при переломе шейки бедра, а также при выраженных деформациях грудной клетки, возникших на фоне множественных компрессионных переломов позвонков.
В период реабилитации после переломов рекомендованы занятия со специалистом по лечебной физкультуре (ЛФК), дыхательная гимнастика, упражнения на укрепление грудных и межрёберных мышц.[12]
Прогноз. Профилактика
При своевременном обнаружении и лечении остеопороза прогноз благоприятный. В то же время остеопоротические переломы сопровождаются ограничением трудоспособности (от временного до постоянного). Поэтому при оценке прогноза необходимо учитывать имеющиеся статистические данные,[1] чтобы акцентировать внимание населения, органов управления и медицинских работников на мерах профилактики:
- Смертность от остеопоротических переломов в первый год составляет 45-52%.
- При этом в первые три месяца после перелома погибает каждый третий пациент.
- Из выживших 33% остаются прикованными к постели, 42% — ограниченно активными, и только 15% выходят из дома.
- К прежнему уровню активности, который был до перелома, возвращается лишь 9% пациентов.
В связи с этим, при остеопорозе с высоким риском переломов рекомендуется ограничить длительные нагрузки на опорно-двигательный аппарат для уменьшения риска компрессионных переломов позвонков, а также ограничить виды деятельности, которые могут привести к падениям, чтобы уменьшить риск переломов дистального предплечья и бедра.
Можно ли вылечить остеопороз
Остеопороз — это хроническое заболевание костей скелета, поэтому вылечить его полностью нельзя. Однако меры профилактики могут замедлить снижение плотности костной ткани.
Профилактика остеопороза
Первичная профилактика остеопороза начинается в детстве. Для создания необходимой пиковой костной массы и прочности костей необходимо употреблять достаточное количество кальция и витамина D[14] и регулярно быть физически активным.[15]
В среднем возрасте профилактика остеопороза заключается в поддержании костной массы, а в старшем возрасте она направлена ещё и на предупреждение падений и раннее выявление и лечение остеопороза с целью профилактики переломов.
Пять шагов к профилактике остеопороза:
- Принимайте рекомендованное количество кальция и витамина D каждый день.
- Поддерживайте физическую активность, улучшайте мышечную силу и равновесие.
- Избегайте курения и употребления алкоголя.
- Обратитесь к врачу, чтобы определить свой уровень риска.
- Определите плотность костной ткани.
Суточная потребность в кальции и витамине D3 [14][16]
| Возрастные группы | Потребность в кальции |
Потребность в витамине D3 |
|---|---|---|
| Подростки с 12 лет | 1200-1500 мг | 200-400 МЕ |
| Беременные и кормящие женщины | 1200-1500 мг | 200-400 МЕ |
| Женщины 25-50 лет | 1000 мг | 200-400 МЕ |
| Женщины после менопаузы (старше 50 лет) |
1000-1500 мг | 800 МЕ |
| Пожилые люди | 1500 мг | 800-2000 МЕ |
Содержание кальция в 100 г продуктов[14]
| Молочные продукты: молоко 3% — 100 мг молоко 1 % — 120 мг творог — 95 мг плавленый сыр — 300 мг твёрдый сыр — 600 мг сметана — 100 мг козий сыр — 300 мг йогурт — 120 мг |
Фрукты и орехи: апельсины — 51 мг сушёные яблоки — 45 мг инжир — 57 мг курага — 170 мг изюм — 56 мг миндаль — 254 мг арахис — 70 мг кунжут — 1150 мг |
|---|---|
| Овощи зеленые: семена подсолнечника — 100 мг салат — 83 мг капуста — 60 мг сельдерей — 240 мг лук — 60 мг фасоль — 40 мг оливки — 77 мг |
Рыба, мясо и хлеб: вяленая рыба с костями — 3000 мг сардина с костями — 350 мг рыба отварная — 20-30 мг говядина — 10-30 мг ржаной хлеб— 60 мг пшеничный хлеб — 30 мг |
Источники витамина D[14]
| Источник | Содержание витамина D в 100 г |
|---|---|
| Лосось дикий | 700-800 МЕ D3 |
| Лосось искусственно выращенный | 100-250 МЕ D2 или D3 |
| Лосось консервированный | 300-600 МЕ D3 |
| Консервированные сардины | 300 МЕ D3 |
| Рыбий жир из трески (одна чайная ложка) | 400-1000 МЕ D3 |
| Яичный желток | 20 МЕ D2 или D3 |
Вторичная профилактика — это комплекс мер, которые применяются, когда заболевание уже установлено. Они направлены на борьбу с его осложнениями, т. е. на предотвращение переломов, и включают в себя:
- Обучение — это важный шаг в контроле своего заболевания.
- Физическая активность — помогает улучшить координацию, мышечную силу, увеличить плотность костной ткани.
- Диета и правила питания — разнообразие рациона, достаточное употребление белка, обогащение питания кальцием и витамином D.
- Отказ от вредных привычек — избегать курения и употребления алкоголя.
- Меры для достижения сохранности пациента — контроль зрения, обеспечение безопасности дома (хорошая освещённость, незагромождённость проходов, использование нескользких ковриков, наличие поручней в ванной, расположение нужных вещей в пределах досягаемости) для предотвращения падения.[17]
Остеопороз, Руководство для врачей, Наумов А.В., Верткин А.Л., 2015.
Остеопороз, лидер среди заболеваний костей и суставов, требует особенно взвешенного подхода в терапии. Недостаточная диагностика и побочные эффекты от медикаментозной профилактики, затрагивающие коронарные артерии, — вот только некоторые из актуальных проблем ведения больных с таким диагнозом.
А.Л. Вёрткин и соавторы детально рассматривают патогенез, диагностику и фармакотерапию остеопороза в неразрывной связи с кардиологическими рисками.
Клинические случаи, данные актуальных исследований и сравнительный анализ схем по профилактике и лечению остеопороза, а также практические рекомендации делают пособие незаменимым в практике терапевтов, травматологов, ревматологов и ортопедов.
Выводы после изучения официальных данных.
Итак, приведенные сведения демонстрируют шокирующий диссонанс между официальными данными и результатами исследований на малых и ограниченных выборках. Однако стоит отметить, что результаты исследований ограниченных выборок более точно соответствуют результатам международных эпидемиологических работ.
Наиболее важной клинико-практической стороной приведенных сведений является КРАЙНЕ НЕ ДОСТАТОЧНАЯ РУТИННАЯ ДИАГНОСТИКА ОСТЕОПОРОЗА.
Это свидетельствует об отсутствии «нацеленности» у практикующих врачей на скрининг и профилактику этого социального заболевания. Вероятно, именно в этом и кроется сложность проблемы остеопороза в практической медицине.
Столь высокий рейтинг остеопороза по медико-социальной значимости обусловлен, в первую очередь, его высокой распространенностью и тяжестью исходов. Эти два обстоятельства сопряжены с увеличением продолжительности жизни и, соответственно, нарастанием инволюционных изменений в организме.
Сегодня мы являемся свидетелями существенного разрыва между теоретическими знаниями о проблеме остеопороза и его последствий и практической реализации этих знаний.
В самом деле, в 2006 г. опубликованы первые, а в 2009-м пересмотренные и дополненные клинические рекомендации Российской ассоциации остеопороза по ведению больных с данным заболеванием, этому предшествовали материалы других Европейских и международных обществ, изучающих вопросы диагностики, профилактики и лечения ОП.
СОДЕРЖАНИЕ.
Ключевые слова и список сокращений.
Введение.
Остеопороз в клинической практике.
Эпидемиология остеопороза и остеопоротических переломов: информация к размышлению.
Эпидемиология переломов в РФ.
Выводы после изучения официальных данных.
Ключевые звенья патогенеза остеопороза.
Остеобластогенез.
Остеокластогенез.
Патология.
Патогенетические взаимосвязи кардиоваскулярных заболеваний и остеопороза.
Общие патогенетические механизмы.
Костные морфогенетические белки (BMP).
Сигнальный путь RANKL-RANK-OPG.
Сигнальный путь Wnt.
Матриксный Gla-белок.
Витамин К.
Фосфаты.
Катепсины.
Остеопонтин.
Паратиреоидный гормон.
Витамин D.
Дислипидемия.
Ренин — ангиотензин — альдостероновая система.
Выводы.
Клиническая фармакология препаратов для лечения остеопороза.
Бисфосфонаты 61
Остеонекроз верхней и/или нижней челюстей.
Противопоказания для применения бисфосфонатов.
Алендронат.
Золедронат.
Ибандронат.
Спектр редких и неожиданных неблагоприятных реакций бисфосфонатов.
Классификация и характеристика неблагоприятных реакций.
Бисфосфонаты.
Редкие HP верхних отделов ЖКТ. рак пищевода и желудка.
Неожиданные HP при приеме БФ — фибрилляция предсердий.
Остеонекроз челюсти.
Подвертельные переломы.
Препараты заместительной гормональной терапии и их производные.
Клиническая фармакология.
Селективные модуляторы эстрогенных рецепторов (СМЭР).
Препараты, стимулирующие костное новообразование.
Выбор лекарств, полипрагмазия и актуальные сведения: «простота и сложность» фармакологической коррекции риска переломов вследствие остеопороза.
Кардиоваскулярный риск и терапия кальцием.
Терапия витамином D.
Сравнительная терапия показаний для назначения препаратов для профилактики и лечения остеопороза.
Фармакотерапия пациентов с сочетанием остеоартроза и остеопороза.
Рекомендации по фармакотерапии остеопороза.
Физическая активность / отсутствие физической активности.
Список литературы.
Купить
.
По кнопкам выше и ниже «Купить бумажную книгу» и по ссылке «Купить» можно купить эту книгу с доставкой по всей России и похожие книги по самой лучшей цене в бумажном виде на сайтах официальных интернет магазинов Лабиринт, Озон, Буквоед, Читай-город, Литрес, My-shop, Book24, Books.ru.
По кнопке «Купить и скачать электронную книгу» можно купить эту книгу в электронном виде в официальном интернет магазине «ЛитРес», и потом ее скачать на сайте Литреса.
По кнопке «Найти похожие материалы на других сайтах» можно найти похожие материалы на других сайтах.
On the buttons above and below you can buy the book in official online stores Labirint, Ozon and others. Also you can search related and similar materials on other sites.
Дата публикации: 22.09.2020 06:28 UTC
Теги:
учебник по медицине :: медицина :: Наумов :: Верткин
Следующие учебники и книги:
- Клиническая электроэнцефалография, Фармакоэлектроэнцефалография, Неробкова Л.Н., Авакян Г.Г., Воронина Т.А., Авакян Г.Н., 2018
- Острый тромбофлебит, Кириенко А.И., Матюшенко А.А., Андрияшкин В.В., 2006
- Клиническая фармакология, Кукес В.Г., Сычев Д.А., 2017
- Клиническая фармакология в педиатрии, Учебное пособие, Булатов В.П., 2006
Предыдущие статьи:
- Основы ухода за хирургическими больными, Глухов А.А., Андреев А.А., Болотских В.И., Боев С.Н., 2008
- Основы реаниматологии и анестезиологии для медицинских колледжей, Зарянская В.Г., 2015
- Основы патологии заболеваний по Роббинсу и Котрану, Том 1, Кумар В., Аббас А.К., Фаусто Н., Астер Дж.К., 2014
- Основы патологии заболеваний по Роббинсу и Котрану, Том 3, Кумар В., Аббас А.К., Фаусто Н., Астер Дж.К., 2016

















 и назначается курсом в лечебных дозах с последующим переводом на профилактическую терапию (Табл. 9) [237-244].
и назначается курсом в лечебных дозах с последующим переводом на профилактическую терапию (Табл. 9) [237-244].