Российское национальное руководство «Приверженность лечению»
Сетевое научное издание
ГБУЗ НИИ СП им. Н.В. Склифосовского / НИИ педиатрии ЦКБ РАН / ФБУН Центральный НИИ эпидемиологии Роспотребнадзора / ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России / ФГАОУ ВО НИУ БелГУ / ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России / ФГАОУ ВО РУДН / ФГБНУ Научный центр неврологии / ФГБНУ НИИ КПССЗ / ФГБНУ Томский НИМЦ РАН / ФГБНУ ФНКЦ РР / ФГБНУ НЦПЗРЧ / ФГБНУ РНЦХ им. Б.В. Петровского / ФГБОУ ВО ВГМУ Минздрава России / ФГБОУ ВО КГМУ Минздрава России / ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России / ФГБОУ ВО МГУ им. М.В. Ломоносова / ФГБОУ ВО МГУПП / ФГБОУ ВО ОмГМУ Минздрава России / ФГБОУ ВО НИМГУ им. Н.П. Огарева / ФГБОУ ВО ОрГМУ
Минздрава России / ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России / ФГБОУ ВО «РАНХиГС при Президенте Российской Федерации» / ФГБОУ ВО РостГМУ Минздрава России / ФГБОУ ВО РязГМУ Минздрава России / ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России / ФГБОУ ВО СГМУ Минздрава России / ФГБОУ ВО СЗГМУ
им. И.И. Мечникова / ФГБОУ ВО СибГМУ Минздрава России / ФГБОУ ВО СтГМУ Минздрава России / ФГБОУ ВО Тверской ГМУ Минздрава России / ФГБОУ ВО УГУ / ФГБОУ ВО ЮУГМУ Минздрава России / ФГБОУ ДПО РМАНПО Минздрава России / ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России / ФГБУ НМХЦ им. Н.И. Пирогова Минздрава России / ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России / ФГБУ «НМИЦ кардиологии им. Е.И. Чазова» Минздрава России / ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России / ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России / ФГБУ НМИЦ ПН им. В.М. Бехтерва Минздрава России / ФГБУ НМИЦ АГП им. В.И. Кулакова, ФГБУ «НМИЦ ТПМ» Минздрава России / ФГБУ «НМИЦ ФПИ» Минздрава России / ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России / ФГБУ «ГВКГ им. Н.Н. Бурденко» Минобороны России / ФГБУ «ЦЭККМП» Минздрава России
Редакционный совет
д.м.н. Николаев Н.А., акад. РАН Мартынов А.И., к.м.н. Скирденко Ю.П., акад. РАН Авдеев С.Н., чл.-корр. РАН Анисимов В.Н., чл.-корр. РАН Арутюнов Г.П., акад. РАН Ашрафян Л.А., проф. Бабунашвили А.М., чл.-корр. РАН Балыкова Л.А., акад. РАН Барбараш О.Л., проф. Васильева И.А., д.м.н. Виноградов О.И., акад. РАН Гинцбург А.Л., акад. РАН Горелов А.В., акад. РАН Драпкина О.М., акад. РАН Иоселиани Д.Г., акад. РАН Карпов Р.С., чл.-корр. РАН Кобалава Ж.Д., акад. РАН Конради А.О., проф. Лазебник Л.Б., чл.-корр. РАН. Ливзан М.А., акад. РАН
Мазуров В.И., чл.-корр. РАН Мартов А.Г., чл.-корр. РАН Марьяндышев А.О., чл.-корр. РАН Моисеев С.В., акад. РАН Намазова-Баранова Л.С., проф. Незнанов Н.Г., проф. Омельяновский В.В., акад. РАН Петров В.И., акад. РАН Поддубная И.В., акад. РАН Полушин Ю.С., акад. РАН Попов С.В., акад. РАН Ройтберг Г.Е., проф. Ройтман Е.В., чл.-корр. РАН Румянцев С.А., чл.-корр. РАН Рычкова Л.В., чл.-корр. РАН Скворцова В.И., чл.-корр. РАН Софронов А.Г., чл.-корр. РАН Танашян М.М., акад. РАН Тахчиди Х.П., чл.-корр. РАН Ткачёва О.Н., чл.-корр. РАН Фадеев В.В., Федяева В.К., акад. РАН Хубутия М.Ш.
Рабочая группа и Комитет экспертов
акад. РАН Авдеев С.Н., Агафонова Ю.А., проф. Агеев Ф.Т., Андреев К.А., чл.-корр. РАН Анисимов В.Н., чл.-корр. РАН Арутюнов Г.П., проф. Ахмедов В.А, акад. РАН Ашрафян Л.А., к.м.н. Бабичева Л.Г., проф. Бабунашвили А.М., чл.-корр. РАН Балыкова Л.А, акад. РАН Барбараш О.Л., проф. Васильева И.А., проф. Викторова И.А., д.м.н. Виноградов О.И., проф. Волчегорский И.А., проф. Галявич А.С., к.м.н. Гаус О.В., акад. РАН Гинцбург А.Л., к.м.н. Гомберг В.Г., Горбенко А.В., акад. РАН Горелов А.В., к.м.н. Горшков А.Ю., акад. РАН Драпкина О.М., д.м.н. Ершов А.В., д.м.н. Ефремова Е.В., проф. Задионченко В.С., проф. Зайцев А.А., Захарова Т.Д., проф. Зырянов С.К., акад. РАН Иоселиани Д.Г., проф. Каневская С.С., акад. РАН Карпов Р.С., д.м.н. Кашталап В.В., чл.-корр. РАН Кобалава Ж.Д., проф. Колбасников С.В., к.п.н. Кондратьева К.О., акад. РАН Конради А.О., проф. Кореннова О.Ю., д.м.н. Корпачева О.В., проф. Лазебник Л.Б., проф. Лебедев О.И., чл.-корр. РАН. Ливзан М.А., д.м.н. Лутова Н.Б., акад. РАН Мазуров В.И., проф. Малявин А.Г., проф. Мареев В.Ю., чл.-корр. РАН Мартов А.Г., акад. РАН Мартынов А.И., чл.-корр. РАН Марьяндышев А.О., акад. РАН Медведева И.В., к.м.н. Михайлова Н.Б., чл.-корр. РАН. Моисеев С.В., д.м.н. Морозова О.Л., акад. РАН Намазова-Баранова Л.С., д.м.н. Напалков Д.А., проф. Недошивин А.О., проф. Незнанов Н.Г., проф. Нечаева Г.И., проф. Никифоров В.С., д.м.н. Николаев Н.А., проф. Омельяновский В.В., Орджоникидзе М.К., проф. Павлинова Е.Б., д.м.н. Пашков А.В., проф. акад. РАН Петров В.И., Писклаков А.В., акад. РАН Поддубная И.В., акад. РАН Полушин Ю.С., акад. РАН Попов С.В., проф. Ребров А.П., акад. РАН Ройтберг Г.Е., проф. Ройтман Е.В., чл.-корр. РАН Румянцев С.А., чл.-корр. РАН Рычкова Л.В., д.м.н. Савельева И.В., проф. Сайфутдинов Р.И., к.м.н. Селимзянова Л.Р., д.м.н. Семиглазова Т.Ю., чл.-корр. РАН Скворцова В.И., к.м.н. Скирденко Ю.П., проф. Совалкин В.И., к.м.н. Советкина Н.В., к.м.н. Сорокин М.Ю., чл.-корр. РАН Софронов А.Г., проф. Стремоухов А.А., д.м.н. Сурков А.Н., чл.-корр. РАН Танашян М.М., акад. РАН Тахчиди Х.П., проф. Терентьев В.П., чл.-корр. РАН Ткачёва О.Н., к.м.н. Токарская Е.А., д.м.н. Тотчиев Г.Ф., Тулупов Р.В., проф. Тумян Г.С., проф. Тюрин В.П., д.м.н. Усов Г.М., д.м.н. Устинова Н.В., чл.-корр. РАН Фадеев В.В., Федорин М.М., Федяева В.К., д.м.н. Фофанова Т.В., акад. РАН Хубутия М.Ш., к.м.н. Шепель Р.Н., проф. Ягода А.В., проф. Якушин С.С.
Приверженность лечению. Российское национальное руководство

В авторский коллектив входит член-корреспондент РАН Танашян М.М.
В руководстве, основываясь на принципах доказательной медицины, обобщен отечественный и мировой опыт изучения и контроля приверженности лечению. Представлена информация о результатах крупнейших российских исследований последних лет в области приверженности лечению в ведущих отраслях медицины. Приведены характеристики основных показателей приверженности, инструменты количественной оценки приверженности лечению, модели поведения пациентов в зависимости от уровня приверженности, прогнозы эффективности вмешательств в зависимости от уровня приверженности, а также выбор врачебных стратегий в зависимости от прогнозируемой эффективности вмешательств. Сформированы шаблоны рекомендаций для пациентов с различным уровнем приверженности лекарственной терапии, медицинскому сопровождению и модификации образа жизни.
Руководство предназначено для практических врачей, клинических фармакологов, руководителей медицинских организаций, организаторов здравоохранения, научных работников, студентов, ординаторов, аспирантов, докторантов, клинических исследователей.
Возврат к списку
-
Архив журнала
/ -
2018
/ - №5
Первый российский консенсус по количественной оценке приверженности лечению (одобрен XII Национальным конгрессом терапевтов — Москва, 22–24 ноября 2017 г.)
DOI: https://dx.doi.org/10.18565/therapy.2018.5.11-32
Н.А. Николаев, А.И. Мартынов, О.М. Драпкина, М.А. Ливзан, С.В. Моисеев, Ю.П. Скирденко, С.С. Бунова, И.А. Викторова, В.С. Задионченко, Л.Б. Лазебник, А.Г. Малявин, А.В. Нелидова, Г.И. Нечаева, Л.А. Пушкарева, А.П. Ребров, Р.И. Сайфутдинов, В.И. Совалкин, В.П. Терентьев, В.П. Тюрин, В.П. Уразов, Г.Б. Федосеев, А.В. Ягода, С.С. Якушин, Л.Н. Ясницкий
1 ФГБОУ ВО «Омский государственный медицинский университет» Минздрава России, Омск, Россия;
2 ФГБОУ ВО «Московский государственный медицинский университет им. А.И. Евдокимова» Минздрава России, Москва, Россия;
3 ФГБУ «Национальный исследовательский медицинский центр профилактической медицины» Минздрава России, Москва, Россия;
4 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский университет), Москва, Россия;
5 МЦ «Семейный доктор», Москва, Россия;
6 Luxoft Professional, LLC, Москва, Россия;
7 ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России, Саратов, Россия;
8 ФГБОУ ВО «Оренбургский государственный медицинский университет» Минздрава России, Оренбург, Россия;
9 ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России, Ростов, Россия;
10 ФГБУ «Национальный медицинский хирургический центр им. Н.А. Пирогова» Минздрава России, Москва, Россия;
11 Information Service Systems Art, LLC, Омск, Россия;
12 ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия;
13 ФГБОУ ВО «Ставропольский государственный медицинский университет» Минздрава России, Ставрополь, Россия;
14 ФГБОУ ВО «Рязанский государственный медицинский университет им. Академика И.П. Павлова» Минздрава России, Рязань;
15 ФГБОУ ВО «Пермский государственный национальный исследовательский университет», Пермь, Россия;
16 ФГАОУ ВО «Национальный исследовательский университет «Высшая школа экономики», Москва, Россия
Первый российский консенсус по количественной оценке приверженности к лечению одобрен XII Национальным конгрессом терапевтов (Москва, 22–24 ноября 2017 г.).
Ключевые слова: приверженность лечению, количественная оценка, рекомендации, российский консенсус
Литература
ФГБУ «Государственный научно-исследовательский центр профилактической медицины» Минздрава России
Кутишенко Н.П.
ФГБУ НИЦ профилактической медицины Минздрава России;
Первый МГМУ им. И.М. Сеченова, Москва
Марцевич С.Ю.
ГНИЦ профилактической медицины Минздрава РФ, Первый МГМУ им. И.М. Сеченова, Москва
Шепель Р.Н.
ФГБУ «Национальный медицинский исследовательский центр профилактической медицины» Минздрава России, Москва, Россия, 101990
Драпкина О.М.
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
Методические рекомендации: «Приверженность к лекарственной терапии у больных хроническими неинфекционными заболеваниями. Решение проблемы в ряде клинических ситуаций»
Авторы:
Лукина Ю.В., Кутишенко Н.П., Марцевич С.Ю., Шепель Р.Н., Драпкина О.М.
Как цитировать:
Лукина Ю.В., Кутишенко Н.П., Марцевич С.Ю., Шепель Р.Н., Драпкина О.М. Методические рекомендации: «Приверженность к лекарственной терапии у больных хроническими неинфекционными заболеваниями. Решение проблемы в ряде клинических ситуаций». Профилактическая медицина.
2020;23(3):2042‑2060.
Lukina IuV, Kutishenko NP, Martsevich SIu, Shepel RN, Drapkina OM. Methodological recommendations: «Adherence to drug therapy in patients with chronic non-communicable diseases. Addressing the problem in a number of clinical situations». Profilakticheskaya Meditsina. 2020;23(3):2042‑2060. (In Russ.)
https://doi.org/10.17116/profmed20202303242

1. Введение
Проблема приверженности к выполнению врачебных рекомендаций (ВР) берет свое начало у истоков медицины. Однако наибольшего развития и значимости вопросы приверженности достигли в эру бурного развития фармакологии и фармакотерапии. Высокую значимость проблемы приверженности подчеркивает посвященный этой теме специальный доклад Всемирной организации здравоохранения (ВОЗ) от 2003 г. [1]. Вопросы приверженности не потеряли своей актуальности и десятилетия спустя.
Несмотря на достигнутые успехи в области изучения этиологии, патогенеза, особенностей течения различных заболеваний, определения риска развития осложнений, выявлении наиболее эффективных и безопасных методов лечения, обоснования целей терапии, многие задачи в лечении и профилактике хронических болезней и их осложнений так и остаются недостижимыми, в том числе, в связи с низкой приверженностью пациентов к назначаемой терапии [1]. Результаты целого ряда исследований подтверждают, что низкая приверженность является одной из значимых причин снижения эффективности терапии, качества жизни пациентов, повышения затрат на лечение, увеличения риска развития различных осложнений, ухудшения прогноза заболевания и жизни [1—3].
По оценкам специалистов, долгосрочная приверженность любому лечению, независимо от заболевания, низкая и не превышает 50% [4, 5].
Тем не менее наиболее уязвимыми в отношении неудовлетворительной приверженности к лечению являются пациенты с хроническими заболеваниями, протекающими малосимптомно или бессимптомно, требующими длительного (нередко пожизненного) выполнения врачебных рекомендаций [2, 6, 7].
Результаты многочисленных работ выявили ряд фактов и особенностей рассматриваемой проблемы:
— Неоднозначность и многообразие определений, терминов по теме приверженности, а также их трактовки.
— Очень большое количество факторов, оказывающих влияние на приверженность к лечению, — многофакторность проблемы.
— Отсутствие метода «золотого стандарта» диагностики и универсальной стратегии повышения приверженности к лечению.
По данным некоторых исследований и систематических обзоров, за последние 30 лет, в принципе, отмечается стагнация в изучении проблемы приверженности, поэтому большинство задач, связанных с ней, до настоящего времени так и остаются нерешенными [8, 9].
Следует подчеркнуть комплексность проблемы приверженности, которая включает в себя выполнение больным ВР по изменению образа жизни, приему лекарственных препаратов и др., приверженность самих врачей к реализации клинических рекомендаций и следованию официальным инструкциям к препаратам, а также особенности обращения лекарственных средств, лекарственное обеспечение и ведение пациентов на разных этапах лечения, и в целом, — организацию, функционирование и контроль системы здравоохранения. Тем не менее ключевым звеном проблемы приверженности по-прежнему остается пациент. По этой причине основные разделы данных рекомендаций относятся именно к приверженности пациентов ВР.
2. Терминология
Историю изменений научных представлений о приверженности и способах решения этой проблемы можно проследить по истории появления разнообразных терминов, связанных с данной тематикой [10].
Первоначально в научных публикациях применялся термин «compliance» (англ. — податливость), в настоящее время используемый все реже, преимущественно, в случаях отражения факта количественного использования лекарственного препарата.
При смене патерналистской модели поведения в отношениях «врач-пациент» на модель сотрудничества, появился термин — «concordance» (англ. — согласие), подчеркивающий большую вовлеченность больного в процесс лечения. Если модель отношения врача и пациента по типу «compliance» предусматривает пассивное подчинение врачу и простое выполнение пациентом врачебных инструкций, то модель «concordance» рассматривает процесс терапии как сотрудничество и партнерство врача и пациента с более активным вовлечением последнего в процесс лечения.
Наиболее популярным, пришедшим на смену предшествующим терминам, стало понятие «adherence» (англ. — приверженность, следование), заключающее в себе основной смысл словосочетания «приверженность к терапии», как степень соблюдения ВР. Большинство врачей отдают предпочтение именно этому термину. По определению ВОЗ приверженность лечению (treatment adherence) — это степень соответствия поведения человека в отношении приема лекарственных препаратов, соблюдения диеты и/или других изменений образа жизни соответственно рекомендациям врача, медицинского работника [1].
Для обозначения продолжительности выполнения больным врачебных назначений в англоязычной научной литературе используется термин «persistence» (англ. — упорство, настойчивость) [11]. Российские авторы вводят близкое к нему понятие «упорства» — продолжительность периода, в течение которого пациент принимал рекомендованное ему лекарственное лечение [12].
Ряд исследователей выделяют в отдельный вид неприверженность к посещению лечащего врача — attendance/non-attendance [13, 14].
Кроме того, появляются различные уточняющие эпитеты, отражающие различные аспекты основного понятия, устойчивые словосочетания:
— потенциальная (готовность пациента выполнять назначения врача) и фактическая (реальное следование ВР) приверженность [15];
— приверженность белого халата (повышение приверженности к лечению перед визитом к врачу) [16];
— «здоровая» приверженность (характеризует модель поведения, свойственную человеку, который самостоятельно стремится к здоровому образу жизни и выполнению всех рекомендаций по улучшению здоровья) [7, 10, 17, 18].
Помимо термина «приверженность» в английском языке появилось антонимичное ему понятие «неприверженности» (nonadherence), которое по аналогии с приверженностью включает ряд терминов:
— «defaulting» (англ. — невыполнение обязательств) — отказ больным начинать прием лекарственных препаратов;
— «nonpersistence» (соответственно, неустойчивость) — несогласие принимать препараты длительно, досрочное самостоятельное прекращение терапии;
— намеренная (intentional) неприверженность — сознательное невыполнение рекомендаций врача, отказ от лечения и непреднамеренная (unintentional) — как правило, связанная с забывчивостью [18, 19];
— рациональная неприверженность — отказ от лечения из-за нежелательных явлений последнего [5, 20].
Основные виды приверженности и термины, используемые для их обозначения, представлены на рис. 1.
Ряд исследователей использует различные термины для обозначения приверженности на разных этапах лечения — фазность приверженности. Впервые о существовании различных фаз в приверженности больных к лечению упоминается в работе B. Vrijens и соавт. (ABC Project Team). Согласно предложенным в этом проекте определению и классификации приверженности, последняя является динамическим процессом, проходящим три взаимосвязанных фазы: начало приема ЛП, соблюдение режима приема ЛП, устойчивость к терапии (initiation, implementation, and persistence) [21]. Данная классификация была поддержана Европейским обществом по приверженности — the European Society for Patient Adherence, COMpliance, and Persistence (ESPACOMP) и введена в соответствующее руководство — Medication Adherence Reporting Guideline (EMERGE) [21, 22].
Согласно предложенной российскими авторами шкале приверженности Национального общества доказательной фармакотерапии (НОДФ) выделяют следующие степени нарушения приверженности:
— частичная приверженность — какие-либо изменения ВР в отношении приема препарата пациентом (дозы, кратности, времени и т.д.);
— частичная неприверженность — преждевременное прекращение приема препарата (нарушение фазы устойчивости к лечению);
— полная (абсолютная) неприверженность — отказ начать терапию [23].
Впрочем, все перечисленные термины являются недостаточно информативными для полного описания поведения человека относительно всех нюансов приема лекарственных препаратов.
NB!
Обращает на себя внимание факт, что терминология по проблеме приверженности, главным образом, представлена на английском языке. В русском языке все многообразие терминов вмещает в себя слово «приверженность», используемое иногда с рядом эпитетов (в ряде случаев, также переводных): намеренная, непреднамеренная, «рациональная», «белого халата» и т.д. С точки зрения филологии, использование термина «приверженность (к) лечению» в русском языке неверно, однако других вариантов и замены данному словосочетанию, ошибочному с точки зрения лексической и семантической сочетаемости, не предлагается [24].
2.1. Методы оценки приверженности к терапии
Следует отметить, что метода «золотого стандарта» для диагностики приверженности к лечению до сих пор не существует — ни один из предлагаемых на сегодняшний день способов не является абсолютно надежным. Существующие методы подразделяются на прямые и косвенные (табл. 1) [5, 25].
Примечание. * — метод непосредственного врачебного контроля перорального приема лекарственного препарата (ЛП) пациентом используется, главным образом, в условиях клинических исследований I фазы или в исследованиях биоэквивалентности ЛП и включает ряд обязательных для выполнения пунктов: выдача пациенту ЛП, прием ЛП под наблюдением врача, последующий тщательный осмотр ротовой полости больного для контроля того, что препарат был проглочен; ** — PDC — proportion of days covered — метод реализуемости выписанных рецептов, MPR — medication possession ratio — метод учета полученных (приобретенных) пациентом лекарственных препаратов
К прямым методам диагностики приверженности относятся непосредственное наблюдение и врачебный контроль приема пациентом лекарственного препарата, измерение концентраций препаратов и их метаболитов в различных биологических средах (моча, кровь, слюна и др.). Современным прямым методом диагностики приверженности является система мониторинга приема лекарственных препаратов, состоящая из принимаемого внутрь микросенсора, который активируется в желудочном соке, и наружного датчика, регистрирующего сигналы этого микросенсора [26]. Информация с воспринимающего датчика может передаваться лечащему врачу и пациенту на специальные мобильные приложения для смартфонов, что позволяет как отслеживать врачу соблюдение режима приема препаратов больным, так, при необходимости, создать систему напоминания для пациента, срабатывающую при пропуске приема лекарства.
NB!
Прямые методы сложны для применения в рутинной клинической практике, а потому редко в ней используются. Эти методы дороги, к тому же, в связи с целым рядом этико-правовых моментов, обычно доступны и применимы только в рамках клинических исследований, в которых получено согласие пациента на забор у него биологического материала, введение микросенсора и прочие процедуры.
К косвенным способам оценки приверженности относятся анкетирование, опрос, интервьюирование больных, оценка дневников самоконтроля пациентов, подсчет использованного препарата, учет выписанных и реализованных рецептов, оценка различных физиологических маркеров и клинического ответа пациентов, использование встроенных электронных «чипов» в упаковки препарата — Medication Events Monitoring System (MEMS) [5, 27].
Среди десятка методов диагностики и контроля того, как больной соблюдает врачебные рекомендации (ВР) по приему лекарственных препаратов и изменению образа жизни, нет ни одного, лишенного недостатков, и с высокой точностью дающего ответы на данные вопросы.
Дневники пациентов
Самостоятельное ведение дневника приема препаратов пациентом — простой способ диагностики приверженности, имеющий, однако, большой недостаток — склонность больных переоценивать свою приверженность к лечению (по сравнению с данными электронного контроля препаратов (MEMS) результаты самооценки оказались на 30% завышены), что значительно снижает надежность метода [27].
Прямой опрос и интервьюирование пациентов врачом
Прямой опрос врачом пациента о приеме препарата (direct questioning), а также более расширенное интервьюирование больного для уточнения различных нюансов соблюдения пациентом ВР, в связи с простотой, удобством, хорошей адаптацией к обычным условиям работы врача, низкой стоимостью использования приобрели широкое распространение в клинической практике [28].
NB!
Как и все косвенные методы, прямой опрос и интервьюирование субъективны и полученные с их помощью результаты следует трактовать с осторожностью. Дополнительными преимуществами указанных методов являются «гибкость» исследования — врач может задать дополнительные вопросы пациенту о соблюдении конкретных врачебных рекомендаций (ВР) в отношении приема того или иного лекарственного препарата, и затем, в соответствии с полученными ответами, откорректировать необходимые вмешательства и предпринять наиболее целесообразные меры по повышению приверженности [18].
Опросники и шкалы (анкетирование)
Одним из наиболее часто используемых и удобных методов оценки приверженности в условиях реальной клинической практики (РКП) является анкетирование пациентов. Согласно одной из классификаций методов оценки приверженности, опросники и шкалы выделяются в отдельную группу, наряду с группами клинических, фармакологических и физических методов [5].
Согласно систематическому обзору T.-M. Nguyen и соавт. в настоящее время существует более 40 опросников, переведенных на английский язык, по оценке приверженности пациентов [29]. Авторы разделили эти опросники на 5 групп: 1) определяющие только поведенческие реакции в отношении приема лекарственных препаратов; 2) оценивающие как поведенческие реакции, так и барьеры, препятствующие высокой приверженности; 3) выявляющие исключительно эти барьеры; 4) диагностирующие факторы, повышающие приверженность к фармакотерапии; 5) в дополнение к факторам, повышающим приверженность, определяют и барьеры, нарушающие приверженность к ВР [29].
Среди опросников наиболее известным, простым и лаконичным признан тест Мориски—Грина, широко применяемый в клинической практике для скрининга приверженности пациентов [30]. Тест включает в себя 4 вопроса (4-item Morisky Medication Adherence Scale — MMAS-4), определяющие пропускает ли больной прием лекарственных препаратов, если чувствует себя хорошо или плохо, забывает ли он принимать лекарства и внимательно ли относится к рекомендованному времени приема препаратов. На каждый вопрос предлагается выбрать положительный или отрицательный ответ (да/нет). Несомненными преимуществами теста является его краткость и, соответственно, быстрота выполнения, универсальность (что позволяет использовать тест у больных различными заболеваниями), простота интерпретации результатов теста. MMAS-4 часто используется в научных исследованиях при изучении различных аспектов проблемы приверженности, в том числе при разработке новых опросников и шкал, в качестве эталонного теста для валидизации новых анкет [31—33].
Однако за видимыми преимуществами шкалы Мориски—Грина скрываются и недостатки этого метода оценки приверженности. По мнению самих авторов, данный тест обладает лишь 44% чувствительностью и 47% специфичностью, т.е. не позволяет выявить практически половину неприверженных пациентов. Эти данные подтвердили F. Pineiro и соавт, проводившие тестирование 6 методик оценки приверженности у больных артериальной гипертензией (АГ). Шкала Мориски—Грина из 4 вопросов показала средние результаты: у приверженных пациентов тест продемонстрировал положительный результат в 66% случаев, а у неприверженных — отрицательный в 44%. Прогностическая ценность теста Мориски—Грина была оценена F. Pineiro и соавт. всего в 39,6% [34].
В 2008 г. М. Green и соавт. провели апробацию нового теста, состоящего из 8 вопросов — MMAS-8 — в группе из 1367 пациентов с АГ [35].
Результаты опроса по новой шкале из 8 вопросов коррелируют с прежним 4-вопросным вариантом (коэффициент корреляции Пирсона = 0,64, р<0,05). Чувствительность и специфичность нового теста составила 93 и 53% соответственно [35, 36].
Тесты Мориски создавались для пациентов, страдающих АГ, однако апробация тестов у больных с другими нозологиями, подтвердило удовлетворительную точность этих шкал и у них. Тем не менее результаты некоторых исследований продемонстрировали не очень высокие показатели чувствительности и отрицательной прогностической способности и усовершенствованной, 8-вопросной версии: 51 и 43% соответственно [37]. По данным российских авторов, оба теста Мориски определяют общую поведенческую реакцию больных в отношении приема лекарственных препаратов, но неудовлетворительно диагностируют приверженность больного в отношении лечения тем или иным конкретным лекарственным препаратом [23, 38].
Шкала Hill—Bone была разработана на Африканском континенте для больных артериальной гипертонией (АГ), поэтому обладает наиболее высокой валидностью при оценке приверженности у темнокожих пациентов с АГ. Шкала включает 14 вопросов, распределенных на 3 субшкалы; определяет поведение пациента в отношении приема антигипертензивных препаратов, уменьшения количества потребляемой соли и посещения лечащего врача [39].
Краткий лекарственный опросник (Brief Medication Questionnaire.) является универсальной шкалой, диагностирующей приверженность к приему конкретных лекарственных препаратов, а также потенциальные и фактические причины неприверженности [40]. Позиционируются очень высокие показатели чувствительности данной шкалы — 80—100%, — которые были подтверждены результатами оценки приверженности с помощью таблетниц с встроенными электронными чипами.
The Self-Efficacy for Appropriate Medication Use Scale (SEAMS) — опросник, созданный мультидисциплинарной командой, валидизированный для оценки приверженности у пациентов с различными хроническими заболеваниями, в том числе у людей с низким уровнем грамотности. Существует 2 версии опросника — полная, состоящая из 21 вопроса, и редуцированная, включающая 13 вопросов [41].
Medication Adherence Report Scale (MARS) — шкала по оценке приверженности, также имеющая 2 версии: 10- и 5-вопросную (MARS-10 и MARS-5), может быть использована для диагностики приверженности к фармакотерапии и у людей с психическими заболеваниями. Лаконичность теста обеспечило ему популярность, перевод на многие языки. Тем не менее результаты исследований на валидность данного теста у пациентов с различными хроническими заболеваниями не однозначны [42].
Medication Satisfaction Questionnaire (MSQ) был разработан для определения приверженности к антипсихотическим препаратам у больных шизофренией и валидизирован именно для этой категории больных. Тест включает всего один вопрос об удовлетворенности пациентов получаемой фармакотерапией, ответы представлены в виде рейтинговой шкалы Ликерта и варьируют от «полностью удовлетворен» до «полностью не удовлетворен» [43].
NB!
1) ни один из известных в настоящее время опросников не лишен субъективизма; 2) практически все опросники переоценивают приверженность пациентов к лечению, не полностью диагностируют неприверженность к терапии, нередко определяют лишь какой-то конкретный вид приверженности, некоторые не выявляют барьеры неприверженности; 3) даже валидизированные опросники при использовании у пациентов разных стран, с разными заболеваниями, демонстрируют различные показатели чувствительности, специфичности и надежности: от отличных до неудовлетворительных; 4) в связи с этим, результаты по оценке приверженности с помощью шкал и опросников следует трактовать с известной долей осторожности; 5) в условиях реальной клинической практики, нередко характеризующихся дефицитом времени врача и ограниченностью технических возможностей (например, предоставления пациентам планшетов или компьютеров для заполнения электронных версий опросников), следует отдавать предпочтение лаконичным шкалам, включающим не более 10 вопросов, не требующим дополнительных технических приспособлений, желательно валидизированным для соответствующей категории больных.
Методы реализуемости выписанных рецептов (PDC) и учета выписанных лекарственных препаратов (MPR)
Метод расчета дней, обеспеченных выданным по рецепту препаратом (от англ. proportion of days covered; PDC), — метод реализуемости выписанных рецептов, так же как и метод учета полученных (приобретенных) пациентом лекарственных препаратов (от англ. medication possession ratio — MPR), часто используется в зарубежных исследованиях и базах данных, но в российской практике в связи с особенностью лекарственного обеспечения сложно применим и для оценки приверженности практически не используется. Методы похожи (по некоторым данным PDC является модификацией метода MPR), в обоих определяется пропорция обеспечения больного препаратом к числу дней, которое прошло от одного до другого визита больного к фармацевту. Результирующие значения PDC и MPR варьируют от 0 до 1 (от 0 до 100%). Тем не менее доказано, что оба метода завышают показатель приверженности и более надежными являются методы опроса пациента о приеме препарата [44—46].
NB!
В заключение рассмотрения различных методов оценки приверженности следует отметить, что диагностика приверженности крайне необходима (так как в случае неприверженности теряется весь смысл лечения), хотя нередко затруднена в силу дефицита времени у врача и отсутствия единого надежного диагностического метода ее определения. В определенных клинических ситуациях или в условиях клинических исследований можно отдать преимущество отдельным методам оценки приверженности к лечению. Отмечено, что точность измерения возрастает при сочетании разных методов.
Рекомендовано:
Оценивать приверженность следует, применяя несколько подходов. В клинической практике, как правило, реализуемы только косвенные методы диагностики приверженности. Сочетанное использование нескольких способов (ведение дневника, подсчет принятых таблеток по пустым блистерам, опросники и др.) повышает точность диагностики приверженности, а также может способствовать улучшению приверженности больных, т.к. неизбежно вовлекает пациента в процесс лечения и его контроля [47, 48].
Факторы, влияющие на приверженность
Проблема приверженности является многофакторной — идентифицировано более 250 факторов, оказывающих влияние на приверженность к лечению. Согласно докладу ВОЗ, посвященному проблеме приверженности, условно все факторы подразделяются на пять групп [1]:
- Факторы, связанные с пациентом.
- Факторы, связанные с врачом и организацией системы здравоохранения.
- Факторы, связанные с заболеванием.
- Факторы, связанные с проводимой терапией.
- Факторы социально-экономические.
Факторы, связанные с пациентом и с заболеванием
Эти группы факторов чрезвычайно тесно связаны между собой.
По уже сложившейся традиции главной фигурой в проблеме приверженности обозначается пациент, что выглядит достаточно логичным — кратко и емко проблему приверженности, обусловленную факторами, связанными с пациентом, сформулировал Чарльз Куп, американский детский хирург: «Лекарство не действует, если больной не принимает его», — однако на современном этапе, по данным достаточно большого количества исследований, такая позиция несколько потеряла свою основательность и аксиоматичность.
Несмотря на то что группа факторов приверженности, связанных с пациентом, на сегодняшний день является самой хорошо изученной, в результатах многочисленных исследований единообразие сведений по данному вопросу отсутствует. Возможными факторами плохой приверженности к выполнению ВР разные авторы называют молодой и старческий возраст, мужской пол, низкий уровень доходов, курение, забывчивость, недоверие к врачу, неверие в успех терапии, низкий уровень грамотности/образования и многие другие [49, 50].
Было показано, что степень приверженности больного ВР четко ассоциируется с показателем самоэффективности. Самоэффективность — психологический термин, обозначающий веру человека в эффективность и успех достижения целей от реализации собственных действий. Высокая самоэффективность является предиктором хорошей приверженности пациента. Самоэффективность позволяют определить опросники SEAMS, BMQ, шкала Hill—Bone) [18].
Согласно выводам крупного анализа данных, включившего 21 систематический обзор результатов 313 РКИ по изучению факторов приверженности, было показано, что роль многих, считавшихся бесспорно значимыми факторами, остается не доказанной. К таким факторам относятся высокий уровень дохода, семейный статус (проживание в браке), высшее образование, а также факторы, связанные с лечением (режим приема препарата), с продолжительностью заболевания, фактор стоимости лечения и наличия страховки, коморбидности (соматические и психические заболевания, за исключением депрессии). Возможное положительное влияние на приверженность по результатам данного аналитического обзора было подтверждено для социально-экономического статуса и наличия социальной поддержки. На приверженность оказывают доказанное отрицательное действие принадлежность к этническим меньшинствам, наличие депрессии, подростковый и старческий возраст (U-образная зависимость приверженности от возраста пациентов). Влияние пола на приверженность, так же как и занятость на работе, по данным различных исследований, было непостоянным, поэтому также считается неподтвержденным [51].
Факторы, связанные с терапией
По результатам крупного аналитического обзора влияние особенностей фармакотерапии на приверженность было выявлено только для некоторых сердечно-сосудистых средств, для всех остальных лекарственных препаратов такой эффект подтвержден не был [51].
Тот факт, что к разным лекарственным препаратам у одного и того же больного может быть разная приверженность, часто не принимается во внимание. Так, по данным исследования M.Viana и соавт., пациенты с ХСН наиболее привержены к терапии ингибиторами АПФ, а наименее — к приему петлевых диуретиков, приверженность к бета-адреноблокаторам занимает промежуточное положение между обозначенными позициями [52]. Результаты исследования S.T. de Vries и соавт. продемонстрировали различную степень приверженности больных к лечению пероральными антидиабетическими, антигипертензивнымии и гиполипидемическими препаратами: пациенты наиболее часто забывали принимать или полностью прекращали прием гиполипидемических препаратов, уменьшали рекомендованную дозу и намеренно пропускали прием гипогликемических средств (намеренная неприверженность). Меньшее число намеренных нарушений приверженности было выявлено в отношении антигипертензивных препаратов: больные реже пропускали их прием, по другим оцениваемым параметрам приверженность к антигипертензивной терапии заняла промежуточное положение между показателями двух других групп [53].
Целый ряд исследований выявил взаимосвязь и взаимовлияние показателей безопасности фармакотерапии и приверженности пациентов к приему лекарственных препаратов: так отсутствие у больных нежелательных явлений (НЯ) лекарственного лечения в анамнезе в несколько раз увеличивает вероятность их хорошей приверженности к ВР, касающимся фармакотерапии; а более половины больных называют главной причиной неприверженности — НЯ лекарственной терапии. Помимо этого, у неприверженных и склонных к самостоятельному изменению и отмене лечения пациентов значимо чаще отмечались НЯ фармакотерапии в анамнезе [54—56]. Опасение побочных эффектов лекарственных препаратов пациенты называют одной из самых частых причин неприверженности к фармакотерапии на всех фазах лечения (начало, соблюдение режима лечения, устойчивость к терапии) [23, 57].
Одной из ведущих причин взаимосвязи между показателями безопасности и приверженности к фармакотерапии является полипрагмазия, особенно часто наблюдаемая у пожилых лиц с высокой коморбидностью [58]. Полипрагмазия повышает вероятность неблагоприятных межлекарственных взаимодействий и, соответственно, НЯ лекарственной терапии, что, в свою очередь, отрицательно сказывается на приверженности к лечению [58, 59].
Отказ пациента от дальнейшего приема лекарственных препаратов при возникновении НЯ фармакотерапии, по мнению J. Garner, следует расценивать как отдельный вид неприверженности — «рациональную неприверженность» [20].
Факторы, связанные с врачом и организацией системы здравоохранения
Несмотря на то что пациенту в проблеме приверженности отводится «центральная» роль, в настоящее время обнаруживается все большее влияние факторов, связанных с врачами и организацией системы здравоохранения.
Врачи не всегда назначают лекарственные препараты согласно клиническим рекомендациям (КР) или отменяют препараты с доказанным действием, назначенные в других медицинских учреждениях; нередко инертны в достижении целевых уровней показателей эффективности проводимой терапии, часто безынициативны в выявлении, определении и регистрации нежелательных явлений лекарственного лечения; не следуют положениям официальных инструкций к лекарственным средствам; иногда рекомендуют медикаментозные препараты с недоказанной эффективностью или относящиеся к III классу КР (что соответствует вреду и/или отсутствию пользы от назначения такого лекарственного средства). В таких случаях хорошая приверженность пациента к выполнению ВР будет скорее во вред, чем во благо его здоровью [47]. По данным российских регистров пациентов с сердечно-сосудистыми заболеваниями (ССЗ), статины были назначены менее 2% больных, перенесшим мозговой инсульт, только в 5—14% случаев пациентам с ишемической болезнью сердца (ИБС) до госпитализации по поводу острого инфаркта миокарда (ОИМ), в 17,8% случаев — больным с ССЗ и гиперхолестеринемией [60, 61]. Частота достижения целевых уровней показателей липидного спектра, по данным наблюдательных исследований, проводимых в условиях реальной клинической практики, еще ниже: в среднем целевой уровень холестерина липопротеидов низкой плотности (ХС ЛПНП) достигают 15—30% пациентов, принимающих статины [62, 63].
Опрос врачей поликлинического звена выявил недостаточное знание клинической фармакологии лекарственных препаратов, применяющихся в лечении сердечно-сосудистых заболеваний (ССЗ), абсолютных противопоказаний к назначению этих препаратов, недостаточную информированность врачей об основных положениях современных клинических рекомендаций по лечению ССЗ [64].
По мнению многих исследователей, большое значение в приверженности пациента к лечению имеют личностные качества лечащего врача: его квалификация, убежденность, заинтересованность в судьбе пациента, а отсутствие постоянного лечащего врача у пациента отрицательно влияет на соблюдение больным любых ВР [65, 66].
Таким образом, для успешного контроля факторов риска необходима не только приверженность пациента к рекомендациям, но и приверженность врача принципам рациональной терапии. Поэтому для врача важно выявить собственные барьеры к приверженности и попытаться их минимизировать.
NB!
При анализе факторов разных групп (согласно классификации ВОЗ), оказывающих различной степени влияние на приверженность, совершенно отчетливо проявляются их тесная взаимосвязь и взаимовлияние. Многофакторность проблемы приверженности, безусловно, является одним из основополагающих аспектов сложности ее решения.
О взаимовлиянии факторов приверженности различных групп упоминается еще в трудах Авиценны: «У постели больного нас двое — врач и болезнь: на чью сторону встанет пациент, тот и победит» [67]. Наиболее близко к идее важности учета взаимовлияния ключевых факторов проблемы приверженности подошел N. Кaplan в книге «Клиническая гипертензиология Каплана» («Kaplan’s clinical hypertension»): «Хотя практические врачи в первую очередь обвиняют больных в плохом контроле АГ, все три игрока — врач, больной и лекарства — вовлечены в процесс» [68]. И именно эта теория лежит в основе разработки основных направлений по решению проблемы приверженности.
2.2. Методы повышения приверженности
Общие сведения по решению проблемы приверженности
Единая стратегия по повышению приверженности к лечению до настоящего времени также не разработана. Наиболее перспективные методы улучшения приверженности пациентов можно объединить в четыре группы.
Рекомендовано:
1) повышение информированности пациентов, так как доказано, что человек лучше привержен к тем действиям, смысл и цель которых он знает и понимает. С этой целью для больных различными заболеваниями или факторами риска организуют специальные школы здоровья. Привлечение родственников больного к процессу лечения нередко способствует повышению приверженности к терапии;
2) оптимизация режима приема лекарственных препаратов. Отмечено, что наилучшим в плане приверженности является режим: «одна пилюля один раз в день». Однако, учитывая обширную коморбидность, имеющуюся у современных пациентов, такой режим лечения является крайне редким. Поэтому для реализации методов данной группы применяют различные напоминания: создание специальных упаковок лекарственных препаратов с указанием дней недели, времени приема (утро-вечер) лекарства; рассылка СМС-сообщений, телефонные звонки больным и др.;
3) улучшение доступности медицинской помощи (в том числе, уменьшение времени ее ожидания);
4) создание качественных отношений врач-пациент, обеспечивающих высокую степень доверия больных своим лечащим докторам. Главной задачей в осуществлении методов данной группы (а также первой группы) является грамотное, качественное, информативное, достаточное по времени консультирование пациентов [5].
Для повышения приверженности врачей к внедрению в практику рекомендованы 5 направлений.
Рекомендовано:
1) внедрение инноваций в процесс создания и использования КР: привлечение врачей в процесс разработки и обсуждения КР; проведение новых исследований для дальнейшего развития и улучшения КР; создание «работающих» КР, чему способствует ясность и языковая доступность, простота изложения, высокая доказательность, эффективность в достижении желаемых целей, удобство для использования в клинической практике и гибкость подходов (возможность индивидуализации), применение мультидисциплинарных решений (врачи, организаторы здравоохранения, страховщики и др.), обязательное документирование и регулярные обновления КР в свете введения новых достижений науки;
2) обучение врачей применению КР в своей клинической практике, начиная со студенческой скамьи и на протяжении всей профессиональной карьеры;
3) обмен информацией между врачами, что позволяет работникам практического здравоохранения сравнить данные своей работы с результатами других врачей, способствует повышению приверженности КР;
4) инвестиции в информационные (IT) инновации, упрощающие использование КР в клинической практике и помогающие врачам в принятии клинических решений;
5) совершенствование системы медицинского страхования в ракурсе повышения заинтересованности врачей придерживаться КР на практике [69].
В России также предпринимаются шаги по усовершенствованию образовательной системы в области медицины и здравоохранения, в частности, вводится балльная аккредитация медицинских работников в рамках новой системы непрерывного медицинского образования.
Подтвердившие свою эффективность методы повышения приверженности, как пациентов, так и врачей, представлены в табл. 2.
Возможно, одной из причин низкоэффективного решения проблемы является ускользание из поля зрения большинства исследователей необходимости одновременного учета и воздействия на факторы разных групп, влияющих на приверженность (согласно классификации ВОЗ), которые, безусловно, тесно связаны между собой. Если провести аналогию с тем, что наиболее эффективными методами лечения признаются те, что влияют на максимальное число ведущих этиологических факторов и патогенетических звеньев болезни, то максимально эффективным должен быть путь воздействия на все или большинство факторов приверженности.
NB!
Главная роль в решении проблемы приверженности должна быть отведена лечащему врачу. Именно врач может и должен предоставить пациенту полную информацию о заболевании, осложнениях болезни, прогнозе здоровья и жизни, основных способах лечения и его задачах, с целью создать мотивацию на строгое и регулярное выполнение всех лечебных и профилактических врачебных рекомендаций.
Именно врач должен назначить больному лечение, соответствующее современным КР и учитывающее все имеющиеся у пациента показания/противопоказания к назначению данной терапии. Именно врач должен создать у пациента мотивацию на сотрудничество и выполнение всех врачебных рекомендаций, тем не менее, не освобождая взрослого дееспособного человека — пациента — от ответственности за свои здоровье и жизнь [71, 72]. Именно с личностью врача в настоящее время связывают эффекты плацебо и ноцебо (соответственно положительного и отрицательного влияния «препарата-пустышки»), достоверного объяснения которым до сих пор не найдено [72]. И только выполнение всех перечисленных задач: назначение пациенту качественной терапии и высокая стойкая приверженность больного этому лечению, позволит достичь основных целей лечения — улучшения прогноза заболевания, жизни, повышение качества жизни [47].
К сожалению, в условиях каждодневной амбулаторно-поликлинической практики лечащий врач, ввиду выраженного дефицита временного, личностного, профессионального и других ресурсов, нередко не имеет возможностей для максимально успешного претворения данных целей в жизнь [73].
Методы повышения приверженности к терапии по группам факторов
С учетом предложенной ВОЗ классификацией факторов приверженности [1], все методы улучшения приверженности можно подразделить на соответствующие группы.
Рекомендовано:
Воздействие на группу факторов, связанных с пациентом
— Обучение пациентов (Школы для больных АГ, СД, ХСН, бронхиальной астмой и др.; информирование больных лечащим врачом; специальная литература для пациентов и т.д.).
— Вовлечение пациента в процесс лечения и контроля его эффективности, безопасности (например, самоконтроль АД, уровень гликемии и т.д.) — внедрение принципов ответственного самолеченияю
— На основании первых двух пунктов — повышение самоэффективности пациентов (веры в эффективность и успех достижения целей от реализации собственных действий).
— Поощрение поддержки со стороны семьи, друзей.
— Стимуляция нелекарственного лечения (изменение образа жизни: отказ от вредных привычек, рациональное питание, регулярная физическая нагрузка, нормализация сна и т.д.).
Воздействие на группу факторов, связанных с врачом
— Сознавать риск низкой приверженности при неэффективности назначенного лечения.
— Четкое определение целей лечения и способов контроля их достижения.
— Делегирование ряда полномочий и ответственности за проводимое лечение пациенту (внедрение принципов ответственного самолечения).
— Совместная работа с фармацевтами.
— Адаптация лечения и поддержки приверженности к нуждам пациента.
— Сохранение контакта с пациентами, пропускающими визиты к врачу.
— Повышение собственного образования в отношении знаний современных клинических рекомендаций, в том числе, по рациональной фармакотерапии пациентов с хроническими заболеваниями.
и с организацией системы здравоохранения:
— Организация удобной медицинской помощи пациентам.
— Усовершенствование взаимодействия между работниками разных звеньев оказания помощи, в том числе между врачами и фармацевтами.
— Повышение образования, квалификации работников здравоохранения, в том числе по вопросам приверженности к лечению.
Способы, связанные с лекарственным лечением
— Стимулировать исключительно рациональное использование лекарственных препаратов (назначение препаратов по показаниям, отказ от назначения «лишних» препаратов, не рекомендованных КР, к которым нет показаний или имеются противопоказания).
— Избегать сложных режимов дозирования.
— Подбирать индивидуальные схемы приема препарата (идеально в отношении приверженности, но сложно осуществимо на практике: утренний, однократный прием).
— Назначать пролонгированные препараты с минимумом побочных эффектов, отдавать предпочтение комбинированному лечению перед монотерапией в высоких дозах, фиксированным комбинациям перед свободными, что позволяет уменьшить количество принимаемых пациентом таблеток.
— Учитывать стоимость лечения.
Несмотря на многообразие предлагаемых на сегодняшний день способов повышения приверженности, их результативность, особенно по влиянию на клинические исходы, низкая или отсутствует вовсе, что продемонстрировали данные крупного систематического обзора с метаанализом [74]. Несмотря на ряд ограничений данного обзора, отмеченных авторами, — отсутствие единой методологии оценки как воздействия на приверженность, так и качества отобранных РКИ, — очевидно, что высоко эффективное и надежное решение проблемы повышения приверженности к фармакотерапии к настоящему времени не найдено, а лишь намечены некоторые перспективы решения данного вопроса для будущих исследований.
2.3. Коморбидность, комбинированная терапия и проблема приверженности
В связи со все возрастающей актуальностью проблемы старения населения планеты, существенно увеличивается число лиц пожилого и старческого возраста, обремененных большим количеством хронических неифекционных заболеваний (ХНИЗ). ХНИЗ, имеющиеся у одного пациента, могут быть как объединены общим патогенезом, так и иметь различные механизмы развития и прогрессирования болезни — коморбидность и полиморбидность, соответственно. В связи со значительным увеличением пациентов с ко- и полиморбидной патологией, закономерно возрастает и лекарственная нагрузка, так как лечение различных заболеваний требует назначения большого количества разных препаратов. Это закладывает основу к возникновению проблем полипрагмазии и нерациональных лекарственных комбинаций. При приеме больным более 5 препаратов в день резко возрастает вероятность лекарственного взаимодействия, являющегося одной из ведущих причин развития неблагоприятных лекарственных реакций: при приеме до 5 ЛС в день НЯ развиваются в 4—5% случаев, а при лечении пятью и более лекарственными препаратами риск развития НЯ возрастает до 45—50%, достигая практически 100% при увеличении количества ЛС более 10 [58, 75]. Тем не менее, данные других, более поздних, исследований не подтверждают наличия зависимости НЯ фармакотерапии от количества лекарственных препаратов [59, 76]. Этот факт может быть объяснен, в том числе, и нивелированием риска НЯ терапии при назначении рационального комбинированного лечения.
Концепция комбинированной терапии актуальна для многих областей медицины, но особенно для гипертензиологии и липидологии. В связи с тем, что целевые уровни АД и ХС ЛПНП для различных категорий пациентов согласно современным КР устанавливаются на все более низких значениях, чем в предыдущих версиях КР, очевидно, что их достижение становится практически невозможным при монотерапии этих состояний.
NB!
На сегодняшний день большинство пациентов нуждаются в комбинированной терапии — только она является основой современной стратегии ведения больных ХНИЗ, реально обеспечивающей возможность достижения целевых уровней показателей эффективности лечения: уровня АД, гликемии, гликированного гемоглобина, ХС ЛПНП и др.
Возможно применение как свободных, так и фиксированных комбинаций лекарственных препаратов. Фиксированные комбинации бывают двух типов: 1) направленные на лечение одного заболевания и/или коррекцию одного показателя (например, комбинации антигипертензивных препаратов), а также 2) разработанные для коррекции различных факторов риска, обычно сопутствующих основной патологии — различные полипиллы (polipill), включающие, например, антигипертензивные, гиполипидемический препараты, дезагрегант. Как правило, фиксированные комбинации являются рациональными. Входящие в их состав компоненты обычно работают по принципу синергизма, когда происходит не механическое сложение эффективности назначаемых совместно препаратов, а потенцирование их действия, что усиливает основной эффект, на который направлено их действие (например, антигипертензивный). Это дает возможность использовать более низкие дозы этих компонентов. Помимо этого, именно рациональная комбинированная терапия приводит к торможению контррегуляторных механизмов, которые практически всегда запускаются на начальном этапе лечения и могут приводить к уменьшению его эффективности. Признанным считается и тот факт, что комбинированная терапия наиболее эффективно предотвращает поражение органов-мишеней и приводит к уменьшению числа различных осложнений ХНИЗ [77].
Еще одним достоинством комбинированной терапии является уменьшение частоты появления побочных реакций и улучшение переносимости лечения. Известно, что с увеличением дозы препарата происходит усиление не только его терапевтического эффекта, но и существенно возрастает риск появления побочных действий. Поэтому лекарственное средство, назначенное в низких дозах, значительно реже вызывает нежелательные реакции, чем назначаемое в субмаксимальных и максимальных дозах. Кроме этого, при грамотном подборе препаратов для совместного применения одно из лекарств в комбинации «противостоит» побочным эффектам другого, и наоборот. Это приводит к снижению риска развития побочных реакций при комбинированной терапии. Так, например, в комбинации ингибитора АПФ (иАПФ) и дигидропиридинового антагониста кальция (ДАК) уменьшается риск периферических отеков, нередко развивающихся при монотерапии ДАК; комбинированные препараты иАПФ и диуретиков редко вызывают нарушения уровня калия крови; а сочетание бета-адреноблокаторов с ДАК — изменения частоты пульса. Дополнительными преимуществами фиксированных комбинаций являются простой и удобный режим приема, упрощение рецептурной прописи, уверенность в оптимальном и безопасном дозовом режиме, более низкая цена, чем у нескольких препаратов в свободной комбинации.
К недостаткам относят фиксированность (неизменяемость) доз компонентов, что затрудняет их раздельную коррекцию; ограничения в подборе компонентов (врач ограничен только представленными на фармацевтическом рынке препаратами фиксированных комбинаций); трудности в идентификации нежелательных явлений [78].
Следует еще раз подчеркнуть, что главные преимущества комбинированной терапии, заключающиеся в усилении основного лечебного действия и уменьшении числа побочных эффектов, присущи лишь так называемым рациональным комбинациям препаратов.
Для оценки влияния комбинированной терапии на приверженность к лечению было выполнено большое число исследований. Основываясь на концепции, что количество препаратов может влиять на приверженность к лечению, причем оптимальной является стратегия «чем меньше таблеток — тем лучше», а наиболее привлекательной в отношении соблюдения ВР по фармакотерапии является назначение одной пилюли один раз в день, становятся очевидны преимущества использования в РКП фиксированных комбинаций или polipill. В крупной наблюдательной программе американских авторов, включавшей почти полмиллиона пациентов с АГ, было показано, что приверженность и к началу терапии, и к длительному приему препаратов значимо выше при использовании фиксированных комбинаций, чем свободных антигипертензивных препаратов или монотерапии АГ [79]. Перспективность применения polipill для повышения приверженности по сравнению с многокомпонентной терапией была подтверждена результатами систематического обзора A. Baumgartner и соавт., хотя авторами подчеркивается ряд ограничений данной работы, в частности, достаточно узкий круг заболеваний, при которых эта проблема изучалась [80].
По данным C. Melikian и соавт. было отмечено, что перевод пациентов с СД 2-го типа, как с монотерапии, так и с комбинированной терапии со свободными компонентами на фиксированную комбинацию антидиабетических препаратов характеризовались более высокой приверженностью к лечению по сравнению с пациентами, которым была назначена свободная комбинация препаратов [81].
Результаты исследования E. Cersosimo и соавт. продемонстрировали, что применение фиксированных комбинаций у пациентов с вновь диагностированным СД 2-го типа снижает клиническую инертность врачей и позволяет быстрее достичь целевого уровня гликированного гемоглобина (НbA1c), что, вероятно, позволяет отсрочить прогрессирование СД, предупреждает развитие осложнений болезни. При пошаговой комбинированной терапии, с постепенным увеличением количества антидиабетических препаратов и титрацией доз, отмечалась высокая приверженность пациентов к лечению, однако целевые значения НbA1c достигались позже и, следовательно, удлинялся период гипергликемии. Тем не менее использование фиксированных комбинаций имело свои недостатки, главным из которых была сложность определения препарата, ответственного за недостаточную эффективность и побочные эффекты лечения [82].
Рекомендовано:
Использование комбинированной терапии, основанной на рациональных свободных и фиксированных комбинациях (последние предпочтительней), — перспективный путь улучшения приверженности на разных фазах лечения; снижения полипрагмазии при повышении эффективности и безопасности лечения пациентов с ХНИЗ, а также уменьшения клинической инертности врачей в отношении достижения целевых показателей эффективности терапии.
Особенности терапии и приверженности к ней у пациентов с ХНИЗ в период сезонных эпидемий ОРВИ, гриппа, COVID-19
Острые респираторные вирусные инфекции (ОРВИ), грипп, а также новая коронавирусная инфекция — COVID-19, как правило, протекают существенно тяжелее у пациентов с ХНИЗ, приводя к декомпенсации состояния, повышению риска развития различных осложнений, связанных как с ХНИЗ, так и с инфекционным заболеванием. В связи с этим мероприятия по поддержанию приверженности пациентов на удовлетворительном уровне чрезвычайно важны, т.к. временный перерыв или полный отказ от терапии ССЗ сами по себе могут приводить к развитию жизнеугрожающих состояний у таких больных [83].
Рекомендовано:
Учитывая возникающие в период эпидемий, карантина и мероприятий по самоизоляции сложности посещения медицинских учреждений, необходимо, по возможности, обеспечить дистанционную связь пациентов с лечащими врачами для решения вопросов о терапии ХНИЗ и ее необходимой коррекции. При контакте с пациентом врачу в ходе прямого опроса обязательно следует задать вопрос о приеме рекомендованных пациенту препаратов для лечения ХНИЗ (необходимо помнить, что к лечению разными препаратами у больных может быть разная приверженность), регулярности этого приема, непреднамеренных и преднамеренных самостоятельных изменений, перерывов или отмены терапии. Лечащим врачам следует мотивировать пациентов на продолжение приема рекомендованной терапии, соблюдение всех врачебных рекомендаций в отношении приема лекарственных препаратов, пояснив опасность возникновения серьезных осложнений ССЗ при самостоятельных изменениях дозы, кратности приема препаратов, перерывах или отмене лечения.
При ухудшении состояния пациенту следует связаться с лечащим врачом либо обратиться за скорой медицинской помощью (СМП). При возникновении симптомов инфекционного заболевания (повышение температуры, кашель, катаральные симптомы и др.) во время эпидемии COVID-19 больному ССЗ необходимо вызвать бригаду СМП. Учитывая, что все пациенты с ССЗ входят в группу риска тяжелого течения COVID-19, им показано лечение в условиях стационара с отделением интенсивной терапии.
На случай развития острого респираторного заболевания и экстренной госпитализации пациентам рекомендуется иметь при себе список всех принимаемых препаратов (с указанием наименования, дозы и кратности приема каждого лекарственного средства), а также запас лекарственных препаратов, которые следует взять с собой в стационар.
При назначении лечения ОРВИ, гриппа или COVID-19 пациентам с ХНИЗ врачам рекомендуется оценить сочетание уже принимаемых пациентом препаратов и назначаемой терапии на предмет нежелательных лекарственных комбинаций. Список возможных комбинаций лекарственных препаратов при лечении COVID-19 у больных ХНИЗ с указанием их рациональности и потенциальных рисков нежелательных взаимодействий приведен на сайте www.covid19-druginteractions.org
Особенности лечения и приверженности к нему у больных с хроническими заболеваниями при острой патологии и оперативных вмешательствах
Пациенты с ХНИЗ входят в группу риска более тяжелого течения острых заболеваний и периоперационных осложнений.
Острые заболевания часто приводят к декомпенсации ХНИЗ, необходимости усиления проводимого лечения, коррекции доз принимаемых препаратов, иногда — назначения дополнительных лекарственных средств. Кроме того, острая патология требует назначения дополнительных фармпрепаратов, которые необходимо оценить на предмет межлекарственного взаимодействия с уже получаемыми средствами.
Экстренные и плановые оперативные вмешательства также нередко требуют коррекции получаемой пациентом терапии. При оказании анестезиологического пособия, как правило, отменяют ингибиторы моноаминоксидазы, некоторые нестероидные противоспалительные препараты. Обычно при хирургических вмешательствах заблаговременно отменяют препараты, действующие на систему гемостаза (для профилактики интра- и постоперационных осложнений): антиагреганты, антикоагулянты. Во избежание развития тромботических осложнений (особенно при высоком/очень высоком риске последних) назначается терапия короткодействующими и поэтому более легко управляемыми аналогами (например, замена оральных антикоагулянтов на препараты гепарина).
Тем не менее все изменения должны выполняться исключительно по рекомендации лечащего врача и под врачебным наблюдением. В то же время значительную роль в успешности лечения острых заболеваний, профилактике постоперационных осложнений и декомпенсации ХНИЗ играет хорошая приверженность пациентов к врачебным назначениям. Результаты исследования K. Norby и соавт. продемонстрировали, что приверженность больных к выполнению рекомендованных мероприятий по предоперационной подготовке значительно снизило число как интра-, так и постоперационных осложнений, продолжительность госпитализации. Кроме того, результаты работы показали, что предшествующая неудовлетворительная приверженность к лечению пациентов с ХНИЗ часто являлась причиной, по которой оперативное вмешательство вынужденно откладывалось или отменялось [84].
Рекомендовано:
Информировать пациентов о строгой необходимости оставаться приверженными к получаемой терапии ХНИЗ в случае острых заболеваний и при подготовке к плановым операциям. Заранее проконсультироваться с лечащим врачом и врачом-анестезиологом о необходимости (или отсутствии таковой) отмены/замены ряда препаратов. Строго выполнять все рекомендации врача по необходимой коррекции терапии ХНИЗ. Для профилактики периоперационных осложнений тщательно выполнять все мероприятия по подготовке к оперативному вмешательству.
3. Заключение
Проблема приверженности к лечению была и остается одной из самых сложных и трудно решаемых, что признают большинство авторов, занимающихся изучением данной темы. Вероятней всего, это объясняется тем, что в приверженность вносят свой вклад очень большое количество факторов, влияющих на совершенно разные стороны этого многогранного понятия. Многофакторность проблемы приверженности к терапии, сложность надежной диагностики и несовершенство методов ее эффективного контроля существенно осложняют, не уменьшая актуальности, решение этой проблемы, а также подчеркивают необходимость дальнейшего поиска наиболее эффективных методов воздействия на приверженность.
Согласно накопленным сведениям из многочисленных исследований по данной проблеме, их систематических обзоров с метаанализом, обозначается ряд перспектив ее дальнейшего изучения и развития. Возможным путем эффективного решения проблемы приверженности является комплексное воздействие на все или хотя бы большинство ее факторов и аспектов, а «ключевая роль» в данном процессе отводится лечащему врачу.
4. Список использованных сокращений
MEMS — Medication Events Monitoring System
MPR — medication possession ratio — метод учета полученных (приобретенных) пациентом лекарственных препаратов
PDC — proportion of days covered — метод реализуемости выписанных рецептов
АГ — артериальная гипертония
АД — артериальное давление
ВР — врачебные рекомендации
ВОЗ — Всемирная организация здравоохранения
ИБС — ишемическая болезнь сердца
КР — клинические рекомендации
ЛС — лекарственные средства
НОДФ — Национальное общество доказательной фармакотерапии
ОИМ — острый инфаркт миокарда
ОРВИ — острая респираторная вирусная инфекция
РКП — реальная клиническая практика
СД — сахарный диабет
СМП — скорая медицинская помощь
ССЗ — сердечно-сосудистые заболевания
ХНИЗ — хронические неинфекционные заболевания
ХС ЛПНП — холестерин липопротеидов низкой плотности
ХСН — хроническая сердечная недостаточность
5. Состав рабочей группы
Лукина Юлия Владимировна — ведущий научный сотрудник отдела профилактической фармакотерапии ФГБУ «НМИЦ TПМ» Минздрава России, к.м.н.
Кутишенко Наталья Петровна — руководитель лаборатории фармакоэпидемиологических исследований ФГБУ «НМИЦ TПМ» Минздрава России, д.м.н.
Марцевич Сергей Юрьевич — руководитель отдела профилактической фармакотерапии ФГБУ «НМИЦ ТПМ» Минздрава России, президент Национального общества доказательной фармакотерапии, председатель секции «Рациональная фармакотерапия» РКО, д.м.н., профессор
Шепель Руслан Николаевич — помощник директора по региональному развитию, руководитель отдела организационно-методического управления и анализа качества медицинской помощи ФГБУ «НМИЦ ТПМ» Минздрава России, главный внештатный специалист-терапевт ЦФО Минздрава России
Драпкина Оксана Михайловна — директор ФГБУ «НМИЦ ТПМ» Минздрава России, проф., д.м.н., член-корр. РАН, главный внештатный специалист по терапии и общей врачебной практике Минздрава России
Комплаентность (англ. patient compliance) в литературе определяется как «соблюдение больным режима и схемы лечения». Этот термин был предложен в 70х годах прошлого столетия [1]. I. E. Leppik дает широкое определение комплаентности с тремя составляющими: тип поведения, степень комплаентности и степень целеустремленности пациента. При этом тип поведения включает прием препарата, регулярность визитов в клинику и правильное выполнение других врачебных рекомендаций [1]. Используется также другой термин — «приверженность терапии» (англ. adherence therapy), под которым понимается соблюдение указаний врача. Эти термины близки по своему смыслу и могут применяться как синонимы [2].
Многие авторы рассматривают проблемы эффективности терапии хронических заболеваний (эпилепсии, психических заболеваний, диабета и др.), первичной и вторичной профилактики с точки зрения соблюдения рекомендаций врача [3, 4]. Между тем проблема недостаточной комплаентности существует во всем мире. Например, в Европе хорошую приверженность профилактическому приему ацетилсалициловой кислоты имели 63% больных. В странах Латинской Америки и Азии хорошая приверженность лечению отмечена лишь у 54% и 55% больных соответственно. В России показатели комплаетности сопоставимы с европейскими (59%) [3–5]. По данным ВОЗ, длительное соблюдение назначений врача при хронических заболеваниях наблюдается лишь в 50% случаев [6].
В России с 2016 г. внедряется новая модель медицинской реабилитации [7]. Согласно этой модели, координацией реабилитационных действий в отношении пациентов с ограничением жизнедеятельности должен заниматься новый специалист — врач–реабилитолог (врач по физической и реабилитационной медицине), а сам процесс реабилитации строится на мультидисциплинарном, пациентцентрированном и проблемноориентированном принципах.
Реабилитационная команда работает по реабилитационному плану, сформированному на основе реабилитационного диагноза [7]. Каждая проблема пациента становится задачей реабилитации для одного из участников реабилитационной мультидисциплинарной бригады (МДБ), что отражается в реабилитационном диагнозе. Реабилитационный диагноз может быть инструментом для повышения комплаентности, при этом каждый специалист МДБ может внести свою лепту в обеспечение приверженности терапии. Не только врач, но и эрготерапевт, медицинская сестра, методист ЛФК имеют возможность вносить в реабилитационный диагноз информацию о пациенте, которая относится к их компетенции и влияет на функционирование больного. Таким образом, в нем не только отражаются нарушения функций, которые обычно определяют выбор врачом лекарственного вещества и формы препарата, но и фиксируются убеждения пациента, его установки, особенности характера, негативный опыт, варианты мотивации, родственники, которые могут способствовать или препятствовать приверженности терапии. Анализ показывает, что даже у пациентов с транзиторной ишемической атакой, т. е. у больных без нарушения функций, в остром периоде заболевания в реабилитационных диагнозах имеются домены Международной классификации функционирования (МКФ), связанные с приверженностью.
Следует добавить, что в новой модели реабилитации «школа пациента», проводимая врачом и психологом, рассматривается в качестве важной и эффективной реабилитационной технологии, которая должна оплачиваться, как и другие интервенции. Таким образом, реабилитационный подход позволяет решить многие проблемы, касающиеся обеспечения приверженности терапии.
В целях реализации проблемноориентированного принципа новой модели реабилитации планирование лекарственной терапии и обеспечение комплаентности следует начать с вопроса пациенту и реабилитационной команде: «Почему пациент не принимает лекарства?» Стратегия повышения приверженности лечению и реабилитации включает следующие задачи:
- выяснить причину и устранить ее;
- если устранить причину невозможно, то адаптировать пациента к данной проблеме;
- перенести заботу о приеме лекарств на родственников или близких;
- найти эффективный способ контроля за приемом лекарств.
В современной литературе выделены 250 факторов, обусловливающих отношение больных к соблюдению режима терапии [8]. Общепризнанным является их разделение на четыре группы: факторы, связанные с пациентом; факторы, связанные с терапией; факторы, связанные с врачом, и факторы, связанные с окружением (социальный аспект) [9]. Комплаентность отражает сложное взаимодействие этих факторов, состав которых меняется в динамике заболевания и на отдаленных этапах может существенно отличаться от начального [10].
С позиций физической и реабилитационной медицины упомянутые выше факторы следует описывать в реабилитационном диагнозе в категориях МКФ [7]. Так, причины низкой комплаентности должны быть рассмотрены с позиций нарушения функций и структур, ограничения деятельности (активности и участия), влияния персональных факторов или факторов внешней среды. В данном обзоре приводятся все факторы, влияющие на комплаентность, в категориях МКФ, а также предложены способы разрешения проблем.
ФАКТОРЫ, СВЯЗАННЫЕ С ПАЦИЕНТОМ
К данной категории по МКФ следует отнести проблемы с функциями (b) и персональные (личностные) факторы пациента (e) (табл. 1). Многие врачи считают, что приверженность пациентов терапии зависит только от них самих, на самом деле пациентам принадлежит важная, но не исключительная роль. Понимание указанной группы факторов позволит врачам и реабилитационной команде изменить способы общения с больными и за счет этого помочь им принимать лекарства и выполнять предписанные рекомендации.
Таблица 1
Факторы снижения приверженности терапии, связанные с пациентом
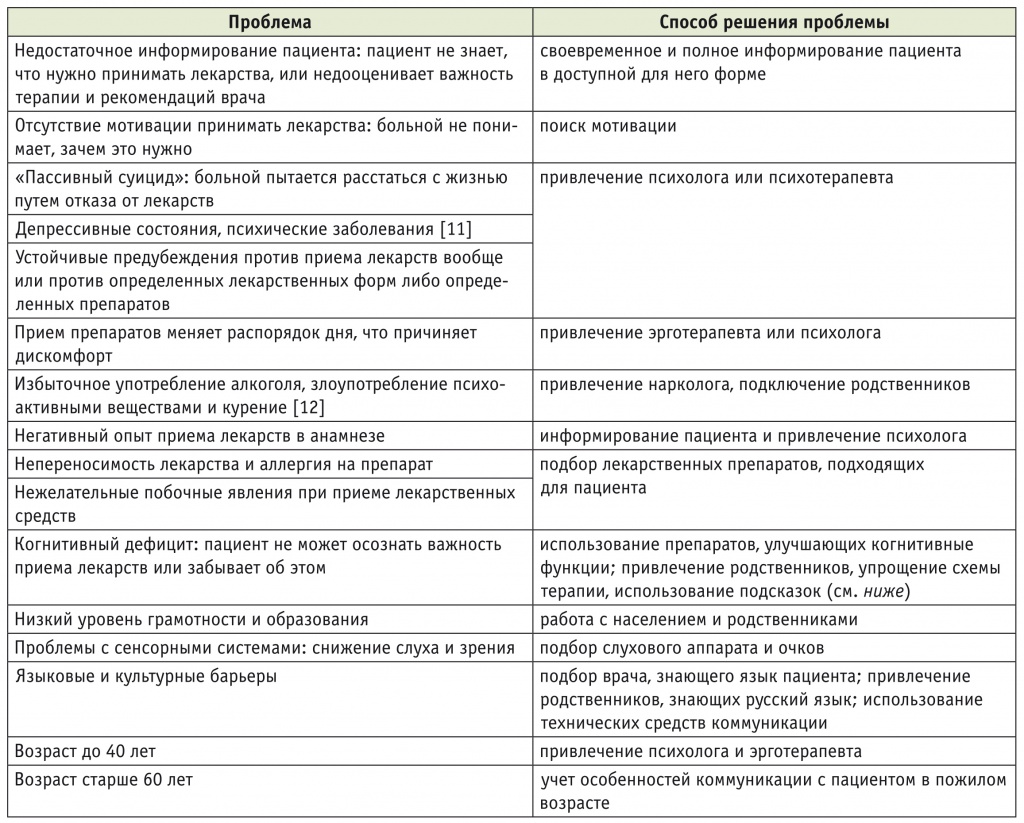
Остановимся подробнее на некоторых аспектах. Грамотность пациента и его родственников означает, что пациент может читать, понимать, помнить медицинские инструкции и действовать согласно полученной информации. Пациенты, имеющие низкий уровень грамотности, менее привержены терапии [13]. Для России характерна ситуация, при которой в деревнях и маленьких городах пациенты не верят в официальную медицину, не доверяют врачам, не привыкли выполнять рекомендации и имеют привычку принимать лекарства курсами, а не постоянно, как это требуется. Данная ситуация связана с низким уровнем организации здравоохранения в этих регионах и с разочарованностью населения оказываемой медицинской помощью. Важной частью проблемы является недостаточное информирование населения о медицине. Если в проблемных регионах повысить качество медицины и проводить регулярные встречи с пациентами и школы для больных и родственников, то в течение нескольких лет проблема может быть решена.
Важным аспектом терапии и реабилитации является информирование пациента. Проведенное нами исследование с участием группы пациентов в остром периоде инсульта показало, что если при поступлении в стационар больных информировать о среде и особенностях лечения их заболевания, то у них не развиваются тревога и депрессия [14]. К информированию о среде следует отнести информацию о числе, месяце и годе на момент поступления, о том, что случилось с пациентом, как он попал в больницу, чем болен, сколько времени проведет в больнице и как долго ему придется лечиться, ознакомление со схемой отделения и др. Происходило также информирование родственников. Данное исследование продемонстрировало, что у всех пациентов при поступлении имеется дефицит информации, который впоследствии может приводить к вторичным эмоциональноаффективным расстройствам, подлежащим лечению с помощью дорогостоящих психоактивных лекарств. Этого можно избежать, если проводить «бесплатную» интервенцию в виде разговора с пациентом, спокойного информирования о среде и ответов на вопросы больного.
В зарубежной литературе появляется все больше данных, свидетельствующих о важности информирования пациентов о деталях заболевания, его возможных осложнениях, об основных принципах и видах лечения в целях повышения приверженности терапии. Обсуждается необходимость рационализации подходов к назначению лекарственных веществ, при этом уделяется внимание не только научнодоказательной обоснованности их применения, но и убеждению пациентов в успешности проводимого лечения, регулярному напоминанию о приеме лекарств, контролю над процессом лечения и соблюдением пациентами рекомендаций [15].
Следует подчеркнуть, что информирование пациента входит в функциональные обязанности врачей, хотя на практике зачастую ими игнорируется.
Доказано, что приверженность выше, если пациент верит в успех терапии [16]. Наряду с грамотным информированием больного большое значение имеет формирование мотивации к соблюдению лекарственной терапии и рекомендаций врача.
Мотивацией пациента к приему лекарств могут быть:
- забота о своем здоровье;
- забота о родственниках — им будет тяжелее ухаживать за инвалидом;
- выгода в будущем (в том числе экономическая) — лучше сейчас принимать лекарства, чтобы потом не было инсульта, инфаркта или осложнений, так как при этом потребуется долгая и дорогая реабилитация;
- соответствие моде — принимать хорошее современное лекарство модно;
- избавление от проблемы — пройдет боль, улучшится память и т. д.
При рассказе о лекарствах следует привлечь внимание пациентов к реальным для них результатам терапии понятными для них словами. Например, многие пациенты убеждены, что препараты для лечения артериальной гипертензии принимаются только с целью снижения артериального давления, а характеристики этих лекарственных средств, которыми оперируют врачи, непонятны пациентам и поэтому не могут быть должным образом оценены. В отношении антигипертензивной терапии больные должны быть проинформированы о том, что данное лечение позволяет избежать инсульта и инфаркта, на несколько лет увеличивает продолжительность жизни, предотвращает развитие возрастных нарушений памяти и внимания, связанных с артериальной гипертензией, и позволяет решить многие другие проблемы, о которых не принято говорить пациентам. При таком представлении лекарств многие больные будут с большей приверженностью придерживаться рекомендаций.
Приведем несколько психологических приемов, которые можно использовать в разговоре с пациентом о лекарствах:
1) не пытайтесь напугать пациента: он может быть уже напуган, хоть и не признается в этом, и будет отторгать информацию в виде защитной реакции;
2) заставлять пациента — не лучшая стратегия: пациент начинает сопротивляться тому, что ему навязывают, так возникают распространенные предубеждения относительно того, что «все лекарства вредны», «врачи получают выгоду от назначения лекарств»;
3) предлагайте альтернативу — несколько похожих лекарств на выбор;
4) обсуждайте финансовый вопрос — готов ли больной тратить деньги на лекарства;
5) спросите у больного, расположен ли он принимать лекарства, и если нет, то что ему мешает; предложите больному выбрать вариант решения данной проблемы;
6) уважайте выбор пациента;
7) если пациент чегото не знает, то это еще не свидетельствует о наличии у него «интеллектуальных проблем»; у больного может быть негативный опыт, и он не всегда в этом виноват;

9) если вы не справляетесь, обратитесь к специалисту (психологу): привлечение коллег — это свойство профессионала;
10) сотрудничайте с пациентом.
Тревога, страх и депрессия могут повлиять на терапию и соблюдение врачебных предписаний. Если у пациента имеются такие состояния, то это может потребовать дополнительной лекарственной терапии. Однако практика работы МДБ показывает, что в российской реальности имеется гипердиагностика эмоциональноаффективных расстройств. Врачи (неврологи, кардиологи) часто необоснованно выставляют диагноз «депрессия», «тревожное расстройство» или «аффективные нарушения». При наличии в реабилитационной команде психолога возможно более точно определить причины страдания пациента, которые врачами часто интерпретируются как депрессия и тревога. За подобными жалобами могут скрываться: дистресс, переживания по поводу агрессивного поведения персонала, особенности характера пациента (замкнутость, интроверсия, флегматичный темперамент и др.), недостаточная информированность, психологические установки, защитная психологическая реакция в виде торможения или ухода от общения и др.
Одним из самых наглядных симптомов стресса является тревога, и с этой точки зрения не любую тревогу нужно подавлять. Тревога и страх могут стать ресурсом для обеспечения комплаентности: вместо того чтобы иметь риск повторного заболевания и испытывать страх смерти, лучше принимать лекарства.
Следует учесть, что не любая депрессия требует лекарственной терапии: во многих ситуациях пациенту может помочь психолог, что особенно важно при лечении и реабилитации пожилых пациентов. Важно помнить, что депрессия является одним из проявлений синдрома «пассивного суицида». Такая форма суицидальных устремлений не осознается пациентом; больной может заявлять, что хочет поправиться, и обещать принимать лекарства, однако будет забывать об их приеме, путать прописанные препараты с другими лекарствами, находить множество «объективных причин», чтобы их не купить, не принять и т. п. К данному синдрому, помимо неприема лекарств, следует отнести отказ от соблюдения диеты и модификации образа жизни, «опасный образ жизни» и др. Синдром достаточно часто встречается в российской практике и нередко остается без должного внимания со стороны медицинских работников. Особенность этого состояния заключается в том, что таких пациентов бесполезно пугать последствиями отказа от приема лекарств и заставлять вести правильный образ жизни: данная стратегия может нанести вред пациенту и способствовать усилению суицидальной наклонности, так как неосознаваемая цель больного и заключается в том, чтобы умереть как можно раньше. Синдром «пассивного суицида» может быть выявлен психологом или психотерапевтом, и именно эти специалисты должны с ним работать.
Наличие устойчивых предубеждений против приема лекарств вообще или против определенных лекарственных форм либо определенных препаратов также требует подключения психолога. Как правило, пациенты скрывают отрицательное мнение о лекарствах, и при поверхностной беседе с лечащим врачом проблема может быть не выявлена. Необходимо обратить внимание на то, что тревожное, и даже фобическое, отношение к лекарственным средствам встречается все чаще.
Следующая проблема, приводящая к нарушению комплаенса, — неумение пациента встроить прием препаратов в график привычной жизни. Если препарат необходимо запивать водой, принимать до или после приема пищи, работающие пациенты достаточно быстро перестают принимать назначенные лекарства систематически. Проблема легко решается при консультировании больного эрготерапевтом, который поможет интегрировать прием лекарств в повседневную жизнь, используя простые приемы и приспособления (мобильные приложения, напоминающие о приеме таблетки за определенное больным время; ношение с собой минимального запаса пищи в тубе, что позволит питаться даже на ходу, и т. п.).
Когнитивные проблемы — распространенные причины, ограничивающие приверженность терапии в разном возрасте. Особенности общения с пациентами, у которых имеются когнитивные нарушения, описаны в статье.
ФАКТОРЫ, СВЯЗАННЫЕ С РЕАБИЛИТАЦИОННОЙ КОМАНДОЙ
Врач, психолог, эрготерапевт, специалист по ЛФК, медицинская сестра и другие специалисты, вовлеченные в оказание медицинской помощи, а также их убеждения и установки являются составляющей здоровья пациента и относятся в МКФ к факторам внешней среды (е). Невежливая медсестра или невнимательный врач могут быть барьером в реабилитации и обеспечении приверженности терапии, а персонал, обученный создавать комфортные условия и уменьшать проявления стресса, способствует успешной реабилитации и повышению комплаентности.
Взаимоотношения между пациентом и медицинским работником — один из факторов, определяющих комплаентность [17, 18]. Доказано, что эмоциональная поддержка, партнерские отношения повышают приверженность лечению, тогда как врачи, которые задают мало вопросов, редко непосредственно контактируют с пациентами, пишут неразборчивые рекомендации в выписках, имеют большее количество пациентов, не соблюдающих режим и схему лечения [17, 18].
Базовым условием достижения хорошей приверженности больного лечению является врачебная квалификация. По данным С. Н. Мосолова, около 50% случаев неэффективности терапии связаны с ее неадекватным применением. Помимо несоблюдения клинических показаний и противопоказаний при назначении лекарств, распространенными ошибками являются проведение терапии низкими дозами, частая смена препаратов без соблюдения необходимой длительности приема, преждевременная отмена терапии и др. [9].
Чтобы обеспечить должную комплаентность, врачу и реабилитационной команде необходимо правильно определять цели терапии и реабилитации, а также быть настойчивыми в их достижении, иметь возможность соблюдать необходимую кратность встреч с пациентом. Наличие цели в медицинской реабилитации имеет принципиальное значение для ее эффективности [19]. Цель устанавливается по мнемоническому правилу SMART, аббревиатура имеет значение «умная цель» и расшифровывается следующим образом: S — Specific (конкретный), M — Measurable (измеримый), A — Attainable, Achievable (достижимый), R — Relevant (актуальный) и T — Timebound (определенный во времени). Цель всегда выстраивается с ориентацией на жизнь пациента и его привычную деятельность. Важно озвучить цель для больного, с тем чтобы он стремился к ее достижению.
Реабилитацию пациента проводит мультидисциплинарная реабилитационная команда, а значит, в обеспечении приверженности терапии могут принимать участие все специалисты МДБ. Поэтому расширение знаний младшего и среднего медицинского персонала, психологов, эрготерапевтов, логопедов и специалистов по лечебной физкультуре по вопросами соблюдения режима терапии в немалой степени способствует повышению согласованности действий реабилитационной команды и больного в процессе терапии и реабилитации [9, 20, 21]. В рамках общей работы по обеспечению комплаентности у специалистов МДБ могут быть специфические задачи, соответствующие их базовому образованию, компетенции и функциональным обязанностям. В таблице 2 приведены примеры задач, которые могут решаться разными специалистами МДБ.
Таблица 2
Задачи по обеспечению приверженности терапии, решаемые специалистами мультидисциплинарной реабилитационной бригады
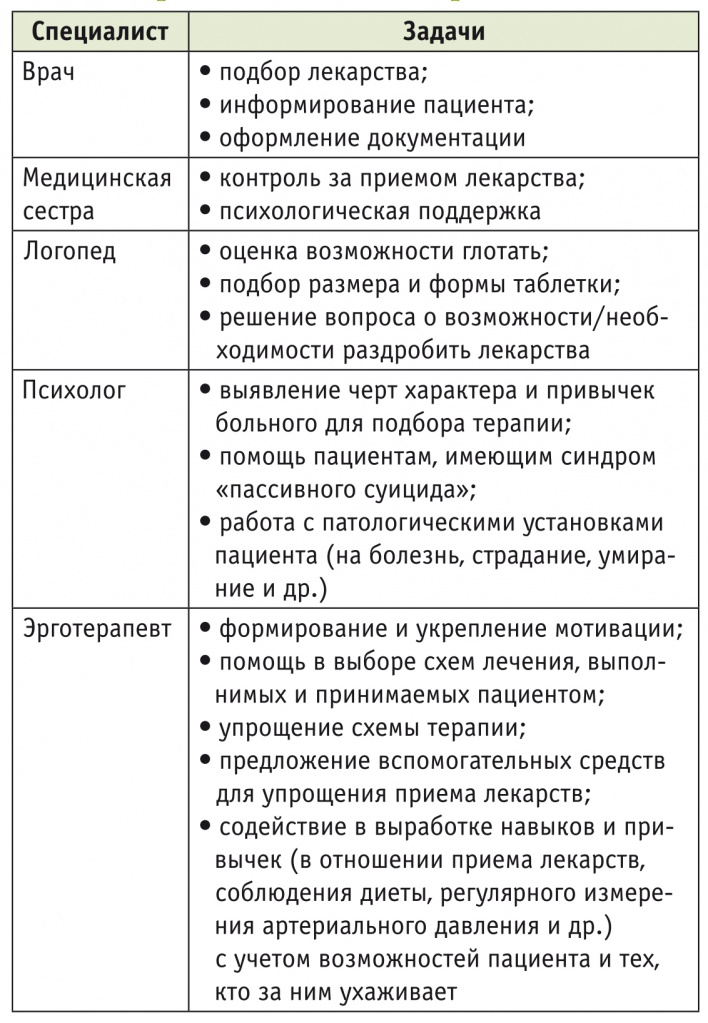
Мультидисциплинарный принцип в работе с приверженностью терапии предусматривает следующие правила:
- каждый участник МДБ должен быть в курсе проводимой лекарственной терапии;
- в команде должно быть единое представление о терапии, так как разногласия могут помешать главной цели — помощи пациенту;
- работа МДБ должна строиться на основе взаимной поддержки и помощи (например, если на занятии по ЛФК пациент сообщил инструктору о своем недовольстве лекарством, то это может стать поводом для рассмотрения вопроса на встрече МДБ);
- в МБД должен присутствовать единый «командный дух», когда все участники направляют свои силы на обеспечение комплаентности и помощи пациенту.
Ответственным за лекарственную терапию и обеспечение комплаентности является лечащий врач, перед которым стоят следующие задачи:
- подобрать препарат, в наибольшей степени подходящий для пациента (с хорошей переносимостью, минимумом нежелательных явлений, удобной формой, помогающий, решающий задачи пациента);
- рассказать о препарате в доступной для пациента форме (зачем принимать, какие задачи решает препарат, каковы его плейотропные эффекты);
- написать и объяснить схему приема лекарства и рассказать, как контролировать терапию, когда ждать эффекта;
- обсудить вопрос взаимодействия с другими препаратами;
- найти мотивацию приема препарата.
Информирование больного может происходить во время беседы с врачом, посредством буклетов и информационных материалов (информационные стенды) и путем проведения «школ пациента».
«Школа пациента»:
- снижает нагрузку на врача в части рассказа о лекарствах и заболевании;
- позволяет пациенту увидеть, что есть такие же больные, как он, которые выздоравливают, принимая те же лекарства;
- дает возможность пациенту задать вопрос или услышать ответ на вопрос, который он боится задать;
- может посещаться пациентом неоднократно, что создает условия для повторения;
- является «клубом по интересам», что способствует снижению коммуникативной депривации;
- осуществляет деятельность, которая занимает пациента;
- представляет собой один из способов реабилитации (и должна оплачиваться по соответствующему тарифу).
При проведении школы должна сохраняться атмосфера комфорта и уюта. Не должно быть принуждения к занятиям: посетитель получает новые знания, потому что ему это интересно, а не потому что его заставляют.
При проведении школ для больных с когнитивными нарушениями необходимо многократно обучать пациентов алгоритмам поведения при изменении в состоянии их здоровья. Многие пациенты с когнитивными нарушениями нуждаются в том, чтобы информация, воспринимаемая при помощи зрительного анализатора, была максимально простой для запоминания.
Приведем аспекты приема лекарств, наиболее актуальные для «школ пациента»:
- лекарства подбираются индивидуально, не следует принимать то же, что принимает сосед;
- не все лекарства вредны;
- многие препараты нужно принимать длительно;
- «лекарственных каникул» не существует;
- вредно пропускать прием лекарства;
- многие препараты для профилактики инсульта обладают массой других полезных свойств (сохраняют память и внимание, увеличивают продолжительность жизни, позволяют избежать инсульта, снижают артериальное давление);
- всегда надо иметь запасную упаковку лекарства;
- готовясь к поездке на дачу или в отпуск, следует продумать количество лекарств, чтобы их хватило на весь период.
ФАКТОРЫ, СВЯЗАННЫЕ С ТЕРАПИЕЙ
Лекарства являются факторами среды (е) для пациента и могут стать как барьерными факторами (полипрагмазия, сложные схемы и неудобные формы приема лекарства), так и поддерживающими (комбинированные препараты, простые схемы приема).
Данные литературы демонстрируют, что чем быстрее происходит подбор эффективного лечения, тем лучше в последующем приверженность больного данному лечению. Меньшее число смен терапевтических схем оказывает позитивное психологическое действие на больного и способствует повышению его комплаентности. Например, при внесении в течение первых 6 месяцев лечения одного изменения в терапию количество некомплаентных пациентов в последующие 6 месяцев составляет лишь 7%, а при двукратном изменении — уже около 25% [9].
Сложность медикаментозного режима (высокая кратность приема препарата и прием нескольких препаратов) негативно сказывается на комплаентности пациентов, а следовательно, и на эффективности лечения. При однократном приеме лекарств комплаентны 87% пациентов, при двукратном — 81%, при трехкратном — 77%, при четырехкратном — всего 39% [12, 13].
Имеется также обратная зависимость между количеством принимаемых препаратов и приверженностью лечению [9]. Авторы выделяют три основные причины:
1) субъективное отношение больного, включая страх приема относительно большого количества препаратов;
2) более высокая стоимость многокомпонентной терапии по сравнению с однокомпонентной;
3) сложность режима приема и, соответственно, бóльшая вероятность нарушений (например, при увеличении количества ежедневно принимаемых таблеток от одной до четырех вероятность соблюдения режима снижается вдвое).
На комплаентность влияет продолжительность лечения. Пациенты обычно комплаентны в первый месяц терапии (уровень приверженности составляет 79,4% [22]). Увеличение сроков течения заболевания и продолжительности лечения приводит к ухудшению комплаентности [9].
К медицинским факторам относят также побочные эффекты лекарств. Важнейшим условием, определяющим соблюдение режима терапии, является хорошая переносимость, т. е. отсутствие какихлибо неприятных субъективных переживаний (дополнительного дистресса), связанных с приемом лекарственного препарата [9]. Важно проинформировать пациента о возможных нежелательных явлениях, что позволит психологически подготовить его к трудностям приема лекарств. Предписывая лекарство, врач должен в письменном виде указать, как его применять: в каком режиме, в какой дозировке и по сколько таблеток в день, в какое время, в течение какого периода, какие обследования ассоциированы с лекарством и каким должен быть контроль эффективности терапии (дневник артериального давления при лечении артериальной гипертензии, дневник боли при лечении болей, контроль липидного спектра при использовании гиполипидемической терапии, контроль МНО при приеме варфарина и т. д.). Эту информацию надо отражать в документах, выдаваемых пациенту на руки, чтобы он в любой момент мог обратиться к ним и уточнить особенности приема лекарственного препарата.
ВЛИЯНИЕ ВНЕШНИХ ФАКТОРОВ
Данная группа факторов по МКФ относится к категории факторов окружающей среды (е). Она включает в себя безработицу, ранний выход на пенсию, инвалидность, определяющие низкий уровень жизни, недостаточно развитую систему медицинского страхования. В эту группу входят также такие факторы системы здравоохранения, как низкая доступность медицинской помощи, длительное ожидание визита к врачу, неудачные посещения поликлиники, которые существенно снижают приверженность лечению [9]. Внедрение в рамках новой модели медицинской реабилитации пациентцентрированного принципа позволит частично решить данную проблему [7]. С другой стороны, развитие технологии дистанционных реабилитационных и лечебных интервенций будет способствовать увеличению доступности медицинской помощи и поможет получить дополнительный инструмент по контролю лекарственной терапии.
Имеются данные, что пациенты, получающие эмоциональную и социальную поддержку со стороны семьи, друзей и медицинских работников, более привержены терапии [23]. Благополучное семейное положение (замужество или женитьба) благоприятно сказывается на комплаентности [13, 24].
При развитии заболевания и, особенно, инвалидности могут страдать не только сами пациенты, но и их родственники [24]. На последних могут быть возложены обязанности по уходу за пациентом, проведению простых реабилитационных мероприятий и контролю за приемом лекарств. Показано, что чем больше ограничена мобильность пациента, тем бо’льшую выраженность имеют депрессия и тревога у родственников [24]. Поэтому у родственников таких пациентов обычно имеется мотивация принимать активное участие в реабилитации. Те из них, кто готов участвовать в процессе реабилитации, могут быть обучены специалистами МДБ. В плане обеспечения приверженности лечению и контроля над лекарственной терапией родственники могут:
- полностью взять на себя выдачу препарата;
- следить за применением лекарств и за режимом приема;
- подготавливать и заполнять таблетницы;
- помогать применять препарат, когда пациент сам не может этого сделать (лекарства могут выдаваться через зонд или добавляться в пищу).
СТРАТЕГИИ ПОВЫШЕНИЯ ПРИВЕРЖЕННОСТИ ТЕРАПИИ
Основа выстраивания стратегии обеспечения приверженности терапии — всесторонний проблемноориентированный анализ ситуации пациента, изучение особенностей жизни, видов деятельности и привычек больного, что позволит определить опорные позиции для подбора терапии. Ниже приводятся некоторые пути повышения комплаентности:
1. Упрощение схемы, например:
- назначение комбинированных препаратов типа «2 в 1» снижает нагрузку по запоминанию и выполнению схемы в 2 раза;
- однократный прием лучше, чем многократный.
2. Выработка навыков и привычек: обучение алгоритму приема лекарств, связанному с подсказками (будильник, программа для телефона, визуальное расписание), модификация среды (таблетницы, таблетницы с таймером и т. п.).
В настоящее время среди пациентов популярны приложения на смартфонах. Такие приложения могут сообщить пациенту о терапии, но не могут произвести никакого действия, т. е. они не решат проблему, но помогут упростить работу над приверженностью. Наиболее популярными приложениями на русском и английском языках для iOS и Android являются: Medisafe, MyTherapy, Tabletten Erinnerung + Sprache, «Пилюлинг», Medication, «Мои Таблетки — напоминания», AnyTimer Pill Reminder, «Напоминалка», Light Pill Reminder и Dosecast.
Перспективным приспособлением для обеспечения комплаентности являются таблетницы с таймером. Наиболее известные из них: GlowCap, AdhereTech, MedReady 1700, MedCenter System [25]. Данные системы связаны с приложением в телефоне и имеют следующие опции:
- напоминают о необходимости приема лекарства;
- отсылают информацию родственникам о принятии/непринятии лекарства пациентом;
- могут работать как дозатор, контролируя количество таблеток, принятых пациентом;
- ведут дневник приема лекарств;
- контролируют количество оставшихся препаратов;
- отсылают автоматический запрос в ближайшую аптеку с просьбой восполнить запас закончившихся таблеток.
3. Использование дополнительной терапии, влияющей на энергетический баланс. Прием препаратов может существенно влиять на поведение и циклы активности пациента, что, в свою очередь, оказывает влияние на его мотивацию и выбор активностей. Так, назначение препаратов, усиливающих метаболические процессы, является отличной основой для проведения тренировок на запоминание или выработку нового навыка (например, иного алгоритма использования руки при парезе).
4. Применение лекарств, влияющих на поведение, при этом надо помнить, что:
- пациенту могут быть назначены препараты, влияющие на мотивацию и нейрогенез, однако сами по себе, без необходимой активности пациента, они будут менее эффективны;
- разведение во времени курса лечения препаратами и программы реабилитации снизит эффективность работы по восстановлению пациента;
- препараты для лечения деменции и коррекции когнитивных процессов позволят повысить внимание и контроль над терапией.
5. Использование дневника приема лекарств и контроля лабораторных тестов, частоты сердечных сокращений и артериального давления; дневника деятельности. Участие пациента в своей судьбе организует его и способствует укреплению дисциплины в целом, что позитивно влияет на процесс лечения и реабилитации.
ЗАКЛЮЧЕНИЕ
Низкая комплаентность — это сложная проблема, причинами которой могут быть как внутренние, так и внешние факторы. Мультидисциплинарный подход в реабилитации дает возможность привлечь к решению проблем комплаентности любого специалиста реабилитационной бригады. Новая модель медицинской реабилитации позволяет получить новые инструменты по работе с приверженностью. Реабилитационный подход требует от реабилитологов анализа ситуации и планирования терапии на долгосрочной основе с оценкой перспектив всей жизни пациента.



