Рекомендации:
— Рекомендуется изначальное назначение пероральных тетрациклинов, таких как доксициклин или лимециклин, в течение как минимум 12 недель, с рассмотрением перерывов в лечении для оценки необходимости в продолжении лечения и для снижения риска антимикробной резистентности.
— Пациентам, которые не реагируют на пероральные тетрациклины, рекомендуется комбинированное лечение с применением перорального клиндамицина 300 мг два раза в день и рифампицин 300 мг два раза в день в течение 10 — 12 недель.
— Рассмотрите применение ацитретина 0,3 — 0,5 мг/кг/день у мужчин и нефертильных женщин, которые не реагируют на лечение антибиотиками.
— Рассмотрите применение дапсона у пациентов, которые не реагируют на лечение антибиотиками.
— При неуспешном применении традиционной системной терапии у пациентов с гидраденитом средне-тяжелой степени, рекомендуется применение адалимумаба 40 мг еженедельно.
— Пациентам, которые не реагируют на адалимумаб, рассмотрите инфликсимаб 5 мг/кг каждые 8 недель.
— Рассмотрите применение 1% раствора клиндамицина.
— Для тщательно отобранных индивидуальных участков поражения во время острой фазы рассмотрите инъекции кортикостероидов непосредственно в участки поражения.
— Рассмотрите применение метформина у пациентов с гидраденитом и сочетанным сахарным диабетом, а также у женщин с гидраденитом и с синдромом поликистозных яичников или беременностью.
— Рассмотрите возможность широкого иссечения для минимизации частоты рецидивов.
— Рассмотрите возможность широкого иссечения у пациентов с неуспешным традиционным системным лечением.
— После выполнения широкого иссечения рассмотрите заживление вторичным натяжением (или лоскут на основе перфорантных сосудов торакодорсальной артерии для подмышечных ран).
— Не рекомендуется применение изотретиноина у пациентов с гидраденитом, если только нет сочетанного умеренно-тяжелого поражения акне лица или туловища.
— Не рекомендуется применение адалимумаба 40 мг через неделю у пациентов с гидраденитом средне-тяжелой степени при неуспешном применении традиционной системной терапии.
— Не рекомендуется применение этанерцепта у пациентов с гидраденитом средне-тяжелой степени при неуспешном применении традиционной системной терапии.
— Не рекомендуется применение криотерапии для лечения участков поражения в острой фазе ввиду боли от процедуры.
— Не рекомендуется применение микроволновой абляции у пациентов с гидраденитом.
Гнойный гидраденит: причины появления, симптомы, диагностика и способы лечения.
Определение
Гнойный гидраденит – это воспаление апокриновых потовых желез.
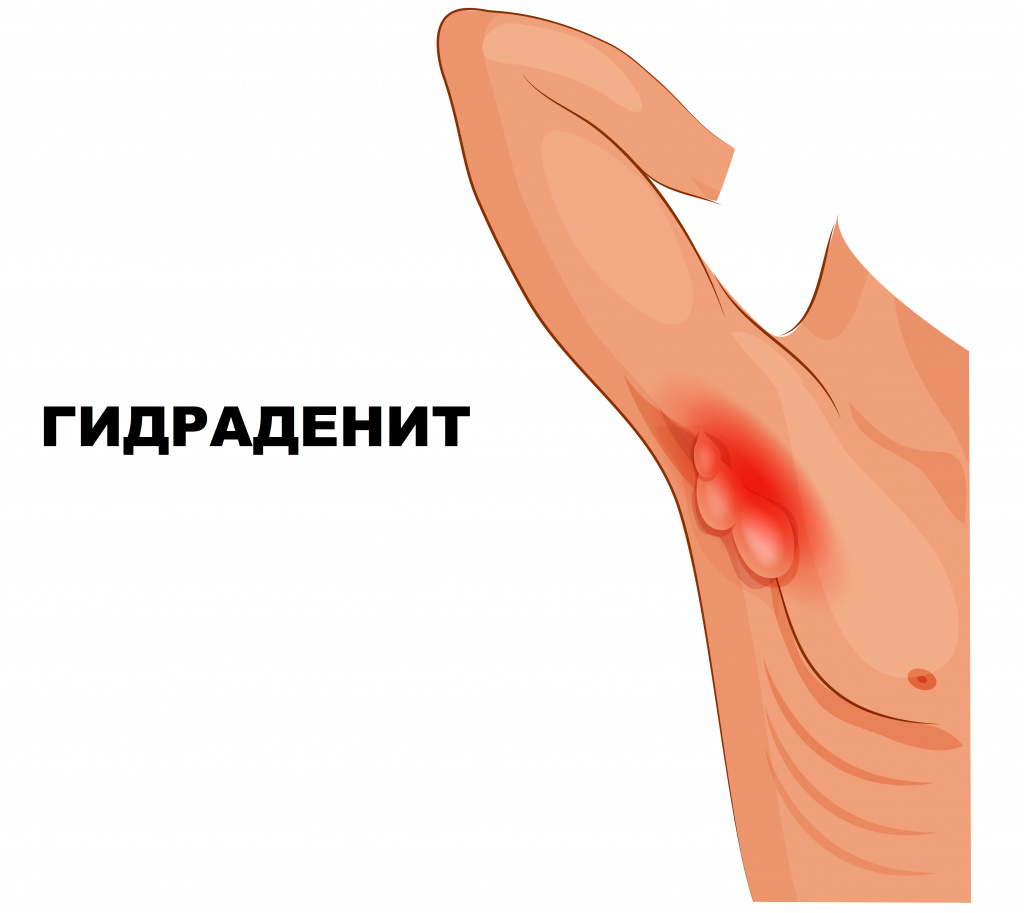
Апокриновые железы не участвуют в терморегуляции, а их секреция тесно связана с половой функцией – манифестирует в период пубертата и угасает с наступлением менопазуы. Этим объясняется тот факт, что заболевание не распространено среди детей и женщин старшего возраста.
Надо заметить, что у женщин апокриновых желез больше, чем у мужчин, в связи с этим гидраденит у них встречается в 4-5 раз чаще.
В общей популяции заболеваемость гнойным гидраденитом составляет примерно 1-4%. Для заболевания характерно хроническое рецидивирующее течение.
Причины возникновения гидраденита
Точный механизм развития гнойного гидраденита до конца не ясен. Большинство исследователей полагают, что в основе заболевания лежит поражение волосяного фолликула – его закупорка с последующим возникновением воспалительного процесса. В результате воспаления стенка фолликула разрывается и его содержимое выходит в дерму, откуда процесс распространяется на апокриновые железы. В дальнейшем происходит инфицирование различными микроорганизмами, как правило, золотистым стафилококком.
Ученые выделяют факторы, которые способствуют развитию гидраденита:
- факторы, снижающие бактерицидную активность кожного сала и пота: загрязнение кожи техническими маслами, горючими жидкостями, нарушение кровоснабжения кожи, переохлаждение или перегрев кожного покрова;
- факторы, повышающие проницаемость кожи: хронические дерматозы, микротравмы (в результате бритья, эпиляции), расчесы, опрелости кожи, гиповитаминозы А и С;
- факторы, снижающие уровень естественной резистентности организма: хронические интоксикации, наличие очагов стафилококковой инфекции в различных органах и тканях, общее переохлаждение и перегревание, нарушения обмена, анемии, переутомление, стресс, гиповитаминозы, эндокринные нарушения (например, сахарный диабет и другие нарушения углеводного обмена);
- факторы, подавляющие нормальную микрофлору кожи и снижающие ее защиту: частое мытье, чрезмерное использование антисептических парфюмерно-косметических средств.
Исследования показали, что чаще болеют хроническим гнойным гидраденитом курильщики, а тяжесть течения заболевания коррелировала с индексом массы тела – чем больше вес человека, тем тяжелее протекает гидраденит.
Классификация гидраденита
Хронический гнойный гидраденит классифицируется по степени тяжести:
- I степень тяжести характеризуется образованием одного или нескольких безболезненных или малоболезненных изолированных узлов и/или абсцессов, которые не склонны к острому прогрессированию и нагноению, фистулообразование («вскрытие» гнойников) и рубцевание отсутствуют.
- II степень тяжести — усиление воспалительного процесса, ограниченного одной локализацией, рецидивирующие узлы и абсцессы не сливаются, вскрываются и образуют свищевые ходы с гнойно-сукровичным отделяемым, некоторые элементы рубцуются.
- III степень тяжести — формируется обширный конгломерат воспалительных инфильтратов, состоящий из сливающихся узлов и абсцессов, усиливается размягчение, образуется множество сообщающихся между собой свищей, которые после заживления рубцуются.
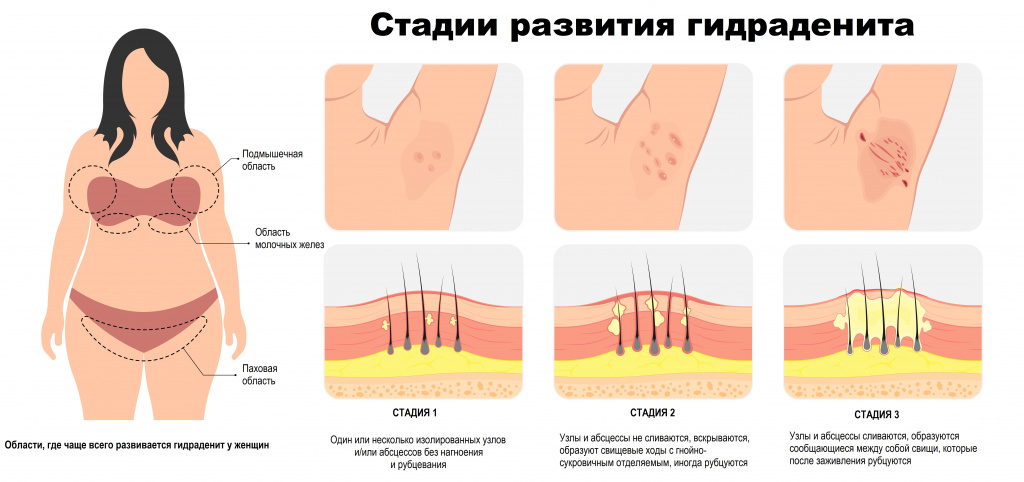
Типичные места локализации гидраденита – подмышечные впадины, где расположено наибольшее количество апокриновых желез, реже – паховая и перианальная области, а также области вокруг сосков и пупка.
В большинстве случаев гидраденит развивается с одной стороны, но иногда процесс может быть двусторонним.
Пациенты отмечают жжение, покалывание, боль или зуд в области поражения, предшествующие развитию заболевания. В глубоких слоях кожи формируются один или несколько плотных узлов диаметром до 3 см. Узлы постепенно увеличиваются, сливаются между собой и спаиваются с окружающими тканями, образуя сплошной болезненный воспалительный инфильтрат багрово-синего оттенка. Через 4-5 дней появляется размягчение (флюктуация), свидетельствующее о наличии гнойного содержимого, узлы вскрываются с появлением отверстия, из которого отделяется гной. После вскрытия гнойника самочувствие пациента, как правило, улучшается. Воспалительный процесс может захватывать несколько потовых желез или мигрировать с одной железы на другую.
После заживления на месте воспаления может остаться рубец.
Диагностика гидраденита
Диагноз «гидраденит» врач может установить на основании характерной клинической картины. Для выявления тяжести процесса и диагностики сопутствующих заболеваний, способных влиять на течение гидраденита, рекомендуют:
- общий (клинический) анализ крови;
Глюкоза (в крови) (Glucose)
Материал для исследования
Сыворотка или плазма крови. Если нет возможности центрифугировать пробу через 30 минут после взятия для отделения сыворотки/плазм…
Креатинин (в крови) (Creatinine)
Синонимы: Анализ крови на креатинин; Сывороточный креатинин; Креатинин сыворотки, оценка СКФ. Сreat; Сre; Blood Creatinine; Serum Creatinine; Serum Creat.
Краткая характеристика определя�…
Билирубин общий (Bilirubin total)
Синонимы: Общий билирубин крови; Общий билирубин сыворотки.
Totalbilirubin; TBIL.
Краткая характеристика определяемого вещества Билирубин общий
Билирубин – это пигм…
Общий белок (в крови) (Protein total)
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок.
Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР.
Краткая характеристика определяемого вещества Общий бе�…
Альбумин (в крови) (Albumin)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристика исследуемого вещества Альбумин
Альбумин – эт…
К каким врачам обращаться
Поставить диагноз и назначить лечение при гидрадените может
хирург
или дерматолог. При рецидивирующем течении могут потребоваться консультации
терапевта
и
эндокринолога
.
Лечение гидраденита
На первой стадии заболевания обычно ограничиваются местной терапией и используют различные антисептические, а также антибактериальные препараты для наружного применения. При прогрессировании процесса и при хроническом рецидивирующем гидрадените назначается системная антибиотикотерапия. Если процесс сопровождается выраженным болевым синдромом, назначают нестероидные противовоспалительные препараты.
При хроническом гидрадените любой стадии своевременное и широкое хирургическое иссечение гнойных очагов является наиболее эффективным способом лечения, предотвращает рецидивы и осложнения, а также улучшает качество жизни пациента.
Объем и вид хирургического вмешательства определяются хирургом индивидуально для каждого пациента, в зависимости от его возраста, степени тяжести и локализации воспалительного процесса, а также сопутствующих патологий.
Осложнения
Формирование рубцов после перенесенного гидраденита, например, в подмышечной области, может привести к ограничению движения конечности.
Кроме того, образование рубцовой ткани способно нарушить работу лимфодренажной системы и стать причиной возникновения отеков рук, ног или гениталий.
К другим тяжелым осложнением гидраденита относится распространение гнойного процесса с развитием флегмоны или сепсиса.
Профилактика гидраденита
Для профилактики гидраденита необходимо соблюдать санитарно-гигиенические нормы, своевременно проводить антисептическую обработку раневых поверхностей, не допускать появления трещин, микротравм (например, в результате бритья или эпиляции подмышечных областей), натирания кожи предметами одежды.
Снизить риск развития гнойно-воспалительного заболевания кожи может лечение общих заболеваний, которые способствуют развитию гнойничковых поражений (сахарный диабет, болезни ЛОР-органов, пищеварительной системы).
Пациентам с хроническим рецидивирующим гидраденитом рекомендован отказ от курения и снижение избыточной массы тела.
Источники:
- Клинические рекомендации «Пиодермии». Разраб.: Российское общество дерматовенерологов и косметологов. – 2020.
- Бурова С.А., Бородулина К.С. Гнойный гидраденит: вопросы патогенеза, оценочные шкалы, лечение (часть 2) // Клиническая дерматология и венерология. – 2019. – Т. 18. – № 3. – С. 265-269.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
2857
16 Апреля
-
2848
16 Апреля
-
2912
09 Апреля
Похожие статьи
Полипы желудка
Полипы желудка: причины появления, симптомы, диагностика и способы лечения.
Жировая дистрофия
Жировая дистрофия: причины появления, симптомы, диагностика и способы лечения.
Пародонтит
Пародонтит – хроническое воспалительное заболевание тканей, окружающих зуб. Постепенно это приводит к потере зубов у взрослого человека и способствует развитию патологических процессов в организме.
Остеомиелит
Остеомиелит: причины появления, симптомы, диагностика и способы лечения.
Введение
Гидраденит супаратива / акне инверса (ГС/АИ) — заболевание, известное ранее как синдром фолликулярной окклюзии. Этот термин был введен D.M. Pillsburry, W.B. Shelley и А.М. Kligman в 1956 г. [1]. Нынешнее название применяется с 2006 г., когда оно (после долгого периода путаницы в терминологии) было утверждено на 1-й Международной конференции по ГС/АИ в Дессау (Германия).
По разным данным, распространенность заболевания в мире колеблется от 1% до 4%. Женщины подвержены ГС/АИ в 3 раза чаще, чем мужчины [2, 3].
Долгое время процесс описывался в виде триады: конглобатные акне и инверсные акне, гидраденит и подрывающий фолликулит или перифолликулит головы [4]. И только в 1975 г. был описан четвертый компонент — пилонидальная киста [1]. Все проявления на коже, несмотря на разную локализацию, характеризуются общим патогенезом и сходными гистопатологическими изменениями, в основе которых лежит фолликулярная гиперкератинизация.
Этиология и патогенез ГС/АИ на сегодняшний день до конца не изучены, поэтому современная медицина не способна представить универсальный протокол лечения таких пациентов.
В основе патогенеза заболевания лежит окклюзия волосяных фолликулов, которая в 30–40% случаев обусловлена генетической предрасположенностью к акне [5], гиперкератинизацией и образованием лимфогистиоцитарного воспаления с гранулематозной реакцией. Только в небольшой части случаев (в 4 из 12) наблюдалось воспаление в апокриновых железах, сопровождавшееся воспалением вокруг эккринных желез, волосяных фолликулов и структур, выстланных эпителием. Эти наблюдения свидетельствуют о том, что структуры, выстланные плоским эпителием, вероятно, представляют собой аномальные расширенные волосяные фолликулы, являются более постоянной диагностической особенностью при гнойном гидрадените, чем при воспалении апокриновых желез, которое, по-видимому, является вторичным явлением [6]. Фолликулярная окклюзия приводит к растяжению и разрыву фолликулов с выходом содержимого в окружающую дерму, что способствует миграции нейтрофилов и лимфоцитов в очаг воспаления [7–9], формируя воспалительный инфильтрат с последующим образованием рубцовой ткани [10].
Общепризнанным является тот факт, что бактерии не влияют на развитие заболевания, но вторичная бактериальная инфекция поддерживает воспалительный процесс и способствует рецидивированию [11].
Гистологическая картина при ГС/АИ не имеет специфических критериев. Поэтому в современной дерматологии до сих пор диагноз устанавливается на основании клинической картины заболевания. При патоморфологическом исследовании на ранних стадиях обнаруживают фолликулярную окклюзию с наличием или отсутствием воспаления, фолликулярные кисты, уменьшение объема сальной железы, гиперплазию, нейтрофильные абсцессы [6]. В тяжелых случаях обнаруживают В-клетки и плазматические клетки в псевдофолликулах, абсцессах и пазухах, окруженные хроническим воспалительным инфильтратом, с наличием гистиоцитов и гигантских клеток, а также большое количество грануляционной ткани [12].
Локализации процесса, путаница в терминологии и отсутствие специфических гистологических изменений часто являются причинами неправильной диагностики — дерматологи ориентируются в описании клинической картины только на проявления воспалительного процесса, упуская из виду распространенность высыпаний и формирование абсцессов. Результатом этого являются ошибочные диагнозы: гидраденит или вульгарные акне, что влечет за собой отсутствие терапевтического успеха.
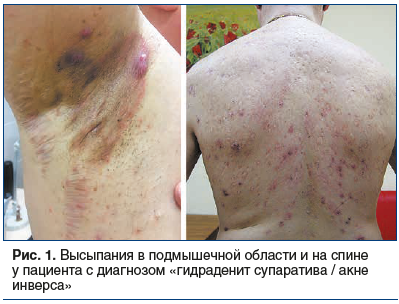
Дебютирует ГС/АИ, как правило, после полового созревания с небольших красных плотных папул или, реже, пустул, которые, постепенно увеличиваясь в размерах, сливаются с окружающими тканями. Постепенно дерматоз трансформируется в хронический воспалительный рецидивирующий процесс с наличием псевдокомедонов, болезненных папул, расположенных в глубоких слоях кожи, с тенденцией к формированию абсцессов, сливающихся в синусы, и с разрешением процесса в рубцы [2–5]. Несомненно, внешне процесс может напоминать вульгарные акне или гидраденит (в зависимости от локализации высыпаний), особенно в самом начале развития, а с учетом возраста пациентов в большинстве случаев такие высыпания определяются как юношеские акне.
Однако высыпания при ГС/АИ связаны с апокриновыми потовыми железами и кроме лица имеют другие типичные места локализации — это преимущественно подмышечная, паховая и аногенитальная области. Также отмечены случаи ГС/АИ в области живота. У женщин заболевание часто развивается в грудной складке, в области промежности, у мужчин — в анальной зоне [8, 13]. Внимание дерматолога может привлечь также то, что содержимое элементов не эвакуируется, а остается внутридермально в виде округлых подкожных образований [14, 15] (рис. 1, 2).
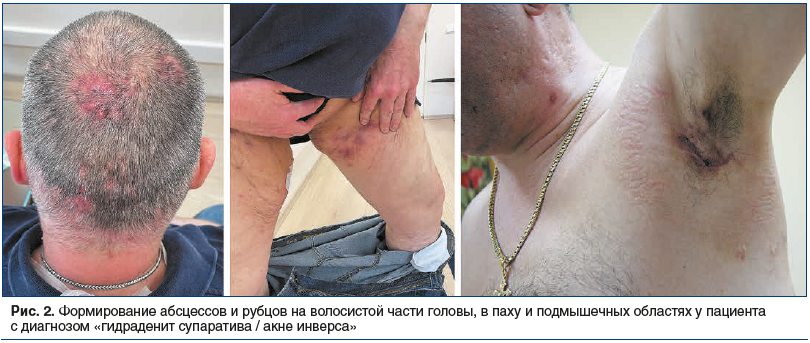
По мере нарастания кожной симптоматики присоединяются общие симптомы. Пациенты жалуются на боль, жжение, обильное потоотделение, слабость, в тяжелых случаях — на невозможность ходить или сидеть, а также на неприятный запах. Такое состояние может продолжаться в течение длительного времени, и, что важно отметить, отсутствует положительная реакция на терапию антибиотиками [5, 16, 17].
Диагностика ГС/АИ
Критерии диагностики заболевания утверждены на 2-м Международном симпозиуме по ГС/АИ (Second International Hidradenitis suppurativa research symposium, 2009). Для постановки диагноза необходимо наличие трех обязательных критериев [18]:
-
Поражения: в начальных стадиях заболевания — глубокие болезненные узлы, абсцессы, дренирующие синусы, рубцы. Вторичные поражения — открытые комедоны по типу «надгробий».
-
Локализация: подмышечная, паховая, анальная области, область промежности, область живота.
-
Хроническое течение с наличием рецидивов.
Проводя дифференциальную диагностику, в первую очередь следует обратить внимание на нетипичные для вульгарных акне места локализации (см. диагностические критерии). Подкрепляет диагноз ГС/АИ отсутствие положительной динамики в ответ на антибиотикотерапию.
При отсутствии высыпаний на лице и дифференциальной диагностике с гидраденитом внимание дерматолога привлечет наличие дренирующих синусов, рубцов, открытых комедонов по типу «надгробий» и локализация не только в подмышечных областях. Немаловажным также является наличие постоянных рецидивов при ГС/АИ.
При дифференциальной диагностике с фурункулом, карбункулом, фолликулярной пиодермией необходимо учитывать характер высыпаний. При ГС/АИ кроме воспалительных элементов, которые, как правило, без хирургического вмешательства самостоятельно не вскрываются, еще присутствуют и макрокомедоны. Дополнительным ориентиром является симметричность высыпаний, характерная для ГС/АИ.
Лечение ГС/АИ
Лечение ГС/АИ требует комплексного подхода, который должен включать немедикаментозные и медикаментозные пути решения проблемы. Необходимо обращать внимание на образ жизни пациента и вредные привычки. Очень большую роль в достижении успеха терапии играют контроль массы тела и отказ от курения.
В.С. Melnik, С.С. Zouboulis опубликовали результаты наблюдения, свидетельствующие о том, что у женщин, страдающих ГС/АИ, отмечается высокая чувствительность к андрогенам [19], поэтому препараты, содержащие андрогены, необходимо исключать из терапии [20]. Внимание пациентов необходимо акцентировать на трех важных фактах. Во-первых, доказано, что на образование фолликулярной окклюзии влияет никотин, вследствие этого у курильщиков заболевание протекает в более тяжелой форме [21]. Во-вторых, ухудшению процесса способствует механическая травматизация высыпаний самими пациентами с последующим более глубоким инфицированием [22]. В-третьих, установлена прямая корреляция между метаболическим синдромом и тяжестью течения ГС/АИ, поэтому всем больным с лишним весом рекомендуется его снижать [21]. Согласно систематическому обзору научной группы альянса ГС/АИ снижение веса (у пациентов с индексом массы тела более 30 кг/м2) с высоким уровнем доказательности способствует уменьшению тяжести заболевания в долгосрочной перспективе [22]. В когортном исследовании, проведенном в Дании, установлено, что возвращение к нормальному весу до полового созревания снижает риск возникновения заболевания до уровня заболеваемости у детей без избыточного веса [22].
Из-за частого сочетания ГС/АИ с болезнью Крона и/или локализации в перианальной области пациента необходимо обследовать у гастроэнтеролога и проктолога [14].
При выборе тактики лечения ГС/АИ практикующим врачам рекомендуется ориентироваться на классификацию этого заболевания, разработанную H.J. Hurley в 1989 г. [9, 19]. Существуют и другие классификации (Sartorius score, the Hidradenitis Suppurativa Severity Index, Physician Global Assessment), но они в основном применяются в клинических научных исследованиях [9].
Согласно классификации Hurley выделяют три стадии заболевания:
I — наличие одного или нескольких изолированных абсцессов без рубцов или пазух.
II — наличие рецидивирующих абсцессов, локализующихся более чем в одной анатомической области. Формирование синусовых ходов.
III — наличие обширных абсцессов с множеством взаимосвязанных пазух, приводящих к формированию рубцов.
Тактика терапии зависит от стадии патологического процесса. При I–II стадии вполне возможно обойтись наружными средствами, в то время как III стадия заболевания рассматривается как показание к биологической терапии [23–25].
Согласно данным современной литературы препаратами первой линии являются антибиотики и стероидные средства на фоне хирургического дренирования гнойных полостей. Согласно рекомендациям European S1 guideline for the treatment of hidradenitis suppurativa/acne inverse, клиндамицин — единственный антибиотик, рекомендуемый для местного применения [9]. У пациентов с I–II стадией ГС/АИ по Херли возможно местное применение клиндамицина 1%, особенно при отсутствии абсцессов [9]. При наличии нескольких поражений и частых обострений может быть рассмотрена терапевтическая группа системных тетрациклинов [26]. Альтернативным вариантом может быть тройной режим приема рифампицина (10 мг/кг 1 р/сут), моксифлоксацина (400 мг 1 р/сут) и метронидазола (500 мг 3 р/сут) в течение 12 нед. с прекращением приема метронидазола через 6 нед. Пациентам со II–III стадией ГС/АИ, у которых имеется несколько активных поражений, следует сразу назначать системный клиндамицин и рифампицин (300 мг 2 р/сут) [27–29]. Антибактериальные препараты оказывают противовоспалительное действие и подавляют рост вторичной бактериальной флоры. Большое значение в терапии имеют высокая дозировка и продолжительная длительность приема препаратов. Схемы лечения системными тетрациклинами и клиндамицином, рекомендуемые при гнойничковых заболеваниях кожи, не дают результата при ГС/АИ, что служит дополнительным дифференциально-диагностическим признаком.
Хорошие результаты наблюдаются при применении в качестве эксфолианта резорцинола 15% 2 р/сут. Его используют как в качестве монотерапии, так и совместно с другими средствами, в зависимости от степени и глубины поражения. Резорцинол обладает кератолитическим, антисептическим действием, а также подавляет зуд [30].
Отдельные авторы предлагают совместное использование метронидазола 400 мг 2 р/сут и клиндамицина 600 мг 3 р/сут внутривенно в течение 2 нед. [31].
Кортикостероидные препараты также являются неотъемлемой частью лечения этого сложного заболевания. Препараты данной группы назначают с целью уменьшения выраженности воспаления. Для системной терапии используется введение триамценолона ацетонида непосредственно в образования [32] или прием внутрь гидрокортизона, дексаметазона, преднизолона. Длительность терапии составляет 7–14 дней [33].
Поскольку имеются наблюдения, подтверждающие взаимосвязь ГС/АИ и повышенной чувствительности к андрогенам [19], оправдано назначение антиандрогенов (ципротерон ацетат, эстрогены, финастерид) [34, 35].
В отношении других препаратов, в частности цитостатиков, имеется меньше публикаций, но в ряде случаев отмечена успешная терапия циклоспорином [36–38].
В современной литературе нет единого взгляда на применение метотрексата в терапии ГС/АИ. В раннем исследовании, проведенном в 2002 г. G.B. Jemec [39], метотрексат использовался в качестве монотерапии на период от 6 нед. до 6 мес., автор отметил ограниченную эффективность препарата при данной патологии. Однако, несмотря на отсутствие эффекта от метотрексата, некоторые исследователи утверждают, что его добавление в низких дозах к терапии биологическими препаратами необходимо с целью предотвращения нейтрализации аутоантител, что предупреждает развитие вторичной резистентности к биологической терапии [9, 40]. Оправдано назначение метотрексата также и при наличии у пациентов с ГС/АИ сопутствующих ревматологических заболеваний [9]. Более поздние исследования, проведенные P. Kozub et al. [41], продемонстрировали, что метотрексат неэффективен ни в качестве монотерапии, ни в сочетании с инфликсимабом. Авторы доказали, что метотрексат не увеличивает клиническую эффективность инфликсимаба [41].
Противоречивость данных об эффективности терапии метотрексатом обсуждается до сих пор. Патогенетически механизм развития заболевания связан с дисфункцией Т-регуляторных клеток и Т-хелперов 17-го типа, что приводит к повышению уровня IL-17А и IL-6, запуская тем самым каскад воспалительных реакций. В данном случае терапевтическое действие метотрексата связано с подавлением Т-хелперов 17-го типа за счет изменения уровней активности и скорости созревания дендритных клеток и Т-лимфоцитов [42]. Однако в литературе нет достаточного количества примеров, когда терапия метотрексатом улучшала течение ГС/АИ [43].
Изотретиноин при данном заболевании может быть неэффективен, поскольку в основе патогенеза заболевания лежит окклюзия волосяных фолликулов с гиперкератинизацией и последующее иммунное воспаление с вовлечением в процесс CD3/CD8 и естественных киллеров (NK-клеток). Была обнаружена отрицательная корреляция между длительностью течения заболевания и процентом NK-клеток, также отмечено увеличение содержания фактора некроза опухоли α и IL-6 [7]. Современные исследования также подтверждают низкую эффективность изотретиноина: около 60% пациентов не реагировали на лечение, а у 13% наблюдались рецидивы [44, 45].
Однако более современный препарат из класса ретиноидов — алитретиноин в дозе 10 мг/сут в течение 2 мес. с последующей поддерживающей дозой 20 мг, согласно данным [46], вызвал стойкую ремиссию у большинства больных. Данное противоречие можно объяснить тем, что алитретиноин (9-цис-агонист ретиноевой и пан-ретиноевой кислот) — новый системный препарат из группы ретиноидов, обладающий противоопухолевой активностью.
Несмотря на многочисленные работы, представленные в мировой литературе, лечение ГС/АИ является очень сложной задачей, ремиссия непродолжительная, составляет менее 1 года или полностью отсутствует, последующие рецидивы приводят к инвалидизации пациента.
Хирургическое вмешательство (либо простое иссечение поврежденных тканей, либо полное местное иссечение с последующей пересадкой кожи) является важной частью ведения таких пациентов и применяется при II–III стадиях заболевания. Важно не только вскрытие воспалительных элементов, но и их дренирование и иссечение дивертикул, как правило, располагающихся глубже основного воспалительного очага [9, 47]. Пациенты с ГС/АИ I–II стадии не нуждаются в хирургических вмешательствах [9].
Встречаются практические рекомендации по применению лазеров при ГС/АИ: carbon dioxide laser [48], NG:Yag laser [49], IPL [50], но наблюдений еще недостаточно, чтобы делать окончательные выводы.
Что касается биологической терапии, то анти-TNFα моноклональные антитела — инфликсимаб и адалимумаб показаны пациентам с III стадией ГС/АИ [9].
Впервые применили адалимумаб у 3 пациентов А.А. Navarini, R.M. Trueb в 2010 г. Все пациенты ранее получали изотретиноин в комбинации с антибиотиком, без эффекта. Применение адалимумаба позволило устранить клинические симптомы и субъективные ощущения. Однако после отмены биологической терапии клинические проявления начали возвращаться, и пациентам назначили повторный курс биологической терапии [51].
В противовес этому исследованию, эффективность адалимумаба доказана в проспективных двойных слепых плацебо-контролируемых исследованиях с участием более 800 больных, что позволило в дальнейшем включить ГС/АИ в перечень показаний для терапии адалимумабом [52, 53].
Адалимумаб следует рассматривать в качестве биологического агента первого выбора при ГС средней/тяжелой степени после неуспешного применения традиционных методов лечения, за которыми следуют инфликсимаб, устекинумаб и анакинра в качестве препаратов второй и третьей линий терапии соответственно [54].
В литературе имеются доказательства эффективности инфликсимаба у 30-летнего пациента с предшествующим неэффективным курсом терапии рифампицином 300 мг/сут, преднизолоном 50 мг/сут и изотретиноином 30 мг/сут. У данного пациента уже после первого введения инфликсимаба наблюдалось значительное уменьшение выраженности воспалительного процесса и снижение болевых ощущений [23]. Положительные результаты также продемонстрированы при лечении другими биологическими препаратами — этанерцептом и устекинумабом [24, 25]. Таким образом, можно сделать выводы, что биологические препараты демонстрируют эффективность у пациентов с ГС/АИ, и поиски оптимальной биологической терапии продолжаются.
Заключение
Гидраденит супаратива / акне инверса до сих пор является загадкой дерматологии. Несмотря на многочисленные исследования в этой области, остаются неясными многие вопросы. Среди них — важный вопрос тактики терапии пациентов с уже сформированной резистентностью к антибиотикам и противопоказаниями к адалимумабу или другим биологическим методам лечения.
Появляются новые теории, которые принципиально меняют концепцию патогенеза, о котором шла речь выше. Два исследования продемонстрировали наличие биопленки в очагах, в основном при тяжелых формах, что объясняет постоянные рецидивы в предыдущих рубцах. Эти данные свидетельствуют о патогенной роли изолированной флоры, вводя новую концепцию болезни — «хозяин — микробиом». Вместо аутовоспалительного процесса с неясным механизмом ГС/АИ можно рассматривать как аутоинфекционный из-за кожной иммунной дисрегуляции. Эта дисрегуляция позволяет аномальной бактериальной инфекции пролиферировать на фоне неадекватной гипервоспалительной реакции вместо эвакуации бактерий из дермы [51].
Эта теория может открыть возможности для разработки новых методов лечения ГС/АИ. Остается еще много вопросов, на которые нужно ответить. В частности, способствует ли ранний микробный сдвиг окклюзии фолликулов? Может ли потеря «микробного щита» быть частично восстановлена посредством иммуномодуляции или трансплантации микробиоты, как это исследовалось при воспалительных заболеваниях кишечника? Экспериментальные исследования в этом направлении уже ведутся, что позволит в скором времени получить более определенные ответы.
Ресурсы по теме
Гнойный гидраденит – это хронический, приводящий к рубцеванию акнеподобный воспалительный процесс, который возникает в области подмышечных ямок, паха, вокруг сосков и ануса. Диагноз ставится при осмотре. Лечение зависит от стадии.
В настоящее время гнойный гидраденит считается хроническим воспалительным состоянием волосяного фолликула и связанных с ним структур. Фолликулярное воспаление и последующая окклюзия приводят к разрыву фолликула и развитию абсцессов, свищевых ходов и рубцов.
Формируются отечные болезненные инфильтраты, напоминающие абсцессы кожи. Эти повреждения часто стерильные. Для хронически протекающего заболевания характерны боль, флуктуация, наличие выделений из очагов поражения и формирование синусовых ходов. В хронических случаях бактериальная инфекция может возникнуть в глубоких нарывах и свищевых ходах. При хроническом поражении кожи подмышечной области сливающиеся воспаленные узелки образуют пальпируемые шнуровидные скопления. Заболевание может приводить к нетрудоспособности из-за боли и неприятного запаха.
-
Клиническая оценка
Диагностика гнойного гидраденита проводится путем обследования. Бактериальные соскобы для исследования должны быть взяты из глубоких гнойников и свищевых ходов у пациентов с хроническим заболеванием, но часто при этом патогенов не обнаруживают. Система определения стадии заболевания по Херли описывает тяжесть заболевания:
-
I стадия: Формирование гнойника, одного или нескольких, без свищевых ходов или рубцов
-
II стадия: Один или несколько, далеко расположенных друг от друга, рецидивирующих гнойников с образованием свищевых ходов или рубцов
-
III стадия: Диффузное или около диффузное разветвление или несколько соединенных между собой свищевых ходов и гнойников по всей зоне поражения
-
I стадия: Клиндамицин местного применения, вводимые внутрь пораженных тканей кортикостероиды и пероральные антибиотики
-
II стадия: более длительные курсы пероральных антибиотиков и иногда дренаж, иссечение или хирургическое вскрывание.
-
III стадия: Инфликсимаб или адалимумаб, часто обширное хирургическое вмешательство, коррекция или пересадка
Цели лечения гнойного гидраденита – предотвращение появления новых поражений, уменьшение воспаления и удаление свищевых ходов.
Для 1-й стадии по Херли типичное лечение включает местное использование раствора клиндамицина 1% 2 раза/день; крем с резорцином 15% наружно 1 раз/день; глюконат цинка перорально (90 мг 1 раз/день); кортикостероиды внутрь поражения (например, от 0,1-0,5 мл раствора триамцинолона ацетонида в концентрации 5-10 мг/мл раз в мес) и короткие курсы пероральных антибиотиков (например, от 7 до 10 дней). Применяют тетрациклин (500 мг 2 раза/день), доксициклин (100–200 мг 1 раз/день), миноциклин (100 мг 1 раз/день) или эритромицин (250–500 мг 4 раза/день) до устранения повреждений. Типичная схема лечения может включать в себя средство для наружного применения (например, подобранного в соответствии с чувствительностью кожи пациента) и пероральный антибиотик; тем не менее, все способы лечения можно использовать как вместе, так и по отдельности. Кожу промывают бензоилпероксидом.
Для II стадии по Херли лечение характеризуется более длительным (например, от 2 до 3 месяцев) курсом тех же пероральных антибиотиков, применяемых для лечения при I стадии болезни; если этого недостаточно, можно добавить клиндамицин в дозировке 300 мг внутрь 2 раза/день и/или рифампицин 600 мг перорально 1 раз/день. Добавление антиандрогенов (например, эстроген перорально или комбинированные пероральные контрацептивы, спиронолактон, ципротерон ацетат [не доступен в США], финастерид или их комбинации) может быть полезным для женщин. Разрез и дренаж могут уменьшить боль абсцесса, но этого недостаточно для контроля заболевания (в отличие от обычных кожных абсцессов). При острых воспалительных поражениях, которые являются не слишком глубокими, предпочтительной является санация раны с помощью панча (т.е. иссечение омертвевших тканей с помощью 5-7 мм панча, с последующим удалением этих тканей, кюретажем или промыванием). Свищевые ходы должны быть иссечены или хирургически вскрыты. Пациенты, у которых глубокие повреждения, должны быть осмотренные пластическим хирургом для рассмотрения хирургического вмешательства и пересадки.
Для III стадии заболевания по Харли медицинская и хирургическая терапии должны быть более агрессивными. Доказательства эффективности в снижении воспаления сильнее в пользу инфликсимаба (5 мг/кг внутривенно в 0-ю, 2-ю и 6-ю недели). В качестве альтернативы, можно применять адалимумаб. Начальная доза составляет 160 мг подкожно в первый день (или разделить дозу на 2 дня подряд), с последующим введением на 15-й день 80 мг подкожно и, начиная с 29 дня, поддерживающая доза по 40 мг подкожно 1 раз в неделю. Использование пероральных ретиноидов (изотретиноин 0,25-0,4 мг/кг 2 раза/день, в течение 4-6 месяцев или ацитретин 0,6 мг/кг 1 раз/день, в течение 9-12 месяцев) было эффективным для некоторых пациентов. Если заболевание сохраняется, то часто требуется масштабное хирургическое вмешательство с пластикой или пересадкой поврежденной области. Аблятивная лазерная коагуляция (CO2 или эрбиевый лазер на иттрий-алюминиевом гранате) является альтернативой хирургическому лечению. Лазерная эпиляция также используется с некоторым успехом.
Рекомендуемые дополнительные меры для всех пациентов с гнойным гидраденитом включают соблюдение надлежащей гигиены кожи, снижения травмирования, обеспечения психологической поддержки и, возможно, избегание диет с высоким гликемическим индексом.
-
Повреждения, как правило, стерильны, за исключением глубоких гнойников и свищевых ходов во время хронического заболевания.
-
Гнойный гидраденит может приводить к нетрудоспособности.
-
Лечить гнойный гидраденит необходимо в соответствии с системой определения стадии заболевания по Херли.
-
Дополнительные меры включают поддержание хорошей гигиены кожи, минимизацию травм, оказание психологической поддержки и, возможно, отказ от высокоуглеводной диеты.
ПРИМЕЧАНИЕ:
Это — Профессиональная версия.
ПОЛЬЗОВАТЕЛИ:
Просмотреть пользовательскую версию

Авторское право © 2023 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.

Барлев Д., кафедра дерматологии, Университет Цинциннати, США; Эйзен Д.Б., отделение дерматологии, Калифорнийский университет в Дэвисе, США ; Алихан А., кафедра дерматологии, Университет Цинциннати, США
Введение
Гнойный гидраденит (ГГ) — это хроническое заболевание потовых желез, которое часто приводит к значительному ухудшению качества жизни больных, увеличению числа обращений за экстренной медицинской помощью и госпитализаций. Наиболее часто ГГ встречается у половозрелых женщин, поражая подмышечные, паховые и аногенитальные области. Итогом воспалительного процесса при ГГ может быть образование свищевых ходов и грубое рубцевание, что повсеместно сопровождается трудностями терапии и невозможностью достижения полной ремиссии. Можно надеяться, что современные научные исследования и новые изыскания о патогенезе и лечении ГГ позволят контролировать данное заболевание у пациентов.
Эпидемиология
Распространённость6 ГГ остается до сих пор предметом споров, встречаемость колеблется в среднем от 0.052 до 1%, по большей части отражая различия в методах учета и охвате населения. Недавнее популяционное всеобщее годовое стандартизированное по возрасту и полу исследование в округе Олмстед в Миннесоте подтвердило тот факт, что ГГ — редко встречаемая патология, выявив уровень заболеваемости в количестве случаев на 100 000 населения. Заболевание чаще выявлялось у лиц женского пола в возрасте 18-44 лет. До настоящего времени нет доказательств о расовой предрасположенности к ГГ, хотя отдельные факты указывают на то, что заболевание может более часто возникать у лиц определенной расы.
Обзор более 846 случаев ГГ в Германии выявил, что такие факторы как мужской пол, длительный анамнез заболевания, ожирение, курение и травматизация кожи в подмышечной, перианальной и околомаммарной областях, являются усугубляющими течение процесса.
Около 1/3 пациентов с ГГ отмечают отягощенную наследственность по данному заболеванию, при чем имеет место аутосомно-доминантный тип наследования. Также замечена четкая связь между ГГ и болезнью Крона: в последнем исследовании с участием 1093 пациентов с воспалительным заболеванием кишечника 23% испытуемых отметили у себя симптомы ГГ. Другими сопутствующими нозологиями при ГГ могут быть: конглобатные угри, фолликулит абсцедирующий подрывающий и перифолликулит Гоффмана, эпителиальный копчиковый ход, спондилоартрит, гангренозная пиодермия и синдром SAPHO (Synovitis — синовит, Acne – акне, Pustulosis – пустулез, Hyperostosis –гиперостоз, Osteitis — остеит). Гипертония, метаболический синдром, депрессия, тревожность, ожирение и никотиновая зависимость также являются частыми спутниками при ГГ. Более того, ожирение и курение не только усугубляют тяжесть ГГ, но и коррелируют с более низким уровнем частоты ремиссий при данном заболевании.
Патогенез
Патогенез ГГ довольно сложный. Если ранее предполагалось, что ГГ представляет собой воспаление апокриновых потовых желез, то на сегодняшний день в развитии заболевания доказана ведущая роль окклюзии фолликулов. Независимо от того, являются ли иммунные нарушения причиной этого или следствием, закупорке фолликулов отводится решающая роль в патогенезе ГГ. Тем не менее оба фактора являются патогенетически важными для развития патологического процесса.
Следует отметить, что последние исследования многочисленных семейных случаев ГГ доказывают роль мутаций гена гамма-секретазы — протеолитического фермента, который расщепляет внутримембранные рецепторы и регулирует кератинизацию фолликулов, что объясняет роль фолликулярной окклюзии в патогенезе заболевания.
Нарушения врожденного и приобретенного иммуннитета при ГГ обуславливают уменьшение экспрессии антимикробных пептидов эпителиального происхождения (таких как рибонуклеаза, человеческий бета-дефензин-3 и Toll-подобный рецептор-4), вследствие чего происходит усиленный воспалительный ответ, а также чрезмерная экспрессия провоспалительных цитокинов (например, интерлейкин (IL)-1, IL-10, фактор некроза опухолей (ФНО) — альфа, IL-17, IL-22).
Кроме того имеют место другие факторы, играющие роль в патогенезе ГГ, такие как: бактериальные биопленки, неправильная секреция апокриновых потовых желез, патологические разрастания эпидермиса, ведущие к формированию свищевых ходов, и недостаточное количество сальных желез. В настоящее время не доказана роль гиперандрогении и дефицита витамина Д при ГГ, хотя замечено, что эти факторы могут влиять на данный патологический процесс.
Клиника
ГГ характеризуется появлением рецидивирующих воспалительных узлов, кист, абсцессов и свищевых ходов в местах локализации апокриновых потовых желез, таких как подмышечная область, пах, перианальная область и/или молочные железы. Элементы часто сопровождаются непрерывным отделяемым. Клиническая картина ГГ очень разнообразна, в зависимости от степени поражения кожи, распространенности процесса, наличия кожных осложнений (образование свищей, отёк тканей, обусловленный лимфостазом, слоновость мошонки), внекожных проявлений (артрит, паренхиматозный кератит) и сопутствующих системных реакций (например, лихорадка и недомогание).
ГГ аногенитальной области трудно дифференцировать от Болезни Крона, особенно в указанной взаимосвязи между этими заболеваниями, учитывая схожую клиническую картину в виде свищей и фистул и аналогичные гистологические характеристики гранулематозного воспаления.
Так как при ГГ имеется хронический воспалительный процесс, то в клинической картине могут быть признаки анемии и гипопротеинемии. Проявления ГГ могут распространяться на прямую кишку, влагалище, уретру и/или мочевой пузырь с образованием свищей. У пациентов с ГГ описаны случаи реактивного артрита и синдрома SAPHO. Помимо этого в очагах хронического воспаления может развиваться плоскоклеточный рак кожи, что служит неблагоприятным прогнозом заболевания.
Стадии ГГ описаны в классификации Херли (Таблица 1) и более новой схеме Сарториуса (Таблица 2). Классификация Херли более клинически удобна, в то время как система Сарториуса используется в основном в исследовательских целях.
Были предприняты поиски биологичксих маркеров, которые помогли бы диагностировать и/или установить зависимость тяжести ГГ. Аналогично клиническим стадиям Сарториуса данные тесты главным образом используются для исследовательских целей, так как диагноз нетрудно устанавливается посредством клинических и топографических данных.
Таблица 1. Стадии ГГ по Херли
| Стадии |
Клиника |
| I |
Формирование единичных или множественных абсцессов без свищевых ходов и рубцевания |
| II |
Единичные или множественные изолированные рецидивирующие абсцессы, сопровождающиеся образованием свищей и рубцов |
| III |
Множественные сообщающиеся свищи и абсцессы на всей площади поражения |
Таблица 2. Шкала оценки ГГ по Сарториусу основывается на подсчете пораженных участков, узлов и свищевых ходов
|
Оценочная шкала ГГ Сарториуса |
|
|
Пораженная анатомическая область (3 балла за каждую локализацию) |
Подмышечная область |
| Количество и тяжесть очагов поражения |
2 балла за каждый узел |
| Наибольшее расстояние между двумя очагами |
Менее 5 см (2 балла) |
| Очаги отчетливо разграничены участками здоровой кожи в каждой области |
Да (0 баллов) |
Лечение
Лечение ГГ варьирует от тяжести процесса, при чем многие методы далеки от научно-доказательной базы. Обычно используется местная и системная терапия часто в комплексе с хирургическим лечением. Ниже в таблице 3 авторами приведена схема лечения ГГ. Нефармакологические средства терапии включают: исключение плотно- прилегающей одежды, покой, уменьшение курения, коррекция сопутствующей депрессии и тревожных расстройств, специализированные группы поддержки и снижение веса.
Болевые ощущения, характерные для ГГ, должны быть купированы у всех пациентов. Принимая во внимание то факт, что ГГ имееет хроническое течение, проблема опиоидной зависимости занимает важное место в терапии. Нестероидные противовоспалительные препараты (НПВП) и ацетаминофен — лекарственные средства первого выбора в терапии боли, в то время как прегабалин, габапентин, селективные ингибиторы обратного захвата серотонина (СИОЗС) и селективные ингибиторы обратного захвата серотонина-норэпинефрина (СИОЗСН) — вторая линия терапии.
Антибиотики
Местные и системные антибактериальные препараты широко используются в лечении ГГ. Рандомизированное контролируемое исследование 30 пациентов, пролеченных в течение 3-х месяцев 1% раствором клиндамицина местно, показало значительное улучшение течения процесса по сравнению с группой плацебо. В другом рандомизированном исследовании Jemec и др. доказали, что эффект применения топического клиндамицина не уступает 3-х месячному системному приему тетрациклина в дозе 500 мг дважды в день.
Тетрациклины обычно используются при легкой и средней степени тяжести ГГ, хотя опубликованные данные (экспериментального характера) относительно их эффективности довольно малочисленны. Обычно при ГГ мы назначаем 100 мг доксициклина один-два раза в сутки с постепенным снижением дозы в зависимости от эффективности терапии. Два проспективных исследования, которые изучали комбинированное применение системного рифампицина и клиндамицина, свидетельствуют о положительных результатах данной комбинации. Однако, большей части пациентов пришлось отменить лечение из-за тяжелых побочных эффектов со стороны желудочно-кишечного тракта.
Таблица 3. Перечень лечебных мер ГГ согласно классификации Херли
| Лечение ГГ по стадиям Херли | ||
| I-II стадии по Херли | Местное, иньекционное и внутриочаговое лечение |
· Местные антибиотики (например, 1% клиндамицин) • Внутриочаговое введение кортикостероидов • Резорцин местно6 • Ботулинотерапия |
| Пероральная терапия |
· Антибактериальные препараты (например, тетрациклин, рифампицин плюс клиндамицин, дапсон) •Гормональная терапия (например, комбинированные оральные контрацептивы, финастерид, спиронолактон) • Метформин |
|
| Хирургические физиотерапевтические методы |
· Минимально инвазивная хирургия • Лазерная терапия (например, Nd:YAG, СО2) •Криотерапия/криоинсуффляция • Фотодинамическая терапия |
|
| II-III стадии по Херли | Включает в себя методы I-II стадий по Херли |
· Более широкий доступ в хирургическом лечении (например, широкое радикальное иссечение) • Системные ретиноиды (ацитретин) • Системные иммунодепрессанты •Биологические препараты (например, адалимумаб, инфликсимаб, устекинумаб, анакинра) |
| Все стадии |
• Обезболивание (местное и системное) • Уменьшение курения • Восполнение дефицита цинка • Антимикробное мыло (например, с хлоргексидином, бензоил пероксидом) |
Дапсон считается относительно малоэффективным препаратам для лечения ГГ. В результате лечения дапсоном 24 пациентов с ГГ улучшение отмечалось только у 9 (38%), в то время как 15 больных (62%) не отметили положительного эффекта.
Несмотря на недостаточность научно-доказательной базы об эффективности таких антимикробных агентов как хлоргексидин и бензоил пероксид, они часто назначаются специалистами для ежедневного ухода за пораженной кожей.
Гормональная терапия
Для пациенток с гормональными нарушениями, которые не отвечают на традиционные методы терапии, допускается назначение таких антиандрогенов как спиронолактон, ципротерона ацетат и комбинированных оральных контрацептивов. Рандомизированное контролируемое исследование 18 женщин, получающих в течение 6 месяцев ежедневно комбинацию 50 мг этинилэстрадиола/500 мг норгестрела или 50 мг этинилэстрадиола/50 мг ципротерона ацетата, продемонстрировало улучшение процесса у 5 пациенток, отсутствие динамики у 4 и ухудшение у 2.
В качестве другого метода гормонального лечения ГГ рекомендуется финастерид. Группа из 3 пациентов детского возраста, получающих финастерид для лечения ГГ, отметила значительное уменьшение воспаления и тяжести процесса. Аналогичное исследование 7 пациентов с ГГ выявило полное разрешение процесса у 3 больных и видимое облегчение течения заболевания у оставшихся 4.
Биологические препараты
Ингибиторы фактора некроза опухоли альфа (ФНО-α) 6 Биологические препараты в последнее время все чаще используются для лечения средних и тяжелых случаев ГГ (Таблица 3). Среди ингибиторов ФНО-α наиболее изученным считается инфликсимаб. В ходе рандомизированного двойного слепого плацебо — контролируемого исследования 38 пациентам была проведена терапия инфликсимабом в разовой дозе 5 мг/кг, иньекции выполнялись на 0, 2 и 6 неделях. В итоге 60% больных в группе инфликсимаба по сравнению с 5,6% пациентов группы, получающих плацебо, отметили положительные результаты терапии в виде уменьшения тяжести процесса на 25-50% согласно бальной системы оценки к 8 неделе лечения. Долгосрочное исследование 10 пациентов, получающих инфликсимаб далее каждые 8 недель после начального курса терапии, продемонстрировало отсутствие эффекта у 2 человек (20%) после применения 5 доз препарата и рецидив заболевания у 5 (50%) после 37 недельного периода лечения. В результате другого проспективного когортного исследования с более частой дозировкой препарата (каждые 4 недели) и последующим наблюдением в течение 60,3 месяцев 9 из 11 пациентов отметили значительное улучшение течения заболевания после окончания лечения. 2 пациента прервали курс на 12 и 19 месяцах терапии.
Адалимумаб в отличие от инфликсимаба пациенты принимают самостоятельно. В двойном слепом рандомизированном контролируемом исследовании 15 пациентов применяли адалимумаба подкожно (п/к) в первоначальной дозе 80 мг с последующим уменьшением до 40 мг один раз в две недели в течение 12 недель. К 12 неделе терапии было выявлено значительное уменьшение количества баллов тяжести ГГ по системе Сарториуса по сравнению с группой пациентов, применявших плацебо. Последнее крупное многоцентровое исследование продемонстрировало большую эффективность еженедельного применения адалимумаба по сравнению с приемом 2 раза в месяц.
Этанерцепт считается препаратом недостаточно эффективным при ГГ. В двойном слепом плацебо — контролируемом исследовании 20 пациентов принимали 50 мг этанерцепта 2 раза в неделю в течение 3 месяцев и далее в открытом исследовании препарат применялся в той же дозировке еще 3 месяца. В итоге никаких значительных отличий в результатах терапии между группами испытуемых выявлено не было.
Другие биологические препараты
Устекинумаб — антитела к интерлейкинам (ИЛ) человека ИЛ-12/ИЛ-23 — может быть эффективным при умеренных и тяжелых случаях ГГ. В небольшом проспективном исследовании трем пациентам устекинумаб назначался п/к в дозе 45 мг. Вторую инъекцию делали 4 недели спустя после первого применения, затем через 12 недель. К 6 месяцу испытаний у одного пациента наступила ремиссия процесса, второй отметил значительное улучшение течения заболевания, и последний не отметил никакого эффекта от терапии. 6 Последние данные о применении анакинры — антител к ИЛ-1 — у пяти пациентов выявили положительные результаты в виде уменьшения баллов тяжести ГГ по системе Сарториуса до 34.8. Отчет об эффективности применения аналога — канакинумаба — также продемонстрировал его положительное действие при ГГ.
Иммунодепрессанты
Циклоспорин используется при тяжелом течении ГГ, трудно поддающемся лечению другими методами, хотя исследования по этому вопросу очень ограничены и относятся к описаниям единичных клинических случаев. В двух сообщениях предлагается применять преднизон у пациентов с сопутствующей гангренозной пиодермией или артритом. Метотрексат также имеет недостаточный уровень доказательности при ГГ. На нашей практике внутриочаговое введение триамцинолона в дозе 5-10 мг/см³ довольно эффективно разрешало воспалительные узлы и кисты, а также препятствовало образованию рубцов. Очень важно убедиться в том, что иньекции не проводятся в места непосредственных гнойных очагов и абсцессов.
Ретиноиды
Изотретиноин продемонстрировал неоднозначные результаты в терапии ГГ. В ретроспективном анализе данных 68 пациентов только 48 из них закончили исследование (29.4% прекратили прием препарата из-за побочных эффектов и/или недостаточной эффективности). У 16 больных (23.5%) произошло разрешение очагов, 14 человек (20.6%) отметили явное улучшение течения процесса, у одиннадцати пациентов (16.2%) замечена положительная динамика и в 7 случаях (10.3%) отсутствовал эффект от проводимой терапии. Из 88 пациентов, наблюдаемых в ходе последнего ретроспективного исследования, только 14 (16.1%) заметили улучшение, у 67 больных (77%) лечение было неэффективным, а у 6 человек (6.9%) была отрицательная динамика. Многие специалисты считают, что ацитретин более эффективен чем изотретиноин при лечении ГГ, возможно на основании первоначальных положительных отзывов. Boer и соавт. в своем ретроспективном исследовании 12 пациентов выявили значительное улучшение или даже полное разрешение процесса у 10 больных и положительную динамику у 2. В то же время Mutasiak и соавт. в проспективном анализе 17 больных отметили менее благоприятные исходы терапии: у 8 пациентов было отмечено уменьшение индекса тяжести ГГ вдвое, однако 8 человек (47%) вынуждены были прекратить исследование из-за недостаточной эффективности или возникновения побочных эффектов. Алитретиноин имеет аналогичный фармакологический механизм как и ацитретин, но отличается более коротким периодом полувыведения и следовательно меньшим тератогенным риском. В одном из исследований 14 женщин детородного возраста, которые получали ежедневно 10 мг алитретиноина на протяжении 24 недель, было зарегистрировано значительное улучшение течения ГГ согласно оценочной системе Сарториуса и Дерматологического индекса качества жизни (ДИКЖ) в 78.5% случаев.
Хирургия
Хирургический методы лечения обычно применяются в лечении умеренных и тяжелых случаев ГГ. Вид хирургического вмешательства зависит от тяжести и локализации процесса и подразумевает 6использование минимального или широкого хирургического доступа. В исследовании 73 пациентов в течение 34 месяцев, перенесших хирургическую фенестрацию, при которой сначала хирургически удаляется поверхностно расположенная воспаленная ткань, а дно очага остается интактным для заживления вторичным натяжением, в 83% рециивов отмечено не было.
Исследование, сравнивающее частоту рецидивов ГГ после вскрытия и дренирования очагов (ограниченное вмешательство и широкий радикальный доступ) показало, что во всех случаях произошло рецидивирование процесса (медиана времени составила 3 месяца): 42.8% рецидивов произошли при ограниченном доступе (медиана времени была равна 11 месяцев), и 27% рецидивов — при широком радикальном доступе (медиана времени — 20 месяцев).
Alharabi с соавт. провели ретроспективный анализ 50 операций с широким хирургическим доступом у 32 пациентов. 26 больных (81.25%) не отметили рецидивов после лечения.
Лазеоро- и светотерапия
Для лечения ГГ рекомендуются различные виды лазеро- и светолечения, как в виде монотерапии так и в комбинации с хирургическими и/или системными методами. Неоднократно сообщалось об использовании фотодинамической терапии (ФДТ). С точки зрения эффективности терапии результаты лечения варьировались от хороших до посредственных. В целом, фактические данные относительно применения ФДТ при ГГ настолько ограничены и недостоверны, что на их основании невозможно сделать какие- либо убедительные выводы.
В ретроспективном исследовании 13 пациентов было изучено применение ванн с псораленом и УФА (ПУВА) терапии два раза в неделю. У 5 больных отмечено полное или почти полное разрешение патологического процесса, у 4 удалось добиться частичного регресса и 4 практически не ответили на терапию или результаты были минимальные. При этом среди 5 больных подтвержденные положительные результаты лечения были подкреплены как минимум 3-х месячным периодом последующего наблюдения за испытуемыми.
Лечение с помощью длинноимпульсного неодимового диодного лазера на алюмоиттриевом гранате (Nd:YAG лазер) продемонстрировало обнадеживающие результаты в одном из рандомизированных исследований. Mahmoud и соавт. отобрали 22 пациента, получающих ежемесячную Nd:YAG лазер терапию на протяжении 4 месяцев, и сообщили о положительной динамике кожного процесса в зоне лечения лазером на 72.7% по сравнению с 22.9% контрольной зоны. Последующее наблюдение 19 пациентов показало, что индекс распространенности и тяжести поражения во всех подвергнутых терапии анатомических зонах в течение дальнейшего 2-х месячного лечения уменьшился в среднем на 31.6%.
Также изучалась эффективность использование интенсивного импульсного излучения. Проспективное рандомизированное исследование эффективности лечения ГГ в подмышечной и паховой области, а также в области молочных желез заключалось в применении интенсивного импульсного излучения с одной пораженной стороны два раза в неделю в течение месяца. Результаты испытания подтвердили заметное уменьшение тяжести процесса по шкале оценки Сарториуса на 55% по сравнению с 10% контрольной, не подвергнутой терапии, области. Последующие 12 месяцев у больных отмечалось уменьшение тяжести течения заболевания согласно балльной системе Сарториуса на 55% по сравнению с 3% нелеченной стороны.
Последние несколько работ продемонстрировали довольно высокую эффективность абляции лазером на диоксиде углерода (CO2). В исследовании, проведенном Hazen и соавт., пациентам проводилась абляция очагов ГГ лазером на диоксиде углерода с последующей марсупиализацией, в итоге достигнуто разрешения патологического процесса. Заслуживает внимания то, что у 17 больных (28%) через 5 недель после лечения отмечалось возникновение постхирургических гипертрофических грануляций.
Другие методы лечения
Криоинсуффляция — недавно описанный метод модифицированной струйной криотерапии, осуществляемый введением жидкого азота непосредственно в каналы при ГГ. Результаты метода ограничены единичными случаями применения у пациентов.
Ботулинотерапия. Описан случай применения 50 единиц ботулинического токсина типа А для лечения ГГ средней степени тяжести (100 единиц ботулотоксина разводятся 4 мл 0.9% р-ра хлорида натрия), который вводился в кожу подмышечной зоны (на протяжении более 3 лет), в результате чего было достигнуто разрешение очагов после повторного введения (через 6 месяцев) с последующей ремиссией в течение года после завершения полного курса терапии.
Таблица 4. Анализ результатов исследований применения биологических препаратов для лечения ГГ.
| Биологические препараты | Автор и тип исследования | Количество пациентов | Дозировка/Частота введения | Длительность наблюден ия от начала терапии | Результат |
| Адалимумаб | Miller и соавт., рандомизиров анное двойное слепое контролируемое исследование | 15 | Адалимумаб 80 мг п/к первоначально, затем 40 мг п/к раз в две недели | 12 недель | Снижение индекса Сарториуса на 10.7 баллов к 6 неделе и 11.3 баллов к 12 неделе по сравнению с 7.5 и 5.8 баллами в группе плацебо соответственно |
| Kimball и соавт., второй этап, параллельное рандомизиров анное плацебо- контролируем ое исследование, состоящее из слепого 16- недельного периода наблюдения (первый этап) и открытого 36-недельного периода (второй этап) | 154 | Адалимумаб 40 мг первоначально; адалимумаб 40 мг раз в две недели; или плацебо. Все пациенты получали адалимумаб 40 мг один раз в две недели в начале второго этапа, но на 28-31 неделе переводились на еженедельный прием препарата при недостаточной эффективности терапии | 16 недель | К 16 неделе 3.9% пациентов, получающих плацебо (2 из 51), 9.6% пациентов, получающих адалимумаб раз в две недели (5 из 52) и 17.6% пациентов еженедельно принимающих препарат (9 из 51) достигли минимальный или незначительный эффект согласно шкале оценки изменения состояния пациента врачом | |
| Инфликсимаб | Paradela и соавт. (2012), проспективное исследование | 10 | Инфликсимаб 5 мг/ кг каждые 8 недель после начальной стандартной насыщающей дозы | 37 недель | У 2 пациентов (20%) после 5 доз не отмечено положительного результата лечения; у 5 (50%) больных зарегистрированы рецидивы болезни |
| Grant и соавт. (2010), рандомизиров анное двойное слепое плацебо- контролируем ое перекрестное исследование | 38 | Инфликсимаб 5 мг/ кг первые 2 инфузии раз в две недели, третья через 4 недели | 8 недель | 60% пациентов в группе, получающей инфликсимаб, по сравнению с 5.6% пациентов, получающих плацебо, отметили уменьшение тяжести проявления заболевания на 25-50% | |
| Moriarty и соавт. (2014), проспективное когортное исследование | 11 | Инфликсимаб 5 мг/ кг каждые 4 недели после начальной стандартной насыщающей дозы | 60.3 месяцев | 9 пациентов отметили значительное улучшение после прохождения курса терапии; у 2 больных к 12 и 19 месяцу соответственно эффекта от лечения не было | |
| Устекинумаб | Gulliver (2012), проспективное когортное исследование | 3 | Устекинумаб 45 мг п/к — первые 2 иньекции раз в месяц, третья — через 3 месяца | 6 месяцев | У 1 пациента отмечена ремиссия заболевания, у второго — улучшение процесса, у третьего больного эффекта от лечения не было |
| Этанерцепт | Adams и соавт. (2010), двойное слепое плацебо- контролируем ое исследование | 20 | Этанерцепт вводился в дозе 50 мг п/к 2 раза в неделю в течение 3 месяцев с последующем назначением без контроля плацебо в дозе 50 мг п/к 2 раза в неделю еще 3 месяца6 | 6 месяцев | Не отмечено статистически значимого отличия в данных оценки изменения состояния пациента врачом, общей оценки пациентом и дерматологическог о индекса качества жизни к 12 или 24 неделе наблюдения между группой, получающей препарат, и группой, получающей плацебо |
| Анакинра | Leslie (2014), проспективное когортное исследование | 5 | Анакинра 100 мг п/к ежедневно | 8 недель | Умеренное снижение на 34.8 баллов по модифицированной шкале Сарториуса |
Цинк
Исследование, в котором приняли участие 22 пациента с легкой и средней степенью тяжести ГГ, ежедневно получавшие 90 мг глюконат цинка в течение не менее 6 ме сяце в с по след ующем кон тролем в среднем в те чение 23.7 ме сяце в, продемонстрировало положительный результат терапии и последующую полную ремиссию процесса у 8 испытуемых и частичную ремиссию у 14 больных.
Метформин
18 из 25 (72%) пациентов, получающих метформин в дозе от 500 мг ежедневно до 500 мг 3 раза в день, отметили значительное уменьшение тяжести процесса по шкале Сарториуса на 12.7 баллов к 24 неделе терапии. У 7 больных лечение было неэффективно.
Вывод
ГГ характеризуется довольно тяжелым течение и значительными затратами на лечение. Существует множество методов, чтобы помочь пациентам с ГГ, тем не менее необходимо оценить все результаты и данные, чтобы определить оптимальный алгоритм терапии данного заболевания. Необходим индивидуальный подход к лечению каждого пациента с акцентом на улучшение качества жизни больных и терапии сопутствующих заболеваний.
Центр глубоких микозов;
ГКБ №81;
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения Москвы
Бородулина К.С.
ГБУЗ «Московский научно-практический центр дерматовенерологии и косметологии» Департамента здравоохранения Москвы, Москва, Россия
Гнойный гидраденит: вопросы патогенеза, оценочные шкалы, лечение (часть 2)
Авторы:
Бурова С.А., Бородулина К.С.
Как цитировать:
Бурова С.А., Бородулина К.С. Гнойный гидраденит: вопросы патогенеза, оценочные шкалы, лечение (часть 2). Клиническая дерматология и венерология.
2019;18(3):265‑269.
Burova SA, Borodulina KS. Hydradenitis suppurativa: issues of pathogenesis, rating scales, treatment. Overview (part 2) (in Russian only). Klinicheskaya Dermatologiya i Venerologiya. 2019;18(3):265‑269. (In Russ.)
https://doi.org/10.17116/klinderma201918031265

Хронический гнойный гидраденит (ХГГ) — заболевание мультифакторное, с хроническим рецидивирующим течением [1]. Апокриновые железы, вовлеченные в патологический процесс при ХГГ, начинают функционировать в пубертате. Ранее некоторые железы, например в ареолах, считали модифицированными апокриновыми железами, теперь признано, что все они являются истинными апокринами [2].
Точный патогенетический механизм заболевания остается неясным. Возможные причины ХГГ связаны с генетическими, экологическими, эндокринными и микробиологическими факторами. В нескольких исследованиях указано на более высокие показатели заболеваемости у курильщиков (70—90%), а также отмечена корреляция между индексом массы тела с тяжестью течения ХГГ. Также одной из причин воспалительного процесса считают некоторые бактерии и их ассоциации, выделяемые из очагов поражения. Тем не менее ХГГ не является классическим инфекционным заболеванием, так как до сих пор не ясно, какая роль в патогенезе отведена бактериям: первичная или вторичная [3]. В настоящее время растет число научных публикаций об этом аспекте заболевания.
Гистологическая картина при ХГГ варьирует. Так, по данным G. Jemec и соавт. [4], при исследовании 60 образцов биопсийного материала лишь в 17 из них отмечена фолликулярная окклюзия, при этом в подмышечной области апокриновые железы вовлекались в воспалительный процесс чаще, чем в паховой. В других исследованиях биопсийного материала показано наличие окклюзии волосяного фолликула вследствие гиперкератинизации, что вело к его расширению, формированию узелков или кист и, в конечном итоге, к разрыву тканей с образованием синусов, фистул и фиброзу [5]. Возможно, гетерогенность гистологической картины и обусловливает трудности в лечении ХГГ.
Дерматологи и хирурги обычно устанавливают диагноз ХГГ на основании характерной локализации и клинической симптоматики, но, к сожалению, часто с длительной диагностической задержкой, когда заболевание приобретает уже III—IV степень тяжести. В среднем время от начала заболевания до установления диагноза занимает около 7 лет [6]. Установлено, что больные обращаются к врачам разных специальностей (хирурги, дерматологи, урологи, проктологи, иммунологи, гомеопаты), длительное время занимаются самолечением, что также способствует позднему диагностированию и отсрочке своевременного адекватного лечения, и, в конечном итоге, утяжелению клинической картины и ухудшению качества жизни.
Выделяют три основных диагностических критерия ХГГ [7]:
1) типичная анатомическая локализация очагов воспаления: подмышечные и паховые области (симметричное поражение);
2) типичные клинические симптомы: умеренный болевой синдром, глубокие узлы, конгломераты узлов, «тяжистая» инфильтрация тканей, абсцедирование, свищевые ходы с гнойным отделяемым, фиброз, рубцы;
3) рецидивирование и хроническое течение.
К дополнительным критериям относят наследственную предрасположенность, наличие ХГГ у родственников; пилоноидальный синус, нагноившуюся крестцово-копчиковую кисту в анамнезе; метаболический синдром, гипергидроз, курение. A. Jørgensen и соавт. [8] изучали клиническую картину у пациентов с различным индексом массы тела (ИМТ) и обнаружили фенотипическую неоднородность у лиц с высоким и низким ИМТ. Авторы акцентировали внимание на том, что эти два фенотипа могут отражать разную этиологию и прогноз, следовательно, требуют разного подхода к тактике ведения.
Для облегчения оценки выраженности клинической картины и степени тяжести процесса в мире используют различные оценочные шкалы, помогающие лечащему врачу выбрать оптимальный алгоритм терапии и тактику ведения пациента с гидраденитом.
В существующих европейских клинических рекомендациях [7] выбор того или иного метода лечения основывается на стадийном подходе, с учетом степени тяжести заболевания по H. Hurley. Позже были предложены другие оценочные шкалы, позволяющие врачу определять показания для терапевтического или хирургического метода лечения данного заболевания в зависимости от выраженности клинической картины.
В соответствии с классификацией по H. Hurley выделяют три степени тяжести ХГГ [9]:
— I степень тяжести характеризуется образованием одного или нескольких безболезненных или малоболезненных изолированных узлов и/или абсцессов, не склонных к острому прогрессированию и нагноению; фистулообразование и рубцевание отсутствуют;
— II степень тяжести — усиление воспалительного процесса, ограниченного одной локализацией, рецидивирующие узлы и абсцессы отграничены друг от друга, не сливаются, вскрываются, образуют свищевые ходы с гнойно-сукровичным отделяемым, некоторые элементы рубцуются;
— III степень тяжести — формируется диффузный конгломерат воспалительных инфильтратов, состоящий из сливающихся узлов и абсцессов, усиливается флюктуация, образуется множество сообщающихся между собой свищей, продолжается рубцевание; ограничения подвижности в суставах из-за боли иногда приводят к контрактурам.
Существует также более сложная система определения индекса тяжести ХГГ — модифицированная оценка Сарториуса, которая предполагает количественный подсчет баллов в зависимости от наличия основных клинических параметров заболевания: число вовлеченных в процесс определенных анатомических зон, количество болезненных узлов, абсцессов, свищевых ходов с гнойным отделяемым, рубцов, поверхностных гнойничков и фолликулитов, расстояние между поврежденными участками, наличие здоровой кожи в очаге поражения [10].
Некоторые авторы [11] используют критерии «Общей врачебной оценки тяжести ХГГ» (HS-PGA). Минимальная степень — один или несколько невоспаленных, безболезненных узлов; легкая степень — 1—4 воспаленных образования, один абсцесс или свищ; средняя степень — менее 10 воспалительных элементов, 1—5 абсцессов и свищей; тяжелая степень — более 10 узлов, 2—5 абсцессов и свищей; очень тяжелая степень тяжести — более 5 абсцессов и свищей.
Существует также шкала оценки индекса тяжести HSSI в баллах: легкая степень — от 0 до 7 баллов, средняя степень — 8—12, тяжелая степень — 13 и более. При подсчете учитывают количество пораженных областей, болевой синдром, число воспалительных элементов, социализацию и т. д. [12, 13].
Для оценки ХГГ одной из последних разработана шкала клинического ответа гнойного гидраденита (HiSCR). Данная шкала была предложена при лечении ХГГ адалимумабом, показывает снижение на 50% и более количества воспалительных элементов и отсутствие признаков увеличения абсцессов или свищей при ХГГ в сравнении с исходным уровнем [14, 15].
Мультидисциплинарный подход к решению проблемы ХГГ обусловливает не только изучение степени тяжести и разработку оценочных шкал, но и анализ лабораторных показателей и выработку наиболее оптимальной тактики в лечении таких больных как дерматологами, так и хирургами. N. Yaşar и соавт. [16] акцентировали внимание на изменении гематологических параметров при ХГГ в зависимости от тяжести заболевания. Было установлено, что уровень гемоглобина был выше на стадии I, чем на стадии III, тогда как гематокрит, средний объем тромбоцитов, уровень концентрации корпускулярного гемоглобина и количество тромбоцитов не отличались при разных стадиях. Количество лейкоцитов и нейтрофилов было выше на III стадии, чем на II, а количество лимфоцитов было ниже на III стадии, чем на II. Данные изменения можно в дальнейшем использовать для оценки тяжести ХГГ.
Лечение ХГГ можно разделить на консервативное и хирургическое. К консервативным методам относят местную, системную и другие виды терапии. Учитывая влияние заболевания на качество жизни, следует уделять повышенное внимание психосоциальной адаптации пациентов. Рекомендации врача должны быть направлены и на снижение факторов риска заболевания. Поскольку курение и ожирение показывают самую сильную корреляцию с тяжестью патологического процесса, больным ХГГ следует рекомендовать отказ от курения и принятие мер по снижению массы тела [2].
В нашей стране подход к лечению ХГГ сходен с лечением глубоких пиодермий и определяется применением противовоспалительных и антибактериальных препаратов [17, 18]. В последних публикациях отечественных авторов показан положительный эффект от терапии ингибиторами ФНО-α, но, к сожалению, эти исследования единичны [19].
В европейских рекомендациях [20] антибиотики упомянуты как препараты первой линии в лечении ХГГ с учетом степени тяжести по H. Hurley. Однако антибактериальная терапия, тем более длительная, часто сопровождается осложнениями со стороны паренхиматозных органов. Кроме того, при невозможности видовой идентификации бактерий в культуре и определения чувствительности микрофлоры из очага поражения антибактериальная терапия может оказаться малоэффективной и вызвать лишь кратковременный эффект. Антибиотики, как правило, применяют при всех степенях тяжести ХГГ и в обязательном порядке в пред- и послеоперационнном периодах. Чаще всего это линкозамиды, тетрациклины, рифампицин, цефалоспорины и т. д.
От применения стероидных препаратов и дапсона отказались ввиду их невысокой клинической эффективности [21—24].
Терапия биологическими препаратами, блокаторами фактора некроза опухоли-α в отношении ХГГ эффективна, но имеет ряд ограничений: не применяется при тяжелых формах заболевания, обильном нагноении и абсцедировании, риске распространения инфекции, инициации иммуносупрессивной терапии, некоторых заболеваниях внутренних органов [25, 26]. Более тщательно изучен адалимумаб, который применяют в дозе 40 мг/нед [27]. Менее популярен этанерцепт, который показал малую эффективность при ХГГ [28].
Опубликованы результаты ряда исследований [29, 30] на небольшом клиническом материале о применении новых иммунных методов воздействия препаратом apremilast — молекулярным селективным ингибитором фосфодиэстеразы 4 (PDE4). Показана некоторая эффективность в лечении ХГГ.
Последние публикации показывают, что своевременное, раннее и широкое хирургическое иссечение гнойных очагов в лечении любых стадий ХГГ — наиболее эффективный способ достижения выздоровления, предотвращения осложнений и рецидивов и быстрого улучшения качества жизни пациентов [31—33]. Объем и вид хирургического вмешательства определяются индивидуально в соответствии с возрастом, степенью тяжести, локализацией воспалительного процесса и общим статусом пациента. Предоперационная подготовка важна, поскольку влияет на исход хирургического вмешательства и дальнейшее выздоровление. Z. Alharbi и соавт. [30] провели ретроспективный анализ 50 операций с широким хирургическим доступом у 32 пациентов, у 81,25% рецидивов после лечения не было.
Описаны и другие методы вмешательств при ХГГ: криоинсуффляция, ботулинотерапия, фотодинамическая терапия (ФДТ). Однако результаты разнородны и единичны [33].
Наряду с традиционными хирургическими методами используют лазерную хирургию. Довольно высокую эффективность показала абляция лазером на диоксиде углерода (CO2). P. Hazen и соавт. [34] на примере 22 пациентов показали положительные результаты в лечении гидраденита с помощью длинноимпульсного неодимового диодного лазера на алюмоиттриевом гранате (Nd: YAG лазер) — 72,7 в сравнении с 22,9%.
В условиях возрастающего интереса к проблеме ХГГ в нашей стране ведется поиск новых медикаментозных средств и оптимальных хирургических методов лечения этого заболевания, создаются алгоритмы ведения пациента в зависимости от давности заболевания, локализации, степени тяжести и распространенности гнойно-воспалительного процесса, разрабатываются правила предоперационной подготовки и послеоперационного ведения пациентов с ХГГ.
Необходимым условием радикального иссечения очагов воспаления и успешности операции является тщательная предоперационная подготовка пациента. С целью максимального купирования перифокального воспаления, уменьшения гнойного отделяемого из свищей, отграничения инфильтратов от здоровой ткани, повышения общей сопротивляемости организма, нормализации температурной реакции, показателей периферической крови и иммунологических показателей проводятся антибиотико- и актинолизатотерапия, а также эвакуация гнойных масс с микроорганизмами из свищевых ходов путем промывания их растворами антисептиков [35, 36].
В нашей стране отсутствует единый алгоритм, который позволил бы определить показания для консервативного и хирургического лечения ХГГ. Изыскание новых методов лечения, а также разработка унифицированной клинической классификации, оценочных шкал являются актуальными задачами на современном этапе.
Таким образом, будущие исследования должны быть направлены на оптимизацию лечения.
Сведения об авторах
Бурова С.А. — https://orcid.org/0000-0003-0017-621X
Бородулина К.С. – https://orcid.org/0000-0001-7670-1450
Автор, ответственный за переписку: Бородулина К.С. —
e-mail: kristinaps2007@mail.ru
Что такое гнойный гидраденит?
Гнойный гидраденит (также называемый болезнь Вернея, болезнь Вельпо) — это хроническое заболевание, характеризующееся опухшими болезненными поражениями, возникающими в области подмышек (подмышечных впадин), паха, анального отдела и молочной железы. Болезнь Вернея возникает из-за обструкции волосяных фолликулов и вторичной инфекции, а иногда и воспаления некоторых потовых желез (апокринных желез).
Гнойный гидраденит прогрессирующее заболевание, при котором единичные, гнойные абсцессы становятся твердыми комочками, затем болезненными, глубоко посаженными, часто воспаленными скоплениями очагов с хроническим просачиванием. Заживление пораженных участков обычно происходит с прогрессирующим рубцеванием (фиброзом) ткани.
При тяжелом течении болезни формируются хронические эпителиальные, иногда взаимосвязанные, синусовые пути. Это часто приводит к попаданию пота и бактерий в окружающие ткани, что вызывает новое воспаление и инфекцию. Гнойный гидраденит может быть чрезвычайно болезненным и изнурительным состоянием, но редко угрожающим жизни; болезнь возникает только тогда, когда бактерия приводит к подавляющей системной инфекции у человека с ослабленным иммунитетом.
Считалось, что гнойный гидраденит является редким заболеванием, потому что сообщалось только о наиболее тяжелых случаях. Гнойный гидраденит был впервые описан в медицинской литературе доктором Вельпо в 1839 году и считался чрезвычайно тяжелой формой прыщей (инверсный акне). Она чаще всего возникает в период полового созревания, поскольку изменения в волосяных фолликулах, вызываются всплеском половых гормонов. Состояние может также начать возникать у пациентов любого возраста после полового созревания, но редко до. Случаи различаются по степени тяжести, но все они требуют некоторого внимания и лечения. Для легких случаев заболевания хватит и домашних средств. Однако при тяжелых формах часто назначают ежедневные лекарства, и в конечном итоге может быть рекомендована радикальная операция. Ранняя диагностика и лечение болезни Вельпо важны, поскольку они могут помочь справиться с симптомами и предотвратить образование новых фурункулов и повреждений.
Признаки и симптомы
Гнойный гидраденит — это хроническое воспалительное заболевание, поражающее потовые железы, известные как апокринные железы. У большинства людей с болезнью рецидивирующие поражения развиваются в подмышечной впадине, паху, вульве или анальной области. Тем не менее, в некоторых случаях состояние может поражать потовые железы молочных желез, кожи головы или других областей. Имеющиеся данные свидетельствуют о том, что у женщин чаще поражаются область подмышек или вульвы, в то время как у мужчин преимущественно анальная область.
Хотя возраст начала может варьироваться, симптомы часто становятся очевидными в период полового созревания или в раннем взрослом возрасте. Заболевание длится много лет, с периодическим улучшением и ухудшением симптомов. Многие вещи могут вызвать вспышки этого заболевания, включая менструацию у женщин, увеличение веса, стресс, гормональные изменения, жар и потливость. В некоторых случаях ранние симптомы, такие как зуд или дискомфорт, могут предшествовать характерным проявлениям заболевания.
Различают 3 клинических стадии болезни. Каждую стадию лучше всего лечить различными методами терапии. В идеале лечение должно остановить прогрессию до стадии 3 как можно дольше. Тем не менее, гнойный гидраденит не излечивается, и болезнь в конечном итоге будет идти своим чередом.
- Стадия 1: В некоторых случаях ранние симптомы, такие как зуд или дискомфорт, могут предшествовать характерным проявлениям состояния (см. фото ниже).
- Стадия 2: Периодически образуются нарывы, с формированием синусовых путей и рубцов. Присутствовать может один или несколько широко разделенных поражений.
- Стадия 3: По всей области поражения наблюдаются диффузные или почти диффузные вовлечения или множественные взаимосвязанные участки и абсцессы.

Обструкция (окклюзия) волосяных фолликулов и разрыв фолликула приводит к развитию чувствительных или болезненных, красноватых узелков и гнойных полостей инфекции (абсцессы). Абсцессы могут самопроизвольно разрываться, выводя наружу гной, который может смешиваться с прозрачной жидкостью (серозно-гнойный), которая часто имеет неприятный запах. При заживлении могут образовываться рубцовые ткани и новые очаги поражения рядом с начальными узлами. В некоторых тяжелых случаях глубокие абсцессы могут дренироваться через аномальные каналы глубоко в тканях кожи, которые соединяют их с поверхностью тела (образование синусового тракта). Повторное заживление и рецидивы приводят к прогрессирующему рубцеванию пораженных тканей, которые могут выглядеть как толстые, похожие на связанные полосы. В чрезвычайно тяжелых случаях состояние может стать обширным и потенциально инвалидизирующим.
Причины и факторы риска
Точная основная причина гнойного гидраденита неизвестна, но состояние, вероятно, является результатом сочетания генетических факторов и факторов окружающей среды.
Симптомы возникают в результате ненормальной обструкции (окклюзии) волосяных фолликулов и вторичной бактериальной инфекции и воспаления с последующим разрывом протоков, распространением инфекции и рубцеванием. Другой возможной причиной является патологическое развитие желез.
Некоторые больные имеют семейную историю болезни, что свидетельствует о том, что генетические факторы могут играть причинную роль. В семейных случаях заболевания был замешан молекулярный комплекс гамма-секретазы.
Затронутые группы населения
Болезни Вельпо поражает женщин примерно в три раза чаще, чем мужчин. Около 1/100 человек страдают от легких случаев заболевания. Состояние обычно становится очевидным в период полового созревания, но почти никогда после 40 лет.
Близкие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы гнойного гидраденита. Сравнения могут быть полезны для дифференциальной диагностики:
- Фурункулез характеризуется развитием воспалительных узелков, известных как фурункулы или карбункулы, из-за инфекции бактерии стафилококк. Фурункулы представляют собой красные, чувствительные или болезненные комки, которые выделяют центральное ядро ткани и гной. Они могут иногда повторяться. Способствующие факторы, которые делают человека уязвимым для фурункулеза, могут включать ожирение, сахарный диабет и плохую гигиену.
- Туберкулез кожи — инфекционное заболевание, вызываемое бактериями Mycobacterium tuberculosis (Палочка Коха).
- Болезнь Крона — воспалительное заболевание кишечника, которое редко может иметь кожные проявления, имитирующие симптомы гнойного гидраденита.
Существует и ряд других заболеваний, которые могут характеризоваться симптомами, похожими на симптомы, связанные с болезнью Вельпо.
Диагностика
Гнойный гидраденит часто остается недиагностированным в течение многих лет, поскольку пациентам слишком стыдно говорить с кем-либо об их симптомах. Диагноз ставится на основании симптомов, истории болезни, обследования и анализов крови. Если присутствует гной или удаление жидкости, образец жидкости может быть отправлен для анализа культуры, чтобы исключить другие кожные заболевания.
— Клиническое обследование.
Ультрасонография волосяных фолликулов и толщины кожи может выявить аномалии и показать, как прогрессирует заболевание. Другими тестами, которые используются при оценке стадии заболевания, являются анализ С-реактивного белка, общий анализ мочи, оценка уровня рецепторов IL-2 в сыворотке крови, оценка скорости оседания эритроцитов, а также общий анализ крови с подсчетом тромбоцитов.
Стандартные методы лечения
Какого либо специфического метода лечения гнойного гидраденита нет. Лечение зависит от того, на каком клиническом этапе находится пациент, и от степени тяжести его состояния. Кроме того, то, что работает для одного пациента, может не работать для другого. Легкие случаи заболевания обычно можно лечить с помощью домашних средств, таких как:
- применение теплых компрессов;
- хорошая гигиена;
- использование антибактериального мыла;
- применение антисептиков и противовоспалительных препаратов;
- ношение свободной одежды.
Для пациентов с болезнью также важно поддерживать здоровый вес и не курить. Люди с избыточным весом испытывают большее трение на своем теле, которое раздражает кожу. Они также более склонны к чрезмерному потоотделению. Оба помогают в раздражении кожи, вызывая вспышку гнойного гидраденита.
Многие пациенты с расстройством испытывают трудности с правильным поддержанием своего веса, потому что физические нагрузки вызывают у них боль. Оставаться здоровым очень важно для замедления прогрессирования заболевания, поэтому необходимо приложить все усилия, чтобы найти силы для упражнений. Многие пациенты сообщают, что плавание не только отлично подходит для поддержания формы, но и обеспечивает временное облегчение при болезненных поражениях.
Умеренные и тяжелые случаи гнойного гидраденита могут потребовать лекарств. Возможные препараты включают:
- антибиотики;
- пероральные ретиноидные препараты;
- противовоспалительные препараты;
- кортикостероиды;
- гормоны и ингибиторы альфа-фактора некроза опухолей.
Другие виды лечения, которые, как было показано, приносят некоторую пользу, включают:
- лазерную терапию углекислым газом;
- лазерное удаление волос;
- лучевую терапию;
- хирургическое вмешательство.
В 2015 году Хумира (адалимумаб) был одобрен для лечения гнойного и умеренного гидраденита. Это первый и единственный FDA-одобренный препарат для лечения взрослых с гнойным гидраденитом.
Хирургическое удаление поражений и пересадка кожи пораженных участков могут быть необходимы в случаях обширных, постоянных рубцовых тканей. Эта операция является обширной, поскольку необходимо удалить не только кожу, содержащую поражения, но и широкие края вокруг пораженного участка. Хирургия долгое время считалась лекарством от этой болезни, но конкретные исследования показали обратное. В идеале, болезнь исчезнет в областях, в которые была пересажена кожа; тем не менее, показатели повторяемости могут быть высокими, особенно если брать только узкие поля. Более ограниченное хирургическое вмешательство, состоящее из вскрытия абсцессов и синусовых путей, может быть полезным для смягчения симптомов, но эти поражения почти всегда повторяются.
Прогноз
Гнойный гидраденит — это хроническое заболевание, т.е. оно не проходит само по себе. Несмотря на текущее лечение, нарывы обычно продолжают возвращаться. Заболевание, как правило, постепенно прогрессирует, нарывы появляются чаще, в большем количестве и затрагивают больше областей тела. Патология не угрожает жизни, но люди с расстройством могут испытывать частые боли, затруднения при движении и чувствовать смущение или стыд из-за своей болезни. Это может вызвать социальную изоляцию, депрессию и/или беспокойство и повлиять на качество жизни человека.
Одно из наиболее опасных кожных заболеваний, требующих помощи врача, — гидраденит — воспаление апокриновых желез. Частый период возникновения заболевания — половое созревание и старческий возраст.
[dcb id=9523]
При попадании микробов в апокриновые железы развивается большой нарыв, внутри которого находится жидкий гной. В отличие от фурункула, гидраденит не имеет некротического стержня и больше похож на флегмону.
Причины развития гидраденита
Апокриновые железы не принимают основного участие в терморегуляции организма. Они активизируются во время стрессовых ситуаций, оказывая влияние на запах и вязкость пота. Основная функция органа — выведение из человеческого организма тяжелых металлов, воды, солей и различных продуктов обмена. Неправильная работа желез и проникновение в них бактерий приводят к воникновению гидраденита.
Гидраденит является разновидностью пиодермии и причины его появления напрямую связаны с наличием гноеродных кокков. Воспаление апокриновых желез при гидрадените — результат разрушительного воздействия стафилококка.
К факторам риска, провоцирующих заболевание относятся:
- Повышенная потливость или гипергидроз.
- Заболевания, травмирование кожи.
- Несоблюдение личной гигиены.
- Неправильное использование дезодорирующих средств.
- Нарушение липидного обмена.
- Условия повышенной влажности или жаркого климата и др.
Симптомы гидраденита
Эту болезнь ещё назывют «сучье вымя», так как в области проникновения стафилококка образуется нарыв, внешне похожий на грудную железу собаки. Чаще гидраденит обнаруживают в области подмышек и паха. Также может возникнуть области половых органов и под грудью.
Нарыв может быть один их образуется сразу несколько, тогда впоследствии они сольются в один большой инфильтрат. У больного иногда может повышаться температура, сопровождающаяся слабостью и недомоганием. Нарывы болезненны.
Поражение часто бывает множественным, когда развивается сразу несколько гнойников. Состояние больного ухудшается, возникает лихорадка, появляются покраснение и сильная боль в области поражения. Иногда инфильтраты нагнаиваются и прорываются с выделением большого количества жидкого гноя. Затем они затягиваются, но вскоре в процесс вовлекаются соседние железы и все начинается снова. Болезнь имеет затяжное течение и может привести к сепсису — заражению крови.
Лечение гидраденита
Болезнь необходимо обязательно лечить, без лечения она может осложниться нагноением и заражением крови. Опасность гидраденита также состоит и в том, что он может приобретать хроническое течение. Наиболее часто эта картина встречается у тех, кто страдает проблемами ожирения, пониженным иммунитетом, сахарным диабетом, а также у людей с дисфункцией половых желез.
Самое опасное осложнение гидрадениьа — воспаление лимфатических узлов и сосудов. Лимфатическая система принимает прямое участие в обменных процессах организма. Ее воспаление может быть чревато многими последствиями. Не менее опасным осложнением является развитие лимфидемы или отека мягких тканей. Если процесс заболевания зашел слишком далеко, то сепсис может оказаться неизбежностью.
Диагноз при гидрадените ставят после взятия анализов. В крови обнаруживается повышение СОЭ и увеличенное количество лейкоцитов, а в отделяемом из гнойников высевается стафилококк.
Лечение дерматолог подбирает индивидуально. На начальной стадии чаще всего применяется симптоматическая терапия. На стадии нагноения болезнь можно вылечить без операции. Пораженные участки обрабатывают антисептическими средствами, убивающими стафилококк и препятствующим распространению инфекции на соседние железы.
Хороший результат дает использование полуспиртовых повязок, способствующих рассасыванию инфильтрата. При сильной боли проводят обкалывание крупных очагов растворами местных анестетиков.
Больному назначаются антибиотики внутримышечно или в таблетках. Для стимуляции иммунитета вводится стафилококковый анатоксин. Помогает выздоровлению назначение витаминов и рассасывающих препаратов.
При абсцессе не избежать хирургического вмешательства. Гнойник вскрывают, обеспечивая отток гнойного экссудата. В исключительных случаях требуется полное иссечение пораженного участка. Применение антибиотиков после проведенной процедуры — обязательное условие.
При безрезультатности консервативной терапии гнойник вскрывают и дренируют, чтобы обеспечить отток содержимого. При рецидивах болезни проводят двухэтапное хирургическое вмешательство:
- Нагноившиеся инфильтраты вскрывают с удалением пораженной подкожной клетчатки, но рану не зашивают, а оставляют открытой. Пациенту назначают курс антибиотиков.
- После того, как раневая поверхность очистится от гноя, иссекают кожу и оставшуюся подкожную клетчатку во всей зоне, пораженной гидраденитом. Дефект закрывают тканями, взятыми у пациента. Только так можно полностью избавиться от рецидивов болезни.
Больные часто интересуются, почему нельзя провести операцию за один раз, не оставляя открытой раны. Дело в том, что при таком методе на коже остаются грубые неэстетичные рубцы, мешающие полноценно двигать рукой или ногой.
После операции больному назначают препараты, повышающие иммунитет, и способствующие быстрому заживлению тканей. Показана УФ — облучение пораженных областей, лазерная и магнитная терапия, электрофорез. Для предотвращения рецидива гидраденита больному назначается повторный курс антибиотиков.
Профилактика развития гидраденита
- Исключение обтягивающего белья.
- Соблюдение правил гигиены.
- Использование качественных гигиенических средств.
- Профилактика инфекционных заболеваний.
- Регулярное укрепление иммунной системы.
Профилактика является наилучшим способом избежать заболевания гидраденитом.
[dcb id=9583]


