Прижизненное донорство почки
Версия: Клинические рекомендации РФ 2023 (Россия)
Категории МКБ:
Донор почки (Z52.4)
Разделы медицины:
Нефрология, Трансплантология
Общая информация
Краткое описание
Разработчик клинической рекомендации:
- Российское трансплантологическое общество
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Клинические рекомендации
Прижизненное донорство почки
Возрастная категория: Взрослые
Пересмотр не позднее: 2025
Дата размещения: 16.03.2023
Статус: Действует
ID: 760
Определение заболевания или состояния (группы заболеваний или состояний)
Прижизненное донорство почки – это процесс, направленный на получение органа от живого донора и последующую трансплантацию удаленной почки другому человеку с хронической болезнью почек 5 стадии (ХБП). Трансплантацию органов от прижизненных доноров стоит рассматривать как оптимальный метод заместительной почечной терапии в связи с ее более успешными результатами (исходя из лучшей выживаемости трансплантатов и реципиентов), а также в связи с недостатком органов от посмертных доноров. Хроническая нехватка донорских органов привела к более широкому прижизненному донорству [1]. На территории Российской Федерации прижизненным донором может являться только близкий родственник. Согласно законодательству РФ, генетическое родство между реципиентом и донором является обязательным условием проведения трансплантации органа, полученного от живого человека [2].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Живой родственный донор почки.
AB0-совместимый донор почки / AB0-несовместимый донор почки.
Этиология и патогенез
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Прижизненное донорство почки – это ятрогенное состояние, возникающее как результат медицинской деятельности, направленной на получение пригодной для трансплантации почки от живого донора с целью ее последующей пересадки пациенту с терминальной ХБП. Удаление одного из парных органов уменьшает массу действующих нефронов, что в результате приводит к снижению скорости клубочковой фильтрации (СКФ), но должно исключать развитие ХБП.
Эпидемиология
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
В 2017 г. в мире программный гемодиализ получали около 3,4 миллиона больных с хронической болезнью почек [3].
В Российской Федерации в 2018 г. заместительную почечную терапию (ЗПТ) получали всего 54953 больных. Показатель обеспеченности ЗПТ в целом в пересчете на 1 млн населения на 31.12.2018 г. в среднем по России составил до 374,4 больных/млн [4]. В 2019 г. 28 из 46 функционирующих центров выполняли родственные трансплантации почки. Из 1473 трансплантаций почки, произведенных в РФ в 2019 г., 183 были от живого родственного донора (в 2018 г. – 200). На долю Москвы и Московской области приходится 8 центров, выполнивших в 2019 г. 124 родственные трансплантации почки, или 66,3% от общего числа родственных пересадок почки в России (в 2018 г. – 117 и 58,5%). 2 центра выполнили 20 и более родственных трансплантаций почки: НМИЦ ТИО им. ак. В.И. Шумакова (68), НМИЦ здоровья детей (21). Средняя частота использования прижизненного донорства почки в 2019 г. составила 12,4% от общего числа трансплантаций почки (в 2018 г. – 14,7%) [5].
Клиническая картина
Cимптомы, течение
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Ввиду того, что прижизненным донором почки выступает практически здоровый человек, до момента проведения нефрэктомии состояние не является патологическим и не имеет клинической картины. Основной целью процесса обследования потенциальных доноров является оценка пригодности донора и минимизация потенциального риска здоровью донора. Это включает выявление противопоказаний к донорству и потенциальных клинических (физических и психосоциальных) рисков. Донорами могут стать лица старше 18 лет, прошедшие полное медицинское обследование, давшие информированное добровольное согласие на проведение нефрэктомии. Изъятие почки у живого донора для трансплантации допустимо только в случае, если по заключению врачебной комиссии медицинской организации с привлечением соответствующих врачей-специалистов, оформленному в виде протокола, его здоровью не будет причинен значительный вред [2, 6].
Потенциальные прижизненные доноры должны оцениваться в соответствии с принятым центром трансплантации протоколом. Рекомендуется определить перечень рутинных скрининговых тестов и дополнительных исследований. Обследования должны проводиться в логической последовательности, чтобы потенциальный донор был защищен от ненужных, особенно инвазивных, процедур до соответствующей стадии оценки.
Пожилой возраст не является абсолютным противопоказанием к донорству, но медицинское обследование пожилых доноров должно быть особенно тщательным – для того чтобы выявить у них относительные или абсолютные противопоказания к прижизненному донорству. И донор, и реципиент должны знать, что пожилой донор может подвергаться большему риску периоперационных осложнений. Это особенно заметно у доноров старше 60 лет. В целом, использование почек от пожилых доноров, по-видимому, является эквивалентной или полезной альтернативой ожиданию почек посмертных доноров [7]. Было показано, что СКФ почки у живого родственного донора является важным определяющим фактором функции почечного трансплантата в отдаленном периоде [8, 9].
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
2.1 Жалобы и анамнез
Критерии установления диагноза для потенциального прижизненного родственного донора неприменимо.
-
Рекомендуется тщательный сбор анамнеза потенциального прижизненного донора почки для выявления всех возможных отклонений в состоянии здоровья [1].
УУР: С (УДД – 5).
Комментарии: рекомендуется осмотр врача-терапевта с изложением полного медицинского анамнеза, объективного статуса, принимаемых препаратов. Целью сбора анамнеза является выявление любого прошлого или настоящего состояния, которое может повлиять на безопасность донора во время операции или в долгосрочной перспективе, а также скрытой или текущей инфекции у донора, которая может быть передана реципиенту путем трансплантации. Особое внимание следует уделять оценке психического и физического здоровья потенциального донора с историей злоупотребления психоактивными веществами или наркотиками. Такие потенциальные доноры всегда должны получить официальную психиатрическую консультацию.
2.2 Физикальное обследование
-
Рекомендуются консультации врачей специалистов: врача-кардиолога, врача-анестезиолога-реаниматолога, врача-сердечно-сосудистого хирурга, врача-радиолога, врача-стоматолога, врача-эндокринолога, врача-нефролога, врача-инфекциониста, врача-уролога, врача-акушера-гинеколога потенциальному прижизненному донору почки для выявления всех возможных отклонений в состоянии здоровья [10, 117];
УУР: C (УДД – 3).
-
Рекомендуется тщательный физикальный осмотр, оценка нутритивного статуса потенциального прижизненного донора почки для выявления всех возможных отклонений в состоянии здоровья [10, 11];
Комментарии: пациенты с умеренным ожирением (ИМТ 30-35 кг/м2) должны пройти тщательную предоперационную оценку, чтобы исключить наличие сердечно-сосудистой патологии, заболеваний дыхательных путей и почек. Данные о безопасности донорства почек у очень тучных пациентов (ИМТ> 35 кг/м2) ограничены, поэтому донорство в данном случае не рекомендуется [11,12, 13].
УУР C (УДД – 5).
-
Рекомендуется осмотр врачом-хирургом потенциального прижизненного донора почки с целью выявления перенесенных ранее оперативных вмешательств [10,11, 118];
УУР: C (УДД – 5).
-
Рекомендуется прием (осмотр, консультация) врача-уролога потенциального прижизненного донора почки с целью исключения онкологической патологии [13,14];
УУР: C (УДД – 5).
-
Рекомендуется осмотр врачом-онкологом (маммологом) для женщин старше 40 лет для исключения наличия новообразования молочных желез [12,13,14,15];
УУР C (УДД – 5).
-
Рекомендуется осмотр врачом-кардиологом потенциального прижизненного донора почки с целью исключения патологии сердечно-сосудистой системы и гипертонии [16,17];
УУР С (УДД – 4).
Комментарии: если артериальное давление выше нормального или потенциальный донор получает постоянную гипотензивную терапию, рекомендуется амбулаторный мониторинг артериального давления. Гипертония является одной из наиболее распространенных причин отказа от прижизненного донорства почки [16]. Рекомендуется, чтобы потенциальные доноры с гипертонией были исключены из донорства, если: артериальное давление не удается контролировать на уровне меньше 140/90 мм рт. ст. при применении одно- или двухкомпонентной терапии; имеются подтвержденные повреждения органов мишеней (ретинопатия, гипертрофия левого желудочка, протеинурия, перенесенные ранее сердечно-сосудистые заболевания). Артериальное давление меньше 140/90 мм рт. ст. считается приемлемым для донорства почки. Субклинический, гипертонический нефросклероз может выявляться у потенциальных доноров почки. Повышение артериального давления после нефрэктомии может увеличить будущий сердечно-сосудистый риск или прогнозируемую частоту возникновения ХБП [17]. Всем прижизненным донорам почек следует рекомендовать свести к минимуму риск гипертонии и ее последствий с помощью таких мер, как отказ от курения, сокращение потребления алкоголя, физические упражнения и, при необходимости, снижение веса. Рекомендуется, чтобы доноры, у которых диагностировали артериальную гипертензию во время обследования до донорства, или у которых развивалась артериальная гипертензия после донорства, принимали лечение в соответствии с клиническими рекомендациями «Артериальная гипертензия у взрослых».
-
Рекомендуется прием (осмотр, консультация) врача-эндокринолога потенциального прижизненного донора почки с целью исключения патологии органов эндокринной системы [18, 122].
УУР С (УДД – 5).
Комментарии: Потенциальные доноры с повышенным риском развития диабета 2 типа из-за семейного анамнеза, гестационного диабета или ожирения должны проходить тест толерантности к глюкозе[123]. Если у обследуемого определяется постоянно повышенный уровень глюкозы натощак и/или нарушения толерантности к глюкозе, следует тщательно оценить риск развития диабета после донорской нефрэктомии. Наличие сахарного диабета у потенциальных доноров почек требует тщательной оценки соотношения рисков для донора и ожидаемых результатов для реципиента.
2.3 Лабораторные диагностические исследования
В связи с тем, что основной целью обследования потенциального прижизненного донора является исключение скрыто протекающих острых или хронических заболеваний или патологических состояний, которые могут послужить причинами отказа в прижизненном донорстве:
-
Рекомендуется определение основных групп по системе AB0, определение антигена D системы Резус (резус-фактор) потенциальному прижизненному донору почки для определения совместимости/несовместимости донора и реципиента по группе крови [10,19,20];
УУР С (УДД – 5).
Комментарии: для выполнения АВ0-несовместимых трансплантаций и трансплантаций у высокосенсибилизированных реципиентов учреждение, выполняющее трансплантации, должно обладать опытом подготовки и проведения десенсибилизации реципиентов почки [10,19,20].
-
Рекомендуется выполнять общий (клинический) анализ крови (количество эритроцитов, тромбоцитов, лейкоцитов, уровень гемоглобина) дифференцированный подсчет лейкоцитов (лейкоцитарная формула) потенциальному прижизненному донору почки с целью диагностики и дифференциальной диагностики анемии [23, 124, 125];
УУР C (УДД – 5).
Комментарии: анемия (согласно классификации ВОЗ, Hb <130 г/л для мужчин и <120 г/л для женщин) должна быть полностью исследована и пролечена. Серповидно-клеточная анемия является абсолютным противопоказанием для прижизненного донорства почки в связи с тем, что у 5-20% пациентов в течение жизни развивается ХБП. Талассемия также является противопоказанием к прижизненному донорству почки, поскольку пациентам периодически требуются гемотрансфузии, и они часто страдают от перегрузки железом и связанных с ней осложнений [23,24,117].
-
Рекомендуются исследование уровня железа сыворотки крови, исследование уровня общего белка в крови, исследование уровня альбумина в крови, исследование уровня мочевины в крови, исследование уровня креатинина в крови, исследование уровня общего билирубина в крови, исследование уровня билирубина связанного (конъюгированного) в крови, исследование уровня билирубина свободного (неконъюгированного) в крови, исследование уровня глюкозы в крови, исследование уровня холестерина в крови, исследование уровня общего кальция в крови, исследование уровня неорганического фосфора в крови, определение активности аспартатаминотрансферазы в крови, определение активности аланинаминотрансферазы в крови, определение активности гамма-глютамилтранспептидаза в крови, определение активности щелочной фосфатазы в крови, исследование уровня гликированного гемоглобина в крови потенциальному прижизненному донору почки с целью диагностики метаболических нарушений [13, 117, 119, 120, 123, 124,125];
УУР С (УДД – 5).
Комментарии: Концентрация глюкозы в сыворотке крови натощак выше 6,1 ммоль/л свидетельствует о возможном нарушении обмена глюкозы и требует проведения теста толерантности к глюкозе [18]. Диабет также может быть диагностирован на основе исследования гликированного гемоглобина HbA1c (результат> 6,5% достаточен для диагностики диабета, в случае выявления в двух повторных исследованиях) [123].
-
Рекомендуется исследование уровня простатспецифического антигена общего в крови, уровня простатспецифического антигена свободного в крови у мужчин старше 40 лет для исключения онкологической патологии [13,14];
УУР C (УДД – 5).
-
Рекомендуется исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня хлоридов в крови, исследование кислотно-основного состояния и газов крови потенциальному прижизненному донору почки с целью диагностики электролитных нарушений [13, 117, 119, 124, 125];
УУР С (УДД – 5).
-
Рекомендуется оценка коагулограммы (ориентировочное исследование системы гемостаза) (уровень фибриногена, антитромбина-III, плазминогена, протромбиновый индекс, АЧТВ) потенциальному прижизненному донору почки с целью диагностики нарушений свертывающей системы крови [13, 117, 119, 120, 124, 125];
УУР С (УДД – 5).
-
Рекомендуется проведение первоначальной оценки потенциальных доноров почки с использованием расчетной СКФ, выраженной в мл/мин/1,73 м2, рассчитанной в результате анализа креатинина, стандартизированного по Международному эталонному стандарту [27, 117, 120, 121];
УУР B (УДД – 3).
Комментарии: после донорства почки наблюдается компенсаторное увеличение функции оставшейся почки у доноров мужского и женского пола в широком возрастном диапазоне. К трем месяцам остаточный клиренс почки увеличивается до средней СКФ около 65-75% по сравнению с функцией почек до нефрэктомии [27].
-
Рекомендуется исследование общего (клинического) анализа мочи потенциального прижизненного донора почки с целью диагностики нарушений функции почек [28,29,117, 119, 121];
УУР В (УДД – 3).
Комментарии: потенциальные доноры, у которых обнаружена лейкоцитурия, могут быть рекомендованы для донорства только в том случае, если доказано, что лейкоцитурия вызвана обратимой причиной – неосложненная инфекция мочевыводящих путей. Лейкоцитурия определяется как наличие 10 или более лейкоцитов в поле зрения. Стерильная лейкоцитурия определяется как постоянное присутствие лейкоцитов в моче при отсутствии бактерий, встречается относительно часто (13,9% женщин и 2,6% мужчин) и может возникать у пациентов, которые уже принимали противомикробные препараты или в случае инфицирования атипичными микроорганизмами. Причина наличия лейкоцитурии должна быть установлена до того, как потенциальный донор приступит к дальнейшему обследованию [30,31].
-
Рекомендуется исследование определения количества белка в суточной моче у потенциальных прижизненных доноров почки с целью выявления протеинурии [28,29, 117, 120];
УУР B (УДД – 3).
Комментарии: протеинурия должна быть определена количественно у всех потенциальных живых доноров почек. Повышенная экскреция белка с мочой является маркером повреждения почек, отражая либо повышенную проницаемость клубочков (альбуминурия), либо пониженную реабсорбцию в канальцах (низкомолекулярную протеинурию). Протеинурия является важным фактором риска как для хронического заболевания почек [28,29], так и для сердечно-сосудистой патологии и смертности [32].
-
Рекомендуется исследование не менее двух анализов мочи у потенциальных прижизненных доноров почки с целью выявления микрогематурии [33-40, 126];
УУР С (УДД – 5).
Комментарии: микрогематурия является распространенным явлением в общей популяции, может указывать на урологическое или нефрологическое заболевания и должна тщательно оцениваться у будущих живых доноров почки. Если присутствует микрогематурия, выполняются необходимые исследования, чтобы исключить такие этиологические факторы, как инфекция, нефролитиаз и рак [34,35,36]. Стойкая бессимптомная микрогематурия присутствует от 2,7 до 25 % случаев у потенциальных доноров, обследованных в США и Японии [37,38]. Злокачественные новообразования мочевыводящих путей, которые наблюдаются у 3–5% пациентов, в целом редко встречаются в возрасте до 40 лет, но диагностируются у 10% пациентов в возрасте старше 60 лет [39,40]. Вышеизложенное свидетельствует в пользу необходимости исследования на персистирующую микрогематурию у потенциальных доноров почки с целью исключения патологий, которые могут являться противопоказанием к донорству почки.
-
Рекомендуется молекулярно-генетическое исследование крови на вирус гепатита B (Hepatitis B virus), вирус гепатита C (Hepatitis C virus), ВИЧ; определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus), определение антител к вирусу гепатита C (Hepatitis C virus), определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1), определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2), определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови потенциального прижизненного донора почки с целью предотвращения инфицирования реципиента почки [41,42,43];
УУР С (УДД– 5).
Комментарии: при прижизненном донорстве почки руководствуются теми же принципами инфекционной безопасности, что и при посмертном донорстве [41,42].
-
Рекомендовано определение-HLA антигенов (генов) I и II классов реципиенту и донору, проба на совместимость иммунных антител реципиента к антигенам главного комплекса гистосовместимости донора. Рекомендуется рассматривать в качестве прижизненного донора родственника с совместимой группой крови (АВ0) и совпадением по лейкоцитарным антигенам человека (HLA), что создает оптимальные условия для успешной трансплантации [10, 44-55, 127];
УУР В (УДД – 3).
Комментарии: HLA-типирование (определение антигенов (генов) главного комплекса гистосовместимости I и II классов) проводится как реципиентам, так и потенциальным родственным донорам. HLA-типирование реципиента и всех потенциальных живых доноров проводится с использованием молекулярно-генетических методов и/или серологического исследования. Обязательно определяются антигены (гены) 3 локусов: HLA-A, HLA-B (I класс), HLA-DRB1 (II класс). Остальные локусы исследуются по усмотрению конкретного трансплантологического центра. Необходимо определять степень несоответствия между донором и реципиентом. Иммунологическая сенсибилизация потенциального реципиента может произойти в результате воздействия аллогенной ткани, несущей чужеродный главный комплекс гистосовместимости: переливание компонентов крови, беременности (включая выкидыш и прерванную беременность) и предшествующая трансплантация. HLA-специфические антитела могут возникать естественным путем в результате перекрестной реактивности с патогенами. В таком случае они называются идиопатическими антителами. Особое внимание следует уделять донорспецифическим антителам. Предварительная проба на совместимость иммунных антител реципиента к антигенам главного комплекса гистосовместимости донора (реакция кросс-матч) между потенциальным донором и реципиентом проводится для подтверждения наличия или отсутствия донорспецифических антител [48]. Присутствие донорспецифических антител у пациента и/или положительный кросс-матч являются противопоказанием к трансплантации, если не применялся протокол десенсибилизации [49,50]. Анализ более 5000 живых неродственных донорских трансплантаций, проведенный в период между 1995 и 2002 годами, показал значительное влияние соответствия HLA на выживаемость почечного трансплантата, но при этом выживаемость даже при плохой совместимости была лучше, чем при трансплантации почки от посмертного донора [51]. Тем не менее более поздний анализ исходов трансплантации почки от живых доноров, проведенный в период между 2000 и 2007 годами, не показал существенного влияния степени соответствия по системе HLA на исход трансплантации [52].
2.4 Инструментальные диагностические исследования
-
Рекомендуется проводить ультразвуковое исследование органов брюшной полости (комплексное) потенциальному прижизненному родственному донору почки с целью исключения патологии органов брюшной полости, видимой патологии (агенезии, дистопии) почек, нефролитиаза [1,10];
УУР C (УДД –5).
-
Рекомендуется проводить дуплексное сканирование артерий почек, дуплексное сканирование сосудов (артерий и вен) нижних конечностей, дуплексное сканирование сосудов малого таза потенциальному прижизненному родственному донору почки с целью исключения критических стенозов и флотирующих тромбов в сосудах [1,10, 117];
УУР В (УДД –3).
-
Рекомендуется прицельная рентгенография органов грудной клетки потенциальному прижизненному родственному донору почки с целью исключения патологии органов грудной клетки [117, 123];
УУР С (УДД –5).
-
Рекомендуется выполнение ЭКГ потенциальному прижизненному родственному донору почки с целью определения имеющихся очагов ишемии или кардиомиопатии [1,10, 125];
УУР C (УДД – 5).
Комментарии: электрокардиография дополняет клиническую оценку и может указывать на наличие ранее существовавшей ишемической болезни сердца или кардиомиопатии. Последнее важно, так как кардиомиопатии, в частности гипертрофическая кардиомиопатия (частота 1: 500), являются наиболее частой причиной внезапной сердечной смерти у практически здоровых людей [56]. Особое внимание следует уделить наличию патологических зубцов Q (> 25% высоты зубца R), блокады левой ножки пучка Гиса, признаков, характерных для гипертрофии левого желудочка, патологических изменений зубца Т и наджелудочковых аритмий. Любое отклонение от нормы должно быть официально отражено в медицинской документации. Дополнительное обследование должно включать эхокардиографию и заключение врача-кардиолога. Нормальная электрокардиограмма не исключает ишемическую болезнь сердца.
-
Рекомендуется выполнение ЭхоКГ, холтеровского мониторирования сердечного ритма, проведение теста с физической нагрузкой с использованием эргометра потенциального прижизненного родственного донора почки с целью определения функционального резерва сердца. При выявлении признаков ишемии миокарда рекомендовано выполнение коронароангиографии для оценки состояния коронарного русла [1,10, 131];
УУР C (УДД –5).
-
Рекомендуется выполнение компьютерной томографии органов брюшной полости и забрюшинного пространства с внутривенным болюсным контрастированием потенциальному прижизненному родственному донору почки с целью определения сосудистой анатомии почек, аномалий, новообразований почек и нефролитиаза [1, 10, 57-62, 117];
УУР B (УДД – 3).
Комментарий: КТ является ключевым инструментальным исследованием. Поскольку данный вид исследования имеет небольшой, но определенный риск для доноров и является относительно дорогостоящим, чаще всего КТ выполняется после окончательно принятого решения о донорстве [57]. Определение артериальной анатомии очень важно для выбора наиболее подходящей для донорства почки. Предпочтение отдают почке с одной артерией и одной веной, поскольку наличие нескольких сосудов может осложнить формирование сосудистых анастомозов у реципиента. Вариации венозного оттока, такие как удвоенные или ретроаортальные почечные вены или крупные поясничные вены, а также удвоенный мочеточник обычно не рассматриваются как противопоказания для донорства. Важность КТ подчеркивается в нескольких исследованиях для выявления нефролитиаза, особенно при его бессимптомном течении [58-60]. Кроме того, существует вероятность «случайных находок». Хотя выявление значительной патологии у потенциальных доноров невелико, одно исследование с участием 1597 потенциальных доноров показало, что 1195 (74,9%) имели в общей сложности 2105 «случайных находок». При этом частота выявленных новообразований составила 17,3%, а количество подтвержденных злокачественных новообразований при этом 0,1% [61]. В другом исследовании у 175 потенциальных доноров компьютерная томография выявила «потенциально значимое внепочечное образование» в 28% случаев [62].
-
Рекомендуется динамическая сцинтиграфия почек и мочевыделительной системы с функциональными пробами при разнице в размерах почек более 2 см потенциальному прижизненному родственному донору почки поскольку это может свидетельствовать о значимой разнице в функции между двумя почками (более 10%). В таких случаях рекомендовано выполнение радиоизотопного исследования, с целью определения функции каждой почки по отдельности, при этом для нефрэктомии выбирается почка с меньшей функцией, вне зависимости от сосудистой анатомии [63, 128,129].
УУР В (УДД – 3).
-
Рекомендуется УЗИ предстательной железы мужчинам старше 40 лет для исключения онкологической патологии [13,14];
УУР C (УДД – 5).
2.5 Иные диагностические исследования
Доноры с артериальной гипертензией
Артериальная гипертензия является частым и в большинстве случаев нераспознанным симптомом, в общей популяции, как правило, ассоциированным с нарушением функции почек. До недавнего времени повышенное артериальное давление являлось абсолютным противопоказанием к прижизненному донорству. Obrador G. с соавт. [64] предложили следующие принципы селекции прижизненных доноров, имеющих повышенные цифры артериального давления:
-
пациенты, принимающие два и более антигипертензивных средств и с цифрами артериального давления выше 140/90 мм рт. ст., не должны рассматриваться в качестве доноров почки;
-
некоторые пациенты с медикаментозно управляемой артериальной гипертензией, отвечающие определенным критериям (моложе 50 лет, с клиренсом креатинина более 80 мл/мин и суточной экскрецией белка менее 300 мг/сут), могут представлять группу низкого риска по развитию почечной патологии в послеоперационном периоде и рассматриваться в качестве потенциальных доноров почки;
-
после нефрэктомии доноры с артериальной гипертензией должны находиться под постоянным наблюдением врача.
Доноры с высоким индексом массы тела
По принятой классификации ожирение определяется значением показателя ИМТ больше 30 кг/м2. Вопрос о возможности использования доноров с повышенным ИМТ связан прежде всего с техническими трудностями выполнения операции, а также с повышенным риском развития периоперационных осложнений. Ожирение сопровождается проявлениями такой сопутствующей патологии, как гипертензия, сердечно-сосудистые заболевания, гиперлипидемия, диабет, а также неалкогольная жировая болезнь печени.
Трансплантаты, полученные от живых доноров с СКФ менее 80 мл/мин, больше подвержены риску потери по сравнению с трансплантатами от лиц с СКФ более 80 мл/мин. Однако результаты трансплантации от пожилых доноров с СКФ, находящихся в пределах 60-70 мл/мин, вполне удовлетворительны.
Использование пожилых доноров почки
Снижение почечной функции во многом связано с процессом старения. Процент нефросклероза в биоптатах почки выше у пожилых доноров. Возраст донора всегда рассматривался как ограничительный фактор для возможного изъятия органа. Это обсуждалось как при трупной трансплантации, так и, тем более, в случаях использования живого донора почки. Предметом дискуссии являются возможность получения полноценного органа и безопасность выполнения нефрэктомии у пожилого донора. По данным многих исследований, отдаленные результаты трансплантации при использовании пожилых доноров не отличаются от показателей выживаемости почек, полученных от доноров молодого и среднего возраста.
Таким образом, использование почечных трансплантатов от лиц старшего возраста нашло место в современной трансплантологии, однако ограниченные функциональные резервы таких почек могут оказать влияние на показатели отдаленной выживаемости.
Донорство при патологии почек
Достаточно часто при обследовании потенциальных живых доноров почки выявляются различные отклонения от норм, а также заболевания со стороны почек и мочевыводящих путей. Наиболее часто ими оказываются варианты строения почек, удвоения мочеточников, кистозные изменения, пиелонефрит, мочекаменная болезнь и т. д. На фоне современной общемировой тенденции к расширению показаний к прижизненному донорству эти аспекты также находятся в центре внимания. Бессимптомный потенциальный донор с анамнезом уролитиаза может рассматриваться как реальный кандидат при соблюдении следующих условий:
-
отсутствует гиперкальциурия, гиперурикемия или метаболический ацидоз;
-
отсутствует цистинурия или гипероксалурия;
-
нет данных о наличии инфекции мочевых путей;
-
отсутствует визуализация множественных конкрементов или нефрокальциноза при КТ.
Потенциальный донор с выявленным единичным микролитом, не имеющий характерной симптоматики, может быть востребован, если отвечает всем вышеперечисленным критериям, а выявленный камень менее 15 мм в диаметре.
Не должны рассматриваться в качестве доноров лица с мочекаменной болезнью, если имеются:
-
двусторонний нефролитиаз или нефрокальциноз;
-
типы конкрементов с высоким уровнем рецидивирования (например, цистиновые камни);
-
проблемные для удаления камни (например, коралловидные);
-
конкременты, связанные с различной наследственной патологией (первичная или тонкокишечная гипероксалурия);
-
рецидивирующие конкременты.
К встречающимся с различной частотой аномалиям развития почек относят подковообразную почку, S – или L – образные почки, различные варианты удвоения чашечно-лоханочных систем и др. Использование подковообразных почек для трансплантации считается вполне допустимым, так как это также позволяет увеличить число проводимых операций при получении удовлетворительных результатов. Различные варианты кровоснабжения, в основном множественного, часто приводят к увеличению проявлений таких осложнений, как тромбоз, и, несомненно, затрудняют проведение собственно трансплантации. Выполнение подобных операций требует максимально тщательной микрохирургической техники.
Таким образом, на современном этапе развития трансплантации почки с использованием живых доноров имеется возможность увеличения количества проводимых трансплантаций за счет применения персонального комплексного подхода на этапах обследования и предоперационной подготовки донора.
Лечение
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
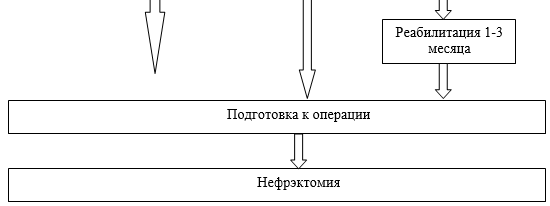
3.1 Предоперационная подготовка
-
Рекомендуется введение антитромботических средств и применение эластической компрессии нижних конечностей потенциальному прижизненному родственному донору почки с целью профилактики тромбообразований [65,66,67];
УУР С (УДД – 5).
Комментарии: тромбоз глубоких вен и тромбоэмболия легочной артерии остаются основными причинами осложнений и смертности в раннем послеоперационном периоде. Следует обратить особое внимание на такие факторы риска, как возраст старше 60 лет, обезвоживание, наличие тромбофилии в анамнезе, ожирение (ИМТ> 30 кг/м2), наличие в анамнезе у родственников первой линии тромбоза глубоких вен, варикозную болезнь вен нижних конечностей в анамнезе, курение, использование заместительной гормональной терапии, применение прогестагенов и эстрогенов (фиксированные сочетания) [66,67].
-
Рекомендовано однократное введение антибактериального препарата системного действия за 1 час до кожного разреза прижизненному родственному донору почки в качестве периоперационной антибиотикопрофилактики [70-74];
УУР С (УДД – 5).
Комментарий: в качестве оптимального препарата рекомендованы цефалоспорины I-II поколения в связи с безопасностью, экономичностью, при этом они обладают достаточным антимикробным спектром против наиболее вероятных возбудителей раневой инфекции (стафилококки и стрептококки) [68,69,70]. Многоцентровое проспективное рандомизированное контролируемое испытание не продемонстрировало разницы в частоте бактериальной, грибковой или вирусной инфекции в зоне хирургического вмешательства в течение одного месяца у реципиентов, получивших разовую дозу антибиотика широкого спектра действия при индукции анестезии, по сравнению с получившими антибиотик каждые 12 часов в течение 3-5 дней [71,72].
-
Рекомендуется предоперационная гидратация с инфузией в течение 2-4 часов до операции и/или болюсом во время операции прижизненному родственному донору почки, что улучшит гемодинамическую стабильность во время оперативного вмешательства [73,74,75];
УУР А (УДД – 1).
3.2 Хирургическое лечение
-
Рекомендуется использование лапароскопической или мануально-ассистированной чрезбрюшинной лапароскопической нефрэктомии у живого донора [76-81];
УУР А (УДД– 1).
Комментарии: эндоскопический (лапароскопический) подход является предпочтительным методом нефрэктомии у живого донора [78,80,81,82,83]. К преимуществам лапароскопического доступа относятся: минимальная потребность в обезболивании, более короткое время госпитализации, быстрое послеоперационное восстановление, уменьшение сроков временной нетрудоспособности, а также хирургический доступ, имеющий хороший косметический эффект. Стандартная ЛДНЭ обычно выполняется через порты 5 и 12 мм, но также может быть выполнена с портами 3 или 3,5 мм [82].
Одним из способов увеличения безопасности ЛДНЭ является использование лапароскопической техники с мануальным ассистированием (hand-assistant laparoscopic technique). Особенностью метода является введение руки хирурга в брюшную полость (или забрюшинно) через мини-доступ с использованием специального порта. Этот метод имеет определенные преимущества по сравнению со стандартной ЛДНЭ: уменьшение времени первичной тепловой ишемии почки, снижение риска развития кровотечений, более короткое время операции, уменьшение частоты урологических осложнений, возможность забора почки забрюшинно. Эндоскопическая техника с мануальной ассистенцией позволяет выполнить быстрое и атравматичное удаление почки. В случае развития интраоперационных осложнений, прежде всего массивного кровотечения, операция может быть быстро остановлена и переведена в открытое вмешательство.
Согласно проведенному недавно систематическому обзору, ЛДНЭ у живого донора также может быть выполнена с помощью роботизированной техники, с аналогичными результатами [83,84]. Однопортовая лапаро-эндоскопическая нефрэктомия позволяет хирургу работать через один разрез (обычно пупок) с многоходовым портом. Этот же или отдельный разрез может быть использован для извлечения почки. Несколько ретроспективных и по крайней мере три проспективных рандомизированных исследования продемонстрировали аналогичную безопасность и результаты с тенденцией к уменьшению боли и улучшению косметических результатов [85]. Однако операция, выполненная через однопортовый доступ, считается технически более сложной по сравнению с классической ЛДНЭ у живого донора, и ее роль еще предстоит определить.
Использование естественного отверстия для извлечения почки (например, трансвагинального доступа) позволяет избежать лапаротомии для извлечения почки, чем достигается лучший косметический эффект. Первоначальные отчеты предполагают, что такой подход безопасен, однако опыт применения этой методики все еще весьма ограничен [86].
-
В центрах, где эндоскопические методы не применяются, у живого родственного донора рекомендовано выполнять открытую нефрэктомию [77,79-81];
УУР А (УДД – 1).
-
Рекомендуется принимать решение об использовании почки от живого родственного донора индивидуально в рамках дооперационной оценки донора и реципиента при наличии множественных почечных артерий или почки с анатомическими аномалиями [87,88];
УУР С (УДД – 4).
Комментарии: проведенный анализ анатомии почечных сосудов у потенциальных доноров показал, что приблизительно у 25 % доноров будет несколько артерий у одной из почек, и около 7 % будут иметь несколько сосудов у обеих почек. Если у обеих почек одинаковое количество сосудов, рекомендовано выполнять донорскую нефрэктомию слева, в связи с более длинной почечной веной. Согласно результатам исследований, множественные почечные артерии ассоциировались с повышенной частотой осложнений у реципиента, но они не оказывают отрицательного влияния на выживаемость пациента или трансплантата [76,81]. Использование почек с анатомическими аномалиями в настоящее время считается только относительным противопоказанием к донорству большинством опытных центров трансплантации. Соответствующие анатомические аномалии могут включать почечные кисты, одиночные камни <1 см, удвоение мочеточников и множественные артерии и вены [87,88].
-
Рекомендуется выбирать донорскую почку с одной почечной артерией для трансплантации, с целью минимизации риска сосудистых осложнений на этапе формирования сосудистых анастомозов [87,88].
УУР С (УДД – 4).
Комментарии: данное утверждение также справедливо в отношении почечных вен.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1. Интраоперационные осложнения и осложнения раннего послеоперационного периода
Нефрэктомия у прижизненных доноров, как и любое другое вмешательство, связано с возможными осложнениями и рисками. Однако тот факт, что операция проводится на здоровом пациенте, усиливает значимость любых осложнений. Перечень возможных осложнений должен быть включен в информированное согласие. Согласно официальным данным, операционная смертность составляет от 0,01% до 0,03% вне зависимости от хирургической техники или состояния донора. В недавно проведенном систематическом обзоре по осложнениям малоинвазивной ЛДНЭ (190 исследований) и мета-анализе (41 исследование) описано 32308 ЛДНЭ. Частота интраоперационных осложнений среди них составила 2,2% (самыми частыми осложнениями являлись кровотечение (1,5% случаев) и повреждение других органов (0,8% случаев), а послеоперационные осложнения возникали в 7% (в 2,6% случаев – инфекционные осложнения, а в 1% случаев – кровотечение). Частота конверсии доступа составила 1,1%, в половине случаев в связи с кровотечением, а в другой половине случаев в связи с повреждением других органов. Частота ревизий составила 0,6%, в большинстве случаев с целью выполнения гемостаза или эвакуации гематомы [109,110].
7.2. Осложнения в отдаленном послеоперационном периоде
Чаще всего отдаленные осложнения связаны с оставшейся почкой. Почечная функция снижается непосредственно после нефрэктомии, а затем улучшается на несколько лет. Однако в отдаленном послеоперационном периоде имеются признаки истощения функционального резерва [111,112]. Несмотря на стойкое увеличение частоты возникновения протеинурии и артериальной гипертензии, частота возникновения хронической болезни почек 5 стадии (0.4-1.1%) не отличается от популяции в целом [113,114]. Риск гибели донора в отдаленном послеоперационном периоде не отличается от такового у населения соответствующего возраста и сопутствующей патологии [110,113].
Медицинская реабилитация
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
4.1. Общие вопросы реабилитации после донорства почки
После донорства почки большинство людей могут вернуться к нормальной повседневной деятельности через две-четыре недели. Последующее наблюдение после донорства почки должно быть сосредоточено на мониторинге и поддержании общего здоровья и здоровья почек, включая ведение здорового образа жизни (например, питания, поддержания веса, регулярных аэробных упражнений), предотвращение потенциально нефротоксичных воздействий (например, употребление табака, нестероидных противовоспалительных препаратов, нефротоксических препаратов), профилактика заболеваний, которые могут вызвать ХБП (например, гипертонии, сахарного диабета, ССЗ), и своевременное лечение таких заболеваний, если они развиваются после донорства почки. Гипертония чаще диагностируется у доноров почек, чем у людей с сопоставимым исходным состоянием здоровья, хотя это может частично отражать более тщательный мониторинг и раннее выявление [89,90].
Раннее выявление и лечение заболеваний, которые потенциально влияют на снижение СКФ, могут защитить донора от дальнейшего ухудшения почечной функции или другого ухудшения здоровья.
Не реже одного раза в год после донорства почки должны выполняться следующие измерения:
- измерение артериального давления;
- измерение ИМТ;
- измерение уровня креатинина в сыворотке крови с оценкой СКФ;
- измерение уровня альбумина в моче.
Необходимо проводить пропаганду здорового образа жизни, включая регулярные упражнения, здоровое питание и воздержание от табакокурения.
4.2. Репродуктивное здоровье у доноров почки
Донорство почки обычно не влияет на возможность забеременеть или иметь нормальное родоразрешение. Некоторые исследования показывают, что у доноров почек может быть небольшое повышение риска осложнений беременности, таких как гестационный диабет, гипертензия, вызванная беременностью, преэклампсия и наличие белка в моче. Обычно женщинам рекомендуется подождать от шести месяцев до года после донорства почки, прежде чем забеременеть [91–98].
Госпитализация
6. Организация оказания медицинской помощи
Госпитализация потенциальных доноров почки производится в плановом порядке после клинического обследования, принятия решения о выполнении операции всеми участниками процесса или необходимости проведения дополнительного обследования в условиях стационара. Условиями для операции являются: нахождение с реципиентом в генетической связи; наличие протоколов врачебной комиссии медицинской организации о необходимости трансплантации почки реципиенту и о возможности нефрэктомии у потенциального донора с указанием, что его здоровью не будет причинен значительный вред.
Показания для плановой госпитализации:
- желание потенциального донора, изложенное в форме добровольного информированного согласия на обследование в качестве прижизненного донора почки, в произвольной форме.
Показания к выписке пациента из стационара:
- отсутствие ранних послеоперационных осложнений, могущих повлиять на здоровье пациента;
- удовлетворительная функция оставшейся почки;
- удовлетворительный психоэмоциональный статус донора почки;
- наличие четких рекомендаций в эпикризе для дальнейшего наблюдения пациента.
Профилактика
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Во время обследования и предоперационной подготовки рекомендуется сообщать потенциальным донорам о том, что общий риск развития ХБП может увеличиваться после донорства почки [99-105];
УУР С (УДД – 4).
Комментарии: во время беседы с донором следует сообщить о факторах, которые могут увеличить риск развития ХБП, такие как возраст, пол, раса, ИМТ и семейный анамнез. Непрерывный успех прижизненного донорства зависит от обеспечения безопасности и отличных долгосрочных результатов здоровья донора. В частности, доноры должны быть уверены, что риск развития прогрессирующей ХБП и преждевременной сердечно-сосудистой смерти остается низким после нефрэктомии. Исследования в Швеции [99,100] и США [101-103] показали, что продолжительность жизни остается большей, а риск развития ХБП остается ниже в когортах доноров по сравнению с населением в целом. Хотя благоприятные результаты у доноров по сравнению с общей популяцией обнадеживают, такие исследования не могут определить, увеличивает ли донорская нефрэктомия риск неблагоприятных результатов по сравнению с риском перед донорством. Для этого потребовалась бы контрольная группа из тех, кто был бы оценен как потенциальный донор, но так им и не стал. В двух исследованиях [103,105] сравнивались доноры с контролем «здоровых недоноров» в попытке решить этот вопрос. Muzaale и соавторы сообщили о долгосрочном наблюдении 96217 человек, ставших донорами, в США в период с 1994 по 2011 год, и сравнили результаты с контрольной группой из 20 024 участников исследования NHANES III. Медиана наблюдения составила 7,6 года для доноров и 15 лет для сопоставимых здоровых не доноров. ХБП развилась у 99 доноров почек в среднем через 8,6 года после нефрэктомии по сравнению с 36 не донорами. Предполагаемый риск развития ХБП через 15 лет после донорства составил 30,8 на 10 000 для доноров и 3,9 на 10 000 в контрольной группе (р <0,001). Риск развития ХБП был оценен как 14 на 10 000 не доноров, 90 на 10 000 доноров и 326 на 10 000 населения США в целом. Те же авторы ранее сообщали, что риск долгосрочной смертности не был повышен у доноров по сравнению с контрольной группой.
- Рекомендуется выполнение общего (клинического) анализа мочи, общего (клинического) анализа крови (количество эритроцитов, тромбоцитов, лейкоцитов, уровень гемоглобина), анализа крови биохимического общетерапевтического (исследование общего белка, альбумина, креатинина, мочевины, аспартатаминотрансферазы, аланинаминотрансферазы), оценка коагулограммы (ориентировочное исследование системы гемостаза) (уровень фибриногена, антитромбина-III, плазминогена, протромбиновый индекс, АЧТВ), физикальное и инструментальное (ультразвуковое исследование ложа удаленной почки) обследование прижизненному родственному донору в раннем послеоперационном периоде (1, 3, 5 сутки) для выявления всех возможных отклонений в состоянии здоровья [1, 106-108];
УУР С (УДД – 5).
Комментарии: дополнительные осмотры, контроль анализов проводятся по показаниям.
- Рекомендуется ежегодное диспансерное наблюдение прижизненного родственного донора врачом-терапевтом, врачом-урологом по месту жительства для выявления всех возможных отклонений в состоянии здоровья [106-108];
УУР C (УДД – 5).
Комментарии: дополнительные осмотры, контроль анализов проводятся по показаниям.
- Рекомендуется информировать женщин о потенциальном повышенном риске гипертонии, вызванной беременностью после донорства почек, что может потребовать специализированной дородовой помощи [91–98, 130].
УУР В (УДД – 3).
Информация
Источники и литература
-
Клинические рекомендации Российского трансплантологического общества
- Данович ГМ. Трансплантация почки. М: ГЭОТАР-Медиа; 2013: 848.
Федеральный закон от 21.11.2011 N 323-ФЗ (ред. от 29.05.2019) «Об основах охраны здоровья граждан в Российской Федерации». Статья 47. Донорство органов и тканей человека и их трансплантация (пересадка).
Fresenius medical care annual report 2018; 2018.
Андрусев АМ, Томилина НА, Перегудова НГ, Шинкарев МБ. 3аместительная терапия терминальной хронической почечной недостаточности в Российской Федерации 2014-2018 гг. Отчет по данным Общероссийского Регистра заместительной почечной терапии Российского диализного общества; 2019.
Готье СВ, Хомяков СМ. Донорство и трансплантация органов в Российской Федерации в 2019 году. XII сообщение регистра Российского трансплантологического общества. Вестник трансплантологии и искусственных органов. 2020; 22(2): 8-34.
Закон РФ от 22.12.1992 N 4180-1 ред. от 29.11.2007 «О трансплантации органов и (или) тканей человека».
Englum BR, Schechter MA, Irish WD, et al. Outcomes in kidney transplant recipients from older living donors. Transplantation 2015; 99: 309-15.
Oien CM, Reisæter AV, Leivestad T, Dekker FW, Line PD, Os I. Living donor kidney transplantation: the effects of donor age and gender on short- and longterm outcomes. Transplantation 2007; 83: 600-6.
Hawley CM, Kearsley J, Campbell SB, et al. Estimated donor glomerular filtration rate is the most important donor characteristic predicting graft function in recipients of kidneys from live donors. Transpl Int 2007; 20: 64-72.
KDIGO Clinical Practice Guideline on the Evaluation and Care of Living Kidney Donors. Transplantation. 2017; 101, N8S-1: 1–106.
Thiessen C, Gordon EJ, Reese PP, et al. Development of a donor- centered approach to risk assessment: rebalancing nonmaleficence and autonomy. Am J Transplant. 2015; 15: 2314–2323.
Delmonico F, Council of the Transplantation Society. A report of the Amsterdam forum on the care of the live kidney donor: data and medical guidelines. Transplantation. 2005; 79 (6 Suppl): S53–S66.
British Transplantation Society / Renal Association UK Guidelines for Living Donor Kidney Transplantation 2018. https://bts.org.uk/wp-content/uploads/2018/07/FINAL_LDKT-guidelines_June-2018.pdf
ОPTN (Organ Procurement and Transplantation Network)/UNOS (United Network for Organ Sharing). OPTN Policies, Policy 14: Living Donation. http://optn.transplant.hrsa.gov/governance/policies/. (Accessed: June 28, 2017).
Cancer Research UK: Cancer Incidence by Age: 2012-2014. http://www.cancerresearchuk.org/health-professional/cancer-statistics/incidence/age — heading-Zero.
Fehrman-Ekholm I, Gabel H, Magnusson G. Reasons for not accepting living kidney donors. Transplantation 1996; 61: 1264-5.
Young A, Karpinski M, Treleaven D, et al. Differences in tolerance for health risk to the living donor among potential donors, recipients, and transplant professionals. Kidney Int 2008; 73: 1159-66.
International Diabetes Federation: Definition and diagnosis of diabetes mellitus and intermediate hyperglycaemia. World Health Organisation (WHO); 2006.
Tydén G, Kumlien G, Berg UB. ABO-incompatible kidney transplantation in children. Pediatr Transplant. 2011; 15(5): 502-4.
Hourmant M, Figueres L, Gicquel A, et al. New rules of ABO-compatibility in kidney transplantation. Transfus Clin Biol. 2019; 26(3): 180-183.
Shaw C, Sharp CC. Could sickle cell trait be a predisposing risk factor for CKD? Nephrol Dial Transplant 2010; 25: 2403-5.
RP Naik, VK Derebail, ME Grams, et al. Association of sickle cell trait with chronic kidney disease and albuminuria in African Americans. JAMA 2014; 312: 2115-25.
Reese PP, Hoo AC, Magee CC. Screening for sickle trait among potential live kidney donors: policies and practices in US transplant centers. Transpl Int 2008; 21: 328-31.
Cetin T, Oktenli C, Ozgurtas T, et al. Renal tubular dysfunction in betathalassemia minor. Am J Kidney Dis 2003; 42: 1164-8.
Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО). Флебология, 2015; 9 (2): 4-46.
Douketis JD, Spyropoulos AC, Spencer FA, et al. Perioperative management of antithrombotic therapy: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2 Suppl): e326-50.
Fenton A., Montgomery E., Nightingale P., Peters A.M., Sheerin N., Wroe A.C., Lipkin G.W. Glomerular filtration rate: new age- and gender- specific reference ranges and thresholds for living kidney donation. BMC Nephrol. 2018; 19: 336. doi: 10.1186/s12882-018-1126-8.
Iseki K, Ikemiya Y, Iseki C, Takishita S. Proteinuria and the risk of developing end-stage renal disease. Kidney Int 2003; 63: 1468-74.
Halbesma N, Kuiken DS, Brantsma AH, et al. Macroalbuminuria is a better risk marker than low estimated GFR to identify individuals at risk for accelerated GFR loss in population screening. J Am Soc Nephrol 2006; 17: 2582-90.
Horan TC, Andrus M, Dudeck MA. CDC/NHSN surveillance definition of healthcare-associated infection and criteria for specific types of infections in the acute care setting. Am J Infect Control 2008; 36: 309-32.
Wise GJ, Schlegel PN. Sterile pyuria. N Engl J Med 2015; 372: 1048-54.
Matsushita K, van der Velde M, Astor BC, et al. Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts: a collaborative meta-analysis. Lancet 2010; 375: 2073-81.
AUA Guidelines 2020: Microhematuria. https://www.urotoday.com/conference-highlights/aua-2020/aua-2020-bladder-health/122536-aua-guidelines-2020-microhematuria.html
Mohr DN, Offord KP, Owen RA, Melton LJ. Asymptomatic microhematuria andurologic disease: a population based study. JAMA 1986; 256: 224-9.
Vivante A, Afek A, Frenkel-Nir Y, et al. Persistent asymptomatic isolated microscopic hematuria in Israeli adolescents and young adults and risk for endstage renal disease. JAMA 2011; 306: 729-36.
Yamagata K, Kobayashi M, Koyama A. A long-term follow up study of asymptomatic haematuria and/or proteinuria in adults. Clin Nephrol 1996; 45: 281-8.
Jaffe JS, Ginsberg PC, Gill R, Harkaway RC. A new diagnostic algorithm for the evaluation of microscopic haematuria. Urology 2001; 57: 889-94.
Koushik R, Garvey C, Manivel C, Matas AJ, Kasiske B. Persistent, asymptomatic microscopic hematuria in prospective kidney donors. Transplantation 2005; 80: 1425-9.
Khadra MH, Pickard RS, Charlton M, Powell PH, Neal DE. A prospective analysis of 1,930 patients with haematuria to evaluate current diagnostic practice. J Urol 2000; 163: 524-7.
Edwards TJ, Dickinson AJ, Natale S, Gosling J, McGrath JS. A prospective analysis of the diagnostic yield resulting from the attendance of 4020 patients at a protocol-driven haematuria clinic. BJU Int 2006; 97: 301-5.
Постановление Правительства РФ от 22.06.2019 N 797 «Об утверждении Правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов и о признании утратившими силу некоторых актов Правительства Российской Федерации».
Guidance on microbiological safety of human organs, tissues and cells used in transplantation. Advisory Committee on the Safety of Blood Tissues and Organs (SaBTO); 2018.
Van Son WJ, The TH. Cytomegalovirus infection after organ transplantation: an update with special emphasis on renal transplantation. Transpl Int 1989; 2: 147-64.
Cook RI, Wreathall J, Smith A, et al. Probabilistic risk assessment of accidental ABO-incompatible thoracic organ transplantation before and after 2003. Transplantation. 2007; 84: 1602–1609.
Montgomery JR, Berger JC, Warren DS, et al. Outcomes of ABO- incompatible kidney transplantation in the United States. Transplantation. 2012; 93: 603–609.
- Данович ГМ. Трансплантация почки. М: ГЭОТАР-Медиа; 2013: 848.
Информация
Список сокращений
АД – артериальное давление
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
ВИЧ – вирус иммунодефицита человека
ВОЗ – Всемирная организация здравоохранения
ГГТП – гамма-глютамилтранспептидаза
ДНК (DNA) – дезоксирибонуклеиновая кислота
ЗПТ – заместительная почечная терапия
ИМТ – индекс массы тела
ЛДНЭ – лапароскопическая донорская нефрэктомия
КТ –компьютерная томография
ПСА – простатспецифический антиген
ПЦР – полимеразная цепная реакция
СКФ – скорость клубочковой фильтрации
УЗИ – ультразвуковое исследование
ХБП – хроническая болезнь почек
ХПН – хроническая почечная недостаточность
ЦМВ (CMV) – цитомегаловирус
ЭБВ – вирус Эпштейна-Барр
ЭКГ – электрокардиография
ЭхоКГ – эхокардиографическое исследование
Hb – гемоглобин
HBV – вирус гепатита В
HCV – вирус гепатита С
HLA – (англ., human leukocyte antigen, лейкоцитарные антигены человека) главный комплекс гистосовместимости человека
IgG – иммуноглобулин G
IgM – иммуноглобулин M
Трансплантация почки – это хирургическая операция: метод заместительной почечной терапии, заключающийся в пересадке человеку почки, полученной от другого человека.
Живой родственный донор – это лицо, прошедшее обследование и признанное пригодным к нефрэктомии с целью последующей пересадки, находящееся в генетической связи с реципиентом и давшее информированное добровольное согласие на удаление одной из почек с целью последующей трансплантации реципиенту.
Прижизненное донорство – это процесс, направленный на получение органа от живого донора, пригодного для последующей трансплантации реципиенту.
Реципиент трансплантированной почки – это пациент, которому проводится оказание медицинской помощи методом трансплантации почки.
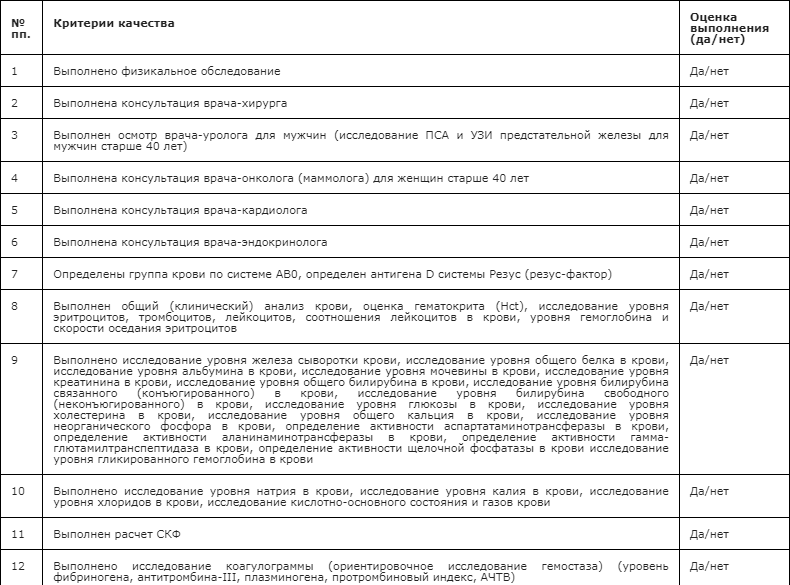
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Конфликт интересов.
Рабочая группа заявляет об отсутствии конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
-
врачи-акушеры-гинекологи;
-
врачи-анестезиологи-реаниматологи;
-
врачи-кардиологи;
-
врачи-нефрологи;
-
врачи общей практики (семейные врачи);
-
врачи организаторы здравоохранения;
-
врачи-терапевты;
-
врачи-урологи;
-
врачи-хирурги;
-
врачи-эндокринологи.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Трансплантация органов, одно из чудес двадцатого века, продолжает спасать и улучшать жизни сотен тысяч пациентов по всему миру. Великие научные открытия и клинические успехи трансплантологов, так же как и бесчисленные акты благородства со стороны доноров органов и их семей, сделали трансплантацию не только видом медицины, спасающим жизнь, но и сияющим символом человеческой солидарности.
Но эти достижения омрачаются множеством сообщений об использовании бедных людей в качестве источника донорских органов и о богатых пациентах-туристах, пересекающих границы для поиска и покупки органов.
В 2004 году Всемирная организация здравоохранения призвала государства, участников организации, «принять меры для защиты беднейших и уязвимых групп населения от трансплантационного туризма и продажи органов и тканей, принимая во внимание широкое распространение международной торговли органами и тканями» (1).
Ввиду неотложного характера проблем, вызванных растущим трансплантационным туризмом и незаконным оборотом донорских органов на фоне глобального их дефицита, с 30 апреля по 2 мая 2008 года в Стамбуле состоялся представительный митинг (Стамбульский Саммит), который объединил более 150 представителей правительственных и медицинских организаций, общественных деятелей, философов и социологов, научных и медицинских сообществ всего мира.
Подготовительная работа была проведена Руководящим Комитетом, который был создан Трансплантационном Обществом (TTS) и Международным обществом нефрологии (ISN) в Дубаи, в декабре 2007 года. Комитет подготовил проект Декларации, который широко обсуждался и пересматривался в свете полученных замечаний. На Саммите этот документ был рассмотрен в рабочих группах и представлен к окончательному утверждению.
Эта Декларация выражает единую точку зрения участников Саммита: всем странам необходимы правовая и профессиональная базы для управления процессами донорства и трансплантации органов, так же как и надзорная система, гарантирующая безопасность донора и реципиента, соблюдение стандартов и запрещение деятельности, противоречащей этическим принципам. Нежелательные действия, противоречащие этике в области трансплантации, могут быть обусловлены, в частности, последствиями глобального дефицита донорских органов. Таким образом, каждая страна должна гарантировать развитие и осуществление программ, предупреждающих дефицит донорских органов, и обеспечивать своим гражданам предоставление донорских органов для трансплантации в пределах своего населения или за счет региональной кооперации.
Терапевтический потенциал посмертного донорства должен быть расширен не только за счет почек, но также и за счет других органов, в соответствии с возможностями каждой страны. Для того чтобы минимизировать использование живых доноров, жизненно необходимыми являются усилия по инициации или улучшению посмертного донорства. Для преодоления недоверия и барьеров, неправильных представлений, мешающих в настоящее время развитию эффективного посмертного донорства, для трансплантации необходимы образовательные программы. Успешные трансплантации возможны только при существовании соответствующей инфраструктуры здравоохранения.
Право на медицинскую помощь является неотъемлемым правом человека, но часто далеким от реальности. Предоставление медицинской помощи для живых доноров органов перед, во время и после операции, как предписывается решениями международных форумов, организованных TTS в Амстердаме и Ванкувере (2-4), является не менее важным, чем лечение реципиентов. Благоприятный исход у реципиента не может оправдать вред, который может быть нанесен живому донору, и трансплантация с использованием прижизненного донорства может расцениваться как успешная, только если и реципиент, и донор в равной мере здоровы после выполненных операций.
Эта Декларация построена на принципах Всеобщей Декларации Прав Человека. Широкое представительство на Стамбульском Саммите отражает важность глобального консенсуса в совместной международной работе для улучшения практики донорства и трансплантации. Декларация будет представлена на рассмотрение соответствующим профессиональным организациям и правительственным медицинским органам. Наследием трансплантологии должно стать торжество дарения жизни одним человеком другому, а не наличие обездоленных жертв незаконного оборота органов и трансплантационного туризма.
Торговля органами — это наем, вербовка, транспортировка и перемещение живых и умерших людей, или их органов, их укрывательство и подделка документов, с применением угроз, силы, служебного положения или других форм принуждения, похищения, мошенничества и обмана; с передачей или получением третьей стороной оплаты или других выгод, для приобретения контроля над потенциальным донором, — для использования в целях получения органов для трансплантации (6).
Трансплантационный коммерциализм – это такая практика и образ действий, при которых орган рассматривается как товар и продукт потребления, который может быть продан, куплен или использован для получения материальной выгоды.
Поездка для выполнения трансплантации – это передвижение органов, доноров и реципиентов или трансплантологов для выполнения операции пересадки, несмотря на юридические ограничения.
Поездка для выполнения трансплантации становится трансплантационным туризмом, если при этом обнаруживается трансплантационный коммерциализм, торговля органами или если компоненты и участники (органы, врачи, трансплантационные центры), участвующие в обеспечении операций пациенту из-за рубежа, подрывают тем самым способность страны к обеспечению трансплантационной помощью собственного населения.
1. Национальные правительства, работающие в соответствии с международными нормами и сотрудничающие с международными и неправительственными организациями, должны развивать и выполнять программы скрининга, предупреждения и лечения заболеваний, приводящих к терминальной недостаточности органов, что должно включать:
а) Развитие клинических и научных исследований;
б) Развитие эффективных программ лечения пациентов с терминальными стадиями заболевания органов, таких как диализ и трансплантация, для сокращения заболеваемости и летальности, в соответствии с международными нормативами;
в) Развитие трансплантации органов как предпочтительного метода лечения для пациентов, не имеющих медицинских противопоказаний.
2. Законодательство каждой страны должно быть разработано в соответствии с международными стандартами и применяться для урегулирования прижизненного и посмертного донорства и трансплантации органов.
а) Должна быть организована и принята такая система донорства и трансплантации, которая обеспечивала бы максимально полное обеспечение органами пациентов, нуждающихся в трансплантации;
б) Практика донорства и трансплантации требует развитых институтов контроля со стороны правительственных медицинских организаций для обеспечения их ответственности и открытости данных;
в) Система контроля предполагает наличие национального регистра для учета прижизненного и посмертного донорства;
г) Ключевыми моментами эффективной программы трансплантации органов и тканей являются просвещение общественности, образование и тренинг медицинского персонала, определение ответственности, обязанностей и отчетности всех участников национальной системы донорства и трансплантации.
3. Органы для трансплантации должны справедливо и беспристрастно распределяться внутри стран и регионов вне зависимости от пола, этнической и религиозной принадлежности, финансового и социального статуса.
а) Финансовые факторы или любая другая материальная выгода не должны влиять на применение правил распределения органов.
4. Первичной целью трансплантации должна быть оптимальная первичная и долгосрочная медицинская помощь для обеспечения здоровья и донора, и реципиента.
а) Финансовые факторы или любая другая материальная выгода не должны влиять на принятие решения относительно здоровья и самочувствия донора и реципиента.
5. Страны, регионы и сопредельные области должны пытаться достигнуть самообеспечения в органном донорстве, обеспечивая достаточное количество органов для своих жителей, используя также региональную кооперацию.
а) Сотрудничество в области органного донорства между странами не противоречит национальным программам по самообеспечению достаточного уровня донорства для своих жителей и предполагает в тоже время защиту уязвимых слоев населения и равенство интересов между донорами и реципиентами, и не нарушает этих принципов;
б) Лечение пациентов из-за рубежа, граждан других государств приемлемо только в том случае, если это не приводит к ухудшению способности страны оказывать трансплантологическую помощь своему собственному населению.
6. Торговля органами и трансплантационный туризм попирают принципы справедливости, равенства и уважения к человеческому достоинству и должны быть запрещены. Трансплантационный коммерциализм избирает своей мишенью обездоленных и уязвимых доноров, что неизбежно ведет к неравенству и несправедливости, и поэтому должен быть запрещен. Резолюция Всемирной Ассамблеи Здравоохранения 44.25 призывает страны препятствовать покупке и продаже донорских органов для трансплантации.
а) Запрещение этих форм деятельности должно означать запрещение всех форм рекламы (включая электронные и печатные средства массовой информации), всех форм ходатайства и посредничества, имеющих целью трансплантационный коммерциализм, трансплантационный туризм и куплю-продажу органов.
б) Такое запрещение должно включать также наказание за такие мероприятия, как обследование доноров и выполнение трансплантаций, равно как и поощрение этих действий, если целью и результатом их является получение выгод от трансплантационного туризма и торговли органами.
в) Деятельность, которая склоняет уязвимых людей или целые их группы (неграмотные, обездоленные, бездомные, нелегальные иммигранты, заключенные, политические или экономические беженцы) к тому, чтобы быть живыми донорами органов, несовместима с противостоянием торговле органами, трансплантационному туризму и коммерциализму.
Следуя этим принципам, участники Стамбульского Саммита предлагают следующие направления для увеличения донорского пула и предотвращения торговли органами, трансплантационного коммерциализма и трансплантационного туризма и для поддержки легитимных, жизнеспасающих трансплантационных программ.
Для необходимости увеличения эффективности посмертного донорства:
1. Правительства, в сотрудничестве с институтами здравоохранения, неправительственными и профессиональными организациями должны предпринять соответствующие действия для увеличения эффективности посмертного донорства. Должны быть приняты меры для устранения препятствий и ограничений.
2. В странах, в которых не развито посмертное донорство или трансплантация, должно быть разработано национальное законодательство, которое бы инициировало развитие такого вида донорства и создавало бы трансплантационную инфраструктуру для наиболее полного использования донорского потенциала таких стран.
3. Во всех странах, в которых существует посмертное органное донорство, терапевтический потенциал этого вида донорства для трансплантации должен быть использован максимально.
4. Страны, в которых посмертное органное донорство существенно развито, должны поддерживать своим опытом, информацией, экспертными оценками и технологией те страны, которые предпринимают попытки улучшить донорство.
Для борьбы с трансплантационным туризмом, трансплантационным коммерциализмом и торговлей органами; для гарантии защиты и безопасности живых доноров и признания их героических поступков должно быть следующее:
1. Представителями правительственных организаций и общественности донорство должно рассматриваться как героический и достойный уважения акт.
2. Медицинская и психосоциальная пригодность живых доноров должна определяться рекомендациями Амстердамского и Ванкуверских форумов (2-4).
а) Механизмы получения информированного согласия должны включать оценку понимания донором предстоящей операции, так же как и оценку психосоциального влияния операции на донора.
б) В ходе обследования у доноров должны быть исключены нарушения в психоэмоциональной сфере с помощью соответствующих специалистов.
3. Для всех тех, кто разрешает трансплантационную практику и принимает в ней участие, обеспечение медицинской помощи донорам органов, даже если они стали жертвами трансплантационных туризма, коммерциализма и торговли органами, является неотъемлемой частью профессиональной ответственности.
4. Структура и система трансплантации и донорства должны гарантировать стандартные подходы, прозрачность отчетов, а также ответственность за поддержку донорства.
а) Должны быть представлены механизмы отчетности и контроля движения донорских органов.
б) Информированное согласие должно получаться как для донорской операции, так и для последующего наблюдения донора.
5. Обеспечение при донорстве включает медицинскую и психосоциальную помощь во время осуществления собственно донорства и на любом этапе после него, при возникновении проблем, так или иначе связанных с донорством органа.
а) В странах, где нет универсального медицинского страхования, необходимым требованием является обеспечение страхования жизни, здоровья, инвалидизации в связи с событием донорства;
б) В тех странах, где есть универсальное медицинское страхование, правительственные службы должны гарантировать доступ к соответствующей медицинской помощи в связи с событием донорства;
в) Для тех, кто жертвует донорский орган, не должно быть препятствий в возможности трудоустройства и страхования жизни и/или здоровья;
г) Всем донорам должна быть предложена психосоциальная помощь как компонент послеоперационного наблюдения;
д) В случае развития органной недостаточности у донора, последний должен быть обеспечен:
i. Поддерживающей терапией, включая диализ для пациентов с почечной недостаточностью, и
ii. Приоритет при распределении трансплантатов как от живых, так и от посмертных доноров, что должно быть интегрировано в существующие правила аллокации.
6. Полная компенсация за акт состоявшегося донорства не должна рассматриваться как оплата за орган, но скорее как компенсация за лечение реципиента.
а) такое восполнение стоимости затрат может осуществляться стороной, ответственной за расходы по лечению реципиента (правительственные органы здравоохранения, страховые компании);
б) расчет стоимости затрат должен выполняться с использованием прозрачной методологии, соответствующей национальным нормам;
в) компенсация в размере утвержденной суммы должна производиться напрямую стационару (госпиталю), обеспечивающему лечение донора;
г) компенсация за понесенные убытки и утраченный доход донора должна осуществляться учреждением, обеспечивающим трансплантацию, а не напрямую от реципиента к донору.
7. Выплаты, связанные с документированным актом донорства, включают также:
а) стоимость психосоциального и медицинского обследований потенциального живого донора, который не стал таковым в силу медицинских, иммунологических проблем, выявленных в ходе обследования;
б) стоимость организационных затрат, вытекающих из подготовки и осуществления процесса донорства (до, после и во время операции) и на всех этапах (междугородние телефонные переговоры, затраты на транспорт, размещение и продовольственное обеспечение);
в) медицинские затраты, связанные с лечением донора после выписки;
г) утраченные доходы, в связи с донорством (в соответствии с национальными нормами).
1. World Health Assembly Resolution 57.18, Human organ and tissue transplantation, 22 May 2004, http://www.who.int/gb/ebwha/pdf_files/WHA57/A57_R18-en.pdf.
2. The Ethics Committee of the Transplantation Society (2004). The Consensus Statement of the Amsterdam Forum on the Care of the Live Kidney Donor. Transplantation 78(4):491-92.
3. Barr ML, Belghiti J, Villamil FG, Pomfret EA, Sutherland DS, Gruessner RW, Langnas AN & Delmonico FL (2006). A Report of the Vancouver Forum on the Care of the Life Organ Donor: Lung, Liver, Pancreas, and Intenstine Data and Medical Guidelines. Transplantation 81(10):1373-85.
4. Pruett TL, Tibell A, Alabdulkareem A, Bhandari M, Cronon DC, Dew MA, Dib-Kuri A, Gutmann T, Matas A, McMurdo L, Rahmel A, Rizvi SAH, Wright L & Delmonico FL (2006). The Ethics Statement of the Vancouver Forum on the Live Lung, Liver, Pancreas, and Intestine Donor. Transplantation 81(10):1386-87.
5. Universal Declaration of Human Rights, adopted by the UN General Assembly on December 10, 1948, http://www.un.org/Overview/rights.html.
6. Based on Article 3a of the Protocol to Prevent, Suppress and Punish Trafficking in Persons, Especially Women and Children, Supplementing the United Nations Convention Against Transnational Organized Crime, http://www.uncjin.org/Documents/Conventions/dcatoc/final_documents_2/convention_%20traff_eng.pdf.
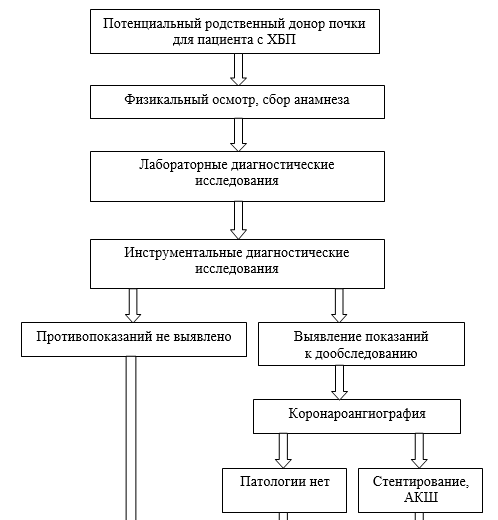
Приложение Б. Алгоритмы действий врача
Б.1. План предварительного обследования потенциального родственного донора почки
1. Основные моменты в медицинском и семейном анамнезе потенциального донора почки, необходимые для изучения:
-
Наличие или отсутствие гематурии, протеинурии, инфекции мочевыводящих путей;
-
Наличие или отсутствие затрудненного мочеиспускания, включая позывы, дизурию;
-
Наличие периферических отеков;
-
Наличие или отсутствие таких заболеваний, как подагра, нефролитиаз, гипертония, сахарный диабет (включая семейный анамнез), ишемическая болезнь сердца, заболевание периферических артерий, другой атеросклероз;
-
Наличие или отсутствие факторов риска сердечно-сосудистых заболеваний;
-
Наличие или отсутствие тромбоэмболии легочной артерии в анамнезе;
-
Наличие или отсутствие серповидноклеточных и других гемоглобинопатий;
-
Наличие или отсутствие расстройств кишечника;
-
Перенесенное или имеющееся злокачественное новообразование;
-
Наличие или отсутствие системного заболевания, которое может поражать почки;
-
Наличие или отсутствие хронической инфекции, например туберкулеза;
-
Семейный анамнез почечного заболевания;
-
Курение;
-
Наличие или отсутствие алкогольной или наркотической зависимости;
-
История психического здоровья;
-
Акушерский анамнез;
-
Периоды проживания за границей, если имеются;
-
Наличие или отсутствие предыдущей проблемы с анестезией;
-
Анамнез боли или травмы в спине или шее.
2. Основные моменты анамнеза в отношении трансмиссивных инфекций:
Перенесенные болезни:
-
Желтуха или гепатит;
-
Малярия;
-
Перенесенные переливания крови;
-
Туберкулез / Семейный анамнез туберкулеза.
Повышенный риск заражения ВИЧ, гепатитом B и C:
-
Гемофилия;
-
Промискуитет;
-
Инфекционный гепатит или сифилис в анамнезе;
-
Анамнез внутривенного употребления наркотиков;
-
Татуировка или пирсинг кожи в течение последних 6 месяцев;
-
Половой партнер – с положительной серологией;
-
Половой партнер – наркоман.
3. Необходимые консультации специалистов:
-
Врача-хирурга (перенесенные операции, настоящая патология);
-
Врача-стоматолога (санация полости рта);
-
Врача-акушер-гинеколога (УЗИ органов малого таза) для женщин, женщинам старше 40 лет также необходима консультация маммолога;
-
Врача-уролога (УЗИ предстательной железы + ПСА крови для мужчин старше 40 лет);
-
Врача-проктолога;
-
Врача-терапевта (с изложением полного медицинского анамнеза, объективного статуса, принимаемых препаратов);
-
Врача-эндокринолога с обследованием на гормоны щитовидной железы (ТТГ, свТ3, Т4св), УЗИ щитовидной железы, гликированный гемоглобин (при показаниях).
4. Стандартные лабораторные исследования потенциального донора:
-
Определение основных групп по системе AB0, антигена D системы Резус
-
Молекулярно-генетическое исследование крови на вирус гепатита B, вирус гепатита C, ВИЧ
-
Определение антигена (HbsAg) вируса гепатита B, определение антител к вирусу гепатита C
-
Определение антител IgM, IgG к ВИЧ1 и ВИЧ2);
-
Определение АТ к бледной трепонеме (Сифилис, RW,);
-
Общий (клинический) анализ крови (количество эритроцитов, тромбоцитов, лейкоцитов, уровень гемоглобина) дифференцированный подсчет лейкоцитов (лейкоцитарная формула);
-
Биохимический анализ крови (креатинин, мочевина, щелочная фосфатаза, АЛТ, АСТ, холестерин общий, ГГТП, билирубин общий, общий белок, глюкоза, мочевая кислота, кальций, фосфор, магний, калий, натрий);
-
Клубочковая фильтрация;
-
Коагулограмма (уровень фибриногена, антитромбина-III, плазминогена, протромбиновый индекс, АЧТВ);
-
Общий (клинический) анализ мочи;
-
Анализ мочи по Нечипоренко;
-
Определение количества белка в суточной моче;
-
Посев мочи.
5. Заключения инструментальных методов исследования:
-
ЭКГ;
-
ЭхоКГ;
-
Холтеровское мониторирование сердечного ритма;
-
Тест с физической нагрузкой с использованием эргометра;
-
Прицельная рентгенография органов грудной клетки или компьютерная томография органов грудной полости;
-
Ультразвуковое исследование органов брюшной полости (комплексное);
-
Компьютерная томография органов брюшной полости и забрюшинного пространства с внутривенным болюсным контрастированием.
Приложение Б2. Алгоритм наблюдения донора почки после нефрэктомии
Ранний амбулаторный период после нефрэктомии (10-40 сутки)
На момент выписки из стационара донор должен быть обеспечен:
-
выписным эпикризом для врачей-специалистов по месту жительства, содержащим полную объективную информацию о выполненном вмешательстве и течении послеоперационного периода;
-
адекватными рекомендациями по уходу за раной, обезболиванию и реабилитации;
-
листом временной нетрудоспособности на время пребывания в стационаре.
Пациент наблюдается в амбулаторных условиях по месту жительства у врача-хирурга/уролога, а также врача-нефролога/терапевта.
При наличии жалоб пациента или при выявлении показаний рекомендована повторная консультация врача-хирурга/уролога, а также врача-терапевта/нефролога по месту жительства вне зависимости от срока после нефрэктомии.
При консультации проводятся следующие виды обследования:
-
Физикальный осмотр;
-
Выявление наличия/отсутствия раневых осложнений;
-
Развернутый клинический анализ крови;
-
Биохимический анализ крови (креатинин, мочевина, АЛТ, АСТ, холестерин общий, билирубин общий, общий белок, глюкоза);
-
Вычисление СКФ;
-
Общий анализ мочи,
-
По показаниям – УЗИ почки.
Дальнейшее наблюдение производится при обращении, возникновении каких-либо жалоб, но не реже 1 раза в год.
С целью выявления необходимости оказания медицинской помощи рекомендован ежегодный осмотр. Целью осмотра является выявление любой возникающей патологии, в том числе почечной недостаточности. Диспансерное наблюдение проводится участковым терапевтом, врачами-специалистами по месту жительства.
Ежегодный осмотр включает оценку:
-
Общего самочувствия и образа жизни;
-
Принимаемых препаратов;
-
Функции оставшейся почки, в том числе определение уровня креатинина и мочевины, общего белка, альбумина, глюкозы в сыворотке крови;
-
Клинического анализа крови;
-
Общего анализа мочи;
-
Артериального давления (при наличии показаний производятся консультации врача-кардиолога, суточное мониторирование АД);
-
Веса и ИМТ.
-
УЗИ почки.
При наличии показаний назначаются консультации врача-нефролога, врача-уролога, врача-хирурга, других специалистов.
Приложение В. Информация для пациента
Кого можно считать родственным донором почки?
Донором может быть человек в возрасте от 18 лет, прошедший полное обследование и признанный пригодным к нефрэктомии (удалению одной почки) с целью последующей пересадки, и находящийся в кровной (генетической) связи с реципиентом (человеком, получающим почку). Желание пожертвовать свою одну почку для пересадки своему родственнику должно быть подтверждено добровольным согласием, изложенным в произвольной форме.
Что представляет собой операция по пересадке почки от живого родственного донора?
Операция производится под наркозом (общей анестезией) и состоит из трех этапов:
Первый этап — это операция забора одной почки у донора. Во многих центрах трансплантации у родственного донора изъятие почки производится при помощи лапароскопии, т. е. через небольшие проколы и небольшие разрезы на животе, с минимальной травматизацией и последующей быстрой реабилитацией после операции. Также возможно производить нефрэктомию и через открытые доступы.
Второй этап – подготовка изъятого органа к трансплантации: производится промывание почки через сосуды специальным консервирующим раствором на короткое время (от 20 до 90 минут), почка помещается в холодный раствор при температуре + 4 градуса.
Третий этап – трансплантация (пересадка) почки реципиенту, выполняемая также под общей анестезией.
Какие преимущества живого донорства почки перед посмертным донорством (от умерших людей)?
К основным преимуществам трансплантации от живых родственных доноров следует отнести лучшие показатели выживаемости реципиентов и трансплантатов как в ближайшие, так и в отдаленные сроки, более предсказуемую и устойчивую функцию пересаженной почки, а также отсутствие длительного периода ожидания с возможностью выполнения трансплантации до начала заместительной почечной терапии. При трансплантации от живого родственного донора очень короткий период консервации почки в холодном растворе, что оказывает минимальное повреждение для пересаживаемой почки. Кроме того, хорошая совместимость между родственным донором и реципиентом по основным лейкоцитарным антигенам позволяет применять менее агрессивную иммуносупрессивную терапию после операции. Все это дает лучшие результаты функции и выживаемости трансплантата, гораздо реже отмечается отсроченная функция трансплантата.
Сколько функционирует пересаженная почка?
В среднем половина из пересаженных почек продолжает функционировать по истечении 12-15 лет, а в случае трансплантации почки от умершего донора 8-10 лет. Есть множество случаев, когда функция трансплантированной почки остается удовлетворительной на протяжении 30 и более лет. Кроме того, накоплен большой опыт по повторным трансплантациям почки.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Людмила Кондрашова – основательница и председатель межрегиональной общественной организации нефрологических пациентов «Нефро-Лига» (с 2008 года)-занималась защитой прав пациентов, участвовала в переговорах с органами государственной власти в сфере здравоохранения и профессиональным медицинским сообществом, участвовала в работе над законами.
Благодаря ее настойчивой работе транспортировка пациентов диализа была включена в программу государственных гарантий, а в список жизненно важных лекарств попали несколько инновационных препаратов.
Людмила Кондрашова умерла 23 декабря 2020 года.
Здравствуйте, дорогие друзья! Сегодня у нас вебинар, который посвящен трансплантации. Мне предварительно прислали достаточно много вопросов. У меня есть небольшая презентация. Небольшая потому, что делать презентацию состоящую из одного текста — это очень скучно, что касается трансплантации — картинок там не так много. И основные вопросы, которые мне задавали, я могу озвучить пока без презентации. Когда будет возможность и это будет необходимо, я буду включать презентацию в мой рассказ.
Показания к трансплантации почки
Показаниями к трансплантации почки являются терминальные стадии любого почечного заболевания потому, что, к сожалению, независимо от лечения заболевания, его возникновения – рано или поздно пациент с серьезным почечным заболеванием приходит к диализу, а потом встает вопрос, как с диализа сойти. Либо он должен пожизненно оставаться на диализе, поскольку почки не работают, либо он стремится к трансплантации, если это для него возможно.
Что означает терминальная стадия? Это означает, что почки утрачивают свои основные функции, в первую очередь, водовыделительную и функцию очищения от токсинов. Также они участвуют в гормональном обмене организма. Они вырабатывают гормон, который отвечает за продуцирование красных кровяных телец, то есть, нашей крови.
Еще вопрос: может ли быть ситуация, что трансплантация назначается без должных показаний или, наоборот, не назначают, хотя больному это показано?
Ответ: Нет, это невозможно. Дело в том, что нужно понимать – существует глобальная проблема острой нехватки донорских органов , тем более, в России. Поэтому, даже те пациенты, кому показана трансплантация, у кого нет к ней серьезных противопоказаний, не все будут трансплантированны. Если у пациента есть показания к трансплантации почки и есть возможность эту трансплантацию сделать, он, естественно, будет трансплантирован. Если же у пациента есть серьезные противопоказания, то, к сожалению, трансплантация для него не возможна. В частности, таким пациентом являюсь я, у меня есть много серьезных противопоказаний. Я никогда не буду трансплантированна и до конца своих дней останусь на диализе.
Особенности пересадки
Трансплантация почки — это хирургическая операция, заключающаяся в пересадке здорового органа от одного человека-донора, другому человеку, который нуждается в трансплантации почки, которая не выполняет свою функцию — реципиенту. Новая почка, как правило, работает за обе почки, которые утратили свою функцию.
Пересаживается почка, вопреки многим представлениям тех, кто далек от трансплантации — что-то слышал случайно в СМИ, что-то сказала соседка, кто-то рассказал на лавочке — на самом деле она пересаживается не назад, не вбок, да, немножко назад и вбок, где располагаются почки здорового человека, — а в брюшину. Пересаживается она либо в правую, либо в левую сторону брюшины, в зависимости от того, какая донорская почка есть у трансплантолога — правая или левая. Это место хорошо тем, что оно защищено костями таза, с одной стороны. Здесь близко подходят сосуды, питающие почку. Достаточно легко подшить новую почку, ее мочеточник к мочевому пузырю. И это место очень удобно для дальнейшего контроля, как живет, как чувствует себя донорский орган после пересадки. Ну, и, соответственно, человек с донорской почкой.
Подготовка к трансплантации
На самом деле, для человека, утратившего функцию почек, подготовка к трансплантации заключается только в одном — вы должны подойти к трансплантации как можно более сохранными. То есть, ваша основная задача — следовать рекомендациям врача и неукоснительно выполнять план лечения, который вам назначен. Если это гемодиализ — никаких пропусков, сокращений процедуры. Если это назначение препаратов, которые препятствуют возникновению осложнений, когда вы на гемодиализе — это неуклонный прием этих препаратов. Также это соблюдение диетических ограничений, поскольку у пациентов диализа есть диетические ограничения, которые могут влиять на состояние пациента. Это соблюдение режима сна, бодрствования и работы, если пациент продолжает работать. То есть, ваша задача — сохранить себя до трансплантации как можно в лучшем виде, скажем так, в наиболее лучшем виде подойти к трансплантации.
Противопоказания к трансплантации
Они делятся на две группы — абсолютные и относительные.
Абсолютные:
- Это низкая приверженность к терапии. Если пациент не компоентен и не привержен к терапии, как правило, это выясняется, когда он еще на диализе и даже не подошел к трансплантации. И с большой долей вероятности можно понимать, что когда он будет трансплантирован, он будет также нарушать режим лечения, режим соблюдения приема препаратов и так далее.
- Это злокачественное новообразование. Со злокачественным новообразованием на трансплантацию не берут. Это совершенно точно.
- Нарушение обмен веществ (оксалоз). Я вам поясню. Оксалоз — это интенсивное образование камней в почках в таком масштабе, что почки погибают от такого обилия камней. К сожалению, это патология, которая возвращается в трансплантате после операции, и возвращается в ста процентах случаев. Поэтому трансплантологи несколько лет назад полностью отказались от трансплантации детей, у которых есть подобного рода заболевания, так как все трансплантации, которые были ими сделаны, были неудачны. Через некоторое время трансплантированная почка погибала опять из-за интенсивного образования камней. Это стопроцентно, и здесь не было исключений, поэтому, к сожалению, с этим заболеванием не трансплантируют.
- Нарушение обмена веществ.
- Активный СПИД и гепатит. Ну, это понятно.
- Активный туберкулез.
- Терминальная стадия другого заболевания. Если, например, у человека легочная гипертензия в последней стадии, у него поражены тяжело легкие, то какой смысл ему пересаживать почку, если он просто не выживет, он даже не переживет самой операции.
- Тяжелая сосудистая патология, поскольку кровоснабжение нового органа, то есть, пересаженной почки требует хорошего кровотока, хорошего кровообращения.
- Наркотическая зависимость.
- Прогнозируемая длительность жизни больного менее пяти лет. Это скажем так, на мой взгляд, достаточно спорное положение. Но у нас по закону люди старше 65-ти лет не трансплантируются. Потому что вероятность того, что человек проживет достаточно большой период, превышающий пять лет, к сожалению, в нашей стране не так велика.
Есть относительные противопоказания. Их тоже достаточно много, но они относительными называются потому, что очень много зависит от той клиники, где вы собираетесь делать трансплантацию. Есть клиники с очень большими возможностями, которые эти относительные противопоказания убирают перед тем, как сделать трансплантацию пациенту.
- Например, пациент поступает с желудочным кровотечением, у него язва, серьезная. Его оперируют, эту язву ушивают, приводят пациента в порядок, в этом смысле все нормализуется, и он, в принципе, готов к трансплантации. То есть, эту проблему убрали, и у него уже нет какого-то противопоказания к трансплантации.
- Это хроническая инфекция мочевыводящих путей, тяжело поддающаяся лечению. Дело в том, что у пересаженной почки мочеточник короче, чем у обычной, поскольку она сидит в брюшине и сидит ближе к мочевому пузырю, поэтому любая инфекция, возникшая в мочевыводящих путях, легче поднимается к пересаженной почке. Здесь выше риски инфицирования самого органа.
- Это некомпенсируемый сахарный диабет. Я думаю, вы знаете, что некомпенсируемый сахарный диабет сам по себе приводит к поражению почек, к хронической почечной недостаточности.
- Инфекционные заболевания в фазе обострения с выраженной клинической картиной
- Неподдающиеся лечению злокачественные опухоли. Но, это понятно.
- Серьезные сопутствующие заболевания, представляющие либо риск для пациента при трансплантации, либо ставящие под сомнение долговременный успех трансплантации. У меня есть свои сопутствующие заболевания, которые, к сожалению, являются для меня противопоказанием к трансплантации.
- Эмоциональная неустойчивость больного и серьезные нарушения психики, потому, что после трансплантации прием препаратов, препятствующих отторжению органа, требует от пациента очень большой внутренней дисциплины. Препараты применяются по часам, пропуски их недопустимы, и даже есть достаточно строгие диетические ограничения, которые пациент должен соблюдать либо до конца своей жизни, либо до того момента, пока функционирует его новая почка.
Вопрос: могут ли взгляды разных специалистов насчет относительных и абсолютных противопоказаний отличаться? То есть, одна клиника не берет пациента, а другая согласна прооперировать.
Ответ: Я вам скажу так. Если с абсолютными противопоказаниями какая-то клиника собирается вас прооперировать — это означает, что она хочет на вас заработать денег потому, что высокотехнологичная медицинская помощь, к которой относится трансплантация, оплачивается из федерального бюджета в полном объеме. Как только пациент встает в лист ожидания, эти деньги, условно, резервируются за ним. И как только операция проведена, учреждение эти деньги получает.
Тем более это касается тех фирм, которые говорят: «Ой, они вас не взяли — да они просто не умеют. А вы нам заплатите, там, сто тысяч долларов, мы вам все пересадим». Да. Только здесь уже возникают вопросы – приживаемости органа, насколько добросовестно это будет сделано, каков будет подбор донорского органа. Поэтому, как правило, серьезные трансплантологи с абсолютными противопоказаниями не берут на трансплантацию.
Относительные противопоказания при должной работе врачей, могут быть убраны в достаточно большой степени, до такого уровня, чтобы человек смог пойти на трансплантацию и смог трансплантироваться.
Как определить, подойдет ли донорская почка
На самом деле, существует три параметра. Группа крови, но сейчас это не настолько принципиально, как было, скажем, десять лет назад потому, что современные методики позволяют пересаживать орган, не учитывая группу крови. Методика иммуносупрессии сейчас позволяет к этому фактору относиться более лояльно. Второй фактор — HLA, расшифровывается как «человеческий лейкоцитарный антиген»- генетический маркер, расположенный на поверхности лейкоцитов, белых кровяных телец. Как правило, три маркера мы получаем от матери и три от отца. Чем выше совместимость вот этих маркеров у донорской почки и у вас, тем дольше почка прослужит вам после трансплантации.
И еще фактор — это антитела. Иммунная система, как правило, к любому чужеродному органу вырабатывает антитела. Иногда в очень больших количествах, иногда почти никак. При первой пересадке делается специальный тест, то есть, кровь донора и кровь реципиента смешивается, и если не происходит никакой реакции, считается, что орган полностью пригоден к пересадке, и здесь никаких сюрпризов нам ждать не приходится в плане отторжения или неприживаемости органа. Это три основных параметра, по которым определяют, подойдет ли почка для трансплантации.
Здесь я прописала порядок обращения в Центр трансплантации. Любой гражданин Российской Федерации, кому показана трансплантация, может получить консультацию в транспланталогическом центре. Как правило, порядок записи на консультацию есть на сайте любого серьезного центра. Это Федеральный научный центр трансплантологии и искусственных органов имени академика В.И. Шумакова, Московский городской научно-исследовательский институт скорой помощи имени Н. В. Склифосовского, Российский научный центр хирургии имени академика Б.В. Петровского. У них всегда есть определенный порядок. Можно позвонить, записаться на консультацию. Существует список документов, которые необходимо с собой иметь, когда ты приходишь на консультацию. Я думаю, не стоит их зачитывать. Наверное, все умеют читать. И, потом, как мне сказали, презентации будут выложены в открытом доступе, и я не имею ничего против. Люди просто могут почитать внимательно, в этом разобраться. Есть порядок оформления на консультацию. Необходимо получить выписку. Если вы на диализе, то у своего диализного врача. Если вы пока на додиализной стадии и наблюдаетесь у нефролога, то — у нефролога. Поэтому, в принципе, к трансплантации вы начинаете двигаться от своего лечащего врача.
Затем вы обращаетесь к тому, кто занимается в поликлинике высокотехнологичной медицинской помощью. Обычно, врач, пишущий вам выписку, указывает, что вам рекомендована трансплантация, то есть высокотехнологичная медицинская помощь. С этим вы уже идете в поликлинику, как правило, по месту жительства. Там обычно есть человек, отвечающий за высокотехнологичную медицинскую помощь, вы делаете часть исследований, которые понадобятся для того, чтобы ваши документы были поданы на комиссию уже регионального органа здравоохранения, который выносит решение о том, что вам нужно выписать направление на высокотехнологичную медицинскую помощь. Это, фактически, означает, что за вами уже резервируются деньги, что вы будете трансплантированы, и что вы можете встать в лист ожидания и с этим уже все в порядке. То есть, ваша задача теперь — ждать, когда будет подходящая почка.
Что такое ВМП
Это высокотехнологичная медицинская помощь. Она является частью специализированной медицинской помощи и связана, обычно, с применением новых технологий и ресурсов, и также высокоемких ресурсных методов лечения.
Многие спрашивают, что такое квота? Квота — это фиксированный объем финансов и услуг, который не может быть превышен и выделяется государством, контролирующим распределение данной услуги своим гражданам. В данном случае речь идет о контроле выделения квот для трансплантации почки. Квота — не совсем верное название. На самом деле это означает, что человек получит трансплантацию почки бесплатно, это раз. А во-вторых, по квоте у нас может лечиться любой человек. Основания для получения квоты- показания к данному виду лечения, а не просто желание.
У бабушки на лавочке голова заболела и она – «пойду-ка я, по ВМП полечусь». Нет, так не пойдет, так не получится. Синонимом получения квоты можно считать направление на получение ВМП. Квота — это название, как бы сказать, – общечеловеческое, а не сугубо медицинское и не юридическое точно. Квота оформляется Талоном-направлением на оказание высокотехнологичной медицинской помощи, выделяется за счет федерального бюджета. Высокотехнологичная медицинская помощь — это всегда федеральный бюджет.
Есть список высокотехнологичной медицинской помощи, который утверждается Минздравом Российской Федерации. С этим списком всегда можно ознакомиться. Если у вас возникают сомнения по поводу любого другого вида лечения: высокотехнологична ли эта медицинская помощь? Положена ли она вам? Бесплатна ли по федеральной квоте? Вы можете всегда этот список открыть, найти свою проблему или заболевание и посмотреть, есть ли оно в этом списке. Трансплантация в данный список входит.
Порядок направления определяется у нас Приказом Министерства здравоохранения от 29 декабря 2014 года № 931. Я не буду зачитывать, как он называется, эти юридические вещи, они все достаточно нудные.
Процедура получения квоты
Для получения талона-направления на ВМП необходимо обратиться в поликлинику по месту жительства, как я говорила, после своего лечащего врача. Поликлиника направляет ваши документы в региональный орган управления здравоохранения. И решение о необходимости открытия талона на высокотехнологичную медицинскую помощь должно быть принято региональным органом здравоохранения в течение десяти дней после того, как были поданы документы.
Вот такая маленькая схемка. Она более наглядная, более запоминающаяся. Потому что я когда эту презентацию делала, получилось очень много текста и мне показалось, что лучше люди пусть увидят эту простую схему – легче запомнить: сначала лечащий врач, потом — поликлиника, потом — региональный орган учреждения здравоохранения. Это то, что нужно, чтобы оформить документы на высокотехнологичную медпомощь, получить на нее направление и смело встать в лист ожидания. Вот документы, необходимые для оформления квоты:
- Заключение комиссии. В региональном органе учреждения здравоохранения будет обязательно комиссия по подбору больных для оказания высокотехнологичной медпомощи. Оно, это решение оформляется протоколом.
- Паспорт пациента.
- Свидетельство о рождении, если это дети.
- Страховой медицинский полис.
- Пенсионный страховой полис.
- Удостоверение об инвалидности, если оно есть.
Кто может быть донором почки
Донором может быть любой совершеннолетний здоровый человек, который находится с вами в кровном родстве. Это обязательное условие, потому что у нас нет так называемого эмоционального донорства, которое существует во многих странах, например, в Европе. Когда, скажем, подруга может отдать почку подруге, с которой они много лет вместе У нас возможно либо прижизненное донорство от родственника кровного, либо посмертное донорство от умершего человека.
Процесс донорства происходит следующим образом. Если это родственная трансплантация, она имеет преимущество перед посмертным донорством потому, что не связывает человека сроками ожидания донорского органа. То есть, можно со своим родственником всегда решить, в какой момент вы оба готовы к операции. Более того, человек, родственник, который готов вам пожертвовать свой орган для трансплантации, в любую секунду может от этого отказаться, и никто – ни врачи, ни сам пациент, которому был этот орган нужен, не имеют права возражать поскольку это совершенно добровольный акт, это дар гуманизма, дар жизни от одного человека другому. Это очень серьезное решение, поэтому обычно, при родственных трансплантациях, даже если мать отдает почку своему сыну, например, или дочке, ребенку, обязательно с человеком беседует психолог перед самой операцией, чтобы понять, какими соображениями он руководствуется, не передумал ли он, не было ли какого-то давления, либо каких-то обстоятельств, которые может быть он неправильно оценил. Ведь когда болен ребенок или твой близкий человек,не всегда можно принять адекватное решение поскольку ты нервничаешь, взвинчен, придавлен ситуацией. Поэтому на самой последней стадии перед операцией психолог обязательно беседует с твоим родственным донором.
Посмертное донорство
Существует два варианта. Первый — это остановка сердца вследствие какой-либо патологии, например, обширнейшего инфаркта. Только в том случае, если в данном лечебном учреждении есть бригада, которая занимается изъятием донорских органов, она может изъять донорские органы в течение тридцати минут. После смерти сердца, его гибели, есть всего 30 минут для того, чтобы остальные органы не погибли от недостатка кислорода и кровоснабжения. Если же это смерть мозга, второй вариант, вследствие обширного инсульта, тяжелейшей травмы головы и так далее, – существует много обстоятельств, – то тогда поддерживается искусственное кровоснабжение, искусственное дыхание, и там есть определенное время на изъятие донорских органов. То есть, легкие нужно изъять не позднее четырех часов. Сейчас, при современных методах консервации и поддерживания жизнедеятельности, почка может ждать, фактически, сутки. Но проблема в том, что процесс этот не быстрый. Смерть мозга констатируется целым консилиумом врачей, куда входят врачи таких специальностей как неврологи, патофизиологи, терапевты. Туда ни в коем случае не входят люди, которые занимаются сами трансплантацией. Трансплантологи в это комиссию не входят. То есть, она работает и заключение свое дает не зависимо от трансплантологической службы. И только когда эта комиссия, проведя все тесты, которые со стопроцентной уверенностью говорят, что — да, мозг этого человека полностью мертв, тогда может произойти изъятие донорских органов. Де-юре и де-факто полная, стопроцентная смерть мозга считается смертью человека.
Сейчас у нас пока действует закон 1992 года, в котором прописана презумпция согласия. То есть, человек при жизни не написавший отказ от донорства, по умолчанию, может быть использован как донор потенциальный. Но таких случаев у нас, на самом деле, не так много и мы узнаем о них только тогда, когда возникает какой-либо скандал на эту тему. К сожалению, лично мне доводилось присутствовать на разных мероприятиях, передачах, куда приглашали родственников тех, у кого взяли органы для трансплантации. Я вас не обманываю, часто вопрос ставился так: если вы берете бесплатно, то мы идем в суд, и это скандал; заплатите нам и берите, чего хотите. К сожалению, так дело обстоит.
На самом деле, добровольное донорство — вопрос этически очень сложный. Мы с 2014 года продвигаем проект, который написали два моих региональных лидера. Обе они трансплантированны. Называется он «Трансплантация. Я — за». Он должен сформировать в обществе положительное отношение к трансплантации и органному донорству, чего у нас нет. У нас эта отрасль медицины окружена таким безумным количеством страшилок, мифов, чудовищных домыслов, что когда мы сталкиваемся просто с обычными людьми на акции, которую проводим в рамках проекта, иногда бывает просто жутко слушать, что они говорят. Например, одна дама рассказала мне ужасную историю, как черные трансплантологи вырезали почку у кошки и пересадили человеку за деньги. Ну, я не могла это никак комментировать. Мне было очень смешно, я постаралась не смеяться очень сильно. Человек даже не включает голову, какого размера почка у кошки и какая она у человека.
Значит, донорская почка может храниться. У нас есть буклет, который вы открываете, разворачиваете и внутри там плакат, на котором поэтапно , в очень понятной форме написано, как проводится трансплантация . Вот здесь внизу шкала (на плакате) — сколько живет донорский орган. Это материалы, которые мы сделали в рамках своего проекта. У нас еще есть здоровенные плакаты, и мы их время от времени раздаем трансплантологам. Они их очень любят. Вот, обычно, сердце, легкие – 4-6 часов, печень — 12 часов, ну, почка сейчас до 24 часов. Это связано, конечно, с улучшением консервирующих технологий. Хотя я вам честно скажу, существует очень много тонкостей. В принципе, выживаемость у органа зависит даже от того, как часто его брали в руки до того, как пересадить. Там есть свои тонкости, которые не всегда рассказывают и, собственно, это ни к чему. Но просто интересно само по себе.
Трансплантация за границей
Да, трансплантации за границей делать можно. Но в отличие от России трансплантация для наших граждан за границей платная. Более того, там есть очень жесткие режимы ожидания донорской почки. То есть, если ты приехал и хочешь пересадить почку за деньги, это не означает, что тебя прооперируют вне очереди. Нет. В среднем в Германии ожидание донорского органа — это 5-7 лет. Пока они не прооперируют всех своих, кто стоял в очереди до тебя —придется ждать — и до тебя дело дойдет через 5-7 лет. Тем более, что Германия в отличие от многих других европейских стран отличается не очень высоким количеством донорских органов на миллион населения. В Испании этот процесс происходит несколько быстрее, но цены достаточно высоки — это где-то от 250 до 750 тысяч, в данном случае, долларов, евро, смотря где вы делаете операцию.
Операция эта платная. Не надо забывать, что в этом случае, к сожалению, платная не только сама операция, но и пребывание в стационаре, который вам понадобится, пока вы будете там лежать прооперированные и так далее. Если вы не знаете языка, вам нужна будет оплата переводчика, обязательно нужен кто-то, кто будет вам помогать в первый послеоперационный период потому, что трансплантация почки на самом деле дело не легкое.
Побочные эффекты
Как я говорю, чтобы трансплантироваться, надо быть на редкость здоровым человеком. Первые полгода большое количество иммуносупрессий, которые принимаются для того, чтобы не отторгся донорский орган. Есть такая иллюзия, что пересадился и здоровый побежал. Нет, это не так. Заболевание, которое было, оно никуда не девается. К сожалению, бывает возврат основного заболевания в трансплантате, но далеко не у всех и не все формы заболеваний. Потом, почка расценивается организмом как чужеродное что-то, вторгшееся, и его задача это чужеродное уничтожить. Для того, чтобы подавить имунный ответ организма, человек вынужден принимать достаточно большое количество препаратов, подавляющих его иммунитет, чтобы компенсировать часть вредных эффектов от этих препаратов, он, как правило, принимает еще гормоны в больших дозировках. А у гормонов есть своя обратная сторона. Они могут вызывать стероидный сахарный диабет и так далее. То есть, у человека могут возникать свои проблемы после трансплантации.
Сразу скажу, по своему опыту, организация наша существует более десяти лет. За то время, что она существует, две трети, кто у нас были на диализе, трансплантировались. Плюс еще мы общаемся с огромным количеством трансплантируемых пациентов. Лучше всего, конечно, трансплантацию переносят молодые. Молодым нечего делать на диализе. Они хорошо переносят трансплантацию, и они легко переносят побочные эффекты, которые могут возникнуть на фоне препаратов после трансплантации. То есть, у организма достаточно ресурса, чтобы эти эффекты как-то нивелировать. У меня есть на терапии парень, 23 года, врожденная патология печени, которому была сделана трансплантация два года назад. Он мне приносил недавно документы и зашел на скрюченных ногах. Я говорю: – Максим, что случилось? – Ой, Людмила Михайловна, я подумал, наверное, 10 км все-таки мне многовато бегать, надо чуть-чуть поменьше. Я говорю: – Ну, ты даешь! Он говорит: – Знаете, иногда сижу и думаю: неужели это все было со мной? Я, говорит, за эти два года уже привык быть здоровым человеком. Причем, по нему совершенно не скажешь, что у него были какие-то серьезные проблемы.
Гемодиализ в ожидании трансплантации
Не всегда пациент находится на гемодиализе в ожидании трансплантации. Идеальный вариант, когда пациент, уже подошедший к гемодиализу в терминальной стадии почечной недостаточности трансплантируется. Как правило, это родственная трансплантация, там нет режима ожидания донорского органа. То есть, вот договорились, все решили, трансплантировались. Это идеальный вариант. Потому что когда пациент попадает на диализ, к сожалению, почки работают 24 часа в сутки, а диализ очищает кровь от 12 до 15 часов в неделю. И этого явно не достаточно, копятся осложнения, организм теряет свой ресурс. Чем дольше вы на диализе, тем меньше вероятность того, что вы будете трансплантированы. Поэтому, чем быстрее происходит процесс трансплантации, тем лучше.
Нефротоксичность
Вопрос: Сколько живет человек после трансплантации и какие есть особенностинаблюдения пациента?
Ответ: Я вам сразу скажу, сколько человек проживет после трансплантации — это совершенно непредсказуемо, абсолютно. Я лично знаю людей, которые перешагнули 20-летний рубеж и знаю одного человека, который подбирается к 30-летнему рубежу. К сожалению, иммуносупрессия, которую человек должен принимать после трансплантации почки, чтобы подавить отторжение органа, токсична и для самой почки. Нефротоксичность, как говорят врачи. Есть такое термин – «хроническое посттрансплантационное отторжение». То есть, организм хронически пытается отторгнуть орган, а лекарство хронически пытается подавить это отторжение. И вот эта борьба, которая происходит в почке, в организме, она негативно влияет на почку, она (почка) постепенно теряет свою функцию, медленно угасая.
У кого-то процессы могут происходить достаточно быстро, но это даже не зависит от иммуносупрессии. Это зависит от организма самого человека. Это зависит от того, какой орган ему достался. Зачастую даже при контроле донорских органов непредсказуемо, как он может себя повести. Я знаю немало случаев, когда трансплантировали моих, им подшивали почку и она начинала работать уже на операционном столе. То есть, человека не успевали еще даже зашить, а почка уже заработала. А бывает отсроченная функция, когда человека прооперировали, все вроде гладко, все хорошо, и анализы хорошие, и по УЗИ все нормально, и другие исследования говорят о том, что все в порядке, а не дает мочи и — все. И вот эта отсроченная функция, она может длиться месяц, может, два. Я знаю человека, который два месяца ждал, пока заработает почка. Это женщина, молодая достаточно.
Продолжительность жизни
Конечно, многое зависит от дисциплины самого человека: соблюдает ли диетические ограничения, вовремя ли принимает препараты, в должное ли время показывается врачу, делает ли он назначенное ему обследование? Это зависит от очень многих факторов. А вообще, если честно, как правило, непредсказуемо. Но если только человек, который трансплантировался, постоянно пил, то да, можно сказать, что она проживет у него недолго. В остальных случаях, это непредсказуемо.
У молодых, как правило, почка живет дольше. У меня много молодых людей пересадилось, и все чувствуют себя очень хорошо. Они во-первых работоспособны, потом подавляющее большинство из них нарожало детей сразу после этого. У нас в институте Шумакова занимаются специально женщинами после трансплантации, которые рожают здоровых детей. Что касается молодых мужчин, то тут проблем вообще нет. Жена выносит, жена родит. Многие из них обзавелись детками, у одной пары растет малышка, ей уже 4 четыре года, они живут в Подмосковье, а еще у меня есть совершенно уникальная пара , они живут в Смоленске, и он и она трансплантированные, и их малышке сейчас уже, наверное, лет пять. Мы очень долго боролись за то, чтобы они не получали дженерические замены, а получили оригинальные препараты. Сейчас много дженериков на рынке. Все приспосабливаются, как могут, потому что, к сожалению, проблема дженериков — никуда не девается в России.
Многие российские компании по программе импортозамещения кинулись делать дженерические замены, которые, к сожалению, очень плохо работают, либо вообще не работают, дают много побочных эффектов и являются достаточно токсичными. Это не мое мнение, это мнение трансплантологов, с которыми я очень тесно общаюсь. В частности, в РНЦХ имени Петровского, институте хирургии, мониторят своих трансплантированных пациентов – кто на каких препаратах идет после трансплантации, что выдают в регионах. Здесь очень много трансплантируется пациентов, которые приезжают из регионов. И по некоторым нашим компаниям у них очень отрицательные отзывы. Поэтому много факторов желанности, но при хороших условиях, почка функционирует хорошо и безотказно годы и годы. Вот у моей доброй подруги почка проработала 24 года. К сожалению, она отторглась – была ситуация, связанная с очень тяжелым стрессом. А это тоже сказывается. Сказывается на всем организме, как у всех у нас, в том числе и на трансплантированном органе.
Терапия после операции
Вопрос: А правильно я понимаю, что терапия, которая назначается пациенту после трансплантации, оплачивается государством, но это как раз часто и оказываются дженерики, и вот здесь могла бы понадобиться помощь благотворительных фондов в закупке оригинальных препаратов.
Ответ: Да, особенно для детей. Извините, я вас перебью. Особенно для детей.
Вопрос: А как долго длится эта терапия?
Ответ: Пожизненно. Единственный случай, при котором данная терапия не нужна — это если вам почку отдал однояйцевый близнец. Это крайне редкий случай. Кстати, первая удачная долговременная трансплантация в мире была сделана именно от однояйцевого близнеца однояйцевому близнецу.
Вопрос: В случае необходимости повторной пересадки, бывают ли такие случаи, делают ли, и оплачивается ли это за счет бюджета?
Ответ: Да, оплачивается за счет бюджета, если это было не потому, что человек кололся, пил, падал с десятого этажа и пришел еще раз одну почку подсадить. Если угасание трансплантата произошло естественным путем, то да, все они подают, как правило, встают снова в лист ожидания. Это совсем другая жизнь, поверьте мне. Я вижу их, они же все на моих глазах. У нас очень много людей трансплантированных, особенно молодые — они совершенно другие. Во-первых, ты не прикован к аппарату искусственной почки три раза в неделю. Ты свободен, ты можешь работать, ты можешь поехать куда хочешь. И, конечно, когда они этой жизнью поживут, после того, как были прикованы к диализу, они хотят снова трансплантировать, чтобы жить нормальной жизнью. Тем более, как правило, когда они молоды, у них появляются уже семьи, появляются дети, они хотят и дальше со своей семьей, со своими детьми, жить полноценно и чувствовать всю вот эту радость жизни.
Жизнь на диализе
Какие есть государственные гарантии по доставке в больницу, везде ли это соблюдается, и какая помощь может понадобиться пациенту, который живет на диализе?
Доставка, транспортировка пациента к месту осуществления процедуры и обратно — это наша головная боль изначальная, с тех пор, как мы образовались, десять лет назад. Дело в том, что десять лет назад, когда появилась нефрология, я была уже три года на диализе. Я попала на диализ в 2005 в очень тяжелом состоянии, совершенно случайно, потому что диализных мест катастрофически не хватало, и меня взяли только потому, что моя мама делала огромную работу для клиники Сеченова. Она проектировщик объектов здравоохранения. Только поэтому меня взяли на диализ в Клинику ревматологии, нефрологии и профпатологии им. Е.М. Тареева. Когда меня привезли в клинику, я выглядела мыслящим водяным шаром. И вытаскивали меня из этого 2,5 месяца, как минимум, и за полгода я пришла в себя и стала похожа на человека.
Диализ стал бурно развиваться, когда его отдали в ОМС — обязательное медицинское страхование. Например, приходил инвестор, говорил: «Я хочу у вас диализный центр построить». Глава региона: «Ок, хорошо. Давай половину ты, половину регион». Сейчас они так делать не хотят. В регионах давно денег нет. И даже если они есть, их давать все равно не хотят. Как правило теперь инвестор, который хочет построить диализный центр, делает это за свои деньги, но оплату за процедуру, произведенную пациенту, он получает из фонда ОМС. Как только коммерсанты поняли, что это гарантированные деньги – ты сделал процедуру и денежки получил гарантированно, все, кому не лень, затопали ногами в диализ, даже те, кто до этого понятия не имел, что такое «медицина», не то что «диализ».
У нас стали расти диализные центры, как грибы, и отчасти сняли проблему транспортировки. Потому что раньше, если диализ где-то и был, то, как правило, в какой-то области, большой иди маленькой, он находился в одном-единственном областном городе, куда должны были люди добираться, как хотят. Никакой транспортировки не было. Пешком, на автобусе, на электричке, выезжаешь ты в пять утра, или ночью, и сутки или чуть больше тебе нужно на то, чтобы получить только процедуру, поскольку ты туда-сюда ездишь восемь часов — это никого не волновало. Мы этой темой очень серьезно занялись после того, как у нас умер пациент в Мурманской области, который проживал в двухстах километрах от центра диализа, и он физически не мог своим ходом добираться три раза в неделю до диализа.
К сожалению, диализ — это процедура жизнеспасающая, и если человек пропускает неделю (максимум — две), он умирает. Он пропустил несколько процедур, поскольку физически не мог добраться до диализа. Он умер. Мы подавали тогда в суд, получили решение Верховного суда, который признал транспортировку неотъемлемой частью процедуры гемодиализа. Но у нас нет прецедентного права, поэтому, к сожалению, мы очень много судимся по транспортировке, половину судов мы выиграем, половину проигрываем, все зависит от региона, честно вам скажу.
Но в прошлом году, после того, как одна из членов нашей организации, Клавдия Старцева, на прямой линии обратилась к президенту, прорвалась каким-то образом, было распоряжение президента изыскать финансовые средства в регионах для транспортировки пациентов диализа. Сейчас что-то сдвинулось. В некоторых регионах действительно выделяют транспорт, начинают возить. Где-то все продолжается так же: никакой транспортировки, хоть как-то узаконенной каким-то местечковым актом, нет. Но транспортировка вошла в Программу государственных гарантий бесплатного оказания гражданам медицинской помощи на 2018-2020 годы. А поскольку она в программу госгарантии вошла, это означает, что она впервые за все это время была признана действительно неотъемлемой частью медицинской услуги.
Пока это все, что нам удалось пробить головой. Дальше посмотрим, как будет все развиваться. Что касается самого диализа, то три раза в неделю, минимум четыре часа потому, что диализ менее четырех часов не считается адекватным. Ну, максимум, пять часов. Есть разные виды диализа. Есть для особо тяжелых пациентов, которые еще связаны с онкологией – там круглосуточный диализ. Там есть специальный врач, который ночью находится с пациентом, который все крутится и крутится на аппарате искусственной почки. Я получаю диализ пять часов три раза в неделю. Я на четырех просто не вымываюсь.
Вопрос: С диализа, так скажем, сойти уже невозможно?
Ответ: Нет, надо понимать четко одну вещь: если вы на диализе — ваши почки погибли. Сойти с диализа, это такой миф, да, но не совсем точное выражение. Есть острые поражения почек обратимые. Они и разделяются поэтому на острые и хронические. Острые, это означает, что, например, человек перепил, по-простому говоря, или выпил не ту жидкость, которую они планировали с приятелями выпить. Или он вдруг поел грибков, а какой-то грибок оказался дико токсичный. И произошло поражение почек.
В этих случаях человека берут на диализ, и в такой ситуации ничто не мешает почке восстановиться. При таких видах поражения, как правило, почки восстанавливаются, но какое-то время человек должен побыть на диализе. В среднем, скажем так, если через три недели они не начали восстанавливаться, то там ловить нечего. Если через три недели пошли процессы восстановления — увеличился диурез, улучшились анализы и так далее, – почки восстанавливаются практически полностью, и человек уходит с диализа. Но таких случаев не очень много. Я знаю один уникальный случай, когда человек был — это мне рассказал мой первый диализный врач, он один из корифеев нашего диализа — 8 лет на диализе, и почки не восстановились из-за тромбоза почечных артерий. У них не стало кровоснабжения, они остановились, он попал на диализ. А диализ проводится с применением гепарина, поскольку ваша кровь все эти часы находится во внешнем контуре, проходит через очищающий диализатор, по системе бежит — чтобы не произошло тромбоза, он делается с применением гепарина. Вот поскольку этот человек 8 лет делал процедуру с гепарином, то у него рассосались тромбы и неожиданно заработали почки, наладилось кровоснабжение. Человек ушел с диализа через несколько лет. Но это уникальный случай.
Школы пациентов
Вопрос: Вы сказали, что чем дольше человек находится на диализе, тем у него меньше возможности пересадить почку. Сколько лет нужно быть на диализе, чтобы трансплантация стала невозможна
Ответ: Вы знаете, на наших конференциях и в школах пациентов очень часто, почти всегда бывают серьезные трансплантологи и на вопрос одного моего регионального лидера — она 19 лет была на диализе: «Есть ли у меня шанс трансплантироваться?» он сказал: «Нет». Но 19 лет на диализе — это большой срок. В то же время, должна сказать, я знаю двух человек: одна девушка у меня трансплантировалась, она была 11 лет на диализе, и в прошлом году трансплантировался мой друг, он был на диализе 15 лет. Сейчас он растит вторую внучку.
Вопрос: А можно ли обращаться в вашу организацию представителям некоммерческого сектора, если вдруг возникают или идут обращения от пациентов с проблемами почечной недостаточности?
Ответ: Да, конечно, мы помогаем независимо от членства организации. Для нас это не имеет значения. У нас на самом деле, де-юре самих членов не так много. Но мы работаем по территории всей России, реально, от Калининграда до Владивостока. Мы проводим очень много акций. Например, ко всемирному дню почки у нас проходят акции, как минимум, в 25 регионах. Причем, это не одна акция. Это три-четыре. Они включают и школы пациента. У нас идут пять социальных проектов больших. Первый — «Здоровые почки для всех». Это для всех абсолютно граждан, условно здоровых, взрослых и детей, для родителей с детьми.
То есть, мы пытаемся сформировать какую-то настороженность у родителей в плане почечных заболеваний потому, что часто они подкрадываются незаметно, и какие-то признаки, которые просвещенный в этом вопросе родитель может заметить у ребенка, другой может не заметить. Мы учим маленьких детей, что полезно, что вредно для почек. У нас для самых маленьких есть сказка, которая называется «Путешествие почек», волонтеры показывают ее в детских садах. Существует благотворительная программа – мои региональные лидеры посещают приюты, детские дома. В рамках, опять-таки, этого проекта мы делали несколько скринингов населения на раннее выявление предрасположенности к почечным заболеваниям. В результате этого скрининга сразу несколько человек попали к нефрологу, а несколько человек должны были быть на диализе уже позавчера, но люди об этом даже не подозревали. Есть «Грамотный пациент». Туда входит наша школа для диализных, для трансплантированных пациентов. Мероприятия во Всемирный день почки. Наши конференции ежегодные. «Трансплантация. Я — за!». Об этом проекте я уже упоминала. Его материалы вы видели.
Сейчас у нас появился совершенно новый проект, он опять-таки связан с трансплантацией, называется «Спорт — для жизни». Наши ребята, трансплантированные, диализные пациенты с прошлого года ездят на спортивные соревнования и привозят оттуда медали. Последний раз привезли из Малаги два серебра и четыре бронзы. Они были на соревнованиях в Польше, завоевали тоже кучу медалей. Были на соревнованиях в дружественном Казахстане. Это направление у нас сейчас очень развивается.
Потом, мои региональные лидеры, очень инициативные, они сейчас время от времени проводят спортивные межрегиональные турниры — например, «Екатеринбург против Ижевска». Сами там все организуют. Меня так ставят в известность: «Вот, мы там будем делать турнир». Ну, пожалуйста, делайте. И еще у нас есть такой проект, он называется «Поздравь больного ребенка — получи детскую улыбку». Обычно на День почки и Новый год мы посещаем детей. В первую очередь, в Санкт-Петербурге. У меня очень активно занимается этим наш региональный лидер Татьяна Тарасова. Мы посещаем детей в детских нефрологических отделениях. И устраиваем для них, как правило, какие-то праздники, концерты, подарки и так далее. Потому что я, во всяком случае, знаю, что такое быть больным ребенком.
Вопрос: Вы хотели показать ролик?
Ответ: Это наши координаты (на экране), если кому-то понадобится. Вот это первое — это наш сайт, нефрологи, координаты и мой телефон, который одновременно является телефоном организации. А второй — это название нашего проекта, связанного с трансплантацией и координаты сайта, именно связанного с этим проектом трансплантацией. Там кстати тоже есть много хорошей информации. Туда тоже можно зайти и почитать какие-то вещи о трансплантации, если нужно что-то узнать.
00:55:12 — 00:56:42 анимационный фильм о трансплантации от проекта «Трансплантация. Я — за!»
Автор
канд. мед. наук А.А. Гусейнов – заведующий Центром амбулаторной хирургии ГБУЗ «ГП №69 ДЗМ», врач-хирург, врач высшей квалификационной категории
Научный редактор
докт. мед. наук, доц. А.Ф. Завалко
Записаться к специалисту можно через ЕМИАС
Трансплантация почки – хирургическая операция, заключающаяся в пересадке человеку или животному почки, полученной от другого человека или животного (донора). Чаще всего является предпочтительным методом лечения пациентов с терминальной стадией (когда почки больше не функционируют нормально) почечной недостаточности.
Кроме того, трансплантация почки обеспечивает значительное преимущество в выживаемости пациентов в дальнейшем (прогнозируемая продолжительность – 10 лет) и лучшее качество их жизни по сравнению с больными, остающимися на диализе.
Показания
Показанием к трансплантации почки является терминальная хроническая почечная недостаточность (ТХПН) – финальный этап течения хронического гломерулонефрита (двустороннее диффузное иммунное воспалительное заболевание почек), хронического пиелонефрита (длительно протекающий воспалительный процесс в почках), диабетической нефропатии (поражение почечных сосудов, возникающее при сахарном диабете), поликистоза почек, травм и урологических заболеваний, врожденных болезней почек. Пациенты с ТХПН для сохранения жизни находятся на заместительной почечной терапии (ЗПТ), к которой относятся хронический гемодиализ, перитонеальный диализ и трансплантация почки.
Трансплантация почки по сравнению с двумя другими вариантами имеет наилучшие результаты в плане продолжительности жизни (увеличивая ее в 1,5–2 раза по сравнению с другими вариантами заместительной почечной терапии) и ее качества.
Противопоказания:
-
множественная миелома;
-
амилоидоз со значительным внепочечным поражением;
-
декомпенсированный цирроз (необходимо рассмотреть возможность одновременной пересадки печени);
-
онкологическое поражение органов;
-
обструктивные заболевания легких в необратимой стадии, декомпенсированная дыхательная недостаточность;
-
тяжелая сердечно-сосудистая недостаточность, не поддающаяся лечению (необходимо заключение врача-кардиолога);
-
прогрессирующее дегенеративное заболевание центральной нервной системы (ЦНС);
-
возраст менее 18 и более 70 лет;
-
обнаружение HBsAg
и HCV, ВИЧ.
Кандидаты на трансплантацию почки
Большинство пациентов с ТХПН имеют множественные сопутствующие заболевания и осложнения, связанные с заболеванием почек. Трансплантация почки позволяет увеличить продолжительность жизни, уменьшить выраженность патологических проявлений, улучшить качество жизни, облегчить социальную и медицинскую реабилитацию пациентов с терминальной стадией почечной недостаточности, а также снизить затраты на лечение данной категории пациентов.
Однако следует учесть, что данная хирургическая процедура сопряжена с определенными анестезиологическими и хирургическими рисками. Кроме того, в связи с необходимостью в продолжительной иммуносупрессивной терапии в послеоперационном периоде возможно появление побочных эффектов, связанных с угнетением иммунной системы. Следовательно, на этапе предоперационной подготовки пациента оцениваются потенциальные противопоказания для проведения трансплантации, а также факторы риска (например, риск возникновения злокачественных новообразований и инфекционных осложнений).
Выбор доноров: преимущества и недостатки
Есть два типа доноров почки: живые и умершие.
Трансплантация почки от живого донора
Изъятие органов и тканей для трансплантации у живого донора допустимо только в случае, если по заключению врачебной комиссии медицинской организации с привлечением соответствующих врачей-специалистов, оформленному в виде протокола, его здоровью не будет причинен значительный вред.
Донорство живой почки обеспечивает лучшую выживаемость трансплантата и реципиента, даже при рассмотрении парного обмена почек, который включает транспортировку органов перед имплантацией.
Трансплантация почки от живых родственных доноров открывает не только реальный на сегодняшний день путь решения проблемы дефицита донорских органов, но и бесспорно является более эффективным методом лечения больных ТХПН как с медицинской, так и с экономической точек зрения.
Критерии отбора/исключения потенциального донора почки
Наиболее приемлемы для донорства кандидаты со следующими характеристиками:
-
возраст от 18 до 70 лет;
-
ИМТ (индекс массы тела) менее 35 кг/м2;
-
отсутствие активного злокачественного новообразования, активной инфекции;
-
адекватная функция почек (СКФ> 80).
Абсолютными противопоказаниями к донорству являются:
-
возраст младше 18 лет и старше 60 лет;
-
артериальная гипертензия (АД выше 140/90 мм рт. ст. или наличие необходимости медикаментозной коррекции для достижения нормального АД), другие заболевания сердечно-сосудистой системы;
-
сахарный диабет;
-
протеинурия (суточная экскреция белка более 250 мг/сутки);
-
почечнокаменная болезнь в анамнезе, пиелонефрит;
-
снижение клубочковой фильтрации (менее 70 мл/мин/1,72 м);
-
микрогематурия (наличие крови в моче сверх величин, составляющих физиологическую норму);
-
урологические аномалии донорской почки;
-
хронические заболевания легких, онкологические заболевания в анамнезе;
-
ожирение (ИМТ более 40 кг/м);
-
положительный результат на вирус иммунодефицита человека (ВИЧ);
-
психические расстройства.
Преимущества трансплантации почки от живого донора:
-
частичное решение проблемы дефицита донорских органов;
-
отсутствие длительного периода ожидания донорского органа;
-
возможность выбора оптимального периода для трансплантации (подготовка донора и реципиента);
-
возможность выполнения трансплантации до начала диализной терапии;
-
возможность применения менее агрессивных режимов иммуносупрессии;
-
обеспечение более высокой ранней функции трансплантата;
-
улучшение краткосрочных (примерно 95 % против 85 % при оценке годичной выживаемости трансплантатов) и отдаленных результатов трансплантации (время полужизни трансплантатов составляет 12–20 лет по сравнению с 10–12 годами при трансплантации трупного органа).
Потенциальный риск для живого донора:
-
психологический стресс;
-
риск осложнений при обследовании донора (ангиография, экскреторная урография);
-
риск послеоперационных осложнений;
-
риск послеоперационной смерти (составляет примерно 1/2000);
-
риск послеоперационных хронических расстройств (протеинурия, артериальная гипертензия).
Трансплантация почки от умершего донора
Доноры со смертью мозга и после сердечной смерти.
Смерть мозга неминуемо приводит к нарушению функций всех органов человека, что обусловлено отсутствием нисходящих регулирующих влияний головного мозга. В свою очередь доноры после полной и необратимой остановки сердечной деятельности на основании международной классификации Маастрих (Maastricht classification) подразделяются на несколько категорий:
1 категория – смерть в результате необратимой остановки сердечной деятельности наступила до госпитализации в стационар (неизвестна давность остановки сердечной деятельности);
2 категория – смерть в результате неэффективных реанимационных мероприятий до госпитализации пациента в стационар;
3 категория – смерть после отключения от систем жизнеобеспечения;
4 категория – остановка сердечной деятельности после установления диагноза смерти головного мозга;
5 категория – внезапная необратимая остановка сердечной деятельности у госпитализированного пациента.
При этом следует отметить, что в Российской Федерации, согласно действующему законодательству, возможно использование только доноров 4-й и 5-й категории по классификации Маастрих.
Важно иметь в виду, что срок функционирования органа, трансплантированного от умершего донора, сокращен, так как имеются факторы риска: возраст донора старше 60 лет или возраст от 50 до 59 лет с артериальной гипертензией в анамнезе, конечная концентрация креатинина выше 1,5 мг/дл или цереброваскулярная причина смерти.
Реабилитация
Сразу после проведения операции по пересадке начинается реабилитация. На процесс приживания почки донора в организме пациента оказывают влияние качество материала, патология, вызвавшая необходимость пересадки, а также правильность организации последующей терапии.
Если осложнения после операции не возникают, то донорский орган начинает правильно работать уже спустя пять–десять дней, а на окончательную нормализацию состояния здоровья и отсутствие проявлений недостаточности почек может потребоваться до нескольких недель.
Профилактика
После трансплантации рекомендуется пожизненное регулярное наблюдение. Оценка функции почечного трансплантата производится ежемесячно в первые 3 месяца, далее – 1 раз в 3 месяца в течение первого послеоперационного года, потом ежегодно.
Список литературы:
-
Хаджибаев Ф. А., Султанов П. К., Эргашев Д. Подбор живого донора для трансплантации почки // Вестник экстренной медицины. 2020. Т. 13, № 3. С. 11–19.
-
Viklicky O., Novotny M., Hruba P. Future developments in kidney transplantation // Current opinion in organ transplantation. 2020. Vol. 25, №1.
P. 92–98. DOI:10.1097/MOT.0000000000000722.