Авторы:
А. И. Черепанин
, А. П. Поветкин
Острый холецистит (ОХ) – заболевание чрезвычайно частое. Это одна из актуальнейших проблем, обсуждаемая с конца прошлого столетия до сегодняшних дней. Количество осложненных форм острого холецистита достигает 35% и не имеет тенденции к уменьшению. Сегодня около половины всех больных, поступающих в хирургический стационар с острым холециститом, подвергаются экстренным или срочным операциям.
Острый холецистит (ОХ) – заболевание чрезвычайно частое. Это одна из актуальнейших проблем, обсуждаемая с конца прошлого столетия до сегодняшних дней. Количество осложненных форм острого холецистита достигает 35% и не имеет тенденции к уменьшению. Сегодня около половины всех больных, поступающих в хирургический стационар с острым холециститом, подвергаются экстренным или срочным операциям.
Операционная травма, высокий операционно-анестезиологический риск, опасность развития послеоперационных осложнений приобретают первостепенное значение и могут привести к летальному исходу в группе пациентов пожилого и старческого возраста. Послеоперационная летальность при остром холецистите колеблется от 2 до 5%. Смещение акцента в сторону использования малотравматичных операций, стремительное внедрение эндоскопических технологий вновь привлекли внимание к проблеме выбора рационального метода лечения острого холецистита. Это особенно актуально в связи с недостаточным количеством сравнительных рандомизированных исследований в хирургии желчнокаменной болезни на сегодняшний день.
Холецистэктомия из мини-доступа (МХЭ) и лапароскопическая холецистэктомия ЛХЭ полностью отвечают требованиям малоинвазивной хирургии и являются признанными операциями выбора при хроническом холецистите. В литературе обсуждаются вопросы сопоставимости операционной травмы при лапароскопической холецистэктомии и холецистэктомии из мини-доступа, появились сведения о выполнении этих вмешательств при остром холецистите с минимальной и даже нулевой летальностью. Но остаются открытыми вопросы преимуществ и недостатков каждого из этих методов в отдельности и в сравнении с традиционной холецистэктомией (ТХЭ), вопросы тактических и технических особенностей выполнения этих операций, а также оценки возможностей применения лапароскопической холецистэктомии и холецистэктомии из минидоступа при различных формах воспаления желчного пузыря и в различные сроки от начала обострения. Остаются неизученными и дискутабельными вопросы использования малотравматичных доступов у пациентов с высоким операционно-анестезиологическим риском, их сравнительная оценка.
Токийское руководство
В 2007 году было опубликовано Токийское руководство (The Tokyo Guidelines — TG) по тактике диагностики и оценке тяжести острого холангита и холецистита. В основу классификации легли результаты сопоставления клинической и морфологической картины 451 случая заболевания острым холециститом. Авторы указывают на высокую чувствительность (91,2%) и специфичность (96,9%) выделенных критериев, которые представлены в таблицах 1 и 2 (в пересмотре от 2013 года — TG13).
Таблица 1. TG13 диагностические критерии острого холецистита
Авторы сообщают о малой чувствительности и специфичности самого симптома Мерфи, а также то, что определение уровня СРБ не является часто применимым тестом в повседневной хирургической практике. Вместе с тем, в рамках приведенной классификации эти показатели дают хороший прогностический результат.
Таблица 2. TG13 критерии оценки тяжести острого холецистита
В данной классификации, а также во многих отечественных и зарубежных руководствах и монографиях указан лимит для принятия решения о хирургическом вмешательстве — 72 часа. С другой стороны, тактика ведения пациентов с острым холециститом в г. Москве регламентируется приказом Департамента здравоохранения г. Москвы № 320 от 13 апреля 2011 года «О единой тактике диагностики и лечения острых хирургических заболеваний органов брюшной полости в лечебно-профилактических учреждениях департамента здравоохранения города Москвы». В приказе сообщается, что при отсутствии признаков распространенного перитонита (абсолютного показания для экстренной операции) дается 12–24 часа для купирования приступа ОХ, а при неэффективности консервативного лечения в течение 48 часов должен быть решен вопрос о проведении хирургического вмешательства.
То есть, с одной стороны, приказом поддерживается соблюдение активно-выжидательной тактики, с другой стороны, делается акцент на сокращении сроков консервативного лечения больных ОХ до 48 часов. Последнее, возможно, связано со стремлением обезопасить пациента от интраоперационных ошибок, риск возникновения которых возрастает на 3–4 сутки от начала заболевания.
Вместе с тем, раннее радикальное лечение ОХ при компенсации функций органов и систем пациента предпочтительнее, чем проведение двух- и более этапного лечения.
Среди последних публикаций обращает на себя внимание исследование Gutt CN, Encke J, Köninger J, et al (Acute Cholecystitis: Early Versus Delayed Cholecystectomy, A Multicenter Randomized Trial // Ann Surg. 2013; 258. p. 385–393). На примере анализа 618 холецистэктомий, выполненных в первые 24 часа после поступления, а также в период с 7 до 45 дней, авторы доказывают безопасность и целесообразность проведения ранних радикальных вмешательств. Кроме этого, по данным TG13, использование эффективной классификации ОХ делает безопасным и расширяет временные границы для радикального хирургического лечения в пределах 72 часов.
Предпосылки для создания специфической системы оценки тяжести состояния больных острым холециститом
Одной из основных проблем при определении тактики в отношении больных ОХ является оценка общесоматического состояния больного, а также состояния, вызванного самим приступом ЖКБ.
Достаточной простым решением данного вопроса, на первый взгляд, может стать применение оценки физического состояния пациента по классификации американского общества анестезиологов (American Society of Anaesthesiologists) — ASA:
Класс I — пациенты без органических, физиологических, биохимических и психических расстройств.
Класс II — слабые или умеренные системные расстройства, связанные или не связанные с предстоящим хирургическим вмешательством.
Класс III — выраженные системные расстройства, связанные или не связанные с предстоящим хирургическим вмешательством.
Класс IV — выраженные системные расстройства, несущие угрозу жизни как в связи с хирургическим вмешательством, так и без него.
Класс V — умирающие пациенты с невысокой вероятностью выжить, у которых хирургическое вмешательство рассматривается в качестве последнего шанса.
Класс VI — пациенты со смертью головного мозга, доноры органов.
Если пациенту предстоит срочная операция, к цифре соответствующего класса добавляется символ «Е-emergence».
I класс не вызывает больших вопросов, так как речь идет о молодых и/или практически здоровых пациентах. Конечно, можно указать на казуистические случаи смерти на фоне видимого благополучия и пр., но для определения тактики на общепопуляционном уровне это не имеет существенного значения.
Класс II уже вызывает некоторые сомнения, так как в нем заключены уже 4 группы пациентов:
1. Слабые системные расстройства, связанные с предстоящим хирургическим вмешательством;
2. Слабые системные расстройства, не связанные с предстоящим хирургическим вмешательством;
3. Умеренные системные расстройства, связанные с предстоящим хирургическим вмешательством;
4. Умеренные системные расстройства, не связанные с предстоящим хирургическим вмешательством.
Возникает дилемма: имеет ли клинический смысл выделение данных категорий пациентов, или же это не влияет на исход хирургического лечения?!
III–V классы объединяет единый вопрос: умрет пациент или нет?
С прогностической точки зрения разработано множество шкал оценки вероятности наступления летальности. В хирургии наиболее валидными оказались SOFA — (Sepsis-related Organ Failure Assessments Score / Sequential Organ Failure Assessment) при оценке больных с сепсисом, и MODS (Multiple Organ Dysfunction Score) — для оценки прочих состояний с полиорганной недостаточностью. Основной проблемой для хирургов является невозможность использовать эти шкалы в общехирургическом отделении ввиду необходимости применять мониторинг ЦВД, сатурации кислорода крови, КЩС артериальной крови и пр., что доступно только в отделениях реанимации и интенсивной терапии (ОРИТ).
Конечно, можно возразить, что пациенты с органной недостаточностью должны находиться в ОРИТ, где такие проблемы не возникают, однако наибольший интерес вызывают пациенты с пограничными состояниями, которым при определенных условиях и должной подготовке можно выполнить радикальное хирургическое лечение в оптимальные для них сроки. Именно в этом состоит основной смысл создания хирургической классификации тяжести состояния больных ОХ.
То есть, с одной стороны, существующие на данный момент классификации тяжести состояния хирургических больных либо неконкретны, как ASA, либо слишком громоздки и требуют специальных исследований, которые практически не доступны для общехирургического отделения.
Прикладная оценка токийских рекомендаций
Рассматривая Токийскую классификацию, можно сделать вывод, что несмотря на свою простоту, она вмещает в себя как общесоматические, так и специфические для обострения ЖКБ параметры. Причем стадии распределены в зависимости от степени анестезиологического риска: от минимального TG13-I до максимального — состояние с дисфункцией органов и систем — TG13-III. Вместе с тем, критерии отражают также хирургическую сторону вопроса: отсутствие осложнений ОХ (TG13-I) и наличие осложнений ОХ (TG13-II).
Степень тяжести TG13-I характерна для пациентов как без выраженных общесоматических проблем (ASA I–II), так и без осложнений со стороны воспаленного желчного пузыря. Хирургическое вмешательство можно считать при этой степени относительно безопасным. TG13-II характеризуется наличием осложнений ОХ, но степень анестезиологического риска имеет промежуточное значение, так как еще допустимо радикальное хирургическое лечение. При TG13-III имеется недостаточность органов и систем, что обуславливает высокий операционно-анестезиологический риск и требует проведения интенсивной терапии и стабилизации пациента. Радикальной операции могут быть подвержены только пациенты I и II степени тяжести состояния. Пациенты со II степенью тяжести, как правило, уже переступили 72-часовой порог, после которого радикальное лечение чревато серьезными техническими осложнениями. Вместе с тем, при стремительном развитии заболевания в течение первых 72 часов еще возможно проведение малоинвазивных радикальных вмешательств, таких как миниинвазивная холецистэктомия (МХЭ) и лапароскопическая холецистэктомия (ЛХЭ). Пациенты с III степенью нуждаются в проведении интенсивной терапии органной недостаточности.
Таким образом, тактика ведения больных с острым холециститом может свестись к очень простой схеме. Если до 72 часов у пациента I степень тяжести по TG13, проводится радикальная операция. Как «золотой стандарт» — ЛХЭ, резерв — МХЭ.
При наличии холедохолитиаза, а также при синдроме Мириззи, необходимо проведение предоперационной ретроградной холангиопанкреатографии (РХПГ), эндоскопической папиллосфинктеротомии (ЭПСТ), а также интраоперационной холангиографии, при эндоскопической неудачной литэкстракции — холедохотомии. Синдром Мириззи часто требует проведения лапаротомии, ЭПСТ малоэффективна. Вмешательство заканчивается наружным дренированием желчевыводящих протоков. Дренажи удаляются на 17–21 сутки при отсутствии клинических и рентгенологических признаков нарушения проходимости протоков.
Если до 72 часов у пациента степень тяжести ОХ TG13-III, проводится интенсивная терапия. Стоит отметить, что критерии органной недостаточности по TG13 сопоставимы с таковыми, применяемыми в вышеописанных и прочих шкалах. Например, в шкале органной дисфункции и/или инфекции ODIN (Organ Dysfunctions and Infection). Логично предположить, что критерии могут быть взаимозаменяемы в зависимости от оснащенности конкретной лаборатории и отделений ЛПУ. Так, измерение МНО, предполагаемое при оценке печеночной недостаточности по TG13, можно заменить измерением билирубина сыворотки (критическое значение > 100 мкмоль/л) и ЩФ (критическое значение — трехкратное превышение) — по ODIN.
Если до 72 часов органная недостаточность (TG13-III) разрешилась, но возникли явления TG13-II (явления деструктивного холецистита, желчного перитонита, абсцессы печени), возможно проведение радикального вмешательства (ЛХЭ, МХЭ) с коррекцией сопутствующих осложнений: дренирование и санация абсцессов, желчевыводящих путей, предоперационное проведение ЭПСТ при холедохолитиазе с последующим интраоперационным дренированием желчных протоков и удалением дренажей на 17–21 сутки при отсутствии клинических и рентгенологических признаков нарушения проходимости протоков.
Если по каким-либо данным (со слов пациента, его родственников и пр.) от начала обострения ОХ прошло 72 часа и у больного I степень тяжести, то такую ситуацию следует трактовать как печеночная колика, и при согласии пациента возможно проведение ЛХЭ или МХЭ.
Тактика при TG13-III через 72 часа идентична таковой, что и до 72 часов. Если же интенсивная терапия не приводит к должной стабилизации пациента, необходимо проведение малоинвазивных паллиативных вмешательств, лечение осложнений — пункция и дренирование ЖП, абсцессов, предоперационное проведение ЭПСТ (при наличии панкреатита — без ХПГ).
При TG13-II, что является логичным продолжением TG13-I при умеренном течении ОХ через 72 часа, возможно только проведение паллиативных мероприятий — пункция и дренирование ЖП, абсцессов, холецистостомия, ЭПСТ.
Во всех спорных случаях при отсутствии TG13-III возможно выполнение диагностической лапароскопии. Например, при подозрении на наличие местного либо местнораспространенного перитонита при общесоматической сохранности пациента вмешательство целесообразно начинать с диагностической лапароскопии, которая может завершиться адекватной и малотравматичной (по сравнению с лапаротомной) санацией брюшной полости и поведением холецистэктомии либо холецистостомии.
Одним из моментов, который не упомянут в TG13, является ситуация с наличием желтухи. С одной стороны, такое состояние можно трактовать как осложнение ЖКБ и присвоить II степень тяжести ОХ. С другой стороны, изменения в желчном пузыре чаще носят вторичный катаральный характер, поэтому отодвигаются на второй план. Вместе с тем, наличие желтухи вносит неблагоприятный вклад в результаты радикального хирургического лечения ЖКБ, поэтому условно данное состояние можно назвать развитием печеночной недостаточности, таким образом, выставляя III степень тяжести по TG13. Это себя оправдывает, так как такие паллиативные мероприятия как ЭПСТ, чрескожное дренирование желчевыводящих протоков и желчного пузыря являются лечебными при данном состоянии. Холецистэктомия возможна в отсроченном порядке после купирования желтухи. Схематично клиническая интерпретация TG13 представлена на рисунке 1.
Рисунок 1. Тактика лечения острого холецистита согласно Токийскому руководству TG13
Использование токийских рекомендаций в собственной практике
В собственной работе мы провели исследование результатов 102 холецистэктомий с использованием малотравматичных технологий МХЭ и ЛХЭ, в том числе так называемых «гибридных» лапароскопических операций, выполненных у больных с острым холециститом в сочетании с грыжами живота. Для сравнения результатов лечения была отобрана контрольная группа из 117 пациентов, перенесших ТХЭ. В эту группу вошли больные, оперированные по срочным показаниям без клинико-инструментальных признаков острого деструктивного холецистита с парапузырными осложнениями, диффузного перитонита или не корригируемого эндоскопическим методом холедохолитиаза, т. е. включены больные, которым потенциально возможно было выполнить холецистэктомию малотравматичными методами.
Нам не удалось выявить патогномоничных клинических симптомов для отбора больных МХЭ, ЛХЭ или ТХЭ, т. к. признаки прогрессирования воспалительного процесса достаточно часто встречались у пациентов обеих групп и различия оказались статистически недостоверны (р > 0,05). Учитывая субъективность и статистическую недостоверность клинико-лабораторных симптомов, мы отдавали предпочтение инструментальным методам диагностики, которые наряду с данными анамнеза, клиниколабораторных показателей в динамике позволяли определить не только возможность выполнения холецистэктомии малотравматичными методами у больных с ОХ, но и выявить признаки возможных технических трудностей во время операции.
Были выделены следующие критерии отбора для выполнения МХЭ:
-
Пациенты с ОХ и давностью заболевания не более 72 часов без клинико-инструментальных данных о поражении внепеченочных желчных протоков и парапузырных осложнений.
-
При давности заболевания более 72 часов, если нет клинико-лабораторных и инструментальных данных за парапузырные осложнения (при наличии развивающихся осложнений вопрос решался индивидуально с учетом противопоказаний к МХЭ).
-
При наличии поражений внепеченочных желчных протоков, которые не были устранены на дооперационном этапе, с давностью заболевания не более 72 часов и отсутствии парапузырных осложнений.
-
При наличии поражения внепеченочных протоков с давностью заболевания более 72 часов, если нет ультразвуковых признаков парапузырных осложнений.
-
Пациенты с повышенным операционно-анестезиологическим риском (ОАР), когда имеются противопоказания для применения эндотрахеального наркоза, но возможно использование ЦСБ (центрального сегментарного блока с сохранением внешнего дыхания).
-
При наличии противопоказаний к ЛХЭ и отсутствии их к МХЭ.
Критерии отбора для выполнения ЛХЭ:
-
Пациенты с ОХ и давностью заболевания не более 72 часов без клинико-инструментальных данных за поражения внепеченочных желчных протоков.
-
При давности заболевания более 72 часов, если нет УЗ признаков парапузырных осложнений.
-
Пациенты с ожирением III–IV степени, низком расположении края печени, когда доступ, применяемый при МХЭ, не позволяет обеспечить необходимый операционный обзор.
-
При подозрении на ОХ, когда с целью уточнения диагноза операция начинается с диагностической лапароскопии и может быть закончена ЛХЭ.
-
Наличие послеоперационных вентральных или пупочных грыж размерами 6–7 см в сочетании с ОХ (Показанием к «мануально-ассистированной» холецистэктомии).
-
При наличии противопоказаний к МХЭ и отсутствии их к ЛХЭ.
Консервативную терапию проводили согласно городскими стандартами г. Москвы. В состав терапии включались антибактериальные препараты широкого спектра, спазмолитики, противовоспалительные препараты, инфузии солевых растворов. Сопутствующие заболевания корригировались со специалистами смежных профессий и дополняли консервативную терапию.
Показанием к холецистэктомии миниинвазивными методами являлось отсутствие положительной динамики на фоне консервативного лечения в течение 12–24 часов.
Под положительной динамикой считали следующее:
-
Наличие УЗ признаков уменьшения толщины и отсутствие слоистости стенок желчного пузыря, сокращение размеров желчного пузыря, миграция конкремента из шейки желчного пузыря.
-
Снижение воспалительных изменений в периферической крови при повторных лабораторных исследованиях.
-
Клиническое улучшение на фоне консервативной терапии.
-
Наличие фиксированного конкремента в шейке желчного пузыря и отсутствии его миграции на фоне проводимой консервативной терапии даже при клинико-лабораторных признаках купирования приступа ОХ.
-
Бескаменный ОХ у пациентов пожилого и старческого возраста, поскольку в большинстве случаев имеет место тромбоз сосудов желчного пузыря, а консервативная терапия является неэффективной.
На основании углубленного ретроспективного анализа мы определили, что 23,5% пациентов поступают в стационар позже 48 часов. Суммируя к этому еще и время, которое нужно для обследования, проведения консервативной терапии и подготовки пациента к оперативному вмешательству, можно заключить следующее: в основной группе в 29,4% случаев больные оперировались в сроки позднее 72 часов, а в 70,6% — в сроки 48–72 часа. Следовательно, декларируемая в литературе 48-часовая модель для выполнения мини-инвазивной холецистэктомии на практике малоосуществима.
В группе сравнения по срочным показаниям при неэффективности консервативной терапии в течение до 24 часов оперировано 15 (12,8%) больных, в сроки 24–72 часа — 58 (49,6%), а позже 72 часов — 44 (37,6%).
Продолжительность операции в обеих группах больных оказалась: 78,5 ± 24,1 мин. при МХЭ, 78,5 ± 29,5 мин. при ЛХЭ и 62,7 ± 17,7 мин. при ТХЭ (р = 0,006). При этом технические трудности, возникшие во время оперативного вмешательства, достоверно не зависели от формы воспаления желчного пузыря, а зависели от парапузырных осложнений в области шейки желчного пузыря. При изучении парапузырных осложнений и конверсии доступа в зависимости от сроков заболевания показано, что основной причиной конверсии являлся плотный парапузырный инфильтрат, который достоверно больше встречается у больных, оперированных после 72 часов.
Различия в частоте интраоперационных осложнений при выполнении малотравматичных ХЭ и ТХЭ оказались недостоверны — 8,8% и 4,27%, соответственно (р > 0,05). Из девяти (8,8%) осложнений, возникших в основной группе, восемь (7,8%) не потребовали расширения доступа и устранены интраоперационно. В одном случае (кровотечение из культи пузырной артерии) потребовало конверсии доступа. Кроме того, при необходимости, в зависимости от сопутствующей хирургической патологии, требующей оперативной коррекции, можно выполнить ХЭ с помощью малотравматичных методов. Поражение внепеченочных желчных путей устраняли двухэтапным методом: выполняли ЭРХПГ и ЭПСТ, после извлечения конкремента выполняли ХЭ малотравматичными методами. Если не удавалось устранить патологию на дооперационном периоде, применяли МХЭ с последующей интраоперационной холангиографией. В основной группе таких пациентов было четыре (3,9%). Еще в одном (0,98%) случае интраоперационной находкой было сочетание пузырно-толстокишечного свища с холедохолитиазом. Все операции успешно были выполнены из мини-доступа. Сочетание же с другой патологией устранялось с помощью видеолапароскопической техники, если не были показания к ТХЭ или конверсии доступа. Так, в четырех (3,9%) случаях применяли «мануально-ассистированную» ХЭ при наличии послеоперационных или пупочных грыж с размерами 6–7 см, и в одном случае (0,98%) аднексэктомию.
Благодаря малотравматичности МХЭ, у 18 (17,6%) больных использовали в качестве анестезиологического обеспечения перидуральную анестезию. Все больные имели тяжелые сопутствующие заболевания и противопоказания для применения эндотрахеального наркоза (ЭТН). Сопутствующие заболевания корригировались на дооперационном периоде, и после стабилизации состояния пациента применяли МХЭ под перидуральной анестезией. В одном случае из-за технических трудностей нам пришлось прибегнуть к конверсии доступа и перейти на ТХЭ. Анестезиологическое пособие также пришлось обеспечить под ЭТН.
В раннем послеоперационном периоде лучшие результаты оказались в основной группе больных. Так, количество послеоперационных осложнений (любое отклонение от гладкого течения послеоперационного периода) в основной группе составило 15 (14,7%), а в контрольной — 30 (25,5%) (р < 0,05). Причем в контрольной группе количество осложнений было больше как за счет осложнений со стороны послеоперационной раны и зоны операции, так и за счет осложнений, обусловленных обострением хронических заболеваний или декомпенсацией сопутствующих сердечно-сосудистых заболеваний (у одной больной в группе сравнения на первые сутки после операции возник пароксизм мерцательной аритмии и сердечно-сосудистая недостаточность, потребовавшие лечение в условиях реанимационного отделения, еще у одной пациентки развился гипертонический криз и острое нарушение мозгового кровообращения).
Тяжелых осложнений, потребовавших релапаротомии, в основной группе не было, в группе сравнения было два (1,7%). У одного пациента (0,85%) — эвентерация, еще у одного в раннем послеоперационном периоде имелись признаки желчного перитонита и ранней спаечной кишечной непроходимости.
После ХЭ из малотравматичных доступов потребность в обезболивании наркотическими анальгетиками составила 2,37 ± 1,2 мл 2% промедола в течение 1,19 ± 0,45 суток, тогда как после ТХЭ — 4,4 ± 1,73 мл в течение 1,87 ± 0,9 суток (р < 0,05). Функция кишечника (отхождение газов) у пациентов основной группы восстановилась через 1,5 ± 0,8 суток, в контрольной группе — через 3,5 ± 1 сутки (р < 0,05). Активизация больных (больным разрешено передвигаться в пределах палаты и по коридору отделения) в основной группе происходила через 1,5 ± 0,5 суток, в контрольной — 2,0 ± 0,5 суток (р < 0,05). Длительность послеоперационного госпитального периода в основной группе в среднем составила 4 ± 1,15 суток, в контрольной группе — 12,14 ± 1,4 суток (р < 0,05). Следует отметить, что выписка пациента на амбулаторное лечение после МХЭ при отсутствии осложнений возможна уже на 3–4 сутки, однако в связи с существующими медико-экономическими стандартами, лечение в стационарах продолжается до 7–8 суток.
С целью определения оптимальных сроков для успешного выполнения холецистэктомии из малотравматичных доступов нами был проведен анализ всех случаев конверсии доступа. В результате исследования установлено, что наиболее частыми причинами расширения операционной раны стали:
-
выраженный спаечный процесс и плотный инфильтрат в подпеченочном пространстве (7 пациентов);
-
кровотечение из культи желчного пузыря в условиях выраженных воспалительных изменений (1 пациент);
-
атипичное строение элементов треугольника Кало и трудности дифференциации в условиях инфильтрата (1 пациент).
На основании анализа мы пришли к выводу, что необходимость в конверсии доступа во многом зависит как от операционной ситуации в каждом конкретном случае, так и от опыта оперирующего хирурга. Наибольшее количество конверсий (7 случаев) пришлось на период освоения метода, в позднем периоде нашей работы число конверсий доступа значительно сократилось. Более того, в процессе совершенствования оперативной техники парапузырные осложнения не всегда являлись показанием к конверсии. Все конверсии, кроме одной (0,98%), были выполнены в сроки после 72 часов от начала заболевания. В последующем для уменьшения количества парапузырных осложнений и неоправданного затягивания консервативной терапии мы старались придерживаться более активной хирургической тактики лечения мини-инвазивными методами в сроки до 72 часов при неэффективности консервативной терапии в течение 12–24 часов.
Таким образом, мы считаем, что оптимальным сроком для выполнения ХЭ из малотравматичных доступов при ОХ без клинико-инструментальных признаков поражения внепеченочных желчных протоков может служить длительность заболевания не более 72 часов и поздние сроки, если нет УЗ признаков парапузырных осложнений. Наличие последних не является абсолютным противопоказанием.
Таким образом, на основании обобщенных данных литературы и собственных результатов, ХЭ из малотравматичных доступов может быть противопоказана в следующих случаях:
-
деструктивный холецистит с развитием диффузного перитонита;
-
необходимость корригировать оперативным путем другие хирургические заболевания из широкого лапаротомного доступа, если этого невозможно выполнить лапароскопическим путем;
-
воспалительные изменения тканей передней брюшной стенки;
-
выраженные рубцово-инфильтративные изменения в области шейки желчного пузыря и печеночно-двенадцатиперстной связки и плотный инфильтрат;
-
общие противопоказания при ЛХЭ и МХЭ (нарушение свертываемости, портальная гипертензия, поздние сроки беременности и т. д.).
С приобретением достаточных навыков операции из мини-доступа и видеолапароскопической техники при остром холецистите мы пришли к выводу, что они имеют значительные преимущества перед традиционной холецистэктомией за счет минимальной травмы передней брюшной стенки.
Со временем нам удалось улучшить полученные результаты, сократив средние сроки госпитализации при проведения малоинвазивных вмешательств до 3–5 суток. Также сокращены сроки принятия решения о хирургическом лечении до 12 часов.
Заключение
Выполненные по строгим показаниям МХЭ либо ЛХЭ сопровождаются незначительным числом осложнений, большинство из которых не являются тяжелыми, сокращаются сроки пребывания больных в стационаре, достигается хороший косметический эффект, больные раньше возвращаются к прежнему социально активному образу жизни. Все вышеперечисленные преимущества позволяют рекомендовать МХЭ и ЛХЭ для более широкого внедрения в клиническую практику при лечении больных острым холециститом.
Литература
Черепанин А. И., Луцевич О. Э., Галлямов Э. А., Поветкин А. П. Острый холецистит // М.: ГЭОТАР-Медиа, 2016. — 224 с.
Gutt CN, Encke J, Köninger J, et al (Acute Cholecystitis: Early Versus Delayed Cholecystectomy, A Multicenter Randomized Trial // Ann Surg. 2013; 258: p. 385–393.
Yokoe M. et al. New diagnostic criteria and severity assessment of acute cholecystitis in revised Tokyo guidelines // J HepatobiliaryPancreat Sci. — 2012. — 19. p. 578–585.
Yokoe M. et al. TG13 diagnostic criteria and severity grading of acute cholecystitis (with videos) // J HepatobiliaryPancreat Sci. — 2013. — 20. p. 35–46.
Материалы являются авторскими, перепечатка разрешена только с письменного согласия редакции.
Review
doi: 10.1002/jhbp.509.
Epub 2018 Jan 8.
Kohji Okamoto
2
, Tadahiro Takada
1
, Steven M Strasberg
3
, Horacio J Asbun
4
, Henry A Pitt
5
, Harumi Gomi
6
, Joseph S Solomkin
7
, David Schlossberg
5
, Ho-Seong Han
8
, Myung-Hwan Kim
9
, Tsann-Long Hwang
10
, Miin-Fu Chen
11
, Wayne Shih-Wei Huang
11
, Seiki Kiriyama
12
, Takao Itoi
13
, O James Garden
14
, Kui-Hin Liau
15
, Akihiko Horiguchi
16
, Keng-Hao Liu
11
, Cheng-Hsi Su
17
, Dirk J Gouma
18
, Giulio Belli
19
, Christos Dervenis
20
, Palepu Jagannath
21
, Angus C W Chan
22
, Wan Yee Lau
23
, Itaru Endo
24
, Kenji Suzuki
25
, Yoo-Seok Yoon
8
, Eduardo de Santibañes
26
, Mariano Eduardo Giménez
27
, Eduard Jonas
28
, Harjit Singh
29
, Goro Honda
30
, Koji Asai
31
, Yasuhisa Mori
32
, Keita Wada
1
, Ryota Higuchi
33
, Manabu Watanabe
31
, Toshiki Rikiyama
34
, Naohiro Sata
35
, Nobuyasu Kano
36
, Akiko Umezawa
37
, Shuntaro Mukai
13
, Hiromi Tokumura
38
, Jiro Hata
39
, Kazuto Kozaka
40
, Yukio Iwashita
41
, Taizo Hibi
42
, Masamichi Yokoe
43
, Taizo Kimura
25
, Seigo Kitano
44
, Masafumi Inomata
41
, Koichi Hirata
45
, Yoshinobu Sumiyama
46
, Kazuo Inui
47
, Masakazu Yamamoto
33
Affiliations
-
PMID:
28941329
-
DOI:
10.1002/jhbp.509
Free article
Review
Tokyo Guidelines 2018: initial management of acute biliary infection and flowchart for acute cholangitis
Fumihiko Miura et al.
J Hepatobiliary Pancreat Sci.
2018 Jan.
Free article
Abstract
The initial management of patients with suspected acute biliary infection starts with the measurement of vital signs to assess whether or not the situation is urgent. If the case is judged to be urgent, initial medical treatment should be started immediately including respiratory/circulatory management if required, without waiting for a definitive diagnosis. The patient’s medical history is then taken; an abdominal examination is performed; blood tests, urinalysis, and diagnostic imaging are carried out; and a diagnosis is made using the diagnostic criteria for cholangitis/cholecystitis. Once the diagnosis has been confirmed, initial medical treatment should be started immediately, severity should be assessed according to the severity grading criteria for acute cholangitis/cholecystitis, and the patient’s general status should be evaluated. For mild acute cholangitis, in most cases initial treatment including antibiotics is sufficient, and most patients do not require biliary drainage. However, biliary drainage should be considered if a patient does not respond to initial treatment. For moderate acute cholangitis, early endoscopic or percutaneous transhepatic biliary drainage is indicated. If the underlying etiology requires treatment, this should be provided after the patient’s general condition has improved; endoscopic sphincterotomy and subsequent choledocholithotomy may be performed together with biliary drainage. For severe acute cholangitis, appropriate respiratory/circulatory management is required. Biliary drainage should be performed as soon as possible after the patient’s general condition has been improved by initial treatment and respiratory/circulatory management. Free full articles and mobile app of TG18 are available at: http://www.jshbps.jp/modules/en/index.php?content_id=47. Related clinical questions and references are also included.
Keywords:
Acute cholangitis; Acute cholecystitis; Biliary drainage; Guidelines; Initial treatment.
© 2018 Japanese Society of Hepato-Biliary-Pancreatic Surgery.
Similar articles
-
Tokyo Guidelines 2018: management bundles for acute cholangitis and cholecystitis.
Mayumi T, Okamoto K, Takada T, Strasberg SM, Solomkin JS, Schlossberg D, Pitt HA, Yoshida M, Gomi H, Miura F, Garden OJ, Kiriyama S, Yokoe M, Endo I, Asbun HJ, Iwashita Y, Hibi T, Umezawa A, Suzuki K, Itoi T, Hata J, Han HS, Hwang TL, Dervenis C, Asai K, Mori Y, Huang WS, Belli G, Mukai S, Jagannath P, Cherqui D, Kozaka K, Baron TH, de Santibañes E, Higuchi R, Wada K, Gouma DJ, Deziel DJ, Liau KH, Wakabayashi G, Padbury R, Jonas E, Supe AN, Singh H, Gabata T, Chan ACW, Lau WY, Fan ST, Chen MF, Ker CG, Yoon YS, Choi IS, Kim MH, Yoon DS, Kitano S, Inomata M, Hirata K, Inui K, Sumiyama Y, Yamamoto M.
Mayumi T, et al.
J Hepatobiliary Pancreat Sci. 2018 Jan;25(1):96-100. doi: 10.1002/jhbp.519. Epub 2017 Dec 16.
J Hepatobiliary Pancreat Sci. 2018.PMID: 29090868
Review.
-
TG13 flowchart for the management of acute cholangitis and cholecystitis.
Miura F, Takada T, Strasberg SM, Solomkin JS, Pitt HA, Gouma DJ, Garden OJ, Büchler MW, Yoshida M, Mayumi T, Okamoto K, Gomi H, Kusachi S, Kiriyama S, Yokoe M, Kimura Y, Higuchi R, Yamashita Y, Windsor JA, Tsuyuguchi T, Gabata T, Itoi T, Hata J, Liau KH; Tokyo Guidelines Revision Comittee.
Miura F, et al.
J Hepatobiliary Pancreat Sci. 2013 Jan;20(1):47-54. doi: 10.1007/s00534-012-0563-1.
J Hepatobiliary Pancreat Sci. 2013.PMID: 23307003
-
Tokyo Guidelines 2018: flowchart for the management of acute cholecystitis.
Okamoto K, Suzuki K, Takada T, Strasberg SM, Asbun HJ, Endo I, Iwashita Y, Hibi T, Pitt HA, Umezawa A, Asai K, Han HS, Hwang TL, Mori Y, Yoon YS, Huang WS, Belli G, Dervenis C, Yokoe M, Kiriyama S, Itoi T, Jagannath P, Garden OJ, Miura F, Nakamura M, Horiguchi A, Wakabayashi G, Cherqui D, de Santibañes E, Shikata S, Noguchi Y, Ukai T, Higuchi R, Wada K, Honda G, Supe AN, Yoshida M, Mayumi T, Gouma DJ, Deziel DJ, Liau KH, Chen MF, Shibao K, Liu KH, Su CH, Chan ACW, Yoon DS, Choi IS, Jonas E, Chen XP, Fan ST, Ker CG, Giménez ME, Kitano S, Inomata M, Hirata K, Inui K, Sumiyama Y, Yamamoto M.
Okamoto K, et al.
J Hepatobiliary Pancreat Sci. 2018 Jan;25(1):55-72. doi: 10.1002/jhbp.516. Epub 2017 Dec 20.
J Hepatobiliary Pancreat Sci. 2018.PMID: 29045062
Review.
-
Tokyo Guidelines 2018: diagnostic criteria and severity grading of acute cholangitis (with videos).
Kiriyama S, Kozaka K, Takada T, Strasberg SM, Pitt HA, Gabata T, Hata J, Liau KH, Miura F, Horiguchi A, Liu KH, Su CH, Wada K, Jagannath P, Itoi T, Gouma DJ, Mori Y, Mukai S, Giménez ME, Huang WS, Kim MH, Okamoto K, Belli G, Dervenis C, Chan ACW, Lau WY, Endo I, Gomi H, Yoshida M, Mayumi T, Baron TH, de Santibañes E, Teoh AYB, Hwang TL, Ker CG, Chen MF, Han HS, Yoon YS, Choi IS, Yoon DS, Higuchi R, Kitano S, Inomata M, Deziel DJ, Jonas E, Hirata K, Sumiyama Y, Inui K, Yamamoto M.
Kiriyama S, et al.
J Hepatobiliary Pancreat Sci. 2018 Jan;25(1):17-30. doi: 10.1002/jhbp.512. Epub 2018 Jan 5.
J Hepatobiliary Pancreat Sci. 2018.PMID: 29032610
Review.
-
Tokyo Guidelines 2018: antimicrobial therapy for acute cholangitis and cholecystitis.
Gomi H, Solomkin JS, Schlossberg D, Okamoto K, Takada T, Strasberg SM, Ukai T, Endo I, Iwashita Y, Hibi T, Pitt HA, Matsunaga N, Takamori Y, Umezawa A, Asai K, Suzuki K, Han HS, Hwang TL, Mori Y, Yoon YS, Huang WS, Belli G, Dervenis C, Yokoe M, Kiriyama S, Itoi T, Jagannath P, Garden OJ, Miura F, de Santibañes E, Shikata S, Noguchi Y, Wada K, Honda G, Supe AN, Yoshida M, Mayumi T, Gouma DJ, Deziel DJ, Liau KH, Chen MF, Liu KH, Su CH, Chan ACW, Yoon DS, Choi IS, Jonas E, Chen XP, Fan ST, Ker CG, Giménez ME, Kitano S, Inomata M, Mukai S, Higuchi R, Hirata K, Inui K, Sumiyama Y, Yamamoto M.
Gomi H, et al.
J Hepatobiliary Pancreat Sci. 2018 Jan;25(1):3-16. doi: 10.1002/jhbp.518. Epub 2018 Jan 9.
J Hepatobiliary Pancreat Sci. 2018.PMID: 29090866
Review.
Cited by
-
Successful Treatment of a Case of Metallo-Beta-Lactamase-Producing Raoultella ornithinolytica Bacteremia by Antimicrobial Stewardship Team Intervention and Therapeutic Drug Monitoring-Based Amikacin Treatment.
Koishi N, Sasano H, Yoshizawa T, Shikuri M, Matsumoto H, Suzuki M, Fukui Y, Chonan M, Kimura T, Ichida H, Saiura A, Naito T.
Koishi N, et al.
Case Rep Infect Dis. 2023 Apr 7;2023:5574769. doi: 10.1155/2023/5574769. eCollection 2023.
Case Rep Infect Dis. 2023.PMID: 37065978
Free PMC article. -
Characteristics and clinical outcomes of acute cholangitis in older patients.
Acehan F, Çamlı H, Kalkan C, Tez M, Altiparmak E, Ates I.
Acehan F, et al.
Eur Geriatr Med. 2023 Apr;14(2):263-273. doi: 10.1007/s41999-023-00763-4. Epub 2023 Mar 21.
Eur Geriatr Med. 2023.PMID: 36941485
-
Bile duct penetrating duodenal wall sign: a novel computed tomography finding of common bile duct stone impaction into duodenal major papilla.
Shintani S, Inatomi O, Bamba S, Imai T, Tomozawa Y, Inoue A, Ota S, Takeda Y, Fujimoto T, Nishida A, Kutsumi H, Watanabe Y, Andoh A.
Shintani S, et al.
Jpn J Radiol. 2023 Mar 9. doi: 10.1007/s11604-023-01406-1. Online ahead of print.
Jpn J Radiol. 2023.PMID: 36892785
-
Comparison between Comprehensive Complication Index (CCI®) and Clavien-Dindo Classification for laparoscopic single-stage treatment of choledocholithiasis with concomitant cholelithiasis.
Llàcer-Millán E, Pavel MC, Memba R, Coronado D, González S, Achalandabaso M, Estalella L, Julià-Verdaguer E, Padilla-Zegarra E, Collins C, Jorba R.
Llàcer-Millán E, et al.
Langenbecks Arch Surg. 2023 Feb 23;408(1):100. doi: 10.1007/s00423-023-02840-5.
Langenbecks Arch Surg. 2023.PMID: 36813935
-
Is Ultrasound-guided Bedside Percutaneous Transhepatic Biliary Drainage Safe and Feasible in Critically Ill Patients with Severe Cholangitis? A Preliminary Single-center Experience.
Singh J, Tripathy TP, Patel R, Chandel K.
Singh J, et al.
Indian J Crit Care Med. 2023 Jan;27(1):16-21. doi: 10.5005/jp-journals-10071-24379.
Indian J Crit Care Med. 2023.PMID: 36756467
Free PMC article.
Publication types
MeSH terms
Substances
LinkOut — more resources
-
Full Text Sources
- CORE
- Ovid Technologies, Inc.
- Wiley
-
Other Literature Sources
- scite Smart Citations
-
Medical
- ClinicalTrials.gov
-
Research Materials
- NCI CPTC Antibody Characterization Program
Оглавление
Ключевые слова
- холецистит,
- острый холецистит,
- холецистэктомия,
- холецистостомия,
- холедохолитиаз,
- холангит,
- механическая желтуха
Список сокращений
ЖКБ – желчнокаменная болезнь
УЗИ – ультразвуковое исследование
МРТ – магнитно-резонансная томография
РКИ – рандомизированное клиническое исследование
ЛХЭ – лапароскопическая холецистэктомия
ОХ – острый холецистит
БДС – большой дуоденальный сосочек
ОЖП – общий желчный проток
ЭРХПГ — эндоскопическая ретроградная холангиопанкреатография
ЧЧХС – чрескожная чреспеченочная холангиостомия
ТЭЛА – тромбоэмболия легочной артерии
УДД – уровень достоверности доказательств
УУР – уровень убедительности рекомендаций
Термины и определения
Доказательная
медицина – подход к медицинской практике, при котором решения о
применении профилактических, диагностических и лечебных мероприятий
принимаются исходя из имеющихся доказательств их эффективности и
безопасности, а такие доказательства подвергаются поиску, сравнению,
обобщению и широкому распространению для использования в интересах
пациентов.
Заболевание – возникающее в связи с воздействием патогенных факторов
нарушение деятельности организма, работоспособности, способности
адаптироваться к изменяющимся условиям внешней и внутренней среды при
одновременном изменении защитно-компенсаторных и
защитно-приспособительных реакций и механизмов организма.
Инструментальная диагностика – диагностика с использованием для
обследования больного различных приборов, аппаратов и инструментов.
Лабораторная диагностика – совокупность методов, направленных на
анализ исследуемого материала с помощью различного специализированного
оборудования.
Медицинское вмешательство – выполняемые медицинским работником и иным
работником, имеющим право на осуществление медицинской деятельности, по
отношению к пациенту, затрагивающие физическое или психическое
состояние человека и имеющие профилактическую, диагностическую,
лечебную, реабилитационную или исследовательскую направленность виды
медицинских обследований и (или) медицинских манипуляций, а также
искусственное прерывание беременности.
Медицинский работник – физическое лицо, которое имеет медицинское или
иное образование, работает в медицинской организации и в трудовые
(должностные) обязанности которого входит осуществление медицинской
деятельности, либо физическое лицо, которое является индивидуальным
предпринимателем, непосредственно осуществляющим медицинскую
деятельность.
Рабочая группа – двое или более людей одинаковых или различных
профессий, работающих совместно и согласованно в целях создания
клинических рекомендаций, и несущих общую ответственность за результаты
данной работы.
Состояние – изменения организма, возникающие в связи с воздействием
патогенных и (или) физиологических факторов и требующие оказания
медицинской помощи.
Синдром – совокупность симптомов с общими этиологией и патогенезом.
Тезис – положение, истинность которого должна быть доказана аргументом, или опровергнута антитезисом.
Уровень достоверности доказательств – отражает степень уверенности в
том. что найденный эффект от применения медицинского вмешательства
является истинным.
Хирургическое вмешательство – инвазивная процедура, может
использоваться в целях диагностики и/или как метод лечения заболеваний.
Хирургическое лечение – метод лечения заболеваний путём разъединения и соединения тканей в ходе хирургической операции.
1. Краткая информация
1.1 Определение
Острый холецистит — воспаление желчного пузыря, сопровождающееся местной и системной воспалительной реакцией.
1.2 Этиология и патогенез
Острый холецистит является самым частым осложнением ЖКБ. Примерно в
90% наблюдений острый холецистит развивается на фоне ЖКБ, а в 10% — при
отсутствии камней в желчном пузыре и поэтому обозначается как острый
бескаменный холецистит (часто развивается у тяжелобольных пожилого
возраста и сопровождается большим числом осложнений и более высокой
летальностью).
Основной причиной возникновения острого воспаления и некробиотических
процессов в стенке пузыря является повышение внутрипузырного давления
до 200-300 мм вод. ст. Как правило (90-95%), оно возникает из-за
нарушения оттока желчи из желчного пузыря в результате обтурации камнем,
комочком слизи или желчным шламмом и др. В патогенезе заболевания
(острого воспаления) важное значение придают лизолецитину
(конвертируется из лецитина желчи фосфолипазой А, высвобождающейся при
травме слизистой желчного пузыря) и повышенной продукции простагландинов
Е и F1a. Возникновение желчной гипертензии является главным фактором в
уменьшении кровоснабжения слизистой желчного пузыря. Снижение
гемоперфузии стенки (особенно в пожилом и старческом возрасте при
наличии склеротических изменений) способствует нарушению слизистого
барьера, проникновению и росту микроорганизмов (выделяют из желчи и
стенки желчного пузыря в 50-60% наблюдений; в 75% выделяют анаэробы),
что в свою очередь увеличивает воспалительную экссудацию в просвет
органа. Очевидно, что процесс экссудации сам по себе ведет к дальнейшему
увеличению внутрипузырного давления, еще большему нарушению
микроциркуляции, усилению повреждения слизистой. Таким образом
формируется патофизиологический порочный «замкнутый круг». У 10-15%
больных ишемия стенки желчного пузыря, развивающаяся на фоне
внутрипузырной гипертензии, приводит к некрозу, перфорации, местному или
диффузному перитониту. Чаще формируется перивезикальный (подпеченочный,
поддиафрагмальный) абсцесс. При газообразующей флоре –
эмфизематозный желчный пузырь.
1.3 Эпидемиология
Заболевания желчного пузыря и желчевыводящих путей — распространенная
патология внутренних органов. ЖКБ страдают до 20% взрослого населения
развитых стран. Число больных с заболеваниями желчевыводящих путей
вдвое превышает число лиц, страдающих гастродуоденальной язвенной
болезнью. В последние годы заболеваемость острым холециститом в стране
возросла в 5 раз.
Холецистэктомии подвергается ежегодно от 350 000 до 500 000 человек,
летальность при этом близка к 1,5%. Сравнительно низкая летальность
достигнута частично за счет относительно раннего выполнения большинства
операций в плановом порядке, вне выраженного обострения холецистита,
частично – за счет широкого внедрения миниинвазивных хирургических
технологий.
1.4 Кодирование по МКБ 10
К80.0 — камни желчного пузыря с острым холециститом
К81.0 — острый холецистит
К80.4 — камни желчного протока с холециститом
К82.2 — прободение желчного пузыря
К83.0 — холангит
1.5 Классификация
По этиологии: калькулезный, бескаменный, паразитарный
По патогенезу: обтурационный, ферментативный, сосудистый
Клинико-морфологические формы: катаральный (обструктивный или
обтурационный), флегмонозный, гангренозный, перфоративный
(деструктивный).
По клиническому течению: легкое, среднетяжелое, тяжелое
2. Диагностика
2.1 Жалобы и анамнез
- Рекомендовано при опросе обратить внимание на боли в правом
подреберье и/или эпигастральной области, иногда с иррадиацией в
поясничную область, сопровождающиеся тошнотой и рвотой.
Уровень убедительности рекомендаций B (уровень достоверности доказательств 4)
Комментарии: Зачастую развитию острого
холецистита предшествуют эпизоды печеночной колики. Необходимо обратить
внимание на наличие в анамнезе эпизодов желтухи и панкреатита.
2.2 Физикальное обследование
- Рекомендовано
при пальпации живота обратить внимание на болезненность и
напряжение мышц в правом подреберье и/или эпигастрии.
Уровень убедительности рекомендаций B (уровень достоверности доказательств 4)
Комментарии: Клинические симптомы острого
холецистита имеют высокую чувствительность и высокую специфичность и
должны быть определены до инструментально-лабораторного обследования
больного. На основании физикального обследования диагноз острого
холецистита не может быть достоверно установлен или отвергнут.
Патогномоничных симптомов острого холецистита нет, хотя сочетание ряда
клинических и лабораторных признаков имеют высокую чувствительность и
специфичность.
Клинические проявления заболевания можно сгруппировать следующим образом:
Местные признаки воспаления желчного пузыря:
Боль имеет место у 72-93% пациентов. Далее по частоте следуют
тошнота и рвота. Мышечная защита имеет место в половине наблюдений,
пальпируемый желчный пузырь и положительный симптом ЩеткинаБлюмберга еще
реже.
Симптом
Мерфи имеет чувствительность до 65%, однако большинство работ
свидетельствует, что диагноз острого холецистита не может быть ни
достоверно поставлен, ни достоверно отвергнут на основании симптома
Мерфи.
Системные
признаки воспаления при остром холецистите: Лихорадка, повышение уровня
С-реактивного белка, лейкоцитоз, в сочетании с ультразвуковой картиной
острого холецистита, имеют чувствительность (до 97%), специфичность
(76%) и положительную прогнозирующую ценность 95% — следует использовать
в процессе принятия решения о диагнозе.
У больных старшей возрастной группы и/или у больных с сахарным
диабетом возможна стертая картина болезни, отсутствие признаков
системной воспалительной реакции и незначительная болезненность при
глубокой пальпации при наличии деструктивных изменений в стенке желчного
пузыря. [32, 118, 51]
2.3 Лабораторная диагностика
- Рекомендовано выполнить Общий анализ крови, биохимический
анализ крови, с определением уровня глюкозы, билирубина, креатинина,
амилазы крови, АЛТ, АСТ, ЩФ, коагулограмму, определение группы крови и
Rh-фактора.
Уровень убедительности рекомендаций B (уровень достоверности доказательств 4)
Комментарии: Ни один лабораторный
анализ, равно как и их сочетание, не позволяют достоверно поставить или
отвергнуть диагноз острого холецистита.
Лабораторное обследование в плане диагностики ОХ
имеет вспомогательное значение и предназначено в основном для вынесения
решения о тяжести состояния больного. [118]
2.4 Инструментальная диагностика
- Рекомендовано выполнить ультразвуковое исследование (УЗИ) органов брюшной полости
Уровень убедительности рекомендаций B (уровень достоверности доказательств 2a)
Комментарии: Ультразвуковой диагноз острого калькулезного холецистита можно установить при наличии:
-увеличения продольного (>8 см) или поперечного (>4 см) размеров,
-утолщения стенки более 3 мм с признаками ее отека и нарушением эхоструктуры (слоистость и неоднородность, «двойной контур»)
-блокирующего конкремента в шейке желчного пузыря
-перивезикального жидкостного скопления.
Высокую специфичность и чувствительность показывает положительный
ультразвуковой симптом Мерфи, заключающийся в усилении или появлении
болей при надавливании датчиком на переднюю брюшную стенку в проекции
визуализируемого дна желчного пузыря при глубоком вдохе больного.
Следует отметить, что ни один из этих признаков сам по себе не
обладает достаточной информативностью для постановки диагноза, поэтому
при выполнении УЗИ необходимо учитывать их наличие в комплексе.
Утолщение стенки желчного пузыря может встречаться не только при остром
холецистите, но также при заболеваниях печени, сердечной и почечной
недостаточности, а также при гипопротеинемии и ряде других заболеваний и
состояний, не требующих неотложного хирургического вмешательства
УЗИ позволяет
дифференцировать острый
обструктивный (катаральный) и острый деструктивный холецистит и
выделить гангренозный холецистит на основании наличия плавающих
внутрипросветных мембран, очагов эхогенных затемнений в соответствии с
наличием газа внутри стенки или в просвете ЖП и явных нарушений
целостности стенки ЖП и перипузырного абсцесса. Особенно информативным
является динамическое УЗИ, выполняемое специально подготовленным
хирургом.
При подозрении на холедохолитиаз у больного с острым калькулезным
холециститом, УЗИ может служить только скрининговым исследованием,
выявляющим наличие желчной гипертензии. Для уточнения диагноза
необходима МРТ-холангиография, ретроградная холангиопанкреатография или
интраоперационная холангиография (интраоперационное УЗИ),
эндосонография. Применение высокотехнологичных дополнительных методов
исследования определяется их наличием в ЛПУ.
Следует отметить, что из всех визуализирующих методов,
максимальное совпадение с послеоперационным гистологическим
исследованием желчного пузыря дает радиоизотопное сканирование, которое
следует провести при наличии оснащения в сомнительных случаях. [11, 53, 63]
2.5 Иная диагностика
Дифференциальный диагноз при подозрении на острый холецистит включает ряд экстра- и интраабдоминальных заболеваний:
• правосторонняя нижнедолевая пневмония
• инфаркт миокарда
• болезненный опоясывающий лишай
• обострение
гастродуоденальной язвенной болезни, в т.ч. перфоративная язва
• острый панкреатит
• гепатит
• острая кишечная непроходимость
• острый аппендицит
Диагностический алгоритм при подозрении на острый холецистит не
отличается от такового при синдроме острых болей в верхней половине
живота.
В диагностически сложных случаях, исчерпав все неинвазивные методы
исследования, хирург должен прибегнуть к диагностической
видеолапароскопии, а при невозможности ее реализации или
неинформативности – к лапаротомии.
При
окончательной формулировке диагноза целесообразно использовать
классификацию Токийского соглашения по острому холециститу (Tokyo
guidelines (2007, 2013)). Эта классификация коррелирует с подходами по
систематизации информации об остром холецистите, которую используют в
отечественной хирургии.
Легкое течение (Grade I):
-острое воспаление желчного пузыря у соматически здоровых пациентов
без сопутствующих заболеваний с умеренными воспалительными изменениями в
стенке желчного пузыря (острый простой холецистит (Королев Б.А.,
Пиковский Д.Л.,1990 г.)) или острый обструктивный холецистит.
Среднетяжелое течение (Grade II):
-анамнез заболевания более 72 часов, пальпируемый желчный пузырь или инфильтрат в правом подреберье, лейкоцитоз более 18х109/л,
верифицированные деструктивные формы острого холецистита с развитием
перипузырных осложнений или желчного перитонита. Наличие одного из
перечисленных признаков позволяет отнести пациента к данной группе. По
терминологии Королева Б.А. и Пиковского Д.Л. (1990) – осложненный
холецистит, или острый деструктивный холецистит.
Тяжелое течение (Grade III):
острый холецистит, сопровождающийся полиорганной недостаточностью,
артериальная гипотония, требующая медикаментозной коррекции, нарушения
сознания, развитие респираторного дистресссиндрома взрослых, повышение
уровня креатинина в плазме, нарушения свертывания крови, тромбоцитопения
(угрожаемая группа, группа повышенного риска).
3. Лечение
Цель лечения — максимально
полное и быстрое снижение уровня общей и местной воспалительной реакции
за счет удаления желчного пузыря или ликвидации внутрипузырной
гипертензии.
При установленном диагнозе «Острый холецистит» пациент подлежит экстренной госпитализации в хирургическое отделение.
3.1Консервативное лечение
- Рекомендовано проведение консервативной терапии в качестве предоперационной подготовки.
Уровень убедительности рекомендаций B (уровень достоверности доказательств 4)
Комментарии: основой консервативной терапии являются: отказ от приема пищи и воды per os, внутривенное введение жидкости и антибактериальная терапия, особенно при наличии признаков обезвоживания и лихорадке.
Для купирования болевого синдрома возможно применение НПВП,
спазмолитиков или опиоидных анальгетиков. Следует отметить, что
использование аналгетиков не влияет на информативность динамического
наблюдения, в том числе на выявление УЗ-симптома Мерфи.
3.2 Хирургическое лечение
- Рекомендовано хирургическое лечение холецистита в срок – до 72 часов от начала заболевания.
Уровень убедительности рекомендаций C (уровень достоверности доказательств 3a)
Комментарии: При установленном диагнозе «Острый
холецистит» больной подлежит экстренной госпитализации в хирургическое
отделение. Цель лечения: максимально полное и быстрое снижение
уровня общей и местной воспалительной реакции за счет удаления желчного
пузыря или ликвидации внутрипузырной гипертензии.
Операция выполняется по мере завершения диагностического процесса
и готовности пациента в зависимости от степени тяжести его
состояния. В стационарах, не располагающих возможностью
круглосуточного адекватного до и интраоперационного обследования
больного и наличием операционной бригады достаточной квалификации,
выполнения «ночных» операций следует избегать.
Ранняя операция холецистэктомия может быть
успешно выполнена с помощью стандартной методики из лапаротомного
доступа, методом минихолецистэктомии или видеолапароскопической
холецистэктомии. [ 95]
- Рекомендовано выполнение видеолапароскопической холецистэктомии.
Уровень убедительности рекомендаций A (уровень достоверности доказательств 1b)
Комментарии: Такой подход обеспечивает
значительное снижение послеоперационной летальности и числа осложнений,
сокращению сроков госпитализации, быстрое выздоровление и возврат к
труду. Анализ РКИ показывает, что при ЛХЭ ниже частота бактериемии и
эндотоксинемии, менее выражены признаки SIRS у больных ОХ с явлениями
перитонита, у пациентов старше 65 лет результаты ЛХЭ достоверно ниже по
числу летальных исходов, послеоперационных осложнений как сердечных, так
и респираторных. При остром, в том числе и гангренозном холецистите,
ЛХЭ безопасна и дает меньше осложнений после операции, чем ОХ.
Число конверсий при ранних операциях (ЛХЭ) достигает 10-15%, т.е. выше,
чем при плановых операциях.
При поступлении больного позже оптимального срока для проведения
ранней операции, видеолапароскопическая холецистэктомия возможна при ее
выполнении достаточно квалифицированным хирургом.
До
20% больных, при давности заболевания более 72 часов, требуют
оперативного лечения в связи с нарастанием воспалительных
явлений. Операция в эти сроки выполняется в условиях плотного
инфильтрата. ЛХЭ сопровождается высоким процентом конверсий и
значительное число публикаций рекомендуют открытую операцию. Решение о
выборе метода операции следует оставить за оперирующим хирургом, однако
опыт авторов рекомендаций говорит в пользу минилапаротомной
холецистэктомии.
- Рекомендованро при тяжелом течении острого холецистита у соматически осложненных пациентов выполнить холецистостомию. [78]
Уровень убедительности рекомендаций B (уровень достоверности доказательств 2b)
Комментарии: Оптимальный срок оперативного лечения острого холецистита – до 72 часов от начала заболевания.
Ранняя операция в вышеуказанные сроки уменьшает риск развития
послеоперационных осложнений и летальности, сокращает суммарное время
лечения и реабилитации.
При среднетяжелом течении острого холецистита ранняя
холецистэктомия должна выполняться опытным хирургом в хирургических
стационарах с достаточным опытом в желчной хирургии.
Ранняя (первые 24 – 72 часа от начала заболевания) лапароскопическая холецистэктомия максимально эффективна и безопасна.
Данные РКИ показывают значительно меньшее число осложнений и летальных исходов при ранних операциях по сравнению с отложенными. [10, 19, 55, 65, 84]
ВЫБОР МЕТОДА ОПЕРАЦИИ.
Лапароскопическая холецистэктомия при остром холецистите предпочтительнее открытой операции.
У больных старше 65 лет, при длительном анамнезе ЖКБ, непальпируемом желчном пузыре, лейкоцитозе более 13х109/л,
ультразвуковых признаках гангренозного холецистита – значительно
возрастает число конверсий при ЛХЭ. Этим больным предпочтительнее
минилапаротомная холецистэктомия или операция из срединного
лапаротомного доступа. При наличии достаточно большого опыта
видеолапароскопических операций при остром холецистите эта методика
может быть применена.
При
наличии острого холецистита и холедохолитиаза, при невозможности
или неэффективности эндоскопического восстановления оттока желчи,
минилапаротомная операция позволяет оставаться в поле миниинвазивной
технологии на достаточном уровне эффективности и безопасности. При
наличии достаточного опыта видеолапароскопических холедохолитотомий
подготовленная бригада может использовать этот вариант оперирования.
- При
возникновении технических трудностей рекомендовано выполнить
своевременную конверсию лапароскопического или минилапаротомного доступа
в открытую операцию до развития осложнений, в т.ч. повреждения
внепеченочных желчных протоков.
Уровень убедительности рекомендаций B (уровень достоверности доказательств 3a)
Комментарии: Холецистэктомия из
минилапаротомного доступа является эффективным и безопасным методом
хирургического лечения острого холецистита, число осложнений,
летальность и сроки реабилитации значительно лучше, чем при традиционном
оперировании.
Сравнение минилапаротомных и лапароскопических операции при ОХ по
данным РКИ показывает принципиально одинаковые результаты по числу
осложнений и летальных исходов. Длительность операции немного выше при
ЛХЭ, но короче и комфортнее послеоперационный период. Через месяц после
операции разницы в уровне восстановления жизненных функций нет.
Особенности оперативного лечения при сопутствующих заболеваниях и осложненном течении острого холецистита.
Минилапаротомия с использование комплекта инструментов
МиниАссистент особенно эффективна при наличии противопоказаний к
пневмоперитонеуму, отсутствии у хирурга достаточного опыта ЛХЭ при
деструктивных формах острого холецистита, сроках выполнения операции
более 72 часов от начала заболевания, необходимости манипуляций на
протоках.
Минилапаротомная холецистэктомия может быть использована в
качестве метода конверсии при возникновении технических трудностей при
лапароскопической операции.
Антибиотикопрофилактика и дренирование подпеченочного пространства.
- Рекомендовано выполнение антибиотикопрофилактики при остром холецистите .
(Уровень убедительности рекомендаций B (уровень достоверности доказательств 1b) [90]
Комментарии: При неосложненном течении
острого холецистита достаточно однократного периоперационного введения
антибиотика.Профилактическая доза антибиотика вводится в пределах одного
часа до начала операции (разреза!). При осложненном течении или
интраоперационной контаминации требуется дополнительное применение
антибиотиков
Выбор антибиотиков основывается на предполагаемом характере микробной флоры.
В большинстве случаев профилактическое применение антибиотиков не превышает срока в 24 часа.
Если пациент уже получает антибиотики, которые перекрывают
предполагаемый микробный спектр, интраоперационная профилактика не
требуется.
При длительности операции более 4 часов возможно повторное введение профилактической дозы антибиотиков.
Осложнения и их профилактика.
Интраоперационные осложнения включают кровотечения и травмы
желчных протоков. Риск травмы желчных протоков составляет от 36 до 47
ранений на 10000 пациентов при лапароскопической операции и от 19 до 29
случаев ранений на 10000 пациентов при лапаротомной операции.
Системный обзор РКИ из 541 пациента показал, что ранняя
лапароскопическая холецистэктомия и отсроченная лапароскопическая
холецистэктомия при остром холецистите имеют одинаковую частоту
повреждений желчных протоков и одинаковую частоту конверсий. Частота
повреждения внепеченочных желчных путей не превышает 1%.
Профилактика интраоперационных осложнений заключается в строгом
соблюдении рекомендаций по срокам выполнения операции при остром
холецистите, своевременном переходе (конверсии) на минилапаротомию
или открытую методику оперирования, тщательное соблюдение правил
выполнения операции.
При выполнении операции холецистэктомии неподготовленным хирургом прогнозировать риск осложнений невозможно.
Послеоперационные осложнения: пластинчатые ателектаз и пневмония, инфаркт миокарда, тромбоэмболические осложнения, ТЭЛА.
В качестве профилактики вышеперечисленных осложнений прежде всего
должны использоваться современные миниинвазивные методы оперирования.
Ранняя активизация, раннее начало орального питания, адекватное
обезболивание и медикаментозная профилактика ВТО по показаниям.
Прогноз при своевременно проведенном радикальном лечении острого
холецистита легкой и средней тяжести прогноз благоприятный. У больных
угрожаемой группы прогноз в основном зависит от характера и степени
компенсации сопутствующих заболеваний.
4. Реабилитация
- Ранний стационарный этап (первые двое суток), когда максимально проявляются изменения, вызванные операцией и наркозом.
- Поздний стационарный этап (3-6 сутки при лапароскопии и до 14
суток при лапаротомии), когда происходит восстановление функций
дыхательной системы, начинается адаптация желудочно-кишечного тракта к
работе при отсутствующем желчном пузыре, активируются процессы
регенерации в зоне вмешательства. - Амбулаторная реабилитация (1–3 месяца в зависимости от типа
операции), когда полностью восстанавливаются функции пищеварительной и
дыхательной систем, физическая активность пациента. - Активное санаторно-курортное лечение проводится через 6–8 месяцев.
5. Профилактика и диспансерное наблюдение
Контрольные обследования пациента:
- осмотр врачом-хирургом и врачом-терапевтом на 3 день после выписки, затем через 1 и 3 недели;
- клинический и биохимический анализы крови через 2 недели после выписки и через 1 год;
- УЗИ назначается в первый месяц по показаниям, через 1 год всем пациентам.
Лечебно-оздоровительные мероприятия:
- постепенное наращивание нагрузки на брюшной пресс (упражнения «ножницы», «велосипед»);
- увеличение темпа и длительности ходьбы;
- дыхательная гимнастика.
Диетотерапия:
- первые 2 месяца рекомендуется умеренная диета с нормальным содержанием белков, углеводов и жиров.
- необходимо исключить блюда, богатые пряностями, экстрактивными веществами, жирное, жареное.
- продукты следует готовить на пару, запекать, отваривать.
- прием пищи небольшими порциями каждые 3 часа.
- после приема пищи в течение 2 часов не следует работать в наклон или ложиться.
- последний прием пищи должен быть как минимум за полтора часа до сна.
6. Дополнительная информация, влияющая на течение и исход заболевания
Острый холецистит, осложненный механической желтухой
Как правило, механическая желтуха обусловлена камнями
супрадуоденального или терминального отдела гепатикохоледоха или его
стриктурой в сочетании с холедохолитиазом. Вероятность одновременного
существования конкрементов в желчном пузыре и протоках при остром
калькулезном холецистите достигает 20% и более.
Практически можно выделить три варианта клинического течения:
— неинфицированный тип окклюзии общего желчного протока
— вклиненный камень БСДК, острый панкреатит
— вклиненный камень ОЖП, холангит
При этом возможен любой вариант острого холецистита – от катарального до гангренозного.
- Ультразвуковое
исследование не обладает достаточной степенью информативности по
отношению к холедохолитиазу и может лишь ориентировать на наличие
признаков желчной гипертензии.
Для
уточнения диагноза рекомендована МР-холангиопанкреатография,
эндоскопическая ретроградная холангиопанкреатография, интраоперационная
холангиография и/или интраоперационное ультразвуковое исследование.
(Уровень убедительности рекомендаций B (уровень достоверности доказательств 1b) [13, 40]
Комментарии:Предпочтительным
следует считать выполнение эндоскопической трансдуоденальной
папиллосфинктеротомии и санации гепатикохоледоха с последующей
холецистэктомией, выполненной одномоментно или в течение ближайших
дней.
При доминировании клиники острого деструктивного холецистита, а также при
невозможности или неэффективности эндоскопического восстановления
желчеоттока, показана одномоментная операция: холецистэктомия,
холедохолитотомия, наружное дренирование холедоха по показаниям.
У
больных угрожаемой группы, при наличии холангита с полиорганной
дисфункцией, методом выбора является этапное лечение. Основой его
являются декомпрессия желчного пузыря и декомпрессия ОЖП.
Чрескожная чреспеченочная холецистостомия считается безопасной
альтернативной манипуляцией по сравнению с одномоментной операцией у
пациентов высокого хирургического риска.
Эндоскопический назо-билиарный дренаж и стентирование
гепатикохоледоха через траспапиллярный эндоскопический доступ также
являются альтернативой в лечении острого холецистита, осложненного
механической желтухой и холангитом. Однако оба метода имеют серьезные
технические трудности и показатели их успешности ниже, чем ЧЧХС.9%%
Критерии оценки качества медицинской помощи
|
№ |
Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
|
1 |
Выполнен осмотр врачом-хирургом не позднее 1 часа от момента поступления в стационар |
4 |
D |
|
2 |
Выполнен |
4 |
D |
|
3 |
Выполнено ультразвуковое исследование органов брюшной полости не позднее 2 часов от момента поступления в стационар |
4 |
D |
|
4 |
Начато |
4 |
D |
|
5. |
Выполнено |
4 |
D |
|
6. |
Выполнена |
4 |
D |
|
7. |
Выполнено морфологическое (гистологическое) исследование препарата желчного пузыря (при хирургическом вмешательства) |
4 |
D |
|
8. |
Выполнено бактериологическое исследование экссудата из |
4 |
D |
|
9. |
Выполнена холецистостомия (при наличии медицинских противопоказаний к хирургическому вмешательству) |
4 |
D |
|
10. |
Отсутствие повторных хирургических вмешательств в период госпитализации (при хирургическом вмешательстве) |
4 |
D |
|
11. |
Отсутствие тромбоэмболических осложнений в период госпитализации |
4 |
D |
|
12. |
Отсутствие гнойно-септических осложнений в период госпитализации |
4 |
D |
Список литературы
- Adedeji OA, McAdam WA. Murphy’s sign, acute cholecystitis and elderly people. J R Coll Surg Edinb. 1996;41:88–89.
- Adusumilli S, Siegelman ES. MR imaging of the gallbladder. Magn Reson Imaging Clin N Am 2002; 10: 165–184.
- Akhan O, Akinci D, Ozmen MN. (2002) Percutaneous cholecystostomy. Eur J Radiol 43:229– 236.
- Akriviadis EA, Hatzigavriel M, Kapnias D, Kirimlidis J, Markantas A,
Garyfallos A. Treatment of biliary colic with diclofenac: a randomized,
double-blind, placebo-controlled study. Gastroenterology.
1997;113:225–231. - Araujo-Teixeria JP, Rocha-Reis J, Costa-Cabral A, Barros H, Saraiva
AC, Araujo-Teixeira AM. Laparoscopic versus open cholecystectomy for
cholecystitis (200 cases). Comparison of results and predictive factors
for conversion. Chirurgie. 1999;124:529–535 - Asai K, Watanabe M, Kusachi S, Tanaka H, Matsukiyo H, Osawa A, et
al. Bacteriological analysis of bile in acute cholecystitis according to
the Tokyo guidelines. J Hepatobiliary Pancreat Sci. 2012;19(4):476–486. - Barish MA, Soto JA. MR cholangiopancreatography: techniques and
clinical applications. AJR Am J Roentgenol1997; 169: 1295–1303. - Benarroch-Gampel J, Boyd CA, Sheffield KM, Townsend CM, Jr, Riall
TS. Overuse of CT in patients with complicated gallstone disease. J Am
Coll Surg. 2011;213:524–530 - Berrgren U, Gordh T, Grama D, Haglund U, Rastad J, Arvidsson D.
Laparoscopic versus open cholecystectomy: hospitalization, sick leave,
analgesia and trauma responses. Br J Surg. 1994;81:1362–1365 - Boo YJ, Kim WB, Kim J, Song TJ, Choi SY, Kim YC, Suh SO. Systemic
immune response after open versus laparoscopic cholecystectomy in acute
cholecystitis: a prospective randomized study. Scand J Clin Lab Invest.
2007;67:207–14. - Borzellino G, Massimiliano Motton A, Minniti F, Montemezzi S,
Tomezzoli A, Genna M. Sonographic diagnosis of acute cholecystitis in
patients with symptomatic gallstones. J Clin Ultrasound. 2016;44:152–8.
doi:10.1002/jcu.22305. Published online September 2015. - Borzellino G, Sauerland S, Minicozzi AM, et al. Laparoscopic
cholecystectomy for severe acute cholecystitis: a meta-analysis of
results. Surg Endosc. 2008;22:8-15. - Boys JA, Doorly MG, Zehetner J, Dhanireddy KK, Senagore AJ. Can
ultrasound common byle duct diameter predict common bile duct stones in
the setting of acute cholecystitis? Am J Surg. 2014;207:432. - Bree RL. Further observations on the usefulness of the sonographic
Murphy sign in the evaluation of suspected acute cholecystitis. J Clin
Ultrasound. 1995;23:169–172. - Brewer BJ, Golden GT, Hitch DC, Rudolf LE, Wangensteen SL. Abdominal
pain. An analysis of 1,000 consecutive cases in a University Hospital
emergency room. Am J Surg. 1976;131:219– 223. - Bridges MD, Jones BC, Morgan DE, Fell SC. Acute cholecystitis and
gallbladder necrosis: value of contrast enhanced helical CT. (abstr) AJR
1999:172[American Roentgen Ray Society 99th Annual Meeting Abstract
Book suppl]:34-35. - Brodsky A, Matter I, Sabo E, Cohen A, Abrahamson J, Eldar S.
Laparoscopic cholecystectomy for acute cholecystitis: can the need for
conversion and the probability of complications be predicted? A
prospective study. Surg Endosc. 2000;14:755–760. - Cameron IC, Chadwick C, Phillips J, Johnson AG. Management of acute
cholecystitis in UK hospitals: time for a charge. Postgrad Med J.
2004;80:292–294. - Catena F, Ansaloni L, Bianchi E, Di Saverio S, Coccolini F,
Vallicelli C, et al. The ACTIVE (Acute Cholecystitis Trial Invasive
Versus Endoscopic) study. Multicenter randomized, double-blind,
controlled trial of laparoscopic (LC) versus open (OC) surgery for acyte
cholecystitis (AC). Hepatogastroenterology. 2013;60(127):1552–6. - Chacon J, Criscuolo P, Kobata C, Ferraro J, Saad S, Reis C.
Prospective randomized comparison of pefloxacin and ampicillin plus
gentamicin in the treatment of bacteriologically proven biliary tract
infections. J Antimicrob Chemother. 1990;26,Suppl B:167–172. - Chandler CF, Lane JS, Ferguson P, Thonpson JE. Prospective
evaluation of early versus delayed laparoscopic cholecystectomy for the
treatment of acute cholecystitis. Am Surg. 2000;66(9):896– 900. - Chatziioannou SN, Moore WH, Ford PV, Dhekne RD. Hepatobiliary
scintigraphy is superior to abdominal ultrasonography in suspected acute
cholecystitis. Surgery. 2000;127:609–615. - Chikamori F, Kuniyosi N, Shibuya S, Takase Y. Early scheduled
laparoscopic cholecystectomy following percutaneous transhepatic
gallbladder drainage for patients with acute cholecystitis. Surg Endosc.
2002;16:1704–1707. - Chopra S, Dodd GD 3rd, Mumbower AL, Chintapalli KN, Schwesinger WH,
Sirinek KR, et al. Treatment of acute cholecystitis in non-critically
ill patients at high surgical risk: comparison of clinical outcomes
after gallbladder aspiration and after percutaneous cholecystostomy. AJR
Am J Roentgenol. 2001;176:1025–1031. - Cohan RH, Mahony BS, Bowie JD, Cooper C, Baker ME, Illescas FF.
Striated intramural gallbladder lucencies on US studies: predictors of
acute cholecystitis. Radiology. 1987;164:31– 3 5. - Cohen-Solal C, Parquet M, Tiffon B, et al. Magnetic resonance
imaging for the visualization of cholesterol gallstones in hamster fed a
new high sucrose lithogenic diet. J Hepatol1995; 22: 486–
494. - Csikesz Т., Ricciardi R., Tseng J.F., Shah S.,A. Current Status of
Surgical Management of Acute Cholecystitis in the United States. World J
Surg (2008) 32:2230-2236 - David V, Reinhold C, Hochman M, et al. Pitfalls in the
interpretation of MR cholangiopancreatography. AJR Am J Roentgenol1998;
170:1055–1059. - Davis CA, Landercasper J, Gundersen LH, Lambert PJ. Effective use of
percutaneous cholecystostomy in high-risk surgical patients:
techniques, tube management, and results. Arch Surg.
1999;134:727–731. - Donald JJ, Cheslyn-Curtis S, Gillams AR, Russell RC, Lees WR.
Percutaneous cholecystolithotomy: is gall stone recurrence inevitable?
Gut. 1994;35:692–695. - Edward A. McGillicuddy, M.D.Kevin M. Schuster, M.D. Elliott Brown,
M.D.Mark W. Maxfield, M.D.Kimberly A. Davis, M.D.Walter E. Longo, M.D.
Acute cholecystitis in the elderly: use of computed tomography and
correlation with ultrasonography The American Journal of Surgery Volume
202, Issue 5 , Pages 524-527, November 2011 - Eskelinen M, Ikonen J, Lipponen P. Diagnostic approaches in acute
cholecystitis; a prospective study of 1333 patients with acute abdominal
pain. Theor Surg. 1993;8:15–20. - Fidler J, Paulson EK, Layfield L. CT evaluation of acute
cholecystitis: findings and usefulness in diagnosis. AJR 1996; 166:1085
–1088 . - Fischer JE, editor. Mastery of Surgery. 5. Philadelphia: Lippincott Williams & Wilkins; 2007.
- Flowers JL, Bailey RW, Scovill WA, Zucker KA. The Baltimore
experience with laparoscopic management of acute cholecystitis. Am J
Surg. 1991;161:388–392. - Fulcher AS, Turner MA, Capps GW. MR cholangiography: technical
advances and clinical applications. RadioGraphics1999; 19: 25–44. - Giger U, Michel JM, Vonlanthen R, Becker K, Kocher T, Kr?henb?hl L.
Laparoscopic cholecystectomy in acute cholecystitis: indication,
technique, risk and outcome. Langenbecks Arch Surg. 2005;390(5):373–80. - Gruber PJ, Silverman RA, Gottesfeld S, Flaster E. Presence of fever
and leukocytosis in acute cholecystitis. Ann Emerg Med. 1996;28:273 - Gurusamy K, Samraj K, Glund C, Wilson E, Davidson R. Meta-analysis
of randomized control trials on the safety and effectiveness of early
versus delayed laparoscopic cholecystectomy for acute cholecystitis. Br J
Surg. 2010;97:141–150. - Gurusamy KS, Giljaca V, Takwoingi Y, Higgie D, Poropat G, ?timac D,
Davidson BR. Ultrasound versus liver function tests for diagnosis of
common bile duct stones. Cochrane Database Syst Rev. 2015;2:CD011548.
doi:10.1002/14651858.CD011548 - Gurusamy KS, Samraj K. Early versus delayed laparoscopic
cholecystectomy for acute cholecystitis. Cochrane Database Syst Rev.
2006;CD005440 - Gurusamy, K. Samraj // Cochrane Database of Systematic Reviews 2007
(edited 2009) , Issue 2. Art. No.: CD006003. DOI:
10.1002/14651858.CD006003.pub2. Электронный ресурс] URL:http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD006003.pub2/abstract;jsessionid=4
E510BE70A33F8030939A0CCCC7874FE.f01t02 - Gurusamy,
KS. Early versus delayed laparoscopic cholecystectomy for people with
acute cholecystitis // KS. Gurusamy et al. // CochraneDatabase of
Systematic Reviews 2013, Issue 6. Art.No.: CD005440. DOI:
10.1002/14651858.CD005440.pub3. - Gurusamy,
KS. Low pressure versus standard pressure pneumoperitoneum in
laparoscopic cholecystectomy / KS. Gurusamy, K. Samraj, BR.
Davidson // Cochrane Database of Systematic Reviews 2009, Issue 2. Art.
No.: CD006930. DOI: 10.1002/14651858.CD006930.pub2. - Gurusamy,
KS. Miniports versus standard ports for laparoscopic cholecystectomy /
KS. Gurusamy et al. // Cochrane Database of Systematic Reviews 2013,
Issue 8. Art. No.: CD006804. DOI:
10.1002/14651858.CD006804.pub3. - Gurusamy, KS. Routine abdominal drainage for uncomplicated open cholecystectomy/ KS.
- Hakansson
K, Leander P, Ekberg O, Hakansson HO. MR imaging in clinically
suspected acute cholecystitis: a comparison with ultrasonography. Acta
Radiol 2000; 41: 322–328. - Halachmi
S, DiCastro N, Matter I, Cohen A, Sabo E, Mogilner JG, et al.
Laparoscopic cholecystectomy for acute cholecystitis: how do fever and
leucocytosis relate to conversion and complications? Eur J Surg.
2000;166:136–140. - Hirota
M, Takada T, Kawarada Y, Nimura Y, Miura F, Hirata K, et al. Diagnostic
criteria and severity assessment of acute cholecystitis: Tokyo
Guidelines. J Hepatobiliary Pancreat Surg. 2007;14:78–82. (clinical
practice guidelines: CPGs). - Hultman
CS, Herbst CA, McCall JM, Mauro MA. The efficacy of percutaneous
cholecystostomy in critically ill patients. Am Surg.
1996;62:263–269. - Hwang
H, Marsh I, Doyle J. Does ultrasonography accurately diagnose acute
cholecystitis? Improving diagnostic accuracy based on a review at a
regional hospital. Can J Surg. 2014;57:162–8. - Hyung
OK, Byung HS, Chang HY, Jun HS. Impact of delayed laparoscopic
cholecystectomy after percutaneous transhepatic gallbladder drainage for
patients with complicated acute cholecystitis. Surg Laparosc Endosc
Percutan. 2009;19:20–24 . - Ito
K, Fujita N, Noda Y, et al. The significance of magnetic resonance
cholangiopancreatography in acute cholecystitis [in Japanese].Nippon
Shokakibyo Gakkai Zasshi 2000; 97: 1472–1479. - Jeffrey
RB, Liang FC, Wong W, Callen PW. Gangrenous cholecystitis: diagnosis by
ultrasound. Radiology 1983; 148:219-221. - Johansson
M, Thune A, Nelvin L, Stiernstam M, Westman B, Lundell L. Randomized
clinical trial of open versus laparoscopic cholecystectomy for acute
cholecystitis. Br J Surg. 2005;92:44– 49. - Johansson
M, Thune A, Nelvin L, Stiernstam M, Westman B, Lundell L. Randomized
clinical trial of open versus laparoscopic cholecystectomy for acute
cholecystitis. Br J Surg. 2005;92:44–9. - Johnson
AB, Fink AS. (1998) Alternative methods for management of the
complicated gall bladder. Semin Laparosc Surg 5:115–120. - Johnson
H Jr, Cooper B. The value of HIDA scans in the initial evaluation of
patients for cholecystitis. J Natl Med Assoc. 1995;87:27–32. - Kendall
JL, Shimp RJ. Performance and interpretation of focused right upper
quadrant ultrasound by emergency. J Emerg Med. 2001;21:7–13. - Keus
F, de Jong JA, Gooszen HG, van Laarhoven CJ. Laparoscopic versus open
cholecystectomy for patients with symptomatic cholecystolithiasis.
Cochrane Database Syst Rev. 2006;18(4):CD006231. - Keus
F, Werner JE, Gooszen HG, et al. Randomized clinical trial of
small-incision and laparoscopic cholecystectomy in patients with
symptomatic cholecystolithiasis: primary and clinical outcomes. Arch
Surg. 2008;143:371-377. - Keus,
F. Open, small-incision, or laparoscopic cholecystectomy for patients
with symptomatic cholecystolithiasis. An overview of Cochrane
Hepato-Biliary Group reviews / F. Keus, G.G. Hein // Cochrane
Database of Systematic Reviews 2010, Issue 1. Art. No.: CD008318. DOI:
10.1002/14651858.CD008318. - Kiewiet
JJ, Leeuwenburgh MM, Bipat S, Bossuyt PM, Stoker J, Boermeester MA. A
systematic review and meta-Analysis of diagnostic performance of imaging
in acute cholecystitis. Radiology. 2012;264:708–20. - Kim
KW, Park MS, Yu JS, et al. Acute cholecystitis at T2-weighted and
manganese-enhanced T1-weighted MR cholangiography: preliminary study.
Radiology2003; 227: 580–584. - Kiviluoto
T, Siren J, Luukkonen P, Kivilaakso E. Randomized trial of laparoscopic
versus open cholecystectomy for acute and gangrenous cholecystitis.
Lancet. 1998;351:321–5. - Kivinen
H, Makela JT, Autio R, Tikkakoski T, Leinonen S, Siniluoto T, et al.
Percutaneous cholecystostomy in acute cholecystitis in high-risk
patients: an analysis of 69 patients. Int Surg. 1998;83:299–302. - Lai
PB, Kwong KH, Leung KL, Kwok SP, Chan AC, Chung SC. Randomized trial of
early versus delayed laparoscopic cholecystectomy for acute
cholecystitis. Br J Surg. 1998;85:764– 767. - Lamki N, Raval B, St. Ville E. Computed tomography of complicated cholecystitis. J Comput Assist Tomogr 1986; 10:319-324.
- Laparoscopy
for abdominal emergencies. Evidence-based guidelines of the European
Association for Endoscopic Surgery / S.Sauerland et al. //
Surg Endosc. — 2006. — Vol. 20.- P. 14–29. - Lau
H, Lo CY, Patuil NG, Yuen WK. Early versus delayed-interval
laparoscopic cholecystectomy for acute cholecystitis. Surg Endosc.
2006;20:82–87. - Lee
SW, Chang CS, Lee TY, Tung CF, Peng YC. The role of the Tokyo
guidelines in the diagnosis of acute calculous cholecystitis. J
Hepatobiliary Pancreat Sci. 2010;17(6):879–884. - Lee
SW, Yang SS, Chang CS, Yeh HJ. Impact of the Tokyo guidelines on the
management of patients with acute calculous cholecystitis. J
Gastroenterol Hepatol. - Lo
CM, Liu CL, Fan ST, Lai EC, Wong J. Prospective randomized study of
early versus delayed laparoscopic cholecystectomy for acute
cholecystitis. Am Surg. 1998;227:461–467. - Loud
PA, Semelka RC, Kettritz U, et al. MRI of acute cholecystitis:
comparison with the normal gallbladder and other entities. Magn Reson
Imaging1996; 14: 349–355. - Malangoni
MA, Song J, Herrington J, Choudhri S, Pertel P. Randomized controlled
trial of moxifloxacin compared with piperacillin-tazobactam and
amoxicillin-clavulanate for the treatment of complicated intra-abdominal
infections. Ann Surg. 2006;244:204–211. - Melin
MM, Sarr MG, Bender CE, van Heerden JA. Percutaneous cholecystostomy: a
valuable technique in high-risk patients with presumed acute
cholecystitis. Br J Surg. 1995;82:1274–1277. - Merriam
LT, Kanaan SA, Dawes JG, Angelos P, Prystowsky JB, Rege RV, et al.
Gangrenous cholecystitis: analysis of risk factors and experience with
laparoscopic cholecystectomy. Surgery. 1999;126:680–685. - Miura
F, Takada T, Kawarada Y, Nimura Y, Wada K, Hirota M, et al. Flowcharts
for the diagnosis and treatment of acute cholangitis and cholecystitis:
Tokyo Guidelines. J Hepatobiliary Pancreat Surg. 2007;14:27–34. - Muller
E, Pitt HA, Thompson JE Jr, Doty J, Mann L, Manchester B. Antibiotics
in infections of the biliary tract. Surg Gynecol Obstet.
1987;165:285–292. - Noble
VE, Liteplo AS, Nelson BP, Thomas SH. The impact of analgesia on the
diagnostic accuracy of the sonographic Murphy’s sign. Eur J Emerg Med.
2010;17:80–83. - Oxford
level [Online] / B. Phillips et al. 1998, updated by J. Howick 2009//
[Электронный ресурс] URL: http://www.cebm.net/index.aspx?o=1025
[дата обращения 10. 10. 2014]. - Park
MS, Yu JS, Kim YH, et al. Acute cholecystitis: comparison of MR
cholangiography and US. Radiology1998; 209: 781–785. - Paulson EK. Acute cholecystitis: CT findings Semin Ultrasound CT MR 2000; 21:56-63.
- Pessaux
P, Regenet N, Tuech JJ, Rouge C, Bergamaschi R, Arnaud JP. Laparoscopic
versus open cholecystectomy: a prospective comparative study in the
elderly with acute cholcystitis. Surg Laparosc Endosc Percutan Tech.
2001;11:252–5. - Purkayastha
S, Tilney HS, Georgiou P, Athanasiou T, Tekkis PP, Darzi AW.
Laparoscopic cholecystectomy versus mini-laparotomy cholecystectomy: a
meta-analysis of randomized control trials. Surg Endosc.
2007;21(8):1294–1300. - Qazi
AR, Solangi RA, Shah PS, Memon GA. Reasons for conversion from
laparoscopic to open cholecystectomy. Medical Forum Monthly. 2010;21:3.
13-17. - Ralls
PW, Halls J, Lapin SA, Quinn MF, Morris UL, Boswell W. Prospective
evaluation of the sonographic Murphy sign in suspected acute
cholecystitis. J Clin Ultrasound. 1982;10:113–115. - Rattner
DW, Ferguson C, Warshaw AL. Factors associated with successful
laparoscopic cholecystectomy for acute cholecystitis. Ann Surg.
1993;217:233–236. - Regan
F, Schaefer DC, Smith DP, et al. The diagnostic utility of HASTE MRI in
the evaluation of acute cholecystitis: half-Fourier acquisition
single-shot turbo SE. J Comput Assist Tomogr1998; 22:
638–642. - Regimbeau
JM, Fuks D, Pautrat K, Mauvais F, Haccart V, Msika S, et al. Effect of
postoperative antibiotic administration on postoperative infection
following cholecystectomy for acute calculous cholecystitis: a
randomized clinical trial. JAMA. 2014;312(2):145–54. - Riall
TS, Zhang D, Townsend CM Jr, Young-Fang K, Goodwin JS. Failure to
perform cholecystectomy for acute cholecystitis in elderly patients is
associated with increased morbidity, mortality, and cost. J Am Coll
Surg. 2010;210:668–679. - Richardson
MC, Bell G, Fullarton GM. Incidence and nature of bile duct injuries
following laparoscopic cholecystectomy: an audit of 5913 cases. West of
Scotland laparoscopic cholecystectomy audit group. Br J Surg.
1996;83:1356–1360. - Rosen
CL, Brown DF, Chang Y, Moore C, Averill NJ, Arkoff LJ, et al.
Ultrasonography by emergency physicians in patients with suspected
cholecystitis. Am J Emerg Med. 2001;19:32–36. - Saad WE, Ginat D. Computed tomography and magnetic resonance cholangiography. Tech Vasc Interv Radiol. 2008;11:74–89.
- Schmidt
M, S?ndenaa K, Vetrhus M, Berhane T, Eide GE. Long-term follow-up of a
randomized controlled trial of observation versus surgery for acute
cholecystitis: non-operative management is an option in some patients.
Scand J Gastroenterol. 2011;46(10):1257–62. - Schofied PF, Hulton NR, Baildam AD. Is it acute cholecystitis? Ann R Coll Surg Engl. 1986;68:14–16.
- Schunemann
HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, et al. Grading
quality of evidence and strength of recommendations for diagnostic
tests and strategies. BMJ. 2008;17(336):1106–1110. - Senapati
PSP, Bhattarcharya D, Harinath G, Ammori BJ. A survey of the timing and
approach to the surgical management of cholelithiasis in patients with
acute biliary pancreatitis and acute cholecystitis in the UK. Ann R Coll
Surg Engl. 2003;85:306–312. - Shakespear1
J.S, Shaaban A.M., Rezvani M. CT Findings of Acute Cholecystitis and
Its Complications. American Journal of Roentgenology. 2010;194:
1523-1529. - Shea
JA, Berlin JA, Escarce JJ, Clarke JR, Kinosian BP, Cabana MD, et al.
Revised estimates of diagnostic test sensitivity and specificity in
suspected biliary tract disease. Arch Intern Med. 1994;154:2573–2581. - Shikata
S, Noguchi Y, Fukui T. Early versus delayed cholecystectomy for acute
cholecystitis: a meta-analysis of randomized controlled trials. Surg
Today. 2005;35:553–560. - Shojaiefard
A, Esmaeilzadeh M, Ghafouri A, Mehrabi A. Various techniques for the
surgical treatment of common bile duct stones: a meta review.
Gastroenterol Res Pract. 2009;2009:840208. - Siddiqui
E, MacDonald A, Chong PS, et al. Early versus delayed laparoscopic
cholecystectomy for acute cholecystitis: a meta-analysis of randomized
clinical trials. Am J Surg. 2008;195:40-47. - Singer
AJ, McCracken G, Henry MC, Thode HC Jr, Cabahug CJ. Correlation among
clinical, laboratory, and hepatobiliary scanning findings in patients
with suspected acute cholecystitis. Ann Emerg Med.
1996;28:267–272. - Solomkin
J, Zhao YP, Ma EL, Chen MJ, DRAGON Study Team. Moxifloxacin is
non-inferior to combination therapy with ceftriaxone plus metronidazole
in patients with community-origin complicated intra-abdominal
infections. Int J Antimicrob Agents. 2009;34:439–445. - Solomkin
JS, Mazuski JE, Bradley JS, Rodvold KA, Goldstein EJC, Baron EJ, et al.
Diagnosis and management of complicated intra-abdominal infection in
adults and children: Guidelines by the Surgical Infection Society and
the Infectious Diseases Society of America. Clin Infect Dis.
2010;50:133–164 (CPGs). - Sosna
J, Copel L, Kane RA, Kruskal JB. (2003) Ultrasound-guided percutaneous
cholecystostomy: update on technique and clinical applications. Surg
Technol Int 11:135–139. - Soyer
P, Brouland JP, Boudiaf M, Kardache M, Pelage JP, Panis Y, et al. Color
velocity imaging and power Doppler sonography of the gallbladder wall: a
new look at sonographic diagnosis of acute cholecystitis. AJR.
1998;171:183–188 - Staniland
JR, Ditchburn J, De Dombal FT. Clinical presentation of acute abdomen:
study of 600 patients. Br Med J. 1972;3:393–398. - Steven M, Strasberg MD. Acute calculous cholecystitis. N Engl J Med. 2008;358:2804–2811
- Sugiyama
M, Tokuhara M, Atomi Y. Is percutaneous cholecystostomy the optimal
treatment for acute cholecystitis in the very elderly? World J Surg.
1998;22:459–463. - Sung
YK, Lee JK, Lee KH, Lee KT, Kang C-I. The clinical epidemiology and
outcomes of bacteremic biliary tract infections caused by
antimicrobial-resistant pathogens. Am J Gastroenterol. 2012;107:473–483. - Takada
et al. TG13: Updated Tokyo Guidelines for the management of acute
cholangitis and cholecystitis // J Hepatobiliary Pancreat Sci. – 2013. –
Vol. 20 — № 1. P. 1–105. [Электронный ресурс] URL:
http://link.springer.com/journal/534/20/1/page/1 [дата обращения 10. 10.
2014]. - Teefey
SA, Baron RL, Radke HM, Bigler SA. Gangrenous cholecystitis: new
observations on sonography. J Ultrasound Med 1991; 134:191-194. - Teixeira
JP, Sraiva AC, Cabral AC, Barros H, Reis JR, Teixeira A. Conversion
factors in laparoscopic cholecystectomy for acute cholecystitis.
Hepatogastroenterology. 2000;47:626–630. - The
Southern Surgeons Club. A prospective analysis of 1518 laparoscopic
cholecystectomies. N Engl J Med. 1991;324:1073–1078. - Thompson
JE Jr, Bennion R, Roettger R, Lally K, Hopkins J, Wilson SE. Cefepime
for infections of the biliary tract. Surg Gynecol Obstet. 1993;177
Suppl:30–34. discussion 35–40. - Trowbridge RL, Rutkowski NK, Shojania KG. Does this patient have acute cholecystitis? JAMA. 2003;289(1):80–6.
- van
den Brink JS, Watanabe Y, Kuhl CK, et al. Implications of SENSE MR in
routine clinical practice. Eur J Radiol2003; 46: 3–27. - van
den Hazel SJ, Speelman P, Tytgat GNJ, Dankert J, van Leeuwen DJ. Role
of antibiotics in the treatment and prevention of acute and recurrent
cholangitis. Clin Infect Dis. 1994;19:279–286. - Varma
DGK, Faust JM. Computed tomography of gangrenous acute postoperative
acalculous cholecystitis. J Comput Assist Tomogr 1988;
12:29-31. - Vitellas
KM, Keogan MT, Spritzer CE, Nelson RC. MR cholangiopancreatography of
bile and pancreatic duct abnormalities with emphasis on the single-shot
fast spin-echo technique. RadioGraphics2000; 20: 939–957. - Watanabe
Y, Dohke M, Ishimori T, et al. Diagnostic pitfalls of MR
cholangiopancreatography in the evaluation of the biliary tract and
gallbladder. RadioGraphics1999; 19: 415–429. - Watanabe
Y, Dohke M, Ishimori T, et al. High-resolution MR
cholangiopancreatography. Crit Rev Diagn Imaging1998; 39(2–3): 115–258. - Weissleder R, Stark DD, Compton CC, et al. Cholecystitis: diagnosis by MR imaging. Magn Reson Imaging1988; 6: 345–348.
- Winbladh
A, Gullstrand P, Svanvik J, Sandstrom P. Systematic review of
cholecystostomy as a treatment option in acute cholecystitis. HPB
(Oxford). 2009;11:183–193. - Yamashita
Y, Kimura T, Matsumoto S. A safe laparoscopic cholecystectomy depends
upon the establishment of a critical view of safety. Surg Today.
2010;40:507–513. - Yamashita
Y, Takada T, Hirata K. A survey of the timing and approach to the
surgical management of patients with acute cholecystitis in Japanese
hospitals. J Hepatobiliary Pancreat Surg. 2006;13:409–415. - Yellin
AE, Berne TV, Appleman MD, Heseltine PN, Gill MA, Okamoto MP, Baker FJ,
Holcomb C. A randomized study of cefepime versus the combination of
gentamicin and mezlocillin as an adjunct to surgical treatment in
patients with acute cholecystitis. Surg Gynecol Obstet. 1993;177
Suppl:23–29; discussion 35–40. - Yokoe
M, Takada T, Mayumi T, Yoshida M, Hasegawa H, Norimizu S, et al.
Accuracy of the Tokyo Guidelines for the diagnosis of acute cholangitis
and cholecystitis taking into consideration the clinical practice
pattern in Japan. J Hepatobiliary Pancreat Sci.
2011;18:250–7. 115. Zacks SL, Sandler RS, Rutledge R et al
(2002) A populationbased cohort study comparing laparoscopic
cholecystectomy and open cholecystectomy. Am J Gastroenterol 97:334340. - Агаджанов
В.Г., Шулутко А.М., Насиров Ф.Н., Чантурия М.О., Натрошвили А.Г.,
Натрошвили И.Г. «Десять лет спустя…» — отдаленные результаты операций из
минидоступа при холецистохоледохолитиазе //Московский хирургический
журнал. 2013. № 4. С. 14-18 - Бебуришвили
А.Г., Панин С.И., Зюбина Е.Н., Быков А.В. Миниинвазивные вмешательства
при остром холецистите: состояние проблемы по данным доказательной
медицины // Анналы хирургической гепатологии. 2011. Т. 16. № 2. С. 83-88 - Бебуришвили
А.Г., Прудков М.И., Шулутко А.М., Натрошвили А.Г., Панин С.И., Нестеров
С.С., Натрошвили И.Г. Концептуальная оценка применения
лапароскопических и минилапаротомных вмешательств в неотложной
абдоминальной хирургии // Хирургия. Журнал им. Н.И. Пирогова. 2013. № 1.
С. 53-57 - Королев Б.А., Пиковский Д. Л. Экстренная хирургия желчных путей .- М.: Медицина, 1990. — 240 с.
- Королев Б.А., Пиковский Д. Л. Экстренная хирургия желчных путей .- М.: Медицина, 1990. — 240 с.
- Кузнецов
H.A., Бронтвейн А.Т., Васильев А.Ю., Витько И.К. Компьютерная
томография в диагностике острого и хронического холецистита // Лечащий
врач. 2000. — №7. — С. 35-40 - Кузнецов
H.A., Бронтвейн А.Т., Васильев А.Ю., Витько И.К. Компьютерная
томография в диагностике острого и хронического холецистита // Лечащий
врач. 2000. — №7. — С. 35-40 - Прудков
М.И., Столин А.В., Кармацких А.Ю. Современные эндохирургические
технологии лечения острого калькулезного холецистита. // Эндоскопическая
хирургия. 2007. Т. 13. № 1. С. 68-69. - Совцов
С.А., Прилепина Е.В. Возможности улучшения результатов лечения острого
холецистита. // Хирургия. Журнал им. Н.И. Пирогова. 2015. № 2. С. 50-55. - Совцов
С.А., Прилепина Е.В. Холецистит у больных высокого риска. Хирургия.
Журнал им. Н.И. Пирогова 2013; 12: 18-23. Клиническая хирургия:
национальное руководство: в 3 т. / под ред. B.C. Савельева, А.И.
Кириенко. — М.: ГЭОТАР-Медиа, 2009. — Т. II. — 832 с. - Совцов
С.А., Прилепина Е.В. Холецистит у больных высокого риска. Хирургия.
Журнал им. Н.И. Пирогова 2013; 12: 18-23. Клиническая хирургия:
национальное руководство: в 3 т. / под ред. B.C. Савельева, А.И.
Кириенко. — М.: ГЭОТАР-Медиа, 2009. — Т. II. — 832 с. - Столин
А.В., Прудков М.И. Возможности хирургического лечения больных острым
калькулезным холециститом, осложненным механической желтухой //
Эндоскопическая хирургия. 2007. Т. 13. № 1. С. 86 - Шулутко
А.М., Агаджанов В.Г., Натрошвили А.Г., Натрошвили И.Г. Минимально
инвазивные операции при холецистохоледохолитиазе // Анналы хирургической
гепатологии. 2013. Т. 18. № 1. с. 38-41 - Шулутко
А.М., Прудков М.И., Бебуришвили А.Г., Ветшев П.С., Агаджанов В.Г.,
Шпаченко Ф.А., Асатрян К.В. Отдаленные результаты хирургического лечения
холецистохоледохолитиаза. //Анналы хирургической гепатологии. 2005. Т.
10. № 3. С. 4449 - Шулутко
А.М., Прудков М.И., Тимербулатов В.М., Ветшев П.С., Бебуришвили А.Г.,
Гарипов Р.М., Агаджанов В.Г., Чантурия М.О., Натрошвили А.Г., Нишневич
Е.В., Столин А.В., Натрошвили И.Г., Кяров Н.Х. Минилапаротомные
технологии при желчекаменной болезни: системный подход или хирургическая
эквилибристика? //Анналы хирургической гепатологии. 2012. Т. 17. № 2.
С. 34-41
Приложение А1. Состав рабочей группы
Бебуришвили А.Г. Д.м.н., профессор, член Российского общества хирургов
Прудков М.И. Д.м.н., профессор, член Российского общества хирургов
Совцов С.А. Д.м.н., профессор, член Российского общества хирургов
Сажин А.В. Д.м.н., профессор, член Российского общества хирургов
улутко А.М. Д.м.н., профессор, член Российского общества хирургов
Натрошвили А.Г. К.м.н., доцент, член Российского общества хирургов
Натрошвили И.Г. К.м.н., член Российского общества хирургов
Конфликт интересов тсутствует
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций: врачи-хирурги
Таблица П1 Уровни достоверности доказательств с указанием использованной классификации уровней достоверности доказательств
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1 уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым» стандартом |
Отдельное РКИ (с узким ДИ) |
|
1с |
Специфичность или чувствительность столь высоки, что положительный или отрицательный результата позволяет исключить/установить диагноз |
Исследование «Все или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2 уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым» стандартом |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай-контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого» стандарта у всех испытуемых |
Отдельное исследование |
|
4 |
Исследование случай-контроль или исследование с некачественным или зависимым «золотым» стандартом |
Серия случаев (и когортные исследования или исследования «случай-контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
Таблица П2. Уровни убедительности рекомендаций с указанием использованной классификации уровней убедительности рекомендаций
|
A |
Согласующиеся между собой исследования 1 уровня |
|
B |
Согласующиеся между собой исследования 2 или 3 уровня или экстраполяция на основе исследований 1 уровня |
|
C |
Исследования 4 уровня или экстраполяция на основе уровня 2 или 3 |
|
D |
Доказательства 4 уровня или затруднительные для обобщения или некачественные исследования любого уровня |
Приложение А3. Связанные документы
- Приказ Министерства здравоохранения Российской Федерации от 15
ноября 2012 г. № 922н «Об утверждении Порядка оказания медицинской
помощи взрослому населению по профилю «хирургия».
Приложение Б. Алгоритмы ведения пациента
Алгоритм диагностики острого холецистита
Алгоритм лечения пациентов с острым холециститом
Приложение В. Информация для пациентов
Для острого холецистита характерны:
- постоянные боли в правой верхней половине живота (правом
подреберье), которые могут отдавать в правую руку, в правую
половину груди и шеи. Нередко им предшествует приступ желчной
колики; - повышение температуры тела;
- чувство горечи во рту,тошнота и рвота, не приносящая облегчения;
- желтуха кожи и склер (наблюдается не всегда).
При подозрении на острый холецистит следует немедленно
обратиться к врачу. Это заболевание
опасно своими осложнениями, которые могут развиться через
несколько суток после начала заболевания:
- гнойным воспалением (эмпиема,гангрена) и прободением желчного пузыря с последующим развитием перитонита – воспаления брюшины;
- развитием подпеченочного абсцесса (ограниченного гнойного очага);
- желчных свищей, сообщающих желчный пузырь с кишечником, желудком или почкой;
- острого панкреатата;
- механической желтухи.
Холангит у взрослых
Версия: Клинические протоколы МЗ РК — 2015 (Казахстан)
Категории МКБ:
Камни желчного протока с холангитом (K80.3), Холангит (K83.0)
Разделы медицины:
Гастроэнтерология, Хирургия
Общая информация
Краткое описание
Рекомендовано
Экспертным советом
РГП на ПВХ «Республиканский центр развития здравоохранения»
Министерства здравоохранения
и социального развития
от «30» сентября 2015 года
Протокол №10
Название протокола: Холангит у взрослых
Холангит – воспалительное заболевание вне- и внутрипеченочных желчных протоков, имеющее острое или хронически-рецидивирующее течение [3].
Код протокола:
Код(ы) МКБ-10:
К80.3 Камни желчного протока с холангитом
К83.0 Холангит
Сокращения, используемые в протоколе:
АЛТ — аланинаминотрансфераза
АСТ – аспартатаминотрасфераза
АЧТВ -активированное частичное тромбопластиновое время
АИХ – аутоимунный холангит
БДС – большой дуоденальный сосочек
ВИЧ – вирус иммунодефицита человека
ГГТП — Гамма-глютамилтранспептидаза
ЖКТ – желудочно-кишечный тракт
ИФА – иммуноферментный анализ
МНО – международное нормализованное отношение
МРТ – магнитно-резонансная томография
ПБЦ – первичный билиарный цирроз
ПТВ – протромбиновое время
ПТИ – протромбиновый индекс
ПСХ – первичный склерозирующий холангит
РЭА – раковый эмбриональный антиген
УЗИ – ультразвуковое исследование
ХВЗК – хронические воспалительные заболевания кишечника
ХЦК – холангиоцеллюлярная карцинома
ЦВД – центральное венозное давление
ЧСС – частота сердечных сокращений
ЧЧХГ – чрескожная чреспеченочная холангиография
ЭПСТ – эндоскопическая папиллосфинктеротомия
ЭРХПГ – эндоскопическая ретроградная холангиопанкреатография
Дата разработки/пересмотра протокола: 2015 год.
Категория пациентов: взрослые.
Пользователи протокола: хирурги, врачи-эндоскописты, гастроэнтерологи, терапевты, врачи общей практики.
Оценка на степень доказательности приводимых рекомендаций [6,11,12,13].
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Клиническая классификация[1]:
По течению:
· острый.
· хронический
По этиопатогенезу:
· первичный (бактериальный, гельминтозный, АИХ, ПСХ);
· вторичный;
· симптоматический.
На почве заболеваний с подпеченочным холестазом:
· камни гепатохоледоха;
· рубцовые и воспалительные стриктуры магистральных желчных протоков и БДС;
· злокачественные и доброкачественные опухоли с окклюзией гепатохоледоха или БДС;
· хронические панкреатиты со сдавлением холедоха.
На почве заболеваний без подпеченочного холестаза:
· билиодигестивные анастомозы и свищи;
· недостаточность сфинктера Одди;
· послеоперационный холангит;
· холестатические гепатиты и билиарный цирроз печени.
По типу воспаления и морфологических изменений:
· катаральный;
· гнойный;
· обструктивный;
· деструктивный негнойный.
Осложнения холангита:
· абсцессы печени;
· некроз и перфорация гепатохоледоха;
· перитонит;
· забрюшинная флегмона;
· сепсис с внепеченочными гнойными очагами;
· бактериально-токсический шок;
· острая почечная недостаточность.
Клиническая картина
Cимптомы, течение
Диагностические критерии постановки диагноза:
Жалобы и анамнез:
Жалобы:
· повышение температуры тела (лихорадка);
· озноб;
· боль в правом подреберье и/или эпигастрии;
· тошнота;
· рвота;
· артериальная гипотензия;
· желтуха;
· кожный зуд;
· потемнение мочи;
· ахоличный стул;
· сухость во рту;
· выраженная слабость;
· изменение сознания вплоть до сопора;
· возможны нарушения психики.
Анамнез [3,9]:
· триада Шарко (озноб, лихорадка, боль в правом подреберье);
· пентада Рейнолда (озноб, лихорадка, боль в правом подреберье, артериальная гипотензия
, нарушение психики);
· желчекаменная болезнь;
· перенесенные операции на гепатопанкреатобилиарной зоне;
· врожденные аномалии желчных протоков (с-м Кароли);
· перенесенная трансплантация печени;
· ранее перенесенные эндоскопические манипуляции на панкреатобилиарной зоне;
· опухолевые поражения желчных протоков, головки поджелудочной железы и БДС;
· стентирование желчных и панкреатических протоков;
· стенотические поражения желчевыводящих протоков.
Физикальное обследование:
· общий осмотр: желтушность склер и кожных покровов, следы расчесов на коже, язык сухой, обложен налетом, тахикардия, повышение температуры тела;
· пальпация: болезненность в правом подреберье и эпигастрии, увеличение печени и селезенки;
· перкуссия: увеличение перкуторных размеров печени
Диагностика
Перечень основных и дополнительных диагностических мероприятий.
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
· сбор жалоб, анамнеза заболевания и жизни;
· физикальное обследование;
· общий анализ крови;
· общий анализ мочи;
· определение желчных пигментов в моче;
· биохимический анализ крови (общий белок и его фракции, мочевина, креатинин, билирубин, АЛТ, АСТ, щелочная фосфатаза, ГГТП, амилаза, глюкоза крови);
· электрокардиографическое исследование;
· УЗИ органов брюшной полости.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
· определение онкомаркеров РЭА, СА 19-9;
· исследование крови на антитела р-ANCA;
· определение антинейтрофильных цитоплазматических Ig G (ANCA combi) в сыворотке крови;
· колоноскопия.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне при экстренной госпитализации и по истечении сроков более 10 дней с момента сдачи анализов в соответствии с приказом МО:
· сбор жалоб, анамнеза заболевания и жизни;
· антропометрия (измерение роста и веса);
· физикальное обследование;
· ЭРХПГ;
Дополнительные диагностические обследования, проводимые на стационарном уровне при экстренной госпитализации и по истечении сроков более 10 дней с момента сдачи анализов в соответствии с приказом МО [2,3,4,5]:
· определение онкомаркеры РЭА, СА 19-9;
· исследование крови на антитела р-ANCA;
· ЧЧХГ;
· эндоскопическое ультразвуковое исследование панкреатобилиарной зоны с тонкоигольной биопсией;
· колоноскопия;
· биопсия печени.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи:
· сбор жалоб, анамнеза заболевания и жизни;
физикальное обследование.
Инструментальные исследования [2,11,12,13]:
· УЗИ органов брюшной полости – расширение вне- и внутрипеченочных желчных протоков, утолщение или истончение стенок гепатикохоледоха, наличие сужений протоков, наличие конкрементов или билиарного сладжа в желчевыводящих протоках, увеличение головки поджелудочной железы, увеличение размеров печени;
· МРТ холангиопанкреатография — расширение вне- и внутрипеченочных желчных протоков, утолщение или истончение стенок гепатикохоледоха, наличие сужений протоков, наличие конкрементов или билиарного сладжа в желчевыводящих протоках, увеличение головки поджелудочной железы, увеличение размеров печени;
· Эзофагогастродуоденоскопия с осмотром дуоденального сосочка – отсутствие поступления желчи, мутная, гнойная желчь, увеличение БДС за счет выбухания интрамуральной части холедоха, гиперемия слизистой в области БДС, сдавление 12-перстной кишки из вне, сужение устья БДС;
· ЭРХПГ – расширение и неравномерность контрастирования вне- и внутрипеченочных желчных протоков, отсутствие контрастирования протоков на определенном уровне, тени конкрементов на фоне контраста, сужение участков желчевыводящих протоков, неравномерность контуров протоков (четкообразные желчные протоки);
· ЧЧХГ — расширение и неравномерность контрастирования вне- и внутрипеченочных желчных протоков, отсутствие контрастирования протоков на определенном уровне, тени конкрементов на фоне контраста, сужение участков желчевыводящих протоков, неравномерность контуров протоков (четкообразные желчные протоки);
· Биопсия печени – применяется для диагностики ПСХ. Выделяют 4 морфологических стадии [3]:
I стадия — Биоптат не имеет специфических морфологических признаков. Типична очаговая атрофия и нарушение рядности эпителия. Возможна очаговая облитерация и деление желчных протоков. В портальных трактах видны признаки умеренной лимфоцитарной воспалительной инфильтрации. Иногда видны лимфоидные фолликулы без герменативных центров, редко гранулемы;
II стадия характеризуется признаками лобулярного гепатита, часто напоминающего хронический гепатит С или аутоимунный гепатит. Характерна пролиферация желчных протоков, но она обычно имеет очаговый характер. Возможен умеренный фиброз портальных трактов. На этой стадии признаки гепатита имеют более серьезное прогностическое значение, нежели поражение желчных протоков;
III стадия характеризуется типичным, но не патогномоничным признаком ПСХ – перидуктулярным фиброзом (симптом «луковой шелухи»). Очень характерно наличие дуктопении и фиброзных полей в местах потери желчных канальцев. На этой стадии в портальных трактах видны только ветви воротной ветви и печеночной артерии (желчные протоки облитерированы), паренхиму рассекают портопортальные фиброзные септы, а воспалительный инфильтрат менее выражен. В перипортальных зонах обнаруживают внутридольковый холестаз, депозиты меди, а иногда и тельца Маллори;
IV стадия характеризуется распространенным фиброзом билиарного типа с признаками билиарного цирроза печени, что в некоторых случаях затрудняет проведение дифференциальной диагностики между ПСХ и ПБЦ.
· Эндоскопическое ультразвуковое исследование панкреатобилиарной зоны Во время манипуляции при обнаружении солидных образований либо подозрении на опухоль панкреатобилиарной зоны возможно выполнение прицельной тонкоигольной биопсии с последующим морфологическим исследованием биоптата.
· Колоноскопия проводится пациентам с ПСХ. [5].
Показания для консультации узких специалистов:
· консультация врача-инфекциониста для исключения вирусных гепатитов;
· консультация гастроэнтеролога при высоких показателях трансаминаз и сопутствующей патологии ЖКТ;
· консультация онколога при подозрении на опухоли панкреатобилиарной зоны;
· консультация кардиолога при патологии сердечно-сосудистой системы и при планировании оперативного лечения;
· консультация эндокринолога при наличии сопутствующей эндокринной патологии;
· консультация анестезиолога при планировании оперативного лечения.
Лабораторная диагностика
Лабораторные исследования:
· общий анализ крови — норма показателей красной крови, лейкоцитоз, со сдвигом лейкоцитарной формулы влево, ускорение СОЭ, увеличение лейкоцитарного индекса интоксикации;
· общий анализ мочи – положительные желчные пигменты;
· биохимический анализ крови – повышение показателей билирубина за счет прямой фракции, повышение щелочной фосфотазы, ГГТП возможно увеличение уровня АЛТ, АСТ, амилазы, также возможно повышение креатинина, мочевины, снижение уровня белка и электролитные нарушения;
· коагулограмма – снижение ПТИ, увеличение фибриногена, положительный фибриноген В, увеличение МНО, увеличение АЧТВ и ПТВ;
· ИФА на гепатиты В и С отрицательные;
· онкомаркеры — могут быть положительными при опухолевой природе холангита;
· антитела p-ANCA могут быть положительными при ПСХ;
Дифференциальный диагноз
Дифференциальный диагноз [2,3,4,5,6,9]:
Таблица – 1. Дифференциальная диагностика холангитов в зависимости от причинного фактора.
| Признаки | ПСХ | Доброкачественные стриктуры желчных протоков | Злокачественные стриктуры желчевыводящих протоков | Холедохолитиаз |
| Начало заболевания | Медленное, отсутствие ярких клинических проявлений, волнообразное течение с периодами ремиссии | Прогрессивно нарастающие клинические проявления, развиваются в короткие сроки (3-7 дней) | Медленно нарастающие клинические проявления с нарастанием явлений желтухи и холангита | Бурное развитие заболевания с яркой клинической картиной холангита |
| Анамнез заболевания | Больше болеет мужской пол, в анамнезе ХВЗК, некурящий образ жизни | Как правило связаны с предшествующим оперативным вмешательством на панкреатобилиарной зоне | Не имеют характерных анамнестических признаков | В анамнезе ЖКБ, острое начало заболевания |
| УЗИ | Расширение вне- и внутрипеченочных желчных протоков | Расширение вне- и/или внутрипеченочных желчных протоков | Расширение вне- и/или внутрипеченочных желчных протоков. Возможно увеличение головки поджелудочной железы, увеличение парааортальных лимфоузлов | Расширение вне- и внутрипеченочных желчных протоков с наличием конкрементов, дающих акустическую дорожку |
| МРТ холангиопанреатография | Четкообразные контуры вне-и внутрипеченочных желчных протоков, иногда наличие доминантных стриктур | Одиночные стриктуры, локализованные в зоне оперативного вмешательства | Стрикутры гепатикохоледоха различных локализаций, возможно увеличение головки поджелудочной железы, лимфоузлов парааортальной зоны | Наличие конкрементов в желчевыводящих протоках |
| Эзофагогастродуоденоскопия с осмотром БДС | Область БДС визуально не изменена, желчь не поступает, либо поступает малыми порциями | Область БДС визуально не изменена, желчь не поступает | При периампулярных опухолях имеются характерные экзофитные либо инфильтративные опухолевые изменения, при других локализациях БДС не изменен, желчь не поступает | Выделение мутной или гнойной желчи через устье БДС, увеличение, напряжение в интрамуральной части холедоха, часто видимое пролабирование БДС в просвет кишки за счет обтурации конкрементом |
| ЭРХПГ, ЧЧХГ | видны участки суженых и расширенных желчных протоков, важно для диагностики доминантных стриктур | Виден участок одиночного сужения с ровными контурами в области оперативного вмешательства с супрастенотическим расширением | Виден одиночный участок сужения с неровными контурами с супрастенотическим расширением в различных частях билиарного тракта | Наличие рентгенконтрастных дефектов наполнения в просвете билиарного дерева, протоки равномерно расширены |
| Биопсия печени | При ПСХ информативна, выделяют 4 клинико- морфологические стадии | Не проводится, не информативна | Не проводится, не иформативна | Не проводится, не иформативна |
| Эндоскопическое ультразвуковое исследование | Множественные участки расширений и сужений желчных протоков | Одиночная стриктура с четкими контурами стенки | Стриктура с утолщенной бугристой стенкой, часто можно визуализировать солидный или опухолевый компонент | Визуализируются конкременты с четкой акустической дорожкой |
Лечение
Цели лечения:
При острых гнойных холангитах —
ликвидация клинических признаков холангита с восстановлением трудоспособности и социального статуса больных [3];
При ПСХ – уменьшение клинических признаков холангита, удлинения периода ремиссии, снижение рисков развития цирроза печени и ХЦК [4].
Тактика лечения [6,7,8,9,10,11,12,13]:
Тактика лечения пациентов с холангитом должна быть максимально персонализирована, но в конечном итоге направлена на восстановление пассажа желчи путем наружного или внутреннего дренирования.
Хирургическое вмешательство:
Острый гнойный холангит:
· хирургическое лечение при остром гнойном холангите направлено на декомпрессию желчных путей. При этом в современных условиях приоритетом является выполнение малоинвазивных и/или эндоскопических методов. При невозможности или безуспешности проведения малоинвазивных вмешательств должно быть выполнено открытое оперативное вмешательство;
· показания к применению того или иного метода декомпрессии необходимо устанавливать строго индивидуально, в зависимости от клинической ситуации, характера, уровня и протяженности препятствия оттоку желчи, с учетом результатов прямых рентгеноконтрастных исследований желчных путей.
Малоинвазивные методы декомпрессии желчевыводящих путей [6,8,10,12,13] (УД 1А):
· эндоскопическая папиллосфинктеротомия, литэкстракция;
· эндоскопическая баллонная дилатация стриктур желчевыводящих протоков;
· стентирование желчных протоков;
· чрескожная чреспеченочная холангиостомия.
Дальнейшая хирургическая тактика зависит от причинного фактора, вызвавшего острый гнойный холангит и проводится в соответствии с протоколами диагностики и лечения данных заболеваний (КП «Рак поджелудочной железы» PH-S-035; КП «Хронический калькулезный холецистит», утвержден протоколом заседания экспертной комиссии по вопросам развития здравоохранения МЗ РК №23 от 12.12.2013 г.).
1. Путем эндоскопической папиллосфинктеротомии можно удалить большинство камней, произвести эндопротезирование или назобилиарное дренирование опухоли дистального отдела холедоха или головки поджелудочной железы. Этот путь является наиболее физиологичным, малотравматичным и распространенным методом декомпрессии. При больших неудалимых камнях следует выполнять традиционную холедохолитотомию с дренированием холедоха Т-образным дренажем.
2. Применение чрескожно-чреспеченочного дренирования желчных путей более целесообразно при высоком блоке желчных путей – на уровне ворот печени (опухоль, стриктура).
3. Несмотря на то что без декомпрессии желчных путей антибиотики в желчь не попадают, массивная антибиотикотерапия должна назначаться в обязательном порядке с целью профилактики септических осложнений.
4. При выраженной эндотоксемии с расстройством функции почек и центральной гемо- динамики больные госпитализируются в реанимационное отделение, а декомпрессия желчных путей производится сразу, как только это позволяет общее состояние больного.
Методы восстановления проходимости желчных протоков при ПСХ [3,4,11] (УД 3С):
· балонная дилатация желчных протоков;
· стентирование желчных протоков;
· реконструктивные операции;
· трансплантация печени.
Решение о проведении оперативного лечения при ПСХ должно решаться консилиумом с участием хирурга, онколога и гастроэнтеролога.
Хирургическое вмешательство, оказываемое в стационарных условиях:
Все малоинвазивные и открытые хирургические вмешательства при холангитах должны проводиться в стационарных условиях.
Послеоперационные осложнения:
В раннем послеоперационном периоде возможно развитие осложнений:
· гнойно-септические осложнения (общие и местные);
· острый панкреатит;
· перитонит;
· холемическое кровотечение;
· печеночно-почечная недостаточность;
· тромбоэмболические осложнения.
Из осложнений, возникающих в позднем послеоперационном периоде, наиболее критичными являются формирование стриктур желчных протоков и холангиогенных абсцессов.
Медикаментозное лечение:
Острый гнойный холангит:
лечение больных с острым гнойным холангитом необходимо начинать сразу после поступления больного в стационар. Нужно иметь в виду, в условиях желчной гипертензии при холангите медикаментозную терапию. Ее целесообразно рассматривать лишь как интенсивную кратковременную подготовку больного к проведению срочной декомпрессии желчных протоков [11,12]. (УД–1А) При угрожаемом состоянии интенсивную терапию следует сочетать с немедленной декомпрессией.
При ПСХ:
Принятие решения о назначении лечения больным с ПСХ требует взвешенной оценки признаков поражения паренхимы печени (гепатита) и недостаточности желчных протоков (холестаза) [11] (УД 3С). В некоторых случаях показано назначение комбинированной терапии:
· урсодезоксихолевая кислота 15-20 мг/кг в сутки постоянно (УД -1 С);
Купирование болевого синдрома:
· гиосцина бутилбромид 20 мг 4 раза в сутки внутримышечно или внутривенно при болевом синдроме до 5 дней (УД — 2С);
· платифиллин 0,2% -1,0 2 раза в сутки внутримышечно или внутривенно в случае отсуствия гиосцина бутилбромида до 5 дней при болях (УД — 2С);
· кеторолак 15мг/мл, 30мг/мл 2 -3 раза в сутки внутримышечно в послеоперационном периоде не более 5 дней (УД — 1С).
Антибактериальная терапия:
· метронидазол 500 мг в 100 мл 3 раза в сутки внутривенно курс 7 дней (УД — 1В);
· ципрофлоксацин 0,2% — 200 мг в 100 мл 2 раза в сутки внутривенно курс 7-10 дней (УД — 1А).
Инфузионная терапия: объем инфузионной терапии определяется степенью дегидротации и должен составлять не более 60 мл/кг в сутки. В тяжелых состояниях инфузионная терапия проводится под контролем ЦВД и ЧСС. Не должно быть резких колебаний ЦВД и увеличения ЧСС.
· натрия хлорид 0,9%;
· сложный раствор натрия лактата;
Средства для парентерального питания применяются в случае невозможности энтерального питания пациентов более 2 суток в до- и послеоперационном периоде.
· раствор декстрозы 10%, 20%, 40%;
· жировая эмульсия для парентерального питания при тяжелых состояниях и невозможности энтерального питания или
Другие препараты в комплексном лечении холангита:
· метоклопрамид 0,5% 2 мл 2 раза в сутки внутримышечно или внутривенно 1-3 дня (УД — 1В).
Применяется при тошноте и рвоте:
· надропарин 0,3 мл 1 раз в сутки 7-10 дней под контролем коагулограммы. Применяется в до- и послеоперационном периоде для профилактики тромбозов и эмболий (УД — 1А).
Немедикаментозное лечение:
Режим I, II.
Диета – стол №5а. Больным холангитом стоит придерживаться строгой диеты. Если болезнь находится в острой стадии, то пациенту необходимо голодать. При улучшении состояния нужно использовать дробный режим питания. Больного стоит кормить до 6 раз в день минимальными порциями. Вся пища готовится только на пару, а холодные напитки строго исключены из рациона. Можно применять в пищу рыбу, мясо и птицу, но обязательно нежирную. Разрешены крупяные каши, черный и пшеничный хлеб, макаронные изделия, кисломолочные и молочные продукты, ягоды и фрукты.
Эластическое бинтование — нижних конечностей при сопутствующей варикозной болезни для профилактики тромбоэмболических осложнений.
Другие виды лечения [6,7,9,10]:
В случаях тяжелого течения холангита с осложнениями в виде септического состояния, признаков печеночно-почечной недостаточности показано применение экстракорпоральных методов детоксикации в соответствии с клиническими протоколами диагностики и лечения данных осложнений.
Методы экстракорпоральной детоксикации при ОГХ:
· плазмаферез (УД 2В);
· ультрафильтрация (УД 2В);
· гемодиафильтрация (УД 2В);
· гемодиализ (УД 2В).
Показания к проведению экстракорпоральных методов детоксикации:
· сепсис;
· печеночно-почечная недостаточность.
Противопоказания:
· агональное состояние больного;
· септический шок.
Правила применения почечно-замещающей терапии указаны в КП «Острая почечная недостаточность» рекомендованной экспертным советом РЦРЗ от 12.12.2014г.
Индикаторы эффективности лечения:
· исчезновение клинических и лабораторных признаков холангита;
· восстановление функциональных возможностей и трудоспособности;
· удовлетворительное самочувствие;
· отсутствие осложнений;
· заживление операционной раны первичным натяжением;
· отсутствие болей;
· нормальные лабораторные показатели;
· удовлетворительные данные УЗИ;
· отсутствие рецидива заболевания.
Препараты (действующие вещества), применяющиеся при лечении
| Гиосцина бутилбромид (Hyoscine butylbromide) |
| Декстроза (Dextrose) |
| Жировая эмульсия для парентерального питания (A fat emulsion for parenteral nutrition) |
| Калия хлорид (Potassium chloride) |
| Кальция хлорид (Calcium chloride) |
| Кеторолак (Ketorolac) |
| Метоклопрамид (Metoclopramide) |
| Метронидазол (Metronidazole) |
| Надропарин кальция (Nadroparin calcium) |
| Натрия лактат (Sodium lactate) |
| Натрия хлорид (Sodium chloride) |
| Платифиллин (Platifillin) |
| Урсодезоксихолевая кислота (Ursodeoxycholic acid) |
| Ципрофлоксацин (Ciprofloxacin) |
Госпитализация
Показания для госпитализации с указанием типа госпитализации:
Показания для экстренной госпитализации:
· острый бактериальный холангит и его осложнения;
· холедохолитиаз с явлениями острого холангита.
Показания для плановой госпитализации:
· холангиты при рубцовых и воспалительных стриктурах магистральных желчных протоков и БДС;
· злокачественные и доброкачественные опухоли с окклюзией гепатохоледоха или БДС;
· хронические панкреатиты со сдавлением холедоха;
· АИХ и ПСХ.
Профилактика
Профилактические мероприятия [3].
При остром гнойном холангите:
· своевременное оперативное лечение при желчекаменной болезни;
· своевременное выявление и лечение опухолевых заболеваний панкреатобилиарной зоны, приводящих к холангиту.
Специфической профилактики ПСХ в настоящее время не существует. ПСХ – это предопухолевое заболевание для ХЦК. ХЦК развивается в результате злокачественной трансформации холангиоцитов.
Дальнейшее ведение:
· после выписки из стационара пациенты, прооперированные по поводу острого гнойного холангита наблюдаются у хирурга/онколога поликлиники в зависимости от причинного фактора. Хирургическое лечение острого гнойного холангита является многоэтапным. Врач поликлиники должен обеспечить своевременную госпитализацию пациента для проведения следующего этапа лечения в специализированное учреждение.
· амбулаторное ведение пациента с ПСХ является мультидисциплинарным и должно включать наблюдение онколога, хирурга и гастроэнтеролога.
Информация
Источники и литература
-
Протоколы заседаний Экспертного совета РЦРЗ МЗСР РК, 2015
- Список использованной литературы (необходимы ссылки валидные исследования на перечисленные источники в тексте протокола):
1) Ю.И. Фишзон-Рысс, Н.А. Пострелов //Клин, медицина.1985.-№11.-С.121-127.
2) А.Н. Катрич Эндоскопическая панкреатобилиарная ультрасонография: методика, клиническое значение. Автореферат диссертации на соискание ученой степени к.м.н. Краснодар, 2008.
3) В.Т. Ивашкин, Т.Л.Лапина Гастроэнтерология (национальное руководство), Москва, 2013 г.
4) В.Г. Авдеев Первичный склерозирующий холангит/ Гепатологический форум. 2009, 1; 24-32.
5) 5.Г.А. Григорьева, Н.Ю. Мешалкина Болезнь Крона, Москва, 2007, с.181
6) Г.А.Ахаладзе Гнойный холангит: вопросы патофизиологии и лечения Consilium medicum Журнал доказательной медицины для практических врачей. Том 05/N 4/2003
7) Ахаладзе Г.Г. Морфологические и микроциркуляторные изменения печени при механической желтухе и холангите / Г.Г. Ахаладзе // XVI Междунар. конгресс хирургов¬гепатологов стран СНГ «Актуальные проблемы хирургической гепатологии»: тезисы докладов. — Екатеринбург, 2009. — С. 108.
Котовский А.Е., Гращенко С.А. и др.. Эндоскопическая папиллосфинктеротомия у больных механической желтухой, осложненной гнойным холангитом. – М.: Третий конгресс ассоциации хирургов им. Н.И. Пирогова. – 2001. – с.113.
9) Багненко С.Ф. Современные подходы к этиологии, патогенезу и лечению холангита и билиарного сепсиса / С.Ф. Багненко, С.А Шляпников, А.Ю. Корольков // Бюллетень сибирской медицины. — 2007. — № 3. — С. 27¬32.
10) Столин А.В. Выбор тактики лечения у больных гнойным холангитом / А.В. Столин, М.И. Прудков, Е.В. Нишневич // Вестник уральской мед. академ. науки. — 2009. — № 3. — С. 126¬129.
11) Young-Mee Lee, M.D., Marshall M. Kaplan, M.D., and the Practice Guideline Committee of the ACG Division of Gastroenterology, New England Medical Center, Tufts University School of Medicine, Boston, Massachusetts PRACTICE GUIDELINES Management of Primary Sclerosing Cholangitis THE AMERICAN JOURNAL OF GASTROENTEROLOGY Vol. 97, No. 3, 2002 © 2002 by Am. Coll. of Gastroenterology ISSN 0002-9270/02/$22.00 Published by Elsevier Science
12) Fumihiko Miura , Tadahiro Takada , Yoshifumi Kawarada , Yuji Nimura , Keita Wada , Masahiko Hirota , Masato Nagino , Toshio Tsuyuguchi , Toshihiko Mayumi , Masahiro Yoshida , Steven M. Strasberg , Henry A. Pitt , Jacques Belghiti , Eduardo de Santibanes, Thomas R. Gadacz, Dirk J. Gouma, Sheung-Tat Fan, Miin-Fu Chen, Robert T. Padbury, Philippus C. Bornman, Sun-Whe Kim, Kui-Hin Liau, Giulio Belli, and Christos Dervenis Flowcharts for the diagnosis and treatment of acute cholangitis and cholecystitis: Tokyo Guidelines J Hepatobiliary Pancreat Surg (2007) 14:27–34 DOI 10.1007/s00534-006-1153-x
13) Tadahiro Takada • Steven M. Strasberg • Joseph S. Solomkin • Henry A. Pitt • Harumi Gomi • Masahiro Yoshida • Toshihiko Mayumi • Fumihiko Miura • Dirk J. Gouma • O. James Garden • Markus W. Bu¨chler • Seiki Kiriyama • Masamichi Yokoe • Yasutoshi Kimura • Toshio Tsuyuguchi • Takao Itoi • Toshifumi Gabata • Ryota Higuchi • Kohji Okamoto • Jiro Hata • Atsuhiko Murata • Shinya Kusachi • John A. Windsor • Avinash N. Supe • SungGyu Lee • Xiao-Ping Chen • Yuichi Yamashita • Koichi Hirata • Kazuo Inui • Yoshinobu Sumiyama Published online: 11 January 2013 Japanese Society of Hepato-Biliary-Pancreatic Surgery and Springer 2012 TG13: Updated Tokyo Guidelines for the management of acute cholangitis and cholecystitis J Hepatobiliary Pancreat Sci (2013) 20:1–7
- Список использованной литературы (необходимы ссылки валидные исследования на перечисленные источники в тексте протокола):
Информация
Список разработчиков протокола с указание квалификационных данных:
1) Мадьяров Валентин Манарбекович – доктор медицинских наук, доцент, заведующий департаментом хирургических болезней НУО «Казахстанско-Российский Медицинский Университет».
2) Меньшикова Ирина Львовна – кандидат медицинских наук, доцент кафедры гастроэнтерологии, гепатологии с курсом эндоскопии РГП на ПХВ «НИИ кардиологии и внутренних болезней» МЗСР РК.
3) Мажитов Талгат Мансурович — доктор медицинских наук, профессор АО «Медицинский университет Астана» врач клинический фармакологии высшей категории, врач-терапевт высшей категории.
Указание на отсутствие конфликта интересов: нет
Рецензенты: Тургунов Ермек Мейрамович – доктор медицинских наук, профессор, хирург высшей квалификационной категории, РГП на ПХВ «Карагандинский государственный медицинский университет» МЗ РК, заведующий кафедрой хирургических болезней №2, независимый аккредитованный эксперт МЗ РК.
Указание условий пересмотра протокола:
Пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.

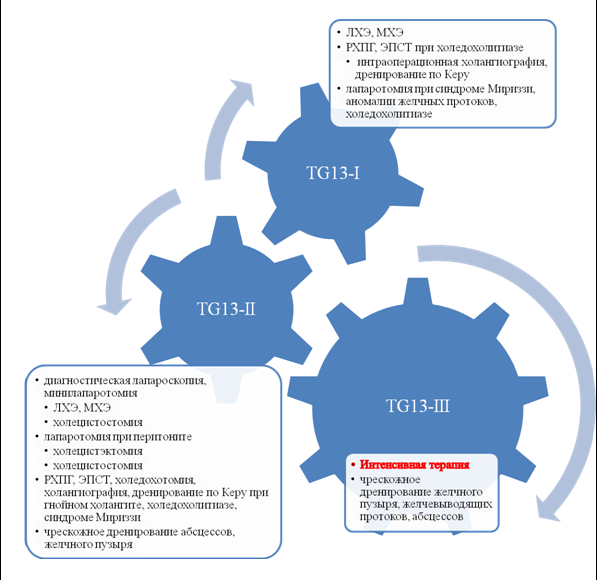



 Котовский А.Е., Гращенко С.А. и др.. Эндоскопическая папиллосфинктеротомия у больных механической желтухой, осложненной гнойным холангитом. – М.: Третий конгресс ассоциации хирургов им. Н.И. Пирогова. – 2001. – с.113.
Котовский А.Е., Гращенко С.А. и др.. Эндоскопическая папиллосфинктеротомия у больных механической желтухой, осложненной гнойным холангитом. – М.: Третий конгресс ассоциации хирургов им. Н.И. Пирогова. – 2001. – с.113.