Описание препарата Твинста® (таблетки, 10 мг+40 мг) основано на официальной инструкции, утверждено компанией-производителем в 2018 году
Дата согласования: 19.09.2018
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Фотографии упаковок
19.09.2018
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки, 5+40 мг | 1 табл. |
| активные вещества: | |
| амлодипина безилат | 6,935 мг |
| (эквивалентно 5 мг амлодипина) | |
| телмисартан | 40 мг |
| вспомогательные вещества | |
| слой телмисартана: натрия гидроксид — 3,36 мг; повидон К25 — 12 мг; меглюмин — 12 мг; сорбитол — 168,64 мг; магния стеарат — 4 мг | |
| слой амлодипина: МКЦ — 125,765 мг; крахмал прежелатинизированный — 53 мг; крахмал кукурузный — 10 мг; кремния диоксид коллоидный — 2 мг; магния стеарат — 2 мг; смесь красителей — 0,3 мг* | |
| * Состоит из 76% железа оксида черного (E172), наименование в НФ — железа оксид), 4% железа оксида желтого (E172), наименование в НФ — железа оксид) и 20% FD&C синего №1 (бриллиантовый голубой FCF алюминиевый лак (E133) |
| Таблетки, 10+40 мг | 1 табл. |
| активные вещества: | |
| амлодипина безилат | 13,87 мг |
| (эквивалентно 10 мг амлодипина) | |
| телмисартан | 40 мг |
| вспомогательные вещества | |
| слой телмисартана: натрия гидроксид — 3,36 мг; повидон К25 — 12 мг; меглюмин — 12 мг; сорбитол — 168,64 мг; магния стеарат — 4 мг | |
| слой амлодипина: МКЦ — 118,83 мг; крахмал прежелатинизированный — 53 мг; крахмал курузный — 10 мг; кремния диоксид коллоидный — 2 мг; магния стеарат — 2 мг; смесь красителей — 0,3 мг* | |
| * Состоит из 76% железа оксида черного (E172), наименование в НФ — железа оксид), 4% железа оксида желтого (E172), наименование в НФ — железа оксид) и 20% FD&C синего №1 (бриллиантовый голубой FCF алюминиевый лак (E133) |
| Таблетки, 5+80 мг | 1 табл. |
| активные вещества: | |
| амлодипина безилат | 6,935 мг |
| (эквивалентно 5 мг амлодипина) | |
| телмисартан | 80 мг |
| вспомогательные вещества | |
| слой телмисартана: натрия гидроксид — 6,72 мг; повидон К25 — 24 мг; меглюмин — 24 мг; сорбитол — 337,28 мг; магния стеарат — 8 мг | |
| слой амлодипина: МКЦ — 125,765 мг; крахмал прежелатинизированный — 53 мг; крахмал кукурузный — 10 мг; кремния диоксид коллоидный — 2 мг; магния стеарат — 2 мг; смесь красителей — 0,3 мг* | |
| * Состоит из 76% железа оксида черного (E172), наименование в НФ — железа оксид), 4% железа оксида желтого (E172), наименование в НФ — железа оксид) и 20% FD&C синего №1 (бриллиантовый голубой FCF алюминиевый лак (E133) |
| Таблетки, 10+80 мг | 1 табл. |
| активные вещества: | |
| амлодипина безилат | 13,87 мг |
| (эквивалентно 10 мг амлодипина) | |
| телмисартан | 80 мг |
| вспомогательные вещества | |
| слой телмисартана: натрия гидроксид — 6,72 мг; повидон К25 — 24 мг; меглюмин — 24 мг; сорбитол — 337,28 мг; магния стеарат — 8 мг | |
| слой амлодипина: МКЦ — 118,83 мг; крахмал прежелатинизированный — 53 мг; крахмал кукурузный — 10 мг; кремния диоксид коллоидный — 2 мг; магния стеарат — 2 мг; смесь красителей — 0,3 мг* | |
| * Состоит из 76% железа оксида черного (E172), наименование в НФ — железа оксид), 4% железа оксида желтого (E172), наименование в НФ — железа оксид) и 20% FD&C синего №1 (бриллиантовый голубой FCF алюминиевый лак (E133) |
Описание лекарственной формы
Овальной формы, двояковыпуклые, двухслойные таблетки без оболочки. Один слой — от белого до почти белого цвета, другой — серо-голубого цвета. На белой поверхности таблеток имеется логотип фирмы и гравировка «А1» (для дозировки 5+40 мг), «А2» (для дозировки 10+40 мг), «А3» (для дозировки 5+80 мг), «А4» (для дозировки 10+80 мг), другая сторона таблетки гладкая.
Фармакологическое действие
Фармакологическое действие
—
гипотензивное.
Фармакодинамика
Твинста® представляет собой комбинированный препарат, содержащий 2 гипотензивных вещества со взаимодополняющим действием, позволяющими контролировать АД у пациентов с артериальной (эссенциальной) гипертензией: АРА II, телмисартан, и блокатор медленных кальциевых каналов (БМКК), производное дигидропиридина, амлодипин.
Комбинация этих веществ обладает аддитивным гипотензивным действием, снижая АД в большей степени, чем каждый отдельный компонент.
Препарат Твинста®, принимаемый 1 раз в сутки, приводит к эффективному и устойчивому снижению АД в течение 24 ч.
Телмисартан
Телмисартан — специфический АРА II (тип AT1), эффективный при приеме внутрь. Обладает высоким сродством к подтипу AT1-рецепторов ангиотензина II, через которые реализуется действие ангиотензина II. Вытесняет ангиотензин II из связи с рецептором, не обладая действием агониста в отношении этого рецептора. Телмисартан связывается только с подтипом AT1-рецепторов ангиотензина II. Связь носит длительный характер. Не обладает сродством к другим рецепторам, в т.ч. к АТ2-рецептору. Снижает концентрацию альдостерона в крови, не ингибирует ренин в плазме крови и не блокирует ионные каналы. Телмисартан не ингибирует АПФ (кининаза II — фермент, который также разрушает брадикинин). Поэтому усиление вызываемых брадикинином нежелательных эффектов не ожидается.
У пациентов телмисартан в дозе 80 мг полностью блокирует гипертензивное действие ангиотензина II. Начало гипотензивного действия отмечается в течение 3 ч после первого приема телмисартана. Действие препарата сохраняется в течение 24 ч и остается значимым до 48 ч. Выраженное гипотензивное действие обычно развивается через 4–8 нед после регулярного приема.
У пациентов с артериальной гипертензией телмисартан снижает сАД и дАД, не оказывая влияния на ЧСС.
В случае резкой отмены телмисартана АД постепенно возвращается к исходному уровню без развития синдрома отмены. Частота развития сухого кашля была значительно ниже у пациентов, получавших телмисартан, в сравнении с применением ингибиторов АПФ.
В ходе двух крупных рандомизированных контролируемых исследований ONTARGET (Исследование глобальных конечных точек при применении телмисартана в рамках монотерапии и в сочетании с рамиприлом) и VA NEPHRON-D (The Veterans Affairs Nephropathy in diabetes — исследование нефропатии при диабете, проводимое департаментом США по делам ветеранов) изучалось применение комбинации ингибитора АПФ в сочетании с АРА II.
Исследование ONTARGET представляло собой исследование, проведенное у пациентов, имеющих в анамнезе сердечно-сосудистые или цереброваскулярные заболевания или сахарный диабет типа 2 с подтвержденным поражением органов-мишеней. Исследование VA NEPHRON-D представляло собой исследование у пациентов с сахарным диабетом типа 2 и диабетической нефропатией.
Эти исследования не показали значительного положительного влияния на почечные и/или сердечно-сосудистые исходы и смертность, тогда как наблюдался повышенный риск развития гиперкалиемии, острой почечной недостаточности и/или артериальной гипотонии по сравнению с монотерапией. Учитывая сходные фармакодинамические свойства, эти результаты также актуальны для других ингибиторов АПФ и АРА II.
Поэтому ингибиторы АПФ и АРА II не должны применяться совместно у пациентов с диабетической нефропатией.
Исследование ALTITUDE (Исследование применения алискирена у пациентов с сахарным диабетом типа 2 с оценкой сердечно-сосудистых и почечных конечных точек) представляло собой исследование, целью которого являлась проверка преимущества добавления алискирена к стандартному лечению ингибитором АПФ или АРА II у пациентов с сахарным диабетом типа 2 и хроническим заболеванием почек, сердечно-сосудистым заболеванием или и тем, и другим. Исследование было прекращено досрочно в связи с повышенным риском неблагоприятных исходов.
Сердечно-сосудистая смерть и инсульт более часто регистрировались в группе алискирена, чем в группе плацебо, а нежелательные явления и серьезные нежелательные явления (гиперкалиемия, артериальная гипотония и нарушение функции почек) чаще отмечались в группе алискирена, чем в группе плацебо.
Наблюдается разница в плазменных концентрациях телмисартана у мужчин и женщин. Cmax и AUC были приблизительно в 3 и 2 раза соответственно выше у женщин по сравнению с мужчинами, без значимого влияния на эффективность.
Амлодипин
Амлодипин — производное дигидропиридина, относится к классу БМКК. Он ингибирует трансмембранное поступление ионов кальция в кардиомиоциты и гладкомышечные клетки сосудов.
Механизм гипотензивного действия амлодипина связан с прямым релаксирующим эффектом на гладкомышечные клетки сосудов, что приводит к уменьшению периферического сосудистогосопротивления и снижению АД.
У пациентов с артериальной гипертензией применение амлодипина 1 раз в сутки обеспечивает клинически значимое снижение АД на протяжении 24 ч. Ортостатическая артериальная гипотензия не характерна во время применения амлодипина вследствие медленного начала действия препарата.
У пациентов с артериальной гипертензией и нормальной функцией почек амлодипин в терапевтических дозах приводил к уменьшению сопротивления сосудов почек, повышению СКФ и эффективного кровотока плазмы в почках без изменения фильтрации или протеинурии.
Амлодипин не приводит к каким-либо метаболическим неблагоприятным эффектам или изменениям концентрации липидов в плазме крови и поэтому подходит для применения у пациентов с бронхиальной астмой, сахарным диабетом и подагрой.
Применение амлодипина у пациентов с сердечной недостаточностью не сопровождается отрицательным инотропным действием (не снижается толерантность к физической нагрузке, не снижается фракция выброса левого желудочка).
Фармакокинетика
Фармакокинетика комбинации фиксированных доз
Скорость и степень всасывания препарата Твинста® эквивалентны биодоступности телмисартана и амлодипина в случае их применения в виде отдельных таблеток.
Фармакокинетика отдельных компонентов
Телмисартан
Всасывание. При приеме внутрь быстро всасывается из ЖКТ. Абсолютная биодоступность телмисартана составляет около 50%. При приеме одновременно с пищей снижение AUC колеблется от 6% (при дозе 40 мг) до 19% (при дозе 160 мг). Через 3 ч после приема внутрь концентрация в плазме крови становится аналогичной концентрации при приеме телмисартана натощак.
Распределение. Связь с белками плазмы крови >99,5%, в основном с альбумином и альфа1 гликопротеином.
Среднее значение видимого Vss — 500 л.
Метаболизм. Метаболизируется телмисартан путем конъюгирования с глюкуроновой кислотой. Метаболиты фармакологически неактивны.
Выведение. T1/2 составляет более 20 ч. Cmax и в меньшей степени AUC увеличиваются непропорционально величине дозы. Данных о клинически значимом накоплении телмисартана, при применении его в рекомендуемых дозах, нет.
Выводится через кишечник в неизмененном виде, почками — менее 1%. Общий плазменный клиренс высокий (приблизительно 1000 мл/мин) по сравнению с печеночным кровотоком (около 1500 мл/мин).
Амлодипин
Всасывание. После приема амлодипина внутрь в терапевтических дозах Cmax в плазме крови достигаются через 6–12 ч. Величина абсолютной биодоступности составляет от 64 до 80%. Прием пищи не влияет на биодоступность амлодипина.
Распределение. Vd амлодипина составляет примерно 21 л/кг. В исследованиях in vitro показано, что у пациентов с артериальной гипертензией приблизительно 97,5% циркулирующего амлодипина связывается с белками плазмы крови.
Метаболизм. Амлодипин в значительной степени (примерно на 90%) метаболизируется в печени с образованием неактивных метаболитов.
Выведение. Выведение амлодипина из плазмы крови происходит двухфазно, T1/2 составляет приблизительно 30–50 ч. Стабильная концентрация в плазме крови достигается после постоянного приема препарата в течение 7–8 дней. Амлодипин выводится почками как в неизмененном виде (10%), так и в виде метаболитов (60%).
Особые группы пациентов
Пожилой возраст. Фармакокинетика телмисартана у пациентов пожилого возраста не отличается от молодых пациентов. У пациентов пожилого возраста отмечается тенденция к снижению клиренса амлодипина, что приводит к увеличению AUC и T1/2.
Почечная недостаточность. Телмисартан связывается с белками плазмы крови и не удаляется при гемодиализе у пациентов с почечной недостаточностью. У пациентов с почечной недостаточностью концентрация телмисартана в плазме крови повышается вдвое. Однако у пациентов, находящихся на гемодиализе, отмечаются более низкие концентрации телмисартана, T1/2 не изменяется. Фармакокинетика амлодипина у пациентов с нарушениями функции почек существенно не изменяется.
Печеночная недостаточность. Исследования фармакокинетики, проводившиеся у пациентов с нарушениями функции печени, показали, что абсолютная биодоступность телмисартана увеличивается почти до 100%. T1/2 у пациентов с нарушениями функции печени не изменяется.
У пациентов с печеночной недостаточностью клиренс амлодипина снижался, что приводило к увеличению значения AUC примерно на 40–60%.
Показания
Артериальная гипертензия (для пациентов, АД которых недостаточно контролируется телмисартаном или амлодипином в монотерапии).
Артериальная гипертензия (для пациентов, которым показана комбинированная терапия).
Пациентам с артериальной гипертензией, получающим телмисартан и амлодипин в виде отдельных таблеток (в качестве замены данной терапии).
Противопоказания
гиперчувствительность к телмисартану или амлодипину, производным дигидропиридина или любому из вспомогательных веществ препарата;
обструктивные заболевания желчевыводящих путей;
тяжелая артериальная гипотензия (сАД менее 90 мм рт.ст.);
обструкция выносящего тракта левого желудочка (включая аортальный стеноз тяжелой степени);
гемодинамически нестабильная сердечная недостаточность после перенесенного острого инфаркта миокарда;
печеночная недостаточность тяжелой степени (класс С по шкале Чайлд-Пью);
шок (включая кардиогенный шок);
одновременное применение с алискиреном у пациентов с сахарным диабетом или почечной недостаточностью (СКФ <60 мл/мин/1,73 м2);
непереносимость фруктозы (из-за наличия в составе препарата сорбитола);
беременность;
период грудного вскармливания;
возраст до 18 лет (эффективность и безопасность не установлены).
С осторожностью
Применение препарата требует тщательного врачебного наблюдения при наличии следующих состояний/заболеваний/факторов риска:
хроническая сердечная недостаточность неишемической этиологии (III–IV функциональный класс по классификации NYHA);
ишемическая болезнь сердца с тяжелым обструктивным поражением коронарных артерий;
острый инфаркт миокарда (и период в течение 1 мес после него);
нестабильная стенокардия;
аортальный стеноз, митральный стеноз, гипертрофическая обструктивная кардиомиопатия;
артериальная гипотензия;
синдром слабости синусного узла (выраженная тахикардия, брадикардия);
одновременное применение с ингибиторами или индукторами изофермента CYP3A4;
двусторонний стеноз почечных артерий или стеноз артерий единственной почки;
почечная или печеночная недостаточность легкой и средней степени тяжести;
состояния после трансплантации почки (в связи с отсутствием опыта применения);
снижение ОЦК вследствие предшествующей диуретической терапии, ограничения приема поваренной соли, диареи или рвоты;
гипонатриемия, гиперкалиемия.
Применение при беременности и кормлении грудью
Специальных исследований препарата Твинста® во время беременности и в период грудного вскармливания не проводилось. Влияния, связанные с отдельными компонентами препарата, описаны ниже.
Телмисартан
Применение АРА II противопоказано во время беременности. При диагностировании беременности прием препарата следует немедленно прекратить. При необходимости должна назначаться альтернативная терапия.
Доклинические исследования телмисартана не выявили тератогенных свойств, но установили наличие фетотоксичности. Известно, что применение АРА II в течение II и III триместров беременности оказывает фетотоксическое действие (снижение функции почек, олигогидрамнион, замедление оссификации черепа плода), а также наблюдается неонатальная токсичность (почечная недостаточность, артериальная гипотензия и гиперкалиемия).
У пациенток, планирующих беременность, АРА II должны заменяться на другие гипотензивные средства, которые характеризуются установленным профилем безопасности при применении во время беременности (если только продолжение лечения АРА II не считается необходимым).
Если АРА II применяются во время беременности, то начиная со II триместра беременности, рекомендуется УЗИ-контроль функции почек и состояния черепа.
Новорожденные, матери которых получали АРА II, должны тщательно наблюдаться в отношении развития артериальной гипотензии.
Амлодипин
Имеющиеся ограниченные данные в отношении воздействия амлодипина или других БМКК не указывают на наличие отрицательных влияний на плод. Однако возможен риск замедления процесса родов.
Амлодипин экскретируется в грудное молоко. Доля дозы, полученной младенцем, оценивалась в диапазоне от 3 до 7%, с максимумом 15%. Влияние амлодипина на детей, находящихся на грудном вскармливании, неизвестно.
Специальных исследований о выделении телмисартана с грудным молоком у женщин не проводилось. В исследованиях на животных выявлено, что телмисартан выделяется с молоком лактирующих животных. Учитывая возможные неблагоприятные реакции, решение о продолжении грудного вскармливания или об отмене терапии должно приниматься с учетом ее значимости для матери.
Исследований влияния на фертильность человека не проводилось.
Способ применения и дозы
Внутрь, вне зависимости от приема пищи, 1 раз в сутки.
Препарат Твинста® может назначаться пациентам, получающим те же дозы телмисартана и амлодипина в виде отдельных таблеток, для удобства терапии и увеличения приверженности лечению.
Препарат Твинста® может назначаться пациентам, у которых применение одного амлодипина или одного телмисартана не приводит к адекватному контролю АД.
Пациенты, принимающие амлодипин в дозе 10 мг, у которых отмечаются нежелательные реакции, ограничивающие прием препарата, например периферические отеки, могут перейти на прием препарата Твинста® в дозе 5+40 мг 1 раз в сутки, что позволит уменьшить дозу амлодипина, но не снизит общее ожидаемое гипотензивное действие.
Лечение артериальной гипертензии у пациента может начинаться с применения препарата Твинста® в том случае, когда предполагается, что достижение контроля АД с помощью какого-либо одного препарата маловероятно. Обычная начальная доза препарата Твинста® — 5+40 мг 1 раз в сутки. Пациенты, которым необходимо более значительное снижение АД, могут начинать прием препарата Твинста® в дозе 5+80 мг 1 раз в сутки.
Если по крайней мере через 2 нед лечения потребуется дополнительное снижение АД, доза препарата может быть постепенно увеличена до максимальной — 10+80 мг 1 раз в сутки.
Препарат Твинста® может применяться вместе с другими гипотензивными препаратами.
Особые группы пациентов
Нарушения функции почек. У пациентов с нарушениями функции почек, в т.ч. пациентов, находящихся на гемодиализе, изменений режима дозирования препарата не требуется. Амлодипин и телмисартан не удаляются из организма при проведении гемодиализа.
Нарушения функции печени. У пациентов с печеночной недостаточностью легкой и средней степени препарат Твинста® должен применяться с осторожностью. Доза телмисартана не должна превышать 40 мг 1 раз в сутки.
Пожилые пациенты. Режим дозирования не требует коррекции.
Дети и подростки в возрасте до 18 лет. Данные по эффективности и безопасности комбинации амлодипин/телмисартан у детей и подростков младше 18 лет отсутствуют.
Побочные действия
Наиболее распространенные нежелательные реакции включают головокружение и периферические отеки. Серьезный обморок может возникнуть в редких случаях (менее 1 случая на 1000 пациентов).
Нежелательные реакции, ранее описанные при применении одного из компонентов (телмисартан или амлодипин), могут также быть потенциальными побочными реакциями при применении препарата Твинста®, даже если они не наблюдались в ходе клинических исследований или во время пострегистрационного периода.
Внутри системно-органных классов по частоте возникновения нежелательных реакций используются следующие категории: очень часто (?1/10); часто (?1/100, </10); нечасто (?1/1000, <1/100); редко (?1/10000, <1/1000); очень редко (<1/10000); частота неизвестна (не может быть подсчитана по имеющимся данным).
Таблица
| Системно-органный класс | Нежелательная реакция | Частота возникновения |
| Инфекционные и паразитарные заболевания |
Инфекции мочевыводящих путей, включая цистит1, инфекции верхних дыхательных путей, включая фарингит и синусит1 | Нечасто |
| Цистит3, сепсис, в т.ч. с летальным исходом1 | Редко | |
| Со стороны крови и лимфатической системы | Анемия1 | Нечасто |
| Тромбоцитопения1, эозинофилия1 | Редко | |
| Лейкопения2, тромбоцитопения2 | Очень редко | |
| Со стороны иммунной системы | Гиперчувствительность1, анафилактическая реакция1 | Редко |
| Гиперчувствительность2 | Очень редко | |
| Со стороны обмена веществ и питания | Гиперкалиемия1 | Нечасто |
| Гипогликемия (у пациентов с сахарным диабетом)1 | Редко | |
| Гипергликемия2 | Очень редко | |
| Нарушения психики | Изменения настроения2 | Нечасто |
| Депрессия3, беспокойство3, бессонница3, спутанность сознания2 | Редко | |
| Со стороны нервной системы | Головокружение3 | Часто |
| Сонливость3, мигрень3, головная боль3, парестезии3 | Нечасто | |
| Обморок3, периферическая нейропатия3, гипестезия3, дисгевзия3, тремор3 | Редко | |
| Экстрапирамидный синдром2 | Очень редко | |
| Со стороны органа зрения | Нарушения зрения2 | Нечасто |
| Зрительные расстройства1 | Редко | |
| Со стороны органа слуха и лабиринтные нарушения | Вертиго3, шум в ушах3 | Нечасто |
| Со стороны сердца | Брадикардия3, ощущение сердцебиения3 | Нечасто |
| Тахикардия1 | Редко | |
| Инфаркт миокарда2, аритмия2, желудочковая тахикардия2, фибрилляция предсердий2 | Очень редко | |
| Со стороны сосудов | Гипотензия3, ортостатическая гипотензия3, приливы3 |
Нечасто |
| Васкулит2 | Очень редко | |
| Со стороны дыхательной системы, органов грудной клетки и средостения | Кашель3, одышка1,2, ринит2 | Нечасто |
| Интерстициальное заболевание легких3 | Очень редко | |
| Со стороны ЖКТ | Боль в животе3, диарея3, тошнота3, метеоризм1, изменение ритма опорожнения кишечника2 | Нечасто |
| Рвота3, гипертрофия десен3, одышка3, сухость в полости рта3, дискомфорт в желудке1 | Редко | |
| Панкреатит2, гастрит1 | Очень редко | |
| Со стороны печени и желчевыводящих путей | Нарушения функции печени1, патология печени1 | Редко |
| Гепатит2, желтуха2, повышение активности печеночных трансаминаз (главным образом отражающих холестаз)2 |
Очень редко | |
| Со стороны кожи и подкожных тканей | Кожный зуд3, гипергидроз1,2, алопеция2, пурпура2, изменение цвета кожи2 |
Нечасто |
| Экзема3, эритема3, ангионевротический отек (с летальным исходом)1, лекарственная сыпь1, токсическая сыпь1, крапивница1 |
Редко | |
| Ангионевротический отек2, мультиформная эритема2, крапивница1, эксфолиативный дерматит2, синдром Стивенса-Джонсона2, реакция фотосенсибилизации2 | Очень редко | |
| Токсический эпидермальный некролиз2 | Частота неизвестна | |
| Со стороны скелетно-мышечной системы и соединительной ткани | Артралгии3, спазмы мышц (судороги икроножных мышц)3, миалгии3 |
Нечасто |
| Боль в спине3, боль в нижних конечностях (ногах)3, боль в сухожилиях (тендинитоподобные симптомы)1 |
Редко | |
| Со стороны почек и мочевыводящих путей | Нарушения функции почек, включая острую почечную недостаточность1, нарушения мочеиспускания2, учащенное мочеиспускание2 | Нечасто |
| Никтурия3 | Редко | |
| Со стороны половых органов и молочной железы | Эректильная дисфункция3, гинекомастия2 | Нечасто |
| Общие расстройства и нарушения в месте введения | Периферические отеки3 | Часто |
| Астения3, боль в грудной клетке3, усталость3, отеки3, боль2 |
Нечасто | |
| Недомогание2, гриппоподобный синдром1 | Редко | |
| Лабораторные и инструментальные данные | Повышение концентрации печеночных ферментов3, повышение концентрации креатинина в крови1, повышение веса2, снижение веса2 | Нечасто |
| Повышение концентрации мочевой кислоты в крови3, повышение активности КФК в крови1, снижение Hb1 | Редко |
1 Ожидающиеся на основании опыта применения телмисартана.
2 Ожидающиеся на основании опыта применения амлодипина.
3 Ожидающиеся при одновременном применении телмисартана и амлодипина.
Дополнительная информация в отношении отдельных компонентов. Нежелательные реакции, ранее сообщавшиеся при применении одного из компонентов препарата (амлодипин или телмисартан), могут усиливаться при применении препарата Твинста®, даже если они не наблюдались в клинических исследованиях или во время постмаркетингового периода.
Дополнительная информация в отношении комбинации компонентов. Периферические отеки, дозозависимая нежелательная реакция на амлодипин наблюдались у пациентов, которые получали комбинацию телмисартана и амлодипина, реже, чем у пациентов, получавших только амлодипин.
Взаимодействие
Взаимодействий между амлодипином и телмисартаном в клинических исследованиях не выявлено.
Специальных исследований лекарственных взаимодействий препарата Твинста® с другими препаратами не проводилось.
Комбинация действующих веществ
Другие гипотензивные средства. При одновременном применении с другими гипотензивными препаратами гипотензивное действие препарата Твинста® может усиливаться.
Препараты, способные снижать АД. Можно ожидать, что некоторые препараты, например баклофен, амифостин, нейролептики и антидепрессанты, благодаря своим фармакологическим свойствам, будут усиливать гипотензивное действие всех гипотензивных средств, включая препарат Твинста®. Кроме того, ортостатическая артериальная гипотензия может усиливаться этанолом.
Кортикостероиды (системное применение). Возможно снижение гипотензивного действия.
Телмисартан
Совместное применение не рекомендовано
Калийсберегающие диуретики или препараты калия. АРА II, такие как телмисартан, снижают потери калия, вызванные применением диуретиков. Применение калийсберегающих диуретиков, например спиринолактона, эплеренона, триамтерена или амилорида, препаратов калия или калийсодержащей соли может привести к значительному увеличению концентрации калия в сыворотке крови. Если сопутствующее применение показано в связи с документированной гипокалиемией, эти лекарственные препараты следует применять с осторожностью и частым контролем сывороточного содержания калия.
Препараты лития. Отмечалось обратимое увеличение концентрации лития в крови, сопровождающееся токсическими явлениями, при приеме ингибиторов АПФ. В редких случаях подобные изменения зарегистрированы при назначении АРА II, в частности телмисартана. При одновременном назначении препаратов лития и АРА II рекомендуется проводить определение содержания лития в крови.
Другие гипотензивные средства. Возможно усиление гипотензивного действия. В одном исследовании при комбинированном применении телмисартана и рамиприла наблюдалось повышение AUC0–24 и Cmax рамиприла и рамиприлата в 2,5 раза. Клиническая значимость этого взаимодействия не установлена.
Двойная блокада РААС (например, совместное применение ингибиторов АПФ или алискирена, прямого ингибитора ренина с АРА II) не рекомендуется из-за возможного нарушения функции почек (включая острую почечную недостаточность).
Совместное применение, требующее соблюдения мер предосторожности
НПВП, включая ацетилсалициловую кислоту (в дозах, применяемых в качестве противовоспалительного средства), ингибиторы ЦОГ-2 и неселективные НПВП, могут снизить выраженность гипотензивного эффекта АРА II. У некоторых пациентов с почечной недостаточностью (например, пациенты с обезвоживанием или пожилые пациенты с почечной недостаточностью) совместное применение АРА II и лекарственных препаратов, которые подавляют активность ЦОГ, может привести к дополнительному ухудшению функции почек, включая возможное развитие острой почечной недостаточности; эти эффекты, как правило, обратимы. Поэтому данную комбинацию следует применять с осторожностью, особенно у пожилых людей. Пациенты должны быть адекватно гидратированы, при этом следует контролировать функцию почек после начала совместного применения данных лекарственных препаратов и периодически после этого.
Рамиприл. В одном исследовании совместное применение телмисартана и рамиприла привело к увеличению значений AUC0–24 и Cmax рамиприла и рамиприлата в 2,5 раза. Клиническая значимость этого наблюдения неизвестна.
Совместное применение, которое следует принимать во внимание
Дигоксин. При совместном применении телмисартана с дигоксином наблюдалось увеличение медианы Cmax дигоксина в плазме крови (49%) и остаточной концентрации дигоксина (20%). При инициировании, коррекции доз и отмене телмисартана следует контролировать концентрации дигоксина в плазме крови, чтобы поддерживать их в терапевтическом диапазоне.
Амлодипин
Совместное применение, требующее соблюдения мер предосторожности
Ингибиторы изофермента CYP3A4. При совместном применении с ингибитором CYP3A4 эритромицином у молодых пациентов и с дилтиаземом у пожилых пациентов концентрация амлодипина в плазме крови возрастала на 22 и 50% соответственно. Однако клиническая значимость этого наблюдения неясна.
Нельзя исключить, что более активные ингибиторы изофермента CYP3A4 (такие как кетоконазол, итраконазол, ритонавир) могут увеличивать концентрации амлодипина в плазме крови в большей степени, чем дилтиазем. Амлодипин следует применять с осторожностью совместно с ингибиторами изофермента CYP3A4. Однако никаких нежелательных эффектов, связанных с таким взаимодействием, отмечено не было.
Индукторы изофермента CYP3A4. При совместном применении известных индукторов CYP3A4 концентрация амлодипина в плазме может варьировать. Таким образом, необходимо контролировать АД и регулировать дозу во время и после сопутствующего лечения, особенно с сильными индукторами CYP3A4 (например, рифампицин, препараты зверобоя продырявленного (Hypericum perforatum).
Грейпфрут и грейпфрутовый сок. Одновременное применение у 20 здоровых добровольцев 240 мл сока грейпфрута с однократной дозой амлодипина 10 мг, принимавшейся внутрь, не приводило к существенному влиянию на фармакокинетические свойства амлодипина.
Одновременное применение препарата Твинста® с грейпфрутом или грейпфрутовым соком не рекомендуется, т.к. у некоторых пациентов в результате повышения биодоступности амлодипина может усиливаться антигипертензивное действие.
Совместное применение, которое следует принимать во внимание
Такролимус. Существует риск повышения концентраций такролимуса при его совместном применении с амлодипином, но фармакокинетический механизм этого взаимодействия до конца не изучен. Во избежание токсичности такролимуса применение амлодипина у пациентов, получающих такролимус, требует мониторинга концентраций такролимуса и коррекции дозы такролимуса, когда это необходимо.
Циклоспорин. Не проводились исследования лекарственных взаимодействий циклоспорина и амлодипина у здоровых добровольцев или в других популяциях, за исключением пациентов, перенесших трансплантацию почек, у которых наблюдалось вариабельное увеличение остаточной концентрации циклоспорина (в среднем 0–40%). Необходимо рассмотреть вопрос о контроле концентраций циклоспорина у пациентов, перенесших трансплантацию почек, получающих амлодипин, а также сократить дозы циклоспорина, если это необходимо.
Симвастатин. Совместное применение амлодипина с симвастатином в дозе 80 мг приводило к увеличению экспозиции симвастатина до 77% по сравнению с монотерапией симвастатином. Поэтому доза симвастатина не должна превышать 20 мг/сут.
Другие препараты. Установлена безопасность совместного применения амлодипина с дигоксином, варфарином, аторвастатином, силденафилом, антацидными лекарственными препаратами (гидроксид алюминия, гидроксид магния, симетикон), циметидином, антибиотиками и пероральными гипогликемическими лекарственными препаратами.
При одновременном применении амлодипина и силденафила показано, что каждый препарат оказывал независимое гипотензивное действие.
Одновременное применение амлодипина с циметидином не оказывало существенного влияния на фармакокинетику амлодипина. Одновременное применение амлодипина с аторвастатином, дигоксином, варфарином или циклоспорином существенно не влияло на фармакокинетику или фармакодинамику этих препаратов.
Передозировка
Симптомы: случаи передозировки не выявлены. Возможные симптомы передозировки складываются из симптомов со стороны отдельных компонентов препарата.
Телмисартан — тахикардия, возможно, брадикардия, головокружение, повышение концентрации креатинина в сыворотке крови, острая почечная недостаточность.
Амлодипин — выраженное снижение АД с возможным развитием рефлекторной тахикардии и симптомами чрезмерной периферической вазодилатации (риск развития выраженной и стойкой артериальной гипотензии, в т.ч. с развитием шока и летального исхода).
Лечение: гемодиализ неэффективен. Контроль состояния больного, терапия должна быть симптоматической и поддерживающей.
С целью купирования блокады кальциевых каналов возможно в/в струйное введение глюконата кальция.
Могут применяться методы лечения передозировки, такие как индукция рвоты, промывание желудка, применение активированного угля, перевод пациента в положение с приподнятыми ногами и введение плазмозамещающих растворов в случае выраженного снижения АД.
Особые указания
Беременность. Применение АРА II не следует начинать во время беременности. За исключением тех случаев, когда продолжение лечения не считается необходимым, у пациенток, планирующих беременность, эти лекарственные препараты должны быть заменены на альтернативные антигипертензивные лекарственные препараты, которые имеют изученный профиль безопасности для использования во время беременности. Когда диагностируется беременность, лечение АРА II следует немедленно прекратить и при необходимости, начать альтернативное лечение.
Печеночная недостаточность. Телмисартан выводится преимущественно с желчью. Ожидается, что у пациентов с обструкцией желчевыводящих путей или печеночной недостаточностью клиренс лекарственного препарата снижается. Кроме того, как и у всех антагонистов кальция, T1/2 амлодипина у пациентов с нарушенной функцией печени увеличивается, а рекомендации по дозированию этого лекарственного препарата не установлены. В связи с этим комбинацию телмисартан + амлодипин у таких пациентов следует применять с осторожностью.
Реноваскулярная артериальная гипертензия. У пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной функционирующей почки, принимающих лекарственные препараты, влияющие на РААС, существует повышенный риск развития выраженной гипотензии и почечной недостаточности.
Нарушения функции почек и состояния после трансплантации почки. Опыт применения препарата Твинста® у пациентов, которым была недавно проведена трансплантация почки, отсутствует. Амлодипин и телмисартан не удаляются при гемодиализе. Пациентам с нарушениями функции почек рекомендуется периодический контроль содержания калия и креатинина в сыворотке крови.
Сниженный ОЦК и/или гипонатриемия. Вследствие ограничения потребления поваренной соли, интенсивной терапии диуретическими средствами, диареи или рвоты может развиваться симптоматическая артериальная гипотензия, особенно после приема первой дозы препарата. Перед применением препарата Твинста® такие состояния требуют коррекции. Если артериальная гипотония возникает на фоне применения препарата Твинста®, пациента необходимо положить на спину и если необходимо, назначить ему в/в введение физиологического раствора. Лечение может быть продолжено после стабилизации АД.
Двойная блокада РААС. Имеются данные, что одновременное применение ингибиторов АПФ, АРА II или алискирена увеличивает риск развития гипотонии, гиперкалиемии и снижения функции почек (включая острую почечную недостаточность). Поэтому двойная блокада РААС путем комбинированного применения ингибиторов АПФ, АРА II или алискирена не рекомендована.
Если лечение с двойной блокадой РААС считается необходимым, его следует проводить только под наблюдением специалиста и при условии тщательного контроля функции почек, концентрации электролитов и АД.
Ингибиторы АПФ и АРА II не должны применяться одновременно у пациентов с диабетической нефропатией.
Другие состояния, характеризующиеся активацией РААС. В случаях зависимости сосудистого тонуса и функции почек преимущественно от активности РААС (например, у пациентов с ХСН или заболеваниями почек, в т.ч. при стенозе почечных артерий) назначение препаратов, влияющих на эту систему, может сопровождаться развитием острой артериальной гипотензии, гиперазотемии, олигурии и в редких случаях — острой почечной недостаточности.
Первичный альдостеронизм. У пациентов с первичным альдостеронизмом гипотензивные лекарственные препараты, механизм действия которых состоит в ингибировании РААС, как правило, неэффективны. Таким образом, применение телмисартана в этиих случаях не рекомендуется.
Сахарный диабет. У пациентов с сахарным диабетом (СД) с дополнительным сердечно-сосудистым риском (т.е. с сопутствующей ИБС) риск развития фатального инфаркта миокарда и внезапной сердечно-сосудистой смерти могут быть увеличены при лечении гипотензивными средствами, такими как APA II и ингибиторами АПФ.
Стеноз аортального и митрального клапанов, гипертрофическая обструктивная кардиомиопатия. У пациентов с аортальным или митральным стенозом или с обструктивной гипертрофической кардиомиопатией применение препарата Твинста®, также как и других вазодилататоров, требует особой осторожности.
Нестабильная стенокардия, острый инфаркт миокарда. Нет данных о применении препарата Твинста® у пациентов с нестабильной стенокардией, в остром периоде и в течение 1 мес после инфаркта миокарда.
Сердечная недостаточность. В клиническом исследовании установлено, что применение амлодипина у пациентов с сердечной недостаточностью неишемической этиологии III и IV функционального класса по классификации NYHA сопровождалось более частым развитием отека легких (несмотря на отсутствие существенного различия в частоте ухудшения сердечной недостаточности по сравнению с плацебо).
Пациенты с сахарным диабетом, получающие инсулин или другие сахароснижающие лекарственные препараты. У данных пациентов гипогликемия может возникнуть при лечении телмисартаном. Поэтому у таких пациентов следует рассмотреть возможность проведения надлежащего мониторинга концентрации глюкозы в крови; может потребоваться коррекция дозы инсулина или сахароснижающих лекарственных препаратов, если это необходимо.
Гиперкалиемия. Во время лечения лекарственными препаратами, которые влияют на РААС, особенно при наличии нарушений функции почек и/или сердечной недостаточности, может возникать гиперкалиемия. Гиперкалиемия может быть фатальной у пожилых пациентов, пациентов с почечной недостаточностью, пациентов с СД, пациентов, которые одновременно получают другие лекарственные препараты, способные повышать концентрацию калия в сыворотке крови, и/или пациентов с интеркуррентными событиями.
Прежде чем рассматривать возможность совместного применения лекарственных препаратов, которые влияют на РААС, необходимо оценить соотношение польза-риск.
Основными факторами риска развития гиперкалиемии являются:
— СД, нарушение функции почек, возраст (>70 лет);
— комбинация с одним или несколькими другими лекарственными препаратами, которые влияют на РААС, и/или пищевыми добавками, содержащими калий. Лекарственные препараты или терапевтические классы лекарственных препаратов, которые могут спровоцировать развитие гиперкалиемии, представляют собой соли, содержащие калий, калийсберегающие диуретики, ингибиторы АПФ, АРА II, НПВП (включая селективные ингибиторы ЦОГ-2), гепарин, иммунодепрессанты (циклоспорин или такролимус) и триметоприм;
— интеркуррентные события, в частности дегидратация, острая декомпенсация сердечной деятельности, метаболический ацидоз, ухудшение функции почек, внезапное ухудшение состояния почек (например, инфекционные заболевания), клеточный лизис (например, ишемия конечности, рабдомиолиз, обширная травма).
У данных пациентов следует тщательно контролировать концентрацию калия в сыворотке крови.
Сорбитол. Каждая таблетка препарата Твинста® содержит 168,64 мг сорбитола.
Прочее. Чрезмерное снижение АД у пациентов с ишемической кардиомиопатией или ишемическим сердечно-сосудистым заболеванием может привести к развитию инфаркта миокарда или инсульта.
Препарат Твинста® эффективен при лечении пациентов негроидной расы (в этой популяции обычно снижена активность ренина в крови).
Влияние на способность к управлению транспортными средствами и механизмами. Исследования влияния на способность к управлению транспортными средствами и управлению механизмами не проводились. Однако следует принимать во внимание, что во время лечения могут отмечаться такие нежелательные реакции, как обморок, сонливость или головокружение. Поэтому во время управления транспортными средствами или механизмами следует соблюдать осторожность. Если пациенты испытывают эти ощущения, им следует избегать выполнения таких потенциально опасных действий, как вождение автотранспорта или управление механизмами.
Форма выпуска
Таблетки, 5+40 мг, 10+40 мг, 5+80 мг, 10+80 мг. По 7 табл. в блистере из Аl/Аl фольги.
По 2 или 4 бл. помещают в картонную пачку.
Производитель
Производство готовой лекарственной формы. Берингер Ингельхайм Фарма ГмбХ и Ко.КГ, Бингер Штрассе, 173, 55216 Ингельхайм-на-Рейне, Германия.
или
Ципла Лтд., участок L-139-L-146, промышленная зона Верна, Верна Гоа, Индия.
Первичная и вторичная упаковка. Берингер Ингельхайм Фарма ГмбХ и Ко. КГ, Бингер Штрассе, 173, 55216 Ингельхайм-на-Рейне, Германия.
Выпускающий контроль качества (производитель). Берингер Ингельхайм Фарма ГмбХ и Ко. КГ, Бингер Штрассе, 173, 55216 Ингельхайм-на-Рейне, Германия.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение. Берингер Ингельхайм Интернешнл ГмбХ, Германия. Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия.
Организация, уполномоченная на принятие претензий от потребителя. ООО «Берингер Ингельхайм», 125171, Москва, Ленинградское ш., 16А, стр. 3.
Тел.: (495) 544-50-44; факс: (495) 544-56-20.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 25 °C, в оригинальной упаковке.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Твинста® (Twynsta®) инструкция по применению
📜 Инструкция по применению Твинста®
💊 Состав препарата Твинста®
✅ Применение препарата Твинста®
📅 Условия хранения Твинста®
⏳ Срок годности Твинста®
Описание лекарственного препарата
Твинста®
(Twynsta®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2018 года.
Дата обновления: 2017.12.14
Код ATX:
C09DB04
(Амлодипин и телмисартан)
Лекарственные формы
| Твинста® |
Таб. 5 мг+40 мг: 14 или 28 шт. рег. №: ЛП-(000345)-(РГ-RU) |
|
|
Таб. 5 мг+80 мг: 14 или 28 шт. рег. №: ЛП-(000345)-(РГ-RU) |
||
|
Таб. 10 мг+80 мг: 14 или 28 шт. рег. №: ЛП-(000345)-(РГ-RU) |
||
|
Таб. 10 мг+40 мг: 14 или 28 шт. рег. №: ЛП-(000345)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Твинста®
Таблетки овальные, двояковыпуклые, без оболочки, двухслойные, один слой от белого до почти белого цвета, другой слой серо-голубого цвета; на белой поверхности — логотип фирмы и гравировка «А1», другая сторона таблетки гладкая.
Вспомогательные вещества: натрия гидроксид — 3.360 мг, повидон К25 — 12.000 мг, меглюмин — 12.000 мг, сорбитол — 168.640 мг, магния стеарат — 6.000 мг, целлюлоза микрокристаллическая — 125.765 мг, крахмал прежелатинизированный — 53.000 мг, крахмал кукурузный — 10.000 мг, кремния диоксид коллоидный — 2.000 мг, смесь красителей — 0.300 мг*.
7 шт. — блистеры (2) — пачки картонные.
7 шт. — блистеры (4) — пачки картонные.
Таблетки овальные, двояковыпуклые, без оболочки, двухслойные, один слой от белого до почти белого цвета, другой слой серо-голубого цвета; на белой поверхности — логотип фирмы и гравировка «А2», другая сторона таблетки гладкая.
Вспомогательные вещества: натрия гидроксид — 3.360 мг, повидон К25 — 12.000 мг, меглюмин — 12.000 мг, сорбитол — 168.640 мг, магния стеарат — 6.000 мг, целлюлоза микрокристаллическая — 118.830 мг, крахмал прежелатинизированный — 53.000 мг, крахмал кукурузный — 10.000 мг, кремния диоксид коллоидный — 2.000 мг, смесь красителей — 0.300 мг*.
7 шт. — блистеры (2) — пачки картонные.
7 шт. — блистеры (4) — пачки картонные.
Таблетки овальные, двояковыпуклые, без оболочки, двухслойные, один слой от белого до почти белого цвета, другой слой серо-голубого цвета; на белой поверхности — логотип фирмы и гравировка «А3», другая сторона таблетки гладкая.
Вспомогательные вещества: натрия гидроксид — 6.720 мг, повидон К25 — 24.000 мг, меглюмин — 24.000 мг, сорбитол — 337.280 мг, магния стеарат — 10.000 мг, целлюлоза микрокристаллическая — 125.765 мг, крахмал прежелатинизированный — 53.000 мг, крахмал кукурузный — 10.000 мг, кремния диоксид коллоидный — 2.000 мг, смесь красителей — 0.300 мг*.
7 шт. — блистеры (2) — пачки картонные.
7 шт. — блистеры (4) — пачки картонные.
Таблетки овальные, двояковыпуклые, без оболочки, двухслойные, один слой от белого до почти белого цвета, другой слой серо-голубого цвета; на белой поверхности — логотип фирмы и гравировка «А4», другая сторона таблетки гладкая.
Вспомогательные вещества: натрия гидроксид — 6.720 мг, повидон К25 — 24.000 мг, меглюмин — 24.000 мг, сорбитол — 337.280 мг, магния стеарат — 10.000 мг, целлюлоза микрокристаллическая — 118.830 мг, крахмал прежелатинизированный — 53.000 мг, крахмал кукурузный — 10.000 мг, кремния диоксид коллоидный — 2.000 мг, смесь красителей — 0.300 мг*.
7 шт. — блистеры (2) — пачки картонные.
7 шт. — блистеры (4) — пачки картонные.
* Смесь красителей состоит из 76% оксида железа черного (E172, наименование в НФ: оксид железа), 4% оксида железа желтого (Е172, наименование в НФ: оксид железа) и 20% FD&C синего №1 (бриллиантового голубого FCF алюминиевого лака) (Е133).
Фармакологическое действие
Комбинированный антигипертензивный препарат, содержащий два активных компонента с взаимодополняющим действием, позволяющих контролировать АД у пациентов с артериальной (эссенциальной) гипертензией: антагонист рецепторов ангиотензина II (телмисартан) и блокатор медленных кальциевых каналов, производное дигидропиридина (амлодипин). Комбинация этих веществ обладает аддитивным антигипертензивным действием, снижая АД в большей степени, чем каждый компонент по отдельности. Препарат Твинста®, принимаемый 1 раз/сут, приводит к эффективному и устойчивому снижению АД в течение 24 ч.
Телмисартан
Телмисартан — специфический антагонист рецепторов ангиотензина II (тип AT1), эффективный при приеме внутрь. Обладает высоким сродством к подтипу AT1-рецепторов ангиотензина II, через которые реализуется действие ангиотензина II. Вытесняет ангиотензин II из связи с рецептором, не обладая действием агониста в отношении этого рецептора. Телмисартан связывается только с подтипом AT1-рецепторов ангиотензина II. Связывание носит длительный характер. Не обладает сродством к другим рецепторам, в т.ч. к АТ2-рецептору. Снижает концентрацию альдостерона в крови, не ингибирует ренин в плазме крови и не блокирует ионные каналы. Телмисартан не ингибирует АПФ (кининазу II) — фермент, который также разрушает брадикинин, поэтому усиление вызываемых брадикинином побочных эффектов не ожидается.
У пациентов телмисартан в дозе 80 мг полностью блокирует гипертензивное действие ангиотензина II. Начало антигипертензивного действия отмечается в течение 3 ч после первого приема телмисартана. Действие препарата сохраняется в течение 24 ч и остается значимым до 48 ч. Выраженный антигипертензивный эффект обычно развивается через 4-8 недель регулярного применения.
У пациентов с артериальной гипертензией, телмисартан снижает систолическое и диастолическое АД, не оказывая влияния на ЧСС.
В случае резкой отмены телмисартана АД постепенно возвращается к исходному уровню без развития синдрома отмены.
Амлодипин
Амлодипин — производное дигидропиридина, относится к классу блокаторов медленных кальциевых каналов. Ингибирует трансмембранное поступление ионов кальция в кардиомиоциты и гладкомышечные клетки сосудов. Механизм антигипертензивного действия амлодипина связан с прямым релаксирующим эффектом на гладкомышечные клетки сосудов, что приводит к уменьшению периферического сосудистого сопротивления и снижению АД.
У пациентов с артериальной гипертензией применение амлодипина 1 раз/сут обеспечивает клинически значимое снижение АД на протяжении 24 ч.
Ортостатическая артериальная гипотензия не характерна при применении амлодипина вследствие медленного начала действия препарата.
У пациентов с артериальной гипертензией и нормальной функцией почек амлодипин в терапевтических дозах приводил к уменьшению сопротивления сосудов почек, повышению скорости клубочковой фильтрации и эффективному кровотоку плазмы в почках, без изменения фильтрации или протеинурии.
Амлодипин не приводит к каким-либо метаболическим неблагоприятным эффектам или изменению содержания липидов плазмы крови, поэтому подходит для применения у пациентов с бронхиальной астмой, сахарным диабетом и подагрой.
Применение амлодипина у пациентов с сердечной недостаточностью не сопровождается отрицательным инотропным действием (не снижается толерантность к физической нагрузке, не снижается фракция выброса левого желудочка).
Фармакокинетика
Скорость и степень всасывания препарата Твинста® эквивалентны биодоступности телмисартана и амлодипина при раздельном применении.
Телмисартан
Всасывание
При приеме внутрь быстро всасывается из ЖКТ. Биодоступность — 50%. При приеме одновременно с пищей снижение AUC колеблется от 6% (при применении в дозе 40 мг) до 19% (при применении в дозе 160 мг). Через 3 ч после приема внутрь концентрация в плазме крови выравнивается, независимо от приема пищи. Cmax в плазме крови и, в меньшей степени, AUC увеличиваются непропорционально величине дозы.
Распределение
Связывание с белками плазмы крови — 99.5%, в основном, с альбумином и альфа1-гликопротеином. Среднее значение видимого Vd в равновесной концентрации 500 л. Данных о клинически существенном накоплении телмисартана не имеется.
Метаболизм
Метаболизируется телмисартан путем конъюгирования с глюкуроновой кислотой. Метаболиты фармакологически неактивны.
Выведение
T1/2 составляет более 20 ч. Выводится в неизмененном виде с калом, выведение с мочой — менее 2%. Общий плазменный клиренс высокий (900 мл/мин) по сравнению с печеночным кровотоком (около 1500 мл/мин).
Фармакокинетика в особых клинических случаях
Наблюдается разница в плазменных концентрациях телмисартана у мужчин и женщин. Cmax и AUC были приблизительно в 3 и 2 раза, соответственно, выше у женщин по сравнению с мужчинами без значимого влияния на эффективность.
Фармакокинетика телмисартана у пациентов пожилого возраста не отличается от фармакокинетики у молодых пациентов.
Телмисартан связывается с белками плазмы крови и не удаляется при гемодиализе у пациентов с почечной недостаточностью. Также отмечаются более низкие концентрации телмисартана в плазме крови, Т1/2 не изменяется.
Исследования фармакокинетики, проводившиеся у пациентов с нарушениями функции печени, показали, что абсолютная биодоступность телмисартана увеличивается почти до 100%. T1/2 у пациентов с нарушениями функции печени не изменяется.
Амлодипин
Всасывание
После приема амлодипина внутрь в терапевтических дозах Cmax в плазме крови достигается через 6-12 ч. Величина абсолютной биодоступности составляет от 64% до 80%. Прием пищи не влияет на биодоступность амлодипина.
Распределение
Vd амлодипина составляет примерно 21 л/кг. В исследованиях in vitro показано, что у пациентов с артериальной гипертензией приблизительно 97.5% циркулирующего амлодипина связывается с белками плазмы крови. Устойчивые концентрации в плазме крови достигаются после постоянного применения препарата в течение 7-8 дней.
Метаболизм
Амлодипин в значительной степени (примерно на 90%) метаболизируется в печени с образованием неактивных метаболитов.
Выведение
Выведение амлодипина из плазмы крови происходит двухфазно. T1/2 составляет приблизительно 30-50 ч. Амлодипин выводится с мочой как в неизмененном виде (10%), так и в виде метаболитов (60%).
Фармакокинетика в особых клинических случаях
У пациентов пожилого возраста отмечается тенденция к снижению клиренса амлодипина, что приводит к увеличению AUC и T1/2.
Фармакокинетика амлодипина у пациентов с нарушениями функции почек существенно не изменяется.
У пациентов с печеночной недостаточностью клиренс амлодипина снижался, что приводило к увеличению значения AUC примерно на 40-60%.
Показания препарата
Твинста®
Для лечения артериальной гипертензии:
- у пациентов, АД которых недостаточно контролируется телмисартаном или амлодипином, применяемых в качестве монотерапии;
- у пациентов, которым показана комбинированная терапия;
- у пациентов, получающих телмисартан и амлодипин в виде отдельных таблеток, в качестве замены данной терапии.
Режим дозирования
Препарат Твинста® принимают внутрь 1 раз/сут, вне зависимости от приема пищи.
Препарат Твинста® можно назначать пациентам, получающим те же дозы телмисартана и амлодипина в виде отдельных таблеток, для удобства терапии и увеличения приверженности к лечению.
Препарат Твинста® можно назначать пациентам, у которых применение амлодипина или телмисартана в качестве монотерапии не приводит к адекватному контролю АД. Пациентов, принимающих амлодипин в дозе 10 мг, у которых отмечаются побочные реакции, ограничивающие применение препарата (например, периферические отеки), можно перевести на применение препарата Твинста® в дозе 40 мг/5 мг 1 раз/сут, что позволит уменьшить дозу амлодипина, но не снизит общий ожидаемый гипотензивный эффект.
Лечение артериальной гипертензии у пациента можно начинать с применения препарата Твинста® в том случае, когда предполагается, что достижение контроля АД с помощью какого-либо одного препарата маловероятно. Рекомендуемая начальная доза препарата Твинста® — 40 мг/5 мг 1 раз/сут. Пациенты, которым необходимо более значительное снижение АД, начальная доза препарата Твинста® может составлять 80 мг/5 мг 1 раз/сут.
Если, по крайней мере, через 2 недели лечения потребуется дополнительное снижение АД, дозу препарата можно постепенно увеличить до максимальной — 80 мг/10 мг 1 раз/сут.
Препарат Твинста® можно применять вместе с другими гипотензивными препаратами.
У пациентов с нарушениями функции почек, в т.ч. у пациентов, находящихся на гемодиализе, изменение дозы препарата не требуется. Амлодипин и телмисартан не удаляются из организма при проведении гемодиализа.
У пациентов с нарушениями функции печени легкой и умеренной степени препарат Твинста® следует применять с осторожностью. Доза телмисартана не должна превышать 40 мг 1 раз/сут.
У пациентов пожилого возраста режим дозирования не требует изменений.
Особенности действия лекарственного препарата при первом приеме или при его отмене
После приема первой дозы телмисартана гипотензивное действие развивается постепенно в течение первых 3 ч, сохраняется в течение 24 ч и остается значимым до 48 ч.
В случае резкой отмены телмисартана АД постепенно возвращается к исходному уровню без развития синдрома отмены.
Побочное действие
Внутри системно-органных классов частота возникновения побочных эффектов классифицируется следующим образом: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10 000, <1/1000); очень редко (<1/10 000); частота неизвестна (не может быть подсчитана по имеющимся данным).
Нежелательные побочные реакции классифицированы по органам и системам в соответствии с терминами MedDRA.
1 ожидающиеся на основании опыта применения телмисартана
2 ожидающиеся на основании опыта применения амлодипина
3 ожидающиеся при одновременном применении телмисартана и амлодипина
Дополнительная информация в отношении отдельных компонентов
Побочные эффекты, о которых ранее сообщалось при применении одного из компонентов препарата (амлодипина или телмисартана), могут усиливаться при применении препарата Твинста®, даже если они не наблюдались в клинических исследованиях или во время постмаркетингового периода.
Дополнительная информация в отношении комбинации компонентов
Периферические отеки, дозозависимый побочный эффект амлодипина, наблюдался реже у пациентов, которые получали комбинацию телмисартана и амлодипина, чем у пациентов, получавших только амлодипин.
Противопоказания к применению
- обструктивные заболевания желчевыводящих путей;
- тяжелая артериальная гипотензия;
- обструкция выходящего тракта левого желудочка (в т.ч. высокая степень аортального стеноза);
- гемодинамически нестабильная сердечная недостаточность после перенесенного острого инфаркта миокарда;
- печеночная недостаточность тяжелой степени;
- шок;
- одновременное применение с алискиреном у пациентов с сахарным диабетом или нарушением функции почек (СКФ менее 60 мл/мин/1.73 м2);
- непереносимость фруктозы и синдром нарушения всасывания глюкозы/галактозы или дефицит сахаразы/изомальтазы;
- беременность;
- период кормления грудью;
- возраст до 18 лет (эффективность и безопасность не установлены);
- повышенная чувствительность к активным компонентам или вспомогательным веществам;
- повышенная чувствительность к другим производным дигидропиридина.
С осторожностью следует назначать препарат при нарушении функции печени, реноваскулярной артериальной гипертензии, первичном альдостеронизме, стенозе аортального и митрального клапанов, гипертрофической обструктивной кардиомиопатии, сердечной недостаточности, сахарном диабете, нестабильной стенокардии, остром инфаркте миокарда, нарушении функции почек, состоянии после трансплантации почки, сниженном ОЦК и/или гипонатриемии, гиперкалиемии, других состояниях, характеризующихся активацией РААС.
Применение при беременности и кормлении грудью
Специальных исследований по применению препарата Твинста® при беременности и в период лактации не проводилось. Влияния, связанные с отдельными компонентами препарата, описаны ниже.
Беременность
Телмисартан
Применение антагонистов рецепторов ангиотензина II противопоказано при беременности. При наступлении беременности применение препарата следует немедленно прекратить. При необходимости следует назначить альтернативную терапию.
Доклинические исследования телмисартана не выявили тератогенных свойств, но установили наличие фетотоксичности.
Известно, что применение антагонистов рецепторов ангиотензина II во II и III триместрах беременности оказывает фетотоксичическое действие (снижение функции почек, олигогидрамнион, замедление оссификации черепа плода), а также наблюдается неонатальная токсичность (почечная недостаточность, артериальная гипотензия и гиперкалиемия).
У пациенток, планирующих беременность, следует заменить антагонисты рецепторов ангиотензина II на другие антигипертензивные препараты, которые имеют установленный профиль безопасности при применении у беременных женщин (если только продолжение лечения антагонистами рецепторов ангиотензина II не считается необходимым).
Если антагонисты рецепторов ангиотензина II применяются при беременности, то, начиная со II триместра беременности, рекомендуется проводить УЗИ почек и костей черепа плода. Новорожденных, матери которых получали антагонисты рецепторов ангиотензина II, следует тщательно наблюдать в отношении развития артериальной гипотензии.
Амлодипин
Имеющиеся ограниченные данные в отношении воздействия амлодипина или других блокаторов кальциевых каналов, не указывают на наличие отрицательного влияния на плод. Однако возможен риск замедления процесса родов.
Период кормления грудью
Специальных исследований о выделении телмисартана и/или амлодипина с грудным молоком у женщин не проводилось. В экспериментальных исследованиях на животных выявлено, что телмисартан выделяется с молоком лактирующих животных. Учитывая возможные неблагоприятные реакции, решение о продолжении кормления грудью или об отмене терапии должно приниматься с учетом ее значимости для матери.
Исследований влияния препарата на фертильность человека не проводилось.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени легкой и средней степени препарат Твинста® следует применять с осторожностью. Доза телмисартана не должна превышать 40 мг 1 раз/сут.
Применение при нарушениях функции почек
У пациентов с нарушениями функции почек, в т.ч. у пациентов, находящихся на гемодиализе, коррекция дозы препарата не требуется. Амлодипин и телмисартан не удаляются из организма при проведении гемодиализа.
С осторожностью следует назначать препарат при нарушениях функции почек, состоянии после трансплантации почки.
Применение у детей
Противопоказан в детском и подростковом возрасте до 18 лет (эффективность и безопасность не установлены).
Применение у пожилых пациентов
У пациентов пожилого возраста режим дозирования не требует изменений.
Особые указания
Во время лечения лекарственными препаратами, которые влияют на РААС, особенно при наличии нарушений функции почек и/или сердечной недостаточности, может возникать гиперкалиемия. У таких пациентов рекомендуется регулярный контроль содержания калия в сыворотке крови. Пациентам с нарушениями функции почек также рекомендуется периодический контроль концентрации креатинина в сыворотке крови. У некоторых пациентов, вследствие подавления РААС, особенно при применении комбинации средств, действующих на эту систему (например, добавление ингибитора АПФ или алискирена, прямого ингибитора ренина, к антагонистам рецепторов ангиотензина II), нарушается функция почек (включая острую почечную недостаточность). Терапия, сопровождающаяся подобной двойной блокадой РААС, не рекомендована и поэтому должна быть ограничена и проводиться строго индивидуально при тщательном контроле функции почек.
В случаях зависимости сосудистого тонуса и функции почек преимущественно от активности РААС (например, у пациентов с хронической сердечной недостаточностью или заболеваниями почек, в т.ч. при стенозе почечных артерий) назначение препаратов, влияющих на эту систему, может сопровождаться развитием острой артериальной гипотензии, гиперазотемии, олигурии, и, в редких случаях, острой почечной недостаточностью.
У пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной функционирующей почки, принимающих лекарственные препараты, влияющие на РААС, существует повышенный риск развития выраженной артериальной гипотензии и почечной недостаточности.
У пациентов с первичным альдостеронизмом антигипертензивные лекарственные препараты, механизм действия которых состоит в ингибировании РААС, как правило, не эффективны. Таким образом, применение телмисартана в таких случаях не рекомендуется.
У пациентов с аортальным или митральным стенозом, или при обструктивной гипертрофической кардиомиопатии применение препарата Твинста®, также как и других вазодилататоров, требует особой осторожности.
В клиническом исследовании установлено, что применение амлодипина у пациентов с сердечной недостаточностью неишемической этиологии III и IV функционального класса (по классификации NYHA) сопровождалось более частым развитием отека легких (несмотря на отсутствие существенных различий в частоте ухудшения сердечной недостаточности по сравнению с плацебо).
У пациентов с сахарным диабетом ИБС может протекать бессимптомно, вследствие чего может быть недиагностированной. Пациентам с сахарным диабетом необходимо пройти соответствующее обследование для диагностики и лечения ИБС (например, пробу с физической нагрузкой) перед началом лечения препаратом Твинста®. У пациентов с сахарным диабетом с сопутствующей ИБС вероятность фатального инфаркта миокарда и внезапной сердечно-сосудистой смерти может быть увеличена при лечении такими антигипертензивными средствами как антагонисты рецепторов ангиотензина II и ингибиторы АПФ.
Нет данных о применении препарата Твинста® у пациентов с нестабильной стенокардией, в остром периоде и в течение одного месяца после инфаркта миокарда.
Ограничение потребления поваренной соли, интенсивная терапия диуретиками, диарея или рвота может привести к снижению ОЦК и/или гипонатриемии, вследствие чего возможно развитие симптоматической артериальной гипотензии, особенно после приема первой дозы препарата. Перед применением препарата Твинста® такие состояния требуют коррекции.
Опыт применения препарата Твинста® у пациентов, которым была недавно проведена трансплантация почки, отсутствует. Амлодипин и телмисартан не удаляются при гемодиализе. Пациентам с нарушениями функции почек рекомендуется периодический контроль содержания калия и креатинина в сыворотке крови.
Рекомендации в отношении дозирования препарата у пациентов с нарушениями функции печени не разработаны, поэтому следует соблюдать осторожность.
Препарат Твинста® эффективен при лечении пациентов негроидной расы (в этой популяции обычно снижена активность ренина в крови).
Влияние на способность к управлению транспортными средствами и механизмами
Исследования влияния на способность к вождению автотранспорта и управлению механизмами не проводились. Однако следует принимать во внимание, что во время лечения могут отмечаться такие нежелательные эффекты, как обморок, сонливость или головокружение. Поэтому следует соблюдать осторожность или избегать выполнения таких потенциально опасных действий, как вождение автотранспорта или управление механизмами.
Передозировка
Случаи передозировки не выявлены. Возможные симптомы складываются из симптомов передозировки отдельных компонентов препарата.
Симптомы передозировки телмисартана: тахикардия, возможно брадикардия, головокружение, повышение концентрации креатинина в сыворотке крови, острая почечная недостаточность.
Симптомы передозировки амлодипина: чрезмерное снижение АД с возможным развитием рефлекторной тахикардии и симптомами чрезмерной периферической вазодилатации (риск развития выраженной и стойкой артериальной гипотензии, в т.ч. с развитием шока и летального исхода).
Лечение: проведение симптоматической и поддерживающей терапии, контроль состояния пациента. Могут применяться такие методы лечения как индукция рвоты, промывание желудка, применение активированного угля. В случае выраженного снижения АД пациента следует перевести в горизонтальное положение с низким изголовьем; рекомендовано введение плазмозамещающих растворов. С целью противодействия блокаде кальциевых каналов показано в/в введение глюконата кальция. Гемодиализ неэффективен.
Лекарственное взаимодействие
Взаимодействие между двумя активными компонентами, входящими в фиксированных дозах в состав данного препарата, в клинических исследованиях не выявлено.
Специальных исследований лекарственного взаимодействия препарата Твинста® с другими препаратами не проводилось.
Комбинация активных компонентов
При одновременном применении с другими гипотензивными препаратами антигипертензивное действие препарата Твинста® может усиливаться.
Можно ожидать, что некоторые препараты (например, баклофен и амифостин), благодаря своим фармакологическим свойствам, будут усиливать гипотензивное действие всех антигипертензивных средств, включая препарат Твинста®. Кроме того, ортостатическая гипотензия может усиливаться этанолом, барбитуратами, наркотическими средствами или антидепрессантами.
При одновременном применении с кортикостероидами (для системного применения) возможно снижение гипотензивного действия.
Основываясь на опыте применения других препаратов, влияющих на РААС, одновременное применение препарата Твинста® и калийсберегающих диуретиков, калийсодержащих добавок, калийсодержащей пищевой соли, других средств, повышающих содержание калия в крови (например, гепарина), может приводить к гиперкалиемии. Поэтому применение подобных комбинаций требует соблюдения осторожности и контроля содержания калия в крови.
Телмисартан
При одновременном применении с другими антигипертензивными препаратами возможно усиление гипотензивного эффекта. В одном исследовании при комбинированном применении телмисартана и рамиприла наблюдалось увеличение AUC0-24 и Cmax рамиприла и рамиприлата в 2.5 раза. Клиническая значимость этого взаимодействия не установлена.
Двойная блокада РААС (например, одновременное применение ингибитора АПФ или алискирена, прямого ингибитора ренина с антагонистами рецепторов ангиотензина II) не рекомендуется из-за возможного нарушения функции почек (включая острую почечную недостаточность).
Отмечалось обратимое увеличение концентрации лития в крови, сопровождающееся токсическими явлениями при применении одновременно с ингибиторами АПФ. В редких случаях подобные изменения зарегистрированы при назначении антагонистов рецептора ангиотензина II, в частности, телмисартана. При одновременном применении препаратов лития и антагонистов рецептора ангиотензина II рекомендуется проводить определение содержания лития в крови.
НПВС, включая ацетилсалициловую кислоту (в дозах, применяемых в качестве противовоспалительного средства), ингибиторы ЦОГ-2 и неселективные НПВС могут вызывать развитие острой почечной недостаточности у пациентов со сниженным ОЦК. Препараты, влияющие на активность РААС, в т.ч. телмисартан, могут обладать синергическим эффектом. У пациентов, получающих НПВС и телмисартан, в начале лечения следует компенсировать ОЦК и провести исследование функции почек.
При одновременном применении НПВС и антигипертензивных препаратов, подобных телмисартану, сообщалось об уменьшении антигипертензивного эффекта посредством ингибирования сосудорасширяющего эффекта простагландинов.
Не выявлено клинически значимого взаимодействия с дигоксином, варфарином, гидрохлоротиазидом, глибенкламидом, симвастатином, ибупрофеном, парацетамолом и амлодипином. Отмечено увеличение средней концентрации дигоксина в плазме крови в среднем на 20% (в одном случае на 39%). При одновременном применении телмисартана и дигоксина целесообразно проводить периодическое определение концентрации дигоксина в крови.
Амлодипин
Одновременное применение препарата Твинста® с грейпфрутом или грейпфрутовым соком не рекомендуется, т.к. у некоторых пациентов в результате повышения биодоступности амлодипина может усиливаться его антигипертензивное действие.
В исследовании у пациентов пожилого возраста было показано, что дилтиазем ингибирует метаболизм амлодипина, вероятно оказывая влияние на CYP3A4 (концентрации амлодипина в плазме крови увеличиваются примерно на 50% и усиливается эффект амлодипина). Нельзя исключить, что более активные ингибиторы CYP3A4 (такие как кетоконазол, итраконазол, ритонавир) могут увеличивать концентрации амлодипина в плазме крови в большей степени, чем дилтиазем.
Одновременное применение с индукторами изофермента CYP3A4 (противосудорожные препараты (например, карбамазепин, фенобарбитал, фенитоин, фосфенитоин, примидон), рифампицин, зверобой продырявленный (Hypericum perforatum)) может привести к снижению концентраций амлодипина в плазме крови. Показано регулярное медицинское наблюдение. Во время применения индукторов CYP3A4, а также после их отмены рекомендуется (по возможности) изменение дозы амлодипина.
Одновременное применение симвастатина в дозе 80 мг с амлодипином, вне зависимости от дозы, способствует увеличению экспозиции симвастатина до 77% по сравнению с монотерапией симвастатином. Поэтому доза симвастатина не должна превышать 20 мг/сут.
При одновременном применении амлодипин пожет повышать системную экспозицию циклоспорина или тасонермина. В таких случаях рекомендуется регулярный контроль концентрации циклоспорина или тасонермина в крови и коррекция дозы при необходимости.
Установлена безопасность одновременного применения амлодипина с тиазидными диуретиками, бета-адреноблокаторами, ингибиторами АПФ, нитратами длительного действия, нитроглицерином (применяемым сублингвально), НПВС, антибиотиками и гипогликемическими препаратами для приема внутрь.
При одновременном применении амлодипина и силденафила показано, что каждый препарат оказывал независимое антигипертензивное действие.
Дополнительная информация
Одновременное применение у 20 здоровых добровольцев 240 мл сока грейпфрута с однократной дозой амлодипина 10 мг, принимавшейся внутрь, не приводило к существенному влиянию на фармакокинетические свойства амлодипина.
Одновременное применение амлодипина с циметидином не оказывало существенного влияния на фармакокинетику амлодипина.
Одновременное применение амлодипина с аторвастатином, дигоксином или варфарином существенно не влияло на фармакокинетику или фармакодинамику этих препаратов.
Условия хранения препарата Твинста®
Препарат следует хранить в оригинальной упаковке, в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Твинста®
Срок годности — 3 года. Препарат нельзя применять по истечении срока годности.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
БЕРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНЕШНЛ ГМБХ
(Германия)
|
|
БЕРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНЕШНЛ ГмбХ ООО «Берингер Ингельхайм» |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Беременность. Применение АРА II не следует начинать во время беременности. За исключением тех случаев, когда продолжение лечения не считается необходимым, у пациенток, планирующих беременность, эти лекарственные препараты должны быть заменены на альтернативные антигипертензивные лекарственные препараты, которые имеют изученный профиль безопасности для использования во время беременности. Когда диагностируется беременность, лечение АРА II следует немедленно прекратить и при необходимости, начать альтернативное лечение.
Печеночная недостаточность. Телмисартан выводится преимущественно с желчью. Ожидается, что у пациентов с обструкцией желчевыводящих путей или печеночной недостаточностью клиренс лекарственного препарата снижается. Кроме того, как и у всех антагонистов кальция, T1/2 амлодипина у пациентов с нарушенной функцией печени увеличивается, а рекомендации по дозированию этого лекарственного препарата не установлены. В связи с этим комбинацию телмисартан + амлодипин у таких пациентов следует применять с осторожностью.
Реноваскулярная артериальная гипертензия. У пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной функционирующей почки, принимающих лекарственные препараты, влияющие на РААС, существует повышенный риск развития выраженной гипотензии и почечной недостаточности.
Нарушения функции почек и состояния после трансплантации почки. Опыт применения препарата Твинста® у пациентов, которым была недавно проведена трансплантация почки, отсутствует. Амлодипин и телмисартан не удаляются при гемодиализе. Пациентам с нарушениями функции почек рекомендуется периодический контроль содержания калия и креатинина в сыворотке крови.
Сниженный ОЦК и/или гипонатриемия. Вследствие ограничения потребления поваренной соли, интенсивной терапии диуретическими средствами, диареи или рвоты может развиваться симптоматическая артериальная гипотензия, особенно после приема первой дозы препарата. Перед применением препарата Твинста® такие состояния требуют коррекции. Если артериальная гипотония возникает на фоне применения препарата Твинста®, пациента необходимо положить на спину и если необходимо, назначить ему в/в введение физиологического раствора. Лечение может быть продолжено после стабилизации АД.
Двойная блокада РААС. Имеются данные, что одновременное применение ингибиторов АПФ, АРА II или алискирена увеличивает риск развития гипотонии, гиперкалиемии и снижения функции почек (включая острую почечную недостаточность). Поэтому двойная блокада РААС путем комбинированного применения ингибиторов АПФ, АРА II или алискирена не рекомендована.
Если лечение с двойной блокадой РААС считается необходимым, его следует проводить только под наблюдением специалиста и при условии тщательного контроля функции почек, концентрации электролитов и АД.
Ингибиторы АПФ и АРА II не должны применяться одновременно у пациентов с диабетической нефропатией.
Другие состояния, характеризующиеся активацией РААС. В случаях зависимости сосудистого тонуса и функции почек преимущественно от активности РААС (например, у пациентов с ХСН или заболеваниями почек, в т.ч. при стенозе почечных артерий) назначение препаратов, влияющих на эту систему, может сопровождаться развитием острой артериальной гипотензии, гиперазотемии, олигурии и в редких случаях — острой почечной недостаточности.
Первичный альдостеронизм. У пациентов с первичным альдостеронизмом гипотензивные лекарственные препараты, механизм действия которых состоит в ингибировании РААС, как правило, неэффективны. Таким образом, применение телмисартана в этиих случаях не рекомендуется.
Сахарный диабет. У пациентов с сахарным диабетом (СД) с дополнительным сердечно-сосудистым риском (т.е. с сопутствующей ИБС) риск развития фатального инфаркта миокарда и внезапной сердечно-сосудистой смерти могут быть увеличены при лечении гипотензивными средствами, такими как APA II и ингибиторами АПФ.
Стеноз аортального и митрального клапанов, гипертрофическая обструктивная кардиомиопатия. У пациентов с аортальным или митральным стенозом или с обструктивной гипертрофической кардиомиопатией применение препарата Твинста®, также как и других вазодилататоров, требует особой осторожности.
Нестабильная стенокардия, острый инфаркт миокарда. Нет данных о применении препарата Твинста® у пациентов с нестабильной стенокардией, в остром периоде и в течение 1 мес после инфаркта миокарда.
Сердечная недостаточность. В клиническом исследовании установлено, что применение амлодипина у пациентов с сердечной недостаточностью неишемической этиологии III и IV функционального класса по классификации NYHA сопровождалось более частым развитием отека легких (несмотря на отсутствие существенного различия в частоте ухудшения сердечной недостаточности по сравнению с плацебо).
Пациенты с сахарным диабетом, получающие инсулин или другие сахароснижающие лекарственные препараты. У данных пациентов гипогликемия может возникнуть при лечении телмисартаном. Поэтому у таких пациентов следует рассмотреть возможность проведения надлежащего мониторинга концентрации глюкозы в крови; может потребоваться коррекция дозы инсулина или сахароснижающих лекарственных препаратов, если это необходимо.
Гиперкалиемия. Во время лечения лекарственными препаратами, которые влияют на РААС, особенно при наличии нарушений функции почек и/или сердечной недостаточности, может возникать гиперкалиемия. Гиперкалиемия может быть фатальной у пожилых пациентов, пациентов с почечной недостаточностью, пациентов с СД, пациентов, которые одновременно получают другие лекарственные препараты, способные повышать концентрацию калия в сыворотке крови, и/или пациентов с интеркуррентными событиями.
Прежде чем рассматривать возможность совместного применения лекарственных препаратов, которые влияют на РААС, необходимо оценить соотношение польза-риск.
Основными факторами риска развития гиперкалиемии являются:
— СД, нарушение функции почек, возраст (>70 лет);
— комбинация с одним или несколькими другими лекарственными препаратами, которые влияют на РААС, и/или пищевыми добавками, содержащими калий. Лекарственные препараты или терапевтические классы лекарственных препаратов, которые могут спровоцировать развитие гиперкалиемии, представляют собой соли, содержащие калий, калийсберегающие диуретики, ингибиторы АПФ, АРА II, НПВП (включая селективные ингибиторы ЦОГ-2), гепарин, иммунодепрессанты (циклоспорин или такролимус) и триметоприм;
— интеркуррентные события, в частности дегидратация, острая декомпенсация сердечной деятельности, метаболический ацидоз, ухудшение функции почек, внезапное ухудшение состояния почек (например, инфекционные заболевания), клеточный лизис (например, ишемия конечности, рабдомиолиз, обширная травма).
У данных пациентов следует тщательно контролировать концентрацию калия в сыворотке крови.
Сорбитол. Каждая таблетка препарата Твинста® содержит 168,64 мг сорбитола.
Прочее. Чрезмерное снижение АД у пациентов с ишемической кардиомиопатией или ишемическим сердечно-сосудистым заболеванием может привести к развитию инфаркта миокарда или инсульта.
Препарат Твинста® эффективен при лечении пациентов негроидной расы (в этой популяции обычно снижена активность ренина в крови).
Влияние на способность к управлению транспортными средствами и механизмами. Исследования влияния на способность к управлению транспортными средствами и управлению механизмами не проводились. Однако следует принимать во внимание, что во время лечения могут отмечаться такие нежелательные реакции, как обморок, сонливость или головокружение. Поэтому во время управления транспортными средствами или механизмами следует соблюдать осторожность. Если пациенты испытывают эти ощущения, им следует избегать выполнения таких потенциально опасных действий, как вождение автотранспорта или управление механизмами.
Твинста — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-002012
Торговое наименование:
Твинста
Группировочное наименование:
амлодипин + телмисартан
Лекарственная форма:
таблетки
Состав:
1 таблетка содержит:
5 мг + 40 мг
Действующие вещества:
амлодипина безилат* 6,935 мг
телмисартан 40,000 мг
*эквивалентно 5,000 мг амлодипина
Вспомогательные вещества:
слой телмисартана: натрия гидроксид 3,360 мг; повидон К25 12,000 мг; меглюмин 12,000 мг; сорбитол 168,640 мг; магния стеарат 4,000 мг;
слой амлодипина: целлюлоза микрокристаллическая 125,765 мг; крахмал прежелатинизированный 53,000 мг; крахмал кукурузный 10,000 мг; кремния диоксид коллоидный 2,000 мг; магния стеарат 2,000 мг; смесь красителей 0,300 мг**.
10 мг + 40 мг
Действующие вещества:
амлодипина безилат* 13,870 мг
телмисартан 40,000 мг
*эквивалентно 10,000 мг амлодипина
Вспомогательные вещества:
слой телмисартана: натрия гидроксид 3,360 мг; повидон К25 12,000 мг; меглюмин 12,000 мг; сорбитол 168,640 мг; магния стеарат 4,000 мг;
слой амлодипина: целлюлоза микрокристаллическая 118,830 мг; крахмал прежелатинизированный 53,000 мг; крахмал кукурузный 10,000 мг; кремния диоксид коллоидный 2,000 мг; магния стеарат 2,000 мг; смесь красителей 0,300 мг**.
5 мг + 80 мг
Действующие вещества:
амлодипина безилат* 6,935 мг
телмисартан 80,000 мг
*эквивалентно 5,000 мг амлодипина
Вспомогательные вещества:
слой телмисартана: натрия гидроксид 6,720 мг; повидон К25 24,000 мг; меглюмин 24,000 мг; сорбитол 337,280 мг; магния стеарат 8,000 мг;
слой амлодипина: целлюлоза микрокристаллическая 125,765 мг; крахмал прежелатинизированный 53,000 мг; крахмал кукурузный 10,000 мг; кремния диоксид коллоидный 2,000 мг; магния стеарат 2,000 мг; смесь красителей 0,300 мг**.
10 мг + 80 мг
Действующие вещества:
амлодипина безилат* 13,870 мг
телмисартан 80,000 мг
*эквивалентно 10,000 мг амлодипина
Вспомогательные вещества:
слой телмисартана: натрия гидроксид 6,720 мг; повидон К25 24,000 мг; меглюмин 24,000 мг; сорбитол 337,280 мг; магния стеарат 8,000 мг;
слой амлодипина: целлюлоза микрокристаллическая 118,830 мг; крахмал прежелатинизированный 53,000 мг; крахмал кукурузный 10,000 мг; кремния диоксид коллоидный 2,000 мг; магния стеарат 2,000 мг; смесь красителей 0,300 мг**.
** Смесь красителей состоит из 76% железа оксида черного (E172, наименование в НФ: железа оксид), 4 % железа оксида желтого (E172, наименование в НФ: железа оксид) и 20% FD&C синего №1 (бриллиантового голубого FCF алюминиевого лака) (E133).
Описание
Овальной формы, двояковыпуклые, двухслойные таблетки без оболочки. Один слой от белого до почти белого цвета, другой слой серо-голубого цвета. На белой поверхности таблеток имеется логотип фирмы и гравировка «А1» (для дозировки 5 мг + 40 мг), «А2» (для дозировки 10 мг + 40 мг), «А3» (для дозировки 5 мг + 80 мг), «А4» (для дозировки 10 мг + 80 мг), другая сторона таблетки гладкая.
Фармакотерапевтическая группа:
гипотензивное средство комбинированное (блокатор «медленных» кальциевых каналов + ангиотензина II рецепторов антагонист)
Код АТХ:
C09DB04
Фармакологические свойства
Фармакодинамика
Твинста представляет собой комбинированный препарат, содержащий два гипотензивных вещества со взаимодополняющим действием, позволяющими контролировать артериальное давление у пациентов с артериальной (эссенциальной) гипертензией: антагонист рецепторов ангиотензина II (АРА II), телмисартан, и блокатор «медленных» кальциевых каналов (БМКК), производное дигидропиридина, амлодипин.
Комбинация этих веществ обладает аддитивным гипотензивным действием, снижая артериальное давление в большей степени, чем каждый отдельный компонент.
Препарат Твинста, принимаемый 1 раз в сутки, приводит к эффективному и устойчивому снижению артериального давления в течение 24 часов.
Телмисартан
Телмисартан — специфический АРА II (тип AT 1), эффективный при приеме внутрь. Обладает высоким сродством к подтипу AT 1 рецепторов ангиотензина II, через которые реализуется действие ангиотензина II. Вытесняет ангиотензин II из связи с рецептором, не обладая действием агониста в отношении этого рецептора. Телмисартан связывается только с подтипом AT 1 рецепторов ангиотензина II. Связь носит длительный характер. Не обладает сродством к другим рецепторам, в том числе к АТ 2 рецептору. Снижает концентрацию альдостерона в крови, не ингибирует ренин в плазме крови и не блокирует ионные каналы. Телмисартан не ингибирует ангиотензинпревращающий фермент (кининаза II — фермент, который также разрушает брадикинин). Поэтому усиление вызываемых брадикинином нежелательных эффектов не ожидается.
У пациентов телмисартан в дозе 80 мг полностью блокирует гипертензивное действие ангиотензина II. Начало гипотензивного действия отмечается в течение 3-х часов после первого приема телмисартана. Действие препарата сохраняется в течение 24 часов и остается значимым до 48 часов. Выраженное гипотензивное действие обычно развивается через 4-8 недель после регулярного приема.
У пациентов с артериальной гипертензией телмисартан снижает систолическое и диастолическое артериальное давление (АД), не оказывая влияния на частоту сердечных сокращений (ЧСС).
В случае резкой отмены телмисартана АД постепенно возвращается к исходному уровню без развития синдрома “отмены”.
Частота развития сухого кашля была значительно ниже у пациентов, получавших телмисартан в сравнении с применением ингибиторов ангиотензинпревращающего фермента (АПФ).
В ходе двух крупных рандомизированных контролируемых исследований ONTARGET (Исследование глобальных конечных точек при применении телмисартана в рамках монотерапии и в сочетании с рамиприлом) и VA NEPHRON-D (The Veterans Affairs Nephropathy in diabetes — исследование нефропатии при диабете, проводимое департаментом США по делам ветеранов) изучалось применение комбинации ингибитора АПФ в сочетании с антагонистом рецепторов ангиотензина II. Исследование ONTARGET представляло собой исследование, проведенное у пациентов, имеющих в анамнезе сердечно-сосудистые или цереброваскулярные заболевания или сахарный диабет 2 типа с подтверждением поражением органов-мишеней. Исследование VA NEPHRON-D представляло собой исследование у пациентов с сахарным диабетом 2 типа и диабетической нефропатией.
Эти исследования не показали значительного положительного влияния на почечные и/или сердечно-сосудистые исходы и смертность, тогда как наблюдался повышенный риск развития гиперкалиемии, острой почечной недостаточности и/или артериальной гипотонии по сравнению с монотерапией. Учитывая сходные фармакодинамические свойства, эти результаты также актуальны для других ингибиторов АПФ и антагонистов рецепторов ангиотензина II.
Поэтому ингибиторы АПФ и антагонисты рецепторов ангиотензина II не должны применяться совместно у пациентов с диабетической нефропатией.
Исследование ALTITUDE (Исследование применения алискирена у пациентов с сахарным диабетом 2 типа с оценкой сердечно-сосудистых и почечных конечных точек) представляло собой исследование, целью которого являлась проверка преимущества добавления алискирена к стандартному лечению ингибитором АПФ или антагонистом рецепторов ангиотензина II у пациентов с сахарным диабетом 2 типа и хроническим заболеванием почек, сердечно-сосудистым заболеванием или и тем, и другим. Исследование было прекращено досрочно в связи с повышенным риском неблагоприятных исходов. Сердечно-сосудистая смерть и инсульт более часто регистрировались в группе алискирена, чем в группе плацебо, а нежелательные явления и серьезные нежелательные явления (гиперкалиемия, артериальная гипотония и нарушение функции почек) чаще отмечались в группе алискирена, чем в группе плацебо.
Наблюдается разница в плазменных концентрациях телмисартана у мужчин и женщин. Сmах и AUC были приблизительно в 3 и 2 раза, соответственно, выше у женщин по сравнению с мужчинами без значимого влияния на эффективность.
Амлодипин
Амлодипин — производное дигидропиридина, относится к классу БМКК. Он ингибирует трансмембранное поступление ионов кальция в кардиомиоциты и гладкомышечные клетки сосудов.
Механизм гипотензивного действия амлодипина связан с прямым релаксирующим эффектом на гладкомышечные клетки сосудов, что приводит к уменьшению периферического сосудистого сопротивления и снижению АД.
У пациентов с артериальной гипертензией применение амлодипина 1 раз в сутки обеспечивает клинически значимое снижение АД на протяжении 24 часов. Ортостатическая артериальная гипотензия не характерна во время применения амлодипина вследствие медленного начала действия препарата.
У пациентов с артериальной гипертензией и нормальной функцией почек амлодипин в терапевтических дозах приводил к уменьшению сопротивления сосудов почек, повышению скорости клубочковой фильтрации и эффективного кровотока плазмы в почках без изменения фильтрации или протеинурии.
Амлодипин не приводит к каким-либо метаболическим неблагоприятным эффектам или изменениям концентрации липидов в плазме крови и поэтому подходит для применения у пациентов с бронхиальной астмой, сахарным диабетом и подагрой.
Применение амлодипина у пациентов с сердечной недостаточностью не сопровождается отрицательным инотропным действием (не снижается толерантность к физической нагрузке, не снижается фракция выброса левого желудочка).
Фармакокинетика
Фармакокинетика комбинации фиксированных доз
Скорость и степень всасывания препарата Твинста эквивалентны биодоступности телмисартана и амлодипина в случае их применения в виде отдельных таблеток.
Фармакокинетика отдельных компонентов:
Телмисартан
Всасывание
При приеме внутрь быстро всасывается из желудочно-кишечного тракта. Абсолютная биодоступность телмисартана составляет около 50%. При приеме одновременно с пищей снижение площади под кривой «концентрация-время» (AUC) колеблется от 6% (при дозе 40 мг) до 19% (при дозе 160 мг). Через 3 часа после приема внутрь концентрация в плазме крови становится аналогичной концентрации при приеме телмисартана натощак.
Распределение
Связь с белками плазмы крови > 99,5%, в основном с альбумином и альфа-1 гликопротеином. Среднее значение видимого объема распределения в равновесной концентрации — 500 л.
Метаболизм
Метаболизируется телмисартан путем конъюгирования с глюкуроновой кислотой. Метаболиты фармакологически неактивны.
Выведение
Период полувыведения (Т V) составляет более 20 часов. Максимальная концентрация в плазме крови (Cmax) и в меньшей степени AUC увеличиваются непропорционально величине дозы. Данных о клинически значимом накоплении телмисартана, при применении его в рекомендуемых дозах, нет.
Выводится через кишечник в неизмененном виде, выведение почками — менее 1%. Общий плазменный клиренс высокий (приблизительно 1000 мл/мин) по сравнению с «печеночным» кровотоком (около 1500 мл/мин).
Амлодипин
Всасывание
После приема амлодипина внутрь в терапевтических дозах максимальные концентрации в плазме крови достигаются через 6-12 часов. Величина абсолютной биодоступности составляет от 64% до 80%. Прием пищи не влияет на биодоступность амлодипина.
Распределение
Объем распределения амлодипина составляет примерно 21 л/кг. В исследованиях in vitro показано, что у пациентов с артериальной гипертензией приблизительно 97,5% циркулирующего амлодипина связывается с белками плазмы крови.
Метаболизм
Амлодипин в значительной степени (примерно на 90%) метаболизируется в печени с образованием неактивных метаболитов.
Выведение
Выведение амлодипина из плазмы крови происходит двухфазно, ТА составляет приблизительно 30-50 часов. Стабильная концентрация в плазме крови достигается после постоянного приема препарата в течение 7-8 дней. Амлодипин выводится почками как в неизмененном виде (10%), так и в виде метаболитов (60%).
Фармакокинетика в особых клинических случаях:
У пациентов пожилого возраста
Фармакокинетика телмисартана у пациентов пожилого возраста не отличается от молодых пациентов. У пациентов пожилого возраста отмечается тенденция к снижению клиренса амлодипина, что приводит к увеличению AUC и ТА.
Пациенты с почечной недостаточностью
Телмисартан связывается с белками плазмы крови и не удаляется при гемодиализе у пациентов с почечной недостаточностью. У пациентов с почечной недостаточностью концентрация телмисартана в плазме крови повышается вдвое. Однако у пациентов, находящихся на гемодиализе, отмечаются более низкие концентрации телмисартана, Т1/2 не изменяется. Фармакокинетика амлодипина у пациентов с нарушениями функции почек существенно не изменяется.
Пациенты с печеночной недостаточностью
Исследования фармакокинетики, проводившиеся у пациентов с нарушениями функции печени, показали, что абсолютная биодоступность телмисартана увеличивается почти до 100%. ТА у пациентов с нарушениями функции печени не изменяется. У пациентов с печеночной недостаточностью клиренс амлодипина снижался, что приводило к увеличению значения AUC примерно на 40-60%.
Показания к применению
Артериальная гипертензия (для пациентов, АД которых недостаточно контролируется телмисартаном или амлодипином в монотерапии).
Артериальная гипертензия (для пациентов, которым показана комбинированная терапия).
Пациентам с артериальной гипертензией, получающим телмисартан и амлодипин в виде отдельных таблеток в качестве замены данной терапии.
Противопоказания
- Гиперчувствительность к телмисартану или амлодипину, производным дигидропиридина или любому из вспомогательных веществ препарата;
- Беременность;
- Период грудного вскармливания;
- Обструктивные заболевания желчевыводящих путей;
- Тяжелая артериальная гипотензия (систолическое АД менее 90 мм рт.ст.);
- Обструкция выносящего тракта левого желудочка (включая аортальный стеноз тяжелой степени);
- Гемодинамически нестабильная сердечная недостаточность после перенесенного острого инфаркта миокарда;
- Печеночная недостаточность тяжелой степени (класс С по шкале Чайлд-Пью);
- Шок (включая кардиогенный шок);
- Одновременное применение с алискиреном у пациентов с сахарным диабетом или почечной недостаточностью (СКФ менее 60 мл/мин/1,73 м2);
- Непереносимость фруктозы (из-за наличия в составе препарата сорбитола);
- Возраст до 18 лет (эффективность и безопасность не установлены).
С осторожностью
Применение препарата требует тщательного врачебного наблюдения при наличии следующих состояний/заболеваний/факторов риска:
- Хроническая сердечная недостаточность неишемической этиологии (III-IV функциональный класс по классификации NYHA);
- Ишемическая болезнь сердца с тяжелым обструктивным поражением коронарных артерий;
- Острый инфаркт миокарда (и период в течение 1 месяца после него);
- Нестабильная стенокардия;
- Аортальный стеноз, митральный стеноз, гипертрофическая обструктивная кардиомиопатия;
- Артериальная гипотензия;
- Синдром слабости синусового узла (выраженная тахикардия, брадикардия);
- Одновременное применение с ингибиторами или индукторами изофермента CYP3A4;
- Двусторонний стеноз почечных артерий или стеноз артерий единственной почки;
- Почечная или печеночная недостаточность легкой и средней степени тяжести;
- Состояния после трансплантации почки (в связи с отсутствием опыта применения);
- Снижение объема циркулирующей крови (ОЦК) вследствие предшествующей диуретической терапии, ограничения приема поваренной соли, диареи или рвоты;
- Гипонатриемия, гиперкалиемия.
Применение при беременности и в период грудного вскармливания
Специальных исследований препарата Твинста во время беременности и в период грудного вскармливания не проводилось. Влияния, связанные с отдельными компонентами препарата, описаны ниже.
Беременность
Телмисартан
Применение АРА II противопоказано во время беременности. При диагностировании беременности прием препарата следует немедленно прекратить. При необходимости должна назначаться альтернативная терапия.
Доклинические исследования телмисартана не выявили тератогенных свойств, но установили наличие фетотоксичности.
Известно, что применение АРА II в течение второго и третьего триместров беременности оказывает фетотоксическое действие (снижение функции почек, олигогидрамнион, замедление оссификации черепа плода), а также наблюдается неонатальная токсичность (почечная недостаточность, артериальная гипотензия и гиперкалиемия).
У пациенток, планирующих беременность, АРА II должны заменяться на другие гипотензивные средства, которые характеризуются установленным профилем безопасности при применении во время беременности (если только продолжение лечения АРА II не считается необходимым).
Если АРА II применяются во время беременности, то, начиная со второго триместра беременности, рекомендуется УЗИ контроль функции почек и состояния черепа. Новорожденные, матери которых получали АРА II, должны тщательно наблюдаться в отношении развития артериальной гипотензии.
Амлодипин
Имеющиеся ограниченные данные в отношении воздействия амлодипина или других БМКК не указывают на наличие отрицательных влияний на плод. Однако возможен риск замедления процесса родов.
Период грудного вскармливания
Амлодипин экскретируется в грудное молоко. Доля дозы, полученной младенцем, оценивалась в диапазоне от 3 до 7 %, с максимумом 15%. Влияние амлодипина на детей, находящихся на грудном вскармливании, неизвестно.
Специальных исследований о выделении телмисартана с грудным молоком у женщин не проводилось. В исследованиях на животных выявлено, что телмисартан выделяется с молоком лактирующих животных. Учитывая возможные неблагоприятные реакции, решение о продолжении грудного вскармливания или об отмене терапии должно приниматься с учетом ее значимости для матери. Исследований влияния на фертильность человека не проводилось.
Способ применения и дозы
Препарат Твинста необходимо принимать 1 раз в сутки.
Внутрь, вне зависимости от приема пищи.
- Препарат Твинста может назначаться пациентам, получающим те же дозы телмисартана и амлодипина в виде отдельных таблеток, для удобства терапии и увеличения приверженности лечению.
- Препарат Твинста может назначаться пациентам, у которых применение одного амлодипина или одного телмисартана не приводит к адекватному контролю АД.
Пациенты, принимающие амлодипин в дозе 10 мг, у которых отмечаются нежелательные реакции, ограничивающие прием препарата, например, периферические отеки, могут перейти на прием препарата Твинста в дозе 5 мг + 40 мг 1 раз в сутки, что позволит уменьшить дозу амлодипина, но не снизит общее ожидаемое гипотензивное действие. - Лечение артериальной гипертензии у пациента может начинаться с применения препарата Твинста в том случае, когда предполагается, что достижение контроля артериального давления с помощью какого-либо одного препарата маловероятно. Обычная начальная доза препарата Твинста — 5 мг + 40 мг 1 раз в сутки. Пациенты, которым необходимо более значительное снижение артериального давления, могут начинать прием препарата Твинста в дозе 5 мг + 80 мг 1 раз в сутки.
Если, по крайней мере, через 2 недели лечения потребуется дополнительное снижение артериального давления, доза препарата может быть постепенно увеличена до максимальной дозы 10 мг + 80 мг 1 раз в сутки.
Препарат Твинста может применяться вместе с другими гипотензивными препаратами.
Применение препарата в особых клинических группах пациентов
Нарушения функции почек
У пациентов с нарушениями функции почек, в том числе у пациентов, находящихся на гемодиализе, изменений режима дозирования препарата не требуется. Амлодипин и телмисартан не удаляются из организма при проведении гемодиализа.
Нарушения функции печени
У пациентов с печеночной недостаточностью легкой и средней степени препарат Твинста должен применяться с осторожностью. Доза телмисартана не должна превышать 40 мг 1 раз в сутки.
Пожилые пациенты
Режим дозирования не требует коррекции.
Дети и подростки в возрасте до 18 лет
Данные по эффективности и безопасности комбинации амлодипин/телмисартан у детей и подростков младше 18 лет отсутствуют.
Побочное действие
Наиболее распространенные нежелательные реакции включают головокружение и периферические отеки. Серьезный обморок может возникнуть в редких случаях (менее 1 случая на 1000 пациентов).
Нежелательные реакции, ранее описанные при применении одного из компонентов (телмисартана или амлодипина), могут также быть потенциальными побочными реакциями при применении препарата Твинста, даже если они не наблюдались в ходе клинических исследований или во время пострегистрационного периода.
Внутри системно-органных классов по частоте возникновения нежелательных реакций используются следующие категории: очень часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); редко (≥ 1/10000, < 1/1000); очень редко (< 1/10000); частота неизвестна (не может быть подсчитана по имеющимся данным).
1) ожидающиеся на основании опыта применения телмисартана
2) ожидающиеся на основании опыта применения амлодипина
3) ожидающиеся при одновременном применении телмисартана и амлодипина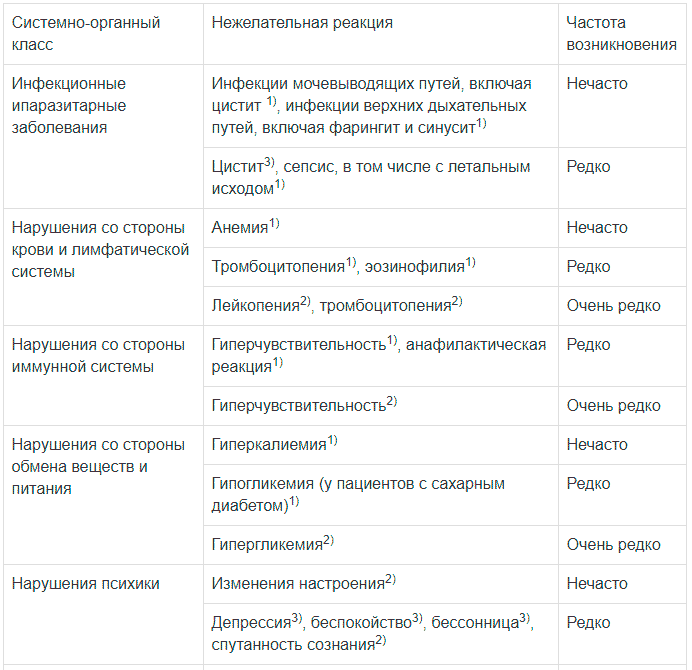
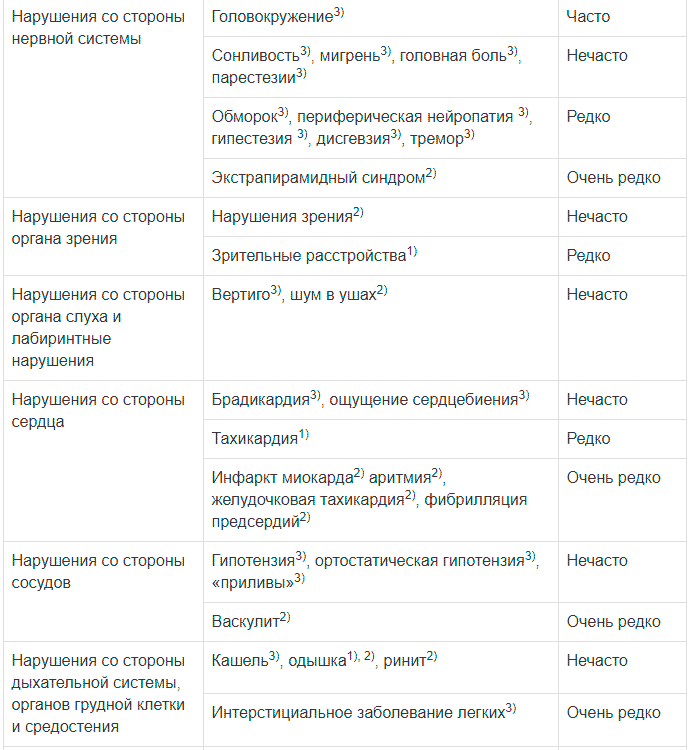
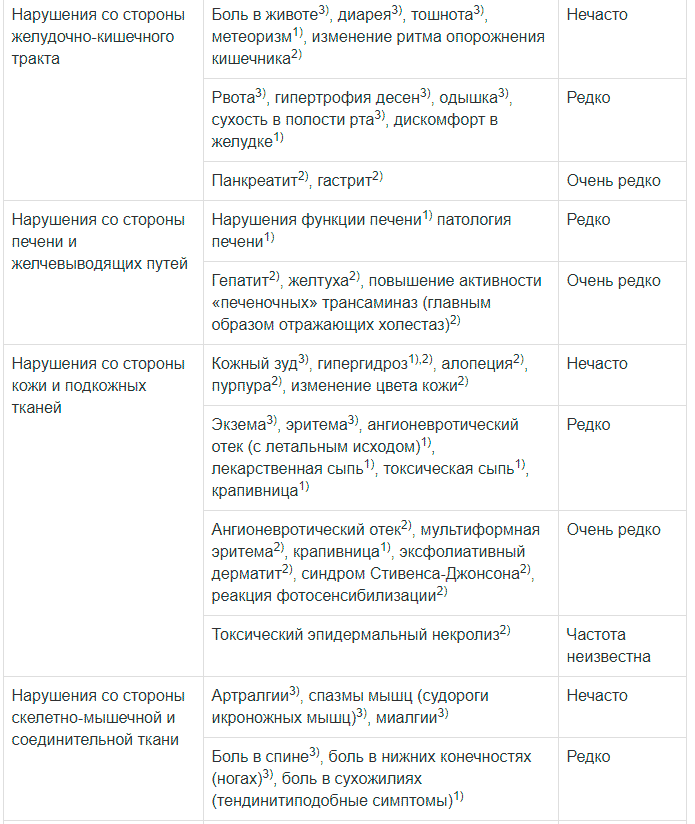
Дополнительная информация в отношении отдельных компонентов
Нежелательные реакции, ранее сообщавшиеся при применении одного из компонентов препарата (амлодипина или телмисартана), могут усиливаться при применении препарата Твинста, даже если они не наблюдались в клинических исследованиях или во время постмаркетингового периода.
Дополнительная информация в отношении комбинации компонентов
Периферические отеки, дозозависимая нежелательная реакция на амлодипин, наблюдались у пациентов, которые получали комбинацию телмисартана и амлодипина, реже, чем у пациентов, получавших только амлодипин.
Передозировка
Симптомы
Случаи передозировки не выявлены. Возможные симптомы передозировки складываются из симптомов со стороны отдельных компонентов препарата. Телмисартан — тахикардия, возможно брадикардия, головокружение, повышение концентрации креатинина в сыворотке крови, острая почечная недостаточность. Амлодипин — выраженное снижение АД с возможным развитием рефлекторной тахикардии и симптомами чрезмерной периферической вазодилатации (риск развития выраженной и стойкой артериальной гипотензии, в т.ч. с развитием шока и летального исхода).
Лечение
Гемодиализ не эффективен. Контроль за состоянием больного, терапия должна быть симптоматической и поддерживающей.
С целью купирования блокады кальциевых каналов возможно внутривенное струйное введение глюконата кальция.
Могут применяться методы лечения передозировки, такие как индукция рвоты, промывание желудка, применение активированного угля, перевод пациента в положение «с приподнятыми ногами» и введение плазмозамещающих растворов в случае выраженного снижения АД.
Взаимодействие с другими лекарственными средствами
Взаимодействий между амлодипином и телмисартаном в клинических исследованиях не выявлено.
Специальных исследований лекарственных взаимодействий препарата Твинста с другими препаратами не проводилось.
Комбинация действующих веществ
Другие гипотензивные средства
При одновременном применении с другими гипотензивными препаратами гипотензивное действие препарата Твинста может усиливаться.
Препараты, способные снижать артериальное давление
Можно ожидать, что некоторые препараты, например, баклофен, амифостин, нейролептики и антидепрессанты благодаря своим фармакологическим свойствам, будут усиливать гипотензивное действие всех гипотензивных средств, включая препарат Твинста. Кроме того, ортостатическая артериальная гипотензия может усиливаться этанолом.
Кортикостероиды (системное применение)
Возможно снижение гипотензивного действия.
Телмисартан
Совместное применение не рекомендовано
Калийсберегающие диуретики или препараты калия
Антагонисты рецепторов ангиотензина II, такие как телмисартан, снижают потери калия, вызванные применением диуретиков. Применение калийсберегающих диуретиков, например, спиринолактона, эплеренона, триамтерена или амилорида, препаратов калия или калийсодержащей соли может привести к значительному увеличению концентрации калия в сыворотке крови. Если сопутствующее применение показано в связи с документированной гипокалиемией, эти лекарственные препараты следует применять с осторожностью и с частым контролем сывороточного содержания калия.
Препараты лития
Отмечалось обратимое увеличение концентрации лития в крови, сопровождающееся токсическими явлениями, при приеме ингибиторов АПФ. В редких случаях подобные изменения зарегистрированы при назначении антагонистов рецептора ангиотензина II, в частности, телмисартана. При одновременном назначении препаратов лития и антагонистов рецептора ангиотензина II рекомендуется проводить определение содержания лития в крови.
Другие гипотензивные средства
Возможно усиление гипотензивного действия. В одном исследовании при комбинированном применении телмисартана и рамиприла наблюдалось повышение AUC0-24 и С mах рамиприла и рамиприлата в 2,5 раза. Клиническая значимость этого взаимодействия не установлена.
Двойная блокада РААС (например, совместное применение иАПФ или алискирена, прямого ингибитора ренина с АРА II) не рекомендуется из-за возможного нарушения функции почек (включая острую почечную недостаточность).
Совместное применение, требующее соблюдения мер предосторожности
Нестероидные противовоспалительные препараты (НПВП), включая ацетилсалициловую кислоту (в дозах, применяемых в качестве противовоспалительного средства), ингибиторы циклооксигеназы-2 (ЦОГ-2) и неселективные НПВП, могут снизить выраженность гипотензивного эффекта антагонистов рецепторов ангиотензина II.
У некоторых пациентов с почечной недостаточностью (например, пациенты с обезвоживанием или пожилые пациенты с почечной недостаточностью) совместное применение антагонистов рецепторов ангиотензина II и лекарственных препаратов, которые подавляют активность ЦОГ, может привести к дополнительному ухудшению функции почек, включая возможное развитие острой почечной недостаточности; эти эффекты, как правило, обратимы. Поэтому данную комбинацию следует применять с осторожностью, особенно у пожилых людей. Пациенты должны быть адекватно гидратированы, при этом следует контролировать функцию почек после начала совместного применения данных лекарственных препаратов и периодически после этого.
Рамиприл
В одном исследовании совместное применение телмисартана и рамиприла привело к увеличению значений AUC0-24 и Cmax рамиприла и рамиприлата в 2,5 раза. Клиническая значимость этого наблюдения неизвестна.
Совместное применение, которое следует принимать во внимание
Дигоксин
При совместном применении телмисартана с дигоксином, наблюдалось увеличение медианы максимальной концентрации дигоксина в плазме крови (49%) и остаточной концентрации дигоксина (20%). При инициировании, коррекции доз и отмене телмисартана следует контролировать концентрации дигоксина в плазме крови, чтобы поддерживать их в терапевтическом диапазоне.
Амлодипин
Совместное применение, требующее соблюдения мер предосторожности
Ингибиторы изофермента CYP3A4
При совместном применении с ингибитором CYP3A4 эритромицином у молодых пациентов и с дилтиаземом у пожилых пациентов концентрация амлодипина в плазме крови возрастала на 22% и 50%, соответственно. Однако клиническая значимость этого наблюдения неясна.
Нельзя исключить, что более активные ингибиторы изофермента CYP3A4 (такие как кетоконазол, итраконазол, ритонавир) могут увеличивать концентрации амлодипина в плазме крови в большей степени, чем дилтиазем. Амлодипин следует применять с осторожностью совместно с ингибиторами изофермента CYP3A4. Однако никаких нежелательных эффектов, связанных с таким взаимодействием, отмечено не было.
Индукторы изофермента CYP3A4
При совместном применении известных индукторов CYP3A4 концентрация амлодипина в плазме может варьировать. Таким образом, необходимо контролировать артериальное давление и регулировать дозу во время и после сопутствующего лечения, особенно с сильными индукторами CYP3A4 (например, рифампицин, препараты зверобоя продырявленного (Hypericum perforatum)).
Грейпфрут и грейпфрутовый сок
Одновременное применение у 20 здоровых добровольцев 240 мл сока грейпфрута с однократной дозой амлодипина 10 мг, принимавшейся внутрь, не приводило к существенному влиянию на фармакокинетические свойства амлодипина. Одновременное применение препарата Твинста с грейпфрутом или грейпфрутовым соком не рекомендуется, так как у некоторых пациентов в результате повышения биодоступности амлодипина может усиливаться антигипертензивное действие.
Совместное применение, которое следует принимать во внимание
Такролимус
Существует риск повышения концентраций такролимуса при его совместном применении с амлодипином, но фармакокинетический механизм этого взаимодействия до конца не изучен. Во избежание токсичности такролимуса применение амлодипина у пациентов, получающих такролимус, требует мониторинга концентраций такролимуса и коррекции дозы такролимуса, когда это необходимо.
Циклоспорин
Не проводились исследования лекарственных взаимодействий циклоспорина и амлодипина у здоровых добровольцев или в других популяциях, за исключением пациентов, перенесших трансплантацию почек, у которых наблюдалось вариабельное увеличение остаточной концентрации циклоспорина (в среднем 0 — 40%). Необходимо рассмотреть вопрос о контроле концентраций циклоспорина у пациентов, перенесших трансплантацию почек, получающих амлодипин, а также сократить дозы циклоспорина, если это необходимо.
Симвастатин
Совместное применение амлодипина с симвастатином в дозе 80 мг приводило к увеличению экспозиции симвастатина до 77% по сравнению с монотерапией симвастатином. Поэтому доза симвастатина не должна превышать 20 мг в сутки.
Другие препараты
Установлена безопасность совместного применения амлодипина с дигоксином, варфарином, аторвастатином, силденафилом, антацидными лекарственными препаратами (гидроксид алюминия, гидроксид магния, симетикон), циметидином, антибиотиками и пероральными гипогликемическими лекарственными препаратами. При одновременном применении амлодипина и силденафила показано, что каждый препарат оказывал независимое гипотензивное действие.
Одновременное применение амлодипина с циметидином не оказывало существенного влияния на фармакокинетику амлодипина. Одновременное применение амлодипина с аторвастатином, дигоксином, варфарином или циклоспорином существенно не влияло на фармакокинетику или фармакодинамику этих препаратов.
Особые указания
Беременность
Применение антагонистов рецепторов ангиотензина II не следует начинать во время беременности. За исключением тех случаев, когда продолжение лечения не считается необходимым, у пациентов, планирующих беременность, эти лекарственные препараты должны быть заменены на альтернативные антигипертензивные лекарственные препараты, которые имеют изученный профиль безопасности для использования во время беременности. Когда диагностируется беременность, лечение антагонистами рецепторов ангиотензина II следует немедленно прекратить, и, при необходимости, начать альтернативное лечение.
Печеночная недостаточность
Телмисартан выводится преимущественно с желчью. Ожидается, что у пациентов с обструкцией желчевыводящих путей или печеночной недостаточностью клиренс лекарственного препарата снижается. Кроме того, как и у всех антагонистов кальция, период полувыведения амлодипина у пациентов с нарушенной функцией печени увеличивается, а рекомендации по дозированию этого лекарственного препарата не установлены. В связи с этим комбинацию телмисартана/амлодипина у таких пациентов следует применять с осторожностью.
Реноваскулярная артериальная гипертензия
У пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной функционирующей почки, принимающих лекарственные препараты, влияющие на ренин-ангиотензин-альдостероновую систему (РААС), существует повышенный риск развития выраженной гипотензии и почечной недостаточности.
Нарушения функции почек и состояния после трансплантации почки
Опыт применения препарата Твинста у пациентов, которым была недавно проведена трансплантация почки, отсутствует. Амлодипин и телмисартан не удаляются при гемодиализе. Пациентам с нарушениями функции почек рекомендуется периодический контроль содержания калия и креатинина в сыворотке крови.
Сниженный объем циркулирующей крови (ОЦК) и/или гипонатриемия
Вследствие ограничения потребления поваренной соли, интенсивной терапии диуретическими средствами, диареи или рвоты может развиваться симптоматическая артериальная гипотензия, особенно после приема первой дозы препарата. Перед применением препарата Твинста такие состояния требуют коррекции. Если артериальная гипотония возникает на фоне применения препарата Твинста, пациента необходимо положить на спину, и, если необходимо, следует назначить внутривенное введение физиологического раствора. Лечение может быть продолжено после стабилизации артериального давления.
Двойная блокада ренин-ангиотензин-альдостероновой системы (РААС)
Имеются данные, что одновременное применение иАПФ, антагонистов рецепторов ангиотензина II или алискирена увеличивает риск развития гипотонии, гиперкалиемии и снижения функции почек (включая острую почечную недостаточность). Поэтому двойная блокада РААС путем комбинированного применения иАПФ, антагонистов рецепторов ангиотензина II или алискирена не рекомендована.
Если лечение с двойной блокадой РААС считается необходимым, его следует проводить только под наблюдением специалиста и при условии тщательного контроля функции почек, концентрации электролитов и артериального давления.
Ингибиторы АПФ и антагонисты рецепторов ангиотензина II не должны применяться одновременно у пациентов с диабетической нефропатией.
Другие состояния, характеризующиеся активацией РААС
В случаях зависимости сосудистого тонуса и функции почек преимущественно от активности РААС (например, у пациентов с хронической сердечной недостаточностью или заболеваниями почек, в том числе при стенозе почечных артерий) назначение препаратов, влияющих на эту систему, может сопровождаться развитием острой артериальной гипотензии, гиперазотемии, олигурии, и, в редких случаях, острой почечной недостаточности.
Первичный альдостеронизм
У пациентов с первичным альдостеронизмом гипотензивные лекарственные препараты, механизм действия которых состоит в ингибировании РААС, как правило, не эффективны. Таким образом, применение телмисартана в таких случаях не рекомендуется.
Сахарный диабет
У пациентов с сахарным диабетом (СД) с дополнительным сердечно-сосудистым риском (т.е. с сопутствующей ишемической болезнью сердца), риск фатального инфаркта миокарда и внезапной сердечно-сосудистой смерти могут быть увеличены при лечении гипотензивными средствами, такими как APA II и ингибиторами ангиотензинпревращающего фермента (иАПФ).
Стеноз аортального и митрального клапанов, гипертрофическая обструктивная кардиомиопатия
У пациентов с аортальным или митральным стенозом, или при обструктивной гипертрофической кардиомиопатии применение препарата Твинста, также как и других вазодилататоров, требует особой осторожности.
Нестабильная стенокардия, острый инфаркт миокарда
Нет данных о применении препарата Твинста у пациентов с нестабильной стенокардией, в остром периоде и в течение одного месяца после инфаркта миокарда.
Сердечная недостаточность
В клиническом исследовании установлено, что применение амлодипина у пациентов с сердечной недостаточностью неишемической этиологии III и IV функционального класса по классификации NYHA сопровождалось более частым развитием отека легких (несмотря на отсутствие существенного различия в частоте ухудшения сердечной недостаточности по сравнению с плацебо).
Пациенты с сахарным диабетом, получающие инсулин или другие сахароснижающие лекарственные препараты
У данных пациентов гипогликемия может возникнуть при лечении телмисартаном. Поэтому у таких пациентов следует рассмотреть возможность проведения надлежащего мониторинга концентрации глюкозы в крови; может потребоваться коррекция дозы инсулина или сахароснижающих лекарственных препаратов, если это необходимо.
Гиперкалиемия
Во время лечения лекарственными препаратами, которые влияют на РААС, особенно при наличии нарушений функции почек и/или сердечной недостаточности, может возникать гиперкалиемия. Гиперкалиемия может быть фатальной у пожилых пациентов, у пациентов с почечной недостаточностью, у пациентов с сахарным диабетом, у пациентов, которые одновременно получают другие лекарственные препараты, которые могут повышать концентрацию калия в сыворотке крови, и/или у пациентов с интеркуррентными событиями.
Прежде чем рассматривать возможность совместного применения лекарственных препаратов, которые влияют на РААС, необходимо оценить соотношение польза-риск.
Основными факторами риска развития гиперкалиемии являются:
- сахарный диабет, нарушение функции почек, возраст (> 70 лет);
- комбинация с одним или несколькими другими лекарственными препаратами, которые влияют на РААС и/или пищевыми добавками, содержащими калий. Лекарственные препараты или терапевтические классы лекарственных препаратов, которые могут спровоцировать развитие гиперкалиемии, представляют собой соли, содержащие калий, калийсберегающие диуретики, иАПФ, антагонисты рецепторов ангиотензина II, НПВП (включая селективные ингибиторы ЦОГ-2), гепарин, иммунодепрессанты (циклоспорин или такролимус) и триметоприм;
- интеркуррентные события, в частности, дегидратация, острая декомпенсация сердечной деятельности, метаболический ацидоз, ухудшение функции почек, внезапное ухудшение состояния почек (например, инфекционные заболевания), клеточный лизис (например, ишемия конечности, рабдомиолиз, обширная травма).
У данных пациентов следует тщательно контролировать концентрацию калия в сыворотке крови.
Сорбитол
Каждая таблетка препарата Твинста содержит 168,64 мг сорбитола.
Прочее
Чрезмерное снижение артериального давления у пациентов с ишемической кардиомиопатией или ишемическим сердечно-сосудистым заболеванием может привести к развитию инфаркта миокарда или инсульта.
Препарат Твинста эффективен при лечении пациентов негроидной расы (в этой популяции обычно снижена активность ренина в крови).
Влияние на способность к управлению транспортными средствами и механизмами
Исследования влияния на способность к управлению транспортными средствами и управлению механизмами не проводились. Однако следует принимать во внимание, что во время лечения могут отмечаться такие нежелательные реакции, как обморок, сонливость или головокружение. Поэтому во время управления транспортными средствами или механизмами следует соблюдать осторожность. Если пациенты испытывают эти ощущения, им следует избегать выполнения таких потенциально опасных действий, как вождение автотранспорта или управление механизмами.
Форма выпуска:
Таблетки 5 мг + 40 мг, 10 мг + 40 мг, 5 мг + 80 мг, 10 мг + 80 мг.
По 7 таблеток в блистер из А1/А1 фольги.
По 2 или 4 блистера вместе с инструкцией по применению в картонную пачку.
Условия хранения
Хранить при температуре не выше 25°С, в оригинальной упаковке.
Хранить в недоступном для детей месте!
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
Берингер Ингельхайм Интернешнл ГмбХ, Германия
Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Производитель
Производство готовой лекарственной формы
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ,
Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия или
Ципла Лтд.,
Участок L-139-L146, Промышленная зона Верна, Верна Гоа, Индия
Первичная и вторичная упаковка
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ,
Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Выпускающий контроль качества (производитель)
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ,
Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Организация, уполномоченная на принятие претензий от потребителя:
ООО «Берингер Ингельхайм»
125171, Москва, Ленинградское шоссе, 16А стр.3
Купить Твинста в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)