Описание
- Естественная поддержка баланса мочевой кислоты с Ayuric
- Пищевая добавка
Богатый танином экстракт получают из съедобного плода дерева Terminalia bellerica; он способствует поддержанию уровней мочевой кислоты в нормальном диапазоне.1
Этот стандартизированный экстракт дерева Terminalia bellerica, на который подана патентная заявка, способствует здоровой экспрессии двух важнейших энзимов, участвующих в метаболизме мочевой кислоты:
- Ксантиноксидаза
- Индуцируемая синтаза оксида азота (iNOS)
Название этого стандартизированного экстракта Terminalia bellerica — контроль мочевой кислоты. Предлагаемая дозировка — одна капсула дважды в день.
| Дополнительные факты | ||
| Размер порции: 1 Вегетарианская капсула | ||
| Обслуживание в контейнере: 60 | ||
| Количество на порцию | % Дневная стоимость | |
| Экстракт аюрведической семечки (плод) [стд. до 15% танинов] | 500 мг | ** |
| **Суточная доза не определена. |
Другие Ингредиенты
Растительная целлюлоза (капсула), микрокристаллическая целлюлоза, стеариновая кислота, диоксид кремния.
Рекомендации по Применению
Перед употреблением внимательно прочитайте информацию на этикетке и следуйте инструкциям.
Указания: принимать по одной (1) капсуле дважды в день после завтрака и ужина, либо согласно рекомендациям лечащего врача.
Предупреждения
Хранить плотно закрытым в сухом прохладном месте.
- Хранить в недоступном для детей месте.
- Не превышать рекомендуемую дозировку.
- Не употреблять в случае повреждения наружной мембраны упаковки.
- При употреблении пищевых добавок проконсультируйтесь с врачом, если вы проходите лечение заболевания, беременны или кормите грудью.
Посетить веб-сайт производителя
Характеристики
Мочевая кислота
Uric acid
Фармакологическое действие
Мочевая кислота — продукт распада нуклеиновых кислот и пуриновых оснований под влиянием ферментов. В организме человека образование мочевой кислоты происходит с помощью ксантиноксидазы в результате ферментативного окисления ксантина. Как правило, в организме присутствует небольшое количество мочевой кислоты, при избыточном количестве, называемом гиперурикемией, может возникать подагра и образование камней в почках. Повышенный уровень мочевой кислоты в сыворотке также связан с более высоким риском развития диабета 2 типа и других заболеваний.
Мочевая кислота увеличивается в ответ на окислительный стресс и проявляет антиоксидантные свойства. Точный механизм антиоксидантного действия мочевой кислоты до конца не выяснен.
Показатели нормы: для мужчин — не более 420 мкмоль кислоты, у женщин — не более 360 мкмоль. В пожилом возрасте может произойти небольшое увеличение этих значений. Уровень мочевой кислоты зависит от возраста, пола и функции почек.
Показания
Не имеет терапевтических показаний.
Исследовался на предмет оценки фармакокинетики, фармакодинамики, эффективности, переносимости и безопасности при использовании в качестве вспомогательного средства при остром ишемическом инсульте.
Способ применения и дозы
В настоящее время недостаточно научной информации для определения подходящего диапазона доз мочевой кислоты.
Информация о действующем веществе Мочевая кислота предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Мочевая кислота, содержатся в инструкции производителя, прилагаемой к упаковке.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Мочевая кислота в крови
: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показания для назначения исследования
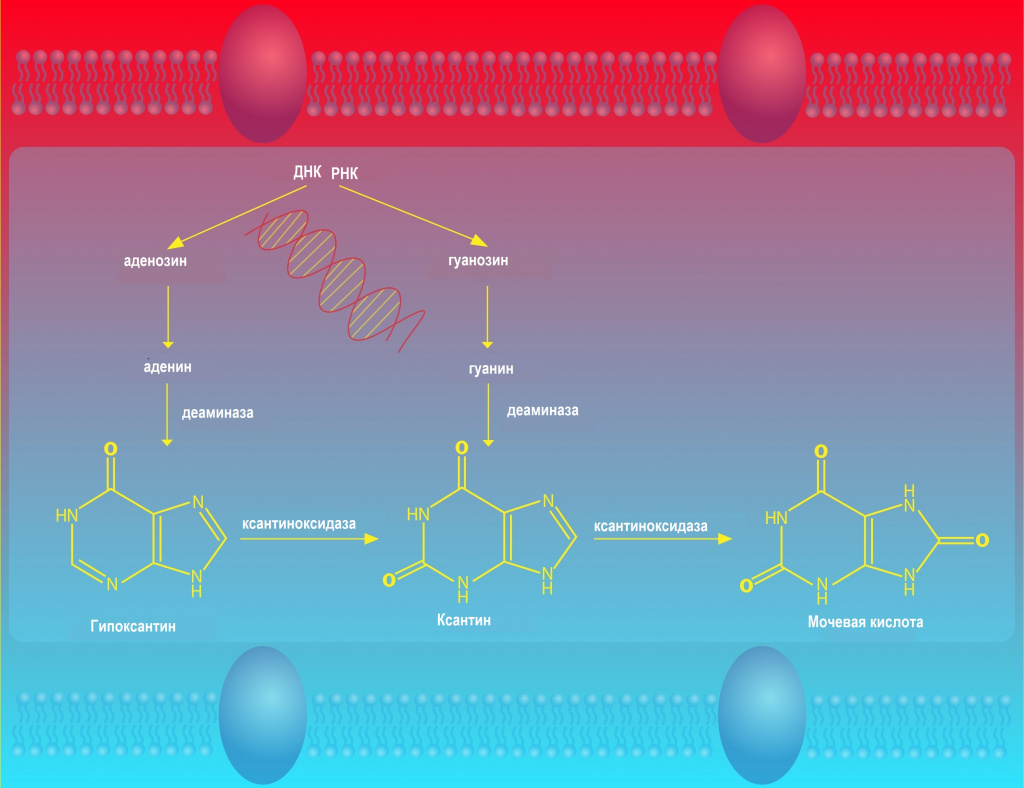
Мочевая кислота – это продукт обмена пуриновых оснований, входящих в состав сложных белков нуклеопротеидов.
Предшественниками мочевой кислоты являются пурины (гуанин и ксантин — составные части нуклеиновых кислот ДНК и РНК), которые образуются эндогенно или поступают с пищей, а также пуриновые нуклеозиды, из которых образованы аденозинтрифосфат (АТФ) и подобные соединения. Под влиянием ферментов в клетках тканей нуклеиновые кислоты распадаются.
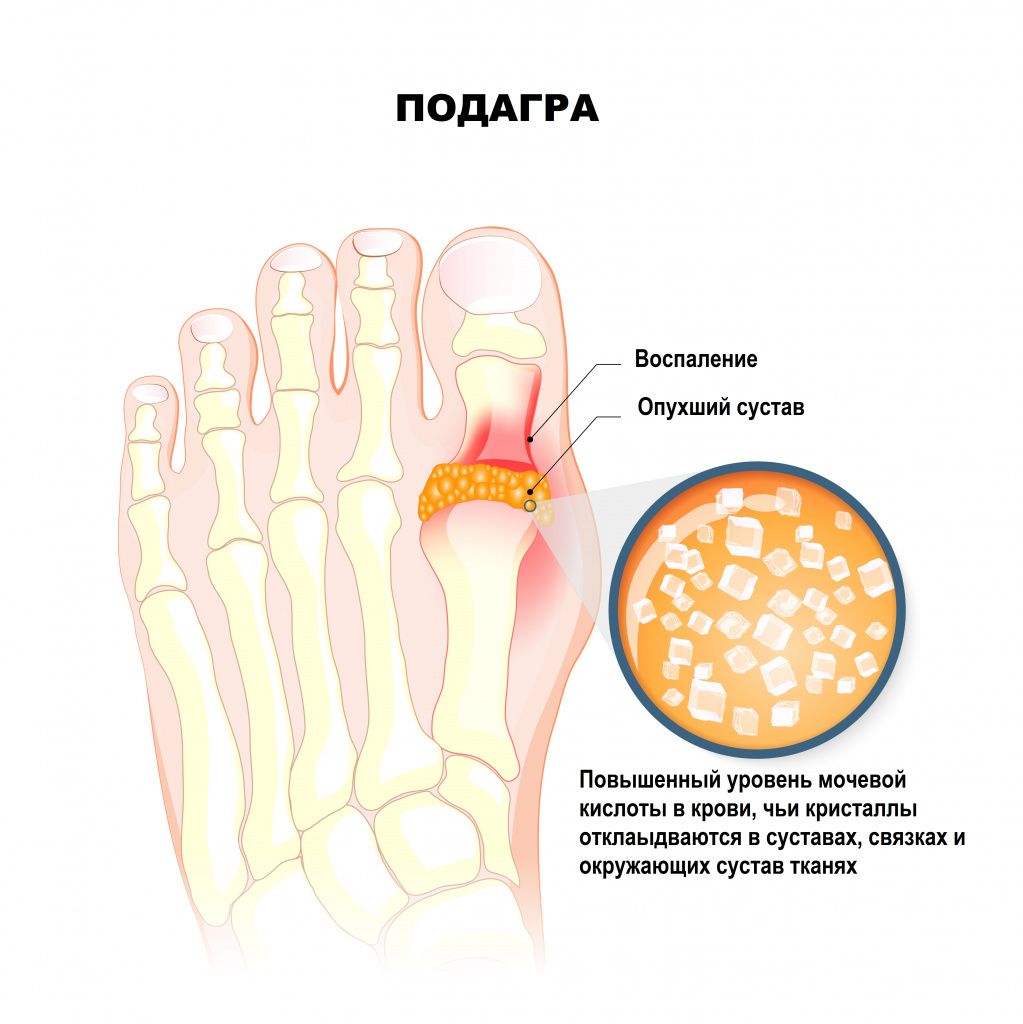
Образование кристаллов моноурата натрия происходит при концентрации мочевой кислоты в сыворотке крови выше 420 мкмоль/л. В некоторых случаях формирование кристаллов возможно и при более низком уровне (360 мкмоль/л).
Отложение кристаллов происходит в суставные и/или околосуставные ткани, почки и другие органы в виде тофусов (лат. tofus — пористый камень). Чаще всего болезнь поражает большой палец ноги, стопу, лодыжку, колено, пальцы рук, запястье и локоть, но может затрагивать любой сустав. Отложение кристаллов моноурата натрия в синовиальной жидкости и близлежащих тканях запускает каскад иммунных реакций. Наличие в суставах и окружающих тканях кристаллов моноурата натрия вызывают хронический воспалительный процесс.
Две трети мочевой кислоты выделяется почками. Одна треть мочевой кислоты под воздействием кишечных бактерий метаболизируется в кишечнике. Обычно процессы синтеза и выделения мочевой кислоты сбалансированы.
Повышение мочевой кислоты в крови может происходить по нескольким причинам:
- при снижении выделения мочевой кислоты с мочой из-за нарушения функции почек, уменьшения объема внеклеточной жидкости, под влиянием алкоголя и некоторых лекарственных средств, голодания и др.);
- при повышении ее продукции в организме:
- при чрезмерном поступлении пуринов с пищей (пурины в большом количестве содержатся в жирном мясе, печени, почках, мясных экстрактах, сухом вине, пиве и др.);
- при повышенном распаде клеток печени при хроническом алкоголизме, гемобластозах, парапротеинемиях, хроническом гемолизе, проведении противоопухолевой терапии.
Потребление большого количества животного белка, избыточная масса тела, повышение артериального давления, прием алкоголя, мочегонных препаратов, резистентность к инсулину, гематологический рак и другие факторы могут повышать уровень мочевой кислоты и способствовать развитию подагры.
Таким образом, показаниями для назначения анализа на уровень мочевой кислоты являются следующие заболевания и состояния:
- первичная подагра;
- вторичная подагра, возникшая на фоне болезней с избыточным образованием мочевой кислоты или нарушающие ее выведение:
- острые инфекционные заболевания (пневмония, рожистое воспаление, туберкулез и др.),
- заболевания печени и желчевыводящих путей,
- сахарный диабет с ацидозом,
- псориаз, экзема, крапивница,
- заболевания почек,
- острая алкогольная интоксикация,
- лимфопролиферативные заболевания, лейкозы.в
Подготовка к процедуре
Взятие крови предпочтительно проводить утром натощак, после 8-14 часов ночного периода голодания (воду пить можно), допустимо днем через 4 часа после легкого приема пищи.
Накануне исследования нужно придерживаться стандартной диеты без избыточного употребления пищи, богатой белками и пуринами.
Исключить повышенные психоэмоциональные и физические нагрузки (спортивные тренировки), прием алкоголя.
Срок исполнения
1 рабочий день — указанный срок не включает день взятия биоматериала.
Что может повлиять на результат
- К повышению мочевой кислоты в сыворотке крови может привести прием следующих лекарственных препаратов: тиазидных диуретиков, анаболических стероидов, никотиновой кислоты, эпинефрина, кофеина, витамина С, бета-адреноблокаторов, фуросемида, кальцитриола, этакриновой кислоты, циклоспоринов, цисплатина, аспаргиназы, клопидогрела, диклофенака, ибупрофена, изониазида, этамбутола, индометацина, пироксикама.
- К понижению мочевой кислоты в сыворотке крови может привести прием аллопуринола, амлодипина, верапамила, хлорпротиксена, винбластина, метотрексата, глюкокортикоидов, имурана, варфарина, леводопы, метилдопы, контрастных веществ, спиронолактона, азатиопринэстрогенов.
Мочевая кислота (в крови) (Uric acid)
Мочевая кислота (в крови) (Uric acid)
Исследование мочевой кислоты применяют в диагностике и контроле лечения подагры, оценке риска мочекаменной болезни.
Синонимы: Анализ крови на мочевую к…
Единицы измерения: мкмоль/л.
Альтернативные единицы измерения: мг/дл.
Коэффициент пересчета: мг/дл х 59,5 => мкмоль/л.
Сдать анализ крови на мочевую кислоту можно в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Нормальные показатели
Референсные значения
| Возраст | Мочевая кислота, мкмоль/л |
| дети до 14 лет | 120 — 320 |
| женщины > 14 лет | 150 — 350 |
| мужчины > 14 лет | 210 — 420 |
Расшифровка показателей
Содержание мочевой кислоты в сыворотке крови зависит от возраста и пола человека. Уровень мочевой кислоты начинает расти во время полового созревания и достигает значений взрослых. У мужчин уровень мочевой кислоты довольно стабильный на протяжении всей жизни и составляет 210-420 мкмоль/л. У женщин репродуктивного возраста более низкий уровень мочевой кислоты обусловлен защитной функцией эстрогенов и составляет 150–350 мкмоль/л. Уровень повышается в период менопаузы, поэтому гиперурикемия у женщин может развиваться в возрасте около 50 лет.
В соответствии с Рекомендациями Европейской антиревматической лиги (European League Against Rheumatism — EULAR) по диагностике и лечению подагры (2006, 2016) гиперурикемией считают уровень мочевой кислоты в сыворотке крови ≥360 мкмоль/л (6 мг/дл). Именно такой уровень повышает риск развития подагры у мужчин в 4 раза и в 17 раз у женщин. Стабильная сывороточная концентрация мочевой кислоты ≤360 мкмоль/л (6 мг/дл) является условием для растворения кристаллов и предупреждения их образования.
Что значат пониженные результаты
Пониженные показатели уровня мочевой кислоты в крови определяются при следующих заболеваниях и состояниях:
- Болезнь Коновалова-Вильсона (врожденное нарушение метаболизма меди, приводящее к тяжелейшим поражениям центральной нервной системы и внутренних органов.).
- Синдром Фанкони (снижение канальцевой реабсорбции мочевой кислоты из-за дефекта развития канальцев почек).
- Прием аллопуринола, рентгеноконтрастных средств, глюкокортикоидов, азатиоприна.
- Ксантинурия – наследственная болезнь, обусловленная недостаточностью ксантиоксидазы и характеризующаяся рецидивирующей гематурией и болями в поясничной области.
- Болезнь Ходжкина — лимфогранулематоз, злокачественное заболевание лимфоидной ткани.
- Низкопуриновая диета.
Что значат повышенные результаты
Повышенные показатели уровня мочевой кислоты в крови определяются при следующих заболеваниях и состояниях:
- Подагра.
- Синдром Леша-Нихана (генетически обусловленная недостаточность фермента гипоксантин-гуанин фосфорибозил-трансферазы — ГГФТ).
- Болезни крови:
- лейкозы,
- миеломная болезнь,
- лимфома,
- полицитемия,
- B12-дефицитная анемия.
- Злокачественные новообразования.
- Заболевания желез внутренней секреции:
- акромегалия,
- сахарный диабет,
- гипопаратиреоз.
- Заболевания почек:
- поликистоз почек,
- почечная недостаточность.
- Пища, богатая пуринами, длительное голодание.
- Токсикоз беременных.
- Ожирение, атеросклероз.
- Прием салицилатов, диуретиков, цитостатиков.
- Употребление алкоголя.
Дополнительное обследование при отклонении от нормы
Для постановки диагноза, а также для контроля качества лечения врачом-терапевтом или ревматологом могут быть рекомендованы дополнительные исследования:
- Выявление кристаллов моноурата натрия в синовиальной жидкости или тофусах.
Рентген костей стопы
Рентгенологическое исследование стопы в двух проекциях позволяет диагностировать травмы и другие патологические изменения, в том числе и плоскостопие.
Рентген костей кисти
Рентгенологическое исследование костей кисти предназначено для диагностики травматических повреждений, патологических изменений, а также оценки развития косте�…
Источники:
- Мясоедова С.Е. Новые возможности уратснижающей терапии при подагре // Трудный пациент. – 2018. – № 3. – Т. 16. – С. 28-31.
- Подагра. Клинические рекомендации. Ассоциация ревматологов России. 2018 г.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
8413
13 Мая
-
16512
04 Мая
-
14096
16 Апреля
Похожие статьи
Лабораторная диагностика угрозы атеросклероза
Атеросклероз хроническое заболевание, характеризующееся специфическим поражением артерий эластического и мышечно-эластического типов. В их стенках происходит разрастание соединительной ткани в сочетании с липидной (жировой) инфильтрацией внутренней оболочки. Это приводит к органным и общим нарушениям кровообращения. Атеросклероз основное заболевание сердечно-сосудистой системы, являющееся причиной стенокардии (грудной жабы), инфаркта миокарда, инсульта и смерти.
Гомоцистеин
Гомоцистеин: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Глюкоза (в крови) (Glucose)
Глюкоза (в крови) (Glucose): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Мочевая кислота — результат трансформации азотистых оснований, в основном выводимый с мочой. Ее концентрация зависит от разницы между количеством, вырабатываемым в организме и выводимым почками. Лишняя мочевая кислота (гиперурикемия) откладывается в виде кристаллов, давая серьезные симптомы.
Анализ на мочевую кислоту в крови или в моче обычно выполняется при симптомах подагры и заболеваний почек. Многих больных, получивших негативный результат, беспокоит вопрос о том, как убрать излишки мочевой кислоты, тем самым уменьшив боль, сопровождающую гиперурикемию.
Что такое мочевая кислота? Откуда она берется в организме?
Мочевая кислота — это конечный и естественный продукт метаболизма пуринов — элемента нуклеиновых кислот (ДНК и РНК) клеток всех организмов. Источники азотистых оснований — внутренний синтез этих соединений и физиологический распад клеток. Некоторые пурины также попадают в организм с продуктами: пивом, красным мясом, копченой рыбой, какао.
Пурины благодаря ферментам деградируют в гепатоцитах печени. Это означает, что конечный продукт их распада должен выводиться, так как больше ни во что не преобразуется. Примерно 70% мочевой кислоты выводится с мочой, фильтруемой через почки, остальное, при участии пищеварительной системы, с калом.
Выведение моч. к-ты затрудняется, например, в случае мочекаменной болезни или подагры. Также это вещество накапливается в больших количествах в крови, в ходе некоторых метаболических заболеваний.
Когда назначаются анализы?
Измерить уровень мочевой кислоты нужно в ряде случаев:
- Подозрение на подагру. Ее симптомы: болезненность, покраснение и отек суставов, особенно воспаление основания сустава большого пальца ноги. Подагра часто вызывает воспаление суставов, особенно первого плюснефалангового сустава.
- Диагностика мочекаменной болезни. Патология связана с выведением большого количества мочевой кислоты. В случае тяжелой почечной колики анализ помогает определить тип мочевых камней у больного. Почечная колика характеризуется сильной болью внизу живота, иррадиирующей вплоть до спины. Также у больных отмечается выраженное уменьшение выделяемой мочи, гематурия или изменение цвета мочи.
- Почечная недостаточность.
- Гестоз у беременных.
Дополнительные (неспецифические) симптомы при повышении мочевой кислоты:
- боль и жжение в области мочевого пузыря;
- Увеличение количества мочи;
- лихорадка;
- боль в животе и поясничной области;
- тошнота и рвота.
Обследование также должно проводиться среди онкологических больных, проходящих химиотерапию и лучевую терапию. Химиотерапия ускоряет разрушение раковых клеток с высвобождением из них пуриновых соединений, впоследствии превращающихся в мочевую кислоту. Также анализы назначаются для контроля за ходом лечения у больных подагрой.
Определение мочевой кислоты в крови и моче. Как подготовиться к исследованию?
Уровень мочевой кислоты может определяться в моче и в сыворотке крови. В случае определения сыворотки венозная кровь берется натощак: желательно выждать 12 часов с момента приема пищи. Важно понимать, что употребление продуктов, богатых пуринами, может фальсифицировать результат, поэтому за двое суток нужно исключить такие продукты из меню.
При подготовке к обследованию нужно избегать физических нагрузок 2-3 дня до анализа. Также нужно ограничить стрессовые факторы. Риск повреждения клеток и временного повышения концентрации мочевой кислоты в крови должен быть сведен к минимуму.
Во время сбора мочи следует придерживаться тех же рекомендаций, что и при подготовке к сывороточному тесту.
Как делают анализ
Измерение концентрации мочевой кислоты заключается в единовременном сборе крови из локтевой вены, с помощью одноразовой иглы и пробирки. Методика проведения теста — спектрофотометрия (колориметрический иммуноферментный метод).
Концентрацию МК в моче можно определить как в одном образце, так и в суточном сборе мочи. Второй метод заключается в сборе всех образцов мочи, сданных в течение 24 часов, в один стерильный сосуд. Затем нужно измерить объем мочи и взять из нее образец, предназначенный для исследования в лаборатории.
Мочевая кислота – нормы для женщин, мужчин и детей
Уровень мочевой кислоты зависит от пола, а дополнительно увеличивается с возрастом, примерно до 70 лет. Анализ результатов испытаний всегда должен основываться на референсных значениях лаборатории, в которой они были выполнены, и находящихся в пределах заданных диапазонов стандартов.
Таблица 1. Средние нормы мочевой кислоты в сыворотке крови (Европа)
| Пол, возраст | Норма мочевой кислоты |
| Мужчины | 300-360 мкмоль/л (5-6 мг/дл) |
| Женщины | 240-300 мкмоль/л (4-5 мг/дл) |
| Дети | 210-240 мкмоль/л (3,5-4 мг/дл) |
Гиперурикемия диагностируется после нескольких определений концентраций выше 420 мкмоль/л (>7 мг/дл). Среднее выведение мочевой кислоты с мочой составляет около 400-650 мг/сут. Верхний предел обычно составляет 800 мг / день (4,8 ммоль / 24 часа).
Приступ подагры может быть у больного с нормальным уровнем мочевой кислоты и наоборот – повышенный уровень мочевой кислоты не всегда дает симптомы подагры. Наиболее частая причина подагры: генетическая склонность к избыточной выработке мочевой кислоты и нарушение выделительной функции почек. Поэтому, перед тестом расскажите врачу о прошлых заболеваниях и о лекарствах, которые вы принимаете.
Низкий и высокий уровень мочевой кислоты — чем это опасно?
Высокий и низкий уровень мочевой кислоты влияет на правильное функционирование организма. МК обладает противоположными эффектами:
- С одной стороны это ненужный продукт метаболических изменений. Поэтому повышение ее концентрации опасно для здоровья. Гиперурикемия приводит к подагре, нефролитиазу и другим заболеваниям почек. Также у людей с повышенной мочевой кислотой часто диагностируются гипотиреоз, гемолитическая анемия и сердечно-сосудистые заболевания, в том числе инфаркт, что говорит о связи этих факторов.
- С другой — мочевая кислота обладает антиоксидантным действием, защищая организм от свободных радикалов и вызванных ими повреждений клеток. Ее дефицит, например, увеличивает риск развития деменции, болезни Паркинсона.
Нельзя самостоятельно интерпретировать результаты анализов. Результат определения мочевой кислоты часто трактуется как вспомогательный к комплексной диагностике.
Расшифровка анализа: высокий уровень мочевой кислоты
Гиперурикемия может быть связана с чрезмерной выработкой МК или ее высвобождением из клеток, например:
- при генетических заболеваниях (болезнь Леша-Нихана, болезнь фон Гирке);
- из-за разрушения клеток в процессе лечения рака, при лучевой терапии или химиотерапии;
- из-за отравления свинцом;
- в случае лейкоза;
- в постменопаузальном периоде.
Гиперурикемия также возникает у людей с больными почками при ацидозе или злоупотреблении алкоголем. Также может повлиять диета с большим количеством белка и физические перегрузки. Ещё повышает уровень мочевой кислоты прием барбитуратов и диуретиков.
Наиболее распространенные симптомы гиперурикемии:
- Почечная колика. Больной чувствует сильную поясничную боль, иррадиирующую в сторону и в нижнюю конечность. Она имеет тенденцию смещаться. Часто боль сопровождается слабостью, лихорадкой и тошнотой;
- Подагра. Сопровождается лихорадкой и слабостью. Это следствие отложения кристаллов моч. к-ты в суставах, в результате чего возникает воспаление суставов.
Расшифровка анализа: низкий уровень мочевой кислоты
Концентрация МК в крови может быть снижена. Однако это не указывает на конкретное заболевание, а скорее возникает как сопутствующий симптом. Снижение может происходить при:
- Болезни Вильсона;
- синдроме Фанкони;
- заболеваниях, связанных с избыточной секрецией гормона роста;
- Синдроме Шварца-Барттера.
Слишком низкий уровень мочевой кислоты также может указывать на продолжающееся воспаление в почках и печени, целиакию, лимфомы и другие виды рака.
Снижают концентрацию препараты, применяемые для лечения гиперурикемии: салицилаты, аллопуринол, пробенецид, эстрогены, кортикотропин, фенотиазины.
Как снизить мочевую кислоту?
Основа лечения гиперурикемии — излечение основного заболевания, так как избыток моч. к-ты может быть результатом врожденных генетических состояний, результатом ожирения, неправильного питания, диабета или обезвоживания.
Чтобы очистить организм от избытка кристаллов мочевой кислоты, нужно увеличить физическую активность и следовать принципам рационального питания.
Диета больных с высоким уровнем мочевой кислоты основывается в первую очередь на употреблении негазированной воды и отказе от крепкого кофе, чая и пива. Также повышают мочевую кислоту в крови напитки, содержащие фруктозу и фруктовые соки. Второй принцип — ограничение пуринов. Это диета, бедная рыбой, красным мясом, бобовыми, грибами.
Количество соли в блюдах следует ограничить, так как избыток натрия тормозит выведение мочевой кислоты с мочой.
Нужно есть больше постного мяса птицы, фруктов и зерновых. Очень хороший эффект дают настои, приготовленные из листьев березы, одуванчика и крапивы.
Назначается фармакотерапия, понижающая мочевую кислоту в крови. Наиболее распространенные лекарства: фебуксостат и аллопуринол. Помимо приема лекарств нужно бросить курить.
Точные рекомендации всегда должны быть согласованы с лечащим врачом (например, урологом, ревматологом), который также принимает решение о необходимости возможной фармакотерапии.
1 капсула содержит
Основные вещества : измельченные створок фасоли обыкновенной (Faseolusvulgaris) ; сухие экстракты : листьев березы плосколистного ( Betula platyphylla) — 60 мг, корня петрушки кудрявой (Petroselinumcrispum) — 60 мг, листья брусники обыкновенной ( Vaccinium vitis-idaea) — 30 мг, травы ромашки ( Matricaria chamomilla ) — 10 мг, натрия — 20 мг, калия цитрат — 20 мг вспомогательные вещества : целлюлоза микрокристаллическая (E 460), двуокись кремния коллоидный, магния стеарат (Е 470) оболочка капсулы : желатин, вода очищенная, титана диоксид (Е 171), железа оксид желтый (Е172), медный комплекс хлорофиллина (Е 141).
Комплексное действие диетической добавки обусловлена синергическим эффектами биологически активных веществ, входящих в состав.
Комбинированная растительное диетическая добавка, благодаря наличию цитратного комплекса, способствует дезинтеграции и выведению почечных камней и камней мочевого тракта. УРИКЛАР обладает спазмолитическим действием, способствует прохождению камней по мочевыводящих путях, уменьшает боли при почечных и мочеточниковых коликах, улучшает функцию почек и повышает диурез.
Оказывает противомикробное и противовоспалительное действие.
Регулирует кристалло-коллоидный баланс, снижает концентрацию в моче элементов, способствующих образованию камней (щавелевая кислота, кальций, гидроксипролин). Препятствует аккумуляции частиц вокруг ядра камня, что предотвращает его дальнейшее увеличение.
При одновременном применении с другими уросептики УРИКЛАР усиливает их бактерицидный эффект.
Створок фасоли содержит бетаин, аргинин, тирозин, холин, микро- и макроэлементы. Основное действие — мочегонное, антибиотическая. Используется при воспалениях почек и отеках, вызванных заболеваниями почек.
Листья березы содержат эфирные масла, сапонины, дубильные вещества, смолы, аскорбиновую и никотиновую кислоты. Основное действие — диуретическое, желчегонное, спазмолитическое, противовоспалительное.
Корень петрушки содержит апонил, миристицин, флавоноиды. Основное действие — диуретическое, противовоспалительное, литолитическим.
Листья брусники содержат гликозид арбутин, урсоловую кислоту и фитонциды. Основное действие — антимикробное, мочегонное, противовоспалительное. Используется при мочекаменной болезни, воспалении мочевого пузыря.
Ромашка обладает антибактериальным, противовоспалительным, репаративный, вяжущее, антиоксидантный, анальгетический и спазмолитический эффекты.
Натрия и калия цитрат имеют эффект заложенные, и используются при мочекаменной болезни, вызванной уратным, цистиновыми и кальциевым камнями.
Рекомендуется в качестве диетической добавки к рациону питания как дополнительный источник флавоноидов, эфирных масел, дубильных веществ, каротиноидов, фитонцидов, органических кислот с целью нормализации функционального состояния мочевыделительной системы и обмена веществ (в частности фосфора, кальция и мочевой кислоты). Биологически активные вещества, входящие в состав диетической добавки УРИКЛАР, обладают мочегонным и противовоспалительным действием; способствуют предупреждению образования камней в почках и мочевыводящих путях.
Принимать взрослым по 1 капсуле 3 раза в сутки, запивая питноюводою (150-200 мл).
Курс применения определяет врач индивидуально.
Перед применением рекомендуется консультация врача.
Беременность и период лактации, острые воспалительные заболевания почек и мочевого пузыря, подагра, чувствительность к составляющим компонентам.
Капсулы № 30 (15 х 2) в блистерах, по 2 блистера в картонной коробке.
Хранить при температуре не выше 25 ° С в сухом, защищенном от света и недоступном для детей месте.
Подагра является наиболее частой причиной артрита [1], что обусловлено отложением кристаллов моноурата натрия (МУН) в суставах и мягких тканях. Для формирования кристаллов МУН необходима персистирующая гиперурикемия. При повышении сывороточного уровня мочевой кислоты (МК) происходит насыщение тканей МУН, что создает условия для его кристаллизации и, соответственно, манифестации подагры [2]. Порог насыщения МК составляет около 7 мг/дл (420 мкмоль/л), хотя для пациентов с подагрой рекомендуется достигать сывороточный уровень МК менее 6 мг/дл (360 мкмоль/л), поскольку такой уровень МК приводит к более быстрому уменьшению кристаллических отложений МУН [3–6].
Достигнутые в настоящее время успехи в понимании основных механизмов развития хронической гиперурикемии и подагры позволили пересмотреть многие положения, лежащие в основе диагностики и лечения заболевания. Между тем, несмотря на успехи в понимании патофизиологии подагры и доступность эффективных методов лечения, подагра остается плохо контролируемым заболеванием во всех странах [7, 8]. Пожалуй, самой распространенной проблемой является низкая приверженность пациентов к снижению сывороточного уровня МК, что главным образом связано с недостаточным пониманием цели терапии подагры и врачами, и пациентами. Целесообразно объяснить пациентам цель лечения [9–11], которая заключается в растворении имеющихся отложений кристаллов МУН путем снижения сывороточного уровня МК ниже точки насыщения сыворотки уратами и купировании приступов артрита, если таковые возникают. Следует также поддерживать сывороточный уровень МК ниже порога насыщения, чтобы избежать образования новых кристаллов.
Целью настоящей статьи было предоставить практический обзор существующих подходов к управлению заболеванием в четырех аспектах: немедикаментозные методы профилактики и лечения гиперурикемии; купирование острого приступа артрита; уратснижающая терапия, направленная на профилактику приступов артрита и образование тофусов; профилактика приступов артрита при инициации уратснижающей терапии.
Лечение подагры в соответствии с современными рекомендациями направлено на улучшение исходов заболевания. Эффективность лечебно-профилактических вмешательств при подагре зависит от четкого следования предложенной в них концепции лечения [4, 12, 13].
Немедикаментозные методы профилактики
Немедикаментозные методы профилактики, нацеленные на модификацию факторов образа жизни, связанных с риском развития гиперурикемии, предусматривают индивидуальное или групповое профилактическое консультирование по актуальным вопросам диетотерапии, контролю массы тела при ожирении, достижению целевых уровней артериального давления, коррекции нарушений углеводного и липидного обмена.
Ожирение является ведущим фактором риска подагры, особенно у мужчин, соответственно, контроль массы тела оказывает существенное влияние на частоту приступов подагры [14]. Снижение веса за счет ограничения общей калорийности пищи и потребления углеводов благотворно влияет на уровни сывороточного урата у пациентов с подагрой [15, 16].
Следует отметить, что в настоящее время пересмотрены некоторые принципиальные позиции по диетотерапии при подагре. Так, рекомендация по жесткому ограничению в пищевом рационе пуринсодержащих продуктов распространяется только на животные производные (мясо, морепродукты), поскольку именно такая мера способствует снижению сывороточного уровня мочевой кислоты. При этом богатая пуринами растительная пища не оказывает существенного влияния на урикемию [4, 17]. Показано, что потребление обезжиренных молочных продуктов [18, 19], растительных масел и овощей ассоциируется с уменьшением риска гиперурикемии и приступов подагры [4, 12]. Витамин С увеличивает почечную экскрецию мочевой кислоты, поэтому его можно использовать в качестве дополнительной меры при терапии подагры [20, 21]. Безопасным в отношении сывороточного уровня МК и риска развития подагры считается потребление небольшого количества сухого вина [20, 22]. При этом потребление пива, в т. ч. безалкогольного, крепких спиртных напитков, а также подслащенных безалкогольных напитков с высоким содержанием фруктозы должно быть ограничено максимально [20, 23–25].
Несмотря на то, что основная масса клинических исследований затрагивают оценку эффективности диетотерапии в аспекте профилактики риска развития подагры, а не управления частотой приступов артрита у лиц с верифицированным диагнозом, рекомендации по модификации образа жизни должны даваться всем пациентам с подагрой, в т. ч. получающим медикаментозную терапию.
Купирование острого приступа подагрического артрита
В современных рекомендациях в качестве препаратов первой линии противовоспалительной терапии рассматриваются нестероидные противовоспалительные средства (НПВС), колхицин и глюкокортикостероиды (ГК) [4, 12, 13]. Сравнительно недавний систематический обзор показал, что НПВС (в том числе селективные ингибиторы ЦОГ-2), ГК (перорально и внутримышечно), колхицин и ингибитор ИЛ-1β (канакинумаб) являются эффективными методами лечения острых приступов [26]. Целесообразность персонифицированного выбора режима терапии обусловлена и индивидуальными особенностями больного, и гетерогенностью собственно подагрического процесса, протекающего с вовлечением многих органов и систем организма, что существенно модифицирует фармакодинамику препаратов, приводя к кумуляции нежелательных эффектов.
Терапия НПВС занимает лидирующие позиции в лечении как острого приступа, так и хронического подагрического артрита. Считается, чем раньше назначен препарат, тем быстрее может быть достигнут анальгетический эффект. НПВС следует использовать в максимальных суточных дозах, которые могут быть уменьшены по мере ослабления симптоматики. Выбор конкретного НПВС во многом зависит от личных предпочтений. И селективные ингибиторы ЦОГ-2, и традиционные НПВС эффективны при лечении острых приступов подагрического артрита. Недавний систематический обзор, объединяющий результаты шести рандомизированных клинических исследований (851 пациент), продемонстрировал одинаковый эффект эторикоксиба (120 мг в сутки), индометацина и диклофенака при остром артрите, с лучшей у эторикоксиба переносимостью со стороны желудочно-кишечного тракта [27]. Другой селективный ингибитор ЦОГ-2 — целекоксиб также обнаружил сопоставимый с индометацином эффект в отношении умеренной и выраженной боли у пациентов с острым подагрическим артритом [28]. Еще в одном систематическом обзоре был сделан вывод о том, что НПВС и селективные ингибиторы ЦОГ-2 обнаруживают эквивалентные преимущества в плане уменьшения боли, отечности и улучшения общего самочувствия, однако традиционные НПВС отличаются большей частотой отмены из-за нежелательных явлений [29].
Колхицин — алкалоид, получаемый из растения безвременника осеннего (Colchicum autumnae), используется для лечения острой подагры на протяжении многих десятилетий. Клинические исследования и ежедневная рутинная практика демонстрируют высокую частоту побочных эффектов при применении колхицина, которые, вероятно, можно объяснить назначением в прошлые годы более высоких доз препарата, чем рекомендованы в настоящее время. По крайней мере, большое многоцентровое исследование пациентов с подагрой и сохраненной функцией почек убедительно показало сопоставимую эффективность двух режимов терапии острого подагрического артрита: низкодозового (1,8 мг колхицина в сутки: 1,2 мг сразу и 0,6 мг через час) и высокодозового (4,8 мг колхицина в сутки: 1,2 мг сразу и по 0,6 мг каждый час; 6 раз), с существенно меньшей частотой побочных эффектов со стороны желудочно-кишечного тракта в группе с низкой дозой. Причем эффективность низких доз колхицина была эквивалентна высоким в том случае, если колхицин в низких дозах назначался в течение первых 12 часов после начала острого приступа артрита [30]. Клиническая практика показывает, что колхицин оказывается гораздо менее эффективным, если его назначают после 12–24 часов от начала приступа. Соответственно, более позднее назначение может потребовать больших доз препарата, что практически всегда заканчивается развитием нежелательных лекарственных реакций.
Согласно современным национальным рекомендациям для купирования острой атаки артрита целесообразным считается назначение у большинства пациентов низких доз колхицина (1,5 мг в первые сутки (1 мг сразу и через 1 час еще 0,5 мг) и по 1 мг со следующего дня) [13].
Назначение ГК для купирования острого приступа подагры возможно в виде внутрисуставных (после удаления синовиальной жидкости), внутримышечных инъекций или внутрь.
Пероральный прием преднизолона в суточной дозе 30–35 мг/сут демонстрирует высокую эффективность [31, 32] и рекомендуется группами Американского колледжа ревматологов (American College of Rheumatology, ACR) и Европейской антиревматической лиги (European League Against Rheumatism, EULAR) в качестве терапии первой линии при лечении острого приступа подагры [12, 33]. При этом стартовая доза преднизолона 30–35 мг/сут назначается на несколько (3–6) дней с последующей быстрой (в течение 1 недели) полной отменой.
Внутримышечное введение ГК может быть применено в случаях полиартикулярного поражения суставов [34]. Внутрисуставные инъекции стероидов оказываются очень эффективными и рекомендуются как ACR, так и EULAR при моно- или полиартикулярном поражении суставов, несмотря на отсутствие рандомизированных клинических исследований [12, 33].
Однако важно отметить, что, вопреки бытующему мнению, прием преднизолона не эффективнее НПВС. Так, сравнение двух режимов терапии (преднизолон 35 мг/сут и напроксен 1000 мг/сут) у пациентов с острым подагрическим артритом показало отсутствие различий в динамике интенсивности боли при сопоставимой частоте нежелательных эффектов [35]. Кроме того, ГК не безопаснее НПВС, поскольку способны усугубить течение артериальной гипертонии и сахарного диабета [36]. В исследовании [37] частота побочных эффектов даже на однократное внутрисуставное введение ГК (бетаметазон 7 мг) оказалась чрезвычайно высокой: у 73% пациентов обнаружилось клинически значимое повышение уровня систолического артериального давления, у 23% — гликемия натощак, у 13% — ЭКГ-признаки ишемии миокарда.
При наличии абсолютных противопоказаний и/или неэффективности НПВС, колхицина и ГК, а также отсутствии текущей инфекции, с целью купирования острого артрита возможно применение моноклональных антител к ИЛ-1 (канакинумаб) [12].
Уратснижающая терапия
Уратснижающая терапия, основной целью которой является предупреждение образования и растворение имеющихся кристаллов МУН, возможна посредством достижения уровня МК ниже точки супернасыщения сыворотки уратами (< 360 мкмоль/л), при котором процесс кристаллизации МК приостанавливается, а депозиты кристаллов в тканях постепенно растворяются. Для пациентов с тяжелой тофусной подагрой, хроническим артритом и частыми атаками предпочтительно поддержание целевого сывороточного уровня МК ниже 300 мкмоль/л, поскольку это способствует более быстрому рассасыванию тофусов [12, 33].
Нужно заметить, что целесообразность регулярного контроля гиперурикемии на фоне уратснижающей терапии признается далеко не всеми исследователями. По крайней мере, данный подход был опротестован группой ACR, которая рекомендовала врачам назначать терапию подагры с целью управления симптомами, а не уровнем урикемии [38]. Между тем многочисленные клинические и патофизиологические исследования свидетельствуют о том, что снижение уровня МК ниже точки насыщения сыворотки уратами является лучшим и самым надежным способом контроля симптомов подагры в долгосрочной перспективе и что назначение уратснижающей терапии без отслеживания темпов снижения уровня урикемии является частым поводом отказа от лечения подагры для многих пациентов [4, 12, 33].
Поскольку у значительной доли больных хроническое воспаление, обусловленное депозитами моноурата натрия, предшествует клинической манифестации заболевания, то зачастую лечащему врачу довольно сложно принять решение, когда начинать лекарственную уратснижающую терапию: сразу после первого приступа или после повторения двух и более атак острого артрита.
Разумеется, уратснижающая терапия показана всем пациентам со стойкой гиперурикемией и острыми атаками артрита (в том числе в анамнезе), хроническим артритом, наличием тофусов (независимо от их локализации и методов выявления: при осмотре, методами лучевой визуализации). Пациентам с дебютом подагры в возрасте моложе 40 лет, при наличии коморбидной патологии (заболевание почек, артериальная гипертензия, ишемическая болезнь сердца, хроническая сердечная недостаточность) уратснижающая терапия должна быть инициирована сразу после первого приступа подагры, вне зависимости от уровня гиперурикемии. Проведение уратснижающей терапии в других случаях (при неосложненной подагре) показано при неэффективности нефармакологических методов лечения.
Уратснижающими препаратами являются аллопуринол и фебуксостат. Мишенью действия этих препаратов является ключевой фермент пуринового обмена — ксантиноксидаза, которая обеспечивает окисление гипоксантина до ксантина и далее ксантина — до МК. В этой сложной реакции превращения МК из гипоксантина высвобождаются супероксидные анионы и молекулярный кислород, способные вызывать оксидативный стресс и повреждение тканей [39].
Аллопуринол является ингибитором ксантиноксидазы, впервые введенным в клинику в шестидесятые годы. Сегодня он признан препаратом базисной терапии подагры. По своей химической природе аллопуринол — аналог гипоксантина. Механизм действия аллопуринола весьма интересен: в начале реакции он действует в качестве субстрата фермента ксантиноксидазы, а затем — в качестве ее ингибитора. Так, вначале ксантиноксидаза гидроксилирует аллопуринол, превращая его в аналог гипоксантина — аллоксантин (оксипуринол). А далее аллоксантин, прочно связываясь с активным центром ксантиноксидазы, содержащим ион молибдена, меняет ее свойства, в результате чего последующего этапа превращения МК не происходит. Кроме ингибирования трансформации гипоксантина в МК, аллопуринол устраняет выработку продуктов оксидативного стресса [39].
В клинической практике широко используемая доза аллопуринола составляет 300 мг/сут (90–95% пациентов с подагрой) [40], но для контроля гиперурикемии этого довольно часто бывает недостаточно. Так, по данным исследования [41] только 53% пациентов с подагрой достигли сывороточного уровня МК менее 6 мг/дл (360 мкмоль/л) на аллопуриноле 300 мг в день, но когда доза препарата была увеличена до 450–600 мг в сутки, то к целевому уровню МК приблизились все 100% испытуемых. В другом исследовании только 26,0% пациентов, получавших 300 мг аллопуринола в сутки, достигли целевого уровня МК ниже 6 мг/дл (360 мкмоль/л), тогда как 78% пациентов смогли достичь целевых значений только при повышении суточной дозы аллопуринола свыше 600 мг в сутки [42]. Таким образом, стандартная доза аллопуринола 300 мг в сутки зачастую недостаточна для достижения цели и должна титроваться в большую сторону, с учетом целевого уровня МК. Еще один важный момент, который должен учитываться при выборе оптимальной дозы препарата, — это состояние функции почек, поскольку ключевой метаболит аллопуринола — оксипуринол выводится главным образом почками [43]. В свое время, чтобы иметь возможность контролировать токсичность препарата, были предложены правила титрования дозы аллопуринола в зависимости от клиренса креатинина [44], но эта мера довольно часто не позволяла достичь целевых уровней МК [45].
В настоящее время рекомендуется назначать аллопуринол в исходно низкой дозе (50–100 мг в сутки) с последующим увеличением дозы (при необходимости) по 100 мг каждые 2–4 недели, что особенно важно у пациентов с почечной недостаточностью [5, 13]. Такое медленное титрование дозы снижает вероятность острого приступа после старта терапии [3]. Хотя в двух недавних исследованиях было показано, что опасения по поводу вероятности развития острой атаки артрита нередко бывают преувеличенными [46, 47]. По крайней мере, приостанавливать ранее начатую уратоснижающую терапию в случае вспышки острого артрита у большинства больных нет оснований.
Во всяком случае, аллопуринол следует назначать не ранее чем через 2 недели после купирования приступа острого артрита, постепенно титруя дозу до эффективной и отслеживая возможные нежелательные явления, частота которых существенно возрастает параллельно увеличению дозы.
К сожалению, аллопуринол относится к препаратам, на высокие дозы которого возможно развитие серьезных нежелательных явлений в виде прогрессирующей почечной недостаточности, гепатотоксичности, тяжелых аллергических реакций, в т. ч. синдрома Стивена–Джонсона, эпидермального некролиза, DRESS-синдрома [48, 49]. К возможным причинам развития таких тяжелых реакций на аллопуринол относят носительство гена HLA-В 5801, которое с высокой частотой встречается в разных этнических популяциях и максимально распространено в Азии (17%). В России носительство аллеля HLA-В 5801 сопоставимо с таковым в азиатских странах и выше, чем в странах Европы [50].
Впервые за 50 лет в качестве альтернативы аллопуринолу был разработан и внедрен в клиническую практику фебуксостат — сильный селективный непуриновый ингибитор ксантиноксидазы. Мощный уратснижающий эффект препарата связан с селективным подавлением двух изоформ ксантиноксидазы. Известно, что фебуксостат образует прочные высокоаффинные связи с активным молибденовым центром как окисленной, так и восстановленной изоформ ксантиноксидазы. Аллопуринол образует комплексы только с восстановленной изоформой фермента. Поскольку обе изоформы ксантиноксидазы, легко обмениваясь ионами молибдена, могут быстро переходить из одной в другую, это позволяет энзиму ускользать от эффекта аллопуринола. На фоне приема аллопуринола восстановленная форма фермента, под действием спонтанной реоксидации молибденового центра, способна очень быстро реактивироваться. Для фебуксостата характерно длительное и плотное заполнение узких каналов, ведущих к молибденовому центру, обеспечивающее прочность связей и устойчивость энзима к действию каскада окислительных кофакторов. Наконец, фебуксостат, в отличие от аллопуринола, не вступает в иные пуриновые и пиримидиновые реакции, что обеспечивает его селективность и адресное воздействие на синтез МК [51].
Важным преимуществом фебуксостата является смешанный (печеночный и почечный) метаболизм. В отличие от аллопуринола, препарат не требует корректировки дозы у пациентов с легкой или умеренной почечной недостаточностью и общей коморбидностью, которая с высокой частотой отмечается у пациентов с подагрой [52]. Недавние исследования показали, что эффективность и безопасность фебуксостата сохраняется у пациентов с клиренсом креатинина ниже 30 мл/мин [53]. Между тем Европейское агентство лекарственных средств (European Medicines Agency, ЕМА) рекомендует взвешенный подход к титрованию дозы фебуксостата пациентам со сниженной (< 30 мл/мин) скоростью клубочковой фильтрации [54].
В ходе масштабных клинических исследований (APEX, FACT, CONFIRMS, CACTUS, FORTE) фебуксостат доказал более мощный, чем у аллопуринола или плацебо, эффект [55].
В рандомизированном двойном слепом многоцентровом исследовании (с общей численностью больных 760 человек, у 35% из которых имелось легкое или умеренное снижение почечной функции) 52?недельная терапия фебуксостатом в дозах, одобренных для использования в ЕС (80 и 120 мг/день), была значительно более эффективной в отношении снижения сывороточного уровня МК у пациентов с гиперурикемией и подагрой, чем аллопуринол, в дозах, обычно назначаемых в клинической практике (100–300 мг/день). Так, целевого уровня МК (< 360 мкмоль/л) достигли 53% пациентов, принимавших 80 мг фебуксостата, 62% больных, принимавших 120 мг фебуксостата, и 21% принимавших 300 мг аллопуринола (р < 0,001) [56].
Фебуксостат продемонстрировал большую эффективность в снижении урикемии, чем аллопуринол, у пациентов с почечной недостаточностью. Так, в ходе 28?недельного многоцентрового двойного слепого исследования III фазы CONFIRMS с участием 2269 пациентов с подагрой, которые были рандомизированы на 4 группы терапии в зависимости от функции почек: фебуксостат в дозах 40 мг/сут и 80 мг/сут и аллопуринол в дозах 200 мг/сут и 300 мг/сут, было обнаружено, что применение аллопуринола в 300 мг/сут и фебуксостата в дозе 40 мг/сут способствует достижению целевого уровня МК (< 360 мкмоль/л) более чем в 45% случаев. У пациентов, получавших фебуксостат в дозе 80 мг/сут, результат статистически значимо превосходил результаты в двух других группах — 67% (р < 0,001). Подобные результаты были получены при сравнении групп с различной степенью почечной недостаточности: 72% больных, получавших 80 мг/сут фебуксостата, достигли целевых уровней МК, тогда как в группах, принимавших 40 мг/сут фебуксостата или аллопуринол, таких больных было 50% и 42% соответственно [57].
В 28?недельном двойном слепом клиническом исследовании, которое включало 1067 пациентов с подагрой и гиперурикемией более 480 мкмоль/л, пациенты были рандомизированы на группы фебуксостат (80, 120 или 240 мг/сут), аллопуринол (100 или 300 мг/сут) или плацебо. В группах больных, получавших фебуксостат, подбор дозы осуществлялся без учета функции почек. В группах, получавших аллопуринол, учитывался уровень креатинина. Так, больные с уровнем креатинина менее 1,5 мг/дл принимали 300 мг аллопуринола, а больные с уровнем креатинина от 1,6 до 2,0 мг/дл соответственно 100 мг аллопуринола в сутки. Фебуксостат вне зависимости от дозы показал большую эффективность в поддержании уровней сывороточного уровня МК ниже 360 мкмоль/л по сравнению с аллопуринолом или плацебо. Так, доля пациентов, достигших целевых значений МК на дозе фебуксостата 80 мг, 120 мг и 240 мг, составила соответственно 76%, 87% и 94%, тогда как количество больных, достигших целевого уровня МК на аллопуриноле в суточной дозе 300/100 мг и плацебо, составило соответственно 41% и 1% (р < 0,05 для всех групп фебуксостата по сравнению с аллопуринолом и плацебо) [58].
В исследованиях с длительным периодом наблюдения, 3–5?летнее лечение фебуксостатом поддерживало целевой уровень МК (< 360 мкмоль/л) у большинства пациентов. Одно из самых продолжительных исследований FOCUS продемонстрировало не только высокую эффективность фебуксостата в отношении достижения целевых уровней урикемии, но и обнаружило весьма устойчивую связь между снижением уровня МК и ликвидацией приступов артрита. Причем по мере продолжения терапии фебуксостатом преимущества терапии становились более очевидными [59].
В более позднем ретроспективном исследовании, в котором сравнивалась эффективность фебуксостата и аллопуринола, также была отмечена большая эффективность фебуксостата (40 мг/сут или 80 мг/сут) по сравнению с аллопуринолом (300 мг/сут) в снижении сывороточного уровня МК. Причем исследование показало, что на терапии фебуксостатом клинический эффект достигается быстрее [60].
Переносимость фебуксостата во всех клинических исследованиях была хорошей, а частота нежелательных явлений низкой [58, 61, 62]. Сообщаемые побочные эффекты включали нарушения функции печени, диарею и доброкачественные кожные высыпания, о которых сообщалось примерно у 3% пациентов во время испытаний фазы III. Сообщения о развитии серьезных кожных реакций были крайне редкими [63]. Причем кожные реакции на фебуксостат проявлялись чаще у пациентов с ранее предшествующей кожной непереносимостью аллопуринола. При этом было показано, что повышенный риск кожных реакций у таких пациентов возникает не из-за перекрестной реактивности, а из-за повышенной вероятности того, что любой пациент с аллергической реакцией на известный препарат развивает реакцию кожи на другое лекарственное средство [64]. Было отмечено, что фебуксостат — препарат выбора для пациентов с предшествующей сыпью или реакцией гиперчувствительности на аллопуринол [65], хотя не исключено, что в редких случаях реакция гиперчувствительности на фебуксостат также возможна [66].
Причины отмены также были реже у фебуксостата, за исключением приступов подагры, которые чаще встречались на терапию фебуксостатом (вероятно, из-за более глубокого и более быстрого снижения сывороточного уровня МК при назначении относительно более высоких доз (120–240 мг/сут) препарата).
Препарат применяется в Европе и США с 2008 г. В настоящее время он разрешен к применению в РФ. Рекомендованная доза фебуксостата — 80 мг 1 раз в день. При необходимости доза может быть увеличена до 120 мг в сутки. Общая тактика применения фебуксостата не отличается от таковой при назначении аллопуринола. Лечение фебуксостатом не рекомендуется начинать во время острого артрита.
Профилактика приступов острого артрита при инициации уратснижающей терапии
Увеличение частоты приступов артрита в течение первых недель и даже месяцев после старта уратснижающей терапии происходит независимо от препарата (аллопуринол, фебуксостат) в результате быстрых изменений сывороточного уровня мочевой кислоты [4, 12, 13]. Для профилактики приступов артрита рекомендовано в течение первых 6 месяцев от инициации терапии использовать колхицин в дозе 0,5–1,0 мг/сут или НПВС в низких дозах (с обязательной гастропротекцией при наличии показаний).
В случаях почечной недостаточности или при лечении статинами врач и пациент должны иметь настороженность в отношении потенциальной нейро- и миотоксичности на применение колхицина в качестве средства профилактики острых приступов артрита. Следует также избегать сочетанного назначения ингибиторов Р-гликопротеина (циклоспорин A) или ингибиторов CYP3А4 (кларитромицин, эритромицин, кетоконазол, дилтиазем, верапамил и др.) [67].
Таким образом, современные подходы к лечению подагры позволяют управлять заболеванием при достижении целевых уровней МК в сыворотке крови, опираясь на технологии профилактического консультирования и обучения пациентов, а также применения ингибиторов ксантиноксидазы. Фебуксостат является хорошо исследованным уратснижающим средством, которое обеспечивает эффективную альтернативу аллопуринолу в лечении подагры у широкого круга пациентов.
Литература
- Roddy E., Choi H. Epidemiology of gout // Rheum Dis Clin North Am. 2014; 40: 155–175.
- Mandal A. K., Mount D. B. The molecular physiology of uric acid homeostasis // Annu Rev Physiol. 2015; 77: 323–334.
- Zhang W., Doherty M., Bardin T., Pascual E., Barskova V., Conaghan P. et al. EULAR evidence based recommendations for gout. Part II: management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT) // Ann Rheum Dis. 2006; 65: 1312–1324.
- Khanna D., Fitzgerald J., Khanna P., Bae S., Singh M., Neogi T. et al. American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia // Arthritis Care Res. 2012; 64: 1431–1446.
- Sivera F., Andrés M., Carmona L., Kydd A., Moi J., Seth R. et al. Multinational evidence-based recommendations for the diagnosis and management of gout: integrating systematic literature review and expert opinion of a broad panel of rheumatologists in the 3 e initiative // Ann Rheum Dis. 2014; 73: 328–333.
- Pascual E., Andrés M., Vela P. Gout treatment: should we aim for rapid crystal dissolution? // Ann Rheum Dis. 2013; 72: 635–637.
- Roddy E., Zhang W., Doherty M. Concordance of the management of chronic gout in a UK primary-care population with the EULAR gout recommendations // Ann Rheum Dis. 2007; 66: 1311–1315.
- Pascual E., Sivera F. Why is gout so poorly managed? // Ann Rheum Dis. 2007; 66: 1269–1270.
- Riedel A., Nelson M., Joseph-Ridge N., Wallace K., MacDonald P., Becker M. Compliance with allopurinol therapy among managed care enrollees with gout: a retrospective analysis of administrative claims // J Rheumatol. 2004; 31: 1575–1581.
- Harrold L., Andrade S., Briesacher B., Raebel M., Fouayzi H., Yood R. et al. Adherence with urate-lowering therapies for the treatment of gout // Arthritis Res Ther. 2009; 11: R46.
- Rees F., Jenkins W., Doherty M. Patients with gout adhere to curative treatment if informed appropriately: proof-of-concept observational study // Ann Rheum Dis. 2013; 72: 826–830.
- Richette P., Doherty M., Pascual E., Barskova V., Becce F., Castaneda-Sanabria J. EULAR evidence-based recommendations for the management of gout // Ann Rheum Dis. 2017; 76 (1): 29–42.
- Елисеев М. С. Подагра. В кн.: Российские клинические рекомендации. Ревматология / Под ред. Е. Л. Насонова. М.: ГЭОТАР-Медиа, 2017. С. 372–385.
- Choi H. K., Atkinson K., Karlson E. W., Curhan G. Obesity, weight change, hypertension, diuretic use, and risk of gout in men: the health professionals follow-up study // Arch Intern Med. 2005; 165 (7): 742–748.
- Dessein P. H., Shipton E. A., Stanwix A. E., Joffe B. I., Ramokgadi J. Beneficial effects of weight loss associated with moderate calorie/carbohydrate restriction, and increased proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study // Ann Rheum Dis. 2000; 59 (7): 539–543.
- Timmers S., Konings E., Houtkooper R. H. et al. Calorie restriction-like effects of 30 days of resveratrol supplementation on energy metabolism and metabolic profile in obese humans // Cell. Metab. 2011. Vol. 14 (5). Р. 612–622.
- Сhoi H. K., Atkinson K., Karlson E. W., Willett W., Curhan G. Purine-rich foods, dairy and protein intake, and the risk of gout in men // N Engl J Med. 2004; 350 (11): 1093–1103.
- Dalbeth N., Wong S., Gamble G. D., Horne A., Mason B., Pool B. Acute effect of milk on serum urate concentrations: a randomised controlled crossover trial // Ann Rheum Dis. 2010; 69 (9): 1677–1682.
- Dalbeth N., Ames R., Gamble G. D. et al. Effects of skim milk powder enriched with glycomacropeptide and G600 milk fat extract on frequency of gout flares: a proof-of-concept randomized controlled trial // Ann Rheum Dis. 2012; 71 (6): 929–934.
- Kanbara A., Seyama I. Effect of urine pH on uric acid excretion by manipulating food materials // Nucleosides, Nucleotides Nucleic Acids. 2011; 30 (12): 1066–1071.
- Towiwat P., Li Z. G. The association of vitamin C, alcohol, coffee, tea, milk and yogurt with uric acid and gout // Int J Rheum Dis. 2015; 18 (5): 495–501.
- Choi H. K. Atkinson K, Karlson E. W., Willett W., Curhan G. Alcohol intake and risk of incident gout in men: a prospective study // Lancet. 2004; 363 (9417): 1277–1281.
- Choi H. K., Curhan G. Soft drinks, fructose consumption, and the risk of gout in men: prospective cohort study // BMJ. 2008; 336 (7639): 309–312.
- Choi H. K., Willett W., Curhan G. Fructose-rich beverages and risk of gout in women // JAMA. 2010; 304 (20): 2270–2278.
- Kedar E., Simkin P. A. A perspective on diet and gout // Adv Chronic Kidney Dis. 2012; 19 (6): 392–397.
- Khanna P., Gladue H., Singh M., FitzGerald J., Bae S., Prakash S. et al. Treatment of acute gout: a systematic review. Semin Arthritis Rheum. 2014; 44: 31–38.
- Zhang S., Zhang Y., Liu P., Zhang W., Ma J., Wang J. Efficacy and safety of etoricoxib compared with NSAIDs in acute gout: a systematic review and a meta-analysis // Clin Rheumatol June. 2015; Epub ahead of print.
- Schumacher H., Berger M., Li-Yu J., Pérez-Ruiz F., Burgos-Vargas R., Li C. Efficacy and tolerability of celecoxib in the treatment of acute gouty arthritis: a randomized controlled trial // J Rheumatol. 2012; 39: 1859–1866.
- Van Durme C., Wechalekar M., Buchbinder R., Schlesinger N., van der Heijde D., Landewé R. Non-steroidal anti-inflammatory drugs for acute gout // Cochrane Database Syst Rev. 2014; 9: CD010–120.
- Terkeltaub R. A., Furst D. E., Bennett K., Kook K. A., Crockett R. S., Davis M. W. High versus low dosing of oral colchicine for early acute gout flare: Twenty-four-hour outcome of the first multicenter, randomized, double-blind, placebo-controlled, parallel-group, dose-comparison colchicine study // Arthritis Rheum. 2010; 62 (4): 1060–1068.
- Man C. Y., Cheung I. T., Cameron P. A., Rainer T. H. Comparison of oral prednisolone/paracetamol and oral indomethacin/paracetamol combination therapy in the treatment of acute goutlike arthritis: a double-blind, randomized, controlled trial // Ann Emerg Med. 2007; 49 (5): 670–677.
- Rainer T. H., Cheng C. H., Janssens H. J., Man C. Y., Tam L. S., Choi Y. F. Oral prednisolone in the treatment of acute gout: a pragmatic, multicenter, double-blind, randomized trial // Ann Intern Med. 2016; 164 (7): 464–471.
- Khanna D., Khanna P. P., Fitzgerald J. D., Singh M. K., Bae S., Neogi T. American College of Rheumatology guidelines for management of gout. Part 2: therapy and antiinflammatory prophylaxis of acute gouty arthritis // Arthritis Care Res (Hoboken). 2012; 64 (10): 1447–1461.
- Bernal J. A., Quilis N., Andrés M., Sivera F., Pascual E. Gout: optimizing treatment to achieve a disease cure // Ther Adv Chronic Dis. 2016; 7 (2): 135–144.
- Janssens H. J., Janssen M., van de Lisdonk E. H., van Riel P. L., van Weel C. Use of oral prednisolone or naproxen for the treatment of gout arthritis: a double-blind, randomised equivalence trial // Lancet. 2008; 371 (9627): 1854–1860.
- Richette P., Bardin T. Should prednisolone be first-line therapy for acute gout? // Lancet. 2008; 372 (9646): 1301.
- Федорова А. А., Барскова В. Г., Якунина И. А., Насонова В. А. Кратковременное применение глюкокортикоидов у больных затяжным и хроническим подагрическим артритом. Ч. III. Частота развития нежелательных реакций // Научно-практическая ревматология. 2009; № 2. С. 38–42.
- Qaseem A., Harris R. P., Forciea M. A. Management of acute and recurrent gout: a clinical practice guideline from the american college of physicians // Ann Intern Med. 2017; 166 (1): 58–68.
- McLean L., Becker M. A. The pathogenesis of gout. Rheumatology Fourth Edition. Edited by Hochberg M. C., Silman A. J., Smolen J. S. Phyladelphia, 2008. P. 1813–27.
- Annemans L., Spaepen E., Gaskin M., Bonnemaire M., Malier V., Gilbert T. Gout in the UK and Germany: prevalence, comorbidities and management in general practice 2000–2005 // Ann Rheum Dis. 2008; 67 (7): 1021–1030.
- Pérez-Ruiz F., Alonso-Ruiz A., Calabozo M., Herrero-Beites A., García-Erauskin G., Ruiz-Lucea E. Efficacy of allopurinol and benzbromarone for the control of hyperuricaemia. A pathogenic approach to the treatment of primary chronic gout // Ann Rheum Dis. 1998; 57: 545–549.
- Reinders M., van Roon E., Jansen T., Delsing J., Griep E., Hoekstra M. et al. Efficacy and tolerability of urate-lowering drugs in gout: a randomised controlled trial of benzbromarone versus probenecid after failure of allopurinol // Ann Rheum Dis. 2009; 68: 51–56.
- Jennings C., Mackenzie I., Flynn R., Ford I., Nuki G., De Caterina R. et al. Up-titration of allopurinol in patients with gout // Semin Arthritis Rheum. 2014; 44: 25–30.
- Hande K., Noone R., Stone W. Severe allopurinol toxicity. Description and guidelines for prevention in patients with renal insufficiency // Am J Med. 1984; 76: 47–56.
- Dalbeth N., Kumar S., Stamp L., Gow P. Dose adjustment of allopurinol according to creatinine clearance does not provide adequate control of hyperuricemia in patients with gout // J Rheumatol. 2006; 33: 1646–1650.
- Taylor T., Mecchella J., Larson R., Kerin K., Mackenzie T. Initiation of allopurinol at first medical contact for acute attacks of gout: a randomized clinical trial // Am J Med. 2012; 125: 1126–1134.
- Hill E., Sky K., Sit M., Collamer A., Higgs J. Does starting allopurinol prolong acute treated gout? A randomized clinical trial // J Clin Rheumatol. 2015; 21: 120–125.
- Lin M. S., Day Y. S., Pwu R. F. et al. Risk estimates for drugs suspected of being associated with Stevens-Johnson syndrpme and toxic epidermal necrolysis: a case-control study // Inern Med J. 2005; 35 (3): 188–190.
- Yaylact S., Demir M. V., Temis T. et al. Allopourinol-induced DRESS syndrome // Indian J Pharmacol. 2012; 44 (3): 412–414.
- Елисеев М. С. Современные возможности терапии подагры: «вверх по спирали» или «бег на месте» // Ревматология, травматология, ортопедия. 2017; 2: 20–22.
- Zhao L., Takano Y., Horiuchi Y. Effect of febuxostat, a novel non-purine, selective inhibitor of xantin oxidase (NP-SIXO), on enzymes in purine and perimidine methabolism pathway // Arthr Rheum. 2003; 48 (suppl. 9): 531.
- Richette P., Clerson P., Périssin L., Flipo R., Bardin T. Revisiting comorbidities in gout: a cluster analysis // Ann Rheum Dis. 2015; 74: 142–147.
- Juge P. A., Truchetet M. E., Pillebout E., Ottaviani S., Vigneau C., Loustau C. Efficacy and safety of febuxostat in 73 gouty patients with stage 4/5 chronic kidney disease: A retrospective study of 10 centers // Joint Bone Spine. 2016; 364 p.
- EMA® product information. 2015; Available at: http://www.ema.europa.eu.
- Frampton J. E. Febuxostat: a review of its use in the treatment of hyperuricaemia in patients with gout // Drugs. 2015, Mar; 75 (4): 427–438. DOI: 10. 1007/s40265–015–0360–7.
- Becker M. A., Schumacher H. R., Jr, Wortmann R. L., MacDonald P. A., Eustace D., Palo W. A. Febuxostat compared with allopurinol in patients with hyperuricemia and gout // N Engl J Med. 2005; 353 (23): 2450–2461.
- Becker M. A., Schumacher H. R., Espinosa L. et al. The urate-lowering efficacy and safety of febuxostat in treatment of hyperuricemia of gout: the CONFIRMS treal // Arthritis Res. Ther. 2010; 12 (2): ID R63.
- Schumacher H., Becker M., Wortmann R., Macdonald P., Hunt B., Streit J. et al. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double-blind, parallel-group trial // Arthritis Rheum. 2008; 59: 1540–1548.
- Schumacher H., Becker M., Lloyd E. et al. Febuxostat is the treatment of gout: 5-yr findingsof the FOCUS efficacy and safety study // Rheumatology (Oxford). 2009; 48 (2): 188–194.
- Singh J., Akhras K., Shiozawa A. Comparative effectiveness of urate lowering with febuxostat versus allopurinol in gout: analyses from large U. S. managed care cohort // Arthritis Res Ther. 2015; 17: 120–139.
- Huang X., Du H., Gu J., Zhao D., Jiang L., Li X. et al. An allopurinol-controlled, multicenter, randomized, double-blind, parallel between-group, comparative study of febuxostat in Chinese patients with gout and hyperuricemia // Int J Rheum Dis. 2015; 17: 679–686.
- Tausche A., Reuss-Borst M., Koch U. Urate lowering therapy with febuxostat in daily practice-a multicentre, open-label, prospective observational study // Int J Rheumatol. 2014; 27: 1–6.
- Chou H. Y., Chen C. B., Cheng C. Y., Chen Y. A., Ng C. Y., Kuo K. L. Febuxostat-associated drug reaction with eosinophilia and systemic symptoms (DRESS) // J Clin Pharm Ther. 2015; 40 (6): 689–692.
- Bardin T., Chales G., Pascart T., Flipo R. M., Korng Ea H., Roujeau J. C. Risk of cutaneous adverse events with febuxostat treatment in patients with skin reaction to allopurinol. A retrospective, hospital-based study of 101 patients with consecutive allopurinol and febuxostat treatment // Joint Bone Spine. 2016; 83 (3): 314–317.
- Chohan S. Safety and efficacy of febuxostat treatment in subjects with gout and severe allopurinol adverse reactions // J Rheumatol. 2011; 38: 1957–1959.
- Abeles A. Febuxostat hypersensitivity // J Rheumatol. 2012; 39: 659–671.
- Terkeltaub R. A. Novel evidence-based colchicine dose-reduction algorithm to predict and prevent colchicine toxicity in the presence of cytochrome P450 3 A4/Pglycoprotein inhibitors // Arthritis Rheum. 2011; 63: 2226–2237.
М. И. Шупина1, кандидат медицинских наук
Г. И. Нечаева, доктор медицинских наук, профессор
Е. Н. Логинова, кандидат медицинских наук
ФГБОУ ВО ОмГМУ МЗ РФ, Омск
1 Контактная информация: mshupina@mail.ru
Урсодезоксихолевая кислота (капсулы, 250 мг), инструкция по медицинскому применению РУ № ЛП-003465
Дата последнего изменения: 10.05.2017
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Фармако-терапевтическая группа
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Состав
Состав на одну капсулу
Активное вещество:
Урсодезоксихолевая кислота 250,00 мг
Вспомогательные вещества:
Крахмал кукурузный 72,80 мг
Кремния диоксид коллоидный безводный 1,60 мг
Магния стеарат 0,60 мг
Оболочка капсулы:
Титана диоксид (Е171) 1,92 мг
Желатин 94,08 мг
Описание лекарственной формы
Твердые желатиновые капсулы № 0, корпус и крышечка белого цвета. Содержимое капсул — порошок белого цвета.
Фармакокинетика
Урсодезоксихолевая кислота абсорбируется в тонкой кишке за счет пассивной диффузии (около 90%), а в подвздошной кишке посредством активного транспорта. Максимальная концентрация в плазме крови (С max ) при приеме внутрь 50 мг через 30, 60, 90 мин — 3,8 ммоль/л, 5,5 ммоль/л и 3,7 ммоль/л соответственно. С max достигается через 1–3 ч. Связь с белками плазмы высокая — до 96–99%. Проникает через плацентарный барьер. При систематическом приеме урсодезоксихолевая кислота становится основной желчной кислотой в сыворотке крови и составляет около 48% от общего количества желчных кислот в крови. Терапевтический эффект препарата зависит от концентрации урсодезоксихолевой кислоты в желчи.
Метаболизируется в печени (клиренс при первичном прохождении через печень) в тауриновый и глициновый конъюгаты. Образующиеся конъюгаты секретируются в желчь. Около 50–70% общей дозы препарата выводится желчью. Незначительное количество не всосавшейся урсодезоксихолевой кислоты поступает в толстый кишечник, где подвергается расщеплению бактериями (7‑дегидроксилирование); образующаяся литохолевая кислота частично всасывается из толстой кишки, но сульфатируется в печени и быстро выводится в виде сульфолитохолилглицинового и сульфолитохолилтауринового конъюгата.
Фармакодинамика
Гепатопротекторное средство, оказывает также желчегонное, холелитолитическое, гиполипидемическое и некоторое иммуномодулирующее действие. Обладая высокими полярными свойствами, урсодезоксихолевая кислота образует нетоксичные смешанные мицеллы с аполярными (токсичными) желчными кислотами, что снижает способность желудочного рефлюктата повреждать клеточные мембраны при билиарном рефлюкс‑гастрите и рефлюкс-эзофагите. Кроме того, урсодезоксихолевая кислота образует двойные молекулы, способные включаться в состав клеточных мембран (гепатоцитов, холангиоцитов, эпителиоцитов ЖКТ), стабилизировать их и делать невосприимчивыми к действию цитотоксичных мицелл. Уменьшая концентрацию токсичных для печеночной клетки желчных кислот и стимулируя холерез, богатый бикарбонатами, урсодезоксихолевая кислота эффективно способствует разрешению внутрипеченочного холестаза. Уменьшает насыщенность желчи холестерином за счет угнетения его абсорбции в кишечнике, подавления синтеза в печени и понижения секреции в желчь; повышает растворимость холестерина в желчи, образуя с ним жидкие кристаллы; уменьшает литогенный индекс желчи. Результатом является растворение холестериновых желчных камней и предупреждение образования новых конкрементов. Иммуностимулирующее действие обусловлено угнетением экспрессии антигенов HLA -1 на мембранах гепатоцитов и HLA -2 на холангиоцитах, нормализацией естественной киллерной активности лимфоцитов и др. Достоверно задерживает прогрессирование фиброза у больных с первичным биллиарным циррозом, муковисцидозом и алкогольным стеатогепатитом, уменьшает риск развития варикозного расширения вен пищевода. Урсодезоксихолевая кислота замедляет процессы преждевременного старения и гибели клеток (гепатоцитов, холангиоцитов и др.).
Фармако-терапевтическая группа
Гепатопротекторное средство.
Показания
- неосложненная желчекаменная болезнь (биллиарный сладж, растворение холестериновых желчных камней в желчном пузыре при функционирующем желчном пузыре; профилактика рецидивов камнеобразования пойле холецистэктомии);
- хронические гепатиты различного генеза;
- токсические (в том числе лекарственные) поражения печени;
- алкогольная болезнь печени;
- неалкогольный стеатогепатит;
- первичный билиарный цирроз печени;
- первичный склерозирующий холангит;
- муковисцидоз;
- дискинезия желчевыводящих путей;
- билиарный рефлюкс-гастрит и рефлюкс-эзофагит.
Противопоказания
- гиперчувствительность;
- рентгенположительные (с высоким содержанием кальция) желчные камни;
- нефункционирующий желчный пузырь;
- желчно-желудочный свищ;
- острый холецистит;
- острый холангит;
- цирроз печени в стадии декомпенсации;
- острые инфекционные заболевания желчного пузыря, желчных протоков и кишечника;
- выраженная печеночная и/или почечная недостаточность;
- обструкция желчевыводящих путей;
- эмпиема желчного пузыря;
- детский возраст до 3-х лет.
С осторожностью
Хотя урсодезоксихолевая кислота не имеет возрастных ограничений в применении, с осторожностью применяют препарат у детей в возрасте от 3-х до 4-х лет, т.к. возможно затруднение при проглатывании капсул.
Применение при беременности и кормлении грудью
Женщинам детородного возраста в период применения препарата рекомендуется применять негормональные средства контрацепции. Применение урсодезоксихолевой кислоты при беременности возможно только в том случае, когда ожидаемая польза для матери превышает потенциальный риск для плода. Данные о выделении урсодезоксихолевой кислоты с грудным молоком в настоящее время отсутствуют. При необходимости применения урсодезоксихолевой кислоты в период лактации следует решить вопрос о прекращении грудного вскармливания.
Способ применения и дозы
Внутрь, не разжевывая, запивая достаточным количеством воды.
При диффузных заболеваниях печени, желчекаменной болезни (холестериновые желчные камни и билиарный сладж): в суточной дозе от 10 мг/кг массы тела до 12–15 мг/кг массы тела (2–5 капсул) непрерывно в течение длительного времени (от нескольких мес до нескольких лет). При диффузных заболеваниях печени суточная доза препарата делится на 2–3 приема, капсулы принимают вместе с едой. При желчекаменной болезни вся суточная доза принимается однократно на ночь. Продолжительность приема препарата для растворения камней — до полного растворения плюс еще 3 мес для профилактики рецидивов камнеобразования.
Для растворения холестериновых камней желчного пузыря рекомендуемая доза урсодезоксихолевой кислоты составляет 10 мг на 1 кг массы тела в сутки, что соответствует:
| Масса тела | Суточная доза |
| До 60 кг | 500 мг (2 капсулы) |
| 61–80 кг | 750 мг (3 капсулы) |
| 81–100 кг | 1000 мг (4 капсулы) |
| Свыше 100 кг | 1250 мг (5 капсул) |
При билиарном рефлюкс-гастрите и рефлюкс-эзофагите : по 250 мг (1 капсула) в сутки, перед сном. Курс лечения — от 10–14 дней до 6 мес., при необходимости до 2-х лет.
При холецистэктомии, для профилактики повторного холелитиаза, рекомендуемая доза — 250 мг 2 раза в сутки в течение нескольких мес.
При токсических, лекарственных поражениях печени, алкогольной болезни печени и атрезии желчных путей: суточная доза по 10–15 мг/кг массы тела в 2–3 приема. Курс лечения — 6–12 мес. и более.
При первичном билиарном циррозе: по 10–15 мг/кг/сут (при необходимости до 20 мг/кг) в 2–3 приема. Курс лечения — от 6 мес до нескольких лет.
Рекомендуется следующий режим дозирования:
| Масса тела | Суточная доза | Утром | Днем | Вечером |
| 47–62 кг | 750 мг (3 капсулы) | 1 капсула | 1 капсула | 1 капсула |
| 63–78 кг | 1000 мг (4 капсулы) | 1 капсула | 1 капсула | 2 капсулы |
| 79–93 кг | 1250 мг (5 капсул) | 1 капсула | 2 капсулы | 2 капсулы |
| 94–109 кг | 1500 мг (6 капсул) | 2 капсулы | 2 капсулы | 2 капсулы |
| Свыше 100 кг | 1750 мг (7 капсул) | 2 капсулы | 2 капсулы | 3 капсулы |
При первичном склерозирующем холангите: по 12–15 мг/кг/сут (до 20 мг/кг) в 2–3 приема. Курс лечения — от 6 мес до нескольких лет.
При неалкогольном стеатогепатите: по 13–15 мг/кг/сут в 2–3 приема. Курс лечения — от 6 мес до нескольких лет.
При муковисцидозе: по 20–30 мг/кг/сут в 2–3 приема. Курс лечения — от 6 мес до нескольких лет.
Детям в возрасте старше 3-х лет препарат назначают индивидуально из расчета 10–20 мг/кг/сут.
Побочные действия
Боль в спине, эпигастральной области и правом подреберье, тошнота, рвота, диарея (может быть дозозависимой), запор, преходящее (транзиторное) повышение активности «печеночных» трансаминаз, аллергические реакции, редко (>0,01% и <0,1%) — кальцинирование желчных камней, обострение ранее имевшегося псориаза, алопеция.
Взаимодействие
Колестимарин, колестипол и антациды, содержащие алюминия гидроксид или алюминия оксид, снижают абсорбцию урсодезоксихолевой кислоты в кишечнике и, таким образом, уменьшают ее всасывание и эффективность. Если же использование препаратов, содержащих хотя бы одно из этих веществ, все же является необходимым, их нужно принимать минимум за 2 ч до приема препарата урсодезоксихолевой кислоты.
Урсодезоксихолевая кислота может усилить всасывание циклоспорина из кишечника. Поэтому у больных, принимающих циклоспорин, врач должен проверить концентрацию циклоспорина в крови и скорректировать дозу циклоспорина в случае необходимости.
В отдельных случаях урсодезоксихолевая кислота может снижать всасывание ципрофлоксацина.
Гиполипидемические лекарственные средства (особенно клофибрат), эстрогены, неомицин и прогестины увеличивают насыщение желчи холестерином и могут снижать способность растворять холестериновые желчные конкременты.
Передозировка
Случаев передозировки не выявлено. В случае передозировки проводят симптоматическое лечение.
Особые указания
Для успешного растворения необходимо, чтобы камни были чисто холестериновые, размером не более 15–20 мм, желчный пузырь заполнен камнями не более чем на половину и желчевыводящие пути полностью сохраняли свою функцию.
При назначении с целью растворения желчных камней необходим контроль активности «печеночных» трансаминаз и щелочной фосфатазы, γ-глутаминтрансферазы, концентрации билирубина. Холецистографию следует проводить каждые 4 недели в первые 3 мес лечения, в дальнейшем — каждые 3 мес. Контроль эффективности лечения проводить каждые 6 мес в ходе УЗИ в течение первого года терапии.
При сохранении повышенных показателей препарат следует отменить. После полного растворения конкрементов рекомендуется продолжить применение в течение по крайней мере 3 мес, для того чтобы способствовать растворению остатков конкрементов, размеры которых слишком малы для их обнаружения и для профилактики рецидива камнеобразования. Если в течение 6–12 мес после начала терапии частичного растворения конкрементов не произошло, маловероятно, что лечение будет эффективным. Обнаружение во время лечения не визуализируемого желчного пузыря является свидетельством того, что полного растворения конкрементов не произошло, и лечение следует прекратить.
Влияние на способность управлять автотранспортом или работать с механизмами
Не имеется данных о влиянии урсодезоксихолевой кислоты на способность управлять автотранспортом и работать с механизмами.
Форма выпуска
Капсулы 250 мг. По 10 капсул в контурной ячейковой упаковке. По 1, 2, 3, 5 или 10 контурных ячейковых упаковок вместе с инструкцией по применению в пачке из картона.
Условия отпуска из аптек
Условия хранения
В защищенном от света месте, при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять препарат после истечения срока годности, указанного на упаковке.
Заказ в аптеках
Выбор региона:
| Название препарата | Цена за упак., руб. | Аптеки |
|---|---|---|
|
Урсодезоксихолевая кислота, капсулы, |
||
|
625.00 |
|
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Отзывы


или
Где проводится: Тонус
Срок выполнения: 1-2 рабочих дня
300 Р
+ Забор материала 300 руб.
- Описание
- Подготовка
- Показания
- Интерпретация результатов
Мочевая кислота — продукт распада пуринов, которые являются структурными элементами нуклеиновых кислот. Удаление ее из организма способствует удалению из организма лишнего азота.
Мочевая кислота выделяется преимущественно через ЖКТ и с помощью почек в составе мочи. В крови мочевая кислота представлена в виде соли, соединена с натрием. Уровень мочевой кислоты в анализе зависит от синтеза и возможностей организма её выведения.
У здоровых людей, потребляющих пищу с большим содержанием пуринов, концентрация мочевой кислоты в анализе повышается. К таким продуктам относятся: мясо, почки, печень, пиво, вино, а также бобовые. При снижении употребления этих продуктов в пищу, уровень мочевой кислоты в анализе снижается. Уровень мочевой кислоты в крови различается по возрасту: у детей показатель ниже. Как правило, у мужчин содержание данного азотистого соединения выше, чем у женщин, но после 60 лет показатели выравниваются.
При подагре наблюдается нарушение пуринового обмена и в результате — повышение уровня в крови мочевой кислоты. Это приводит к повреждениям тканей организма. При этом кристаллы данного вещества откладываются в жидкости, заполняющей полости суставов, что приводит к характерной клинической картине подагры.
Снижение функции почек приводит к снижению выделения мочевой кислоты с мочой и задержке ее в системном кровотоке. Таким образом, необходимо сдать анализ на мочевую кислоту в сыворотке при хронических патологиях почек, приводящих к нарушениям их функции. Отложение уратов в мочевыделительной системе вследствие повышения концентрации мочевой кислоты в крови приводит к образованию конкрементов.
Мочевая кислота в сыворотке может возрастать при применении цитостатиков, особенно это выражено при распространенном опухолевом процессе, когда огромное количество опухолевых клеток гибнет. Иногда этиология увеличения концентрации мочевой кислоты в сыворотке крови остается неизвестной.
Сдать анализ на мочевую кислоту в сыворотке крови следует утром–с восьми до одиннадцати часов. Перед взятием крови следует не употреблять пищу в течение 8-14 часов, не нагружать себя пищей накануне исследования. Вода разрешается.
За несколько дней до анализа на мочевую кислоту в сыворотке следует снизить употребление пищи с высоким содержанием пуриновых оснований, не употреблять алкоголь.
Сдать анализ на мочевую кислоту в крови следует для:
- Диагностики подагры
- Определения этиологии мочекаменной болезни
- Оценки функции почек
- Диагностики лимфопролиферативных заболеваний
Повышение концентрации мочевой кислоты в крови наблюдается при:
- Подагре
- Почечной недостаточности различной генеза
- Гемобластозах, миеломной болезни, лимфомах
- Употреблении алкогольных напитков
- Усилении катаболизма при опухолях
- Токсикозе беременных
- B12 – дефицитной анемии
- Приеме лекарственных препаратов: салицилатов, цитостатических препаратов, диуретиков.
- Голодании
- Синдроме Леша – Нихана
- Тяжелой физической нагрузке, высокопуриновой диете
- Идиопатической семейной гиперурикемии
Снижение концентрации мочевой кислоты в крови наблюдается при:
- Болезни Вильсона
- Употреблении пищи, преимущественно с низким содержанием пуринов
- Ксантинурии
- Лимфогранулематозе
- Синдроме Фанкони
- Приеме ЛС (аллопуринол, ГКС, азатиоприн, рентгеноконтрастных средств)
- Патологии проксимальных канальцев почек.