Все новости о наличии вакцины Спутник М будут в первую очередь публиковаться в наших группах Вконтакте и в Телеграм, добавляйтесь в группы!
Инструкция по применению Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Отпускается по рецепту
Лекарственные формы вакцины Спутник М
раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент II
Международное непатентованное название
Вакцина для профилактики COVID-19
Состав Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Состав на 1 дозу: Компонент I содержит: Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0±1,5) х 10(10) частиц. Вспомогательные вещества: трис (гидроксиметил) аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат 80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол (спирт этиловый) 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Группа: Вакцины
Производители: НИЦЭМ им. Н.Ф. Гамалеи (Медгамал)(Россия)
Показания к применению Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Профилактика COVID-19 у подростков в возрасте от 12 до 17 лет (включительно).
Способ применения и дозировка Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом I в дозе 0,5 мл, затем, через 3 недели — компонентом II в дозе 0,5 мл. После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Перед иммунизацией флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона! Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту. Не допускается хранение размороженного препарата! Повторное замораживание не допускается!
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата, путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Противопоказания Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
- Гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания,
- обострение хронических заболеваний — вакцинацию проводят через 2-4 недели после выздоровления или наступления ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры; возраст до 12 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента II:
- тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура тела выше 40 °С и т.п.) на введение компонента I вакцины.
Фармакологическое действие
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2. Иммунологические свойства и безопасность вакцины изучали в клиническом исследовании у добровольцев обоего пола в возрасте от 12 до 17 лет включительно. Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: уровень сероконверсии составил 100 %. Иммунизация препаратом Гам-КОВИД-Вак-М формирует антиген-специфический клеточный противоинфекционный иммунитет у 93,2 % обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНгамма). Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Побочное действие Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией; общим недомоганием; утомляемость, головная боль) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции. Реже отмечаются: тошнота, диспепсия, иногда — заложенность носа увеличение регионарных лимфоузлов, паническая атака. У некоторых пациентов возможно развитие аллергических реакций, кратковременное изменение лабораторных показателей крови повышение уровня билирубина, снижение уровня нейтрофилов) в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак-М после вакцинации были зарегистрированы следующие НЯ: «Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения. Частота развития — очень часто и часто. «Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: заложенность носа. Частота развития — редко. «Нарушения со стороны нервной системы»: головная боль; головокружения — редко. «Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия — редко. «Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей. Все НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось. Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок. Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени. Специфических антидотов к препарату не существует. Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства. Взаимодействие с другими лекарственными средствами Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Взаимодействие Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2 раствор для инъекций 0,5 мл/доза (1 доза) 0,5мл компонент I
Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Особые указания
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах. Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов: с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний); со злокачественными новообразованиями. Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Отсутствует опыт клинического применения Гам-КОВИД-Вак-М при беременности.
Согласно результатам изучения репродуктивной токсичности на животных не установлено отрицательного влияния на течение беременности, эмбриофетальное развитие (на самках) и пренатальное развитие потомства. В связи с этим применять препарат Гам-КОВИД-Вак- М при беременности следует только в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22-х недель беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак-М у женщин, кормящих грудью, и младенцев отсутствуют. В настоящий момент нет данных выделяется ли вакцина с молоком. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации. У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц. Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Условия хранения
Хранить в защищенном от света месте, при температуре не выше минус 18 С. Повторное замораживание не допускается. Хранить в недоступном для детей месте. Условия транспортирования: при температуре не выше минус18 С.
Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2
Регистрационный номер
Торговое наименование
Гам-КОВИД-Вак-М
Международное непатентованное наименование
Лекарственная форма
раствор для внутримышечного введения
Состав
Состав на 1 дозу.
Компонент Ⅰ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0 ± 1,5) × 1010 частиц.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат 80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол (спирт этиловый) 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Компонент Ⅱ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 5 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0 ± 1,5) × 1010 частиц.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат-80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол (спирт этиловый) 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Описание
Компонент Ⅰ. Раствор замороженный — плотная затвердевшая беловатого цвета масса.
После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент Ⅱ. Раствор замороженный — плотная затвердевшая беловатого цвета масса.
После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путём, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент Ⅰ и компонент Ⅱ.
В состав компонента Ⅰ входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S-вируса SARS-CoV-2, в состав компонента Ⅱ входит вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммуногенность
Иммунологические свойства и безопасность вакцины изучали в клиническом исследовании у добровольцев обоего пола в возрасте от 12 до 17 лет включительно.
Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: уровень сероконверсии составил 100 %.
Иммунизация препаратом Гам-КОВИД-Вак-М формирует антиген-специфический клеточный противоинфекционный иммунитет у 93,2 % обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания
Профилактика COVID-19 у подростков в возрасте от 12 до 17 лет (включительно).
Противопоказания
- Гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжёлые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2–4 недели после выздоровления или наступления ремиссии. При нетяжёлых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры;
- возраст до 12 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента Ⅱ:
- тяжёлые поствакцинальные осложнения (анафилактический шок, тяжёлые генерализованные аллергические реакции, судорожный синдром, температура тела выше 40 °C и т.п.) на введение компонента Ⅰ вакцины.
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжёлых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Отсутствует опыт клинического применения Гам-КОВИД-Вак-М при беременности. Согласно результатам изучения репродуктивной токсичности на животных не установлено отрицательного влияния на течение беременности, эмбриофетальное развитие (на самках) и пренатальное развитие потомства. В связи с этим применять препарат Гам-КОВИД-Вак-М при беременности следует только в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22-х недель беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак-М у женщин, кормящих грудью, и младенцев отсутствуют. В настоящий момент нет данных выделяется ли вакцина с молоком. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом Ⅰ в дозе 0,5 мл, затем, через 3 недели — компонентом Ⅱ в дозе 0,5 мл.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Перед иммунизацией флакон с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
▼ Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи, с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путём внесения информации в соответствующей раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно лёгкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, утомляемость, головная боль) и местные (болезненность в месте инъекции, гиперемия, отёчность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Реже отмечаются: тошнота, диспепсия, иногда — заложенность носа увеличение регионарных лимфоузлов, паническая атака. У некоторых пациентов возможно развитие аллергических реакций, кратковременное изменение лабораторных показателей крови повышение уровня билирубина, снижение уровня нейтрофилов) в сыворотке крови.
В рамках проведённых клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак-М после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отёк, зуд в месте вакцинации, астения. Частота развития — очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: заложенность носа. Частота развития — редко.
«Нарушения со стороны нервной системы»: головная боль; головокружения — редко.
«Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия — редко.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей. Все НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебнопрофилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжёлой степени. Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому приём препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
▼ Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объёма клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном законодательством порядке.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, компонент Ⅰ — 0,5 мл/доза + компонент Ⅱ — 0,5 мл/доза, 6 месяцев.
По 0,5 мл (1 доза) каждого компонента препарата во флаконы нейтрального стекла, герметично укупоренные пробками из резины, обжатые алюмопластиковыми колпачками.
1 флакон компонента Ⅰ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного; 1 флакон компонента Ⅱ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
По 5 флаконов компонента Ⅰ или компонента Ⅱ помещают в контурную ячейковую упаковку из плёнки поливинилхлоридной. По 1 или 2 контурные ячейковые упаковки с компонентом Ⅰ или компонентом Ⅱ вместе с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
Хранение
Хранить в защищённом от света месте, при температуре не выше минус 18 °C. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Условия транспортирования
При температуре не выше минус 18 °C.
Срок годности
Компонент Ⅰ — 6 месяцев. Компонент Ⅱ — 6 месяцев.
Не применять по истечении срока годности.
Условия отпуска из аптек
Для лечебно-профилактических и санитарно-профилактических учреждений.
Производитель
Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ),
Российская Федерация
Производитель
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
Выпускающий контроль качества
Филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России, Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почётного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации (ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России).
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Тел: 8 499-193-30-01, факс: 8 499-193-61-83.
E-mail: info@gamaleya.org
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 (Gam-COVID-Vac Combined vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus) инструкция по применению
📜 Инструкция по применению Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
💊 Состав препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
✅ Применение препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
📅 Условия хранения Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
⏳ Срок годности Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Описание лекарственного препарата
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
(Gam-COVID-Vac Combined vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus)
Основано на официально утвержденной инструкции по применению препарата и подготовлено для электронного издания справочника Видаль 2020 года, дата обновления: 2022.04.15
Владелец регистрационного удостоверения:
Код ATX:
J07BX03
(Вакцины против COVID-19)
Лекарственные формы
| Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 |
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
|
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): амп. 5 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/1 доза (жидкий препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/1 доза (жидкий препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): амп. 5 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 1.0 мл/2 дозы (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 1.0 мл/2 дозы (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (замороженный препарат): фл. 1 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (замороженный препарат): фл. 1 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (жидкий препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (жидкий препарат): фл. 1 шт. рег. №: ЛП-006395 |
Раствор для в/м введения (компонент I* и компонент II).
Замороженный препарат
Компонент I*. Раствор замороженный — плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
* Идентичен составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
0.5 мл (1 доза компонента I) — флаконы (1) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1, 2, 5, 10) — пачки картонные.
3.0 мл (5 доз компонента I) — флаконы (типа 10R) (1) — пачки картонные.
3.0 мл (5 доз компонента I) — флаконы (типа 10R) (10) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (типа 6R) (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (1) — пачки картонные с держателем.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
Компонент II. Раствор замороженный — плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
0.5 мл (1 доза компонента II) — флаконы (1) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (5) — упаковки ячейковые контурные (2) — пачки картонные.
3.0 мл (5 доз компонента II) — флаконы (типа 10R) (1) — пачки картонные.
3.0 мл (5 доз компонента II) — флаконы (типа 10R) (10) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (типа 6R) (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (1) — пачки картонные с держателем.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
Жидкий препарат
Компонент I*. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
* Идентичен составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
3.0 мл (5 доз компонента I) — флаконы (1) — пачки картонные с держателем.
3.0 мл (5 доз компонента I) — флаконы (1) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (типа 6R) (1) — пачки картонные×.
Компонент II. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
3.0 мл (5 доз компонента II) — флаконы (1) — пачки картонные с держателем.
3.0 мл (5 доз компонента II) — флаконы (1) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (типа 6R) (1) — пачки картонные×.
× На флаконы каждого компонента препарата наклеивают этикетку самоклеящуюся.
Фармакологическое действие
Характеристика. Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент I и компонент II.
В состав компонента I входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2, что соответствует составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
В состав компонента II входит рекомбинантный аденовирусный вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев: средний геометрический титр у добровольцев, иммунизированных Гам-КОВИД-Вак, на 42 день составил 9009.0, а на 180 день — 1708.0.
В группе Плацебо средний геометрический титр на 42 день составил 55.6, а на 180 день — 110.2. Сероконверсия к 42 дню наблюдается у 99.1% вакцинированных добровольцев и сохраняется к 180 дню у 93.9%.
У добровольцев на 42 сутки после вакцинации отмечается достоверное увеличение вируснейтрализующих антител в сыворотке крови, который сохраняется и на 180 день.
Иммунизация препаратом Гам-КОВИД-Вак формирует напряженный антиген-специфический клеточный противоинфекционный иммунитет практически у всех обследованных добровольцев (формирование антиген-специфичных клеток обеих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
По данным III фазы рандомизированного плацебо контролируемого клинического исследования эффективность вакцины составляет более 91% для дикого штамма (Ухань) и по результатам полученным через полгода в условиях доминирования штамма дельта — 70.5% от симптомов коронавирусной инфекции. Таким образом, иммунизация достоверно снижает вероятность заболевания. В отношении среднетяжелых, тяжелых и очень тяжелых случаев эффективность составляет более 88% в течении полугодового периода наблюдения
По результатам опубликованных данных применения вакцины за рубежом, в рамках клинической практики в Венгрии на ноябрь 2021 у 820560 вакцинированных, показана 85.7% эффективность векторной вакцины Спутник-V. Эффективность против смерти, связанной с COVID-19, варьировала от 95.4% до 100% в разных возрастных когортах, демонстрируя очень высокую и стойкую эффективность как в старшей, так и в младшей возрастных когортах.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10-й день (препаратом Спутник Лайт, соответствующего компоненту I препарата Гам-КОВИД-Вак), что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания. С учетом рекомендаций ВОЗ для достижения уровня коллективного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID-19 по эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в т.ч. у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
Показания препарата
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Режим дозирования
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом I дозе 0.5 мл, затем, через 3 недели — компонентом II в дозе 0.5 мл.
Допускается, при необходимости, однократная вакцинация компонентом I в дозе 0.5 мл.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконов) и АО «Биннофарм» (ампул) и АО «Р-Фарм» (флаконов)
Перед вакцинированием флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Вскрывают ампулу по цветной точке.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт- УфаВИТА» (флаконы, ампулы) и ЗАО «ЛЕККО» (флаконы)
Замороженный препарат
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается! Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Ампулу вскрывают по кольцу и/или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0.5 мл!
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа; невскрытой ампулы — не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0.5 мл. Одному пациенту вводить 1 дозу (0.5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов
Жидкий препарат
Внимание! Замораживание флакона или ампулы с раствором не допускается! Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом I или II достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37°С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Ампулу вскрывают по кольцу и/или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0.5 мл!
Многодозовые флаконы
Если последующие инъекции по какой- либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Однодозовые ампулы
Содержимое одной ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов
Применение вакцины производства ЗАО «БИОКАД» (флаконов)
Перед вакцинированием флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0.5 мл!
Повторное замораживание не допускается!
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Применение вакцины производства АО «Р- Фарм». компонент I (флаконы) и ООО СПУТНИК ТЕХНОПОЛИС», компонент II (флаконы)
Внимание! К использованию непригоден препарат с дефектами укупорочной системы и/или нарушенной маркировкой флакона, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Многодозовые флаконы. Перед вакцинированием флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0. 5 мл!
Если последующие инъекции по какой- либо причине откладываются, допускается хранение вскрытого или невскрытого размороженного флакона при комнатной температуре не более 2 часов
Повторное замораживание не допускается!
Неиспользованная вакцина подлежит уничтожению.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней.
Частота встречаемости определяется следующим образом: часто (>1/100, <1/10), нечасто (>1/1000, <1/100), редко (>1/10000, <1/1000), очень редко (>1/10000, включая единичные случаи.
Категории частоты были сформированы на основании клинических исследований препарата. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
В рамках проведенных клинических исследований и в рамках фармаконадзора были зарегистрированы следующие нежелательные реакции.
Общие нарушения и реакции в месте введения: часто — гипертермия, боль, отек, зуд в месте вакцинации, озноб, астения; нечасто — пирексия, снижение аппетита.
Желудочно-кишечные нарушения: очень редко — тошнота, рвота, диспепсия.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень редко — заложенность носа, першение в горле, ринорея.
Со стороны кожи и подкожной клетчатки: очень редко — ангиоотек, крапивница и сыпь (эритематозная, папулезная).
Со стороны мышечной, скелетной и соединительной ткани: часто — миалгия, артралгия, скелетно-мышечная боль; нечасто — остеоартрит.
Со стороны иммунной системы: очень редко — анафилактический шок, анафилактическая реакция и гиперчувствительность.
Со стороны крови и лимфатической системы: очень редко — увеличение регионарных лимфоузлов.
Со стороны нервной системы: очень редко — головная боль; головокружения, обмороки; сообщается о единичных случаях воспалительной полиневропатии (причинно-следственная связь с лекарственным препаратом не установлена — частота данных событий в популяции имеет сезонный характер и может быть связана с различными причинами: провоцирующими факторами могут быть инфекционные заболевания вирусной и бактериальной этиологии, хирургические вмешательства, травматическое повреждение периферических нервов, любая вакцинация, аутоиммунные и системные заболевания).
Со стороны органа зрения: нечасто — фотофобия.
Лабораторные и инструментальные данные: разнонаправленные отклонения показателей иммунологического статуса — повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B- лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина E (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A(IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови — увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение СОЭ, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонение показателей биохимического анализа крови — повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови. Отклонения в общем анализе мочи — эритроциты в моче. Большинство нежелательных явлений (НЯ) завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Противопоказания к применению
- гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ- вакцинацию проводят после нормализации температуры;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента II:
- тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура выше 40°С и т.д.) на введение компонента I вакцины.
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и
сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение одного компонента для иммунизации в связи со снижением функции иммунной системы, для формирования иммунного ответа показана полная вакцинация двухкомпонентной вакциной Гам-КОВИД-Вак.
Применение при беременности и кормлении грудью
По результатам исследований на животных, репродуктивная токсичность и тератогенность отсутствуют. Клинические исследования Гам-КОВИД-Вак при беременности не проводились. В связи с этим применять препарат Гам-КОВИД-Вак при беременности следует в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22 недели беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак у женщин, кормящих грудью, и младенцев отсутствуют. В настоящее время неизвестно, способны ли действующие вещества, входящие в состав вакцины, проникать в грудное молоко. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с хроническими заболеваниями печени.
Применение при нарушениях функции почек
С осторожностью применять у пациентов с хроническими заболеваниями почек.
Применение у детей
Противопоказание: возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности.
Особые указания
У пациентов, получающих иммуносупрессивную терапию и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
При принятии врачом (медицинским работником) решения о необходимости одновременного введения Гам-КОВИД-Вак с другой вакциной, не допускается их смешивание в одном шприце и введение в один участок тела.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Лекарственное взаимодействие
Специальных исследований лекарственного взаимодействия не проводилось.
Взаимодействие с вакциной для профилактики гриппа изучено в доклинических исследованиях, показано отсутствие снижения иммуногенности как вакцины Гам-КОВИД-Вак (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2), так и гриппозной вакцины в эксперименте при их одновременном введении. Ожидается отсутствие снижения иммуногенности для расщепленных, субъединичных и полимерсубъединичных гриппозных вакцин.
Не допускается смешивание вакцины Гам-КОВИД-Вак с другими вакцинами или иными лекарственными средствами в одном шприце, т.к. нет данных о фармацевтическом взаимодействии.
Условия хранения препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Замороженный препарат
Производственные площадки ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, ЗАО «БИОКАД», Россия: Компонент I — 1 год. Компонент II — 1 год.
Производственные площадки АО «ГЕНЕРИУМ», Россия, ОАО «Фармстандарт-УфаВИТА», Россия: Компонент I — 9 месяцев. Компонент II — 9 месяцев.
Производственные площадки АО «Биннофарм», Россия, ЗАО «ЛЕККО», Россия: Компонент 1 — 6 месяцев. Компонент II — 6 месяцев.
Производственная площадка АО «Р-Фарм», Россия: Компонент 1-6 месяцев.
Производственная площадка ООО «СПУТНИК ТЕХНОПОЛИС», Россия: Компонент II — 6 месяцев.
Не применять по истечении срока годности.
Хранить в недоступном для детей месте.
Жидкий препарат
Производственные площадки АО «ГЕНЕРИУМ», Россия, ОАО «Фармстандарт-УфаВИТА», Россия: Компонент I — 6 месяцев. Компонент II — 6 месяцев.
Производственные площадки ЗАО «ЛЕККО», Россия, ЗАО «БИОКАД», Россия: Компонент I — 2 месяца. Компонент II — 2 месяца.
Не применять по истечении срока годности
Хранить в недоступном для детей месте.
Условия реализации
Для лечебно-профилактических учреждений.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
В Башкирию завезли первую партию долгожданной вакцины «Спутник М» для вакцинации от коронавируса детей и подростков с 12 лет. Совместно с экспертами Минздрава республики отвечаем на самые главные вопросы родителей, где и как могут ее получить желающие.
Это какая-то новая вакцина? Как узнать ее состав?
«Спутник М» — это старый, добрый, проверенный «Спутник V», разведенный в пять раз. Как и во взрослой вакцине, в нем нет живой и способной к размножению части вируса. Что такое векторная вакцина: ученые взяли хорошо изученный вирус, «кастрировали» его, чтобы тот не мог размножаться, и на освободившееся место вставили «запчасти» вируса, против которого направлена вакцина. Технологии уже несколько десятков лет, так устроены многие другие вакцины. В «Спутнике V» для основы используется аденовирус, вызывающий у человека «простуду». Подробнее мы рассказывали по этой ссылке.
Инструкция и состав есть в публичном доступе, вот ссылка.
Как проверяли эффективность и безопасность вакцины?
Детскую вакцину с лета испытывали в двух столичных клиниках: Морозовской и больнице имени З. А. Башляевой. В первом и втором этапе принимали участие сто волонтеров с 12 до 17 лет. Им вводили препарат дважды с интервалом в три недели, только в условиях стационара. Первая группа получила одну десятую часть взрослой дозы, вторая — одну пятую. По итогам врачи приняли решение остановиться на дозировке 1/5. Третий этап проходил уже в 12 поликлиниках Москвы, в нем принимали участие 3000 подростков: 2400 получили вакцину, 600 – плацебо.
Вот что показали исследования: в целом подростки реагируют на вакцину хорошо. Единственный побочный эффект «Спутника М» – повышение температуры максимум до 37,4 градуса. В редких случаях ныло место укола, появилась заложенность носа, головная боль и нарушения со стороны желудочно-кишечного тракта. Максимум в течение двух-трех дней все симптомы пропадали. Вакцина безопасная, ее эффективность около 93%. Проще говоря, у девяти из десяти подростков образуются антитела, защищающие от заражения коронавирусом, а также длительный Т-клеточный иммунный ответ.
Как будет проходить вакцинация?
Вакцинация подростков будет добровольная. Если вы решили оградить ребенка от ковида, нужно будет написать согласие. Дети после 15 лет могут подписать его самостоятельно.
Вводить препарат, как и «оригинальный», будут дважды.
После вакцинации нужно будет полчаса посидеть в поликлинике под присмотром врачей, чтобы не было никаких реакций.
Пока получить вакцину можно будет только в поликлиниках по месту жительства. Когда откроются новые точки, мы обязательно расскажем.
Минздрав РФ заявил, что вакцинация рекомендована всем школьникам начиная с 12 лет, но в первую очередь — ослабленным детям, имеющим хронические заболевания.
Где-нибудь в мире уже прививают детей?
Да, вакцинация идет уже более чем в сорока странах. Тинейджерам делают прививки в США, странах Евросоюза, Канаде, Австралии, Израиле и многих других. В Америке привили больше половины подростков.
Первой страной, где разрешили прививать маленьких детей, стал Китай: в июле прошлого года власти одобрили использование препаратов для вакцинации начиная с трех лет и уже вакцинировали ими почти сто миллионов человек.
Какие у прививки противопоказания
Противопоказания у «Спутника М» похожи на те, что у «Спутника V»:
Аллергия на компоненты вакцины. В первую очередь на полиэтиленгликоль.
Тяжелые аллергические реакции в прошлом, анафилаксия. Это когда после введения аллергена отекают губы, язык и горло, становится тяжело дышать.
Анафилактический шок или судорожный синдром после введения первого компонента вакцины.
Простуда, грипп или другие заболевания. Делать вакцину можно только через 2-4 недели после исчезновения симптомов. При нетяжелой простуде или вирусной кишечной инфекции – сразу после снижения температуры.
При хронических заболеваниях почек, печени, нарушениях функции щитовидной железы, сахарном диабете, эпилепсии, серьезном сердечно-сосудистом заболевании вроде миокардита, болезни кроветворения, остром нарушении мозгового кровообращения, аутоиммунном или онкологическом заболевании, перед прививкой нужно обязательно проконсультироваться с врачом.
Что с прививками для детей до 12 лет?
Их пока нет, разработка в России только-только началась. Минздрав России уже одобрил проведение всех фаз клинических исследований вакцины от коронавируса для детей на базе «Спутника». В нем примут участие 2,3 тысячи пациентов. Как пишет ТАСС, испытания пройдут на базе трех московских медицинских учреждений: в Морозовской детской городской клинической больнице, Детской городской клинической больнице имени Башляевой, а также в Первом Московском государственном медицинском университете имени Сеченова. Окончание исследований запланировано на 31 декабря 2023 года.
Пресс-служба Министерства здравоохранения Республики Башкортостан (информация сайта Башинформ)
-
1.
Вакцина от Ковида для детей – Спутник М-
1.1.
Состав вакцины Спутник М -
1.2.
Испытания вакцины от коронавируса для детей и подростков -
1.3.
Эффективность вакцины для клеточного иммунитета -
1.4.
Есть ли другие названия у Спутник М вакцины -
1.5.
Производитель вакцины для детей от 12 лет
-
1.1.
-
2.
Вакцинация детей от коронавируса в России-
2.1.
Когда начнется вакцинация подростков от коронавируса? -
2.2.
Как будет проходить вакцинация детей -
2.3.
Могут ли привить ребенка без ведома родителей -
2.4.
Будет ли вакцинация детей обязательна?
-
2.1.
-
3.
Противопоказания вакцины для детей -
4.
Безопасна ли вакцинация для ребёнка? -
5.
Другие вакцины для детей от COVID-19 -
6.
Что говорят врачи о вакцинации детей и подростков от COVID-19
Вакцинация — надежный способ создать иммунитет, защитить организм от тяжелого течения болезни и развития осложнений. Во всем мире развернута массовая прививочная компания для того, чтобы взять под контроль COVID-19. Рассматривается вопрос о вакцинации детей и подростков.
Важно! Вся информация в статье носит ознакомительный характер и не является руководством к действию. Назначать лечение при COVID-19 должен врач с учетом тяжести заболевания. Самолечение опасно для вашего здоровья!
Вакцина от Ковида для детей – Спутник М
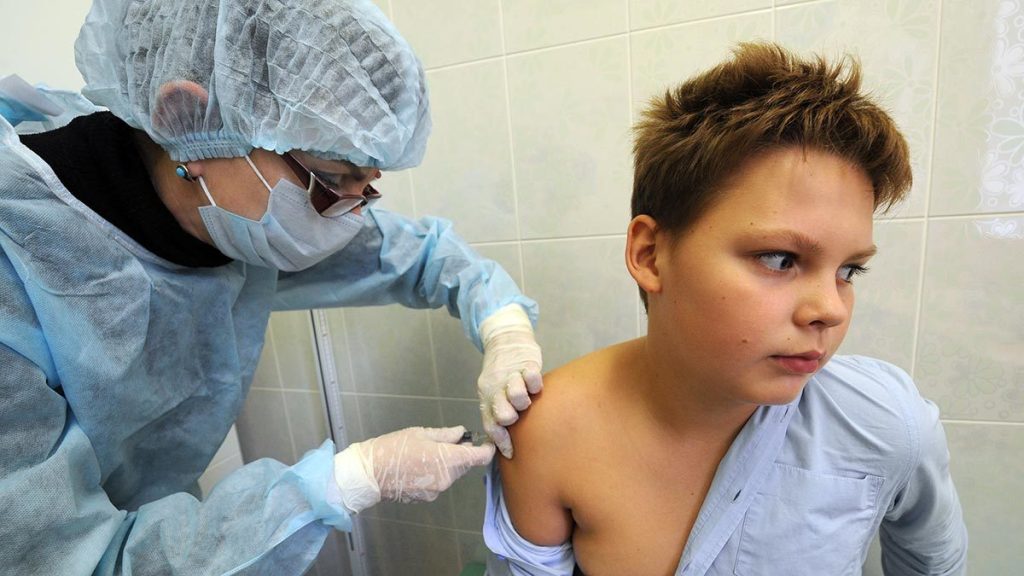
В начале пандемии коронавируса считалось что дети, если и болеют, то переносят инфекцию легко. Однако с приходом нового штамма “дельта” ситуация изменилась. Подростки и дети младшего возраста стали чаще заражаться, переносят болезнь тяжело, с высокой температурой, сильным поражением легких и постковидным синдромом.
Снизить вероятность инфицирования и уменьшить риск развития осложнений можно с помощью вакцинации. Гам-Ковид-Вак V (Спутник V) стала одной из первых противокоронавирусных вакцин в мире зарегистрированных для иммунизации лиц младше 18 лет. В 2021 году стартует вакцинация детей в России препаратом Спутник М.
Состав вакцины Спутник М
Вещество представляет собой обезвреженные частицы аденовирусов из которых был удален генетический материал и вживлен ген, ответственный за кодирование шип-белка коронавируса. Вакцина Спутник для подростков разработана специалистами Национального исследовательского центра эпидемиологии и микробиологии имени Н. Ф. Гамалеи.
Поскольку вектор лишен гена размножения, он не способен вызвать заболевание у привитого человека, а лишь доставляет в организм генетический материал вируса, против которого делается прививка. После проникновения чужеродных частиц в клетку происходит синтез S-белка коронавируса, что приводит к выработке специфических антител.
Через 21 день необходима повторная вакцинация, которая призвана усилить иммунный ответ. Для того чтобы иммунная система, уже столкнувшаяся с векторными частицами первого компонента вакцины, не привела к инактивации препарата, во втором компонента используются генетически модифицированные аденовирусы другого штамма. Применение двух различных вариантов векторов позволит увеличить шансы на успешную доставку белка коронавируса в клетку и запустит иммунную реакцию.
Даже если у человека имеется иммунитет к 5-му серотипу аденовируса, компонент, созданный на основе 26-го серотипа, выполнит свою «работу» и приведет к формированию стойкой иммунной защиты.
Спутник М вакцина для детей и подростков по составу является полным аналогом Спутника V, концентрация которого была снижена в 5 раз. Из-за особенностей работы иммунной системы в детском возрасте, такого количества векторных частиц достаточно, чтобы выработать необходимые антитела.
В состав I компонента Гам-Ковид-Вак-М, входят:
- Рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2.
- Вспомогательные вещества: трис (гидроксиметил) аминометан, натрия хлорид, сахароза, полисорбат, магния хлорида гексагидрат, ЭДТА динатриевая соль дигидрат, этанол 95%, вода для инъекций.
Второй компонент вакцины отличается тем, что содержит модифицированные аденовирусные частицы 5 серотипа, несущие ген S-белка вируса Covid-19.
Испытания вакцины от коронавируса для детей и подростков
Клинические исследования начались летом 2021 года на базе двух московских больниц. С 11 ноября 2021 года препарат находится на третьей фазе испытаний. На этом этапе будет изучено влияние вакцины, возможные побочные эффекты и ее эффективность при участии 3000 подростков: 2400 получат вакцину, 600 – плацебо.
Вакцина от коронавируса для подростков испытывается только на здоровых добровольцах в возрасте от 12 до 17 лет. Детям младшего возраста в настоящее время прививку не делают из-за отсутствия данных об эффективности и безопасности препарата у данной категории населения. Спутник М был зарегистрирован Министерством Здравоохранения Российской Федерации 24 ноября 2021 года.
Эффективность вакцины для клеточного иммунитета
Новая вакцина для детей Спутник М приводит не только к 100% сероконверсии и выработке достаточного количества специфических защитных антител на 42-ой день от начала иммунизации. Но и к формированию стойкого клеточного противоинфекционного иммунитета у 93,2% привитых, что указано в официальной инструкции к препарату.
Эти два вида адаптивной защиты дополняют друг друга и увеличивают шансы успешно противостоять вирусному заболеванию. Гуморальный иммунитет, представленный антителами, нарушает внеклеточные патогены, в то время как клеточный иммунитет разрушает внутриклеточные чужеродные частицы.
Есть ли другие названия у Спутник М вакцины
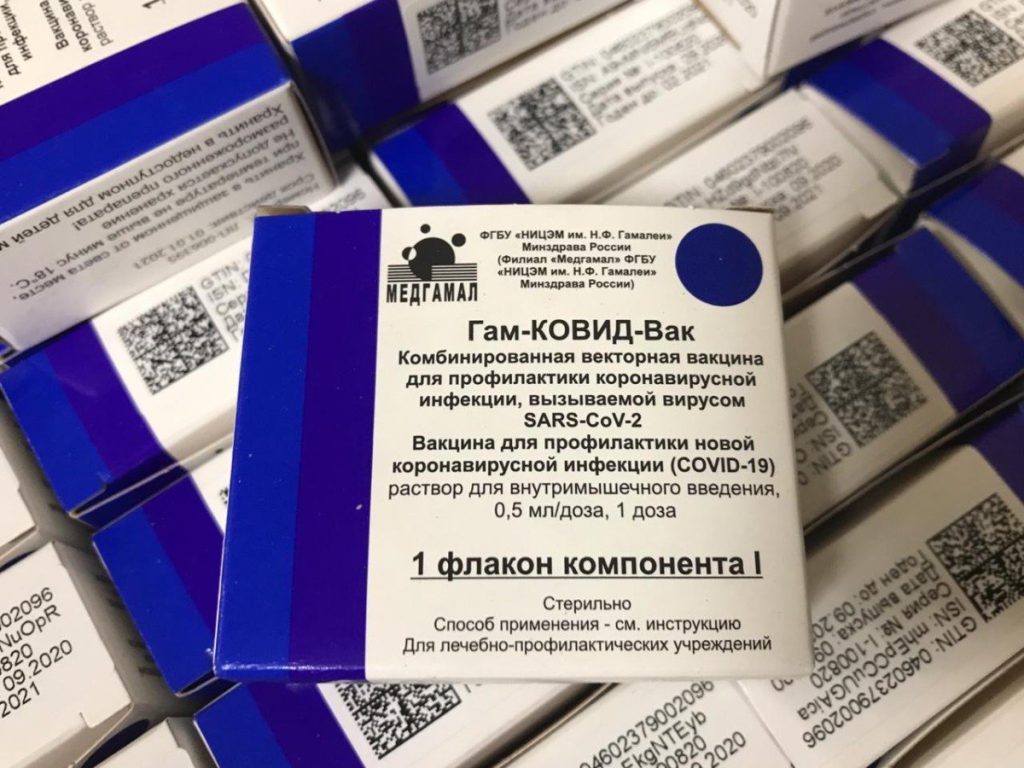
Гам-Ковид-Вак М и «Спутник М» — это одна и та же вакцина, у которой есть медицинское и торговое названия.
Gam-COVID-Vak M — это техническое название, под которым зарегистрирован препарат. Оно было сформировано по названию научного центра в котором вакцина был произведена. Спутник М, известный в англоязычных странах как Sputnik M представляет собой брендовое наименование вакцины, по которому ее легко узнать среди других. Буква “М” в названии вакцины по словам директора НИЦ им. Гамалеи, в котором были разработаны также Спутник V и Лайт, означает “для маленьких”, то есть может применяться у детей до 18 лет.
Производитель вакцины для детей от 12 лет
Вакцина от коронавируса для детей от 12 лет и подростков «Спутник М» будет производиться в филиале научного центра им. Гамалеи «Медгамал». Наряду с ним массовым выпуском препарата займутся следующие компании:
- Biocad, «Биннофарм Групп».
- «Р-Фарм».
- Компания «Генериум».
- «Лекко» и «Фармстандарт-УфаВита».
- Компания «БиоИнтегратор» (ГК «ХимРар»).
По словам Директор по развитию RNC Pharma Николая Беспалова производственный цикл для выпуска вакцины Спутник М будет занимать 40-45 дней, технология полностью отработана на Спутнике V, поэтому массовое производство будет налажено в ближайшее время. Ожидаемая стоимость препарата будет на 30% ниже чем у Гам-Ковид-Вак V и составит приблизительно 600 руб.
Дорогой читатель, мы собрали всю самую важную и актуальную информацию о COVID-19 на 1 странице — главное о коронавирусе.
Также, доступна актуальная статистика по: России, Москве, Подмосковью и городам, СпБ и всем регионам РФ и странам мира.
Вакцинация детей от коронавируса в России
Разработка вакцины от коронавируса для детей велась давно. Первые этапы клинических испытаний были проведены в июле на базе 12 московских медицинских учреждений. Новая фаза испытаний, после которой вакцину запустят выпустят в оборот, стартовала в ноябре 2021.
Когда начнется вакцинация подростков от коронавируса?
Ожидается, что масштабная иммунизация лиц младше 18 лет начнется с конца декабря 2021 года, когда вакцина от Covid-19 для подростков и детей поступит в гражданский оборот. Предварительно будут получены данные о ходе 3 фазы клинических испытаний на здоровых добровольцах, а также завершен контроль качества первых серий препарата.
Как будет проходить вакцинация детей
Вакцинация подростков от Ковид препаратом Гам-Ковид-Вак М будет проводиться в два этапа с интервалом 21 день, по аналогии со Спутником V. Перед прививкой необходим осмотр врача, который даст свое разрешение на введение препарата или предоставит справку о медицинском отводе. Здоровым детям, без тяжелых сопутствующих патологий сдавать анализы и проходить дополнительные обследования перед иммунизацией не нужно.
Во время осмотра врач:
- Оценит общее состояние ребенка, желающего делать прививку от ковид-19.
- Соберет информацию о наличии хронических заболеваний, том как протекали предыдущие вакцинации.
- Проведет измерение температуры тела, аускультацию легких, измерение артериального давления и оценку состояния слизистых оболочек.
Если состояние ребенка позволяет, врач дает добро на использование вакцины для подростков Спутник М. При обнаружении каких-либо патологических состояний, например, при случайном выявлении повышенной температуры или признаках ОРВИ, дается временный медицинский отвод на 2-4 недели.
Детям и подросткам с хроническими патологиями, онкологическими заболеваниями, перенесшим трансплантацию костного мозга или пересадку органов, необходимо обратиться к своему лечащему врачу для решения вопроса об иммунизации против коронавирусной инфекции КОВИД19 в индивидуальном порядке.
После осмотра специалиста и получения согласия на процедуру, медицинская сестра обработает кожу ребенка в проекции дельтовидной мышцы антисептическим раствором и введет препарат внутримышечно. При невозможности введения вакцины в область верхней трети плеча (повреждения области инъекции, состояния после ампутации, врожденные аномалии) препарат вводится в латеральную широкую мышцу бедра.
После прививки необходимо в течение 15-30 минут оставаться под наблюдением медицинского персонала. В случае если не возникает никаких нежелательных проявлений или они незначительные, ребенка могут отпустить домой.
Могут ли привить ребенка без ведома родителей
Вице-премьер министр Татьяна Голикова сообщила, что вакцинация будет проводиться только после получения письменного разрешения родителей или законных опекунов, или по собственному согласию лиц, достигших 15-ти летнего возраста. Гам-Ковид-Вак М не входит в Национальный календарь прививок и на данный момент является добровольной.
Привить ребенка без уведомления его законных представителей невозможно.
Будет ли вакцинация детей обязательна?
В России начинается вакцинация подростков? На данный момент Спутник М не входит в национальный календарь прививок и вакцинация против коронавирусной инфекции является добровольной. Принуждение к прививке будет расцениваться как дискриминация.
Обязательная вакцинация подростков может быть введена после одобрения специальной комиссией и включения ее в график прививок детей в России. Тогда отказаться от нее можно будет только при наличии абсолютных противопоказаний к препарату.
Ввиду отсутствия данных о лекарственной совместимости, Спутник М не следует смешивать в одном шприце с другими медикаментами и иммунными препаратами. Перерыв между вакцинацией от Ковид-19 и других инфекций должен составлять 14 дней.
Положительно, согласен(а) сделать прививку своему ребенку
40.52%
Отрицательно, не согласен(а) сделать прививку своему ребенку
35.42%
Не знаю, нужно больше информации о результатах исследования вакцины для детей
24.05%
Проголосовало: 686
Противопоказания вакцины для детей
Противопоказаниями к иммунизации являются такие состояния:
- Индивидуальная непереносимость одного или нескольких составляющих препарата, в том числе и вспомогательных веществ, тяжелые аллергические реакции в анамнезе.
- Острые инфекционные заболевания, острые неинфекционные и обострение хронических патологий. Вакцинация в данном случае проводится спустя 2-4 недели после нормализации температуры или выздоровления.
Противопоказаниями к введению II компонента Спутника М являются анафилактический шок и отек Квинке в ответ на первый компонент вакцины.
С осторожностью разрешено вакцинировать детей и подростков с хроническими патологиями печени, почек, сахарным диабетом, аутоиммунными заболеваниями. В индивидуальном порядке решается вопрос об иммунизации лиц с онкологическими патологиями, врожденными и приобретенными иммунодефицитами, пациентов находящихся на химиотерапии или лечении иммуносупрессорами.
Кратковременные нежелательные реакции, такие как повышение температуры тела до 37,4-37,5 градусов, гриппоподобный синдром, не являются основанием для получения медицинского отвода от введения второго компонента препарата.
Безопасна ли вакцинация для ребёнка?
По словам директора центра Гамалеи А. Гинцбурга вакцина спутник для детей является безопасной и в редких случаях приводит к возникновению тяжелых побочных эффектов. К нежелательным явлениям, которые могут наблюдаться после вакцинации, относят:
- Гриппоподобный синдром (общая слабость, повышенная утомляемость, головная боль, ломота в мышцах, повышение температуры тела до 37,5 градусов) в течение нескольких дней;
- Гиперемия кожи, локальный отек, боль в месте инъекции (верхняя треть плеча или наружная сторона бедра);
- Тошнота, диспептические явления (ощущение переполнения, тяжести в желудке, отрыжка, рвота, вздутие), запор, диарея, снижение аппетита;
- Увеличение, болезненность лимфатических узлов, заложенность носа, ринорея, першение в горле;
- Кратковременное изменение показателей общего и биохимического анализа крови (увеличение или снижение числа лейкоцитов, повышение уровня билирубина и печеночных трансаминаз);
- Панические атаки, повышение уровня тревожности.
В редких случаях развиваются аллергические реакции, такие как кожный зуд, сыпь, крапивница. Для снижения выраженности нежелательных реакций и устранения неприятных симптомов после вакцинации можно применять нестероидные противовоспалительные средства (парацетамол, ибупрофен) и антигистаминные препараты.
Другие вакцины для детей от COVID-19
Несмотря на то, что дети и подростки, не имеющие никаких серьезных сопутствующих патологий крайне редко болеют вирусом тяжело, они являются основным источником распространения инфекции. Бессимптомный носитель вируса может заразить своих одноклассников из группы риска, пожилых родственников, знакомых.
Для того чтобы снизить темпы распространения коронавирусной инфекции и остановить пандемию, во многих странах мира началась вакцинация подростков от коронавируса. Наряду со Спутником М, одной из первых вакцин, одобренных для иммунизации лиц младше 18 лет, стал препарат Комирнати (Пфайзер).
Pfizer вакцина для подростков разработана на платформе мРНК, которая вводит в клетку код спайк-белка вируса SARS-CoV-2. В клетках иммунизированного человека данный код считывается, организм самостоятельно начинает выработку антигена.
Иммунная система распознает чужеродный белок и начинает выработку специфических антител и клеток памяти. Pfizer вакцина для детей от 12 лет применяется во многих странах Европы, США, в Канаде, и Австралии.
Также как и Гам-Ковид-Вак М препарат вводится дважды, с интервалом в 21-28 дней. Перечень противопоказаний и побочных эффектов у вакцин одинаковый, за исключением того что М-РНК вакцины не рекомендованы лицам, у которых в анамнезе или после введения первой дозы развилось воспаление сердечной мышцы (миокардит).
В настоящее время по указу президента ведется разработка новых вакцин, а также исследование влияния существующих препарат на организм детей от 5 лет. В вакцинах детям до года концентрация активного вещества будет снижена в 10 раз по сравнению со Спутником V.
Что говорят врачи о вакцинации детей и подростков от COVID-19
Ковид-19 — опасное инфекционное заболевание, характеризующееся высокой заразностью, тяжелым течением и способностью вызывать после себя серьезные последствия.
К осложнениям коронавирусной инфекции у детей относятся:
- Пневмония, фиброзы, спонтанный пневмоторакс.
- Миокардиты.
- Синдром мультисистемного воспаления.
- Декомпенсация тяжелых хронических патологий (сахарный диабет, хроническая почечная и печеночная недостаточность), активизация аутоиммунных болезней, рецидивы рака, отторжение трансплантированных органов.
К последствиям перенесенной коронавирусной инфекции также относятся синдром хронической усталости, депрессия, тревожные расстройства. Снизить вероятность инфицирования, развития тяжелых форм и осложнений возможно с помощью иммунизации.
В настоящее время вакцинация Спутником подростков и детей и подростков от коронавируса носит рекомендательный характер, однако специалисты настоятельно призывают родителей не откладывать прививку. С приходом штамма “Дельта” дети стали болеть чаще, также участились и случаи тяжелого течения болезни.
Спутник М вакцина от коронавируса для детей снижает вероятность развития серьезных осложнений у каждого ребенка индивидуально, а также способствует формированию коллективного иммунитета. Директор Национального института им. Гамалеи Александр Гинцбург призывает родителей вакцинировать своих детей. По его словам прививка абсолютно безопасна для маленьких пациентов.
Поделитесь своим мнением либо опытом – пишите комментарии. Понравилась статья? – Поделитесь ею с друзьями в социальных сетях.
По словам министра здравоохранения М. Мурашко, препарат Спутник-М хорошо показал себя за время проведения клинических испытаний и по завершению контроля, в течение 3 недель будет введен в массовый гражданский оборот.
Эксперт НИЦ им. Гамалеи вирусолог А. Альтштейн утверждает что вакцина Ступник М представляет собой практически то же самое, что и препарат Sputnik V, только в существенно меньшей дозе. Поэтому есть полная уверенность в том, что вакцина безопасна и есть все основания для начала ее массового применения. По словам специалиста, после вакцинации значительной части детей и подростков заболеваемость коронавирусом в России существенно снизится.
Дорогой читатель, мы собрали всю самую важную и актуальную информацию о COVID-19 на 1 странице — главное о коронавирусе.
Также, доступна актуальная статистика по: России, Москве, Подмосковью и городам, СпБ и всем регионам РФ и странам мира.

Врач высшей квалификационной категории по фтизиатрии и пульмонологии. 25 лет рабочего стажа в практической, терапевтической медицине. Эксперт и автор статей Coronavirus-Control.ru
Задать вопрос
Дорогие читатели, если у вас возникли вопросы по статье — пожалуйста, задавайте их в комментариях, непременно на них отвечу. Также, поделитесь своим опытом течения болезни, выздоровления — это будет ценно для всех.
Загрузка…