Таблетки, покрытые пленочной оболочкой, 300 мг
Одна таблетка содержит
активное вещество – тенофовира дизопроксила фумарата 300 мг (эквивалентно 245 мг тенофовира дизопроксила),
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристалическая, натрия кроскармеллоза, крахмал прежелатинизированный, магния стеарат,
состав пленочной оболочки: Opadry II White 32K18425 (лактозы моногидрат, гипромеллоза, титана диоксид Е171, триацетин).
Таблетки, покрытые пленочной оболочкой, белого цвета, миндалевидной формы, с тиснением «GILEAD» и «4331» с одной стороны таблетки.
Противоинфекционные препараты для системного применения. Противовирусные средства для системного применения. Противовирусные препараты прямого действия. Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы. Тенофовира дизопроксил.
Код АТХ J05AF07
Тенофовира дизопроксила фумарат является водорастворимым сложным эфиром-пролекарством, которое in vivo быстро преобразуется в тенофовир и формальдегид.
Тенофовир в клетках преобразуется в тенофовира монофосфат и активный компонент тенофовира дифосфат.
Фармакокинетика
Всасывание
После перорального введения ВИЧ-инфицированным пациентам тенофовира дизопроксила фумарат быстро всасывается и преобразуется в тенофовир. Введение многократных доз тенофовира дизопроксила фумарата с едой ВИЧ-инфицированным пациентам приводило к средним (коэффициент вариации, % [CV, %]) значениям для тенофовира Cmax, AUC и Cmin 326 (36.6 %) нг/мл, 3,324 (41.2 %) нг·ч/мл и 64.4 (39.4 %) нг/мл, соответственно. Максимальные концентрации тенофовира наблюдаются в сыворотке крови в пределах 1 часа после введения натощак и в пределах 2 часов при его приеме с едой. При пероральном введении тенофовира дизопроксила фумарата пациентам натощак пероральная биодоступность составляла приблизительно 25 %. Введение тенофовира дизопроксила фумарата с богатой жирами пищей повышало пероральную биодоступность, при этом значение AUC тенофовира увеличивалось приблизительно на 40 %, а Cmax – приблизительно на 14 %.
После первой дозы тенофовира дизопроксила фумарата, полученной после богатой жирами пищи, медианное значение Cmax в сыворотке было в диапазоне значений от 213 до 375 нг/мл. Однако введение тенофовира дизопроксила фумарата с низкокалорийной пищей не оказывает существенного влияния на фармакокинетику тенофовира.
Распределение
После внутреннего внутривенного введения объем распределения тенофовира в равновесном состоянии равен примерно 800 мл/кг. После перорального введения тенофовира дизопроксила фумарата тенофовир распределяется во многие ткани, при этом наибольшие концентрации наблюдаются в почках, печени и в содержимом кишечника (доклинические исследования). In vitro связывание тенофовира с белками плазмы или сыворотки крови составляло менее 0.7 и 7.2 %, соответственно, в диапазоне концентраций тенофовира от 0.01 до 25 мкг/мл.
Биотрансформация
Исследования in vitro показали, что ни тенофовира дизопроксила фумарат, ни тенофовир не являются субстратами ферментов CYP450. Более того, при концентрациях, существенно превышающих (примерно в 300 раз) те, что наблюдаются in vivo, тенофовир не ингибировал in vitro лекарственный метаболизм, опосредованный какой-либо из основных изоформ CYP450 человека, участвующих в биотрансформации (CYP3A4, CYP2D6, CYP2C9, CYP2E1 или CYP1A1/2). Тенофовира дизопроксила фумарат при концентрации 100 мкмоль/л не оказывал влияния ни на одну из изоформ CYP450 за исключением CYP1A1/2, где наблюдалось небольшое (6 %), но статистически значимое снижение метаболизма субстрата CYP1A1/2. На основании этой информации можно сделать вывод о малой вероятности возникновения клинически значимых взаимодействий между тенофовира дизопроксила фумаратом и лекарственными средствами, метаболизм которых опосредован CYP450.
Выведение
Тенофовир выводится главным образом почками, как путем фильтрации, так и активной тубулярной транспортной системой, при этом после внутривенного введения приблизительно 70 – 80 % дозы выводится в неизмененном виде с мочой. Общий клиренс оценивался приблизительно в 230 мл/ч/кг (приблизительно 300 мл/мин.). Почечный клиренс оценивался приблизительно в 160 мл/ч/кг (около 210 мл/мин.), что превышает скорость гломерулярной фильтрации. Это указывает на то, что тубулярная секреция является важной частью выведения тенофовира. После перорального введения окончательный период полувыведения тенофовира составляет от 12 до 18 часов.
Исследованиями было установлено, что путем активной тубулярной секреции тенофовира является входной ток к проксимальной канальцевой клетке с помощью транспортеров органического иона человека (hOAT) 1 и 3 и выходной ток к моче с помощью резистентного ко многим препаратам белка 4 (multidrug resistant protein 4 – MRP 4).
Линейность-нелинейность
Показатели фармакокинетики тенофовира не зависели от дозы тенофовира дизопроксила фумарата в диапазоне от 75 до 600 мг и не испытывали воздействия повторного введения при любом уровне дозы.
Возраст
Исследование фармакокинетики не проводились у пациентов старшего возраста (старше 65 лет).
Пол
Ограниченные данные о фармакокинетике тенофовира у женщин указывают на отсутствие значимого влияния пола.
Этническая принадлежность
Не проводилось специфических исследований фармакокинетики у различных этнических групп.
Педиатрические пациенты
ВИЧ-1: Фармакокинетические параметры тенофовира в равновесном состоянии оценивали у 8 подростков (возраст от 12 до 18 лет) с массой тела ≥ 35 кг, инфицированных ВИЧ-1. Средние (± SD) значения Cmax и AUCtau составляли 0.38 ± 0.13 мкг/мл и 3.39 ± 1.22 мкг·ч/мл, соответственно. Экспозиция к тенофовиру, которая была достигнута у подростков, получавших пероральные суточные дозы тенофовира дизопроксила 245 мг (в форме фумарата), была подобна экспозициям, которые были достигнуты у взрослых, получавших разовые суточные дозы тенофовира дизопроксила 245 мг (в форме фумарата).
Хронический гепатит В: Равновесная экспозиция тенофовира у подростков (возраст от 12 до 18 лет), инфицированных вирусом гепатита В, которые получали пероральную суточную дозу тенофовира дизопроксила 245 мг (в форме фумарата) была подобна экспозициям, достигаемым у взрослых, которые получали дозы тенофовира дизопроксила 245 мг (в форме фумарата) в режиме один раз в сутки.
У детей младше 12 лет или у детей с нарушением функции почек исследования фармакокинетики таблеток тенофовира дизопроксила (в форме фумарата) 245 мг не проводились.
Нарушения функции почек
Параметры фармакокинетики тенофовира определялись после введения разовой дозы 245 мг тенофовира дизопроксила 40 пациентам неинфицированным ВИЧ и вирусом гепатита В с почечными нарушениями различной степени, которые определялись соответственно исходному значению клиренса креатинина (нормальная функция почек, если CrCl > 80 мл/мин; небольшие нарушения – при CrCl = 50‑79 мл/мин; умеренные – при CrCl = 30‑49 мл/мин. и тяжелые – при CrCl = 10‑29 мл/мин). По сравнению с пациентами с нормальной функцией почек средняя (% CV) экспозиция тенофовира увеличилась с 2,185 (12 %) нг·ч/мл у лиц с CrCl > 80 мл/мин. до, соответственно, 3,064 (30 %) нг·ч/мл, 6,009 (42 %) нг·ч/мл и 15,985 (45 %) нг·ч/мл у пациентов с незначительными, умеренными и тяжелыми нарушениями функции почек. Ожидается, что увеличение интервала между введением препарата приведет к более высоким пиковым концентрациям в плазме крови и меньшим уровням Cmin у пациентов с почечными нарушениями по сравнению с пациентами, имеющими нормальную функцию почек. Клиническое значение этого неизвестно.
У пациентов с терминальной стадией заболевания почек (CrCl < 10 мл/мин.), которым был необходим гемодиализ, концентрации тенофовира между диализами значительно увеличивались в течение 48 часов, достигая среднего значения Cmax 1,032 нг/мл и среднего значения AUC0‑48h 42,857 нг·ч/мл.
Рекомендуется, чтобы интервал между введениями тенофовира дизопроксила (в форме фумарата) в дозе 245 мг был изменен у пациентов с клиренсом креатинина < 50 мл/мин. или у пациентов, уже имеющих ESRD (терминальную стадию заболевания почек) и нуждающихся в диализе (см. раздел «Способ применения и дозы»).
Фармакокинетика тенофовира у пациентов без гемодиализа с клиренсом креатинина < 10 мл/мин. и у пациентов с ESRD (терминальной стадией заболевания почек), контроль состояния которых осуществляется путем перитонеального или других форм диализа, не исследовалась.
Фармакокинетика тенофовира у детей с нарушением функции почек не исследована. Данные для рекомендации по коррекции дозы отсутствуют (см. разделы «Способ применения и дозы» и «Особые указания»).
Нарушения функции печени
Разовую дозу тенофовира дизопроксила 245 мг вводили пациентам, не инфицированным ВИЧ и вирусом гепатита В, с разными степенями нарушений функции печени, определяемыми соответственно классификации Child‑Pugh‑Turcotte (CPT). Не отмечалось существенных изменений параметров фармакокинетики тенофовира у пациентов с нарушением функции печени, что указывало на отсутствие необходимости в коррекции дозы. Средние (% CV) значения Cmax и AUC0‑∞ тенофовира составляли 223 (34.8 %) нг/мл и 2,050 (50.8 %) нг·ч/мл, соответственно, у лиц без нарушений функции печени, 289 (46.0 %) нг/мл и 2,310 (43.5 %) нг·ч/мл у лиц с умеренными нарушениями функции печени и 305 (24.8 %) нг/мл и 2,740 (44.0 %) нг·ч/мл у лиц с тяжелыми нарушениями функции печени.
Внутриклеточная фармакокинетика
В мононуклеарных клетках периферической крови (PBMCs) человека, которые не воспроизводятся, период полувыведения тенофовира дифосфата составляет приблизительно 50 часов, тогда как в стимулированных фитогемоглютинином PBMCs этот показатель составлял приблизительно 10 часов.
Фармакодинамика
Тенофовира дизопроксила фумарат – это фумаратная соль пролекарства тенофовира дизопроксила. Тенофовира дизопроксил всасывается и преобразуется в активное вещество тенофовир, которое является аналогом нуклеозид монофосфата (нуклеотида). Затем тенофовир преобразуется в активный метаболит, тенофовира дифосфат, который является облигатным терминатором цепи, с помощью конструктивно экспресированных клеточных ферментов. Тенофовира дифосфат имеет внутриклеточный период полувыведения 10 часов в активизированном состоянии и 50 часов в состоянии покоя в мононуклеарных клетках периферической крови (peripheral blood mononuclear cells – PBMCs). Тенофовира дифосфат ингибирует обратную транскриптазу ВИЧ‑1 и полимеразу вируса гепатита В путем конкуренции прямого связывания с природным субстратом диоксирибонуклеотида и обрывом цепи ДНК после присоединения к ДНК. Тенофовира дифосфат является слабым ингибитором клеточных полимераз α, β и γ. В анализах in vitro тенофовир при концентрациях до 300 мкмоль/л также показал отсутствие влияния на синтез митохондриальной ДНК или образование молочной кислоты.
Информация относительно ВИЧ
Активность против ВИЧ in vitro
Концентрация тенофовира, необходимая для 50 % ингибирования (EC50) лабораторного штамма ВИЧ-1IIIB дикого типа в лимфоидных клетках, составляла 1–6 мкмоль/л; ЕС50 для ингибирования первичных изолятов ВИЧ-1 подтипа В в мононуклеарах периферической крови составляла 1.1 мкмоль/л. В первичных моноцитах/макрофагах тенофовир также обладает активностью в отношении ВИЧ-1 подтипов A, C, D, E, F, G, O, а также ВИЧBaL. Тенофовир оказывает угнетающее действие на ВИЧ-2 in vitro, при этом ЕС50 в МТ-4 клетках составляет 4.9 мкмоль/л.
Резистентность
В условиях in vitro и у некоторых пациентов были выделены штаммы ВИЧ-1 с мутацией К65R гена обратной транскриптазы, обладающие пониженной чувствительностью к тенофовиру. Тенофовира дизопроксила фумарат не следует использовать у ранее получавших антиретровирусную терапию больных, инфицированных штаммом ВИЧ с мутацией К65R Кроме того, тенофовир вызывает замещение K70E в обратной транскриптазе ВИЧ-1, что приводит к небольшому снижению чувствительности к тенофовиру.
Пациенты, ВИЧ-1 у которых экспрессировал 3 или более мутаций, связанных с аналогами тимидина, включающих замены M41L или L210W в обратной транскриптазе, показали сниженный ответ на терапию препаратом Виреад®.
Информация относительно ВГВ
Активность против ВГВ in vitro: антивирусную активность тенофовира против вируса гепатита В в условиях in vitro оценивали на клеточной линии HepG2 2.2.15. Значения EC50 для тенофовира находились в пределах от 0.14 до 1.5 мкмоль/л, а значения СС50 (50 % цитотоксическая концентрация) превышали > 100 мкмоль/л.
Резистентность
Не было установлено мутаций ВГВ, которые вызваны резистентностью к тенофовира дизопроксила фумарату. По результатам клеточных тестов для штаммов ВГВ, экспрессирующих отвечающие за резистентность к ламивудину и телбивудину мутации rtV173L, rtL180M и rtM204I/V, была показана чувствительность к тенофовиру в диапазоне от 0.7 до 3.4 значений чувствительности вируса дикого типа. Для штаммов ВГВ, экспрессирующих мутации rtL180M, rtT184G, rtS202G/I, rtM204V и rtM250V, отвечающие за резистентность к энтекавиру, была показана чувствительность к тенофовиру в диапазоне от 0.6 до 6.9 значений чувствительности вируса дикого типа. Штаммы ВГВ, экспрессирующие мутации rtA181V и rtN236T, отвечающие за резистентность к адефовиру, показали чувствительность к тенофовиру в диапазоне от 2.9 до 10 значений чувствительности вируса дикого типа. Вирусы с мутацией rtA181T сохраняли чувствительность к тенофовиру, при этом ЕС50 превышала в 1.5 раза показатель для вируса дикого типа.
Демонстрация преимущества тенофовира дизопроксила фумарата основывается на вирусологическом, биохимическом и серологическом ответах на препарат, наблюдавшихся, главным образом, у ранее не получавших лечения взрослых пациентов с HbeAg-положительным и HbeAg-отрицательным хроническим гепатитом В и компенсированным либо декомпенсированным заболеванием печени. Препарат применяли у пациентов, которые ранее не получали лечения, а также тех, которые ранее лечились ламивудином, адефовира дипивоксилом, и пациентов с мутациями вируса, вызванные резистентностью к ламивудину и (или) адефовира дипивоксилу в исходном состоянии. Польза была также продемонстрирована на основании гистологического ответа, полученного у пациентов с компенсированным заболеванием.
Инфекция ВИЧ-1
Таблетки Виреад® 245 мг, покрытые пленочной оболочкой, предназначены для лечения ВИЧ-1 инфицированных взрослых в комбинации с другими антиретровирусными препаратами.
Таблетки Виреад® 245 мг, покрытые пленочной оболочкой, предназначены для лечения ВИЧ-1 инфицированных подростков в возрасте от 12 до 18 лет, у которых отмечалась резистентность к нуклеозидным ингибиторам обратной транскриптазы или их токсическое воздействие, что исключало возможность применения препаратов первой линии.
Выбор препарата Виреад® для лечения пациентов с ВИЧ-1 инфекцией, ранее получавших антиретровирусную терапию, должен быть основан на результатах индивидуальных тестов на резистентность вируса и (или) результатах ранее проведенного лечения пациентов.
Инфекция вирусом гепатита В
Таблетки Виреад® 245 мг, покрытые пленочной оболочкой, предназначены для лечения хронического гепатита B у взрослых с:
· компенсированным заболеванием печени, с признаками активной репликации вируса, постоянным повышением уровня аланинаминотрансферазы (АЛТ) в сыворотке крови и гистологическим проявлением активного воспаления и/или фиброза (см. раздел «Фармакодинамика»);
· признаком ламивудин-резистентного вируса гепатита В (см. разделы «Побочные действия» и «Фармакодинамика»);
· декомпенсированным заболеванием печени (см. разделы «Особые указания», «Побочные действия» и «Фармакодинамика»).
Таблетки Виреад® 245 мг, покрытые пленочной оболочкой, предназначены для лечения хронического гепатита B у подростков в возрасте от 12 до 18 лет с:
· компенсированным заболеванием печени и признаками активного иммунного заболевания, т.е. активной репликации вируса, постоянным повышением уровня аланинаминотрансферазы (АЛТ) в сыворотке крови и гистологическим проявлением активного воспаления и/или фиброза (см. разделы «Особые указания», «Побочные действия» и «Фармакодинамика»).
Лечение должен начинать врач, имеющий опыт в лечении ВИЧ-инфекции и (или) хронического гепатита B.
Взрослые
Рекомендованная доза для лечения ВИЧ и хронического гепатита В: по одной таблетке один раз в сутки перорально с едой.
Хронический гепатит В
Оптимальная продолжительность лечения неизвестна. Лечение может быть прекращено при указанных ниже обстоятельствах.
· Лечение пациентов с положительной реакцией на антиген вируса гепатита В (HBeAg) без цирроза должно продолжаться не менее 6-12 месяцев после подтверждения сероконверсии HBe (исчезновение антигенов вируса гепатита В и ДНК-вируса гепатита В с выявлением анти-НВе) или до сероконверсии HBs, либо исчезновения эффективности (см. раздел «Особые указания»). После прекращения лечения необходимо регулярно проверять уровни АЛТ и ДНК-вируса гепатита В в сыворотке крови с целью установления каких-либо поздних рецидивов виремии.
· Лечение пациентов с отрицательной реакцией на антиген вируса гепатита В без цирроза должно продолжаться, как минимум, до сероконверсии HBs или появления признаков исчезновения эффективности лечения. В случае пролонгированного лечения, продолжающегося более 2 лет, рекомендуется регулярно проводить повторный пересмотр лечения, чтобы подтвердить приемлемость для пациента продолжения выбранной терапии.
Дети
ВИЧ-1: в возрасте от 12 до 18 лет и с массой тела ≥ 35 кг рекомендованная доза Виреад® составляет по одной таблетке один раз в сутки перорально с едой (см. разделы «Побочные действия» и «Фармакодинамика»).
Хронический гепатит В: в возрасте от 12 до 18 лет и с массой тела ≥ 35 кг, рекомендованная доза Виреад® составляет по одной таблетке один раз в сутки перорально с едой (см. разделы «Побочные действия» и «Фармакодинамика»).
Оптимальная продолжительность лечения на настоящее время не установлена.
Пропущенная доза
Если прием дозы был пропущен и прошло менее 12 часов от обычного времени приема дозы, то пациенту следует как можно скорее принять Виреад® вместе с едой и вернуться к обычному режиму приема препарата. Если в случае пропущенного приема дозы прошло более 12 часов и приближается время приема следующей дозы препарата, то пациенту не следует принимать пропущенную дозу, но необходимо вернуться к обычному режиму приема препарата.
Если в течение 1 часа после приема Виреад® у пациента возникла рвота, следует принять еще 1 таблетку. Если рвота у пациента возникла более, чем через 1 час после приема Виреад®, то еще 1 таблетку принимать не следует.
Особые группы пациентов
Пациенты пожилого возраста
На сегодняшний день нет данных, на основании которых можно дать рекомендации относительно дозирования для пациентов в возрасте старше 65 лет (см. раздел «Особые указания»).
Нарушения функции почек
Тенофовир выводится из организма через почки, поэтому пациенты с почечной дисфункцией имеют повышенную экспозицию тенофовира.
Взрослые
Данные о безопасности и эффективности применения тенофовира дизопроксила фумарата у взрослых пациентов с умеренными и тяжелыми нарушениями функции почек (клиренс креатинина < 50 мл/мин.) ограничены. Оценка показателей безопасности относительно незначительных нарушений функции почек (клиренс креатинина 50–80 мл/мин.) в долгосрочной перспективе не проводилась. По этой причине пациентам с нарушениями функции почек тенофовира дизопроксила фумарат необходимо применять, если потенциальная польза лечения считается превышающей потенциальный риск. Коррекция интервала дозирования рекомендуется для пациентов с клиренсом креатинина < 50 мл/мин.
Незначительные нарушения функции почек (клиренс креатинина 50-80 мл/мин.). Ограниченные данные, полученные в результате клинических исследований, свидетельствуют в пользу сохранения для пациентов с незначительными нарушениями функции почек дозирования тенофовира дизопроксила (в форме фумарата) по 245 мг один раз в сутки.
Умеренные нарушения функции почек (клиренс креатинина 30-49 мл/мин.). Прием 245 мг тенофовира дизопроксила (в форме фумарата) каждые 48 часов рекомендуется на основе моделирования фармакокинетических данных разовой дозы у ВИЧ-отрицательных субъектов и субъектов, не инфицированных вирусом гепатита В, с разными степенями почечных нарушений, в том числе с терминальной стадией почечной недостаточности, требующей гемодиализа. Однако такое дозирование не было подтверждено в рамках клинических исследований. Поэтому клиническую реакцию на лечение и функцию почек у таких пациентов необходимо внимательно контролировать (см. раздел «Особые указания» и «Фармакокинетика»).
Тяжелые почечные нарушения (клиренс креатинина < 30 мл/мин.) и пациенты, находящиеся на гемодиализе
Соответствующая коррекция дозы не может быть применена из-за отсутствия таблетки с другим содержанием действующего вещества, поэтому применение препарата для пациентов этой группы не рекомендуется. Если альтернативное лечение отсутствует, можно применить продленные интервалы введения следующим образом:
— тяжелые почечные нарушения: по одной таблетке Виреад® принимать каждые 72-96 часов (дважды в неделю);
— пациенты, находящиеся на гемодиализе: по одной таблетке Виреад® принимать каждые 7 суток после завершения сессии гемодиализа*.
Указанные коррекции интервала приема препарата не были подтверждены в рамках клинических исследований. Моделирование дает основания предположить, что длительный интервал приема таблеток Виреад® 245 мг не является оптимальным и может привести к повышенной токсичности и, возможно, к недостаточному ответу. По этой причине клиническую реакцию на лечение и функцию почек необходимо внимательно контролировать (см. раздел «Особые указания» и «Фармакокинетика»).
* Как правило, введение один раз в неделю, допуская 3 сессии гемодиализа в неделю, продолжительностью приблизительно 4 часа каждый, или после 12 часов кумулятивного гемодиализа.
Нельзя дать рекомендации относительно дозирования для пациентов без гемодиализа с клиренсом < 10 мл/мин.
Дети
Не рекомендуется применять тенофовира дизопроксила фумарат у детей с нарушением функции почек (см. раздел «Особые указания»).
Нарушения функции печени
Для пациентов с нарушениями функции печени нет необходимости в коррекции дозы (см. раздел «Особые указания» и «Фармакокинетика»).
При прекращении приема Виреад® пациентов с хроническим гепатитом B, с или без сопутствующего инфицирования ВИЧ, необходимо внимательно наблюдать с целью выявления признаков обострения гепатита (см. раздел «Особые указания»).
Способ применения
Таблетку следует глотать. При затрудненном глотании препарат Виреад® можно принимать, перемешав одну измельченную таблетку не менее чем со 100 мл воды, апельсинового или виноградного сока.
Краткое описание профиля безопасности
ВИЧ-1 и гепатит В. Редко сообщалось о случаях нарушений функции почек, почечной недостаточности и нечасто — о случаях проксимальной почечной тубулопатии (в том числе синдром Фанкони), которые иногда приводили к костным аномалиям (редко – к переломам), у пациентов, принимавших тенофовира дизопроксила фумарат. Для пациентов, принимающих Виреад®, рекомендуется наблюдение за почечной функцией (см. раздел «Особые указания»).
ВИЧ-1. Наиболее часто встречающиеся побочные действия возникающие после лечения тенофовира дизопроксила фумаратом в сочетании с другими антиретровирусными препаратами, были нарушения со стороны желудочно-кишечного тракта от незначительной до средней степени тяжести. Не рекомендуется одновременное применение тенофовира дизопроксила фумарата и диданозина, поскольку это может привести к повышению риска побочных реакций (см. раздел «Лекарственные взаимодействия»). Редко сообщалось о случаях заболевания панкреатитом и лактат-ацидозом, иногда с летальным исходом (см. раздел «Особые указания»).
Гепатит В. Наиболее частым побочным действием тенофовира дизопроксила фумарат была тошнота.
Сообщалось о случаях обострения гепатита у пациентов, получавших терапию, а также у пациентов, прекративших лечение гепатита В (см. раздел «Особые указания»).
Сводная таблица побочных действий
Оценка побочных действий, вызванных приемом тенофовира дизопроксила фумарат, основывается на данных по безопасности, полученных в ходе клинических исследований и постмаркетингового анализа. Все побочные действия указаны в таблице 1.
Побочные действия с потенциальным (или, как минимум, возможным) отношением к лечению приводятся ниже по классам систем органов и частоте. В рамках каждой группы по частоте, побочные действия приведены в порядке уменьшения серьезности. Побочные действия по частоте определяются как: очень часто (≥ 1/10), часто (от ≥ 1/100 до < 1/10), нечасто (от ≥ 1/1000 до < 1/100) и редко (от ≥ 1/10 000 до < 1/1000).
Таблица 1. Краткие данные о побочных действиях, связанных с приемом тенофовира дизопроксила фумарата, на основании клинического исследования и постмаркетингового анализа.
|
Частота |
Тенофовир дизопроксил фумарат |
|
Нарушения со стороны обмена веществ и питания |
|
|
Очень часто |
Гипофосфатемия1 |
|
Нечасто |
Гипокалиемия1 |
|
Редко |
Лактат-ацидоз |
|
Нарушения со стороны нервной системы |
|
|
Очень часто |
Головокружение |
|
Часто |
Головная боль |
|
Нарушения со стороны желудочно-кишечного тракта |
|
|
Очень часто |
Диарея, рвота, тошнота |
|
Часто |
Боль в животе, вздутие живота, метеоризм |
|
Нечасто |
Панкреатит |
|
Нарушения со стороны печени и желчевыводящих путей |
|
|
Часто |
Повышенный уровень трансаминаз |
|
Редко |
Жировая дегенерация печени, гепатит |
|
Нарушения со стороны кожи и подкожных тканей |
|
|
Очень часто |
Высыпания |
|
Редко |
Ангионевротический отек |
|
Нарушения со стороны скелетно-мышечной и соединительной ткани |
|
|
Нечасто |
Рабдомиолиз1, мышечная слабость1 |
|
Редко |
Остеомаляция (проявляется как боль в костях и нечасто является одной из причин переломов)1, 2, миопатия1 |
|
Нарушения со стороны почек и мочевыводящих путей |
|
|
Нечасто |
Повышенный креатинин, проксимальная почечная тубулопатия (в том числе синдром Фанкони) |
|
Редко |
Острая почечная недостаточность, почечная недостаточность, острый тубулярный некроз, нефрит (в том числе острый интерстициальний нефрит)2, нефрогенный несахарный диабет |
|
Общие расстройства и нарушения в месте введения |
|
|
Очень часто |
Астения |
|
Часто |
Усталость |
1Побочное действие может возникнуть как следствие проксимальной почечной тубулопатии. Не считается, что оно причинно связано с тенофовира дизопроксила фумаратом при отсутствии этого заболевания.
2Побочное действие было установлено во время постмаркетингового исследования, но не наблюдалось во время рандомизированных контролируемых исследований или программы расширенного доступа к тенофовира дизопроксила фумарату. Категория частоты была установлена по статистическим расчетам на основе общего количества пациентов, принимавших тенофовира дизопроксила фумарат в рамках рандомизированных контролируемых исследований и программы расширенного доступа (n = 7,319).
Описание отдельных побочных действий
ВИЧ-1 и гепатит В
Нарушение функции почек. Поскольку Виреад® может привести к нарушению работы почек, рекомендуется наблюдать за функцией почек (см. разделы «Особые указания» и «Побочные действия. Краткие данные о профиле безопасности»). Проксимальная почечная тубулопатия обычно проходит или его тяжесть снижается после прекращения приема тенофовира дизопроксила фумарата. Однако у некоторых пациентов сниженный клиренс креатинина полностью не восстанавливался, несмотря на отмену тенофовира дизопроксила фумарата. Пациенты с риском нарушения функции почек (например, имеющие риск нарушения функции почек в исходном состоянии, при поздних стадиях ВИЧ-инфекции или получающие сопутствующее лечение нефротоксическими препаратами) имеют повышенный риск неполного восстановления почек после отмены тенофовира дизопроксила фумарата (см. раздел «Особые указания»).
ВИЧ-1.
Взаимодействие с диданозином. Одновременное применение тенофовира дизопроксила фумарата и диданозина не рекомендуется, так как это приводит к повышению системного воздействия диданозина на 40–60 %, что может увеличить риск возникновения побочных действий, связанных с диданозином (см. раздел «Лекарственные взаимодействия»). Редко сообщалось о случаях заболевания панкреатитом и лактат-ацидозом, иногда с летальным исходом.
Показатели метаболизма. Возможно увеличение массы тела, а также уровня липидов и глюкозы в крови во время антиретровирусной терапии (см. раздел «Особые указания»).
Синдром иммунной реактивации. У ВИЧ-инфицированных пациентов с тяжелой иммунной недостаточностью на момент начала комбинированной антиретровирусной терапии (КАРТ) может возникнуть воспалительная реакция на асимптоматические или остаточные оппортунистические патогены (см. раздел «Особые указания»).
Остеонекроз. Сообщалось о случаях остеонекроза, особенно относительно пациентов с общепризнанными факторами риска, поздней стадией ВИЧ-инфекции или длительным воздействием комбинированной антиретровирусной терапии (КАРТ). Частота возникновения указанного явления неизвестна (см. раздел «Особые указания»).
Гепатит В
Обострение гепатита во время лечения. В рамках исследований среди пациентов, которые ранее не принимали нуклеозиды, повышение уровня АЛТ во время лечения с превышением верхнего предела нормы более, чем в 10 раз, и превышением начального уровня более, чем в 2 раза, наблюдалось у 2.6 % пациентов, получавших лечение тенофовира дизопроксила фумаратом. Во время лечения рекомендуется регулярно наблюдать за функцией печени (см. раздел «Особые указания»).
Обострение гепатита после прекращения лечения. После прекращения терапии гепатита В у пациентов, инфицированных вирусом гепатита В, возникали клинические и лабораторные признаки обострения гепатита (см. раздел «Особые указания»).
Подростки
ВИЧ-1
Побочные действия, которые наблюдались у подростков, проходивших лечение тенофовира дизопроксила фумаратом, соответствовали тем, которые наблюдались в клинических исследованиях тенофовира дизопроксила фумарата у взрослых (см. разделы «Сводная таблица побочных действий» и «Фармакодинамика»).
Поступали сообщения об уменьшении минеральной плотности костей у подростков. Среди подростков, инфицированных ВИЧ-1, Z-критерии минеральной плотности костей, наблюдаемые у субъектов, которые получали тенофовира дизопроксила фумарат, были ниже, чем эти же критерии, наблюдаемые у субъектов, которые получали плацебо.
Хронический гепатит В
Побочные действия, которые наблюдались у подростков, получающих тенофовира дизопроксила фумарат, соответствовали тем, что наблюдались в клинических исследованиях тенофовира дизопроксила фумарата у взрослых (см. разделы «Сводная таблица побочных действий» и «Фармакодинамика»).
Уменьшение минеральной плотности костей наблюдалось у подростков, инфицированных вирусом гепатита В. Z-критерии минеральной плотности костей, наблюдаемые у субъектов, которые получали тенофовира дизопроксила фумарат, были ниже, чем эти же критерии, наблюдаемые у субъектов, которые получали плацебо (см. разделы «Особые указания» и «Фармакодинамика»).
Другие особые категории пациентов
Пациенты пожилого возраста. Исследование тенофовира дизопроксила фумарата среди пациентов в возрасте старше 65 лет не проводилось. Пациенты пожилого возраста в большей степени склонны иметь пониженную почечную функцию, поэтому во время лечения тенофовира дизопроксила фумаратом этой популяции необходимо соблюдать осторожность (см. раздел «Особые указания»).
Пациенты с нарушением функции почек. Поскольку тенофовира дизопроксила фумарат может привести к нефротоксичности, рекомендуется внимательно контролировать функцию почек у взрослых пациентов с нарушением функции почек, принимающих Виреад® (см. разделы «Способ применения и дозы», «Особые указания» и «Фармакокинетика»).
Ламивудин-резистентные и рефрактерные к лечению препаратом Hepsera пациенты. Не было обнаружено новых побочных действий, вызванных приемом тенофовира дизопроксила фумарата у инфицированных ВГВ ламивудин-резистентных и рефрактерных к лечению препаратом Hepsera пациентов которые получали лечение препаратом Виреад®.
Пациенты с декомпенсированным заболеванием печени. Не было обнаружено новых побочных действий, вызванных приемом тенофовира дизопроксила фумарата у инфицированных ВГВ пациентов с декомпенсированным заболеванием печени которые получали лечение препаратом Виреад®.
Отчетность о подозреваемых побочных реакциях
Отчетность о подозреваемых побочных реакциях после регистрации лекарственного средства имеет важное значение и позволяет продолжать мониторинг соотношения польза/риск лекарственного средства. Работников здравоохранения просят сообщать о любых подозреваемых побочных реакциях через национальную систему отчетности.
— повышенная чувствительность к активному веществу или к какому-либо из вспомогательных веществ.
Исследования взаимодействия проводились только на взрослых.
На основании результатов экспериментов in vitro и известного пути выведения тенофовира возможность взаимодействий, опосредованных CYP450, при участии тенофовира и других лекарственных средств низкая.
Одновременное применение не рекомендовано
Виреад® не следует применять с другими лекарственными средствами, содержащими тенофовира дизопроксила фумарат или тенофовира алафенамид.
Виреад® не следует применять одновременно с адефовира дипивоксилом.
Диданозин. Одновременное применение тенофовира дизопроксила фумарата и диданозина не рекомендуется (см. раздел «Особые указания» и таблицу 2).
Лекарственные средства, которые выводятся через почки. Поскольку тенофовир выводится преимущественно почками, одновременное применение тенофовира дизопроксила фумарата с лекарственными препаратами, снижающими почечную функцию или конкурирующими за активную канальцевую секрецию путем транспортных белков hOAT 1, hOAT 3 или MRP 4 (например, с цидофовиром), может повышать концентрацию тенофовира в сыворотке крови и (или) лекарственных препаратов, вводимых одновременно.
Необходимо избегать применения тенофовира дизопроксила фумарата с одновременным или недавним применением нефротоксических лекарственных средств (например, аминогликозидов, амфотерицина B, фоскарнета, ганцикловира, пентамидина, ванкомицина, цидофовира и интерлейкина-2) (см. раздел «Особые указания»).
Учитывая, что такролимус может влиять на функцию почек, рекомендуется тщательное наблюдение при его одновременном применении с тенофовира дизопроксила фумаратом.
Другие взаимодействия
Взаимодействия между тенофовира дизопроксила фумаратом и другими лекарственными препаратами представлены ниже в Таблице 2 (увеличение обозначено «↑», уменьшение – «↓», отсутствие изменений – «↔», два раза в сутки – «b.i.d.» и один раз в сутки – «q.d.»).
Исследования, проведенные с другими лекарственными средствами
Не наблюдалось клинически значимых фармакокинетических взаимодействий при одновременном применении тенофовира дизопроксила фумарата с эмтрицитабином, ламивудином, индинавиром, эфавирензом, нельфинавиром, саквинавиром (усиленным ритонавиром), метадоном, рибавирином, рифампицином, такролимусом и гормональным контрацептивом норгестиматом/этинилэстрадиолом.
Тенофовира дизопроксила фумарат следует принимать вместе с едой, поскольку пища повышает биодоступность тенофовира (см. раздел «Фармакокинетика»).
Перед тем, как начать терапию тенофовира дизопроксила фумаратом, следует предложить анализ на антитела к ВИЧ всем пациентам, инфицированным вирусом гепатита В (см. ниже раздел «Одновременное инфицирование ВИЧ‑1 и гепатитом B»).
ВИЧ-1
Несмотря на то, что эффективное подавление вируса при антиретровирусной терапии значительно снижает риск передачи вируса половым путем, остаточный риск исключить невозможно. Следует применять меры профилактики передачи вируса в соответствии с национальными рекомендациями.
Хронический гепатит В
Пациенты должны быть проинформированы об отсутствии доказательств того, что тенофовира дизопроксила фумарат предотвращает риск передачи ВИЧ или вируса гепатита В другим лицам путем полового контакта или попадания в кровь. Необходимо продолжать принимать соответствующие меры предосторожности.
Одновременное применение с другими лекарственными средствами
— Виреад® не следует применять с другими лекарственными средствами, содержащими тенофовира дизопроксила фумарат или тенофовира алафенамид.
— Виреад® не следует применять одновременно с адефовира дипивоксилом.
— Не рекомендуется одновременное применение тенофовира дизопроксила фумарата и диданозина. Одновременное применение тенофовира дизопроксила фумарата и диданозина приводит к 40–60 % повышению системной экспозиции диданозина, что может увеличивать риск связанных с диданозином побочных действий (см. раздел «Лекарственные взаимодействия»). Сообщалось о нечастых, иногда летальных, случаях панкреатита и лактат-ацидоза. Одновременное применение тенофовира дизопроксила фумарата и диданозина в дозе 400 мг в сутки было связано со значительным уменьшением количества клеток CD4, возможно из-за межклеточного взаимодействия, что повышает фосфорилированный (то есть активный) диданозин. Применение диданозина в уменьшенной дозировке 250 мг вместе с терапией тенофовира дизопроксила фумаратом, было связано с сообщениями о высокой частоте вирусологически неудачного лечения при нескольких исследованных комбинациях для лечения ВИЧ-1 инфекции.
Тройная терапия с нуклеозидами/нуклеотидами
Поступали сообщения о высокой частоте вирусологически неудачного лечения и о появлении резистентности на ранней стадии у ВИЧ-пациентов, если тенофовира дизопроксила фумарат сочетался с ламивудином и абакавиром, а также с ламивудином и диданозином по схеме введения 1 раз в сутки.
Влияние на функцию почек и кости у взрослых
Влияние на функцию почек. Тенофовир, главным образом, выводится почками. Поступали сообщения о почечной недостаточности, нарушениях функции почек, повышенном уровне креатинина, гипофосфатемии и проксимальной тубулопатии (включая синдром Фанкони) при применении тенофовира дизопроксила фумарата в клинической практике (см. раздел «Побочные действия»).
Контроль функции почек. Рекомендуется определение клиренса креатинина у всех пациентов до начала лечения тенофовира дизопроксила фумаратом и наблюдение за функцией почек (клиренс креатинина и уровень фосфата в сыворотке) после 2-4 недель лечения, после 3 месяцев лечения, а затем – каждые 3-6 месяцев при отсутствии риска нарушения функции почек. Пациенты с повышенным риском нарушения почечной функции нуждаются в более частом наблюдении за функцией почек.
Ведение пациентов с нарушением функции почек. Если уровень фосфата в сыворотке крови < 1.5 мг/дл (0.48 ммоль/л) или клиренс креатинина снижен до < 50 мл/мин. у пациента, получающего тенофовира дизопроксила фумарат, необходимо провести повторную оценку функции почек в течение 1 недели, включая определение уровня глюкозы в крови, калия в крови и концентрации глюкозы в моче (см. раздел «Побочные действия», проксимальная тубулопатия). Следует также рассмотреть необходимость отмены лечения тенофовира дизопроксила фумаратом у взрослых пациентов со снижением клиренса креатинина до < 50 мл/мин. или снижением уровня фосфата в сыворотке крови до < 1.0 мг/дл (0.32 ммоль/л). Прерывание приема тенофовира дизопроксила фумарата также рекомендуется в случае прогрессирующего снижения функции почек, если не удается обнаружить другую причину этого состояния.
Совместное применение и риск почечной токсичности. Необходимо избегать применения тенофовира дизопроксила фумарата с одновременным или недавним применением нефротоксических лекарственных средств (например, аминогликозидов, амфотерицина B, фоскарнета, ганцикловира, пентамидина, ванкомицина, цидофовира и интерлейкина-2). Если одновременного применения тенофовира дизопроксила фумарата и нефротоксических средств избежать невозможно, необходимо еженедельно наблюдать за функцией почек.
У пациентов, получающих тенофовира дизопроксила фумарат и имеющих факторы риска нарушения функции почек, зарегистрированы случаи острой почечной недостаточности после начала приема высоких доз или нескольких нестероидных противовоспалительных препаратов (НПВП). При одновременном приеме НПВП и тенофовира дизопроксила фумарата следует тщательно следить за функцией почек.
Повышенный риск поражения почек отмечен у пациентов, получающих тенофовира дизопроксила фумарат в сочетании с ритонавиром или усиленным кобицистатом ингибитором протеаз. Такие пациенты нуждаются в тщательном наблюдении за функцией почек (см. раздел «Лекарственные взаимодействия»). При наличии факторов риска поражения почек следует тщательно оценить необходимость совместного применения тенофовира дизопроксила фумарата с усиленными ингибиторами протеаз.
Не было проведено клинических оценок тенофовира дизопроксила фумарата у пациентов, получающих лекарственные средства, которые выводятся тем же путем – почками, включая транспортные белки транспортеров органических анионов человека (human organic anion transporter – hOAT) 1 и 3 или MRP 4 (например, цидофовир – известное нефротоксическое лекарственное средство). Эти почечные транспортные белки могут быть причиной тубулярной секреции и частично почечного выведения тенофовира и цидофовира. Поэтому фармакокинетика лекарственных средств, которые выводятся тем же почечным путем, включая транспортные белки hOAT 1 и 3 или MRP 4, может изменяться в случае одновременного применения. При отсутствии крайней необходимости, одновременное применение лекарственных средств, которые выводятся одинаково почечным путем, не рекомендуется. Если такого применения избежать невозможно, следует еженедельно наблюдать за функцией почек (см. раздел «Лекарственные взаимодействия»).
Нарушение функции почек. Безопасность тенофовира для почек исследовалась в очень ограниченной степени у пациентов с нарушением почечной функции (клиренс креатинина < 80 мл/мин).
Пациенты с клиренсом креатинина < 50 мл/мин., в том числе пациенты, которым необходим гемодиализ. Данные о безопасности и эффективности действия тенофовира дизопроксила фумарата для пациентов с нарушенной функцией почек ограничены. По этой причине тенофовира дизопроксила фумарат необходимо применять, только если потенциальная польза лечения считается превышающей потенциальный риск. Применение тенофовира дизопроксила фумарата пациентам с тяжелыми нарушениями функции почек (клиренс креатинина < 30 мл/мин.) и пациентам, которым необходим гемодиализ, не рекомендуется. Если ни одно альтернативное лечение недоступно, необходимо корректировать интервал дозирования и внимательно следить за функцией почек (см. раздел «Способ применения и дозы» и «Фармакокинетика»).
Воздействие на кости. У ВИЧ-инфицированных пациентов во время клинических исследований, в котором лечили тенофовира дизопроксила фумаратом наблюдали небольшое уменьшение минеральной плотности бедренных и позвоночных костей после 144 недель лечения, однако, не наблюдалось повышенного риска переломов или признаков клинически существенных отклонений состояния костей от нормы.
Наиболее выраженное снижение МПК наблюдалось у пациентов, получавших тенофовира дизопроксила фумарат в составе схемы лечения, включавшей в себя усиленный ингибитор протеазы. Следует рассмотреть альтернативные схемы лечения для пациентов с остеопорозом, у которых повышен риск переломов.
Костные аномалии (которые нечасто были одной из причин переломов) могут быть связаны с проксимальной почечной тубулопатией (см. раздел «Побочные действия»). При подозрении или выявлении костных аномалий, необходимо получить соответствующие консультации.
Влияние на функцию почек и кости у детей
Отдаленные последствия влияния на кости и токсическое воздействие на почки у детей окончательно не установлены. Кроме того, не до конца установлена обратимость токсического воздействия на почки. Поэтому рекомендуется использовать многосторонний подход для адекватного определения в каждом отдельном случае соотношения польза/риск лечения, принятия решения о соответствующем наблюдении в ходе лечения (включая принятие решения об отмене терапии) и рассмотрения целесообразности применения дополнительных препаратов.
Контроль функции почек. Перед началом лечения необходимо провести оценку функции почек (клиренс креатинина и уровень фосфата в сыворотке), а также необходимо осуществлять наблюдение в ходе лечения, как и для взрослых (см. выше).
Ведение пациентов с нарушением функции почек. Если у любого пациента детского возраста, получающего тенофовира дизопроксила фумарата, уровень фосфата в сыворотке крови определяется как < 3.0 мг/дл (0.96 ммоль/л), необходимо провести повторную оценку функции почек в течение 1 недели, включая определение уровня глюкозы в крови, калия в крови и концентрации глюкозы в моче (см. раздел «Побочные действия», проксимальная тубулопатия). При подозрении на аномалии со стороны почек или обнаружении таких аномалий необходимо проконсультироваться с нефрологом с целью рассмотрения необходимости отмены лечения тенофовира дизопроксила фумаратом. Прерывание приема тенофовира дизопроксила фумарата также рекомендуется в случае прогрессирующего снижения функции почек, если не удается обнаружить другую причину этого состояния.
Совместное применение и риск почечной токсичности. Необходимо следовать тем же рекомендациям, которые применимы для взрослых (см. выше).
Нарушение функции почек. Не рекомендуется применять тенофовира дизопроксила фумарат у детей с нарушением функции почек (см. раздел «Способ применения и дозы»). Не следует начинать терапию тенофовира дизопроксила фумаратом у детей с нарушением функции почек, а также необходимо отменить лечение у тех пациентов детского возраста, у которых нарушение функции почек развилось в течение терапии тенофовира дизопроксила фумаратом.
Воздействие на кости. Виреад® может стать причиной уменьшения минеральной плотности костей. Влияние изменения минеральной плотности костей, связанного с тенофовира дизопроксила фумаратом на здоровье костей в отдаленной перспективе и на риск переломов в будущем в настоящее время неизвестно (см. раздел «Фармакодинамика»).
При выявлении костных аномалий у детей или при подозрении на таковые необходимо проконсультироваться с эндокринологом и/или нефрологом.
Заболевания печени
Данные относительно безопасности и эффективности для пациентов с пересаженной печенью очень ограничены.
Данные относительно безопасности и эффективности приема тенофовира дизопроксила фумарата для пациентов, инфицированных гепатитом В, с декомпенсированным заболеванием печени и степенью > 9 по классификации Child-Pugh-Turcotte (CPT), ограничены. Такие пациенты могут иметь более высокий риск серьезных побочных действий со стороны печени и почек. Вследствие этого необходимо тщательно контролировать гепатобилиарные и почечные параметры у данной популяции пациентов.
Обострение гепатита
Обострение во время лечения. Спонтанные обострения хронического гепатита типа B являются относительно частыми и характеризуются временным повышением уровня аланинаминотрансферазы (АЛТ) в сыворотке крови. После начала антивирусного лечения у некоторых пациентов может повышаться уровень АЛТ в сыворотке крови (см. раздел «Побочные действия»). У пациентов с компенсированным заболеванием печени эти повышения уровня АЛТ в сыворотке крови обычно не сопровождаются повышением концентрации билирубина в сыворотке крови или печеночной декомпенсацией. Пациенты с циррозом печени могут иметь повышенный риск печеночной декомпенсации после обострения гепатита, а потому за ними необходимо тщательно наблюдать во время лечения.
Обострение после прекращения лечения. Также сообщалось об остром приступе гепатита у пациентов, прекративших лечение гепатита B. Обострения после лечения обычно связаны с повышением ДНК вируса гепатита В, и большинство из них оказываются самоограниченными. Однако сообщалось о тяжелых обострениях, включая летальные случаи. В течение 6 месяцев после прекращения лечения гепатита В необходимо регулярно контролировать функциональное состояние печени по клиническим и лабораторным показателям. В случае необходимости может быть целесообразным возобновление лечения гепатита B. Для пациентов с развитым заболеванием печени или циррозом прекращение лечения не рекомендуется, поскольку обострение гепатита после лечения может привести к печеночной декомпенсации.
У пациентов с некоменсированным заболеванием печени обострения гепатита особенно серьезные, а иногда летальные.
Сопутствующее инфицирование гепатитом C или D. Данные относительно эффективности тенофовира у пациентов с сопутствующим инфицированием вирусом гепатита C или D отсутствуют.
Сопутствующее инфицирование ВИЧ‑1 и гепатитом B. В связи с риском развития ВИЧ-резистентности у пациентов с сопутствующим инфицированием ВИЧ/вирусом гепатита В тенофовира дизопроксила фумарат необходимо применять только как часть соответствующей антиретровирусной комбинированной схемы. Пациенты, у которых ранее были нарушения функции печени, включая хронический активный гепатит, имеют повышенную частоту нарушений функции печени во время комбинированной антиретровирусной терапии, и за ними необходимо наблюдать в соответствии со стандартной практикой. При наличии признаков ухудшения течения заболевания печени у таких пациентов, следует рассмотреть вопрос о необходимости перерыва в лечении или отмене лечения. Однако необходимо отметить, что повышение уровня АЛТ может быть частью клиренса у больных вирусным гепатитом В во время лечения тенофовиром, см. выше «Обострение гепатита».
Применение с некоторыми противовирусными средствами для лечения гепатита C
Было показано, что одновременный прием тенофовира дезопроксила фумарата с ледипасвиром/софосбувиром или софосбувиром/велпатасвиром повышает концентрацию тенофовира в плазме крови, в особенности при применении совместно со схемой лечения при ВИЧ, включающей в себя тенофовира дизопроксила фумарат и фармакокинетический усилитель (ритонавир или кобицистат). Безопасность тенофовира дизопроксила фумарата на фоне приема ледипасвира/софобусвира или софобусвира/велпатасвира и фармакокинетического усилителя не была установлена. Следует принимать во внимание потенциальные риски и пользу, связанные с совместным применением ледипасвира/софосбувира или софосбувира/велпатасвира с тенофовира дизопроксила фумаратом, принимаемым в сочетании с усиленным ингибитором протеазы ВИЧ (например, атазанавиром или дарунавиром), в особенности у пациентов с повышенным риском развития нарушения функции почек. Пациентов, получающих ледипасвир/софосбувир или софосбувир/велпатасвир одновременно с тенофовира дизопроксила фумаратом и усиленным ингибитором протеазы ВИЧ, следует наблюдать на предмет побочных реакций, связанных с тенофовира дизопроксила фумаратом.
Вес и показатели метаболизма
Возможно увеличение веса и повышение уровня липидов и глюкозы в крови во время антиретровирусной терапии. Такие изменения могут частично быть связаны с контролем заболевания и образом жизни. Относительно липидов в некоторых случаях имеются доказательства эффективности лечения, тогда как в отношении увеличения массы тела нет убедительных доказательств, связывающих его с тем или иным видом лечения. Относительно мониторинга уровня липидов и глюкозы в крови см. установленные рекомендации по лечению ВИЧ. В случае клинической необходимости необходимо контролировать нарушение метаболизма липидов.
Нарушения митохондриальной функции при воздействии in utero
Нуклеозидные аналоги способны воздействовать на митохондриальную функцию в различной степени; наиболее выраженным это воздействие является для ставудина, диданозина и зидовудина. Поступали сообщения о митохондриальной дисфункции у ВИЧ-отрицательных детей раннего возраста, подвергшихся воздействию нуклеозидных аналогов in utero и (или) в постнатальный период; они касались преимущественно схем лечения, включавших в себя зидовудин. Основными побочными реакциями, о которых сообщалось, были гематологические нарушения (анемия, нейтропения) и метаболические нарушения (гиперлактатемия, гиперлипаземия). Эти явления часто носили кратковременный характер. Поступали редкие сообщения о неврологических нарушениях, которые начинались позднее (гипертония, конвульсии, аномальное поведение). На сегодняшний день неизвестно, являются ли такие неврологические нарушения временными или постоянными. Эти результаты следует принимать во внимание для любого ребенка, подвергшегося воздействию аналогов нуклеозида in utero, у которого наблюдаются тяжелые клинические проявления неизвестной этиологии, в особенности неврологические проявления. Эти результаты не влияют на текущие национальные рекомендации о применении антиретровирусного лечения беременным женщинам для профилактики вертикальной передачи ВИЧ.
Синдром иммунной реактивации
У ВИЧ-инфицированных пациентов с тяжелой иммунной недостаточностью на момент введения КАРТ может возникнуть воспалительная реакция на асимптоматические или остаточные оппортунистические патогены, что может быть причиной серьезных клинических состояний или усиления симптомов. Как правило, такие реакции наблюдались в течение первых нескольких недель или месяцев начала КАРТ. Соответствующими примерами являются цитомегаловирусный ретинит, генерализованные и (или) очаговые микобактериальные инфекции и пневмония Pneumocystis jiroveci. Любые воспалительные симптомы необходимо оценивать и при необходимости назначать лечение.
Также сообщалось об аутоимунных нарушениях (например, болезни Грейвса) при синдроме иммунной реактивации. Однако описанное время проявления таких нарушений более вариабельно и эти явления могут возникнуть через много месяцев после начала лечения.
Остеонекроз
Хотя этиология считается многофакторной (включая применение кортикостероидов, употребление алкоголя, тяжелое угнетение иммунитета, высокое значение индекса массы тела), о случаях остеонекроза сообщалось, в частности, относительно пациентов с развитым ВИЧ-заболеванием и (или) длительным влиянием комбинированной антиретровирусной терапии (КАРТ). Пациентам следует рекомендовать обратиться за советом к врачу, если они испытывают боли в суставах, негибкость суставов или затруднения во время движений.
Пациенты пожилого возраста
Тенофовира дизопроксила фумарат не был исследован у пациентов старше 65 лет. Пациенты старшего возраста имеют большую вероятность ухудшения функции почек, поэтому необходимо быть осторожным при лечении тенофовира дизопроксила фумаратом пациентов пожилого возраста.
Виреад® содержит лактозы моногидрат. Поэтому данный препарат не следует принимать пациентам с такими редкими наследственными заболеваниями, как непереносимость галактозы, недостаточность лактазы лопарей (саамов), или синдром мальабсорбции глюкозы и галактозы.
Фертильность, беременность и грудное вскармливание
Беременность
Ограниченные данные, полученные от беременных женщин (в пределах 300 – 1,000 беременностей, завершившихся рождением ребенка), указывают на отсутствие пороков развития или токсического воздействия на плод/новорожденного, которые были бы связаны с тенофовира дизопроксила фумаратом. Исследования на животных не указывали на токсическое воздействие на репродуктивную функцию. При необходимости можно рассмотреть целесообразность применения тенофовира дизопроксила фумарата во время беременности.
Кормление грудью
Исследования показали, что тенофовир выделяется в грудное молоко. Данные о влиянии тенофовира на новорожденных и детей первого года жизни недостаточны. Поэтому Виреад® не следует применять в период кормления грудью.
В целом рекомендуется, чтобы инфицированные женщины c ВИЧ- и вирусом гепатита В не кормили грудью во избежание передачи ВИЧ ивируса гепатита В ребенку.
Фертильность
Имеется ограниченное количество клинических данных о влиянии тенофовира дизопроксила фумарата на фертильность. Исследования на животных не выявили неблагоприятного влияния тенофовира дизопроксила фумарата на фертильность.
Пациенты младше 12 лет
В связи с отсутствием клинических данных о безопасности и эффективности препарата Виреад® 300 мг у детей младше 12 лет, его применение не рекомендуется.
Особенности влияния лекарственного средства на способность управлять транспортом и другими потенциально опасными механизмами
Исследования относительно влияния тенофовира на способность управлять автотранспортом и использовать механизмы не проводились. Пациентов следует проинформировать о сообщенных случаях головокружения при лечении тенофовира дизопроксила фумаратом.
Симптомы: в случае передозировки пациент должен находиться под наблюдением относительно признаков токсичности (см. раздел «Побочные действия»). Следует применять стандартную поддерживающую терапию по мере необходимости.
Лечение: тенофовир может выводиться с помощью гемодиализа, медианное значение клиренса тенофовира составляет 134 мл/мин. Неизвестно, выводится ли тенофовир с помощью перитонеального диализа.
По 30 таблеток в полиэтиленовом флаконе с влагопоглотителем, закрытом крышечкой, которую не могут открыть дети.
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке.
Хранить при температуре не выше 30 °С.
Хранить в недоступном для детей месте!
5 лет
Не применять по истечении срока годности.
По рецепту
Производитель
Такеда ГмбХ, Бетрибсстетте Ораниенбург, Леницштрассе 70-98, 16515, Ораниенбург, Германия.
Владелец регистрационного удостоверения
Гилеад Сайенсиз, Инк., 333 Лейксайд Драйв, Фостер Сити, Калифорния 94404, США.
МАВИРЕТ не оказывает или оказывает незначительное влияние на способность управлять транспортом и работать с механизмами.
Лекарственное средство МАВИРЕТ содержит лактозу
Если у Вас есть непереносимость некоторых сахаров, проконсультируйтесь с врачом перед
началом приема лекарственного средства МАВИРЕТ.
Как принимать лекарственное средство Мавирет
Всегда принимайте это лекарственное средство так, как Вам назначил Ваш лечащий врач.
Проконсультируйтесь с Вашим лечащим врачом, в случае если Вы не уверены. Ваш врач определит длительность Вашего лечения.
Как много принимать
Рекомендованная доза лекарственного средства МАВИРЕТ 100 мг/40 мг – три таблетки один раз в день. Три таблетки в одном блистере — это дневная доза.
Как принимать
Принимайте лекарственное средство вместе с едой.
Проглатывайте таблетки целиком
Таблетки следует проглатывать целиком или по половине, не разжевывать, не раздавливать и не разламывать на мелкие части.
Если после приема лекарственного средства МАВИРЕТ возникла рвота, то это может повлиять на содержание лекарственного средства в крови и сделать его работу не такой эффективной.
Если рвота возникла в течение 3 часов после приема дозы, то следует принять дополнительную дозу лекарственного средства МАВИРЕТ.
Если прошло более 3-х часов после приема дозы и возникла рвота, то дополнительная доза не требуется и следующий прием лекарственного средства должен быть по запланированному ранее графику.
Если Вы приняли дозу большую, чем должны были
Если Вы случайно приняли дозу большую, чем рекомендованная Вам врачом, то Вам следует обратиться к врачу в ближайшее лечебное учреждение. Возьмите с собой упаковку лекарственного средства, чтобы показать врачу, что вы приняли.
Если Вы забыли принять лекарственное средство Мавирет
Очень важно не пропускать прием лекарственного средства.
Если Вы все же пропустили время приема лекарственного средства, определите, сколько времени прошло с последнего приема лекарственного средства МАВИРЕТ:
Если прошло менее 18 часов с момента, когда Вы должны были принять очередную дозу, то примите дозу лекарственного средства МАВИРЕТ как можно скорее. Следующая доза должна быть принята в обычное время.
Если прошло более 18 часов с момента, когда Вы обычно принимаете лекарственное средство МАВИРЕТ, подождите и примите следующую дозу по обычному графику. Не принимайте двойную дозу (близко по времени).
Если у Вас есть вопросы касательно приема этого лекарственного средства — обратитесь к Вашему лечащему врачу.
Возможные нежелательные реакции
Это лекарственное средство может стать причиной возникновения нежелательных реакций, как и любое другое лекарственное средство. Нежелательные реакции могут возникать не у всех.
Сообщите Вашему лечащему врачу, если Вы отметили у себя любое з перечисленных ниже нежелательных эффектов:
Очень часто возникают: могут встречаться у более чем 1 человека из 10
Чувство усталости
Головная боль
Часто возникают: могут встречаться у 1 человека из 10
Чувство тошноты (рвота)
Диарея
Чувство слабости или недостаток сил (астения)
Сообщения о нежелательных реакциях
Если Вы обнаружили у себя нежелательную реакцию на применение данного лекарственного средства, сообщите об этом Вашему лечащему Врачу, даже если эти реакции не перечислены в инструкции по применению.
Также Вы можете сообщить о возникшей нежелательной реакции по указанному адресу, телефону или на почту:
1-й Загородный переулок, 20, 10 этаж, офис 30 (1007),
Минск, Республика Беларусь, 220073.
Тел.: + 375 17 256 97 37.
Факс: +375 17 256 97 47.
E-mail: .
Сообщая о нежелательных реакциях, Вы тем самым помогаете собирать информацию о безопасности этого лекарственного средства.
Как хранить лекарственное средство Мавирет
Хранить в недоступном для детей месте.
Не требует особых условий хранения.
Не использовать по истечении срока годности указанного на упаковке.
Неиспользованное лекарственное средство или отходы следует утилизировать в соответствии с местными нормами законодательства.
Из чего состоит лекарственное средство Мавирет
Активными веществами являются глекапревир и пибрентасвир. Каждая таблетка содержит 100 мг глекапревира и 40 мг пибрентасвира.
Другие составляющие таблетки:
Ядро таблетки: коповидон (К 28), витамина Е (токоферол) полиэтиленгликоль сукцинат, кремния диоксид безводный, полиэтиленгликоля монокаприлат (тип II), натрия кроскармеллоза, натрия стеарилфумарат
Покрытие таблетки: гипромелоза 2910 (Е 464), лактозы моногидрат титан диоксид, макрогол 3350, железа оксид красный (Е 172).
Как выглядит лекарственное средство Мавирет и что содержится в упаковке
Лекарственное средство МАВИРЕТ — это продолговатые двояковыпуклые таблетки розового цвета, покрытые пленочной оболочкой, и с тиснением «NXT» на одной стороне.
Лекарственное средство МАВИРЕТ упаковано в блистер из фольги, содержащий 3 таблетки. Всего в картонной пачке лекарственного средства МАВИРЕТ 84 таблетки вместе с инструкцией по медицинскому применению, которые содержатся в 4-х пачках картонных, каждая из которых содержит 21 таблетку.
Производитель
Выпуск серии
Эббви Дойчленд ГмбХ и Ко. КГ, Германия Abbvie Deutschland GmbH & Со. KG, Germany.
Владелец регистрационного удостоверения
Эббви Биофармасьютикалс ГмбХ, Швейцарская Конфедерация
AbbVie Biopharmaceuticals GmbH (Switzerland).
Мавирет — инструкция по применению
Синонимы, аналоги
Статьи
РЕГИСТРАЦИОННЫЙ НОМЕР
ЛП-004804
ТОРГОВОЕ НАИМЕНОВАНИЕ
Мавирет
МЕЖДУНАРОДНОЕ НЕПАТЕНТОВАННОЕ ИЛИ ГРУППИРОВОЧНОЕ НАИМЕНОВАНИЕ
Глекапревир + Пибрентасвир
ЛЕКАРСТВЕННАЯ ФОРМА
Таблетки, покрытые пленочной оболочкой
СОСТАВ
Действующие вещества: глекапревир 100.0 мг, пибрентасвир 40.0 мг
Вспомогательные вещества: коповидон К 28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия. натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadryu II 32F240023)’. гипромеллоза 2910. лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
ОПИСАНИЕ
Продолговатые двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета с гравировкой «NXT» на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА
Противовирусное средство
КОД ATX
Не присвоен.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Механизм действия
Препарат Мавирет — это комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах — глекапрсвира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Глекапревир
Глекапревир представляет собой ингибитор протеазы вируса гепатита С (ВГС) NS3/4A. которая необходима для протеолитического расщепления кодирующего вирус гепатита С полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A, и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз вируса гепатита С NS3/4A из клинических изолятов вируса генотипов la, lb, 2а, 2Ь, За, 4а. 5а и 6а со значениями IC50 от 3,5 до 11,3 нМ.
Пибрентасвир
Пибрентасвир является пангенотипным ингибитором белка NS5A вируса гепатита С, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная иктивностъ
Значения ЕС5о глекапрсвира и пибрентасвира против полноразмерных или гибридных репликонов. кодирующих NS3 или NS5A из лабораторных штаммов, представлены в таблице 1.
Таблица 1. Активность глекапрсвира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
|
Подтип ВГС |
ЕС50 глекапрсвира, нМ |
ЕС50 пибрентасвира, нМ |
|
1а |
0.85 |
0,0018 |
|
lb |
0.94 |
0,0043 |
|
2а |
2,2 |
0,0023 |
|
2Ь |
4,6 |
0,0019 |
|
За |
1,9 |
0,0021 |
|
4а |
2.8 |
0,0019 |
|
5а |
Н/П |
0,0014 |
|
6а |
0.86 |
0,0028 |
Н/П — неприменимо.
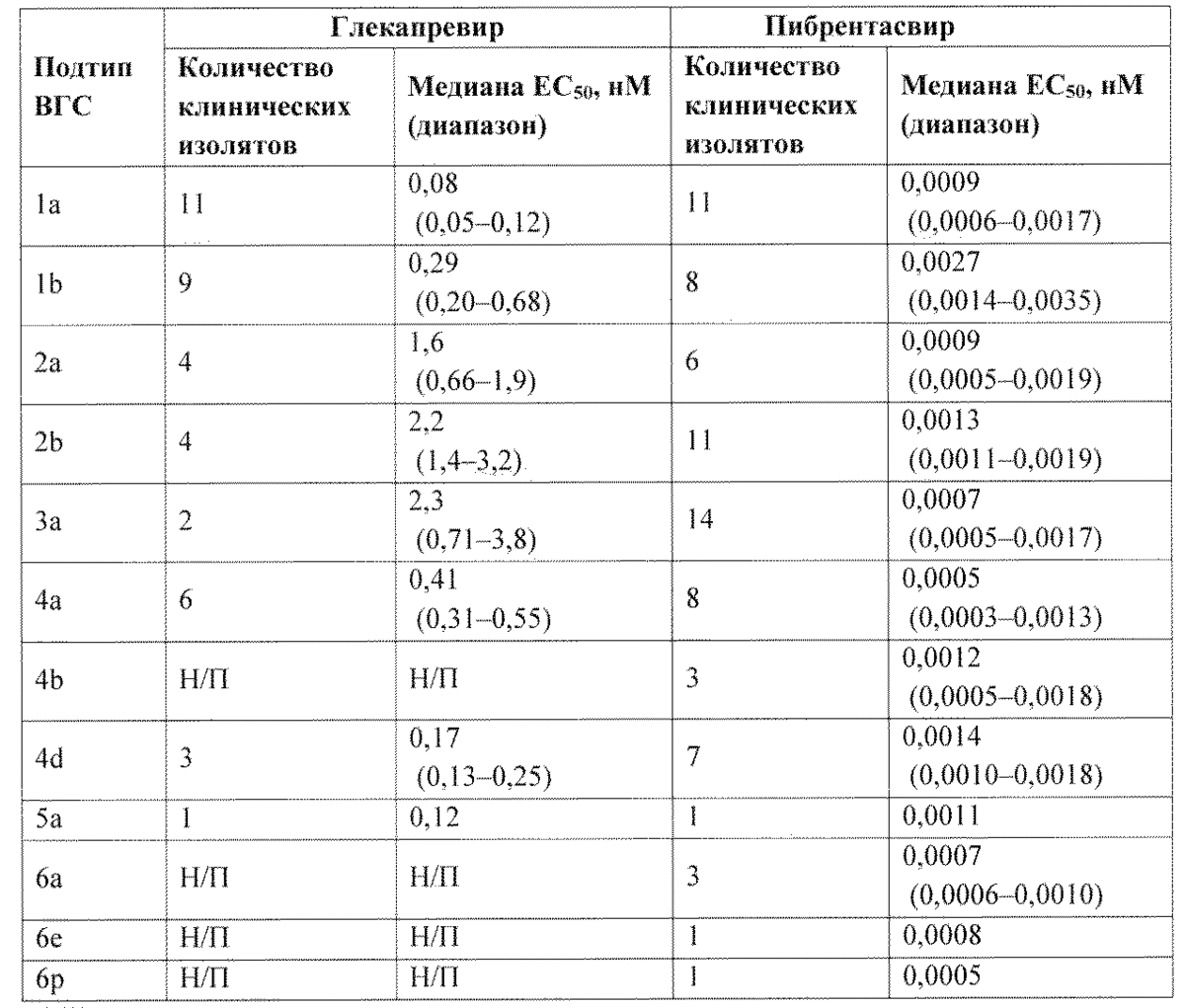
Значения ЕС50 глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в таблице 2.
Таблица 2. Активность глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1-6
Н/П — неприменимо.
Активность in vitro
Оценка комбинации глекапрсвира и пибрентасвира на репликонных клеточных культурах генотипа ВГС 1 не выявила каких-либо признаков антагонизма противовирусной активности. Резистентность
В культуре клеток
Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A. выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54. 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапрсвира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1-4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе За, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58. 92 или 93 в NS5A в генотипах 1-6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе За замены в аминокислотах А30К или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и За (включая A30K+Y93H в генотипе За) демонстрируют снижение чувствительности к пибрентасвиру. Применение у детей
Нет данных о применении препарата у детей.
Применение у пациентов пожилого возраста
В клинические исследования препарата Мавирет были включены 328 пациентов в возрасте 65 лет и старте (13,8% от общего числа пациентов). Частота достижения вирусологического ответа в группе пациентов в возрасте > 65 лет была аналогична таковой у пациентов в возрасте < 65 лет.
Фармакокинетика
Фармакокинетические свойства компонентов препарата Мавирет представлены в таблице 3.
|
Таблица 3. Фармакокинетические свойства компонентов препарата Мавирет у здоровых добровольцев |
||||||||||||||||||||||||||||||||||||||||||
|
a. Медиана Ттах у здоровых добровольцев после приема однократной дозы глекапрсвира и пибрентасвира
b. Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров
c. Прием однократной дозы [14С] глекапрсвира или [|4С] пибрентасвира в исследованиях массового баланса
d. Окислительные метаболиты или их продукты обмена составляли 26 % радиоактивной дозы. Метаболиты глекапрсвира в плазме нс наблюдались.
У пациентов с хроническим гепатитом С без цирроза, после 3 дней монотерапии либо только глекапревиром 300 мг в день (N=6) или только пибрентасвиром 120 мг в день (N=8), геометрическое среднее значения AUC24 составило 13600 нг-ч/мл для глекапрсвира и 459 нг-ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекресного взаимодействия между глекапревиром и пибрентасвиром. Основываясь на популяционной фармакокинетической модели для препарата Мавирет при хроническом гепатите С, установившиеся значения AUC24 для глекапрсвира и пибрентасвира были 4800 и 1430 нг-ч/мл у пациентов без цирроза (N=1804), и 10500 и 1530 нг-ч/мл у пациентов с циррозом печени (N=280), соответственно. По сравнению со здоровыми пациентами (N=230), популяционные оценки AUC24, ss были аналогичны (разница в 10%) для глекапрсвира и на 34 % ниже для пибрентасвира у пациентов, инфицированных вирусом гепатита С без цирроза.
Линейность / нелинейность
AUC глекапрсвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы (при приеме 1200 мг один раз в день, наблюдалась в 516 раз больше экспозиция, чем 200 мг один раз в день). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы до 120 мг (120 мг один раз в день наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг один раз в день), но установленная линейная фармакокинетика в дозах > 120 мг. Нелинейное увеличение экспозиции <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром составляет в 3 раза выше по сравнению с применением только пибрентасвира. У глекапрсвира наблюдалось меньшее влияние пибрентасвира.
Особые группы пациентов
Раса/этническая принадлежность
Не требуется коррекция дозы препарата Мавирет в зависимости от расы или этнической принадлежности.
Пол/масса тела
Не требуется коррекция дозы препарата Мавирет в зависимости от пола или массы тела. Пациенты пожилого возраста
У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется. Популяционный фармакокинетический анализ ВГС-инфицированных пациентов в возрасте от 18 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапрсвира и пибрентасвира.
Пациенты с нарушением почечной функции
Значение AUC глекапрсвира и пибрентасвира повышалось не более, чем на 56 % у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с пациентами с нормальной функцией почек. Значение AUC глекапрсвира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница <18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапрсвира на 86 % выше, а пибрентасвира на 54 % выше, чем у
пациентов с нормальной функцией почек. Мри оценке концентраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
В целом, изменения воздействия препарата Мавирет у ВГС-инфицированных пациентов с нарушением функции почек на диализе или без него, не были клинически значимыми. Пациенты с печеночной недостаточностью
Мри приеме рекомендованнной дозы значение AUC глекапрсвира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Мью было на 33 % выше, класса 13 — на 100% выше, а класса С — в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени. Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26 % выше у пациентов с печеночной недостаточностью класса В и на 114% — класса С. При оценке концетраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема препарата Мавирет пациентами с ВГС и компенсированным циррозом печени, воздействие глекапрсвира было примерно в 2 раза выше, а пибрентасвира — аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапрсвира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Показания к применению
Лечение хронического гепатита С у взрослых.
Противопоказания
• Повышенная чувствительность к любому действующему веществу препарата или к
любому из вспомогательных веществ.
• Пациенты с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью), см.
разделы «Способ применения и дозы» и «Фармакокинетика».
• Совместное применение со следующими препаратами: атазанавир. аторвастатин,
симвастатин, дабигатрана этексилат, препараты, содержащие эстрадиол, сильными индукторами Р-гликопротеина и CYP3A, например, рифампицин, карбамазепин, препараты зверобоя продырявленного Hypericum perjoratum, фенобарбитал, фенитоин, примидон, (см. раздел «Взаимодействие с другими лекарственными средствами»).
• Детский возраст до 18 лет.
• Дефицит лактазы, недостаточность лактозы, глюкозо-галактозная мальабсорбция.
С ОСТОРОЖНОСТЬЮ
Препарат Мавирет не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг в день).
Препарат Мавирет следует применять с осторожностью со следующими препаратами: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ Беременность
Данные о применении глекапрсвира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности. Исследования глекапрсвира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапрсвира. что исключило возможность дальнейших исследований. В качестве меры предосторожности, препарат Мавирет не рекомендуется применять во время беременности.
Период грудного вскармливания
Неизвестно, выделяется ли глекапревир или пибрентасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапрсвира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию препаратом Мавирет или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины. Фертильность
Исследования влияния глекапрсвира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапрсвира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз препаратов.
Способ применения и дозы
Для приема внутрь.
1аблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать. Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С.
Дозы
Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг (три таблетки по 100 мг/40 мг) один раз в сутки во время еды.
В таблицах 1 и 2 представлена рекомендуемая продолжительность лечения препаратом Мавирет на основе данных, полученных на популяции пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. с компенсированным циррозом печени или без него.
|
Таблица 1. Рекомендованная продолжительность лечения для пациентов, ранее не получавших лечение |
||||||||
|
|
Таблица 2. Рекомендованная продолжительность лечения для пациентов, не ответивших на предыдущую терапию пегилированным интерфероном (пег-ИНФ) + рибавирнн (совместно с софосбувиром или без него) или софосбувир + рибавирин |
|||||||||||
|
|||||||||||
|
Для пациентов, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A см информацию в разделе «Особые указания». |
Пропуск приема препарата
В случае пропуска приема препарата Мавирет его можно осуществить в течение 18 часов после планового времени приема. Если с момента планового времени приема препарата Мавирет прошло более 18 часов, не следует принимать пропущенную дозу, а следующую дозу следует принять в обычное время по расписанию. Не следует принимать двойную дозу препарата.
Если в течение 3 часов после приема препарата Мавирет произошла рвота, то необходимо принять дополнительную дозу препарата. Если рвота произошла позднее 3 часов после применения препарата Мавирет, то прием дополнительной дозы не требуется.
Применение у пациентов пожилого возрасти
У пожилых пациентов коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушенной функцией почек
У пациентов почечной недостаточности, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушением функции печени
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата Мавирет не требуется. Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью) (см. разделы «Противопоказания», «Особые указания»). Дети
Отсутствуют данные о безопасности и эффективности применения препарата Мавирет у детей и подростков в возрасте до 18 лет.
Пациенты после трансплантации печени
Пациентам после трансплантации печени препарат Мавирет необходимо применять в течение как минимум 12 недель (см. раздел «Особые указания»).
Следует рассмотреть увеличение продолжительности терапии (в течение 16 недель) у пациентов с генотипом 3, которые ранее получали терапию пег-ИФН + рибавирин (совместно с софосбувиром или без него) или софосбувир + рибавирин.
Пациенты с ко-инфекцией ВГС/ВИЧ-1
Следует выполнять рекомендации, указанные в Таблице 1 и 2. Рекомендации по дозированию препарата Мавирет при совместном применении с препаратами для терапии ВИЧ-1 представлены в разделе «Взаимодействие с другими лекарственными средствами».
Побочное действие
Резюме профиля безопасности
Оценка безопасности препарата Мавирет у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам исследований фазы 2 и 3, в которых участвовали около 2 300 пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. получавших Мавирет в течение 8, 12 или 16 недель.
Наиболее частыми нежелательными реакциями (частота > 10 %) были головные боли и утомляемость. Менее чем у 0,1 % пациентов, получавших лечение препаратом Мавирет, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение препаратом Мавирет по причине развития нежелательных реакций, составила 0.1 %. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Таблица нежелательных реакций
Сообщалось о развитии следующих нежелательных реакций у пациентов, получавших лечение препаратом Мавирет. Ниже приведен список нежелательных реакций, сгруппированных согласно классу систем органов и по частоте встречаемости. Частота встречаемости определяется следующим образом: очень часто (> 1/10), часто (от >1/100 до < 1/10), нечасто (от > 1/1 000 до < 1/100), редко (от >1/10 000 до < 1/1 000) и очень редко (< 1/10 000).
Таблица 1. Нежелательные реакции, наблюдавшиеся при приеме препарата Мавирет
|
Частота развития |
Нежелательные реакции |
|
Нарушения со стороны нервной системы |
|
|
Очень часто |
Головная боль |
|
Нарушения со стороны желудочно-кишечного тракта |
|
|
Часто |
Тошнота, диарея |
|
Общие нарушения и реакции в месте введения |
|
|
Очень часто |
Утомляемость |
|
Часто |
Астения |
Описание отдельных нежелательных реакций
Нежелательные реакции у пациентов с тяжелым нарушением функции почек, включая пациентов на диализе
Безопасность препарата Мавирет у пациентов с хронической болезнью почек (стадия 4 или стадия 5, включая пациентов на диализе) и хронической инфекцией, вызванной вирусом гепатита С генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него) была оценена на 104 пациентах. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17 %) и утомляемость (12 %).
Оценка безопасности у пациентов с коинфекцией ВГС/ВИЧ-1
Общий профиль безопасности у пациентов с коинфекцией ВГС/ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови
У 1,3 % пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше верхней границы нормы, что было связано с глекапревир-опосредованным ингибированием белков-переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ. Прямая гипербилирубинемия наблюдалась у 0,3 % пациентов.
ПЕРЕДОЗИРОВКА
Наибольшая задокументированная доза, принятая здоровыми добровольцами, составила 1200 мг один раз в день в течение 7 дней для глекапрсвира и 600 мг один раз в день в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5 раз ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапрсвира (700 мг или 800 мг) 1 раз в день в течение > 7 дней. В случае передозировки, необходимо контролировать состояние пациента на наличие признаков токсического поражения (см. раздел «Побочное действие»). Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапрсвира и пибрентасвира.
Взаимодействие с другими лекарственными препаратами
Возможное влияние препарата Мавирет на другие лекарственные препараты
Глекапревир и пибрентасвир — это ингибиторы Р-гликопротеина (P-GP), белка резистентности рака молочной железы (BCRP) и полипептида, транспортирующего органические анионы (ОАТР) 1В1/3.
Одновременное применение с препаратом Мавирет может привести к повышению концентрации в плазме препаратов, являющихся субстратами Р-гликопротеина (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или ОАТР1В1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). См. рекомендации по лекарственному взаимодействию с чувствительными субстратами Р-гликопротеина, BCRP и ОАТР1В1/3 в таблице 1. Для других субстратов Р-гликопротеина. BCRP и ОАТР1В1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир — это слабые ингибиторы изоферментов системы цитохрома Р450 CYP3A и уридин-глюкуронозилтрансферазы (UGT) 1А1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1AI (ралгегравир) при одновременном приеме с препаратом Мавирет.
Применение глекапрсвира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1A2, CYP2C9, CYP2C19, CYP2D6. UGT1А6, UGT1А9. UGT1А4, UGT2B7, OCTI, ОСТ2, ОАТ1, ОАТЗ, МАТЕ1 и МАТЕ2К.
Пациенты, получающие антагонисты витамина К
На фоне лечения препаратом Мавирет может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг международного нормализованного отношения (МНО). Потенциальное влияние других лекарственных препаратов на препарат Мавирет
Совместный прием с сильными индукторами Р-гликопротеина/СУРЗА
Лекарственные препараты, являющиеся сильными индукторами Р-гликопротеина и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон), могут вызвать существенное снижение концентрации глекапрсвира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта препарата Мавирет и потере вирусологического ответа. Применение таких препаратов одновременно с препаратом Мавирет противопоказано (см. раздел «Противопоказания»).
Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются умеренными индукторами Р-гликопротеина и CYP3A, может вызвать снижение концентрации глекапрсвира и пибрентасвира в плазме крови (окскарбазепин. эсликарбазепин, лумакафтор. кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. раздел «Особые указания»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков Р-гликопротеина и (или) BCRP. Глекапревир также является субстратом транспортеров печеночного захвата ОАТР1В1/3. Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются ингибиторами Р-гликопротеина и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир), может замедлить выведение глекапрсвира и пибрентасвира и может вызвать повышение экспозиции противовирусных препаратов в плазме крови. Лекарственные препараты, являющиеся ингибиторами ОАТР1В1/3 (элвитегравир. циклоспорин, дарунавир. лоиинавир), могут вызвать повышение системной концентрации глекапрсвира.
Установленные и другие потенциально возможные лекарственные взаимодействия
В таблице 1 приведено влияние отношения средних значений, вычисленных методом наименьших квадратов (90-процентный доверительный интервал) на концентрацию препарата Мавирет и сопутствующих лекарственных препаратов. Направление стрелки указывает направление изменения воздействия (Сmax и AUC) глекапрсвира, пибрентасвира и сопутствующего лекарственного препарата ( ↑—увеличение более чем на 25 %, ↓ — снижение более чем на 20 %, ↔ — нет изменения (снижение на менее или равно 20 % или увеличение на менее или равно 25 %).
Таблица 1. Взаимодействия между препаратом Мавирет и другими лекарственными средствами
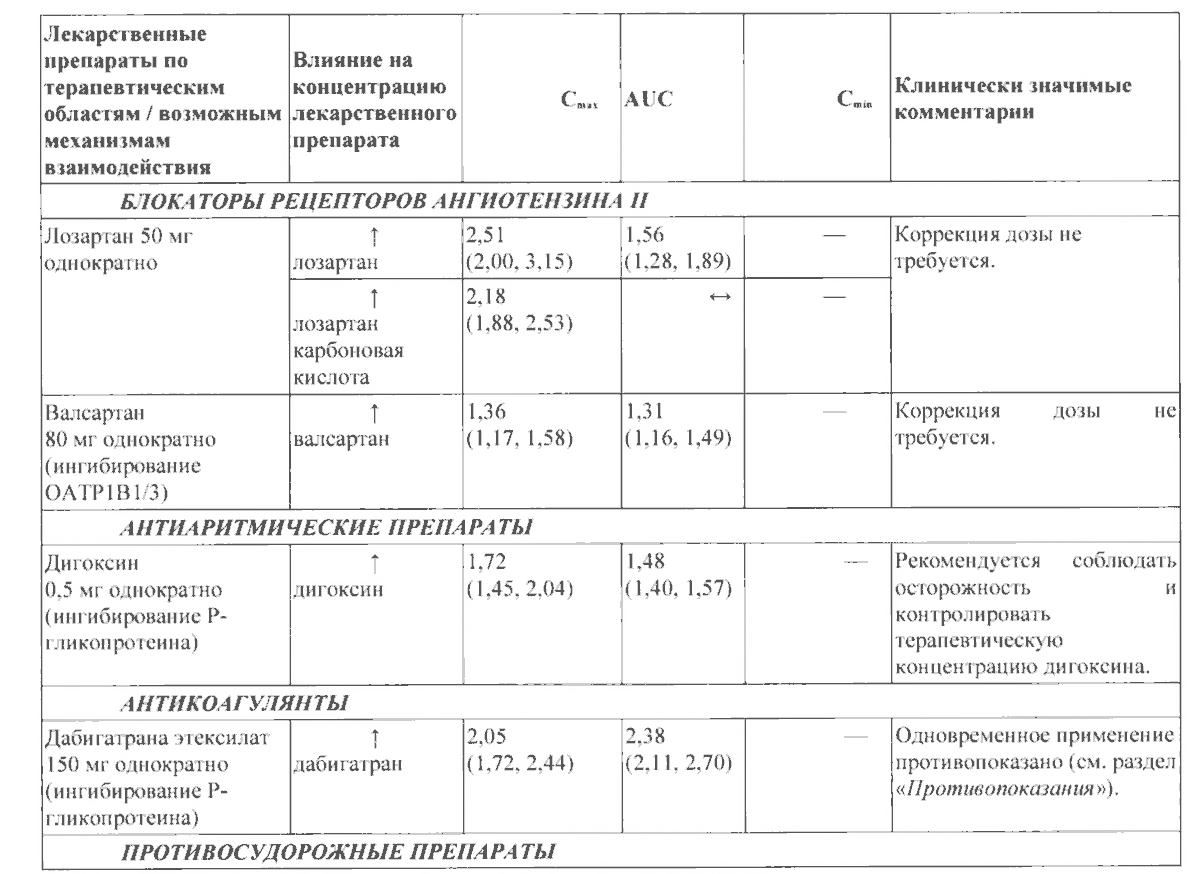
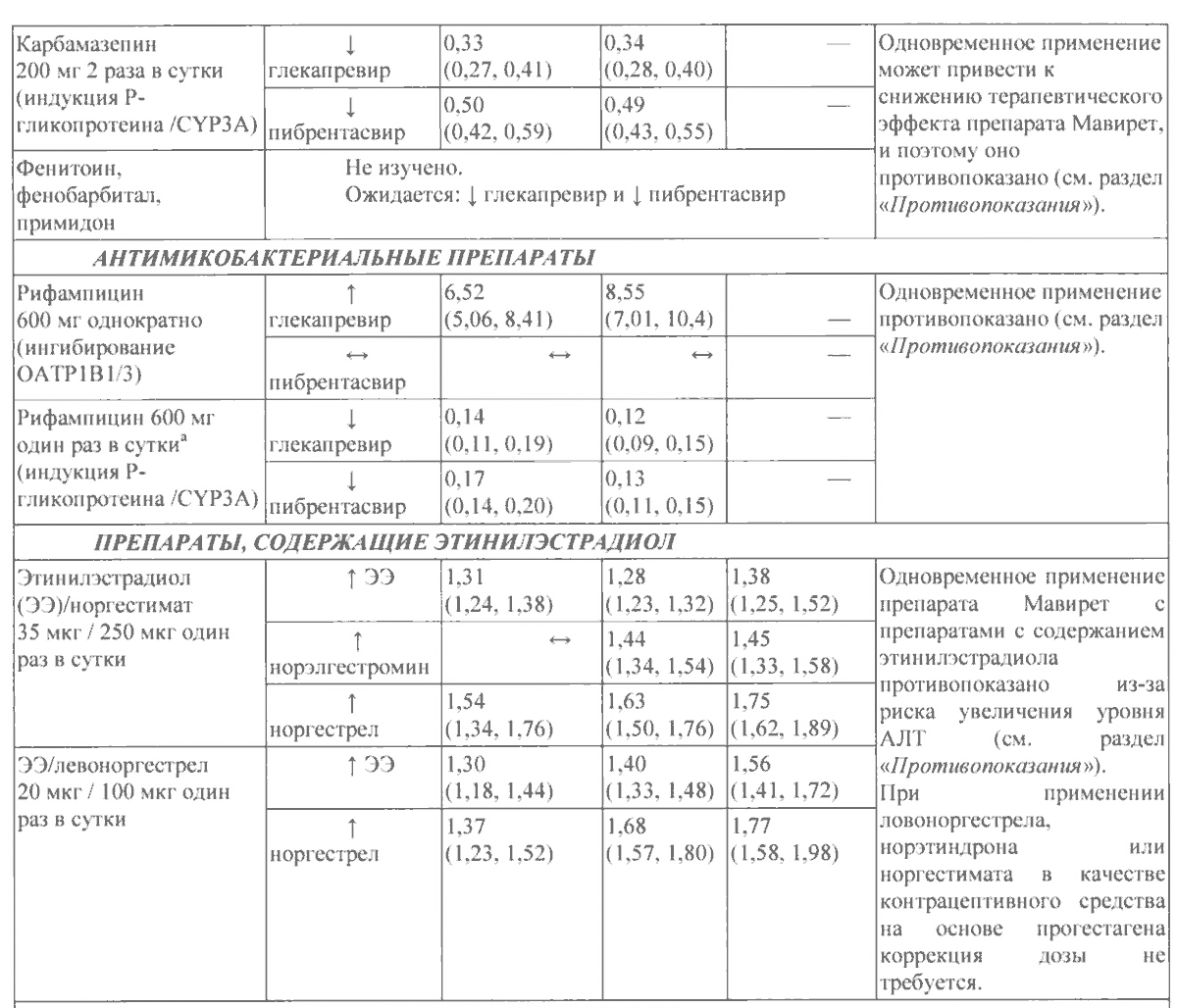
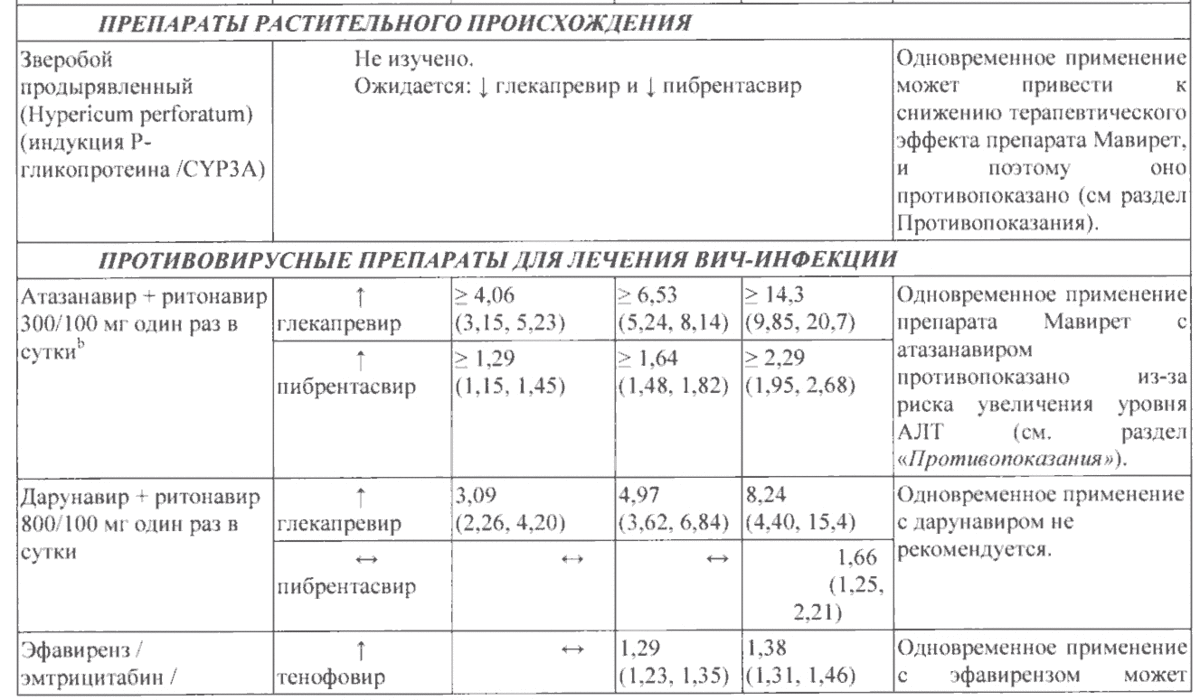


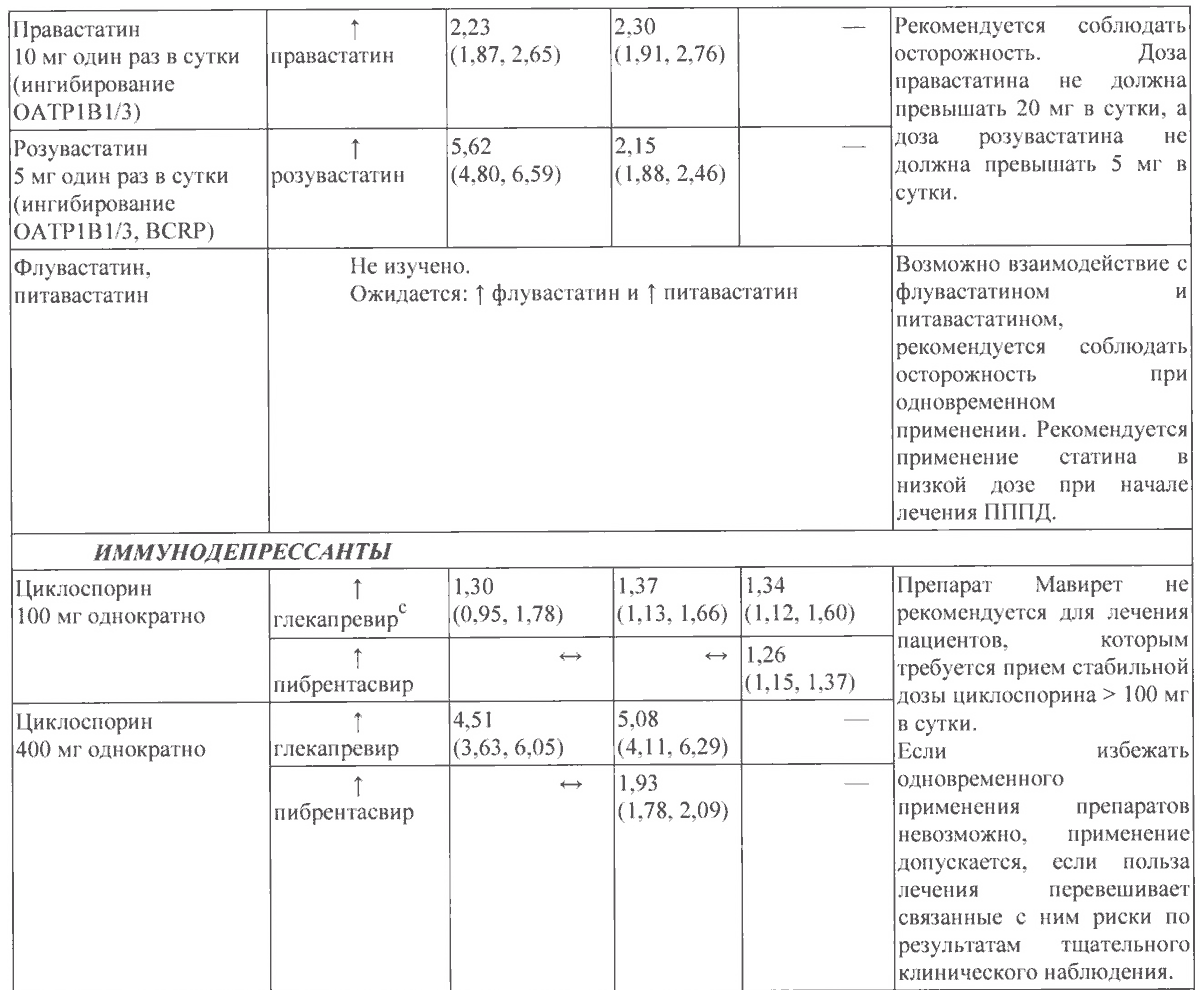

Г1ППД — противовирусный препарат прямого действия
a. Влияние рифампицина на глекапревир и пибрентасвир через 24 часа после приема последней дозы рифампицина.
b. Указано влияние атазанавира и ритонавира на первую дозу глекапрсвира и пибрентасвира.
c. Экспозиция глекапрсвира у инфицированных ВГС пациентов после трансплантации, получавших циклоспорин в дозе 100 мг в сутки или меньше, была в 4 раза выше, чем у тех. кто нс получал циклоспорин.
Дополнительные исследования межлекарственного взаимодействия проводились со следующими лекарственными препаратами: абакавир. амлодипин, бупренорфин, кофеин, декстрометорфан, долутегравир. эмтрицитабин. фелодипин. ламивудин. ламотриджин, метадон, мидазолам. налоксон, норэтиндрон или другие контрацептивные средства, содержащие прогестин, рилпивирин, тенофовир алафенамид и толбутамид. Клинически значимого взаимодействия не выявлено.
ОСОБЫЕ УКАЗАНИЯ
Реактивация вирусного гепатита В
Во время лечения противовирусными препаратами прямого действия сообщалось о реактивации вируса гепатита В, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие ВГВ. Пациенты с коинфекцией ВГВ/ВГС подвержены риску реактивации ВГВ. поэтому следует проводить их мониторинг и ведение с соблюдением современных рекомендаций.
Пациенты после трансплантации печени
Безопасность и эффективность применения препарата Мавирет у пациентов, перенесших трансплантацию печени, не оценивались. Лечение препаратом Мавирет в соответствии с рекомендованным способом применения и дозами (см. раздел «Способ применения и дозы») должно основываться на оценке потенциальной пользы и рисков для каждого конкретного пациента.
Нарушение функции печени
Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. разделы «Способ применения и дозы», «Противопоказания»).
Пациенты, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A
Была изучена вероятность развития устойчивости к глекапревиру/пибрентасвиру у пациентов, инфицированных вирусом генотипа 1, и ограниченного количества пациентов, инфицированных вирусом генотипа 4, не ответивших на предшествующую схему терапии. Как и ожидалось, риск неудачи терапии был выше у пациентов с предшествующей терапией включающей оба класса препаратов (ингибиторы NS5A и NS3/4A). Методика для прогнозирования неудачи терапии на основе исходных данных об устойчивости к терапии не определена. Развитие устойчивости к обоим классам препаратов было основной находкой у пациентов, не ответивших на терапию глекапревиром/пибрентасвиром. Данные о повторном лечении пациентов, инфицированных вирусом генотипов 2, 3, 5 и 6, отсутствуют. Применение препарата Мавирет не рекомендуется для повторного лечения пациентов, ранее получавших лечение ингибиторами NS3/4A и/или NS5A.
Взаимодействие с другими лекарственными препаратами
Подробную информацию см. в разделе «Взаимодействие с другими лекарственными средствами».
Влияние на способность управлять транспортных средствами, механизмами
Препарат Мавирет не оказывает влияния или оказывает незначительное влияние на способность к вождению транспортных средств и управлению механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые пленочной оболочкой. 100 мг + 40 мг.
По 3 таблетки, покрытые пленочной оболочкой, в блистере из поливинилхлорид/полиэтилен/полихлоротрифторэтилена и алюминиевой фольги.
По 7 блистеров в пачке картонной, по 4 пачки картонных вместе с инструкцией по применению в пачке картонной.
СРОК годности
2 года. Не использовать после истечения срока годности, указанного на упаковке.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 25 °C.
Хранить в местах, недоступных для детей.
УСЛОВИЯ ОТПУСКА
Отпускается по рецепту.
ВЛАДЕЛЕЦ РЕГИСТРАЦИОННОГО УДОСТОВЕРЕНИЯ
ООО «ЭббВи», Россия
125047, г. Москва, ул. Лесная, д. 7, этаж 4, помещение 1
Производитель
Производитель готовой лекарственной формы
Фурнье Лэбораториз Айрлэнд Лимитед, Ирландия / Fournier Laboratories Ireland Limited, Ireland Эннгроув, Карригтвохилл, Ко. Корк, Ирландия / Anngrove, Carrigtwohill, Со. Cork. Ireland Фасовщик (первичная упаковка), упаковщик (вторичная упаковка), выпускающий контроль
качества
ЭббВи Дойчланд ГмбХ и Ко.КГ, Германия / AbbVie Deutschland GmbH & Со.KG. Germany Кыолльштрассе, 67061 Людвигсхафен, Германия / Knollstrasse. 67061 Ludwigshafen. Germany
НАИМЕНОВАНИЕ И АДРЕС ОРГАНИЗАЦИИ, УПОЛНОМОЧЕННОЙ ПРИНИМАТЬ ПРЕТЕНЗИИ НА ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ
ООО «ЭббВи», Россия
125047, г. Москва, ул. Лесная, д.7,
БЦ «Белые Сады», здание «А»
тел. (495) 258 42 77
факс(495)258 42 87
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Обобщенные научные материалы по действующему веществу препарата АВИФАВИР (таблетки, покрытые пленочной оболочкой, 200 мг)
Дата последней актуализации: 28.01.2021
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Фармакология
- Показания к применению
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Особые указания
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Владелец РУ
Кромис ООО
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
www.grls.rosminzdrav.ru, 2020.
Фармакологическая группа
Фармакология
Фармакодинамика
Противовирусная активность in vitro
Фавипиравир обладает противовирусной активностью против лабораторных штаммов вирусов гриппа А и В (полумаксимальная эффективная концентрация (EC50) 0,014–0,55 мкг/мл). Для штаммов вирусов гриппа А и В, резистентных к адамантану (амантадин и римантадин), осельтамивиру или занамивиру, ЕС50 составляет 0,03–0,94 и 0,09–0,83 мкг/мл соответственно. Для штаммов вируса гриппа А (включая штаммы, резистентные к адамантану, осельтамивиру и занамивиру), таких как свиной грипп типа А и птичий грипп типа А, включая высокопатогенные штаммы (в т.ч. H5N1 и H7N9), ЕС50 составляет 0,06–3,53 мкг/мл.
Для штаммов вирусов гриппа А и В, резистентных к адамантану, осельтамивиру и занамивиру, ЕС50 составляет 0,09–0,47 мкг/мл, перекрестная резистентность не наблюдается.
Фавипиравир ингибирует вирус SARS-CoV-2, вызывающий новую коронавирусную инфекцию (COVID-19). ЕС50 в клетках Vero Е6 составляет 61,88 мкмоль, что соответствует 9,72 мкг/мл.
Механизм действия
Фавипиравир метаболизируется в клетках до рибозилтрифосфата фавипиравира (РТФ фавипиравира) и избирательно ингибирует РНК-зависимую РНК-полимеразу, участвующую в репликации вируса гриппа. РТФ фавипиравира (1000 мкмоль/л) не показал ингибирующего действия на α-ДНК человека, но показал ингибирующее действие в диапазоне от 9,1 до 13,5% на β- и в диапазоне от 11,7 до 41,2% на γ -ДНК человека. Ингибирующая концентрация (IC50) РТФ фавипиравира для полимеразы II РНК человека составила 905 мкмоль/л.
Резистентность
После 30 пересевов в присутствии фавипиравира не наблюдалось изменений в восприимчивости вирусов гриппа типа А к фавипиравиру, резистентных штаммов также не наблюдалось. В проведенных клинических исследованиях не обнаружено появление вирусов гриппа, резистентных к фавипиравиру.
Фармакокинетика
Всасывание
Фавипиравир легко всасывается в ЖКТ. Тmах составляет 1,5 ч.
Распределение
Связывание с белками плазмы составляет около 54%.
Метаболизм
Фавипиравир в основном метаболизируется альдегидоксидазой и частично — до гидроксилированной формы — ксантиноксидазой. В клетках метаболизируется РТФ фавипиравира. Из других метаболитов, кроме гидроксилата, в плазме крови и моче человека регистрировали также конъюгат глюкуроната.
Выведение
В основном фавипиравир выводится почками в виде активного метаболита гидроксилата, небольшое количество — в неизмененном виде. Т1/2 составляет около 5 ч.
Особые группы пациентов
Нарушение функции печени. При приеме фавипиравира пациентами с печеночной недостаточностью легкой и средней степени тяжести (классы А и В по классификации Чайлд-Пью) увеличение Сmах и AUC составило 1,5 и 1,8 раза соответственно по сравнению со здоровыми добровольцами. У пациентов с печеночной недостаточностью тяжелой степени тяжести (класс С по классификации Чайлд-Пью) увеличение Сmах и AUC составляло 2,1 и 6,3 раза соответственно.
Нарушение функции почек. У пациентов с почечной недостаточностью средней степени тяжести (СКФ <60 и ≥30 мл/мин) остаточная концентрация фавипиравира (Ctrough) увеличивалась в 1,5 раза по сравнению с пациентами без нарушения функции почек. У пациентов с почечной недостаточностью тяжелой и терминальной степени тяжести (СКФ <30 мл/мин) фавипиравир не изучался.
Показания к применению
Лечение новой коронавирусной инфекции (COVID-19).
Противопоказания
Повышенная чувствительность к фавипиравиру; печеночная недостаточность тяжелой степени тяжести (класс С по классификации Чайлд-Пью); почечная недостаточность тяжелой и терминальной степени тяжести (СКФ <30 мл/мин); беременность или планирование беременности; период грудного вскармливания; детский возраст до 18 лет.
Ограничения к применению
Подагра и гиперурикемия в анамнезе (возможно повышение уровня мочевой кислоты в крови и обострение симптомов); печеночная недостаточность легкой и средней степени тяжести (классы А и В по классификации Чайлд-Пью); почечная недостаточность средней степени тяжести (СКФ <60 и ≥30 мл/мин); пожилой возраст.
Применение при беременности и кормлении грудью
В доклинических исследованиях фавипиравира в дозировках, схожих с клиническими или меньшими, наблюдалась гибель эмбриона на ранней стадии и тератогенность.
Фавипиравир противопоказан беременным женщинам, а также мужчинам и женщинам во время планирования беременности. При назначении фавипиравира женщинам, способным к деторождению (в т.ч. в постменопаузе менее 2 лет), необходимо подтвердить отрицательный результат теста на беременность до начала лечения. Повторный тест на беременность необходимо провести после окончания приема фавипиравира.
Необходимо использовать эффективные методы контрацепции (презерватив со спермицидом) во время применения фавипиравира и после его окончания: в течение 1 мес женщинам и в течение 3 мес мужчинам.
При назначении фавипиравира кормящим женщинам необходимо прекратить грудное вскармливание на время приема и в течение 7 дней после его окончания, т.к. основной метаболит фавипиравира попадает в грудное молоко.
Побочные действия
Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с новой коронавирусной инфекцией (COVID-19), перечислены ниже.
Со стороны нервной системы: головная боль, головокружение.
Со стороны сердца: фибрилляция предсердий.
Со стороны ЖКТ: диарея, тошнота, рвота, запор, глоссит, дискомфорт в эпигастральной области.
Со стороны кожи и подкожных тканей: зуд.
Общие расстройства и нарушения в месте введения: боль в грудной клетке, астения, энантема.
Данные лабораторных и инструментальных обследований: повышение активности АЛТ, ACT и других печеночных ферментов, повышение уровня мочевой кислоты в крови.
Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с гриппозной инфекцией (данные анализа в совокупной популяции, объединенной для оценки безопасности), представлены ниже. Частота возникновения нежелательных реакций оценивалась по классификации ВОЗ как очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000); частота неизвестна (установить частоту по имеющимся данным не представляется возможным).
Со стороны крови и лимфатической системы: часто — нейтропения, лейкопения; редко — лейкоцитоз, моноцитоз, ретикулоцитопения.
Со стороны обмена веществ и питания: часто — гиперурикемия, гипертриглицеридемия; нечасто — глюкозурия; редко — гипокалиемия.
Со стороны иммунной системы: нечасто — сыпь; редко: экзема, зуд.
Со стороны дыхательной системы, органов грудной клетки и средостения: редко — бронхиальная астма, боль в горле, ринит, назофарингит.
Со стороны ЖКТ: часто — диарея; нечасто — тошнота, рвота, боль в животе; редко — дискомфорт в животе, язва двенадцатиперстной кишки, кровянистый стул, гастрит.
Со стороны печени и желчевыводящих путей: часто — повышение активности АЛТ, ACT, ГГТ; редко — повышение активности ЩФ, повышение концентрации билирубина в крови.
Другие: редко — аномальное поведение, повышение активности КФК, гематурия, полип гортани, гиперпигментация, нарушение вкусовой чувствительности, гематома, нечеткость зрения, боль в глазу, вертиго, наджелудочковые экстрасистолы, боль в грудной клетке.
Взаимодействие
Фавипиравир не метаболизируется CYР450, главным образом метаболизируется альдегидоксидазой и частично ксантиноксидазой.
Фавипиравир ингибирует альдегидоксидазу и изофермент CYP2C8, но не индуцирует цитохром CYР450.
Таблица
Взаимодействие фавипиравира с другими ЛС
| ЛС | Признаки, симптомы и лечение | Механизм действия и факторы риска |
| Пиразинамид | Гиперурикемия | Дополнительно повышается реабсорбция мочевой кислоты в почечных канальцах |
| Репаглинид | Может повыситься концентрация репаглинида в крови, возможно развитие нежелательных реакций на репаглинид | Ингибирование CYP2C8 приводит к повышению концентрации репаглинида в крови |
| Теофиллин | Концентрация фавипиравира в крови может повыситься, возможно развитие нежелательных реакций на фавипиравир | Взаимодействие с ксантиноксидазой может привести к повышению концентрации фавипиравира в крови |
| Фамцикловир, сулиндак | Эффективность данных ЛС может быть снижена | Ингибирование фавипиравиром альдегидоксидазы может привести к снижению концентрации активных форм данных ЛС в крови |
Передозировка
Сообщения о передозировке фавипиравира отсутствуют.
Способ применения и дозы
Внутрь, за 30 мин до еды, режим дозирования зависит от массы тела пациента. Прием фавипиравира должен осуществляться после лабораторного подтверждения диагноза и/или при наличии характерной клинической симптоматики.
Меры предосторожности
При развитии побочного действия необходимо сообщать об этом в установленном порядке для осуществления мероприятий по фармаконадзору.
Поскольку в исследованиях фавипиравира на животных наблюдалась смерть эмбрионов и тератогенность, фавипиравир нельзя назначать беременным и предположительно беременным женщинам.
При назначении фавипиравира женщинам, способным к деторождению (в т.ч. в постменопаузе менее 2 лет), необходимо подтвердить отрицательный результат теста на беременность до начала лечения. Женщинам, способным к деторождению, необходимо в полной мере объяснить риски и тщательно проинструктировать их о необходимости использовать наиболее эффективные методы контрацепции с их партнерами во время приема фавипиравира и в течение 1 мес после его окончания (презерватив со спермицидом). При предположении о возможном наступлении беременности необходимо незамедлительно прекратить прием фавипиравира и проконсультироваться с врачом.
При распределении в организме человека фавипиравир попадает в сперму. При его назначении пациентам-мужчинам необходимо в полной мере объяснить риски и тщательно проинструктировать их о необходимости использовать наиболее эффективные методы контрацепции при сексуальных контактах во время приема фавипиравира и в течение 3 мес после его окончания (презерватив со спермицидом). Дополнительно необходимо проинструктировать пациентов-мужчин о необходимости не вступать в сексуальные контакты с беременными женщинами.
При распределении в организме человека фавипиравир попадает в грудное молоко. При его назначении кормящим женщинам необходимо в полной мере объяснить риски и тщательно проинструктировать о необходимости прекратить грудное вскармливание на время приема фавипиравира и в течение 7 дней после его окончания.
Влияние на способность управлять транспортными средствами, механизмами. Во время приема фавипиравира следует соблюдать осторожность при управлении транспортными средствами и работе с механизмами.
Особые указания
Данное ЛС зарегистрировано по процедуре регистрации, предназначенной для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению фавипиравира и будет дополняться по мере поступления новых данных. Применение фавипиравира возможно только в условиях стационарной медицинской помощи.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Наименование
Витавирин.
Формы выпуска
Порошок.
МНН
Имидазолилэтанамид пентандиовой кислоты.
ФТГ
Противовирусное средство.
Описание
Порошок от белого до белого с желтоватым оттенком цвета с запахом лимона, допускается наличие мягких комков.
Состав
Активное вещество: имидазолилэтанамид пентандиовой кислоты – 90 мг;
вспомогательные вещества: сукралоза, ароматизатор лимон лайм, маннит (Е421).
Фармакотерапевтическая группа
Противовирусные средства для системного применения. Противовирусные средства прямого действия.
Код АТС: J05AX21
Фармакологическое действие
Фармакодинамика
Противовирусный лекарственный препарат.
В доклинических и клинических исследованиях имидазолилэтанамид пентандиовой кислоты показал эффективность в отношении вирусов гриппа типа А (A(H1N1), в том числе «свиной» A(H1N1)pdmO9, A(H3N2), A(H5N1) и типа В, аденовируса, вируса парагриппа, респираторно-синцитиального вируса; в доклинических исследованиях: коронавируса, метапневмовируса, энтеровирусов, в том числе вируса Коксаки и риновируса.
Витавирин способствует ускоренной элиминации вирусов, сокращению продолжительности болезни, уменьшению риска развития осложнений.
Механизм действия реализуется на уровне инфицированных клеток за счет стимуляции факторов врожденного иммунитета, подавляемых вирусными белками. В экспериментальных исследованиях, в частности, показано, что имидазолилэтанамид пентандиовой кислоты повышает экспрессию рецептора интерферона первого типа IFNAR на поверхности эпителиальных и иммунокомпетентных клеток. Увеличение плотности интерфероновых рецепторов приводит к повышению чувствительности клеток к сигналам эндогенного интерферона. Процесс сопровождается активацией (фосфорилированием) белка-трансмиттера STAT1, передающего сигнал в ядро клетки для индукции противовирусных генов. Показано, что в условиях инфекции, препарат стимулирует выработку антивирусного эффекторного белка МхА, ингибирующего внутриклеточный транспорт рибонуклеопротеидов различных вирусов, замедляя процесс вирусной репликации.
Лекарственный препарат Витавирин вызывает повышение содержания интерферона в крови до физиологической нормы, стимулирует и нормализует сниженную α-интерферон продуцирующую способность лейкоцитов крови, стимулирует γ-интерферон продуцирующую способность лейкоцитов. Вызывает генерацию цитотоксических лимфоцитов и повышает содержание NK-T клеток, обладающих высокой киллерной активностью по отношению к зараженным вирусами клеткам. Противовоспалительное действие обусловлено подавлением продукции ключевых провоспалительных цитокинов (фактора некроза опухоли (TNF-α), интерлейкинов (1L-1β и IL-6)), снижением активности миелопероксидазы.
В экспериментальных исследованиях показано, что совместное использование имидазолилэтанамида пентандиовой кислоты с антибиотиками повышает эффективность терапии на модели бактериального сепсиса, в том числе, вызванного пенициллин-резистентными штаммами стафилококка.
Проведенные экспериментальные токсикологические исследования свидетельствуют о низком уровне токсичности и высоком профиле безопасности препарата. По параметрам острой токсичности имидазолилэтанамид пентандиовой кислоты относится к 4 классу токсичности – «Малотоксичные вещества» (при определении LD50 в экспериментах по острой токсичности летальные дозы препарата определить не удалось).
Лекарственный препарат не обладает мутагенными, иммунотоксическими, аллергизирующими и канцерогенными свойствами, не оказывает местнораздражающего действия. Витавирин не влияет на репродуктивную функцию, не оказывает эмбриотоксического и тератогенного действия.
При курсовом приеме лекарственного препарата один раз в сутки происходит его накопление во внутренних органах и тканях. При этом качественные характеристики фармакокинетических кривых после каждого введения препарата были тождественными: быстрое повышение концентрации препарата после каждого введения через 0,5-1 час после приема и затем медленное снижение к 24 часам.
Метаболизм
Лекарственный препарат не метаболизируется в организме и выводится в неизменном виде.
Выведение
Основной процесс выведения происходит в течение 24 часов. За этот период выводится 80 % принятой дозы: 34,8 % выводится во временном интервале от 0 до 5 часов и 42,5 % во временном интервале от 5 до 24 часов. Из них 77 % выводится через кишечник и 23 % – через почки.
Показания к применению
Лечение и профилактика гриппа А и В и других острых респираторных вирусных инфекций (аденовирусная инфекция, парагрипп, респираторно-синцитиальная инфекция).
Способ применения и режим дозирования
Внутрь, независимо от приема пищи.
Содержимое пакета растворить в стакане воды, перемешать и выпить как можно скорее.
Для лечения гриппа и острых респираторных вирусных инфекций взрослым назначают по одному пакету один раз в день (90 мг). Длительность лечения 5-7 дней (в зависимости от тяжести состояния).
Прием препарата начинают с момента появления первых симптомов заболевания, желательно не позднее 2 суток от начала болезни.
Для профилактики гриппа и острых респираторных вирусных инфекций после контакта с больными лицами взрослым назначают по одному пакету один раз в день (90 мг), в течение 7 дней.
Не следует пропускать очередной прием суточной дозы препарата (влияние пропуска очередной суточной дозы препарата на эффективность лечения не изучено). В случае пропуска очередной суточной дозы препарата, следует принять следующую дозу как можно раньше и продолжить прием один раз в сутки исходя из нового времени приема препарата (утро, день, вечер). Не следует принимать двойную дозу препарата.
Особые категории пациентов
Пожилые пациенты: коррекции дозы не требуется.
Пациенты с нарушением функции печени и/или почек: коррекции дозы не требуется.
Дети и подростки
Не применяется у детей младше 18 лет.
Побочное действие
Частота развития нежелательных реакций приведена в следующей градации: редко – могут возникать менее чем у 1 человека из 1 000.
Аллергические реакции (редко).
Сообщение о нежелательных реакциях
В случае возникновения нежелательных реакций, в том числе, не указанных в инструкции по применению, следует обратиться к врачу.
Противопоказания
— повышенная чувствительность к активному веществу или любому другому компоненту лекарственного препарата;
— беременность и период кормления грудью;
— детский возраст до 18 лет.
Передозировка
Случаи передозировки препарата не описаны.
Меры предосторожности
Лекарственный препарат не оказывает седативного действия, не влияет на скорость психомоторной реакции и может использоваться у лиц различных профессий, в т.ч. требующих повышенного внимания и координации движений.
Не рекомендуется одновременный прием других противовирусных препаратов.
Применение во время беременности и в период кормления грудью
Беременность
Применение препарата во время беременности не изучалось.
Период кормления грудью
Применение препарата в период кормления грудью не изучалось, поэтому при необходимости применения препарата в данный период следует прекратить грудное вскармливание.
Влияние на способность к управлению автотранспортом и другими потенциально опасными механизмами
Не изучалось, однако, учитывая механизм действия и профиль нежелательных реакций, можно предположить, что препарат не оказывает влияния на способность управлять транспортными средствами и механизмами.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействия
Случаев взаимодействия Витавирина с другими лекарственными препаратами не выявлено.
Условия хранения
В защищенном от влаги месте при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
Упаковка
По 3,0 г в пакеты из материала упаковочного многослойного (пленка полиэтилентерефталатная/пленка полипропиленовая/фольга алюминиевая/пленка полиэтиленовая). По 7 пакетов вместе с инструкцией по медицинскому применению в пачке из картона.
Условия отпуска из аптек
Без рецепта.
Купить Витавирин порошок для приготовления раствора для приема внутрь 90мг в пакетах №7
Цена на Витавирин порошок для приготовления раствора для приема внутрь 90мг в пакетах №7
Инструкция по применению для Витавирин порошок для приготовления раствора для приема внутрь 90мг в пакетах №7