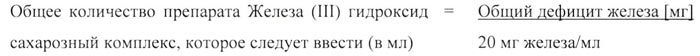СУИФЕРРОВИТ-А инструкция по применению
📜 Инструкция по применению СУИФЕРРОВИТ-А
💊 Состав препарата СУИФЕРРОВИТ-А
✅ Применение препарата СУИФЕРРОВИТ-А
📅 Условия хранения СУИФЕРРОВИТ-А
⏳ Срок годности СУИФЕРРОВИТ-А
Описание лекарственного препарата ветеринарного назначения СУИФЕРРОВИТ-А
Основано на официально утвержденной инструкции по применению
препарата СУИФЕРРОВИТ-А для специалистов
и утверждено компанией-производителем для электронного издания справочника Видаль Ветеринар
2013 года
Дата обновления: 2012.11.19
Лекарственная форма
|
|
СУИФЕРРОВИТ-А |
Раствор д/инъекций рег. №ПВР-2-4.0/02566 |
Форма выпуска, состав и упаковка
Раствор для инъекций в виде непрозрачной жидкости красно-бурого цвета, без осадка, без запаха; хорошо смешивается с водой.
Вспомогательные вещества: витамины группы В: тиамин (вит. В1), рибофлавин (вит. В2), пиридоксин (вит. В6), никотинамид (вит. РР), кальция пантотеноат (вит. В5), фенол, вода д/и.
Расфасован по 10, 20, 100, 200 мл в стеклянные флаконы или по 400, 450, 500 мл в бутылки стеклянные для крови, трансфузионных и инфузионных препаратов, герметично укупоренные резиновыми пробками и обкатанные алюминиевыми колпачками.
Каждый флакон или бутылку маркируют с указанием наименования организации- производителя, ее товарного знака и адреса, наименования лекарственного средства, наименования и содержания действующих веществ, количества лекарственного средства, мл; надписи «Для животных», способа применения, номера серии, срока годности, даты изготовления (месяц, год), обозначения ТУ, условий хранения. Снабжается инструкцией по применению.
Свидетельство о регистрации № ПВР-2-4.0/02566 от 27.08.10
Фармакологические (биологические) свойства и эффекты
Суиферровит-А при в/м или п/к введении всасывается и депонируется в печени и кроветворных органах, таким образом восполняя дефицит в организме железа, меди, кобальта и селена.
Витамины группы В стимулируют процессы кроветворения, в сочетании с железодекстрановым комплексом, усиливают эритропоэз.
Аминокислотно-пептидный комплекс нормализует и активизирует обмен веществ, восстанавливает белковый состав крови, благоприятно действует на иммунную систему, повышая резистентность организма, ускоряет прирост массы тела.
Трехвалентное железо и микроэлементы (медь, кобальт, селен) в лекарственном препарате находятся в форме сложного гидроксид-полиизомальтозного (декстранового) комплекса, способствующего пролонгированному эффективному усвоению.
Биологическое действие объединенного микроэлементного и амино-пептидного комплексов в Суиферровите-А существенно усиливается, благодаря синергическому эффекту.
Суиферровит-А способствует профилактике анемии, отечной болезни и микроэлементозов, отставании в развитии, нарушения обмена веществ, стресса.
Антианемическое действие препарата обусловлено наличием железа (III), меди, кобальта и селена, которые необходимы для синтеза гемоглобина.
Суиферровит-А обладает общеукрепляющим действием, особенно после перенесенных тяжелых заболеваний. Усиливает воспроизводительную функцию животных, способствует восстановлению шерстного покрова, нормализует работу печени, усиливает аппетит.
Суиферровит-А по степени воздействия на организм относится к 4 классу опасности (по ГОСТ 12.1.007-76) — веществам малоопасным.
Показания к применению препарата СУИФЕРРОВИТ-А
- для профилактики и лечения анемии, отечной болезни, нарушения минерального и белкового обмена, отставания в развитии, при стрессах;
- в качестве средства восстановительной терапии после заболеваний, травм, трудных родов, истощения после тяжелой зимовки.
Порядок применения
Суиферровит-А вводят п/к, в/м или в/в. При п/к и в/м введении в месте укола иглы кожу предварительно смещают в сторону, чтобы лекарственное средство не вытекало после инъекции.
В зимнее время перед применением Суиферровит-А подогревают на водяной бане до 36-38°С.
С профилактической целью Суиферровит-А применяют 1 раз в неделю, с лечебной — 2 раза в неделю. Кошкам и собакам с лечебной целью Суиферровит-А применяют 2-3 раза в неделю.
Длительность курса составляет 2-4 недели.
Рекомендуемые профилактические дозы лекарственного средства на одно животное представлены в таблице.
Побочные эффекты
В месте инъекции лекарственного средства может наблюдаться изменение пигментации кожи, исчезающее самопроизвольно в течение нескольких дней.
Побочных явлений и осложнений при введении Суиферровита-А в рекомендуемых дозах не установлено, за исключением индивидуальной повышенной чувствительности к компонентам лекарственного средства.
Противопоказания к применению препарата СУИФЕРРОВИТ-А
- индивидуальная повышенная чувствительность к компонентам лекарственного средства.
Особые указания и меры личной профилактики
Не допускается смешивание Суиферровита-А с другими лекарственными средствами.
Продукцию животноводства во время и после применения Суиферровита-А используют в пищевых целях без ограничений.
При работе с Суиферровитом-А следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными средствами для животных.
Флаконы из-под Суиферровита-А запрещается использовать для пищевых продуктов.
Условия хранения СУИФЕРРОВИТ-А
Препарат следует хранить в сухом, защищенном от прямых солнечных лучей, недоступном для детей месте при температуре от -2°С до +25°С.
Срок годности СУИФЕРРОВИТ-А
Срок годности при соблюдении условий хранения — 2 года, после вскрытия флакона — 12 ч. Флаконы, не использованные в течение 12 ч, подлежат последующей утилизации.
СУИФЕРРОВИТ-А отзывы
Помогите другим с выбором, оставьте отзыв об СУИФЕРРОВИТ-А
Оставить отзыв
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005089
Торговое наименование:
Железа (III) гидроксид сахарозный комплекс
Международное непатентованное или группировочное наименование:
железа (III) гидроксид сахарозный комплекс
Лекарственная форма:
раствор для внутривенного введения
Состав
1 мл препарата содержит:
Действующее вещество:
Железа (III) гидроксид сахарозный комплекс в пересчете на железо (III) – 20,0 мг;
Вспомогательные вещества:
Натрия гидроксид (в виде 10% раствора) – для доведения pH до 10,5 – 11,1, вода для инъекций – до 1,0 мл
Описание:
Раствор коричневого цвета.
Фармакотерапевтическая группа:
Противоанемическое средство, препарат железа для парентерального введения.
Код ATX:
В03АС
Фармакологические свойства
Фармакодинамика
Механизм действия
Активный компонент препарата Железа (III) гидроксид сахарозный комплекс – железосахарозный комплекс – состоит из ядра многоядерного гидроксида железа (III), окруженного большим количеством нековалентно связанных молекул сахарозы. Средняя молекулярная масса этого комплекса примерно равна 43 кДа. Структура многоядерного железосодержащего ядра сходна со структурой ядра белка ферритина – физиологического депо железа. Этот комплекс предназначен для создания управляемого источника утилизируемого железа для белков, отвечающих за транспорт и депонирование железа в организме (соответственно трансферрина и ферритина).
После внутривенного введения многоядерное железосодержащее ядро этого комплекса захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. На следующем этапе железо используется для синтеза гемоглобина, миоглобина и других железосодержащих ферментов, либо хранится преимущественно в печени в форме ферритина.
Фармакокинетика
Распределение
Феррокинетика железо-сахарозного комплекса, меченного 52Fe и 59Fe, оценивалась у пациентов с анемией и хронической почечной недостаточностью. В течение первых 6-8 часов 52Fe захватывался печенью, селезенкой и костным мозгом. Считается, что захват радиоактивной метки селезенкой, богатой макрофагами, является типичным для захвата железа ретикулоэндотелиальной системой.
После внутривенного введения однократной дозы препарата железа (III) гидроксид сахарозного комплекса, содержащей 100 мг железа, здоровым добровольцам максимальные суммарные концентрации железа в сыворотке достигались через 10 минут после инъекции, при этом средняя концентрация составляла 538 мкмоль/л. Объем распределения центральной камеры полностью соответствовал объему плазмы (около 3 л).
Биотрансформация
После инъекции сахароза по большей части распадается, а многоядерное железосодержащее ядро захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. Через 4 недели после введения утилизация железа эритроцитами составляет от 59 до 97%.
Выведение
Средняя молекулярная масса железо-сахарозного комплекса примерно равна 43 кДа, что достаточно много для предотвращения выведения через почки.
Выведение железа почками в первые 4 часа после инъекции дозы препарата железа (III) гидроксид сахарозного комплекса, содержащей 100 мг железа, составляло менее 5% от введенной дозы. Через 24 часа суммарная концентрация железа в сыворотке снижалась до уровня перед введением. Выведение сахарозы почками составляло около 75% от введенной дозы.
Показания для применения
Для лечения железодефицитных состояний в следующих случаях:
- при клинической потребности в быстром восполнении запасов железа;
- у пациентов, которые не переносят пероральные препараты железа или не соблюдают режим лечения;
- при наличии активного воспалительного заболевания кишечника, когда пероральные препараты железа неэффективны.
Противопоказания для применения
- повышенная чувствительность к железо-сахарозному комплексу, раствору железосахарозного комплекса или к любому из компонентов данного лекарственного препарата;
- анемия, не обусловленная дефицитом железа;
- наличие признаков перегрузки железом или врожденные нарушения процессов его утилизации;
- I триместр беременности.
С осторожностью
Пациентам с бронхиальной астмой, экземой, поливалентной аллергией, аллергическими реакциями на иные парентеральные препараты железа и лицам, имеющим низкую железосвязывающую способность сыворотки и/или дефицит фолиевой кислоты железа (III) гидроксид сахарозный комплекс нужно назначать с осторожностью. Также осторожность требуется при введении препаратов железа пациентам с печеночной недостаточностью, с острыми или хроническими инфекционными заболеваниями и лицам, у которых повышены показатели ферритина сыворотки крови в связи с тем, что парентерально вводимое железо может оказывать неблагоприятное действие при наличии бактериальной или вирусной инфекции.
Применение при беременности и в период грудного вскармливания
Умеренное количество данных по применению препарата железа (III) гидроксид сахарозный комплекс беременными женщинами во II и III триместрах беременности не выявило каких-либо угроз для матери или новорожденного.
Однако железа (III) гидроксид сахарозный комплекс следует применять во время II и III триместра беременности только тогда, когда потенциальная польза для матери превышает потенциальный риск для плода
Применение препарата в первом триместре беременности противопоказано.
Результаты исследований на животных не выявили прямых или опосредованных вредных воздействий на течение беременности, развитие эмбриона/плода, роды или постнатальное развитие.
Количество данных по выделению железа с грудным молоком человека после внутривенного введения железо-сахарозного комплекса ограничено. В рамках небольшого клинического исследования здоровые, кормящие грудью матери с дефицитом железа получали 100 мг железа в виде железо-сахарозного комплекса. Через 4 дня после лечения содержание железа в грудном молоке не повышалось, и разницы в сравнении с контрольной группой (n=5) не наблюдалось. Нельзя исключить тот факт, что железо из препарата железа (III) гидроксид сахарозный комплекс может поступать новорожденному/младенцу с молоком матери, поэтому следует проводить оценку соотношения риска и пользы.
Способ применения и дозы
Применение
Препарат Железа (III) гидроксид сахарозный комплекс вводится только внутривенно: путем капельной инфузии, или медленной инъекции, или непосредственно в венозный участок диализной системы.
Перед использованием ампулы/флаконы следует осмотреть на предмет отсутствия осадка или повреждений. Использовать следует только ампулы/флаконы с однородным, не содержащим осадка раствором коричневого цвета.
Каждая ампула/флакон препарата Железа (III) гидроксид сахарозный комплекс предназначены исключительно для одноразового использования. Любые остатки неиспользованного лекарственного препарата или его отходы следует утилизировать в соответствии с локальными требованиями.
Введение препарата Железа (III) гидроксид сахарозный комплекс должно осуществляться под наблюдением медицинского персонала, имеющего опыт диагностики и лечения анафилактических реакций, в условиях специализированного отделения. Должна быть обеспечена возможность проведения противошоковой терапии, включающая 0,1% раствор эпинефрина (адреналина), антигистаминные и/или кортикостероидные препараты. Тест-доза не является надежным прогностическим фактором развития в последующем реакций гиперчувствительности, в связи с чем ее предварительное введение не рекомендуется.
Во время введения препарата и непосредственно после введения пациенты должны находиться под наблюдением врача. При появлении первых признаков анафилактических реакций применение препарата должно быть немедленно прекращено.
Необходимо наблюдать за каждым пациентом в течение как минимум 30 минут после каждого введения препарата Железа (III) гидроксид сахарозный комплекс в терапевтической дозе на предмет отсутствия нежелательных явлений.
Внутривенная капельная инфузия
Железа (III) гидроксид сахарозный комплекс разводится только стерильным 0,9% (масса/объем) раствором натрия хлорида (NaCl). Разведенный раствор должен быть прозрачным, коричневого цвета. Разведение следует производить непосредственно перед инфузией, а полученный раствор следует вводить следующим образом:
| Доза препарата Железа (III) гидроксид сахарозный комплекс (мг железа) | Доза препарата Железа (III) гидроксид сахарозный комплекс (мл препарата Железа (III) гидроксид сахарозный комплекс) | Максимальный объем разведения стерильного 0,9% (масса/объем) раствора NaCl | Минимальное время инфузии |
| 100 мг | 5 мл | 100 мл | 15 минут |
| 200 мг | 10 мл | 200 мл | 30 минут |
| 300 мг | 15 мл | 300 мл | 1,5 часа |
| 400 мг | 20 мл | 400 мл | 2,5 часа |
| 500 мг | 25 мл | 500 мл | 3,5 часа |
Разведение препарата до более низких концентраций железа недопустимо по причинам, связанным со стабильностью раствора.
Внутривенная инъекция
Железа (III) гидроксид сахарозный комплекс может вводиться путем медленной внутривенной инъекции со скоростью 1 мл неразведенного раствора в минуту и его доза не должна превышать 10 мл (200 мг железа) на инъекцию.
Инъекция в венозный участок диализной системы
Железа (III) гидроксид сахарозный комплекс можно вводить во время сеанса гемодиализа непосредственно в венозный участок диализной системы при соблюдении тех же условий, что и для внутривенной инъекции.
Дозы
Для каждого пациента следует индивидуально рассчитывать кумулятивную дозу препарата Железа (III) гидроксид сахарозный комплекс, которую нельзя превышать.
Расчет дозы
Общая кумулятивная доза препарата Железа (III) гидроксид сахарозный комплекс, эквивалентная общему дефициту железа (мг), определяется на основании содержания гемоглобина (Нb) и массы тела (МТ). Дозу препарата Железа (III) гидроксид сахарозный комплекс следует индивидуально рассчитывать для каждого пациента в соответствии с общим дефицитом железа, рассчитанным по нижеприведенной формуле Ганзони, например:
Общий дефицит железа [мг] = масса тела [кг] × (целевое содержание гемоглобина – фактическое содержание гемоглобина) [г/л] × 0,24* + депонированное железо [мг]
При массе тела менее 35 кг: Целевое содержание гемоглобина = 130 г/л, а количество
При массе тела 35 кг и больше: Целевое содержание гемоглобина = 150 г/л, а количество депонированного железа = 500 мг
* Коэффициент 0,24 = 0,0034 (содержание железа в гемоглобине = 0,34%) × 0,07 (масса крови ~ 7% от массы тела) × 1000 (перевод [г] в [мг])
Общее количество препарата Железа (III) гидроксид сахарозный комплекс (мл), которое следует ввести, в зависимости от массы тела, фактического содержания гемоглобина и целевого содержания гемоглобина**:
| Масса тела [кг] | Общее количество препарата Железа (III) гидроксид сахарозный комплекс (20 мг железа на мл), которое следует ввести | |||||||
| гемоглобин 60 г/л | гемоглобин 75 г/л | гемоглобин 90 г/л | гемоглобин 105 г/л | |||||
| мг Fe | мл | мг Fe | мл | мг Fe | мл | мг Fe | мл | |
| 5 | 160 | 8 | 140 | 7 | 120 | 6 | 100 | 5 |
| 10 | 320 | 16 | 280 | 14 | 240 | 12 | 220 | 11 |
| 15 | 480 | 24 | 420 | 21 | 380 | 19 | 320 | 16 |
| 20 | 640 | 32 | 560 | 28 | 500 | 25 | 420 | 21 |
| 25 | 800 | 40 | 700 | 35 | 620 | 31 | 520 | 26 |
| 30 | 960 | 48 | 840 | 42 | 740 | 37 | 640 | 32 |
| 35 | 1260 | 63 | 1140 | 57 | 1000 | 50 | 880 | 44 |
| 40 | 1360 | 68 | 1220 | 61 | 1080 | 54 | 940 | 47 |
| 45 | 1480 | 74 | 1320 | 66 | 1140 | 57 | 980 | 49 |
| 50 | 1580 | 79 | 1400 | 70 | 1220 | 61 | 1040 | 52 |
| 55 | 1680 | 84 | 1500 | 75 | 1300 | 65 | 1100 | 66 |
| 60 | 1800 | 90 | 1580 | 79 | 1360 | 68 | 1140 | 57 |
| 65 | 1900 | 95 | 1680 | 84 | 1440 | 72 | 1200 | 60 |
| 70 | 2020 | 101 | 1760 | 88 | 1500 | 75 | 1260 | 63 |
| 75 | 2120 | 106 | 1860 | 93 | 1580 | 79 | 1320 | 66 |
| 80 | 2220 | 111 | 1940 | 97 | 1660 | 83 | 1360 | 68 |
| 85 | 2340 | 117 | 2040 | 102 | 1720 | 86 | 1420 | 71 |
| 90 | 2440 | 122 | 2120 | 106 | 1800 | 90 | 1480 | 74 |
** При массе тела менее 35 кг: Целевое содержание гемоглобина = 130 г/л
При массе тела 35 кг и больше: Целевое содержание гемоглобина = 150 г/л
Для перевода гемоглобина (ммоль) в гемоглобин (г/л) умножьте первое значение на 16. Если общая необходимая доза превышает максимальную разрешенную однократную дозу, ее следует разделить на несколько введений.
Если через 1-2 недели не наблюдается улучшения гематологических параметров, первоначальный диагноз следует пересмотреть.
Расчет дозы для восполнения запасов железа после кровопотери или при сдаче аутологичной крови
Дозу препарата Железа (III) гидроксид сахарозный комплекс, необходимую для компенсации дефицита железа, можно рассчитать по следующим формулам:
Если количество потерянной крови известно: введение 200 мг железа (10 мл препарата Железа (III) гидроксид сахарозный комплекс) должно приводить приблизительно к такому же повышению концентрации гемоглобина, что и переливание 1 порции крови (400 мл с концентрацией гемоглобина = 150 г/л).
Количество железа, которое необходимо восполнить [мг] = количество порций потерянной крови × 10 мл Или
Необходимый объем препарата Железа (III) гидроксид сахарозный комплекс [мл] = количество порций потерянной крови × 200 мг
Если содержание гемоглобина ниже желаемого: формула предполагает, что депо железа пополнять не требуется.
Количество железа, которое необходимо восполнить [мг] = масса тела [кг] * 0,24 × (целевое содержание гемоглобина – фактическое содержание гемоглобина) [г/л]
Пример:
При массе тела = 60 кг и снижении содержания гемоглобина = 10 г/л
=> = 150 мг железа необходимо восполнить
=> необходимо 7,5 мл препарата Железа (III) гидроксид сахарозный комплекс
Максимальная переносимая разовая и недельная дозы указаны ниже в разделах «Стандартные дозы» и «Максимальная переносимая разовая и недельная дозы».
Стандартные дозы
Пациенты взрослого и пожилого возраста
5-10 мл препарата Железа (III) гидроксид сахарозный комплекс [мл] (100-200 мг железа) 1-3 раза в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Дети
Имеется лишь умеренное количество данных о применении препарата у детей в рамках исследований. В случае клинической необходимости применения не рекомендуется превышать дозу 0,15 мл препарата Железа (III) гидроксид сахарозный комплекс (3 мг железа) на кг массы тела не чаще 3 раз в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Максимально переносимая разовая и недельная дозы
Пациенты взрослого и пожилого возраста
Максимальная переносимая доза в сутки, вводимая в виде инъекции не чаще 3 раз в неделю:
• 10 мл препарата Железа (III) гидроксид сахарозный комплекс (200 мг железа), вводимые в течение минимум 10 минут.
Максимальная переносимая доза в сутки, вводимая в виде инфузии не чаще 1 раза в неделю:
• Пациенты с массой тела более 70 кг: 500 мг железа (25 мл препарата Железа (III) гидроксид сахарозный комплекс), вводимые в течение минимум 3,5 часов.
• Пациенты с массой тела 70 кг и менее: 7 мг железа/кг массы тела, вводимые в течение минимум 3,5 часов.
Следует строго придерживаться времени инфузии, указанного в разделе «Применение», даже если пациент не получил максимальной переносимой разовой дозы.
Побочное действие
Наиболее частой нежелательной лекарственной реакцией (НЛР), регистрировавшейся в рамках клинических исследовании препарата Железа (III) гидроксид сахарозный комплекс, являлось изменение вкусовых ощущений, которое наблюдалось с частотой 4,5 явления на 100 субъектов. Наиболее важными серьезными нежелательными лекарственными реакциями, связанными с применением препарата Железа (III) гидроксид сахарозный комплекс, являлись реакции гиперчувствительности, которые наблюдались в рамках клинических исследований с частотой 0,25 явления на 100 субъектов.
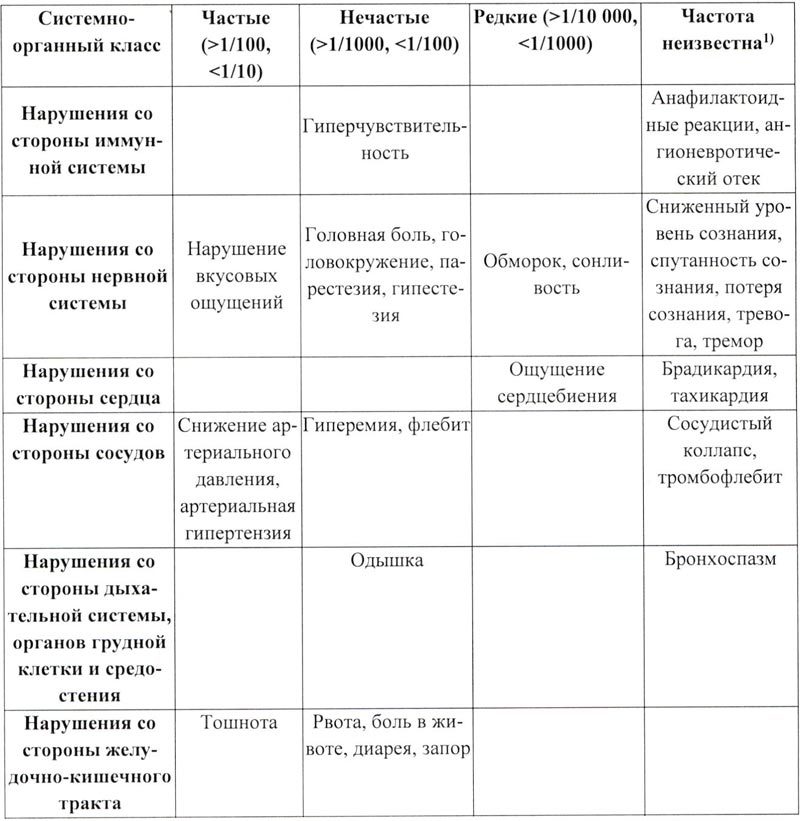
В таблице ниже представлены нежелательные лекарственные реакции, зарегистрированные после применения препарата Железа (III) гидроксид сахарозный комплекс в рамках клинических исследований, а также в пострегистрационном периоде.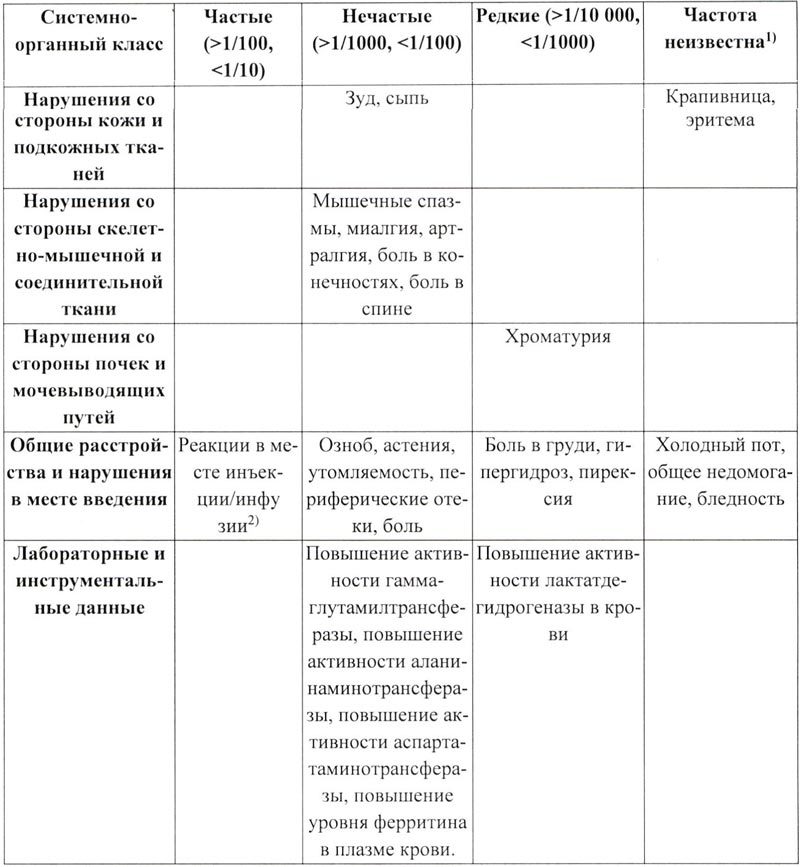
1) Спонтанные сообщения, полученные в пострегистрационном периоде
2) Наиболее частые: боль в месте инъекции/инфузии, экстравазация в месте инъекции/инфузии, раздражение в месте инъекции/инфузии, реакция в месте инъекции/инфузии, изменение окрашивания кожи в месте инъекции/инфузии, кровоподтек в месте инъекции/инфузии, зуд в месте инъекции/инфузии.
Передозировка
Передозировка может вызывать перегрузку железом, которая может проявляться симптомами гемосидероза. Передозировку следует лечить с использованием хелатирующего средства для связывания железа или в соответствии со стандартами медицинской практики.
Взаимодействия с другими лекарственными препаратами
Как и при применении всех парентеральных препаратов железа, препарат Железа (III) гидроксид сахарозный комплекс не рекомендуется применять одновременно с пероральными препаратами железа, поскольку всасывание перорального железа может снижаться, поэтому терапию пероральными препаратами железа следует начинать не ранее, чем через 5 дней после последней инъекции.
Железа (III) гидроксид сахарозный комплекс можно смешивать только со стерильным 0,9% (масса/объем) раствором натрия хлорида. При смешивании с другими растворами или лекарственными препаратами имеется риск выпадения осадка и/или взаимодействия. Совместимость с контейнерами из других материалов, помимо стекла, полиэтилена и поливинилхлорида, не изучена.
Особые указания
Парентерально вводимые препараты железа могут вызывать аллергические или анафилактоидные реакции, которые потенциально могут быть летальными, поэтому в наличии должны иметься противоаллергические препараты, а также оборудование для проведения сердечно-легочной реанимации и соответствующих процедур. После предшествовавших неосложненных введений парентеральных комплексов железа также отмечались реакции гиперчувствительности. После каждой инъекции препарата Железа (III) гидроксид сахарозный комплекс за всеми пациентами следует наблюдать на предмет отсутствия нежелательных явлений в течение как минимум 30 минут.
Пациентам, имеющим в анамнезе бронхиальную астму, экзему, другие виды атопических аллергий или аллергические реакции на другие парентеральные препараты железа, препарат Железа (III) гидроксид сахарозный комплекс следует применять с осторожностью, поскольку такие пациенты в особенности могут иметь риск развития аллергической реакции. Пациентам с нарушением функции печени парентеральное железо следует применять только после тщательной оценки соотношения риска и пользы. Пациентам с нарушением функции печени, когда перегрузка железом является провоцирующим фактором, не следует применять парентеральное железо. Для того чтобы избежать перегрузки железом, рекомендуется проводить тщательный мониторинг уровня железа в организме.
Парентеральное железо следует применять с осторожностью при наличии острой или хронической инфекции. Пациентам с бактериемией рекомендуется прекратить применение препарата Железа (III) гидроксид сахарозный комплекс. У пациентов с хронической инфекцией следует провести оценку соотношения риска и пользы.
Следует избегать проникновения препарата в околовенозное пространство, поскольку это может привести к появлению боли, развитию воспаления и окрашиванию кожи в коричневый цвет. В случаях непреднамеренного проникновения препарата в околовенозное пространство лечение следует проводить в соответствии со стандартами медицинской практики.
Железа (III) гидроксид сахарозный комплекс следует применять только в тех случаях, когда показание к применению подтверждено результатами соответствующих исследований (например, уровень ферритина в сыворотке, уровень насыщения трансферрина, содержание гемоглобина (Нb), эритроцитарные показатели – MCV. МСН, МСНС).
Срок годности после первого вскрытии контейнера
С микробиологической точки зрения, препарат следует использовать незамедлительно.
Срок годности после разведения 0,9% раствором натрия хлорида (NaCl)
Химическая и физическая стабильность после разведения при комнатной температуре (15-25 °С) составляет 12 часов. Однако с микробиологической точки зрения, препарат следует использовать сразу после разведения. Если препарат не был использован сразу же после разведения, тот, кто использует данный раствор, несёт ответственность за условия и время хранения после разведения, которое в любом случае не должно превышать 3 часов при комнатной температуре, кроме тех случаев, когда разведение было выполнено в контролируемых и надлежащих асептических условиях.
Влияние на способность управлять транспортными средствами, механизмами
Данных о влиянии на способность управлять транспортными средствами или работать с другими механизмами не имеется. Однако некоторые нежелательные реакции (такие, как головокружение, спутанность сознания и прочие (указаны в разделе «Побочное действие»)) могут оказывать негативное влияние на способность управлять транспортными средствами или работать с другими механизмами. Пациентам, у которых отмечаются данные нежелательные реакции, рекомендовано воздержаться от управления транспортными средствами или работы с другими механизмами до полного исчезновения данных симптомов.
Форма выпуска
Раствор для внутривенного введения 20 мг/мл.
По 5 мл во флаконы бесцветного нейтрального стекла I гидролитического класса, герметично укупоренные резиновыми пробками, обжатые алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
По 1 флакону вместе с инструкцией по применению в пачку из картона.
По 5 флаконов в контурную ячейковую упаковку из пленки поливинилхлоридной. По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия хранения
В оригинальной упаковке, защищенном от света месте при температуре не выше 25 °С.
Не замораживать.
Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый район, пос. Стрельна, ул. Связи, д. 34, лит. А.
Производитель
ЗАО «БИОКАД», Россия, 143422, Московская обл., Красногорский район, с. Петрово-Дальнее.
Организация, принимающая претензии потребителей
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый район, пос. Стрельна, ул. Связи, д. 34, лит. А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
- Описание
Описание
КМП-М ветеринарный препарат пр.-во РБ, флак. 400 мл, Минск
Регион: Вся Беларусь, Минск
Обновлено: 23-11-2019 15:47
Инструкция по применению препарата КМП-м
1. Общие сведения
1.1. КМП-м (КМР-м)
1.2. КМП-м комплексный инъекционный препарат на основе биоэдементов. В 1 см. куб. препарата содержится, мг: железа-15,0, йода-6,7, магния-6,0, селена-0,34.
1.3. Препарат представляет собой жидкость темно-коричневого цвета, допускается наличие осадка.
1.4. КМП-м выпускают по 100, 200, 250 и 400 см в стеклянных флаконах. Хранят по списоку Б в защищенном от света месте при температуре от +20 до +25°С. Срок годности 2 года.
2. Фармакологические свойства
2.1. Фармакологические свойства препарата “КМП-м” обусловлены влиянием на организм животных биоэлементов, входящих в его состав.
2.2. Железо в организме животных связано с многими белками и ферментами (гемоглобин, миоглобин, тренсферин, ферритин, гемосидерин, цитохромы, каталаза, пероксидаза и др.), которые осуществляют транспорт, связывание, резервирование кислорода и играют важную роль в процессахтканевого дыхания. Данный микроэлемент влияет на рост и развитие животных, состояние эритропоэза, обмен веществ, иммунитет, устойчивость к неблагоприятным факторам внешней среды.
2.3. Йод необходим для нормального функционирования щитовидной железы и биосинтеза ею тироидных гормонов (трийодтиронина и тироксина) регулирующих уровень основного обмена, терморегуляцию, кроветворение , состояние иммунитета, энергию роста, деятельность центральной нервной и сердечно-сосудистой систем, желудочно-кишечного тракта.
2.4. Магний в организаме, животных влияет на активночть многих ферментов в связи с чем, необходим для обеспечения энергетических вопросов и нормальной работы сердечно-сосудистой системы, регуляции нервно-мышечной проходимости , синтеза белков и жиров, обмены глюкозы, транспорта многих жизненно важных веществ и передачи наследственной информации.
2.5. Селен входит в состав ряда специфических белков организма, которые регулируют проницаемость клеточных мемюран, обеспечивают подвижность и жизнеспособность половых клеток, предохраняют липиды клеточных структур от переоксидации, повышают активность иммунокомпетентных клеток, а также способствует обмену многихвитаминов и нормальному функционированию щитовидной железы.
З. Порядок применения препарата
3.1. КМП-м применяют в качестве лечебно-профилактического средства при энзоотическом зобе, беломышечной болезни, тоесической дистрофии печени, железодефицитной анемии, гипомагниемии, а также для повышения неспецифической резистентности организма молодняка, воспроизводительной способности самок, профилактики послеродовых заболеваний, лечения и профилактики субклинического мастита у коров.
3.2. Препарат вводят животным подкожно или внутримышечно:нетелям и коровам за 5-15 дней до предполагаемого осеменения на 3-7 месяце стельности и за 25-45 дней до отела в дозе 15-20 см.куб. телятам лечебная доза составляет 2,5 см.куб. на 10 кг. живой массы (но не более 10 см.куб. на животное), профилактическая – 1,5 см.куб. на 10 кг живой массы: оснрвным свиноматкам КМП-м назначают за 8-12 дней до отъема поросят и за 20-25 дней до опороса в дозе 10-12 см.куб. на инъекцию, а ремонтным свинкам – за 7-14 дней до предполагаемого осеменения (покрытия) и за 20-25 дней до опороса в дозе 8-10 см.куб. поросятам -сосунам с целью профилактики анемии препарат инъекцируют дважды- на 3-5 и 10-15 дни жизни из расчета 1,5 см.куб./кг. живой массы. Поросятам более старшего возраста КМП-м назначают из расчета 0,5 см.куб. на 1 кг живой массы (но не более 5 см.куб. на животное). При необходимости дополнительных обработок животных, препарат вводят в тех же дозах, но не ранее, чем через 10 дней после первого назначения препарата.
3.3. В рекомендуемых дозах КМП-м у животных не вызывает осложнений и побочных эффектов. Однако за сутки до массовых обработок скота необходимо поставить на 5-7 животных пробу на переносимость.
3.4. Противопоказанием к применению препарата КМП-м является обработка животных в течение 10-ти последних дней препаратами, содержащими селен, железо, йод.
3.5. Убой животных на мясо разрешается через 3 дня после последнего применения препарата, молоко используют без ограничений.
4. Меры личной профилактики
4.1. При работе с препаратом следует соблюдать общепринятые меры личной гигиены и правила техники безопасности.
5. Порядок предъявления рекламаций
5.1. В случае возникновения осложнений после применения препарата, его использование прекращают и потребитель обащается в Государственное ветеринарное учреждение , на территории которой он находится. Ветеринарными специалистами этого учреждения производится соблюдения всех правил по применению препарата в соответствии с инструкцией. При подтверждении выявления отрицательного воздествия на организм животного, ветеринарными специалистами отбираются пробы в необходимом количестве для проведения лаборатоных испытаний, пишется акт отбора проб и направляется в Государственное учреждение “Белорусский государственный ветеринарный центр” (г. Минск, ул. Красная. 19-а. тел. 290-42-75) для подстверждения на соответствие нормативных документов.
https://apk-belarus.com
Подробнее: https://apk-belarus.com/ru/trade/i-822/
Похожие товары
Тривитамин (для инъекций)
ИНСТРУКЦИЯ
1. Общие сведения
1. Торговое наименование лекарственного препарата: «Тривитамин A, Д3, E для инъекций (раствор витаминов А, Д3, Е в масле)» (Trivitaminum A, D3, E pro injectionibus (Solutio vitaminorum A, D3, E oleosa)).
Международное непатентованное наименование: ретинол, кальциферол, токоферол.
2. Лекарственная форма: раствор для инъекций.
Лекарственный препарат содержит в 1 мл в качестве действующих веществ 30000 МЕ витамина А (ретинола ацетата или ретинола пальмитата), 40000 МЕ витамина Д3 (холекальциферола), 20 мг витамина Е (токоферола ацетата), а в качестве вспомогательного вещества - масло подсолнечное или соевое – до 1 мл.
3. По внешнему виду «Тривитамина A, Д3, E для инъекций (раствора витаминов А, Д3, Е в масле)» представляет собой стерильную прозрачную маслянистую жидкость от светло-желтого до светло-коричневого цвета с запахом, свойственным растительному маслу.
Срок годности лекарственного препарата при соблюдении условий хранения - 2 года со дня производства. Срок годности после первого вскрытия – 24 часа. Запрещается использовать препарат после окончания срока годности.
4. Лекарственный препарат выпускают расфасованным по 5, 10, 50, 100 мл в стеклянных флаконах и по 400 мл в стеклянных бутылках соответствующей вместимости, укупоренных резиновыми пробками, укрепленными алюминиевыми колпачками. Каждую единицу потребительской упаковки снабжают инструкцией по применению препарата.
5. Хранят в закрытой упаковке производителя, в сухом, защищенном от прямых солнечных лучей месте, отдельно от продуктов питания и кормов, при температуре от 50С до 250С.
6. «Тривитамин A, Д3, E для инъекций (раствор витаминов А, Д3, Е в масле)» следует хранить в недоступном для детей месте.
7. Неиспользованный лекарственный препарат утилизируют в соответствии с требованиями законодательства.
8. Отпускается без рецепта ветеринарного врача.
II. Фармакологические свойства
9. «Тривитамин A, Д3, E для инъекций (раствор витаминов А, Д3, Е в масле)» относится к фармакологической группе комбинированных витаминных препаратов.
10. Комбинированный витаминный лекарственный препарат, в котором витамины А, Д3 и Е приведены в физиологически обоснованных соотношениях и действуют синергически. Действие лекарственного препарата определяется эффектами входящих в его состав витаминов.
Витамин А ускоряет рост, повышает защитные функции организма, улучшает состояние эпителия, способствует его регенерации.
Витамин Д3 регулирует минеральный обмен. При недостатке витамина Д3 у животных наблюдается рахит, остеомаляция, тетанические судороги.
Витамин Е является антистерильным витамином. При его недостатке у животных наблюдается бесплодие, торможение роста, поражение центральной нервной системы (энцефаломаляция), перерождение печени и мышечной ткани, нарушение обмена жиров и углеводов.
«Тривитамин A, Д3, E для инъекций (раствор витаминов А, Д3, Е в масле)» нормализует обмен веществ, профилактирует гиповитаминозы и заболевания, развивающиеся на их фоне. Лекарственный препарат положительно воздействует на многие процессы, протекающие в организме, в том числе защитные функции, регенерацию кожного покрова, рост, репродукцию, сопротивляемость инфекциям.
По степени воздействия на организм препарат относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1.007).
-
III. Порядок применения
11. «Тривитамин A, Д3, E для инъекций (раствор витаминов А, Д3, Е в масле)» применяют животным для профилактики и лечения гиповитаминозов А, Д, Е и заболеваний, развивающихся на их фоне (ксерофтальмия, рахит, остеомаляция), для повышения плодовитости и жизнеспособности молодняка, а также для борьбы с бесплодием у крупного рогатого скота и свиней
12. Противопоказанием к применению лекарственного препарата является повышенная индивидуальная чувствительность животных к ретинолу, кальциферолу, токоферолу.
13. С лечебной целью лекарственный препарат вводят животным внутримышечно или подкожно один раз в неделю в течение 3-4 недель в следующих дозах:
Группа животных
Внутримышечно или подкожно, мл/голову
Крупный рогатый скот
2,5
Лошади
1,5
Жеребята, телята
2,0-3,0
Овцы, козы
1,0
Ягнята, поросята
0,5
Свиньи
1,5
Куры
0,2
Собаки
0,5-1,0
Кролики, кошки
0,2-0,3
С профилактической целью препарат вводят в тех же дозах однократно каждые 2-3 недели в течение 2-4 месяцев.
Одновременно с назначением Тривитамина A, D3, E для инъекций необходимо балансировать рационы животных по кальцию, магнию и микроэлементам.
14. Симптомы передозировки не установлены.
15. Особенностей действия при первом приеме препарата и его отмене не установлено.
16. Препарат рекомендуется применять во время беременности и лактации.
17. Следует избегать пропусков при введении очередной дозы препарата, так как это может привести к снижению эффективности. В случае пропуска одной дозы необходимо ввести ее как можно скорее. Далее курс лечения необходимо возобновить в предусмотренных дозировках и схеме применения.
18. При применении лекарственного препарата в соответствии с настоящей инструкцией побочных явлений и осложнений, как правило, не отмечается. В случае появления аллергических реакций использование препарата прекращают и назначают антигистаминные средства и симптоматическое лечение.
19. Лекарственный препарат совместим с другими лекарственными препаратами и кормовыми добавками.
20. Продукцию животноводства и птицеводства во время и после применения «Тривитамина A, Д3, E для инъекций (раствора витаминов А, Д3, Е в масле)» используют без ограничений.
-
IV. Меры личной профилактики
21. При работе с препаратом следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными препаратами ветеринарного назначения. При работе с препаратом запрещается пить, курить, принимать пищу. По окончании работы необходимо тщательно вымыть руки с мылом.
22. При случайном контакте лекарственного препарата с кожей или слизистыми оболочками глаз, их необходимо промыть большим количеством проточной воды. Людям с гиперчувствительностью к компонентам препарата следует избегать прямого контакта с препаратом.
23. В случае появления аллергических реакций или при случайном попадании препарата в организм человека следует немедленно обратиться в медицинское учреждение (при себе иметь инструкцию по применению препарата или этикетку).
24. Пустую тару из-под лекарственного препарата запрещается использовать для бытовых целей, она подлежит утилизации с бытовыми отходами.
Коричневый непрозрачный раствор.
Каждая ампула (2 мл) содержит 100 мг железа (Ш) в виде комплексного соединения декстрана с гидроксидом железа (III).
Вспомогательные вещества: гидроксид натрия, хлористоводородная кислота (для регулирования pH), вода для инъекций.
Противоанемические средства. Средства на основе трехвалентного железа для парентерального введения.
Код ATX: В03АС.
Фармакодинамические свойства
После внутримышечного введения часть гидроксида железа (III) запасается в виде ферритина, образующегося в митохондриях печени. Ферритин состоит из белковой оболочки — апоферритина, в которой железо находится в форме гидратированных мицелл фосфата окиси железа.
Транспорт железа в плазме осуществляется с помощью бета-глобулина трансферрина, синтезирующегося в печени. Каждая молекула трансферрина связывает два атома железа. Железо в комплексе с трансферрином переносится к клеткам организма, где оно используется для синтеза гемоглобина, миоглобина и некоторых ферментов. Трансферрин также принимает косвенное участие в защите организма против инфекций.
После парентерального введения комплексного соединения декстрана с гидроксидом железа (III) концентрация гемоглобина увеличивается быстрее, чем после приема внутрь солей железа (II), несмотря на то, что кинетика усвоения железа не зависит от метода его введения.
Комплекс декстрана с гидроксидом железа (III) достаточно велик по размерам и поэтому не выводится через почки. Образующееся комплексное соединение стабильно и в физиологических условиях не выделяет ионов железа. Железо в полинуклеарных ядрах связано в виде структуры, аналогичной таковой у ферритина в физиологических условиях.
Имеющиеся данные подтверждают точку зрения о том, что Феррум Лек обеспечивает такие же физиологические изменения, какие наблюдаются и при естественном всасывании железа.
Фармакокинетические свойства
После внутримышечного введения комплексное соединение декстрана с гидроксидом железа (III) абсорбируется в основном в лимфатической системе и проникает в систему циркулирующей крови спустя 3 суток. Несмотря на отсутствие данных о биодоступности, известно, что относительно большая часть введенного внутримышечно комплексного соединения декстрана с гидроксидом железа (III) не абсорбируется в мышечной ткани даже спустя более продолжительное время. Биологический период полувыведения комплексного соединения декстрана с гидроксидом железа (III) составляет 3-4 суток.
Макромолекулярный комплекс декстрана с гидроксидом железа (III) захватывается ретикулоэндотелиальной системой и распадается на компоненты — железо и декстран. Железо затем связывается с ферритином и в меньшей степени — с трансферрином. Затем это железо используется в костном мозге для синтеза гемоглобина, т.е. участвует в эритропоэзе.
Декстран либо подвергается метаболизму, либо выводится.
Железо выводится в незначительном количестве.
Данные о доклинической безопасности
Сообщалось, что декстран железа является тератогенным и эмбриоцидным у неанемичных беременных животных при высоких единичных дозах выше 125 мг/кг. Наибольшая рекомендуемая доза в клиническом применении составляет 20 мг/кг. Однако подробная информация о данных исследованиях отсутствует.
In vitro и in vivo исследования генотоксичности показали мутагенную активность после введения высоких доз комплексов железа декстрана. Однако значимость этих результатов неясна. Комплекс железа декстрана не был мутагенным при введении субтоксических доз.
Лечение всех форм железодефицитных состояний, если пероральные препараты железа неэффективны и/или не переносятся пациентами.
— повышенная чувствительность к активному веществу или вспомогательным компонентам препарата;
— анемия, не связанная с дефицитом железа;
— перегрузка железом или наследственные нарушения утилизации железа;
— тяжелые реакции гиперчувствительности на другие лекарственные средства на основе железа для парентерального введения в анамнезе.
Парентеральное введение препаратов железа может вызвать реакции гиперчувствительности, включая тяжелые и потенциально летальные анафилактические/анафилактоидные реакции. Имеются сообщения о возникновении реакций гиперчувствительности после введений парентеральных комплексов железа, проходивших ранее без осложнений.
Риск возникновения реакций гиперчувствительности возрастает у пациентов с известной аллергией, включая лекарственную аллергию, тяжелую астму, экзему или другие проявления атопической аллергии в анамнезе.
Существует также повышенный риск реакций гиперчувствительности к парентеральным препаратам железа у пациентов с иммунными или воспалительными заболеваниями (например, системная красная волчанка, ревматоидный артрит).
Данный препарат следует вводить только при наличии персонала, обученного выявлению анафилактических реакций и оказанию неотложной помощи, в условиях, где имеется полное реанимационное оснащение. Побочные реакции у каждого пациента необходимо оценивать, по меньшей мере, в течение 30 минут после каждого введения препарата. Если при применении препарата возникают реакции гиперчувствительности или признаки непереносимости — лечение необходимо немедленно прекратить. Должны быть доступны средства для сердечно- легочной реанимации и оборудование для борьбы с острыми анафилактическими/анафилактоидными реакциями, включая раствор адреналина 1:1000 для инъекций. При необходимости следует назначить дополнительное лечение антигистаминными препаратами и/или кортикостероидами.
Пациентам с нарушением функции печени парентеральное введение железа можно осуществлять только после тщательной оценки соотношения риск/польза. А у пациентов с нарушением функции печени, где провоцирующим фактором является перегрузка железом его следует избегать. Во избежание перегрузки железом его содержание рекомендуется тщательно контролировать.
Парентеральное введение железа должно проводиться с осторожностью при острых или хронических инфекциях. При бактериемии данный препарат отменяют. У пациентов с хронической инфекцией необходимо оценить соотношение пользы и риска.
Могут возникать гипотензивные реакции при слишком быстром внутримышечном введении. В случае внутримышечного введения железо-углеводных комплексов не исключается риск канцерогенеза. Такие осложнения были обнаружены в экспериментальных условиях воспроизведения саркомы, когда в исследованиях на животных внутримышечные и подкожные инъекции железо-углеводных комплексов приводили к развитию сарком у крыс, мышей, кроликов и хомяков, но не у морских свинок. Накопленная информация и независимые оценки показывают, что риск развития саркомы у человека минимален. Длинный латентный период между потенциально канцерогенной инъекцией и появлением опухоли делает невозможным точно оценить риск для человека.
Побочные реакции, возникающие после введения препаратов железа, могут привести к усилению сердечно-сосудистых осложнений у пациентов с уже существующей сердечно-сосудистой патологией.
Из-за отсутствия опыта не рекомендуется применение внутримышечных инъекций Феррум Лек у детей младше 4 месяцев.
Беременность
На основании умеренного количества данных (300-1000 случаев беременности) не было отмечено нежелательного влияния парентеральных препаратов железа на организм матери или новорожденного при их применении женщинами на втором и третьем триместре беременности.
Адекватные и хорошо контролируемые испытания эффективности и безопасности лекарственного средства у беременных женщин не проводились. Поэтому перед применением Феррум Лек во время беременности требуется тщательная оценка польза/риск, и его не следует применять во время беременности без явной необходимости (см. «Меры предосторожности»). Для лечения железодефицитной анемии, возникающей в первом триместре беременности, во многих случаях может применяться пероральная форма препаратов железа. Лечение Феррум Лек должно ограничиваться вторым и третьим триместрами, если учитывать преимущества, превышающие потенциальный риск как для матери, так и для плода.
Исследования на животных не указывают на прямое или косвенное вредное воздействие в отношении репродуктивной токсичности (см. «Данные доклинической безопасности»).
Лактация
Доклинические данные не указывают на прямые или косвенные вредные воздействия для детей на грудном вскармливании.
Применение препарата Феррум Лек не влияет на способность управлять транспортными средствами и работу с механизмами.
Тем не менее, если после применения данного препарата возникают такие симптомы, как головокружение, спутанность сознания и предобморочное состояние пациент не должен управлять транспортными средствами или работать с механизмами до их полного исчезновения.
Данный препарат не следует назначать одновременно с препаратами железа для приема внутрь, поскольку всасывание последних будет снижено. Терапию препаратами железа для приема внутрь следует начинать не ранее чем через 5 дней после последнего парентерального введения железа.
Высокие дозы декстрана железа (5 мл или более) приводят к окрашиванию образцов сыворотки крови, взятых через четыре часа после применения декстрана железа в коричневый цвет. Препарат может вызвать ложное увеличение концентрации билирубина и ложное уменьшение концентрации кальция в сыворотке крови.
Во время и после каждого введения данного препарата следует тщательно отслеживать признаки и симптомы реакций гиперчувствительности.
Данный препарат должен вводиться только при наличии персонала, обученного выявлению анафилактических реакций и оказанию неотложной помощи, в условиях, где имеется возможность оказывать реанимационные мероприятия. Побочные реакции необходимо оценивать по меньшей мере в течение 30 минут после каждого введения препарата.
Данный препарат можно вводить только внутримышечно. Его нельзя применять для внутривенного введения ни в виде инъекций, ни в виде инфузий.
Расчет дозы
Восполнение железа при железодефицитной анемии
Дозы Феррум Лек необходимо подбирать индивидуально в соответствии с общим дефицитом железа, который рассчитывается по следующей формуле:
общий дефицит железа (мг) = масса тела (кг) х (целевой уровень гемоглобина (г/л) — фактический уровень гемоглобина (г/л)) х 0,24* + депонированное железо (мг)
Масса тела до 35 кг: целевой уровень гемоглобина = 130 г/л и депонированное железо =15 мг/кг массы тела
Масса тела 35 кг и более: целевой уровень гемоглобина = 150 г/л и депонированное железо = 500 мг
*Коэффициент 0,24 = 0,0034 х 0,07 х 1000
(Содержание железа в гемоглобине = 0,34%; общий объем крови = 7% массы тела; коэффициент 1000 = перевод из граммов в миллиграммы).
Пример:
Масса тела пациента: 70 кг
Фактический уровень гемоглобина: 80 г/л
Общая доза железа = 70 х (150 — 80) х 0,24 + 500 = 1700 мг железа.
Общее число ампул Феррум Лек, которое необходимо ввести = общий дефицит железа (мг) / 100 мг
Таблица: общая доза Феррум Лек в миллилитрах (количество ампул), которую необходимо ввести, на основе фактического уровня гемоглобина и массы тела
|
Масса тела
|
Общая доза Феррум Лек в миллилитрах (количество ампул), которую нужно ввести:
|
|||
|
Hb 60 г/л |
Hb 75 г/л |
Hb 90 г/л |
Hb 105 г/л |
|
|
5 |
3 (1,5) |
3(1,5) |
3 (1,5) |
2(1,0) |
|
10 |
6 (3,0) |
6(3,0) |
5 (2,5) |
4(2,0) |
|
15 |
10 (5,0) |
9 (4,5) |
7(3,5) |
6 (3,0) |
|
20 |
13 (6,5) |
11(5,5) |
Ю (5,0) |
8 (4,0) |
|
25 |
16(8,0) |
14 (7,0) |
12 (6,0) |
11(5,5) |
|
30 |
19(9,5) |
17 (8,5) |
15 (7,5) |
13 (6,5) |
|
35 |
25 (12,5) |
23 (11,5) |
20 (10,0) |
18 (9,0) |
|
40 |
27(13,5) |
24 (12,0) |
22(11,0) |
19 (9,5) |
|
45 |
30 (15,0) |
26 (13,0) |
23(11,5) |
20 (10,0) |
|
50 |
32 (16,0) |
28 (14,0) |
24 (12,0) |
21 (10,5) |
|
55 |
34 (17,0) |
30 (15,0) |
26(13,0) |
22(11,0) |
|
60 |
36 (18,0) |
32 (16,0) |
27(13,5) |
23 (11,5) |
|
65 |
38 (19,0) |
33 (16,5) |
29(14,5) |
24 (12,0) |
|
70 |
40 (20,0) |
35 (17,5) |
30(15,0) |
25 (12,5) |
|
75 |
42 (21,0) |
37(18,5) |
32 (16,0) |
26 (13,0) |
|
80 |
45 (22,5) |
39(19,5) |
33 (16,5) |
27 (13,5) |
|
85 |
47 (23,5) |
41 (20,5) |
34 (17,0) |
28 (14,0) |
|
90 |
49 (24,5) |
43 (21,5) |
36(18,0) |
29 (14,5) |
Если спустя 1-2 недели после начала введения Феррум Лек гематологические параметры не меняются, следует уточнить поставленный диагноз.
Расчет общей дозы для возмещения железа вследствие кровопотери
Доза Феррум Лек для компенсации постгеморрагического железодефицита рассчитывается по следующей формуле:
если известно количество потерянной крови: введение 200 мг в/м (4 мл или 2 ампулы Феррум Лек) приводит к увеличению уровня гемоглобина, которое эквивалентно 1 единице крови (400 мл крови с содержанием гемоглобина 150 г/л)
Количество железа, которое следует возместить (мг)=число потерянных единиц крови х 200
или
Объем Феррум Лек в миллилитрах (количество ампул)=число потерянных единиц крови х 4 (х 2);
если известен сниженный уровень гемоглобина, используйте следующую формулу, учитывая то, что депонированное железо возмещать не нужно:
железо, которое следует возместить (мг)=масса тела (кг) х (целевой уровень гемоглобина (г/л) — фактический уровень гемоглобина (г/л)) х 0,24
Например, пациенту с массой тела 60 кг и дефицитом гемоглобина 10 г/л следует возместить 150 мг железа, что составляет 1 1/2 ампулы Феррум Лек (3 мл).
Обычные суточные дозы
Дети с 4-х месяцев жизни: 0,06 мл Феррум Лек/кг массы тела/сутки (3 мг железа/кг/сутки).
Взрослые и пожилые пациенты: 1-2 ампулы Феррум Лек (100-200 мг железа), в зависимости от уровня гемоглобина.
Если нет побочных реакций, препарат вводится по индивидуально подобранной схеме, пока общая требуемая доза не будет достигнута.
Ежедневная доза, как правило, не должна превышать 0,5 мл (25 мг железа) для детей весом до 5 кг, 1,0 мл (50 мг железа) для детей весом до 10 кг и 2,0 мл (100 мг железа) для других пациентов.
Если рассчитанная общая доза Феррум Лек, которую необходимо ввести, превышает максимальную суточную дозу, ее следует разделить на несколько дней, и вводить ежедневно активным пациентам или 1-2 раза в неделю малоактивным/иммобилизованным пациентам.
Указания по применению/обращению и введению
Неправильное хранение ампул может привести к выпадению осадка. Перед использованием ампулы следует внимательно осмотреть. Можно использовать лишь те ампулы, которые содержат однородный раствор без осадка.
Если в ампулах появился осадок или истек срок хранения, их необходимо уничтожить. Вскрытая ампула должна быть немедленно использована.
Содержимое ампул Феррум Лек не следует смешивать с другими лекарствами.
Во избежание боли и окрашивания кожи очень важно проводить внутримышечные инъекции осторожно и правильно. Феррум Лек вводится только внутримышечно (ни в коем случае внутривенно!) глубоко в ягодичную мышцу, чередуя по очереди правую и левую.
Внутримышечные инъекции Феррум Лек проводятся в верхний наружный квадрант ягодичной мышцы. Минимальная длина иглы для взрослых — 50 мм, для пациентов с избыточной массой тела — от 80 до 100 мм, для детей — 32 мм. Перед инъекцией кожу следует продезинфицировать и сдвинуть на 2 см вниз для уменьшения вытекания лекарства после инъекции. После инъекции кожу отпускают и удерживают место инъекции под давлением в течение 1 минуты.
Если во время инъекции пациент стоит, он должен перенести вес на ногу, противоположную месту инъекции, если лежит, он должен лежать в положении на боку на стороне, противоположной месту инъекции.
Передозировка может вызвать перегрузку железом, которая может проявиться гемосидерозом. При необходимости передозировку необходимо лечить препаратами, образующими хелатные соединения с железом, или в соответствии со стандартной медицинской практикой. При хроническом повторном введении высоких доз железа избыток железа накапливается в печени и вызывает воспалительный процесс, который может привести к фиброзу.
Информация о нежелательных реакциях представлена в соответствии с системно-органной классификацией MedDRA и частотой встречаемости. Категории частоты определяются по следующей классификации: очень часто (≥1/10), часто (≥1/100, но <1/10), нечасто (≥1/1 000, но <1/100), редко (≥1/10 000, но <1/1 000), очень редко (<1/10 000), частота неизвестна (на основании имеющихся данных оценить невозможно.
Нежелательные реакции, которые были зарегистрированы после введения парентеральных препаратов железа в клинических испытаниях и спонтанно в постмаркетинговых условиях.
Нарушения со стороны иммунной системы
Нечасто: реакции гиперчувствительности.
Частота неизвестна1: анафилактоидные реакции, включая одышку, крапивницу, сыпь, зуд, тошноту и озноб; ангиоэдема.
Острые тяжелые анафилактоидные реакции (внезапное затруднение дыхания и/или острая сердечно-сосудистая недостаточность); имеются сообщения о смертельных исходах.
Описаны тяжелые отсроченные реакции, характеризующиеся артралгией, миалгией и иногда лихорадкой.
Нарушения со стороны нервной системы
Часто: дисгевзия.
Нечасто: помутнение зрения, онемение, головная боль, головокружение, парестезия, гипоэстезия.
Редко: пароксизм, беспокойство, обморок, сонливость.
Частота неизвестна1: угнетенное состояние сознания, спутанное сознание, потеря сознания, беспокойство, тремор, судороги.
Нарушения со стороны органа слуха и лабиринта
Очень редко: временная глухота.
Нарушения со стороны крови и лимфатической системы
Очень редко: гемолиз, лимфаденопатия.
Частота неизвестна: лейкоцитоз.
Нарушения со стороны сердца
Редко: аритмия, сильное сердцебиение.
Частота неизвестна1: тахикардия, брадикардия, сердечная недостаточность.
Нарушения со стороны сосудов
Часто: артериальная гипертензия, артериальная гипотензия.
Нечасто: приливы жара, сосудистая недостаточность.
Частота неизвестна1: сосудистая недостаточность.
Нарушения со стороны дыхательной системы, грудной клетки и органов средостения
Нечасто: одышка.
Частота неизвестна1: бронхоспазм.
Желудочно-кишечные нарушения
Часто: тошнота.
Нечасто: рвота, боль в животе, диарея, запор.
Нарушения со стороны кожи и подкожных тканей
Нечасто: зуд, сыпь.
Частота неизвестна1: крапивница, эритема.
Нарушения со стороны мышечной, скелетной и соединительной ткани
Нечасто: мышечные спазмы, миалгия, артралгия, боли в конечностях, боли в спине.
Нарушения со стороны почек и мочевыводящих путей
Редко: хроматурия.
Общие нарушения и реакции в месте введения
Часто: реакции в месте введения2.
Нечасто: лихорадка, озноб, астения, усталость, периферические отеки, боль, флебит, тромбофлебит.
Редко: боль в грудной клетке, гипергидроз, пирексия.
Частота неизвестна1: холодный пот, недомогание, бледность, тромбофлебит, боль и жжение в месте введения.
Лабораторные и инструментальные данные
Нечасто: увеличение уровня аланинаминотрансферазы, аспартатаминотрансферазы, гамма- глутамилтрансферазы, ферритина в сыворотке.
Редко: увеличение уровня лактатдегидрогеназы крови.
1Спонтанные сообщения в постмаркетинговом периоде.
2Наиболее часто сообщалось: при внутривенном/внутримышечном введении отмечаются такие местные осложнения, как боль, раздражение, реакция, окрашивание, гематома и жжение в месте введения.
Сообщения о нежелательных реакциях
Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного препарата с целью обеспечения непрерывного мониторинга соотношения «польза — риск». Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях на лекарственный препарат через национальные системы сообщения о нежелательных реакциях и неэффективности лекарственных препаратов.
Пациенту, если у него возникают какие-либо нежелательные реакции, следует проконсультироваться с врачом. Данная рекомендация распространяется на любые нежелательные реакции, в том числе, на не указанные в листке-вкладыше. Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Хранить при температуре не выше 25 °C.
Не замораживать.
Хранить в недоступном для детей месте.
5 лет.
Не использовать по истечении срока годности.
Отпускается по рецепту.
Только для применения в условиях стационара.
Раствор для внутримышечного введения в стеклянных ампулах по 2 мл. 5 или 50 ампул, маркированных красным кольцом и красной точкой, вместе с инструкцией в картонной коробке.
Информация о производителе
Лек д.д., Веровшкова 57, Любляна, Словения.